Влияние индапамида на уровень радикалов кислорода, продуцируемых фагоцитами крови пациентов с сердечной недостаточностью
Статьи Опубликовано в журнале, Российский кардиологический журнал № 4 (96)/2012 Асташкин Е. И., Глезер М. Г., Петров Е. А., Соколова И. Н.Первый Московский Государственный медицинский университет им. И. М. Сеченова, Москва, Россия.
Асташкин Е. И. - д. б.н., профессор, заведующий лабораторией экстремальных состояний, профессор кафедры патологии, Глезер М. Г. - д. м.н., профессор, зав. лабораторией функциональных методов исследования и рациональной фармакотерапии сердечно-сосудистых заболеваний, профессор кафедры профилактической и неотложной кардиологии, Петров Е. А. - к. б.н., ст.науч.сотр. лаборатории экстремальных состояний, Соколова И. Н. - к. м.н., ст.науч.сотр. лаборатории функциональных методов исследования и рациональной фармакотерапии сердечно-сосудистых заболеваний.
Цель. Изучить влияние на уровень свободных радикалов кислорода, генерируемых фагоцитами крови и изолированными нейтрофилами пациентов с сердечной недостаточностью (СН), тиазидоподобного диуретика индапамида (Ind).
Материал и методы. В пробах цельной крови и на изолированных нейтрофилах, полученных от 15 пациентов с СН функционального класса по NYHA, оценивали образование радикалов кислорода на хемилюминометре "Биотокс-7" в присутствии люминофоров - люцигенина (30 мкМ) и люминола (50 мкМ). В качестве стандартных стимуляторов фагоцитов крови и нейтрофилов применяли бактериальный трипептид (FMLP, 3 мкМ) и форболовый эфир (РМА, 1 мкМ). Образование супероксид - анионов (О2) и гидроксил-радикалов регистрировали в непрерывном режиме во времени в количестве импульсов в сек и оценивали по интегральным значениям хемилюминесценции (светосумма за 10 мин). Ингибирующий эффект различных концентраций индапамида оценивали как выраженность снижения (%) от максимального свечения, вызванного стандартными стимуляторами. Изучена антиоксидантная активность индапамида в бесклеточной среде, генерирующей гидроксил-радикалы.
Статистическая обработка результатов проведена с использованием программы SigmaPlot.
Результаты. Исходно в крови пациентов с СН были обнаружены предактивированные (праймированные) фагоциты, о чем свидетельствует "спонтанное" образование супероксид- анионов, которое возникает в результате адгезии нейтрофилов на стенках кюветы. РМА вызывал резкое усиление образования радикалов кислорода. В суспензиях нейтрофилов индапамид концентрационно-зависимым образом (0,5-2 мкМ) на максимуме ответа на РМА снижал уровень супероксид-анионов до базальных значений. Аналогичный эффект индапамида наблюдался в образцах цельной крови пациентов с СН. FMLP увеличивал генерацию радикалов кислорода и потенцировал последующий ответ фагоцитов на PMA. Индапамид (2 мкМ), добавленный после FMLP и РМА, снижал уровень супероксид- анионов до исходных значений, наблюдаемых в отсутствие стимуляторов. Первоначальная обработка образцов крови пациентов с СН индапамидом снижала спонтанное образование радикалов кислорода, а также амплитуды последующих ответов на FMLP и РМА. Антиок сидантный эффект индапамида (10 мкМ) наблюдался и в бесклеточной системе, что свидетельствует о его прямом взаимодействии с радикалами кислорода.
Заключение. Индапамид в низких концентрациях оказывает выраженный антиоксидантный эффект, что может быть значимым при лечении пациентов с СН.
Ключевые слова: сердечная недостаточность, фагоциты крови, нейтрофилы, индапамид, антиоксидантный эффект.
Indapamide effects on free oxygen radicals produced by blood phagocytes in patients with heart failure
Astashkin E. I., Glezer M. G., Petrov E. A., Sokolov I. N.
I. M. Sechenov First Moscow State Medical University, Moscow, Russia.
Aim. To study the effects of a thiazide-like diuretic indapamide (Ind) on the levels of free oxygen radicals generated by blood phagocytes and isolated neutrophils in patients with heart failure (HF).
Material and methods. Using whole blood samples and isolated neutrophils of 16 HF patients (NYHA Functional Class II-III), the generation of free oxygen radicals was examined with a chemiluminometre "Biotox-7", in the presence of luminophores - lucigenin (30 mkM) and luminol (50 mkM). The standard stimulators of blood phagocytes and neutrophils were bacterial tripeptide (FMLP, 3 mkM) and phorbol ester (PMA, 1 mkM). The generation of superoxide anions (O2) and hydroxyl radicals was continuously assessed by the number of impulses per second and presented as integral chemiluminescence (summary value for 10 minutes). Inhibiting effects of varied Ind concentrations were assessed by the decrease (%) in the peak stimulated luminescence. Antioxidant activity of Ind was studied in the cell-free medium generating hydroxyl radicals. Statistical analysis of the data was performed with the use of SigmaPlot software.
Results. At baseline, the blood of HF patients contained pre-activated (primed) phagocytes, as shown by the "spontaneous" production of superoxide anions due to neutrophil adhesion on cuvette walls. PMA markedly increased the production of oxygen radicals. In the neutrophil suspension, Ind dose-dependently (0,5-2 mkM) reduced the peak PMA response levels of superoxide anions up to the baseline levels. Moreover, Ind demonstrated a similar effect in whole blood samples of HF patients. FMLP increased the production of oxygen radicals and potentiated the subsequent response of phagocytes to PMA. Ind (2 mkM), when added after FMLP and PMA, reduced the post-stimulation levels of superoxide anions up to baseline values. The initial exposure of blood samples to Ind decreased spontaneous generation of oxygen radicals and the magnitude of subsequent response to FMLP and PMA. Antioxidant effects of Ind were also observed in the cell-free medium, which suggests a direct interaction between Ind and oxygen radicals.
Conclusion. Low Ind concentrations provided a marked antioxidant effect, which could be clinically significant in the management of HF patients.
Key words: heart failure, blood phagocytes, neutrophils, indapamide, antioxidant effect.
В результате хронического воздействия различных видов стресса: перегрузки давлением (при гипертензии) или объемом (например, при регургитации крови вследствие поражения клапанов сердца и в других условиях), а также после инфаркта миокарда, возникает ремоделирование сердца, которое часто заканчивается возникновением сердечной недостаточности (СН) [1]. Одним из важнейших факторов, ответственных за развитие ремоделирования сердца, является оксидативный стресс. Радикалы кислорода играют активную роль в гипертрофии миокарда, развитии фиброза, потере эластичности, повреждении структуры макромолекул и гибели различных типов клеток сердца, что сопровождается развитием дисфункции миокарда, дилатацией желудочков [2] и другими клиническими проявлениями СН. Ведущим источником образования значительных количеств радикалов кислорода являются различные изоформы НАДФН-оксидазного ферментативного комплекса семейства Nox, экспрессированных как на мембра нах клеток сердца (кардиомиоциты, эндотелиальные клетки, гладкомышечные клетки сосудов, фибробласты, и др.) [3], так и на нейтрофилах и моноцитах, поступающих из крови в область повреждения и гибели кардиомиоцитов [4, 5].
Поиск новых подходов для регуляции активности фагоцитов, торможения образования радикалов кислорода и уменьшения их уровня, включая фармакологические воздействия, является актуальной медико-биологической задачей, связанной с предупреждением поражения различных органов и тканей при СН и других патологиях.
Целью работы было изучить влияние тиазидоподобного диуретика индапамида на образование радикалов кислорода фагоцитами крови пациентов с сердечной недостаточностью.
Материал и методы
Исследование проведено у 15 пациентов с СН II-III функционального класса по классификации Нью-Йоркской ассоциации сердца (NYHA), проходивших лечение в условиях кардиологического отделения московской ГКБ № 59.
Все пациенты, в соответствии с рекомендациями по ведению пациентов с СН [6], получали ингибиторы ангиотензин-превращающего фермента, бетаадреноблокаторы, петлевые диуретики, 9 из этих пациентов получали антагонисты альдостерона.
В исследование включали пациентов в стабильном состоянии (отсутствие изменения в состоянии или терапии в течение 7 дней, предшествующих исследованию), подписавших информированное согласие на проведение терапии и взятие крови для производства анализов.
В исследование не включали:
В работе использовали реактивы фирмы Sigma: люцигенин, люминол, форбол-миристат ацетат (РМА), формил пептид (FMLP), индапамид, диметилсульфоксид, гемоглобин, пероксид водорода, двухступенчатый градиент фиколл-гипака, а также раствор гепарина (Гедеон Рихтер).
Влияние индапамида на уровень радикалов кислорода было изучено на образцах цельной крови, в суспензиях изолированных нейтрофилов и в бесклеточной среде, генерирующей радикалы кислорода. Эффект оценивали по степени снижения (в %) радикалов кислорода по сравнению с максимальным действием стандартных стимуляторов.
Кровь забирали из локтевой вены утром натощак до очередного приема лекарственных препаратов в пластиковые пробирки, содержание гепарина 30 МЕ/мл. К исследуемым образцам добавляли люминофор люцигенин (конечная концентрация 30 мкМ). Измерение хемилюминисценции проводили на пробах цельной крови объемом 50 мкл и пробах суспензий нейтрофилов - 100 мкл.
Нейтрофилы выделяли из периферической крови пациентов на двухступенчатом градиенте плотности фиколл/гипак. Клетки отмывали и затем культивировали в бесцветной среде Хенкса. Жизнеспособность изолированных нейтрофилов определяли в тесте с витальным красителем - трипановым синим. В опытах использовали суспензии нейтрофилов (1 млн клеток на мл) (не менее 95% живых клеток).
Для исследований в бесклеточной системе к раствору Хенкса (100 мкл) последовательно добавляли люминол (30 мкМ), затем раствор гемоглобина и на их фоне - пероксид водорода (100 мкМ).
Спонтанное и индуцированное стандартными стимуляторами (бактериальный трипептид - FMLP, 3 мкМ и форбол меристат-ацетат-PMA, 1 мкМ), образование радикалов кислорода (супероксид-анионов О2 и гидроксил-радикалов) регистрировали при 25°С на хемилюминометре "Биотокс"-7 (Россия) в непрерывном режиме.
Хемилюминесценцию измеряли в количестве импульсов в сек и оценивали по интегральным значениям светосуммы за 10 минут. Каждое воздействие изучалось не менее чем в 4-6 отдельных опытах.
Статистическую обработку результатов проводили с использованием программы SigmaPlot. Данные представлены в виде среднего арифметического значения ± стандартного отклонения. Достоверными считали различия при р<0,05).
Результаты
При изучении хемолюминесценции образцов цельной крови и суспензий нейтрофилов пациентов с СН было отмечено спонтанное монотонное увеличение уровня радикалов кислорода во времени, которое возникает в результате взаимодействия клеток со стенками кюветы. Относительное увеличение этого показателя варьировало от 1,5 до 2,3 раза. Добавление PMA (1 мкМ) к суспензии нейтрофилов сопровождалось выраженным увеличением в среднем в 3,3±1,2 раза уровня супероксид-анионов.
Добавление индапамида на максимуме ответа на PMA приводило к выраженному снижению уровня радикалов кислорода. Данный ингибиторный эффект регистрировался при концентрациях индапамида от 0,5 мкМ и выше.
На рисунке 1 в качестве примера приведено изменение хемилюминисценци суспензии нейтрофилов, выделенной из крови пациента Б. с СН II ФК по NYHA.
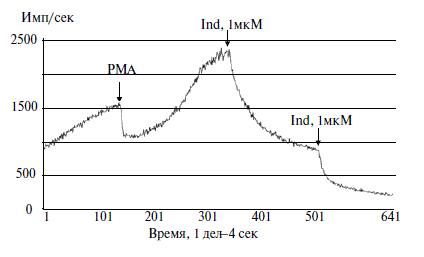
На рисунке 2 приведена концентрационная зависимость ингибиторных эффектов индапамида.
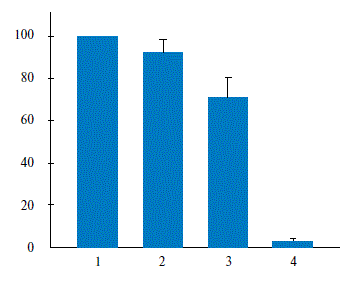
*- наличие достоверного (р=0,01) различия по сравнению с действием PMA.
Видно, что индапамид в концентрации 0,1 мкМ снижал уровень радикалов кислорода, однако этот эффект был недостоверен; но в концентрациях 0,5; 1,0 и 2,0 мкМ эффекты были статистически достоверными.
Аналогичные данные по концентрационной зависимости индапамида были получены на пробах цельной крови (рис. 3).
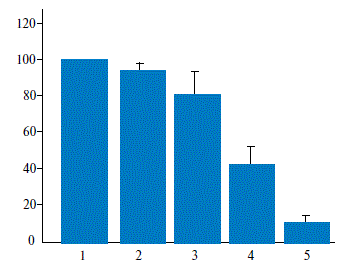
Видно, что индапамид оказывал ингибиторные эффекты в более высоких концентрациях, чем в суспензиях нейтрофилов.
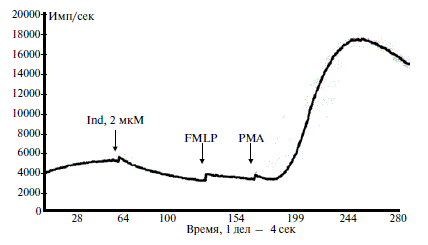
На рисунке 4 показан типичный ответ на добавление индапамида к пробе цельной крови одного из пациентов.
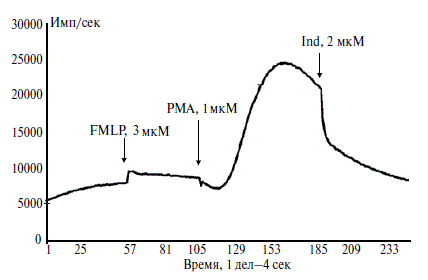
Примечание: по оси абсцисс - время (1 деление - 4 сек); по оси ординат - хемилюминесценция в имп/сек.
Индапамид в концентрации 2 мкМ снижал уровень радикалов кислорода, индуцированных добавлением FMLP и PMA, до исходных значений.
Индапамид эффективно снижал спонтанную хемилюменсценцию и амплитуду ответа на стандартные стимуляторы (рис. 5).
Примечание: Ind - 2 мкМ; FMLP - 3 мкМ; РМА - 1 мкМ.
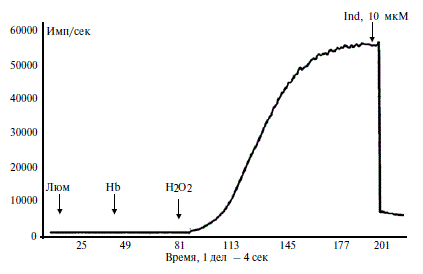
При проведении серии опытов в бесклеточной системе, в которой радикалы кислорода образуются в результате действия пероксида водорода на ионы железа с переменной валентностью, локализованные в гемоглобине, индапамид (10 мкМ) снижал уровень радикалов кислорода до базального значения (рис. 6).
Обсуждение
Характерной особенностью фагоцитов крови практически всех пациентов с СН является наличие предактивированных (праймированных) фагоцитов, о чем свидетельствует "спонтанное" образование супероксид - анионов, наблюдаемое в первые минуты измерений. В состоянии покоя фагоциты крови не могут в выраженной степени подвергаться стимуляции, сопровождающейся секреций протеолитических ферментов, больших количеств радикалов кислорода и освобождением других биологически высоко - активных соединений, способных вызывать повреждение клеток крови и сосудов. Физиологический смысл такого запрета, очевидно, обусловлен предупреждением цитотоксического воздействия стимулированных фагоцитов на свое микроокружение в кровеносном сосуде. При развитии воспаления в какой либо ткани, включая сердце, фагоциты крови получают химические сигналы, которые возникают при гибели клеток. Такие сигналы активируют метаболизм фагоцитов, а также индуцируют экспрессию на их плазматической мембране молекул адгезии, что способствует торможению их перемещения с током крови и заканчивается фиксацией на поверхности эндотелиальных клеток сосудов в пораженной ткани. В это время осуществляется переход фагоцитов из состояния покоя в состояние предактивации (праймирования), что потенцирует последующий ответ фагоцитов на стимулирующие агенты в зоне воспаления. Полученные данные позволяют сделать заключение о том, что в крови пациентов с СН находятся предактивированные фагоциты, которые морфологически не отличаются от покоящихся клеток. Наличие таких клеток, по-видимому, может выступать в качестве маркера воспаления в сердце при этой патологии.
Результаты, полученные в данном исследовании, свидетельствуют о том, что индапамид в низких концентра циях оказывает выраженный антиоксидантный эффект на образцы цельной крови и суспензии изолированных нейтрофилов у пациентов с СН. Характерным признаком СН является асептическое воспаление, которое обусловлено повреждением и некрозом клеток сердца вследствие оксидативного стресса, нарушения ионного гомеостаза и перегрузки кардиомиоцитов ионами Са [2]. Асептическое воспаление находит свое отражение в увеличении в крови уровней провоспалительных цитокинов и возрастании количества провоспалительных клеток, среди которых важное значение имеют фагоциты крови - нейтрофилы и моноциты [5], поступающие в пораженную область миокарда. Фагоциты ответственны за удаление поврежденных и погибших клеток сердца, что создает благоприятные условия для последующей клеточной репарации и восстановления функциональной активности миокарда, а при инфаркте миокарда - за образование соединительно-тканного рубца. Однако неадекватный ответ фагоцитов на активацию вызывает генерацию больших количеств супероксиданионов НАДФН-оксидазным ферментативным комплексом фагоцитов, что, наряду с секрецией протеолитических ферментов, неблагоприятно действует на высокочувствительные к оксидативному стрессу эндотелиальные клетки микрососудов и способствует нарушению потока крови [4, 5]. Экспериментально показано, что снижение уровня радикалов кислорода или подавление хемотаксиса и активности фагоцитов эффективно уменьшает повреждение клеток сердца [7, 8].
Диуретики являются основным классом препаратов, который используют для лечения пациентов с СН при появлении признаков застоя, причем при минимальных проявлениях рекомендуют начинать терапию с тиазидных или тиазидоподобных диуретиков [6]. Кроме того, показано, что диуретики являются одним из наиболее эффективных классов препаратов для предупреждения развития СН у пациентов с артериальной гипертонией [9]. Индапамид - тиазидоподобный диуретик, который оказывает выраженное антигипертензивное действие. Причем, кроме прямого салуретического эффекта, он обладает дополнительными видами активности, включая вазодилатирующее действие, расслабление гладких мышц артерий, уменьшение периферического сопротивления сосудов, уменьшение гипертрофии левого желудочка, снижение риска неблагоприятных сердечно-сосудистых событий у пациентов с артериальной гипертонией [10]. Показано также, что индапамид оказывает антиоксидантное действие как в модельных системах, так и в гомогенатах клеток: он вызывал элиминацию стабильных свободных радикалов дифенил-пикрилгидразина, снижал образование малонового диальдегина из липидных пероксидов в гомогенате мозга крыс, а также уменьшал окисление линоленовой кислоты в системе ксантин/ксантиноксидаза, генерирующей супероксид-анионы [11, 12]. Необходимо отметить, что антиоксидантной активностью обладает тиазидоподобный диуретик индапамид и его метаболит 5-ОН индапамид, но не тиазидные диуретики [13]. Очевидно, что это может быть связано со структурными особенностями индапамида. В его молекулу входит остаток индола и одна сульфонамидная группа, но нет тиазидного кольца. Снижение уровня свободных радикалов под влиянием индапамида в эксперименте на гипертензивных крысах линии Dahl оказывало цитопротекторный эффект на клетки почек [14]. Показано, что у спонтанно гипертензивных крыс индапамид предупреждал развитие фиброза миокарда, но не влиял на активность NOS, а также экспрессию двух изоформ этого фермента - eNOS и iNOS в левом желудочке. По-видимому, защитное влияние индапамида в отношении фиброза связано с его антиоксидантными свойствами, но не с системой оксида азота [15].
Важно подчеркнуть, что действие низких концентраций индапамида на уровни радикалов кислорода в нашей работе было получено на провоспалительных фагоцитах крови пациентов с СН, а не на лабораторных животных. В связи с этим можно предположить, что индапамид может оказывать противовоспалительное и антиоксидантное действие не только при СН, но и других сердечно-сосудистых заболеваниях.
Следует также отметить, что антиоксидантное действие индапамида может быть обусловлено его прямым взаимодействием с радикалами кислорода, о чем свидетельствуют результаты опытов в бесклеточной системе.
Эти результаты хорошо согласуются с ранее полученными данными на других модельных системах in vitro, генерирующих радикалы кислорода: изолированных клетках и сердцах лабораторных животных, а также в опытах на лабораторных животных in vivo [9-15]. Такой эффект индапамида, по крайней мере, отчасти, может быть ответственен за уменьшение уровня супероксид - анионов в суспензиях нейтрофилов и образцах цельной крови пациентов с СН, подвергшихся воздействию стимуляторов.
1. Swynghedauw B. Molecular mechanisms of myocardial remodeling. Physiol Rev. 1999; 79 (1): 215-62.
2. Santos C. X. C., Anilkumar N., Zhang M., et al. Redox signaling in cardiac myocytes. Free Radic Biol Med. 2011; 50 (7): 777-93.
3. Sirker A., Zhang M., Murdoch C. et al. Involvement of NADPH oxidases in cardiac remodeling and heart failure Am J Nephrol. 2007; 27 (6): 649-60.
4. Jordan J. E., Zhi-Qing Zhao, Vinten-Johansen J. The role of neutrophils in myocardial ischemia-reperfusion injury. Cardiovasc. Res., 1999, 43, 860-78.
5. Vinten-Johansen J. Involvement of neutrophils in the pathogenesis of lethal myocardial reperfusion injury. Cardiovasc. Res. 2004; 61 (3): 481-97.
6. National guidelines and OSSN for the diagnosis and treatment of chronic heart failure (third revision) Heart failure. 2010; 11 (1):3-62 Russian (Национальные рекомендации ВНОК И ОССН по диагностике и лечению ХСН (третий пересмотр) Сердечная Недостаточность. 2010; 11 (1): 3-62).
7. Viswanathan G. Neutrophils and myocardial injury: Cause or Effect-That is the Question! South. Med. J. 2008; 101 (1): 7-8.
8. Rashidi F., Rashidi A., Golmohamadi A., et al. Does absolute neutrophilia predict early congestive heart failure after acute myocardial infarction? A cross-sectional study. South. Med. J. 2008; 101 (1): 19-23.
9. Sciarretta S., Palano F., Tocci G., et al. Antihypertensive treatment and development of heart failure in hypertension: a Bayesian network meta-analysis of studies in patients with hypertension and high cardiovascular risk. Arch Intern Med. 2011;171 (5): 384-94.
10. Waeber B., Rotaru C., Feihl F. Position of indapamide, a diuretic with vasorelaxant activities, in antihypertensive therapy. Expert Opin Pharmacother. 2012; 13 (10): 1515-26.
11. Uehara Y., Shirahase H., Nagata T., et al. Radical scavengers of indapamide in prostacyclin synthesis in rat smooth muscle cell. Hypertension. 1990; 15 (2):216-24.
12. Tamura A., Seto T., Fujii T. Antioxidant activity of indapamide and its metabolites. Chem Pharm Bull (Tokyo). 1990; 38 (1): 255-7.
13. Uehara Y, Kawabata Y, Shirahase H. et al. Oxygen radical scavengers and renal protection by indapamide diuretic in salt-induced hypertention of Dahl strain rats. J Cardiovasc Pharmacol. 1993; 22, Suppl 6: S42-6.
14. Vergely C., Walker M. K., Zeller M. et al. Antioxidant properties of indapamide, 5-OH indapamide and hydrochlorothiazide evaluated by oxygen-radical absorbing capacity and electron paramagnetic resonance Mol.Cell Biochem. 1998; 178 (1-2): 151-5.
15. Janega P., Kojsova S., Jendekova L. et al. Indapamide-Induced Prevention of Myocardial Fibrosis in Spontaneous Hypertension Rats Is Not Nitric Oxide-Related. Physiol Res. 2007; 56 (6): 825-8.
