Нейротропный подход к лечению мультиинфарктной деменции с использованием холина альфосцерата
Статьи Опубликовано в журнале:
« Международный неврологический журнал » №3 (65), 2014г. Alberto MURATORIO1, Ubaldo BONUCCELLI1, Angelo NUTI1, Noe BAVPISTINI2, Stefano PASSERO2, Vittoria CARUSO2, Barbara BATANI2, Alberto BARONI3, Federico MAYER3, Tiziana SORBI3, Attilio FRANCIOSI4, Gianni MORO4, Luciano AGOSTINI5, Massimo PICCIRILLI5, Diana SCATOZZA6
1Istituto di Clinica Neurologica, Università di Pisa, Ospedale S. Chiara, Pisa
2 Istituto di Clinica delle Malattie Nervose e Mentali, Università di Siena, Siena
3 Centro di Geriatria Fraticini, I.N.R.C.A., Firenze
4 Servizio di Neurologia, Ospedale Civile di Arzignano, Vicenza
5 Clinica Neurologica, Università di Perugia, Perugia
6 Direzione Medico Scientifica, Italfarmaco S.p.A., Milano, Italy
Резюме. Многоцентровое открытое рандомизированное контролируемое клиническое исследование было проведено с целью сравнительной оценки эффективности и переносимости холина альфосцерата (L-α-глицерилфосфорилхолина) и цитиколина (ЦДФ-холина), используемых в дозе 1 г/сут внутримышечно, у 112 пациентов с мультиинфарктной деменцией легкой или средней степени тяжести.
После 90-дневного периода лечения пациенты находились под наблюдением в течение еще 90 дней без проведения терапии для контроля продолжительности сохранения результатов. Всего 97 пациентов завершили период лечения, из них 73 завершили период наблюдения. Восемнадцать пациентов выбыло из исследования вследствие несоблюдения режима и схемы терапии, а 21 выбывший пациент не находился под наблюдением ни в одном из центров. До начала исследования пациенты находились под наблюдением 2 недели, в течение которых были отменены все другие препараты, которые могли повлиять на результат исследования. Контроль клинической эффективности осуществлялся путем сравнения результатов в начале исследования, через 30 дней, в конце лечения и в конце периода наблюдения по следующим психометрическим тестам: шкале клинической гериатрической оценки компании «Сандоз» (Sandoz Clinical Assessment Geriatric (SCAG) Rating Scale), шкале оценки деменции Блесседа (Blessed Dementia Scale, BDS), шкале Блесседа для оценки информации, памяти и концентрации (Blessed Information, Memory, Concentration test, BIMC), шкала памяти Векслера (Wechsler Memory Scale, WMS), шкала быстрой оценки степени нарушения трудоспособности 2 (Rapid Disability Rating Scale 2, RDRS-2), шкале беглости речи (Word Fluency Test, WFT), жетонному тесту (Token test)*, а также простому копированию рисунков (Simple Drawing Copy, SDC). У пациентов, получавших холина альфосцерат, в конце лечения отмечалось значительное улучшение когнитивных и поведенческих функций, а также способности к самообслуживанию по сравнению с исходными значениями. Это улучшение также было очевидным и в конце периода наблюдения. Сравнение клинических результатов терапии холина альфосцератом и цитиколином показывает, что согласно оценкам по BDS, WMS, RDRS-2 и SDC, выполненным по окончании терапии, а также согласно оценкам по BDS, WMS, SCAG и Token test, выполненным по окончании периода наблюдения, более эффективной была терапия холина альфосцератом, нежели цитиколином.
* - Жетонный тест (the Token Test) был разработан для количественной оценки нарушений понимания речи пациентами с дисфазией.
Введение
Процесс старения мозга характеризуется целым рядом расстройств, затрагивающих локальный метаболизм, региональное кровоснабжение и доступность нейротрансмиттеров, которые приводят к прогрессирующей деградации процессов формирования памяти. Это «физиологическая» психическая деградация, которая может быть компенсирована или может усугубляться другими патологическими процессами, такими как болезнь Альцгеймера и сосудистая деменция.
Мультиинфарктная деменция (МИД), составляющая 20 % от общего числа всех деменций [2], характеризуется множественными инфарктами, различными по степени и локализации. Диагноз может быть поставлен на основании клинических данных и диагностических исследований [2, 3]. Клинический подход к тактике ведения сосудистых деменций и МИД заключается в предотвращении процесса дальнейшего повреждения мозговой ткани путем контроля известных факторов риска, таких как агрегация тромбоцитов и образование тромбов, высокое артериальное давление, диабет и нарушение уровня липидов в крови [2].
Исследования, проведенные у пациентов с болезнью Альцгеймера или МИД, показали, что когнитивные нарушения связаны с ослаблением работы холинергической системы [4], а именно потерей холинергических нейронов и уменьшением выработки нейротрансмиттера ацетилхолина [5, 6]. Кроме того, была установлена прямая положительная корреляция между наличием холина и концентрацией ацетилхолина в головном мозге [7, 8].
Экспериментальное наблюдение, проводимое в условиях пониженного холинергического синтеза и повышенного нейронного запроса, в котором нейроны повышают свою способность захватывать экзогенный холин [9, 10], показывает, что системное введение предшественника холина противодействует биохимическим нарушениям в холинергической системе и тем самым улучшает когнитивную функцию.
Холина альфосцерат* является производным фосфатидилхолина, который увеличивает синтез и высвобождение ацетилхолина как in vitro [11], так и in vivo [12] в экспериментах на животных, а также предотвращает скополамин-индуцированный холинергический дефицит и амнезию у молодых и старых крыс [1].
Аналогичные результаты были получены у здоровых волонтеров, у которых повторное пероральное введение холина альфосцерата (1200 мг в день в течение 10 дней) предотвращало появление амнестического дефицита, вызываемого скополамином [13].
Цель нашего исследования заключалась в сравнении результатов 3-месячного лечения холина альфосцератом и цитиколином при оценке когнитивных и поведенческих функций у пациентов с легкой и средней степенью тяжести МИД, а также в наблюдении длительности сохранения этих эффектов в течение 3-месячного периода при отсутствии терапии.
Пациенты и методы
В исследование были включены мужчины и женщины в возрасте от 50 до 80 лет. Диагноз МИД ставился при наличии двух или более параметров: деменция, диагностированная при клиническом обследовании, оценке по шкале деменции Блесседа (Blessed Dementia Scale, BDS) и других скрининговых обследованиях когнитивных функций; патологические изменения, выявляемые при нейропсихологических тестах, например по шкале памяти Векслера (Wechsler Memory Scale, WMS); и патологические отклонения, выявляемые при помощи нейрорадиологических методов обследования, например, при наличии одного или нескольких очагов низкой плотности, подтверждаемых с помощью компьютерной томографии, или одного или нескольких очагов инфаркта в белом веществе, подтверждаемых с помощью магнитно-резонансной томографии, в соответствии с критериями Loeb [14]. Критерии исключения были следующими: оценка по модифицированной шкале ишемии Hachinski от 5 до 10 баллов [15]; 12–24 балла по краткой шкале оценки психического статуса [16], оценка по шкале депрессии Гамильтона менее 22 [17]; 3–5-я стадии по шкале ухудшения общего состояния Reisberg [18]. Все пациенты дали информированное согласие на участие в исследовании.
Пациентов не включали в исследование, если они имели первичные дегенеративные неврологические заболевания; деменцию вследствие инфекционных, воспалительных, метаболических или эндокринных заболеваний; болезнь Паркинсона, психические заболевания, перенесенный в анамнезе инсульт в течение 6 месяцев, предшествующих исследованию; опухолевые и травматические поражения головного мозга. Также исключили алкоголизм или злоупотребление наркотиками; предыдущее лечение нейролептиками, антидепрессантами, ноотропными препаратами или метилдопой, резерпином или клофелином.
В течение 3 месяцев лечения, а также 3 месяцев последующего наблюдения допускалось применение сопутствующей терапии низкими дозами транквилизаторов, если она применялась ранее на протяжении более 3 месяцев, а также антиагрегантов и антагонистов кальция.
Дизайн исследования
В данном открытом контролируемом рандомизированном клиническом исследовании приняли участие пять клинических или университетских центров. За две недели до начала исследования были получены истории болезни всех пациентов, и каждый пациент прошел нейропсихологическую оценку, а также клинические и неврологические обследования. Биохимический скрининг включал стандартные лабораторные анализы крови и мочи. В течение этого 2-недельного периода был отменен прием любых препаратов, которые могли как-либо повлиять на результат исследования. Пациенты, которые соответствовалm и критериям включения, были рандомизированы в две группы терапии: холина альфосцерата или цитиколина в дозе 1 г/сут внутримышечно. Период лечения продолжался 90 дней, после чего пациенты находились под последующим динамическим наблюдением в течение 90 дней без приема препаратов.
Параметры оценки
Клиническую эффективность терапии определяли с помощью следующих шкал и нейропсихологических тестов: шкалы оценки деменции Блесседа, шкалы Блесседа для оценки информации, памяти и концентрации (Blessed Information, Memory, Concentration test, BIMC) [19]; шкалы клинической гериатрической оценки компании Сандоз (Sandoz Clinical Assessment Geriatric (SCAG) Rating Scale) [20]; шкалы памяти Векслера [21]; шкалы беглости речи (Word Fluency Test, WFT) [22]; жетонного теста (Token test) [23]; простого копирования рисунков (Simple Drawing Copy, SDC) [24]; шкалы быстрой оценки степени нарушения трудоспособности 2 (Rapid Disability Rating Scale 2, RDRS-2) [25].
Клиническую переносимость оценивали путем регистрации неблагоприятных эффектов, которые имели место во время лечения. Биологическую переносимость оценивали с помощью ряда лабораторных исследований, в том числе общего анализа крови, липидного профиля, уровня гликемии, электролитов, исследования функции печени и почек и полного анализа мочи, которые выполнялись перед исследованием и в конце периода лечения.
Основные показатели состояния организма, такие как систолическое и диастолическое артериальное давление и частота сердечных сокращений, измерялись на каждом медицинском осмотре.
Статистический анализ
Для оценки эффективности переменных был использован дисперсионный анализ по плану с расщепленными делянками. Для выполнения множественных сравнений в пределах одной терапевтической группы и между группами использовалась дисперсия суммарной погрешности.
Результаты
Из 112 пациентов, включенных в исследование, 97 завершили период лечения, из них 73 завершили период последующего наблюдения. Пятнадцать пациентов выбыли в первом периоде исследования и три — во время периода последующего наблюдения, в основном вследствие плохого соблюдения режима терапии; 21 пациент в одном из центров не завершил период последующего наблюдения вследствие организационных проблем.
Из 97 пациентов (63 мужчины и 34 женщины), которые завершили период лечения, 48 получали холина альфосцерат и 49 — цитиколин. Эти две группы были сопоставимы по полу и возрасту (табл. 1).
Тяжесть заболевания была одинаковой в обеих группах пациентов, как это было оценено по психометрическим тестам, проводимым перед включением пациентов в исследование (табл. 2). Среди 73 пациентов (48 мужчин и 25 женщин), которые завершили период последующего наблюдения, 36 были из терапевтической группы, принимавшей холина альфосцерат, и 37 — из группы цитиколина.
Период терапии
В табл. 3 приведены средние значения (± стандартное отклонение (СО)) результатов обследований пациентов, завершивших период терапии. В начале исследования результаты обследований пациентов, рандомизированных в терапевтические группы, одна из которых принимала холина альфосцерат, а другая — цитиколин, были похожими. По завершении периода терапии анализ, проведенный внутри каждой из групп, показал, что у пациентов, получавших холина альфосцерат, значительно улучшились по сравнению с исходными значениями оценки по BDS и BIMC (P При терапии цитиколином также наблюдали улучшение, но изменения коснулись только результатов по WFT, которые значительно отличались от исходных (Р Период последующего наблюдения
Результаты исследований 73 пациентов, завершивших период последующего наблюдения, представлены в табл. 4. По окончании периода последующего наблюдения результаты обследования 36 пациентов в терапевтической группе, получавшей холина альфосцерат, ничем не отличались от результатов, полученных в конце периода терапии, и по-прежнему значительно отличались от исходных значений (P Спустя 90 дней после прекращения терапии у 37 пациентов в терапевтической группе, получавшей цитиколин, оценка в баллах по всем тестам, кроме теста беглости речи, была ниже, чем в конце периода терапии (P Обсуждение и заключение
Мультиинфарктная деменция — это сm cиндром, который в первую очередь обусловлен фокальным или генерализованным (мультифокальным) снижением кровоснабжения нескольких областей головного мозга, что приводит к местной гипоксии или аноксии (ишемическому инфаркту) с последующими неврологическими нарушениями [26]. Все эти вместе взятые факторы составляют нейропатологическую основу прогрессирующего ухудшения умственной деятельности, поведения и личности, что выражается клинически как деменция [27].
Таблица 1.
Характеристики пациентов в начале исследования
| Характеристика | Холина альфосцерат | Цитиколин |
|---|---|---|
| Количество пациентов | 57 | 55 |
| Пол | ||
| Мужчины | 39 | 38 |
| Женщины | 18 | 17 |
| Возраст (лет), среднее значение ± СО | 68,6 ± 6,5 | 68,5 ± 6,3 |
| Рост (см), среднее значение ± СО | 166,5 ± 6,9 | 166,6 ± 7,3 |
| Вес (кг), среднее значение ± СО | 67,8 ± 8,2 | 68,6 ± 8,8 |
| Сопутствующие заболевания | ||
| Сердечно-сосудистые | 24 | 15 |
| Респираторные | 0 | 4 |
| Желудочно-кишечные | 4 | 0 |
| Кожные | 0 | 1 |
| Опорно-двигательной системы | 2 | 6 |
| Эндокринологические | 2 | 1 |
| Почек | 2 | 1 |
| Метаболические расстройства | 2 | 3 |
Таблица 2.
Исходные психометрические характеристики
| Шкала | Холина альфосцерат | Цитиколин |
|---|---|---|
| Модифицированная шкала ишемии Hachinski | 7,79 ± 1,38 | 7,51 ± 1,47 |
| Шкала депрессии Гамильтона | 9,82 ± 4,74 | 9,07 ± 4,52 |
| Краткая шкала оценки психического статуса | 19,59 ± 2,89 | 19,85 ± 3,15 |
| Оценка ухудшения общего состояния Reisberg | 3,65 ± 0,66 | 3,45 ± 0,68 |
Таблица 3.
Результаты исследований в период лечения (среднее значение ± СО)
| Шкала | Препарат | Исходное значение | Через 30 дней | По окончании терапии |
|---|---|---|---|---|
| BDS | Холина альфосцерат | 7,13 ± 4,98 | 6,22 ± 4,53а | 5,78 ± 4,43а |
| Цитиколин | 6,31 ± 3,99 | 6,43 ± 4,16б | 6,62 ± 4,70в | |
| BIMC | Холина альфосцерат | 26,61 ± 5,88 | 27,73 ± 6,54г | 28,38 ± 7,06а |
| Цитиколин | 28,05 ± 5,57 | 28,60 ± 6,01 | 28,99 ± 6,42 | |
| SCAG | Холина альфосцерат | 43,44 ± 13,65 | 42,30 ± 11,98 | 39,98 ± 12,12а |
| Цитиколин | 43,08 ± 14,41 | 42,22 ± 13,10 | 41,65 ± 13,95 | |
| WMS | Холина альфосцерат | 72,00 ± 10,38 | 81,00 ± 13,65a | 83,80 ± 14,24а |
| Цитиколин | 71,54 ± 11,60 | 74,09 ± 13,21в | 74,54 ± 14,19в | |
| RDRS-2 | Холина альфосцерат | 27,91 ± 5,51 | 27,36 ± 5,18 | 26,64 ± 4,55а |
| Цитиколин | 26,14 ± 5,28 | 25,67 ± 5,01 | 26,04 ± 5,49б | |
| WFT | Холина альфосцерат | 7,56 ± 6,63 | 8,39 ± 7,08 | 9,58 ± 7,94а |
| Цитиколин | 7,93 ± 5,52 | 9,64 ± 6,86а | 9,71 ± 7,65а | |
| Token test | Холина альфосцерат | 25,69 ± 5,78 | 27,08 ± 5,49а | 27,57 ± 5,24а |
| Цитиколин | 26,57 ± 5,64 | 27,38 ± 5,67 | 27,30 ± 5,43 | |
| SDC | Холина альфосцерат | 11,42 ± 5,29 | 11,67 ± 5,17 | 12,55 ± 5,28г |
| Цитиколин | 12,39 ± 4,61 | 12,93 ± 4,78 | 12,34 ± 4,74б | |
| Примечания: здесь и в табл. 4: а — Р б — P в — P г — P | ||||
Таблица 4.
Результаты исследований в течение периода последующего наблюдения (среднее значение ± СО)
| Шкала | Препарат | Исходное значение | По окончании терапии | Период наблюдения |
|---|---|---|---|---|
| BDS | Холина альфосцерат | 6,45 ± 5,29 | 5,09 ± 4,35а | 5,27 ± 4,59а |
| Цитиколин | 5,62 ± 4,14 | 5,88 ± 4,89в | 5,94 ± 5,55в | |
| BIMC | Холина альфосцерат | 27,25 ± 5,95 | 28,75 ± 7,20г | 29,28 ± 7,1а |
| Цитиколин | 27,82 ± 5,94 | 29,01 ± 6,88 | 28,35 ± 7,16 | |
| SCAG | Холина альфосцерат | 40,00 ± 12,59 | 36,86 ± 11,12а | 37,03 ± 12,56а |
| Цитиколин | 40,57 ± 13,56 | 38,89 ± 13,08 | 41,00 ± 14,92б | |
| WMS | Холина альфосцерат | 72,43 ± 10,64 | 84,14 ± 14,71а | 82,64 ± 15,52а |
| Цитиколин | 71,54 ± 11,60 | 74,54 ± 14,19в | 73,59 ± 15,76в | |
| RDRS-2 | Холина альфосцерат | 27,00 ± 5,52 | 26,08 ± 4,20г | 26,17 ± 4,89г |
| Цитиколин | 26,67 ± 5,56 | 25,54 ± 5,83 | 26,27 ± 6,52 | |
| WFT | Холина альфосцерат | 7,36 ± 5,41 | 9,24 ± 6,96а | 9,24 ± 6,97а |
| Цитиколин | 7,67 ± 5,85 | 9,51 ± 7,88г | 9,46 ± 8,38г | |
| Token test | Холина альфосцерат | 25,17 ± 6,19 | 27,30 ± 5,47а | 27,05 ± 5,64а |
| Цитиколин | 25,37 ± 5,81 | 26,26 ± 5,75 | 25,35 ± 6,48б | |
| SDC | Холина альфосцерат | 9,67 ± 4,44 | 11,33 ± 4,81а | 10,45 ± 4,89 |
| Цитиколин | 10,71 ± 3,50 | 10,65 ± 3,81б | 10,46 ± 4,05 |
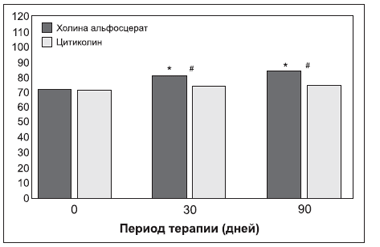
Рисунок 1. Общая оценка по шкале памяти Векслера у пациентов, получавших холина альфосцерат и цитиколин.
Множественные сравнения в процессе терапии (* — Р
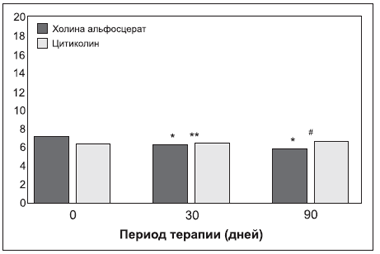
Рисунок 2. Общая оценка по шкале оценки деменции Блесседа у пациентов, получавших холина альфосцерат и цитиколин.
Множественные сравнения в процессе терапии по сравнению с исходными значениями (* — Р и между терапевтическими группами (** — Р
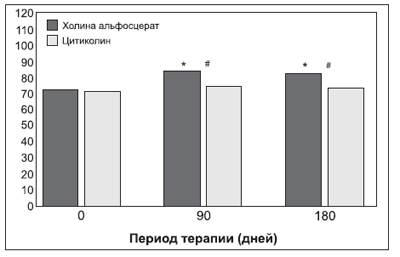
Рисунок 3. Общая оценка по шкале памяти Векслера в процессе терапии и в период
последующего наблюдения по сравнению с исходными значениями (* — Р и между терапевтическими группами (# — Р
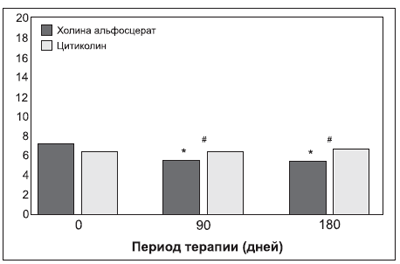
Рисунок 4. Общая оценка по шкале оценки деменции Блесседа у пациентов в процессе терапии и последующего периода наблюдения
по сравнению с исходными значениями (* — Р
Многочисленные исследования, проведенные с целью установления критериев правильной постановки диагноза МИД, показали, что исход клинико-диагностического и психометрического тестирования коррелирует с биохимическими и инструментальными данными [14]. Надежность психометрических тестов делает необходимым их применение при оценке терапевтической эффективности фармакологических препаратов, при условии, что использовался набор тестов, разработанный с целью выявления различных аспектов деменции [28].
Наше исследование было проведено с целью выявить влияние 3-месячной терапии холина альфосцератом на когнитивную и поведенческую симптоматику у пациентов, страдающих МИД легкой и средней степени тяжести, а также отследить длительность сохранения клинических результатов. Мы сравнили результаты терапии холина альфосцератом и цитиколином; холина альфосцерат является широко изученным препаратом, применяемым в лечении деменции [29, 31]. Результаты, полученные в этом исследовании, показывают, что прием холина альфосцерата в дозе 1 г/сут в течение 90 дней оказывает положительное влияние на память, когнитивные и поведенческие функции, оцениваемые по BDS, BIMC, SCAG, WMS и RDRS-2, а также на афазию и апраксию, оцениваемые с помощью WFT, Token test и SDC.
Исследование определило, что лечение холина альфосцератом было значительно эффективнее, чем терапия цитиколином, который существенно не улучшал любой из исследуемых параметров, за исключением афазии. Результаты, полученные при применении холина альфосцерата, подтверждают выводы, сделанные в экспериментальных исследованиях [1, 11, 32, 33], и указывают на возможную клиническую значимость способности холина альфосцерата повышать уровень нейромедиатора ацетилхолина в головном мозге [12] и улучшать холинергическую передачу [34]. Кроме того, положительное влияние на психические функции и поведение, выявленное в нашем исследовании, было отмечено и в других клинических исследованиях, которые показали, что терапия холина альфосцератом улучшает память, когнитивные и поведенческие функции и праксию у пациентов с сосудистыми или первичными сенильными церебральными нарушениями [35, 37].
Улучшение когнитивных и поведенческих показателей у пациентов, получавших в нашем исследовании холина альфосцерат, сохранялось по истечении 3-месячного периода последующего наблюдения. Эти результаты заслуживают внимания, учитывая, что естественный ход сосудистой деменции приводит к прогрессирующей потере когнитивных функций и нарушению социальных навыков [26]. Abbati и соавт. [38] также наблюдали длительный эффект холина альфосцерата по сравнению с оксирацетамом у пациентов, страдавших органическим сенильным церебральным синдромом и принимавших лечение холина альфосцератом или оксирацетамом в той же дозе (1 г/сут) на протяжении такого же периода (12 недель). Экспериментальные исследования [39, 40] показали, что холина альфосцерат обладает нейропротекторной активностью в отношении нервных структур, участвующих в процессе формирования памяти и запоминания информации, а также центральных областей головного мозга, регулирующих поведение и эмоции. Эту гипотезу о возможном нейропротекторном эффекте холина альфосцерата следует проверить в будущих долгосрочных клинических исследованиях. * - Холина альфосцерат производства компании Italfarmaco SpA, Милан, Италия, зарегистрирован в Украине под торговым названием Глиатилин.
Список литературы
1. Govoni S., Battaini F., Lopez СМ. et al. Effetto antiamnesico di alfa-glicerilfosforilcolina: partecipazione di neuroni colinergici e поп colinergici // Basi Raz. Тек 1991; 21 (Suppl. 2): 59-66.
2. Loeb С Vascular dementia // Dementia. 1990; 1: 175-184.
3. Loeb С Clinical criteria for the diagnosis of vascular dementia // Eur. Neurol. 1988; 28: 87-92.
4. Carlsson A. Brain neurotransmitters in ageing and dementia: Similar changes across diagnostic dementia groups // Gerontology. 1987; 33: 159-167.
5. De Feudis F.V. Central cholinergic system, cholinergic drugs and Alzheimer’s disease. An overview // Drugs Today. 1988; 24: 473-490.
6. Wesnes K., Simpson P., Kidd A. An investigation of the range of cognitive impairments induced by scopolamine 0.6 mg s.c. // Hum. Psychopharmacol. 1988; 3: 27-41.
7. Cohen E.L., Wurtmann R.J. Brain acetyl choline increase after systemic choline administration // Life Sci. 1975; 16: 1095-1102.
8. Schmidt D.E., Wecker L. Central nervous system effects of choline administration evidence for temporal dependence // Neuropharmacology. 1981; 20: 535-539.
9. Wecker L., Schmidt D.E. Central cholinergic function in the rat relationship to choline administration // Life Sci. 1979; 25: 375-384.
10. Wecker L., Goldberg A.M. // International symposium on cholinergic mechanisms. — New York: Plenum Press, 1981.
11. Missale C, Sigala S., Rizzonelli P., Spano P.F. Trasmissione colinergica nel ratto dopo trattamento acuto e cronico cona-GFC // Basi Raz. Ter. 1991; 21 (Suppl. 2): 23-26.
12. Lmperato A., Zocchi A., Angelucci L. Studio «in vivo» degli effetti e del meccanismo d’azione di colina alfoscerato sulla trasmissione colinergica striatale ed ippocampale // Basi Raz. Ter. 1991; 21 (Suppl. 2): 15-22.
13. Canal N., Franceschi M., De Moliner P., Castiglioni С Effetti di colina alfoscerato nella prevenzione delle amnesie indotte da scopolamina e benzodiazepina // Basi Raz. Ter. 1991; 21 (Suppl. 2): 75-78.
14. Loeb C, Gandolfo С Diagnostic evaluation of degenerative and vascular dementia // Stroke. 1983; 14: 399-401.
15. Hachinski V.C., Lassen H.A., Marschal J. Multi-infarct 30. Motta L., Fichera G, Tiralosi G. et al. La citicolina net dementia, a cause of mental deterioration in the elderly // Lancet. trattamento delle cerebrovasculopatie croniche // G. Gerontol. 1984; 1974; 2: 207-209. 32: 753-754.
16. Folstein M.F., Folstein S.E., McHug P.R. Mini Mental 31. Cucinotta D., Romagnoli S., Godoli G. et al. Comparison of State // J. Psychiatr. Res. 1975; 12: 189-198. sulfomucopolysaccharides and cytidine diphosphocholine in the treat-
17. Hamilton M. A rating scale for depression // J. Neurol. ment of multi-infarct dementia // Curr. Ther. Res. 1988; 43: 12-20. Neurosurg. Psychiatr. 1960; 23: 56-62. 32. Canonico PL., Nicoletti F., Scapagnini U. Effetti neurochi-
18. Reisberg B., Ferris S.H., De Leon M.J. et al. The Global De- mici e comportamentali di a-GFC (colina alfoscerato) // Basi Raz. terioration Scale for assessment of primary degenerative dementia // Ter. 1990; 20 (Suppl. 1): 53. Am. J. Psychiatry. 1982; 139: 1136-1139. 33. Drago F., DAgata V, Nardo L. et al. Effetti comportamentali
19. Blessed G., Tomlinson B.E., Roth M. The association be- di a-GFC in modelli di interazione farmacologica // Basi Raz. Ter. tween quantitative measures of dementia and senile changes in the 1991;
21 (Suppl. 2): 67-70. cerebral grey matter of elderly subjects // Br. J. Psychiatry. 1968; 34. Schettini G, Florio T, Ventura C. et al. Effetto del trattamen- 114: 797-811. to prolungato con a-GFC (colina alfoscerato) sull’apprendimento,
20. Venn R.D. The Sandoz Clinical Assessment Geriatric (SCAG) sulla memoria e sulla trasduzione del segnale recettoriale in animali Scale // Gerontology. 1983; 29: 185-198. giovani e invecchiati // Basi Raz. Ter. 1991; 21 (Suppl. 2): 27-34.
21. Wechsler D. A standardized memory scale for clinical use // 35. Frattola L., Piolti R., Bassi S. et al. Multicenter clinical J. Psychol. 1945; 19: 87-95. comparison of the effects of choline alphoscerate and cytidine di-
22. Barbizet J., Duizabo J., Flavigny R. Role des lobes Frontaux phosphocholine in the treatment of multi-infarct dementia // Curr. dans le langage. Un etude neuropsychologique experimentale // Rev. Ther. Res. 1991; 49: 683-693. Neurol. 1975; 131: 525-544. 36. Di Perri R., Coppola G, Ambrosio L.A. et al. A multicentre trial
23. De Renzi E., Vignolo L.A. The Token test: A sensitive test to evaluate the efficacy and tolerability of a-glycerylphosphorylcholine to detect receptive disturbances in aphasia // Brain. 1962; 85: versus cytidine diphosphocholine in patients with vascular dementia // 665-678. J. Lnt. Med. Res. 1991; 19: 330-341.
24. Arrigoni C, De Rossi E. Constructional apraxia and hemi- 37. Bassi S., Albizzati M.G, Piolti R., Frattola L. Esperienza spheric locus of lesion // Cortex. 1964; 1: 170-197. clinica con colina alfoscerato in pazienti affetti da demenza degen-
26. Linn M.W., Linn B.S. The Rapid Disability Rating Scale-2 // erativa primaria e multinfartuale // Gnosis. 1990; 5: 55-62. J. Am. Geriatr. Soc. 1982; 30: 378-382. 38. Abbati C, Rondi G, Rosola R. et al. Nootropic therapy of
26. Scheinberg P. Dementia due to vascular disease. A multifacto- cerebral aging // Adv. Ther. 1991; 8: 251-276. rial disorder // Stroke. 1988; 19: 1291-1299. 39. Amenta F., Bronzetti E., Mancini M. et al. Lnvecchiamento
27. Diagnosis and treatment of old age dementias // Ban ТА., del sistema colinergico ippocampale. Effetti del trattamento con colina Lehmann H.E. (eds). Modern problems in pharmacopsychiatry. — alfoscerato // Basi Raz. Ter. 1991; 21 (Suppl. 2): 35-40. Vol. 23. — Basel: Karger, 1989. — 1-20. 40. Vega J.A., Del Valle M., Amenta F Aspetti immunocitochimici
28. Spinnler H., Tognoni G. Standardizzazione e taratura del sistema nervoso centrale nella senescenza: sensibilita al trattamento italiana di test neuropsicologici // Ltal. J. Neurol. Sci. 1987; 6 con colina alfoscerato // Basi Raz. Ter. 1991; 21 (Suppl. 2): 47-54. (Suppl. 8): 8-20. Перевод с англ. П. Огилько
29. Moglia A., Arrigo A., Bono G. et al. Citicoline in patients with Оригинал статьи опубликован в журнале chronic cerebrovascular disease (CCVD): Quantitative EEG study // Current Therapeutic Research, 1992, Vol. 52, № 5 Curr. Ther. Res. 1984; 36: 309-313.
