Сравнительное клинико-фармакологическое изучение разных лекарственных форм нифедипина у больных артериальной гипертонией в пожилом возрасте
СтатьиОпубликовано в:
Кардиология (Kardiologiya) »» N1, 2000 Л.Б. ЛАЗЕБНИК, О.О. КУЗНЕЦОВ, С.Ф. СОКОЛОВ, В.И. МАЛАХОВ, А.П. РОДИОНОВ, B.C. КУДРИН, И.А. КАБАНОВА
Clinicopharmacological comparison of nifedipine dosage forms in older patients with arterial hypertension
L.B. LAZEBKIK, O.O. KUZNETSOV, S.F. SOKOLOV, V.I. MALAKHOV, A.P. RODIONOV, V.S. KUDRIN, I.A. KABANOVA
Кафедра геронтологии и гериатрии Российской медицинской академии последипломного образования. Российский кардиологический научно-производственный комплекс Минздрава Российской Федерации. Государственный институт доклинической и клинической экспертизы лекарств. Институт фармакологии РАМН. Москва
Дискуссия по поводу безопасности применения блокаторов кальциевых каналов, в частности препарата дигидропиридинового ряда нифедипина, при лечении артериальной гипертонии и ИБС, начавшаяся в 1995 г. [1, 2], привела в настоящее время к пониманию того, что отдаленные результаты лечения зависят от используемой лекарственной формы препарата.
Короткодействующие формы нифедипина, назначаемые в больших дозах, повышают риск неблагоприятных исходов [1-3]. Это может быть связано с вариабельностью уровня АД на протяжении суток и повышением активности симпатико-адреналовой (САС) и, возможно, ренин-ангиотензиновой системы [4-6]. В противоположность этому проведенные исследования показали, что длительнодействуюшие формы нифедипина значительно снижают частоту неблагоприятных исходов в сравнении с плацебо [7] и по отдаленным результатам лечения не отличаются от бета-блокаторов и диуретиков [8, 9].
В отличие от короткодействуюших форм, нифедипины длительного действия снижают вариабельность АД и не оказывают стимулирующего нейрогуморального действия [4-6]. Остается актульной задача по классификации лекарственных форм нифедипина с учетом продолжительности их действия и особенностей фармакодинамических эффектов.
Целью настоящего исследования явилось изучение различий фармакологических эффектов трех лекарственных форм нифедипина, различающихся по своим фармакокинетическим параметрам.
Материал и метолы
Изучали следующие лекарственные формы нифедипина: препарат коринфар в жидкой лекарственной форме - ЖФН (капли во флаконах), драже коринфара по 10 мг (ДН) и таблетки коринфара уно по 50 мг (ретардная форма нифедипина - РФН) производства "Плива" (Германия)
Исследование проводили у 12 больных мягкой и умеренной артериальной гипертонией в сочетании с ИБС в возрасте от 62 до 72 лет (в среднем 67+/-4 года). Средняя масса тела 78+/-7 кг, рост 176+/-7 см.
В исследование включали больных без нарушений функции почек, печени и не имевших в анамнезе язвенной болезни желудка и двенадцатиперстной кишки. Согласно протоколу, перед включением в исследование в течение 5-дневного (контрольного) периода больные не должны были принимать нифедипин, а также лекарственные средства, которые могли бы изменить фармакокинетику исследуемого препарата (диуретики, барбитураты и др.). Всем пациентам за 24 ч перед первым приемом препарата проводили 24-часовое мониторирование ЭКГ и АД.
После контрольного периода в условиях открытого перекрестного исследования в соответствии с планом рандомизации однократно назначали ЖФН в дозе 10 мг. ДН в дозе 10 мг и РФН в дозе 50 мг (прием ЖФН осуществлялся после предварительного разведения в 100 мл воды, таблетированные лекарственные формы препарата не разжевывались). Перед каждым приемом препарата за 1 ч начинали суточное мониторированне ЭКГ и АД. В ходе исследования пациенты получали все три изучаемые лекарственные формы нифедипина. Период между исследованиями составлял 24 ч в случае приема ЖФН и ДН, не менее 5 дней после приема РФН.
Холтеровское мониторирование ЭКГ проводили с помощью аппаратуры "Asirocard" (ЗАО "Медитек", Россия), АД - с использованием прибора "АВР Медитех" (Венгрия). Пробы крови брали через имплантированный в локтевую вену катетер в фиксированные точки времени. За 20-25 мин до приема препарата отбирали контрольную пробу крови в объеме 10 мл.
После приема препаратов производили cepийные заборы крови с временными интервалами, которые зависели от изучаемой лекарственной формы нифедипина: 0,17, 0,33, 0,5, 0,75, 1,0, 1,5, 2,0, 3,0, и 4,0 ч для ЖФН; 0,5, 1,0, 1,5, 2,0, 3,0, 4,0, 6,0, 8,0 и 12,0 ч для ДН; 0,5, 1,0, 2,0, 4,0, 6,0, 8,0, 12,0, 24,0 и 36,0 ч для РФН. Пробы крови брали в положении больного сидя после 10-минутного периода покоя. В свободные промежутки времени пациенты находились в привычном для них режиме двигательной активности.
Кровь центрифугировали при 3000 об/мин, плазму декантировали в полипропиленовые пробирки и хранили при -20°С в темноте. После окончания исследования проводили обработку проб для их качественного и количественного анализа по описанной ниже методике. Кроме определения концентрации нифедипина в сыворотке крови проводили определение уровня катехоламинов: дофамина, 3,4-диоксифенилуксусной кислоты, норадреналина и адреналина [10].
Метод количественного определения нифедипина в плазме крови. К 4 мл плазмы добавляли внутренний стандарт (из расчета на 1 мл плазмы 250 нг феназепама). 0,1 мл 35% NaOH и 16 мл диэтилового эфира, встряхивали 15 мин, центрифугировали при 3000 об/мин, отбирали органический слой и упаривали досуха. К остатку добавляли 0,1 мл ацетонитрила. Пробы анализировали на высокоэффективном жидкостном хроматографе фирмы "Hewlett Packard 1050", интегратор фирмы "Hewlett Packard 3395". Колонка "Sverisorb С" 5 мк, длина 25 см, диаметр 4,6 мм. Для определения нифедипина использовали длину волны 280 нм. Подвижной фазой служили цитратно-фосфатный буфер, ацетонитрил, метанол в соотношении 55:30:15. Скорость потока подвижной фазы 1 мл/мин. Внутренний стандарт - феназепам. Время выхода нифедипина в указанных условиях составляло 5,6 мин. Процент экстракции - 75+/-5. Линейный диапазон определяемых концентраций составлял от 5 до 250 нг/мл.
Для оценки фармакодинамических эффектов нифедипина в контроле и в каждый момент взятия крови определяли систолическое и диастолическое АД, а также среднюю за 5 мин продолжительность интервала R-R. Под гипотензивным эффектом нифедипина понимали снижение диастолического АД на 10 мм рт. ст. и более по сравнению с контрольным уровнем.
Статистический анализ проводили с использованием t-статистики для непарных и парных величин (статистический пакет Microsoft Excel).
Результаты исследования
Изучавшиеся лекарственные формы нифедипина имеют значительные различия в фармакокинетике. После приема ЖФН наблюдалось быстрое поступление препарата в кровоток, что проявилось стремительным нарастанием концентрации препарата в плазме крови с быстрым достижением максимума и последующим резким ее снижением (рис. 1).
Рис. 1. Фармакокинетика различных лекарственных форм нифедипина.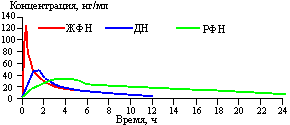
Величина среднего пребывания нифедипина в крови (MRT) после приема ЖФН составляет всего 1,6 ч. В отличие от ЖФН после приема ДН концентрация препарата в плазме нарастает медленнее и также медленнее убывает. После приема РФН аналогичные фармакокинетические процессы после приема РФН замедлены в еще большей степени.
Сравнительные фармакокинетические показатели, характеризующие скорость всасывания и длительность пребывания нифедипина в крови, трех лекарственных Форм представлены в табл. 1. Обращают на себя внимание достоверно более высокие значения Сmax и более низкие значения MRT, характерные для ЖФН и в меньшей степени для ДН в сравнении с РФН.
Таблица 1. Основные фармакокинетические показатели трех лекарственных форм нифедипина
| Показатель | ЖФН | ДН | РФН |
| Cmax, нг/мл | 123,93+/-33,9 | 46,88+/-12** | 33,88+/-12,6** |
| Тmax, нг/мл | 0,37+/-0,16 | 1,21+/-0,33 | 4,0+/-1,86 |
| MRT, ч | 1,6+/-0,18 | 4,57+/-0,77 | 16,29+/-1,6 |
Значения диастолического АД, измеренные в контрольные сутки в момент времени, соответствующий будущему времени приема препаратов, и контрольные значения непосредственно перед приемом препаратов составили соответственно 84+/-6, 83+/-5, 84+/-3 и 83+/-6 мм рт. ст., не отличаясь достоверно друг от друга.
После приема нифедипина происходило снижение как систолического, так и диастолического АД (рис. 2). Снижение диастолического АД в среднем достигало максимума к 30-й минуте после приема ЖФН, будучи статистически значимым (р<0,05) уже на 10-й минуте. Статистически достоверное снижение диастолического АД после приема ДН определено на 30-й минуте, оно достигало максимума к 3-му часу. На фоне действия РФН достоверное снижение диастолического АД наступало на 2-м часу и достигало максимума к 12-му часу. На 12-м часу средний уровень диастолического АД после приема ДН достоверно не отличался от такового в соответствующий час контрольных суток (74+/-6 и 79+/-5 мм рт.ст. соответственно), в то время как на фоне РФН различия были достоверными (69+/-7 и 79+/-5 мм рт. ст. соответственно; р<0,03). К 24-му часу после приема РФН средние значения диастолического АД также отличались от соответствующих его величин в контрольные сутки (71+/-8 и 82+/-4 мм рт. ст.; р<0,03).
Рис. 2. Снижение диастолического АД после приема разных лекарственных форм нифедипина. 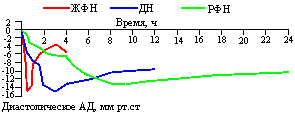
Максимальная степень снижения диастолического АД не имела достоверных различий между лекарственными формами нифедипина и составила 14,6+/-10,3, 15,0+/-6,0 и 13,3+/-8,1 мм рт.ст. для ЖФН, ДН и РФН соответственно.
Систолическое АД претерпевало изменения, повторяющие изменения диастолического АД (рис. 3), причем значения систолического АД тесно коррелировали со значениями диастолического АД (r = 0,93, 0,96 и 0,95 при p<0,005 соответственно для ЖФН, ДН и РФН).
Рис. 3. Снижение систолического АД после приема разных лекарственных форм нифедипина. 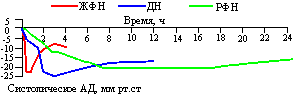
Изменения длительности интервала R-R, хотя и имели тенденцию к укорочению в ранние сроки после приема ЖФН и ДН, не были статистически значимыми.
Гипотензивный эффект после приема ЖФН наступал в среднем через 0,4+/-0,2 ч и сохранялся до 1,8+/-1,2 ч. После приема ДН он достигался через 1,5+/-0,8 ч и сохранялся до 9,2+/-3,4 ч. После приема РФН гипотензивный эффект развивался к 6,3+/-3,8 ч и сохранялся более 24 ч. Различия во времени начала и окончания гипотензивного эффекта между тремя лекарственными формами нифедипина статистически значимы при p<0,001.
Концентрация нифедипина в момент наступления гипотензивного эффекта существенно превышала таковую в момент его исчезновения для всех трех лекарственных форм препарата (табл. 2). При этом концентрация в начале эффекта была наиболее высокой после приема ЖФН, наиболее низкой после приема РФН (различия значимы при сравнении форм нифедипина между собой).
Концентрация препарата в момент исчезновения гипотензивного эффекта после приема ЖФН была выше, чем после приема ДН и РФН, а в двух последних случаях различия не имели статистической значимости (см. табл. 2). Кроме того, указанная величина не имела достоверных отличий от начальных терапевтических концентраций ДН и РФН.
Таблица 2. Средние концентрации нифедипина в момент наступления и исчезновения гипотензивного эффекта при приеме трех лекарственных форм препарата
| Показатель | ЖФН (1) | ДН (2) | РФН (3) | Р1-2 | Р1-3 | Р2-3 |
| Концентрация препарата при наступлении эффекта, нг/мл | 89,8+/-42,4 | 35,2+/-7,4 | 24,9+/-8,2 | <0,002 | <0,0004 | <0,01 |
| Концентрация препарата при исчезновении эффекта, нг/мл | 29,5+/-8,8 | 6,5+/-5,1 | 10,6+/-8,8 | <0,001 | <0,0005 | <0,25 |
| P | <0,009 | <0,002 | <0,01 | - | - | - |
Уровень норадреналина, который успешно был оценен у 10 пациентов, существенно не различался перед приемом каждой из лекарственных форм нифедипина. После приема препаратов при оценке в момент времени, совпадавший с достижением индивидуальной для каждого пациента максимальной концентрации нифедипина, уровень норадреналина в среднем повышался, что было в большей степени выражено в случае приема ЖФН, но наблюдаемые различия не имели статистической значимости (табл. 3).
Таблица 3. Уровни норадреналина в контроле и при максимальной концентрации нифедипина после приема разных его лекарственных форм
| Лекарственная форма | Контроль | Препарат | Прирост |
| (нмоль/мл) | |||
| ЖФН | 0,18+/-0,29 | 0,62+/-0,80 | 0,44+/-0,85 |
| ДН | 0,21+/-0,19 | 0,42+/-0,46 | 0,22+/-0,52 |
| РФН | 0,23+/-0,21 | 0,42+/-0,43 | 0,20+/-0,24 |
| Достоверность различий | нд | нд | нд |
Прирост концентрации норадреналина умеренно коррелировал с концентрацией нифедипина, при которой в начальную фазу изменения АД отмечалось развитие гипотензивного эффекта (начальная терапевтическая концентрация; r = 0,58; p<0,001). Высокая корреляция этих показателей сохранялась при их раздельной оценке для ЖФН (r = 0,67; р<0,05) и ДН (r = 0,77; p<0,01), а для РФН корреляция была умеренной, результат - статистически незначимым (r = 0,45; р<0,15). В свою очередь начальная терапевтическая концентрация нифедипина имела обратную тесную корреляцию со временем наступления терапевтического эффекта, что наилучшим образом описывалось следующей логарифмической зависимостью:
Y = 22,214 Ln(x) + 56,944 (r = 0,75; p<0,0005).
Обсуждение
Разделение лекарственных форм нифедипина на препараты короткого и длительного действия исходно предполагает применение в различных клинических ситуациях и, следовательно, разные отдаленные результаты лечения. Важнейшим отличием галенических форм нифедипина является то, что препараты короткого действия способны в большей степени активизировать САС, что подтверждается результатами прямого изучения уровня норадреналина в крови [5]. Активация САС в свою очередь является одной из реакций организма в ответ на периферическую вазодилатацию и снижение АД, происходящие под влиянием нифедипина.
Установлено, что скорость поступления препарата в системный кровоток определяет степень выраженности ответной реакции организма. Быстрое достижение определенной концентрации нифедипина в крови приводит к меньшему снижению диастолического АД по сравнению со случаем, когда эта же концентрация достигается путем постепенного повышения [11]. В первом случае отмечается значительное увеличение ЧСС, указывающее на активацию САС.
Таким образом, быстрое поступление нифедипина в кpовь не только приводит к развитию нежелательных нейрогуморальных реакций, но и оказывается менее эффективным в плане снижения диастолического АД.
Результатом противодействия нейрогуморального ответа снижению АД под влиянием нифедипина оказываются более высокие концентрации препарата, необходимые для достижения терапевтического эффекта. Чем быстрее нарастает концентрация, тем выше должен быть ее уровень для достижения эффекта.
Это положение наглядно демонстрируют результаты настоящего исследования. Чем короче при приеме той или иной лекарственной формы нифедипина был период Tmax, тем выше оказывалась начальная терапевтическая концентрация нифедипина. Аналогичная зависимость обнаруживается, если величину терапевтической концентрации нифедипина соотнести со временем наступления терапевтического эффекта. Эта концентрация, кроме того, имела положительную корреляцию с приростом уровня норадреналина, указывая на связь между активацией САС и степенью противодействия снижению АД.
Рассматривая величину терапевтических концентраций как косвенный показатель степени активации САС, можно заключить, что для всех изучавшихся лекарственных форм нифедипина появление гипотензивного эффекта сопряжено с большей выраженностью активации САС, по сравнению с моментом исчезновения гипотензивного эффекта.
Обращает на себя внимание тот факт, что степень активации САС в случае приема РФН, которая по фармакокинетическим параметрам приближается к наиболее длительнодействующей гастроинтестинальной форме нифедипина [8], в период наступления эффекта сопоставима со степенью активации САС в период исчезновения эффекта после приема ЖФН, которая является наиболее короткодействующей из всех существующих пероральных форм. Между этими двумя крайними по фармакокинетическим параметрам лекарственными формами находится ДН. Сопоставление его клинико-фармакологических показателей с двумя другими формами указывает на его принадлежность скорее к длительнодействуюшим лекарственным формам: начальная терапевтическая концентрация не отличается от концентрации исчезновения эффекта ЖФН, а концентрация при исчезновении эффекта не отличается от таковой РФН. В дополнение к этому необходимо отметить, что уровни норадреналина при приеме ДН и РФН по абсолютным значениям и его приросту не различались, но были ниже, чем при использовании ЖФН, хотя различия не имели статистической значимости.
Таким образом, результаты настоящей работы показывают, что при разделении лекарственных форм нифедипина на короткодействующие и длительнодействующие, необходимо учитывать не только их фармакокинетические параметры, но и фармакодинамические эффекты, которые могут иметь существенное значение для оценки лекарственных форм с промежуточными фармакокинетическими показателями.
Коринфар - Инструкция
ЛИТЕРАТУРА 1. Psaty B.M., Heckben S. R., Koepsell T.D. et al. The risk of myocardial infarction associated with antihypertensive drug therapies. JAMA 1995; 274:620-625.
2. Furberg C.D., Psaty B.M., Meyer J.V. Dose-related increase in moitelitv in patients with coronary heart disease. Circulation 1995:92.4326-1331.
3. Pahor M., Gurinik J.M., Corti M.C. et al. Long-term survival and use of antihypenensive medications in older persons. J Am GeriatrSoc 1995:43: 1191-1197.
4. Frohlich E.D., McLoughlin M.J., Losern C.J. et al. Hemodynamic comparison of two nifedipine formulations in patients with essential hypertension. Am J Cardiol 1991:68: 1346-1350.
5. Grossman E., Messerli F.H. Effect of calcium antagonists on sympathetic activity. Eur Heart J 19: Suppl F: F27-F31.
6. Ruzicka M., Leenen F.H. Relevance of intermittent increases in sympathetic activity for adverse outcome on short-acting calcium antagonists. In: Hypertension: Pathophysiology, Diagnosis and Management. Eds. J.H. Laragh, B.M. Brenner, 2nd ed. New York: Raven Press 1995: 2815-2825.
7. Gong L., Zhang W., Zhu Y. et al. Shanghai trial of nifedipine in elderly (STONE). J Hypertens 1996:14: 1237-1245.
8. Kloner R.A., Vetrovec G. Long-acting calcium chanel blockers nifedipine GITS and amiodipine in hypertension. Rate of myocardial infarclion. J Am Coil Cardiol 1996; 27:Suppl A: 177A: Abstract.
9. Leader S.G., Mallick R., Briggs N.C. Myocardial infarction in newly diagnosed hypertensive Medical patients free of coronary heart disease and treated with calcium channel blockers. Am J Med 1997:102: 150-157.
10. Kontur P., Dowson R., Monjan A. Manipulation of mobile phase parameter for the HPLC separation of endogenous monoamines in rat brain tissue. J Neurosci Methode 1984:11: 5-18.
11. Kleinbloesern C.H., van Brummelen P., Danlof M. et al. Rate of increase in the plasma concentration of nifedipine as major determinant of its hemodynamic effects in humans. Clin Pharmacol Ther 1987:41: 26-30.
Поступила 20.10.99
Коринфар - Досье препарата
