Критерии безопасности переливания коллоидных растворов у больных с острым повреждением легких
СтатьиОпубликовано в журнале:
Анестезиология и реаниматология № 2, 2006
И. И. Серебрийский, Г. М. Галстян, Н. Б. Боровкова, В. М. Городецкий
Гематологический научный центр РАМН, Москва
Criteria for the safety of transfusion of colloidal solutions in patients with acute lung lesions
I. I. Serebriysky, G. M. Galstyan, N. B. Borovkova, V. M. Gorodetsky The prospective study explored the hemodynamic effects of colloidal solution replacement therapy and the criteria for its safety in patients with acute lung parenchymatous lesions (ALPL) attended by hypoalbuminemia and coagulopathy. There were 68 observations of the effects of colloidal solutions: 20% albumin solution (n=25), freshly frozen plasma (FFP) (n=20), 6% hydroxyethylated starch (HES) 130/0.4 9:1 (n=23). The colloidal solutions were infused at a constant rate; the infusion was stopped until pulmonary wedge pressure (PWP) was 25% greater than its baseline value. Before and after infusion, the parameters of central hemodynamics and oxygen transport, extravascu-lar lung water index (ELWI), pulmonary vascular permeability index (PVPI), and colloid-osmotic pressure (COP) were measured. The infusion volumes were 3.8±0.4, 13.7±1.4, and 13.4±1.3 ml/kg for 20% albumin solution, 6% HES 130/0.4, and FFP, respectively. The PWP-COP gradient increased in all groups. After FFP infustion, there was an increase in ELWI and lung shunt. After 20% albumin solution, there was a delayed increase in ELWI. There was no rise in ELWI after 6% HES administration. In the 20% albumin solution group, the increased ELWI was recorded in patients who had positive baseline PWP-COP gradients (p In patients with ALPL, FFP infusion may lead to an increase in the accumulation of extravascular lung water. A negative preinfusion PWP-COP gradient is a safety criterion for the infusion of 20% albumin solution in patients with ALPL. The increased PVPI in combination with a positive PWP-COP gradient is an aggravating factor.
Переливание различных коллоидных растворов — основа терапии многих критических состояний: острой массивной кровопотери, сепсиса, септического шока. ожогов, перитонита, панкреатита, травм, дегидратации, гипоальбуминемии, гипопротеинемии, дефицита факторов свертывающей системы крови и т. д. [9, 29]. В отделениях интенсивной терапии стран Европы для восполнения объема циркулирующей крови у больных в критических состояниях часто используются коллоидные растворы: у 18% больных в виде монотерапии, у 65% в сочетании с кристаллоидными растворами и только у 17% больных с этой целью применяется монотерапия кристаллоидными растворами [29]. В то же время, несмотря на почти полувековую историю применения коллоидных растворов, большое число клинических и экспериментальных работ, проведенных за это время, продолжается дискуссия о том, выбор какого препарата оптимален в той или иной клинической ситуации [9]. Одним из активно обсуждаемых вопросов является применение коллоидных растворов у больных с острым повреждением легких. Для проведения инфузионной терапии у этой категории больных коллоидные растворы предпочитают использовать 39% опрошенных врачей отделений интенсивной терапии [29]. Предпочтительное использование коллоидов по сравнению с кристаллоидами у больных с острой дыхательной недостаточностью объясняется тем, что солевые растворы снижают коллоидно-осмотическое давление (КОД), повышая риск развития отека легких [9]. При сравнении действия различных инфузионных растворов в терапии шока показано, что при использовании только кристаллоидных растворов отек легких развился у 70% больных, тогда как при переливании коллоидных растворов это осложнение отмечено лишь в 25% случаев [32]. В то же время есть данные, что в условиях повышенной сосудистой проницаемости различные коллоиды по-разному влияют на функцию легких [33].
При высокой легочной сосудистой проницаемости и низком КОД переливание гидроксиэтилкрахмала (ГЭК), не проникающего через сосудистый эндотелий, может уменьшить выраженность интерстициального отека легких [14, 26]. В экспериментальных работах на животных показана способность ГЭК ослаблять выраженность отека при ожогах [43], ишемическом/реперфузионном повреждении [42], сепсисе [39]. Имеются сообщения о способности растворов ГЭК уменьшать капиллярную утечку при повышенной легочной сосудистой проницаемости [34, 38]. Однако эти данные нуждаются в дальнейшем клиническом изучении.
Противоречивы сведения о безопасности переливания растворов альбумина. В 1998 г. были опубликованы результаты метаанализа применения альбумина в критических состояниях [7], в котором утверждалось, что при переливании растворов альбумина больным с гиповолемией, ожогами и гипоальбуминемией на каждые 17 больных, леченных альбумином, приходился 1 дополнительный летальный исход [17]. Эти результаты метаанализа вызвали бурную дискуссию, были выявлены его существенные методологические недостатки [40]. Позже были опубликованы многочисленные исследования, свидетельствовавшие о безопасности переливания растворов альбумина. В многоцентровом контролируемом рандомизированном исследовании группы SAFE (The Saline versus Albumin Fluid Evaluation), включавшем 6997 больных, показано, что переливание альбумина больным в критических состояниях не оказывает отрицательного влияния на течение органной патологии, выживаемость больных, длительность ИВЛ. пребывание в стационаре или палате интенсивной терапии [28]. J.-L. Vincent и соавт. [36], проанализировав побочные эффекты, отмеченные при введении растворов альбумина в течение 3 лет, установили, что при переливании 648 т альбумина, т. е. 1,62 ·107 доз раствора, содержащего 40 г альбумина, не было зарегистрировано ни одного смертельного осложнения, связанного с инфузией препарата, и лишь в 7,1% случаев отмечены тяжелые осложнения (анафилактический шок, токсикодермия, дыхательная недостаточность, апноэ) [36].
Одним из наиболее серьезных осложнений, отмеченых при введении альбумина у больных с острым легочным повреждением, является усиление отека легких вследствие утечки альбумина в интерстициальное пространство [5]. Но одновременно имеются данные и об эффективности применения альбумина при лечении острого повреждения легких. В контролируемом рандомизированном исследовании у больных с острым повреждением легких добавление альбумина к терапии фуросемидом значительно повышало оксигенацию крови по сравнению с контрольной группой [20]. Одно из возможных объяснений этого феномена — повышение КОД плазмы у леченных альбумином больных [14, 20]. Кроме того, показано, что инфузия гиперонкотического раствора альбумина при повреждениях легких, вызванных шоком, оказывает иммуномодулирующее и антиоксидантное действие, подавляя экспрессию адгезивных молекул [23, 24].
Переливание свежезамороженной плазмы (СЗП), в котором нередко возникает необходимость при ДВС-синдроме, массивной кровопотере, тяжелом потреблении факторов свертывания, как известно, может сопровождаться развитием острого повреждения легких, связанного с трансфузиями (TRALI — transfusion-related acute lung injury). Однако недостаточно изучено непосредственное действие переливания СЗП на центральную гемодинамику, транспорт кислорода, течение отека легких.
Таким образом, проблема оценки безопасности переливания того или иного коллоидного раствора при остром повреждении легких/остром респираторным дистресс-синдроме остается актуальной [35].
Цель настоящей работы — в проспективном исследовании оценить влияние на центральную гемодинамику, транспорт кислорода и содержание внесосудистой воды легких переливания трех основных коллоидных растворов, наиболее часто применяемых у больных, находящихся в критических состояниях, СЗП, альбумина и ГЭК, и на основании полученных данных предложить критерии безопасности применения этих растворов
Материал и методы. Критерии включения больных в исследования. В исследование включены больные гемобластозами. поступившие в отделение реанимации Гематологического научного центра РАМН в связи с развитием у них острого повреждения легких, отвечавших следующим критериям: острое начало дыхательной недостаточности, наличие двустороннего инфильтративного поражения легких по данным рентгенографического исследования, снижение респираторного коэффициента paO2/FiO2 менее 300.
Всем больным при поступлении выполняли рентгенографию или компьютерную томографию легких, фибробронхоскопию с бронхоальвеолярным лаважем. Диагноз поражения легких устанавливали на основании клинических данных: результатов рентгенографического исследования легких, цитологического и микробиологического исследований лаважной жидкости.
У всех больных имелась клиническая картина сепсиса с острым повреждением легких, которое было обусловлено пневмониями бактериальной, грибковой, вирусной и пневмоцистной этиологии. У 2 больных пневмонии сочетались с неинфекционными причинами поражения легких: массивный цитолитический синдром после цитостатической терапии, реакция трансплантат против хозяина после неродственной трансплантации костного мозга.
Группы больных. У больных исследовали гемодинамические эффекты трех коллоидных растворов: 20% растзора альбумина ("Baxter", США, "Plasbumin". "Bayer", Германия), 6% раствора ГЭК 130/0,4 9:1 (Волювен, фирмы "Фрезениус-Каби", Германия) и СЗП.
Показаниями к переливанию растворов альбумина служили гипоальбуминемия и низкое КОД (см. таблицу) Выбор гиперонкотического раствора альбумина был обусловлен тем, что он наиболее эффективно способен повысить КОД при минимальном объеме введенной жидкости.
Изменение параметров в результате введения коллоидных растворов
| Параметр | 20% альбумин (n=25) V=3,8±0,4 мл/кг | 6% ГЭК (n=23) V=13,7±1,4 мл/кг | СЗП (n=20) V=13,4±1,3 мл/кг | |||
| до | после | до | после | до | после | |
| СИ, л/мин · м2 | 5,3±0,2 | 5,9±0,2* | 5,4±0,3 | 5,9±0,4* | 5,4±0,4 | 6,1±0,4* |
| УИ. мл/м2 | 47±3 | 54±3* | 50 ±4 | 56±4* | 49±3 | 57±3* |
| ИССС, дин. · с · см5 · м2 | 1181±75 | 1117±75 | 1176±103 | 1144±101 | 1170±90 | 1103±88 |
| АДСР, мм рт. ст. | 85,6±5,5 | 92,9±3,8* | 82,9±3,7 | 90,1±3,5* | 83,1±3,2 | 90,6±3,5* |
| ДЛАср, мм рт. ст. | 26,1± 1,5 | 30,4±1,3* | 25,9±1,3 | 30,4±1,6* | 27,0±1,7 | 31,3± 1,4* |
| ЦВД, мм рт. ст. | 11,3±0,9 | 13,8±1,1* | 10,3±1,1 | 13,8±1,0* | 10,1±1,1 | 12,0±1,2- |
| ДЗЛА, мм рт. ст. | 16,0±1,4 | 20,6±1,6* | 14,9 ±1,1 | 19,3±1,2* | 14,5±0,9 | 20,0±1,2* |
| PаО2/FiO2 | 210±21 | 228±24 | 242±45 | 223, 24 | 247±27 | 254±32 |
| СаО2, мл/дл | 8,7 ±0,5 | 8,0±0,4* | 8,3±0,5 | 7,6±0,3 | 8,3±0,4 | 7,6±0,3* |
| DO2I, (мл/мин)/м2 | 450±27 | 453±35 | 473±35 | 458±33 | 444±31 | 465±37 |
| Qs/Qt | 33,5±2,0 | 33,8± 2,1 | 30,4±2,6 | 33,2±2,5 | 28,9±2,6 | 32±3,4* |
| Гемоглобин, г/л | 6,2±0,4 | 5,7±0,3* | 6,1 ±0,3 | 5,4±0,2* | 5,8±0,3 | 5,3±0,3* |
| Альбумин, г/л | 29,2±1,2 | 35,5±1,1* | 31,3±1,3 | 27,1±1,1* | 31,6±2,0 | 33,0±1,2 |
| КОД. мм рт. ст. | 20,1±0,8 | 22,6±0,6* | 22,2±0,8 | 22,9±0,9 | 22,0±0,8 | 23,2±0,8* |
| Градиент ДЗЛА-КОД, мм рт. ст. | -4,1±1,5 | -1,8±1,8* | -6,7±1,7 | -2,3±2,0* | -8,1±1,1 | -1,7±1,8- |
| ИВВЛ, мл/кг | 16,7±1,8 | 18,2±2,1 | 17,1±1,8 | 18,1±2,1 | 17,2±2,0 | 19,8±2,5* |
| ИВГОК, мл/м2 | 1000±59 | 1010±52 | 964±50 | 1026±59 | 995±55 | 1038±64 |
| ИПЛС | 3,2±0,3 | 3,4±0,4 | 3,5±0,4 | 3,5±0,5 | 3,3±0,4 | 3,5±0,4 |
Показанием к переливанию СЗП явился ДВС-синдром, выявлявшийся у больных гемобластозами, сепсисом и острым повреждением легких.
У больных с острым повреждением легких растворы ГЭК переливались с целью уменьшения легочной сосудистой проницаемости и выраженности интерстициального отека легких, так как подобный эффект ГЭК был отмечен ранее в экспериментальных работах [14, 26, 34, 38, 39]. Выбор волювена был обусловлен тем, что большинство больных, включенных в исследование, имели тромбоцитопению (менее 50 · 109/л), нарушения коагуляционного гемостаза и геморрагический синдром. В этих условиях среди синтетических коллоидных растворов волювен является наиболее безопасным раствором, поскольку оказывает наименьшее влияние на плазменный и тромбоцитарный гемостаз [1].
Всего в исследование вошло 68 наблюдений. В зависимости от вводимого коллоидного раствора больные были разделены на 3 группы. В группе больных, получавших раствор 20% альбумина. — 25 человек, в группе больных, получавших раствор 6% ГЭК 130/0.4 — 23, в группе больных, которым вводили СЗП — 20. Возраст больных был от 19 до 75 лет (средний возраст 45,3 г 3,3 года).
Протокол обследования. У всех больных устанавливали катетер Сван—Ганса 7 Fr ("В. Braun", США), в легочную артерию — через интрадюссер 8,5 Fr. стоящий в подключичной или внутренней яремной вене. Измерение сердечного выброса проводили путем введения в венозный ход катетера 5 мл 5% раствора глюкозы, охлажденного до температуры 0-5°С. Измерение выполняли не менее 3 раз, после чего вычисляли среднее значение сердечного выброса. Параметры центральной гемодинамики и транспорта кислорода (среднее давление в легочной артерии, ДЗЛА, сердечный индекс, ударный индекс, легочный шунт (Qs/Qt), альвеолярно-артериальный градиент. содержание кислорода в артериальной крови, индекс доставки кислорода) фиксировали и рассчитывали с помощью компьютерной программы мониторинговой системы "HPI092A" ("Hewlett-Packard", США) по общепринятым формулам.
Параметры внутригрудных волемических показателей измеряли метолом транспульмональной термодилюции с помошью прибора "PiCCOpIus" ("Pulsion Medical Systems", Германия). Для этого больным выполняли катетеризацию бедренной артерии катетером "Pulsiocath" 5 Pr (PV2015L20. "Pulsion Medical Systems", Германия) для регистрации АД к изменений температуры артериальной крови с помощью термистера. расположенного на его конце. В центральный венозный катетер болюско вводили 15 мл 5% раствора глюкозы, охлажденного до температуры 0-8°C. Термистер бедренного артериального катетера регистрировал изменение температуры. По параметрам температурной кривой прибором "PiCCOpius" выполняли расчет индекса внутригрудного объема крови — ИВГОК, мл/м2 (норма — 850-1000 мл/м2) индекса внесосудистой воды легких — ИВВЛ, мл на 1 кг массы тела (норма — 3-7 мл /кг) и индекса проницаемости легочных СОСУДОВ — ИПЛС (норма — 1,0-3,0) [2, 3].
Измерение КОД проводили на осмометре "Osrnomat 050" ("Gonotec", Германия) (норма > 25 мм рт. ст.).
Исследование газов крови и КЩС проводили на газовом анализаторе ABL 700 ("Radiometer". Дания).
Обследование, включавшее измерение параметров центральной гемодинамики, транспорта кислорода, внутригрудных волемических показателей, газов крови. КОД и концентрации альбумина, выполняли непосредственно перед началом каждой инфузии и сразу после ее окончания. У 16 больных из каждой группы измерение ИВВЛ выполняли также через 1 ч после окончания инфузии.
Проводимая терапия. Всем больным проводилась респираторная поддержка или оксигенотерапия. У 60% больных проводилась ИВЛ в контролируемом по объему режиме (респиратор "TBird AYS III", "Bird Product Corporation", Австралия), у 20% — неинвазивная вентиляции легких в режиме поддержки давлением (респиратор "Bi-PAP Vision", "Respironics Inc.". CША, у 20% — ингаляция кислорода через лицевую маску с резервуаром. Параметры респираторной поддержки и оксиге-нотерапии во время введения коллоидных растворов не меняли.
Введение всех коллоидных растворов выполняли с помощью инфузионного насоса "Infusomat fmS" ("В. Braun Melsungen AG", Германия) с постоянной скоростью. Во время введения коллоидных растворов другие инфузии не проводились. Введение прекращали в случае нарастания дыхательной недостаточности (уменьшение насыщения гемоглобина кислородом поданным пульсоксиметрии) или при возрастании ДЗЛА до 18 мм рт. ст., если до начала введения этот показатель не превышал 14 мм рт. ст., или на 25% от исходного уровня, если ДЗЛА исходно было выше 14 мм рт. ст. либо при увеличении ИВГОК выше нормы. Переливая коллоидные растворы при ДЗЛА, превышающем 16-18 мм рт. ст., мы учитывали опасность возникновения острой левожелудочковой недостаточности. Однако у большинства больных проводилась респираторная терапия с положительным давлением в конце выдоха 10-12 см вол. ст., которая не прекращалась при проведении измерений, и влияла на величину ДЗЛА. Кроме того. ДЗЛА является надежным показателем преднагрузки только при нормальной растяжимости левого желудочка, которая редко остается таковой у больных сепсисом, при проведении ИВЛ [4]. В этих условиях повышенные центральное венозное давление и/или ДЗЛА не всегда отражают увеличенную преднагрузку. Показано, что при сепсисе даже при нормальных и высоких значениях барометрических показателей у больных может сохраняться гиповолемия [2]. В этих условиях более адекватным является волемический мониторинг, проводимый с помощью транспульмональной термодилюции [2]. Ни в одном случае нашего исследования острая левожелудочковая недостаточность и/или нарастание гипоксемии не явились причиной прекращения инфузии.
Для 20% раствора альбумина скорость введения составляла 200 мл/ч, для 6% ГЭК и СЗП — 750 мл/ч. Объемы вводимых растворов варьировали у разных больных в зависимости от достижения принятых в протоколе критериев (см. таблицу).
Статистическая обработка проведена с помощью программы "Origin 6.0" ("Microcal Software, Inc.", США). Данные в работе представлены в виде среднее±стандартная ошибка средней.
Результаты исследования и их обсуждение. Во время введения коллоидных растворов ни в одном случае не было зафиксировано снижения насыщения гемоглобина кислородом по данным пульсоксиметрии. У всех больных инфузия завершалась при увеличении ДЗЛА до величин, принятых в протоколе исследования. Объемы введенных коллоидных растворов составили: для 20% — раствора альбумина 3,8±0,4 мл/кг (от 150 до 500 мл). для 6% ГЭК 130/0,4 - 13,7±1,4 л/кг (от 500 до 1500 мл) и для СЗП — 13,4±1,3 мл/кг (от 400 до 1750 мл). Эти объемы не зависели от исходной выраженности острой дыхательной недостаточности, определяемой по коэффициенту р2О2/FiO2, а также от выраженности отека легочной ткани, оцениваемого по величине внесосудистой воды легких.
У большинства больных гемобластозами, включенных в исследование, до начала инфузии коллоидных растворов отмечалась выраженная анемия (см. таблицу), которая существовала у них уже длительное время. Анемия была обусловлена как основным гематологическим заболеванием. так и миелотоксическим действием предшествующего цитостатического химиотерапевтического лечения. Все пациенты в плановом порядке получали трансфузии эритроиитной массы и были адаптированы к этому уровню гемоглобина, у многих из них отмечалась резистентность к трансфузиям эритроцитов.
Сниженный уровень гемоглобина у больных сопровождался низким содержанием кислорода в артериальной крови, который составлял при включении в исследование в среднем 8 мл/дл (норма 17-20 мл/дл) (см. таблицу). Низкое содержание кислорода в артериальной крови компенсировалось гиперкинетическим типом гемодинамики. который регистрировался перед введением растворов у большинства больных. Высокий сердечный индекс (5,3-6 л/мин · м2 при норме 2,5-4 л/мин · м2). выявляемый у больных, приводил к тому, что индекс доставки кислорода был незначительно ниже нормы, составляя в среднем 450 (мл/мин)/м2 (норма 550-650 (мл/мин)/м2) (см. таблицу).
У большей части больных регистрировалась легочная гипертензия — среднее давление в легочной артерии было повышено до 26-27 мм рт. ст. (см. таблицу). Среднее значение ДЗДЛ до начала инфузии во всех группах было ниже 18 мм рт. ст. (см. таблицу). Величина легочного шунта у большинства больных значительно превышала норму (см. таблицу). КОД исходно было снижено во всех группах. Содержание внесосудистой воды легких до начала введения растворов превышало норму более чем в 2 раза. Внутригрудной объем крови до начала инфузии был в пределах нормальных величин и при проведении инфузии достоверно не изменялся (см. таблицу).
После переливания растворов альбумина и плазмы отмечалось достоверное снижение содержания кислорода в артериальной крови, обусловленное гемодилюцией и снижением уровня гемоглобина (см. таблицу). Эго снижение содержания кислорода компенсировалось увеличением сердечного выброса, в результате доставка кислорода достоверно не изменялась. Также достоверно не менялись альвеолярно-артериальный градиент и pаО2/FiО2.
Введение всех исследуемых коллоидных растворов сопровождалось увеличением сердечного и ударного индексов, АД, легочного артериального давления и ДЗЛА. При этом, хотя ДЗЛА повышалось до 20 мм рт. ст., внутригрудной объем крови оставался в пределах верхней границы нормы (см. таблицу). КОД увеличивалось только после переливания СЗП и 20% альбумина.
Несмотря на повышение КОД после переливания всех растворов, регистрировалось увеличение градиента ДЗЛА-КОД, т. е. рост гидростатического давления превышал увеличение КОД плазмы.
ИВВЛ непосредственно после окончания введения альбумина и ГЭК достоверно не изменялся (см. таблицу).
В то же время отмечено нарастание внесосудистой воды легких и шунта после переливания плазмы. Это нарастание внесосудистой воды легких не сопровождалось гипоксемией или ухудшением показателей транспорта кислорода.
У 16 больных из каждой группы ИВВЛ был измерен через 1 ч после окончания введения растворов. Спустя час в группе больных, получавших раствор 20% альбумина, был обнаружен дальнейший достоверный прирост внесосудистой воды легких по сравнению как с величиной до инфузии (с 15,8±1,8 до 19,1±2,5 мл/кг; p Особенно большим был прирост внесосудистой воды легких у больных, у которых до начала инфузии положительный градиент ДЗЛА-КОД сочетался с повышенным ИПЛС. Сам по себе в отдельности индекс проницаемости легочных сосудов не являлся предиктором увеличения содержания внесосудистой воды легких после инфузии (рис. 2).
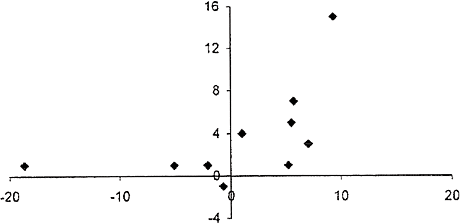
Рис. 1. Зависимость изменения ИВВЛ (на оси ординат) после введения 20% раствора альбумина от значения градиента ДЗЛА-КОД до введения (по оси абсцисс).
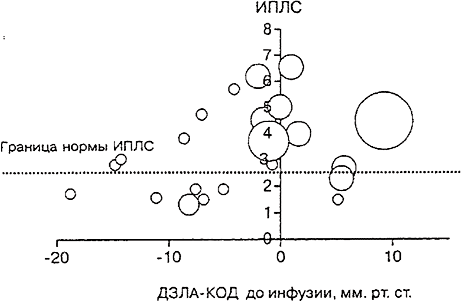
Рис. 2. Зависимость изменения внесосудистой воды легких (диаметр кругов) после переливания 20% раствора альбумина от факторов риска.
Градиент ДЗЛА-КОД до начала инфузии (по оси ординат) и индекс проницаемости легочных сосудов (ИПЛС) (по оси абсцисс). Имеется корреляция между приростом внесосудистой воды легких и значением градиента ДЗЛА-КОД. При сочетании положительного значения градиента ДЗЛА-КОД и ИПЛС более 3 увеличение внесосудистой воды легких после инфузии альбумина резко возрастает.
В литературе до сих пор нет единой точки зрения на конечную цель заместительной терапии коллоидными растворами. При коррекции гиповолемии в качестве критерия эффективности проводимого лечения авторы предлагают использовать различные показатели: уменьшение артериальной гипотензии, уменьшение тахикардии, увеличение ударного объема, сердечного выброса, индекса ударного объема левого желудочка, увеличение доставки кислорода, отсутствие зависимости потребления кислорода от его доставки, снижение величины уровня лактата артериальной крови, уменьшение градиента рСО2 слизистой желудка, достижение определенного уровня ДЗЛА или центрального венозного давления, увеличение конечно-диастолического объема правого и/ или левого желудочков и т. д. [7, 14, 21, 31, 37]. Также продолжаются дискуссии о безопасных объемах инфузии при терапии коллоидными растворами. Особенно остро проблема мониторинга инфузионной терапии стоит у больных с острой дыхательной недостаточностью, у которых ее проведение может ухудшить дыхательную функцию.
В нашем исследовании объемы изоонкотических растворов 6% ГЭК и СЗП (в среднем 13-14 мл/кг), приведшие к равному повышение ДЗЛА, оказались одинаковыми, а объем гиперонкотического раствора 20% альбумина, вызывавшего сходные изменения, — приблизительно в 3-4 раза меньшим (в среднем 3,8 мл/кг), т. е. гемодинамический эффект коллоидных растворов был пропорционален КОД этих растворов.
В настоящем исследовании до начала инфузионной терапии КОД было снижено у большинства больных. Причиной этого снижения являлась гипоальбуминемия. Известно, что гипопротеинемия является маркером развития ОРДС [19]. Нормальный сывороточный уровень общего белка выявляется лишь у 8% больных с ОРДС [19]. Гипопротеинемия и гипоальбуминемия значимо чаще выявляются при ОРДС, чем при кардиогенном отеке легких [6]. Кроме того, низкий уровень сывороточного белка у больных ассоциируется с более тяжелым течением ОРДС и худшим прогнозом [19].
При отеке легких большее значение имеет не столько КОД плазмы, сколько градиент между силой, выталкивающей жидкость из сосудистого русла, т. е. гидростатическим давлением, которое характеризуется ДЗЛА, и силой, удерживающей ее в русле, т. е. КОД плазмы [6, 14]. Увеличение этого градиента ассоциируется с более частым развитием отека легких и смертностью [16, 25, 26, 30, 41], что подтверждается результатами изучения диффузии радиоактивно меченого DTPA — вещества с мол. массой 504 Д, сопоставимой с мол. массой молекулы воды. Транслокация этого вещества во внесосудистое пространство легких коррелирует с величиной градиента ДЗЛА-КОД как при кардиогенном, так и некардиогенном отеке легких [30]. В то же время в большинстве работ исследователи не выявили связи между выраженностью отека легких и значением градиента ДЗЛА-КОД [8, 16].
Нами также не зафиксировано корреляции между градиентом ДЗЛА-КОД и величиной внесосудистой воды легких. Однако, учитывая значение этого градиента в патогенезе развития отека легких, многие исследователи, оценивая эффекты инфузионной терапии, уделяют ему особое внимание. Именно потому, что введение кристаллоидных растворов приводит к увеличению этого градиента, а инфузии коллоидных растворов его либо уменьшают, либо не изменяют [27], многие предпочитают использование коллоидных растворов при ОРДС [9, 29].
Как же влияют на ДЗЛА и КОД изучаемые растворы? По данным ряда исследователей [27], вливание 5% раствора альбумина приводит к большему на 20% увеличению КОД, чем инфузия такого же объема 6% раствора ГЭК. По другим данным, инфузия 5% альбумина и 6% ГЭК оказывает одинаковое действие на изменения КОД, ДЗЛА и содержание внесосудистой воды легких [12]. В нашем исследовании, несмотря на увеличение КОД после введения СЗП и альбумина, после переливания всех растворов градиент ДЗЛА-КОД достоверно увеличивался, т. е. их влияние на центральную гемодинамику было более выраженным, чем действие на КОД. Инфузия 6% ГЭК приводила к снижению концентрации альбумина в сыворотке, хотя КОД при этом оставался без изменений. Одновременно после переливания всех коллоидных растворов отмечалось и снижение уровня гемоглобина (см. таблицу). Этот факт можно объяснить гемодилюцией. Плазма и 6% ГЭК в равной степени увеличивают объем циркулирующей плазмы [22]. Мы не измеряли объем циркулирующей крови, однако ранее было показано, что при нормоволемической гемодилюции объем циркулирующей крови после введения 6% ГЭК 130/0.4 увеличивается на 98 + 12% от объема перелитого раствора [18]. Таким образом, возникающая после переливания 6% ГЭК гипоальбуминемия является относительной и не отражает изменение значения КОД плазмы.
Несмотря на повышение КОД, трансфузия СЗП привела к достоверному увеличению содержания внесосудистой воды легких, что можно объяснить гетерогенным составом белков СЗП. В условиях повышенной сосудистой проницаемости и увеличения градиента ДЗЛА-КОД белковые молекулы малой массы покидают сосудистое русло, проникают в интерстициальное пространство и увеличивают выраженность интерстициального отека. Основным показанием к трансфузии СЗП являются коагулопатия, потребление и дефицит факторов свертывания. В этих условиях СЗП является единственным препаратом, который способен комплексно возместить недостающие факторы свертывания, причем доза переливаемой плазмы должна быть достаточно большой. Известно, что доза СЗП 10 мл/кг повышает уровень факторов свертывания в среднем на 10% [15]. S. I. Dara соавт. [11] проанализировали результаты переливания плазмы у 115 больных с коагулопатиями в критических состояниях. Объем переливаемой плазмы в этой работе (от 10 до 17 мл/кг) был сопоставим с объемом вводимой плазмы в нашем исследовании (13 мл/кг). Авторы установили, что среди больных, которым переливали плазму, острое повреждение легких встречалось в 18% случаев, в то время как среди больных, которым плазма не переливалась, — лишь в 4% (р = 0,021) [11]. Исходя из этого, при возникновении необходимости в трансфузии плазмы у больных с повышенной легочной сосудистой проницаемостью инфузионная терапия должна проводиться с учетом возможного усиления интерстициального отека легких, который может возникнуть даже без признаков объемной перегрузки. Добавление к терапии диуретиков может ослабить этот побочный эффект плазмы.
В отличие от плазмы окончание инфузии 20% раствора альбумина не сопровождалось нарастанием внесосудистой воды легких. Введение 20% раствора альбумина приводило к значительному повышению концентрация альбумина и КОД. В результате, несмотря на увеличение ДЗЛА, больные оказывались как бы в более выгодном положении, чем после переливания ГЭК. Однако клиническая практика показывает, что в условиях повышенной сосудистой проницаемости одного поддержания КОД недостаточно для обеспечения безопасности инфузии. При восполнении объема циркулирующей плазмы во время операции аортокоронарного шунтирования переливание 20% раствора альбумина приводило к большему увеличению КОД, чем переливание 3% ГЭК (200/0,5), но при этом сопровождалось увеличением внесосудистой воды легких и снижением рО2 в артериальной крови [9]. В нашем исследовании непосредственно после окончания инфузии ГЭК и альбумина мы не регистрировали нарастания артериальной гипоксемии и выраженности отека легких. Но спустя 1 ч после окончания переливания 20% раствора альбумина эти побочные эффекты были отмечены у части больных. Одним из факторов риска развития этого побочного эффекта является положительное значение градиента ДЗЛА-КОД до инфузии. Тем более, что, как показано выше, при введении альбумина происходит более быстрый рост ДЗЛА, чем КОД плазмы.
Однако не выявлено связи между объемом внесосудистой воды легких и значением градиента ДЗЛА-КОД, поскольку этот градиент не отражает еще одного фактора, ответственного за нарастание воды в легких, — проницаемости легочных сосудов. В экспериментах на крысах было показано, что переливание 25% раствора альбумина в дозе 1 г/кг здоровым животным приводило к значительному повышению КОД плазмы (максимально на 58%), но не сопровождалось изменениями содержания внесосудистой воды в легких [10]. Введение эндотоксина вызывало снижение КОД плазмы и повышение содержания внесосудистой воды в легких. Если после эндотоксина вводили альбумин в той же дозе, то это приводило к более медленному и менее выраженному увеличению КОД плазмы, чем у здоровых животных. Одновременно регистрировалось большее нарастание содержания воды в легких, чем в группе животных, получавших только эндотоксин [10]. В работе по изучению диффузии альбумина в интерстициальную ткань легкого было показано, что клиренс радиоактивного меченного альбумина при некардиогенном отеке легких достоверно выше, чем при кардиогенном, и коррелирует с величиной градиента ДЗЛА-КОД. При кардиогенном отеке легких этой корреляции не наблюдается [30]. Перечисленные исследования еще раз подтверждают, что в условиях эндотоксинемии, повышенной сосудистой проницаемости, помимо соотношения гидростатического и коллоидного давлений в сосудистом русле при оценке эффектов коллоидных растворов на функцию легких, необходимо принимать во внимание проницаемость легочного эндотелия, повышенное значение которого является как бы фактором, запускающим второй механизм нарастания интестициального отека — утечку альбумина в интерстициальное пространство.
Тот факт, что у наблюдавшихся нами больных отсроченное увеличение внесосудистой воды легких развивалось только после переливания альбумина и не было отмечено после инфузии ГЭК, может быть объяснено разницей в массе и размере молекул, составляющих эти вещества, а также различной проницаемостью эндотелия для разных по размеру молекул, определяющих КОД. Мол. масса альбумина составляет 69 кД, а ГЭК 130/0,4 — 130 кД. Поэтому в условиях повышенной сосудистой проницаемости более мелкие молекулы альбумина легче покидают сосудистое русло и перемещаются в легочный интерстиций, чем крупные молекулы ГЭК. В нашем исследовании, несмотря на то что после переливания 6% ГЭК не регистрировался прирост КОД, а градиент ДЗЛА-КОД достоверно увеличивался, тем не менее не наблюдалось увеличения содержания внесосудистой воды легких. Данные нашего исследования показывают, что использование только одного индекса проницаемости не может предсказывать увеличение внесосудистой воды легких после введения альбумина. Для достоверной оценки безопасности применения альбумина у больных с острым повреждением легких необходимо одновременное использование и градиента ДЗЛА-КОД, и индекса проницаемости легочных сосудов.
Уменьшить или избежать этого отсроченного побочного эффекта переливания раствора альбумина можно путем добавления к терапии диуретиков [13, 20]. Применение диуретиков после введения 20% альбумина сопровождалось снижением гидростатического давления и уменьшением объема циркулирующей плазмы с увеличением КОД, приводя в конечном счете к уменьшению градиента ДЗЛА-КОД. Уменьшение же градиента в свою очередь приводит к уменьшению перехода жидкости во внесосудистое пространство. Основываясь на результатах работы по изучению диффузии меченого альбумина в интерстициальную ткань легких при ОРДС [30], можно утверждать, что уменьшение этого градиента сопровождается снижением скорости утечки альбумина из сосудистого русла в интерстициальную ткань легких.
Выводы
- У больных с острым повреждением легких переливание раствора ГЭК 130/0,4 9:1 в объеме до 14 мл/кг является безопасным и не приводит к увеличению внесосудистой воды легких. У больных на ИВЛ ГЭК может переливаться до повышения индекса внутригрудного объема крови до верхней границы нормы.
- В условиях повышенной сосудистой проницаемости (индекс проницаемости легочных сосудов ≥3) переливание свежезамороженной плазмы может приводить к нарастанию внесосудистой воды легких.
- Критерием безопасности переливания 20% раствора альбумина при остром повреждении легких является отрицательное значение градиента ДЗЛА-КОД. В этих условиях препарат может переливаться даже при повышенной сосудистой проницаемости. Положительное значение градиента ДЗЛА-КОД является фактором риска развития отека легких после переливания гиперонкотического раствора альбумина.
- Повышенное значение индекса проницаемости легочных сосудов является отягощающим фактором при сочетании с отрицательным значением градиента ДЗЛА-КОД и приводит к увеличению выраженности отека легких после инфузии 20% раствора альбумина.
- Нарастание содержания внесосудистой воды легких после инфузии 20% раствора альбумина у больных с острым повреждением легких может происходить отсроченно.
- При необходимости переливания естественных коллоидных растворов больным с острым повреждением легких их введение желательно сочетать с назначением диуретиков.
Литература
- Буланов А.Ю. Трансфузионная тактика восполнения операционной кровопотери у больных с тромбоцитопениями и гемофилией А: Автореф. дис. ... канд. мед. наук. — М., 2003.
- Киров М.Ю., Кузьков В.В., Бьертнес Л.Я. Недашковский Э. В. // Анестезиол. и реаниматол. — 2003. — № 4. — С. 41-45.
- Кузькин В.В., Киров М.Ю., Недашкоеский Э.В. // Анестезиол. и реаниматол. — 2003. — № 4. — С. 67—71.
- Марина П.Л. Интенсивная терапия: Пер. с англ. — М., 1998.
- Сепсис в начале XXI века: классификация, клинико-диагностическая концепция и лечение: Метод. рекомендации. - М., 2004.
- Arif S.К., Verheij J., Groeneveid A.B.J., Raijmakers P.G.H.M. // Intensive Care Med. - 2002. - Vol. 28. -P. 310-317.
- Bendjelid K., Romand J.-A. // Intensive Care Med. — 2003 — Vol. 29. - P. 352-360.
- Boldt J., von Borman В., Kling D. et al. // Herz. — 1985. — Bd 10. N 6. - S. 366-375.
- Boldt J. // intensive Care Med. — 2000. — Vol. 26. -P. 1181-1192.
- Camacho M.Т., Totapally B.R., Torbat D.I.. Wolfsdorf J. // Chest. — 2001. - Vol. 120. - P. 1655—1662.
- Dara S.I.,. Rana R., Afessa B. et al. // Crit. Care Med. -2005. - Vol. 33. - P. 2667-2671.
- Gallagher J.D., Moore R.A., Kerns D. et al. // Anesth. Anaig. - 1985. - Vol. 64, N 8. - P. 753-758.
- Greg S. Martin, Robert J. et al. // Crit. Care Med. - 2002. -Vol. 30. 10. - P. 2175—2182.
- Groeneveld J. // Crit Care. - 2000. - Vol. 4. - Suppl. 2. -P. S16-S20.
- Hellstern P., Muntean W., Schramm W. et al. // Thromb. Res. 2002. - Vol. 107. - P. S53-S57.
- Hirakawa A. Sakamoto H., Masumi K. et al. // J. Vet. Med. Sci. - 1993. - Vol. 55, N 6. - P. 995-1000.
- Human albumin administration in critically ill patients: Systematic review of randomized controlled trials. Cochrane Injuries Group Albumin Reviewers // Br. Med. J. — 1998. — Vol. 317, N 7153. - P. 235-240.
- Jacob M., Rehm M., Orth V., Ltsch M. et al. // Anaesthesist. — 2003. - Bd 52. - S. S96-904.
- Mangialardi R.J., Martin G.S., Bernard G.R. et al. // Crit. Care Med. - 2000. - Vol. 28. — P. 3137-3145.
- Martin G.S., Moss M.. Wheeler A.P. et al. // Crit. Care Med. - 2005. - Vol. 33. -P. 1681-1687.
- Michard R. Alava S., Zarka V. et al. // Chest. - 2003. -Vol. 124. - P. 1900-1908.
- Persson J., Grande P.-O. // Intensive Care Med. — 2005. — Vol. 31. - P. 296-301.
- Powers K.A., Kapus A., Khadaroo R.G. et al. // Surgery. — 2002. - Vol. 132. - P. 391-398.
- Powers K.A., Kapus A., Khadaroo R.G. et al. // Crit. Care Med. - 2003. - Vol. 31. - P. 2355-2363.
- Rackow E.C., Fein I.A. // Crit. Care Med. - 1978. - Vol. 6, N 6. - P. 360-363.
- Rackow E.C., Fein I.A., Siegel J. // Chest. - 1982. -Vol. 82. - P. 433-437.
- Rackow E.C. Folk J.L, Fein I.A. et al. // Crit. Care Med. -1983. - Vol. 11. - P. 839-850.
- SAFE Study Investigators A Comparison of Albumin and Saline for Fluid Resuscitation in the Intensive Care Unit. // N. Engl. J. Med. - 2004. - Vol. 350. - P. 2247-2256.
- Schortgen F., Deye N., Brochard N. // Intensive Care Med. — 2004. - Vol. 30. - P. 2222-2229.
- Sibbald W.J., Driedger A.A., Moffat J.D. et al. // J. Appl. Physiol. - 1981. - Vol. 50, N 6. - P. 1337-1347.
- Silva E., De Backer D., Creteur J., Vincent J.L. // Intensive Care Med. - 2004. - Vol. 30, N 3. - P. 423-429'.
- Stein L., Bernard J., Morisette M. // Circulation. — 1975. — Vol. 52. - P. 483-489.
- Taylor R.J., Pearl R. // .Anesth. Analg. — 1996. — Vol. 83. — P. 209-212.
- Tian J., Lin X., Guan R., Xu J.-G. // Anesth. Analg. - 2004. - Vol. 98. - P. 768-774.
- Vincent J.-L. // Crit Care. - 2000. - Vol. 4. - Suppl. 2. - P. SI-S2.
- Vincent J.-L., Wilkes M.M., Navickis R.J. // Br. J. Anaesth. - 2003. - Vol. 91. - P. 625-630.
- Wagner J.G., Leatherman J.W. Right // Chest. - 1998. -Vol. 113. - P. 104S-1054.
- Webb A.R., Tighe D., Moss R.F. et al. // Crit. Care Med. -1991. - Vol. 19. - P. 409-416.
- Webb A.R., Moss R.F., Tighe D. et al. // Intensive Caer Med. - 1992. - Vol. 18. - P. 348-355.
- Webb A.R. // Crit. Caer. - 2000. - Vol. 4. - Suppl. 2. - P. S26-S32.
- Weil M.H., Henning R.J., Morissette M., Michaels S. // Am. J. Med. - 197S. - Vol. 64, N 4. - P. 643-650.
- Wisselink W.. Patetsios P., Panetta T.F. et al. // J. Vase. Surg. - 1998. -Vol. 27. - P. 109-116.
- Zikira В., King T.S., Stanford J. Freeman H. P. // Arch. Surg. - 1989. - Vol. 125. - P. 930-934.
