Эффективность Мексидола у пациентов разных возрастных групп с хронической ишемией головного мозга с когнитивными нарушениями
СтатьиВ.В. Захаров1, О.Н. Ткачева2,3, Э.А. Мхитарян2,3 3, А.И. Федин2
1 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия;
2 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия;
3 Российский геронтологический научно-клинический центр ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, Москва, Россия
Резюме
Цель исследования. Оценить эффективность последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 в сравнении с плацебо у пациентов с хронической ишемией головного мозга (ХИМ) разных возрастных подгрупп.
Материал и методы. Представлен субанализ данных международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования МЕМО, в котором участвовали 318 пациентов (25% мужчин) в возрасте от 40 до 90 (медиана 60) лет. Эффективность лечения оценивалась в трех возрастных группах: 40—60 (n=163), 61—75 (n=141) и 76—90 (n=13) лет. В качестве первичной конечной точки эффективности рассматривалось увеличение в динамике суммы баллов по шкале MoCA в виде абсолютной разницы между суммой баллов до начала лечения и на 75-й день терапии. В качестве вторичных конечных точек эффективности рассматривалась динамика суммы баллов по следующим опросникам и шкалам: тест замены цифровых символов, опросник качества жизни SF-36, шкала субъективной оценки астении MFI-20, опросник вегетативных нарушений Вейна, шкала тревоги Бека, шкала двигательной активности Тинетти.
Результаты. Положительная динамика выраженности когнитивных, эмоциональных и двигательных нарушений в группах 40—60 и 61—75 лет через 75 дней терапии была выявлена у больных, получавших как Мексидол, так и плацебо, однако у пациентов, получавших Мексидол, эти изменения оказались более выраженными, на что указывают более высокие значения медианы абсолютной разницы суммы баллов изучаемых показателей.
Заключение. Результаты исследования показали, что у пациентов с ХИМ значимо более выраженное улучшение когнитивных и двигательных функций, повышение качества жизни, уменьшение выраженности вегетативных нарушений, астении и тревожности через 75 дней терапии наблюдались на фоне применения Мексидола по сравнению с плацебо. Полученные результаты свидетельствуют о целесообразности применения Мексидола для лечения пациентов разного возраста с ХИМ.
Ключевые слова: когнитивные нарушения, хроническая ишемия мозга, Мексидол, Мексидол ФОРТЕ 250, этилметилгидроксипиридина сукцинат, исследование МЕМО.
Как цитировать:
Захаров В.В., Ткачева О.Н., Мхитарян Э.А., Федин А.И. Эффективность Мексидола у пациентов разных возрастных групп с хронической ишемией головного мозга c когнитивными нарушениями (результаты субанализа международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования МЕМО). Журнал неврологии и психиатрии им. С.С. Корсакова. 2022;122(11 вып. 2):73-80.
Efficacy of Mexidol in patients with chronic brain ischemia and cognitive impairment of different age groups (results of sub-analysis of the international multicenter, randomized, double-blind, placebo-controlled study of sequential therapy in patients with chronic brain ischemia MEMO)
V.V. Zakharov1, O.N. Tkacheva2-3, E.A. Mkhitaryan2-3, A.I. Fedin2
1 Sechenov First Moscow State Medical University (Sechenov University), Moscow, Russia;
2 Pirogov Russian National Research Medical University, Moscow, Russia;
3 Russian Clinical and Research Center of Gerontology, Pirogov Russian National Research Medical University, Moscow, Russia
Abstract
Objective. To assess the efficacy of sequential therapy with Mexidol and Mexidol FORTE 250 in comparison with placebo in patients of different age groups with chronic brain ischemia.
Material and methods. The study is sub-analysis of data of the international multicenter, randomized, double-blind, placebo-controlled study of sequential therapy in patients with chronic brain ischemia (MEMO), which included 318 patients (25% men) in the age of 40—90 (median 60) years. All subjects were subdivided into 3 age subgroups: 40—60 years (n=163), 61 —75 years (n=141) and 76—90 years (n=13). The primary efficacy endpoint was the dynamic of increase of total score by MoCA scale, i.e. the absolute value of difference by MoCA scale at the point of day 75 comparing to values before treatment. As secondary efficacy endpoints results of dynamic by following questionnaires and scales were used: digit symbol substitution test, the Health Survey SF-36, asthenia subjective assessment scale (MFI-20), Vane questionnaire, Beck anxiety scale, Tinetti scale.
Results. After 75 days of treatment positive dynamic was revealed in cognitive, emotional and motor impairment in patients of 40—60 and 61—75 age subgroups both in groups of Mexidol and placebo, but in group of Mexidol the changes were more prominent which is proved by significantly higher values of median of absolute difference of total score of studied parameters. Conclusion. The results of trial showed that in patients of different age-subgroups with chronic brain ischemia the improvement in cognitive, motor impairment and quality of life, as well as decrease in vegetative impairment, asthenia and anxiety are observed after 75 days of treatment both in Mexidol and placebo group, but in Mexidol group these changes are more prominent. The data obtained confirm the expediency of the use of sequential therapy with Mexidol and Mexidol FORTE 250 in patients of different age subgroups with chronic brain ischemia.
Keywords: cognitive impairment, chronic brain ischemia, Mexidol, Mexidol FORTE 250, ethylmethylhydroxypyridine succinate, MEMO trial.
To cite this article:
Zakharov VV, Tkacheva ON, Mkhitaryan EA, Fedin AI. Efficacy of Mexidol in patients with chronic brain ischemia and cognitive impairment of different age groups (results of sub-analysis of the international multicenter, randomized, double-blind, placebo-controlled study of sequential therapy in patients with chronic brain ischemia MEMO). S.S. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2022;122(11 vyp 2):73-80. (In Russ.).
Число пациентов с недементными когнитивными расстройствами (КР) достаточно велико, однако определение показателей заболеваемости и распространенности в популяции, в том числе у пожилых пациентов, сопряжено с методологическими сложностями [1]. В связи с улучшением диагностики умеренных КР (УКР) в последнее время их распространенность в популяции, по данным различных исследований, составляет от 5 до 29%. Заболеваемость оценивается как 8—58 новых случаев/1000 человек/год, а вероятность прогрессирования УКР в дементные КР составляет приблизительно 15% [2]. Распространенность УКР у лиц в возрасте 60 лет и старше составляет от 5,0 до 36,7% [1, 3].
Сосудистые КР (СКР) наряду с болезнью Альцгеймера являются одной из самых частых причин когнитивного снижения. СКР — группа патогенетически и клинически разнородных состояний, которые развиваются в результате повторных острых нарушений мозгового кровообращения и/или хронической ишемии головного мозга (ХИМ). Критериями диагноза СКР являются наличие КР на фоне фонового сосудистого заболевания и доказательства связи КР с данным сосудистым заболеванием. Особенности КР при цереброваскулярной патологии зависят от локализации и патогенетического механизма церебрального повреждения. При ХИМ когнитивный дефицит обусловлен нарушением корково-подкорковых связей и проявляется прежде всего снижением темпа познавательной деятельности, нарушением внимания и управляющих функций. Кроме того, СКР часто сопровождаются эмоциональными и поведенческими расстройствами [4].
При ишемии (как острой, так и хронической) происходит резкое усиление окислительных процессов, что в сочетании с недостаточностью системы антиоксидантной защиты приводит к окислительному стрессу [5]. Особая опасность развития окислительного стресса в ЦНС определяется значительной интенсивностью окислительного метаболизма мозга. Головной мозг составляет 2% от общей массы человека, но при этом утилизирует от 20 до 35% всего потребляемого кислорода (O2). Интенсивность потребления O2 нейронами в десятки раз превышает потребности других клеток и тканей (350—450 мкл О2/г в 1 мин по сравнению с 70—90 мкл О2/г в 1 мин для сердца, 1,6—2,4 мкл О2/г в 1 мин для скелетных мышц, 9—24 мкл О2/г в 1 мин для фагоцитирующих лейкоцитов) [6—10]. Дополнительным фактором развития окислительного стресса в ткани мозга является высокое содержание в ней липидов (около 50% сухого вещества), ненасыщенные связи которых — субстрат перекисного окисления липидов. При этом активность ферментативных антиоксидантных систем (каталаза, глутатионпероксидаза) в мозге значительно ниже, чем в других тканях, что еще больше повышает риск развития патологических последствий окислительного стресса.
Учитывая важную роль процессов окислительного стресса в развитии КР, патогенетически оправданно включать в схему терапии ХИМ антиоксидантные препараты. Мексидол (этилметилгидроксипиридина сукцинат) — оригинальный российский антиоксидант и антигипоксант, синтезирован в НИИ фармакологии АМН в середине 1980-х годов [11].
Мексидол состоит из двух связанных и функционально значимых соединений: 2-этил-6-метил-3-гидроксипиридина и сукцината, сочетание которых обусловливает его мультимодальные свойства. Основные эффекты Мексидола — антиоксидантный, антигипоксантный и мембраностабилизирующий, а также уменьшение глутаматной эксайтотоксичности. Благодаря их сочетанию Мексидол оказывает ноотропное, антиамнестическое, анксиолитическое и другое действие [11, 12]. Эффективность Мексидола у пациентов с острой и хронической цереброваскулярной патологией продемонстрирована в ряде клинических исследований [5, 10, 13—15].
Для определения эффективности и безопасности применения последовательной терапии препаратами Мексидол в растворе и Мексидол ФОРТЕ 250 в таблетках у пациентов с ХИМ было проведено международное многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование (МЕМО) [14]. Оно продемонстрировало обоснованность и целесообразность длительного последовательного применения Мексидола и Мексидола ФОРТЕ 250 при лечении пациентов с ХИМ. Преимуществами препарата являются сочетание широты терапевтического эффекта с высоким профилем безопасности, отсутствие седативного, миорелаксирующего, стимулирующего эффектов [11, 13]. Учитывая мультимодальное действие Мексидола, его применение крайне актуально у старшей возрастной группы пациентов в целях снижения рисков полипрагмазии и развития нежелательных побочных реакций [16].
Данные доказательной медицины об эффективности и безопасности лекарственных средств у пожилых крайне ограниченны, так как возраст старше 65 лет до сих пор остается одним из основных критериев невключения в рандомизированные контролируемые исследования [17]. Между тем эффективность и безопасность терапии у пожилых может существенно отличаться от таковых у лиц среднего и молодого возраста, что связано с возрастными изменениями физиологии, приводящими в свою очередь к изменениям фармакокинетики и фармакодинамики многих лекарственных средств, что может быть обусловлено изменением плотности и чувствительности рецепторов, пострецепторными нарушениями и ухудшением регуляции гомеостатических механизмов [18]. В связи с этим остается актуальным вопрос о сопоставимости результатов РКИ в разных возрастных группах пациентов, включенных в исследование.
По результатам субанализа исследования эффективности и безопасности длительной последовательной терапии препаратом Мексидол у пациентов с полушарным ишемическим инсультом в остром и раннем восстановительном периодах (ЭПИКА) показана равная эффективность препарата по исследуемым шкалам во всех возрастных группах. Также, по результатам данного субанализа, во всех исследуемых подгруппах препарат Мексидол в режиме последовательной терапии обладал благоприятным профилем переносимости и безопасности [16].
Цель исследования — оценить эффективность последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 у пациентов разных возрастных групп с ХИМ.
Материал и методы
Представлены данные субанализа результатов международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования МЕМО, в котором участвовали 318 пациентов (25% мужчин, 75% женщин) в возрасте от 40 до 90 лет (медиана 60 лет; интерквартильный размах от 53 до 67 лет), проведенного с учетом возраста больных.
Критерии включения: возраст от 40 до 90 лет; установленный в течение 1—5 предыдущих лет диагноз ХИМ (код по МКБ-10 I.67.8); наличие синдрома УКР (по DSM-5); наличие лейкоареоза и/или признаков асимптомных инфарктов мозга по данным МРТ, проведенной в течение предшествующих 12 мес; отсутствие изменений проводимой терапии в течение предшествующего месяца; ишемический инсульт в течение 12 мес до включения в исследование; другие возможные причины когнитивного дефицита; психические нарушения (кроме синдрома УКР); аффективные расстройства; декомпенсация соматических заболеваний.
Участники были рандомизированы в две равные группы по 159 больных. Пациенты 1-й группы получали Мексидол 500 мг (10 мл) в/в капельно или медленно струйно 1 раз в сутки в течение 14 дней с последующим применением Мексидол ФОРТЕ 250 в дозировке 250 мг (табл. 1) 3 раза в сутки в течение 60 дней. Во 2-й группе было использовано плацебо, имеющее ту же лекарственную форму, схожий внешний вид, способ применения, а также упаковку и маркировку.
Таблица 1.
Результаты нейропсихологического обследования пациентов возрастной группы 40—60 лет (популяция ITT), баллы Me [Q25%; Q75%]
Table 1.
Results of neuropsychological examination of patients aged 40—60 years (ITT population), Me scores [Q25%; Q75%]
| Показатель | 1-я группа (n=80) | 2-я группа (n=83) | p |
| Шкала MoCA | |||
| исходно | 22,5 [21; 24] | 23 [21; 24] | 0,656 |
| через 75 дней | 26 [25; 28] | 24 [23; 26] | <0,001 |
| абсолютная разница, баллы | 4 [3; 5] | 2 [1; 3] | <0,001 |
| Pисх — 75дней | <0,001 | <0,001 | |
| Опросник SF-36 (физический компонент здоровья) | |||
| исходно | 48 [40; 52] | 47 [41; 52] | 0,997 |
| через 75 дней | 52 [45,5; 54,5] | 49 [44; 53] | 0,118 |
| абсолютная разница, баллы | 2 [0; 6,5] | 2 [0; 6] | 0,346 |
| Pисх — 75дней | <0,001 | 0,001 | |
| Опросник SF-36 (психологический компонент здоровья) | |||
| исходно | 45 [35,5; 52] | 42 [39; 51] | 0,729 |
| через 75 дней | 52 [45,5; 56] | 49 [41; 53] | 0,011 |
| абсолютная разница, баллы | 5 [1; 11] | 1 [-1; 9] | 0,010 |
| Pисх — 75дней | <0,001 | 0,002 | |
| Шкала MFI-20 | |||
| исходно | 58,5 [46,5; 67] | 60 [48; 66] | 0,729 |
| через 75 дней | 48 [38,5; 58,5] | 54 [43; 64] | 0,028 |
| абсолютная разница, баллы | -8 [-16,5; 0,5] | -2 [-11; 4] | 0,020 |
| Pисх — 75дней | <0,001 | 0,006 | |
| Шкала тревоги Бека | |||
| исходно | 10 [6; 15,5] | 9 [6; 14] | 0,633 |
| через 75 дней | 5 [2,5; 10] | 7 [4; 12] | 0,026 |
| абсолютная разница, баллы | -3 [-8; -0,5] | -1 [-4; 1] | 0,005 |
| Pисх — 75дней | <0,001 | 0,001 | |
| Опросник А.М. Вейна | |||
| исходно | 26 [14; 34] | 25 [17; 36] | 0,889 |
| через 75 дней | 16 [9; 32,5] | 20 [14; 28] | 0,185 |
| абсолютная разница, баллы | -4,5 [-12; 0] | -3 [-10; 0] | 0,503 |
| Pисх — 75дней | <0,001 | <0,001 | |
| Тест замены цифровых символов | |||
| исходно | 35 [28,5; 41,5] | 35 [27; 41] | 0,829 |
| через 75 дней | 46 [36; 53] | 39 [30; 47] | 0,004 |
| абсолютная разница, баллы | 6,5 [3,5; 16] | 5 [1; 8] | 0,003 |
| Pисх — 75дней | <0,001 | <0,001 | |
| Шкала Тинетти | |||
| исходно | 35 [32; 37] | 35 [31; 38] | 0,860 |
| через 75 дней | 38 [35,5; 39] | 36 [34; 38] | 0,002 |
| абсолютная разница, баллы | 2 [0; 4] | 0 [0; 3] | 0,002 |
| Pисх — 75дней | <0,001 | 0,001 | |
Обследование пациентов включало физикальный осмотр, оценку демографических и антропометрических данных, измерение артериального давления, частоты сердечных сокращений, дыхательных движений и температуры тела, электрокардиограмму, общий и биохимический анализы крови, общий анализ мочи, определение скорости клубочковой фильтрации. При помощи данных методик больные были обследованы до начала терапии (визит 1, рандомизация), на 14-й (визит 2), 28±2 (визит 3), 44±2 (визит 4) и 75±2 (визит 5) дни.
В качестве первичной конечной точки эффективности рассматривалось увеличение в динамике суммы баллов по шкале MoCA, т.е. абсолютная разница между суммой баллов до начала лечения и на 75-й день терапии. В качестве вторичных конечных точек эффективности рассматривалась динамика суммы баллов по остальным опросникам и шкалам: тесту замены цифровых символов, опроснику SF-36, шкале MFI-20, опроснику вегетативных нарушений А.М. Вейна, шкале тревоги Бека, шкале двигательной активности Тинетти.
Анализ эффективности был проведен для популяции ITT (Intent-to-treat) — 317 рандомизированных пациентов, для которых имелись данные хотя бы одного визита после рандомизации, а также для 312 пациентов, завершивших исследование в соответствии с протоколом PP (Per protocol) в целях подтверждения полученных результатов. Для проведения субанализа по возрасту пациенты были разделены на три подгруппы: 40—60 (n=163), 61—75 (n=141) и 76—90 (n=13) лет. В каждой возрастной подгруппе пациенты 1-й и 2-й групп были сопоставимы по исходной тяжести неврологических, когнитивных, эмоциональных, поведенческих и иных нарушений (табл. 1—4).
Таблица 2.
Результаты нейропсихологического обследования пациентов (популяция ITT) возрастной группы 61—75 лет, баллы, Me [Q25%; Q75%]
Table 2.
Results of neuropsychological examination of patients (ITT population) of the age group 61—75 years, points, Me [Q25%; Q75%]
| Показатель | 1-я группа (n=73) | 2-я группа (n=68) | p |
| Шкала MoCA | |||
| исходно | 21 [19; 23] | 22 [21; 23] | 0,524 |
| через 75 дней | 25 [23; 27] | 24 [22; 25] | 0,002 |
| абсолютная разница, баллы | 4 [2; 6] | 3 [1; 3] | <0,001 |
| Pисх — 75дней | <0,001 | <0,001 | |
| Опросник SF-36 (физический компонент здоровья) | |||
| исходно | 43 [38; 50] | 43 [36; 47,5] | 0,513 |
| через 75 дней | 47 [40; 52] | 46 [41; 50] | 0,317 |
| абсолютная разница, баллы | 1 [-2; 7] | 1 [-1; 6] | 0,733 |
| Pисх — 75дней | 0,016 | 0,002 | |
| Опросник SF-36 (психологический компонент здоровья) | |||
| исходно | 44 [36; 51] | 48 [40,5; 52] | 0,110 |
| через 75 дней | 51 [47; 56] | 50 [44; 56] | 0,850 |
| абсолютная разница, баллы | 5 [0; 13] | 2 [-2; 9] | 0,049 |
| Pисх — 75дней | <0,001 | 0,001 | |
| Шкала MFI-20 | |||
| исходно | 61 [56; 72] | 57,5 [51; 68] | 0,139 |
| через 75 дней | 56 [44; 64] | 53 [43; 63] | 0,855 |
| абсолютная разница, баллы | -6 [-16; 1] | -2 [-13; 2] | 0,305 |
| Pисх — 75дней | <0,001 | 0,001 | |
| Шкала тревоги Бека | |||
| исходно | 9 [6; 17] | 9 [5; 15] | 0,507 |
| через 75 дней | 5 [2; 9] | 7 [4; 12] | 0,117 |
| абсолютная разница, баллы | -3 [-8; -1] | -2 [-4; 0] | 0,008 |
| Pисх — 75дней | <0,001 | 0,003 | |
| Опросник А.М. Вейна | |||
| исходно | 26 [18; 38] | 23,5 [17; 39] | 0,595 |
| через 75 дней | 16 [8; 27] | 19 [11; 31] | 0,192 |
| абсолютная разница, баллы | -7 [-14; 0] | -2 [-10; 0] | 0,024 |
| Pисх — 75дней | <0,001 | 0,001 | |
| Тест замены цифровых символов | |||
| исходно | 30 [24; 36] | 33,5 [25,5; 39,5] | 0,166 |
| через 75 дней | 39 [30; 51] | 39 [30; 48] | 0,486 |
| абсолютная разница, баллы | 8 [4; 15] | 4 [0; 12] | 0,016 |
| Pисх — 75дней | <0,001 | <0,001 | |
| Шкала Тинетти | |||
| исходно | 32 [28; 35] | 33,5 [28,5; 37] | 0,149 |
| через 75 дней | 36 [32; 38] | 35 [32; 38] | 0,299 |
| абсолютная разница, баллы | 3 [1; 6] | 1 [0; 5] | 0,002 |
| Pисх — 75дней | <0,001 | <0,001 | |
Таблица 3.
Результаты оценки по шкале MoCA пациентов возрастной группы 76—90 лет исходно и через 75 дней, баллы
Table 3.
Results of evaluation on the MoCA scale of patients in the age group of 76—90 years at baseline and after 75 days, points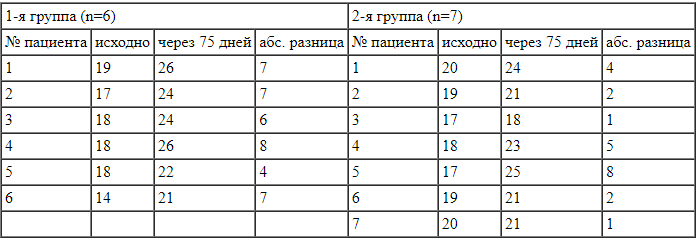 Таблица 4.
Таблица 4.
Динамика оценки по шкале MoCA пациентов возрастной группы 76—90 лет в течение 75 дней
Table 4.
Dynamics of evaluation on the MoCA scale of patients in the age group of 76—90 years for 75 days
| Показатель | 1-я группа (n=6) | 2-я группа (n=7) | p |
| Шкала MoCA, баллы, Ме [Q25%; Q75%] | |||
| исходно | 18 [17; 18] | 19 [17; 20] | 0,253 |
| через 75 дней | 24 [22; 26] | 21 [21; 24] | 0,153 |
| абсолютная разница, баллы | 7 [6; 7] | 2 [1; 5] | 0,054 |
| Pисх — 75дней | 0,028 | 0,018 | |
| Доля пациентов с когнитивными нарушениями (MoCA < 25 баллов), n (%) | |||
| исходно | 6 (100) | 7 (100) | — |
| через 75 дней | 4 (66,7) | 7 (100) | 0,192 |
| Pисх — 75дней | 0,157 | — | |
Статистическая обработка данных выполнена с использованием валидированного специализированного программного обеспечения Tibco Statistica v.13. Анализ соответствия вида распределения переменных закону нормального распределения не проводился, в связи с чем для расчетов использовались методы непараметрической статистики. Количественные и качественные порядковые переменные представлены как Me [Q25%; Q75%], где Me — медиана, Q25% — 25-й процентиль, Q75% — 75-й процентиль. Категориальные переменные представлены как « (%), где « — число пациентов, % — процент от общего числа. Для сравнения двух групп использовались критерии Манна—Уитни, х2 Пирсона или двусторонний точный тест Фишера. Для оценки динамики показателей на фоне терапии внутри группы использовались критерии Уилкоксона и х2 Мак-Немара. Различия считались статистически значимыми при двустороннем значении p<0,05.
Результаты
Проспективное 75-дневное исследование завершили 312 (98,1%) пациентов, досрочно завершили исследование 6 (1,9%) больных. Причинами досрочного завершения в 1-й группе оказались невозможность или отказ пациента следовать требованиям протокола (n=1) и отзыв информированного согласия (n=1), во 2-й — невозможность или отказ пациента следовать требованиям протокола (n=1) и отзыв информированного согласия (n=3).
Возрастная подгруппа 40—60 лет
Первичная конечная точка эффективности
Исходно пациенты обеих групп не различались по сумме баллов по шкале MoCA (см. табл. 1), при этом КР (MoCA <25 баллов) были выявлены у 100% обследуемых (табл. 5). Через 75 дней в 1-й группе сумма баллов по шкале MoCA оказалась больше (см. табл. 1), а доля лиц с КР — в 1,7 раза меньше (см. табл. 5), чем во 2-й. На фоне терапии значимое увеличение суммы баллов по шкале MoCA отмечено в обеих группах, однако в 1-й группе эта динамика была более выраженной: так, Me абсолютной разницы суммы баллов по MoCA была в 2 раза больше, чем во 2-й (см. табл. 1).
Таблица 5.
Динамика доли пациентов с КР (MoCA <25 баллов) в возрасте 40—60 лет в течение 75 дней
Table 5.
Dynamics of the proportion of patients with cognitive impairments (MoCA <25 points) aged 40—60 years for 75 days
| Показатель | 1-я группа (n=80) | 2-я группа (n=83) | p |
| Исходно, n (%) | 80 (100) | 83 (100) | — |
| Через 75 дней, n (%) | 30 (37,5) | 53 (65,4) | <0,001 |
| Pисх — 75дней | <0,001 | <0,001 |
Вторичные конечные точки эффективности
Исходно пациенты обеих групп были сопоставимы по всем исследуемым параметрам (см. табл. 1). Через 75 дней в 1-й группе сумма баллов по опроснику SF-36 (психологический компонент здоровья), шкале Тинетти и тесту замены цифровых символов оказалась значимо больше, а по шкале MFI-20 и шкале тревоги Бека — ниже, чем во 2-й. На фоне терапии значимая положительная динамика, заключающаяся в уменьшении либо увеличении суммы баллов по шкале или опроснику, выявлена в обеих группах для всех тестов, однако в 1-й группе эти изменения оказались более выраженными: так, Me абсолютной разницы суммы баллов по опроснику SF-36 (психологический компонент здоровья), шкале Тинетти, тесту замены цифровых символов, шкале MFI-20 и шкале тревоги Бека были больше, чем во 2-й группе. При оценке по опросникам А.М. Вейна и SF-36 (физический компонент здоровья) не было обнаружено различий по сумме баллов через 75 дней и Me абсолютной разницы суммы баллов между группами.
Возрастная группа 61—75 лет
Первичная конечная точка эффективности
Исходно пациенты обеих групп не различались по сумме баллов по шкале MoCA (см. табл. 2), при этом КР (MoCA <25 баллов) были выявлены у 100% обследуемых (табл. 6). Через 75 дней в 1-й группе сумма баллов по шкале MoCA оказалась больше (см. табл. 2), а доля больных с КР — в 1,5 раза меньше (см. табл. 6), чем во 2-й. На фоне терапии значимое увеличение суммы баллов по шкале MoCA отмечено в обеих группах, однако в 1-й группе эта динамика была более выраженной: так, Me абсолютной разницы суммы баллов по MoCA была в 1,3 раза больше, чем во 2-й (см. табл. 2).
Таблица 6.
Динамика доли пациентов с КР (MoCA <25 баллов) в группе в возрасте 61 —75 лет в течение 75 дней
Table 6.
Dynamics of the proportion of patients with cognitive impairments (MoCA <25 points) in the group aged 61 —75 years for 75 days, n/(%)
| Показатель | 1-я группа (n=73) | 2-я группа (n=68) | p |
| Исходно, n (%) | 73 (100) | 68 (100) | — |
| Через 75 дней, n (%) | 38/71 (53,5) | 52/67 (77,6) | 0,003 |
| Pисх — 75дней | <0,001 | <0,001 |
Вторичные конечные точки эффективности
Исходно и через 75 дней пациенты обеих групп сопоставимы по всем исследуемым параметрам (см. табл. 2). Несмотря на отсутствие значимых межгрупповых различий по сумме баллов всех тестов через 75 дней, Me абсолютной разницы суммы баллов по опроснику SF-36 (психологический компонент здоровья), шкале тревоги Бека, опроснику А.М. Вейна, шкале Тинетти и тесту замены цифровых символов оказались больше в 1-й группе (см. табл. 2). На фоне терапии значимая положительная динамика, заключающаяся в уменьшении либо увеличении суммы баллов по шкале или опроснику, выявлена в обеих группах для всех тестов, однако в 1-й группе в пяти из семи тестов эти изменения оказались более выраженными, на что указывают более высокие значения Me абсолютной разницы суммы баллов.
Возрастная подгруппа 76—90 лет
Первичная конечная точка эффективности
В связи с малым количеством участников в обеих группах представлены результаты оценки по шкале MoCA исходно и через 75 дней для каждого пациента (см. табл. 3). Через 75 дней сумма баллов по шкале MoCA увеличилась у всех пациентов в обеих группах, однако в 1-й группе абсолютная разница суммы баллов оказалась несколько больше (диапазон от 4 до 8, Me=7), чем в группе плацебо (диапазон от 1 до 8, Me=2) (см. табл. 3, 4). Несмотря на малый размер выборки, был выполнен статистический анализ с использованием методов непараметрической статистики, применение которых допустимо и в малых выборках. Исходно и через 75 дней пациенты обеих групп не различались по сумме баллов по шкале MoCA (см. табл. 4). На фоне терапии в обеих группах отмечено значимое увеличение суммы баллов по шкале MoCA, а при сравнении групп по абсолютной разнице суммы баллов более выраженная динамика выявлена в 1-й группе (p=0,054). В 1-й группе через 75 дней доля больных с КР уменьшилась на 1/3, эта динамика была статистически незначимой, вероятно, из-за малого количества наблюдений (см. табл. 4). При этом во 2-й группе через 75 дней доля пациентов с КР осталась неизменной и составила 100%.
Вторичные конечные точки эффективности
Исходно и через 75 дней пациенты обеих групп были сопоставимы по всем исследуемым показателям, за исключением суммы баллов по шкале MFI-20 через 75 дней, которая оказалась значимо ниже в 1-й группе — 52,5 [47; 55] балла против 58 [56; 61] баллов во 2-й (p=0,038), однако Me абсолютной разницы суммы баллов по шкале MFI-20 при этом не различались: —15,5 [—25; —2] балла против -10 [-18; 0] баллов соответственно (p=0,391). На фоне терапии в 1-й группе отмечено снижение суммы баллов по шкале MFI-20 (p=0,043), шкале Бека (p=0,028), шкале Тинетти (p=0,028) и тесту замены цифровых символов (p=0,028); во 2-й группе — только по шкале MFI-20 (p=0,046). В 1-й группе Me абсолютной разницы суммы баллов по шкале тревоги Бека 5 [-6; -4] баллов против —2 [-4; 0] баллов; p=0,038 и шкале Тинетти — 6 [5; 8] баллов против 1 [-1; 4] балла; p=0,046 оказались значимо больше, чем во 2-й группе. При оценке по тесту замены цифровых символов в 1-й группе выявлена тенденция к большему значению Me абсолютной разницы суммы баллов — 11,5 [8; 22] балла против 6 [-3; 6] баллов (p=0,054). Me абсолютной разницы суммы баллов по опроснику SF-36, шкале MFI-20 и опроснику Вейна не различались между группами.
Таким образом, в подгруппе пациентов в возрасте 76—90 лет преимущество Мексидола над плацебо (либо тенденция к преимуществу) отмечено только для теста замены цифровых символов, шкале тревоги Бека, шкале Тинетти, что, наиболее вероятно, связано с малым размером выборки. Поскольку применение методов статистического анализа в малых выборках имеет определенные ограничения, полученные результаты следует интерпретировать с осторожностью.
Заключение
Результаты исследования показали, что у пациентов с ХИМ улучшение когнитивных и двигательных функций, повышение качества жизни, уменьшение степени выраженности вегетативных нарушений, астении и тревожности через 75 дней терапии наблюдалось в обеих группах, однако у больных, получавших Мексидол, эти изменения были более выраженными, на что указывают значительно более высокие значения Me абсолютной разницы суммы баллов изучаемых показателей — показателя, являющегося первичной и вторичной конечными точками эффективности. Субанализ продемонстрировал наиболее значимые преимущества Мексидола над плацебо у пациентов в возрасте 40—60 и 61—75 лет. У пациентов в возрасте 76—90 лет преимущество Мексидола над плацебо (либо тенденция к преимуществу) отмечено только для теста замены цифровых символов, шкал тревоги Бека и Тинетти, что, наиболее вероятно, связано с малым размером выборки.
Таким образом, в исследовании МЕМО подтверждена эффективность длительной последовательной терапии Мексидолом в отношении когнитивных, эмоциональных и двигательных нарушений у пациентов с ХИМ различных возрастных групп. Полученные результаты свидетельствуют о целесообразности проведения длительной последовательной терапии препаратами Мексидол и Мексидол ФОРТЕ 250 у пациентов разного возраста с ХИМ.
Статья подготовлена при поддержке фармацевтической компании «Векторфарм».
The article was prepared with the support of the pharmaceutical company «Vectorpharm».
ЛИТЕРАТУРА/REFERENCES
1. Боголепова А.Н., Васенина Е.Е., Гомзякова Н.А. и др. Клинические рекомендации «Когнитивные расстройства у пациентов пожилого и старческого возраста». Журнал неврологии и психиатрии им. С.С. Корсакова. 2021;121(10-3):6-137.
Bogolepova AN, Vasenina EE, Gomzyakova NA, et al. Clinical Guidelines for Cognitive Disorders in Elderly and Older Patients. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2021;121(10-3):6-137.
2. Ritchie K. Mild cognitive impairment: an epidemiological perspective. Dial Clin Neurosci. 2004;6(4):401-408.
3. Sachdev PS, Lipnicki DM, Kochan NA, et al. The Prevalence of Mild Cognitive Impairment inDiverse Geographical and Ethnocultural Regions: The COSMIC Collaboration. PLoS One. 2015;10(11):e0142388.
4. Sachdev P, Kalaria R, O’Brien J, et al. Internationlal Society for Vascular Behavioral and Cognitive Disorders. Diagnostic criteria for vascular cognitive disorders: a VASCOG statement. Alzheimer Dis Assoc Disord. 2014;28(3):206-218.
5. Чуканова Е.И., Чуканова АС. Эффективность и безопасность препарата Мексидол ФОРТЕ 250 в рамках последовательной терапии у пациентов с хронической ишемией мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(9):39-45.
Chukanova EI, Chukanova AS. Efficacy and safety of the drug mexidol FORTE 250 as part of sequential therapy in patients with chronic ischemia of the brain. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2019;119(9):39-45. (In Russ.).
6. Chan PH. Cellular Antioxidant Defense Mechanisms. Ed. Chow CK. Boca Raton FL: CRC Press; 1988:89-109.
7. Wolfe LS. Eicosanoids: prostaglandins, thromboxanes, leucotrienes and other derivatives of carbon-20 unsaturated fatty acids. J Neurochem. 1982;38(1):1-14.
8. Packer L, Prilipko Y, et al. Free Radicals in the Brain: Aging, Neurological and Mental Disordes. Berlin: Springer-Verlag; 1992.
9. Zhang F, White J, Iadecola C. Nitric Oxide Donors Increase Blood Flow and Reduce Brain Damage in Focal Ischemia: Evidence that Nitric Oxide is Beneficial in the Early Stages of Cerebral Ischemia. J Cerebral Blood Flow Metabol. 1994;14:217-226.
10. Чуканова Е.И., Чуканова А.С., Родионова Д.М. Гипоксия и оксидантный стресс при недостаточности мозгового кровообращения и эффективные пути их коррекции. Журнал неврологии и психиатрии им. С.С. Корсакова. 2022;122(8):35-40.
Chukanova EI, Chukanova AS, Rodionova DM. Hypoxia and oxidative stress in cerebral circulation insufficiency — effective ways of correction. Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2022;122(8):35-40. (In Russ.).
11. Воронина Т.А. Мексидол: спектр фармакологических эффектов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2012;112(12):86-90.
Voronina TA. Mexidol: the spectrum of pharmacological effects. Zhurnal Nevrologii i Psikhiatrii im. S.S. Korsakova. 2012;112(12):86-90. (In Russ.).
12. Щулькин А.В. Современные представления об антигипоксическом и антиоксидантном эффектах мексидола. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2018;118(12-2):87-93.
Shchulkin AV. Modern ideas about the antihypoxic and antioxidant effects of mexidol. Journal of Neurology and Psychiatry named after S.S. Korsakov. Special issues. 2018;118(12-2):87-93. (In Russ.).
13. Журавлева М.В., Прокофьев А.Б., Сереброва С.Ю. и др. Эффективность и безопасность применения этилметилгидроксипиридина сукцината у пациентов с хронической ишемией головного мозга. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(6):119-124.
Zhuravleva MV, Prokofiev AB, Serebrova SYu, et al. Efficacy and safety of ethylmethylhydroxypyridine succinate in patients with chronic cerebral ischemia. S.S. Korsakov Journal of Neurology and Psychiatry = Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2020;120(6):119-124. (In Russ.).
14. Федин А.И., Захаров В.В., Танашян М.М. и др. Результаты международного многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования оценки эффективности и безопасности последовательной терапии пациентов с хронической ишемией мозга препаратами Мексидол и Мексидол ФОРТЕ 250 (исследование МЕМО). Журнал неврологии и психиатрии им. С.С. Корсакова. 2021;121(11):7-16.
Fedin AI, Zakharov VV, Tanashyan MM, et al. Results of an international multicenter, randomized, double-blind, placebo-controlled study assessing the efficacy and safety of sequential therapy with Mexidol and Mex-idol FORTE 250 in patients with chronic brain ischemia (MEMO). Zhurnal nevrologii i psikhiatrii im. S.S. Korsakova. 2021;121(11):7-16. (In Russ.).
15. Стаховская Л.В., Шамалов Н.А., Хасанова Д.Р. и др. Результаты рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных группах исследования эффективности и безопасности мексидола при длительной последовательной терапии у пациентов в остром и раннем восстановительном периодах. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(3-2):55-65.
Stakhovskaya LV, Shamalov NA, Khasanova DR, et al. Results of a randomized, double-blind, multicenter, placebo-controlled, parallel-group study of the efficacy and safety of mexidol in long-term sequential therapy in patients in acute and early recovery period. Journal of Neurology and Psychiatry named after S.S. Korsakov. 2017;117(3-2):55-65. (In Russ.).
16. Стаховская Л.В., Мхитарян Э.А., Ткачева О.Н. и др. Эффективность и безопасность Мексидола у пациентов разных возрастных групп в остром и раннем восстановительном периодах полушарного ишемического инсульта (результаты субанализа рандомизированного двойного слепого мультицентрового плацебо-контролируемого в параллельных группах исследования ЭПИКА). Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2020;120(8):49-57.
Stakhovskaya LV, Mkhitaryan EA, Tkacheva ON, et al. Efficacy and safety of Mexidol across age groups in the acute and early recovery stages of hemispheric ischemic stroke (results of additional subanalysis of a randomized double blind multicenter placebo-controlled, in parallel groups trial EPICA). Zhurnal nevrologii i psikhiatrii imeni S.S. Korsakova. 2020;120(8):49-57. (In Russ.).
17. Vitale C, Fini M, Spoletini I, et al. Under-representation of elderly and women in clinical trials. Int J Cardiol. 2017;232:216-221.
18. Общие принципы фармакотерапии у лиц пожилого и старческого возраста: Методические рекомендации. Под ред. Ткачевой О.Н. М.: Прометей; 2019:66.
General principles of pharmacotherapy in elderly and senile personsta: Methodological recommendations. Ed. Tkacheva ON. M.: Prometheus; 2019:66.
