Функциональные расстройства билиарного тракта. Диагностика. Лечение.
СтатьиАгафонова Н.А., Яковенко Э.П., Яковенко А.В., Иванов А.Н.
Анатомо-физиологические особенности билиарного тракта
Билиарный тракт включает внутрипеченочный и внепеченочный отделы билиарной системы. Начальным звеном билиарного тракта является внутрипеченочная интралобулярная билиарная система, представленная межклеточными желчными каналикулами (желчные канальцы), стенками которых являются каналикулярные (билиарные) полюса двух смежных гепатоцитов. Желчные канальцы имеют диаметр 1 — 2 мкм, их просвет ограничен печеночными клетками (гепатоцитами) и они не имеют собственной стенки. Каждая печеночная клетка участвует в образовании, по крайней мере, двух желчных канальцев. Желчные каналикулы, сливаются друг с другом и на периферии печеночной дольки образуют более крупные перилобулярные желчные ходы, выстланные холангиоцитами (терминальные дуктулы, холангиолы, канальцы Геринга). Холангиолы, проходя через пограничную пластинку печеночной дольки, в портальных трактах сливаются и образуют междольковые желчные протоки, стенки которых внутри выстланы холангиоцитами, а снаружи покрыты соединительнотканной оболочкой, в более крупных из них имеется также гладкомышечные волокна.
Далее желчь из каждой доли печени поступает в правый (длиной 1 см) и левый (длиной 2 см) печеночные протоки и после их слияния - в общий печеночный проток (длиной 2 — 3 см). Общий печеночный проток покидает ворота печени и соединяется с пузырным протоком, длиной 3—4 см. В месте слияния печеночного и пузырного протоков находится сфинктер Мирицци. От места соединения общего печеночного и пузырного протоков начинается общий желчный проток (холедох) длиной 5 — 8 см, впадающий в двенадцатиперстную кишку (ДПК). Таким образом, формируется внепеченочная часть билиарного тракта, включающая желчные протоки левой и правой доли, общий печеночный проток, желчный пузырь (ЖП), пузырный проток и большой дуоденальный сосочек (БДС). (рис.1).
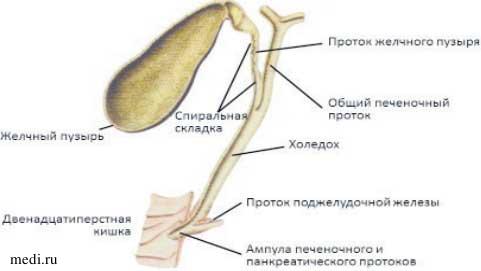
Рисунок 1. Строение внепеченочного билиарного тракта
Холедох располагается между листками печеночно-двенадцатиперстной связки идет вниз позади верхней горизонтальной части ДПК, между ее нисходящей частью и головкой поджелудочной железы, а иногда и через ее ткань и, соединившись с главным протоком поджелудочной железы (Вирсунгов проток), открывается на медиальной стенке нисходящей части ДПК в составе сфинктера Одди (СФО). В холедохе различают: супрадуоденальный, ретродуоденальный, ретропанкреатический, интрапанкреатический и интрамуральные отделы. Ширина протоков составляет: печеночного - от 0,4 до 1,6 мм, пузырного - от 1,5 до 3,2 мм, холедоха - по рентгенологическим данным от 2 до 9 мм; по данным ультразвукового исследования - от 2 до 6 мм, после удаления желчного пузыря - от 4 до 10 мм. Все желчные протоки имеют идентичное строение. Они выстланы кубическим эпителием, а крупные протоки— цилиндрическим эпителием. Слизистая оболочка протоков имеет большое количество слизистых желез, выполняющих секреторную функцию. Эпителий протоков осуществляют также всасывательную и синтетическую (синтез иммуноглобулинов, преимущественно А) функции. В крупных желчных протоках выражена соединительнотканная оболочка с наличием единичных мышечных элементов и только в пузырном и общем желчном протоках имеются сфинктеры (сфинктер Люткенса и сфинктер холедоха, соответственно).
Сфинктер Одди.
Терминальный отдел холедоха охвачен тремя слоями мышц, образующих СФО, названный так по имени R. Oddi, описавшего данное мышечное образование в 1887 году. СФО - фиброзно-мышечное образование, окружающее конечные отделы холедоха и главного панкреатического протока, а также общий их канал в толще стенки ДПК, который открывается БДС, называемым также Фатеровым сосочком. При слиянии холедоха и протока поджелудочной железы образуется веретенообразное расширение - ампула Фатера, имеющая диаметр около 2-4 мм, реже - 10 мм. В ряде случаев ампула может отсутствовать. В ампуле находится своеобразный клапанный аппарат, образуемый продольными и поперечными складками слизистой оболочки, который вместе со сфинктерным аппаратом участвует в процессе желчеотделения. Высота БДС варьирует от 2 мм до 2 см. Место расположения Фатерова соска вариабельно, но, как правило, находится на медиальной стенке нисходящего отдела ДПК в 12-14 см от привратника. На несколько сантиметров проксимальнее БДС расположена малая папилла - сосочек, сформированный устьем добавочного (Санториниевого) протока поджелудочной железы.
В норме СФО состоит из трех образований:
1. Сфинктер общего желчного протока -наиболее мощный, он отграничивает полость общего желчного протока от полости БДС.
2. Сфинктер главного панкреатического протока, обычно развит слабо.
3. Сфинктер ампулы БДС, окружающий общий канал.
На Рисунке 2 представлены три варианта взаимоотношения дистальных отделов общего желчного и главного панкреатического протоков в ампуле БДС. Наиболее распространенный вариант (около 80%) - протоки сливаются под слизистой ДПК и имеют общий канал (Y-образная форма). Наличие общего канала при слиянии холедоха и главного панкреатического протока имеет большое значение в патогенезе формирования и прогрессировании патологии поджелудочной железы при заболеваниях билиарного тракта. В ряде случаев (около 10%) отмечено параллельное расположение протоков, они не сливаются, имеют раздельные устья. Возможен третий вариант - слияние протоков происходит до кишечной стенки (10%). СФО регулирует поступление желчи в кишечник во время процесса пищеварения и препятствует обратному забрасыванию дуоденального содержимого и желчи в желчные протоки и проток поджелудочной железы.
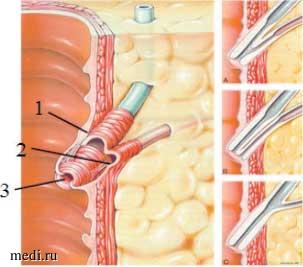 Рисунок 2. Анатомические элементы сфиктера Одди
Рисунок 2. Анатомические элементы сфиктера ОддиЖелчный пузырь (ЖП) имеет форму вытянутого мешка объемом 40—60 мл. ЖП располагается в передней части правой продольной борозды печени. Стенка ЖП состоит из слизистой, мышечной и соединительнотканной оболочек, толщина ее в норме составляет 3 мм. Мышечная оболочка ЖП представлена тремя слоями мышечных волокон, имеющих разное направление (поперечное, продольное и косое) и предназначена для осуществления сократительной функции в период пищеварения и тонических сокращений в межпищеварительный период для перемешивания и сгущения желчи. Слизистая оболочка имеет многочисленные выросты, увеличивающие всасывательную поверхность ЖП, благодаря которой осуществляется концентрирование печеночной желчи (в 6—10 раз) в основном за счет всасывания воды. Часть стенки, обращенная в брюшную полость, покрыта брюшиной. В ЖП различают дно, тело и шейку. Шейка ЖП вместе с пузырным протоком располагается в гепатодуоденальной связке. В месте перехода шейки в пузырный проток мышечный слой несколько гипертрофируется и волокна его направляются циркулярно, образуя сфинктер Люткенса.
При удалении ЖП он отсекается от шейки и оставляется культя пузырного протока не более 1 см, в случае ее больших размеров культя может трансформироваться в подобие ЖП с клиническими проявлениями.
ЖП выполняет следующие важные функции: концентрацию и накопление желчи в межпищеварительный период; сокращение и эвакуацию желчи в ДПК для участия в процессе пищеварения; поддержание давления в системе желчевыводящих путей; гормональную - выделение слизистой ЖП антагониста ХЦК - антихолецистокинина.
Состав и формирование желчи
Продукция желчи гепатоцитами идет непрерывно в течение суток, в среднем 12-15 мл на килограмм массы тела и может составлять в объеме от 600 до 1500 мл/сутки.
Формирование желчи складывается из следующих этапов:
- Захват из крови ряда ее компонентов (желчных кислот, билирубина, холестерина и др.) на уровне базолатеральной мембраны;
- Метаболизм, а также синтез новых составляющих и их транспорт в цитоплазме гепатоцитов;
- Выделение их через каналикулярную (билиарную) мембрану в желчные канальцы;
- Поступление желчи во внутрипеченочную билиарную систему (желчные протоки);
- Накопление и концентрация желчи в ЖП;
- Поступление желчи в тонкую кишку, всасывание ее компонентов и поступление их в энтерогепатическую циркуляцию.
Через базолатеральную мембрану гепатоцитов обеспечивается поступление из плазмы крови (из пространств Диссе) в цитоплазму гепатоцитов желчных кислот (ЖК), аминокислот, неконъюгированного билирубина, глюкозы и ряда эндогенных и экзогенных ксенобиотиков, в том числе лекарственных средств, растительных стеролов и ксенобиотиков. Эти процессы осуществляются благодаря наличию в составе базолатеральных мембран Na+-K+-АТФазы, а также специфических и неспецифических белков-переносчиков для органических анионов, обладающих перекрестной реактивностью. Функционирование Na'-K'-АТФазы обеспечивает энергетический потенциал и ионное равновесие клетки, а также нормальную текучесть (проницаемость) клеточных мембран. К основным белкам-переносчикам относятся: транспортирующий органические анионы белок, транспортирующий Na+/ЖК белок, Na+-H+- и Na+-HСO3-ионообменники, осуществляющие перенос ионов через мембрану и поддерживающие в гепатоцитах нормальный уровень рН.
В гепатоците из холестерина синтезируются две первичные ЖК: холевая и хенодезоксихолевая, которые конъюгируются с аминокислотами - глицином или таурином. Конъюгация обеспечивает их растворимость в воде даже при кислых значениях рН, делает их устойчивыми к преципитации ионами кальция и снижает их проницаемость через клеточные мембраны. В гепатоцит из энтерогепатической циркуляции также поступают первичные конъюгированные и деконъюгированные ЖК. Первые в неизмененном виде, а вторые - после реконъюгации вновь секретируются в желчь. Вторичные ЖК (дезоксихолевая и литохолевая), которые являются продуктами микробного метаболизма соответственно из холевой и хенодезоксихолевой кислот, попадая из энтерогепатической циркуляции в гепатоцит, конъюгируются. Дезоксихолевая кислота связывается с глицином или таурином и циркулируют вместе с первичными ЖК. Литохолевая кислота наряду с глицином, таурином конъюгируется и с сульфатами, что резко снижает ее всасывание и поступление в энтерогепатическую циркуляцию. Последнее имеет огромный биологический смысл, а именно: сохранение целостности гепатоцитов и билиарного эпителия. Реже в энтерогепатическую циркуляцию включается урсодезоксихолевая кислота (УДХК), которая является продуктом микробной модификации первичных ЖК. Максимальное содержание ее в общем пуле ЖК не превышает 5%.
Внутриклеточный транспорт ЖК от базолатеральной до каналикулярной мембраны гепатоцита осуществляется цитозольными протеинами (3-а-гидрокси-стероиддегидрогеназа и др.). В этот процесс также вовлекаются эндоплазматический ретикулум и аппарат Гольджи. Большое значение придается трансцитозольному везикулярному транспорту ЖК, билирубина и липидсодержащих субстанций. Время прохождения компонентов желчи от базолатеральной до каналирулярной мембраны составляет около 10 минут.
Каналикулярная секреция является наиболее важным этапом формирования желчи. Компоненты желчи поступают в каналикулы 4 путями:
1. Активный транспорт простых молекул с участием АТФ-зависимых помп;
2. Экзоцитоз липид- и протеинсодержащих везикул;
3. Индуцированная ЖК везикулизация молекул фосфолипидов из поверхности каналикулярных мембран;
4. Пассивный ток жидкости из пространств Диссе через плотные межклеточные соединения.
Экскреция компонентов желчи из гепатоцитов осуществляется с участием АТФ-зависимых транспортных белков, способных перемещать компоненты желчи из цитоплазмы в просвет канальцев против градиента концентраций. К транспортным системам относятся: специфический белок-переносчик ЖК, мультиспецифический переносчик органических анионов (билирубина, ЖК, глютатиона, растительных стеролов и др.), белок-переносчик для фосфолипидов, белки-ионообменники и др. В результате их функционирования в канальцы поступают ЖК и их соли, а также ряд других осмотически активных веществ (глутатион, бикарбонаты). Последние участвуют в формировании зависимой и независимой от ЖК фракций желчи, составляющих по 225 мл/ сутки каждая. Вода диффундирует в канальцы по осмотическому градиенту из синусоидов через плотные межклеточные соединения, в среднем 150 мл/сутки. Соединения, которые активно транспортируются в каналикулы из гепатоцитов и участвуют в формировании желчи, обозначаются как первичные компоненты желчи (конъюгированные ЖК, органические анионы и др.). Они не способны проходить через межклеточные соединения канальцев. Первичные компоненты желчи, и в первую очередь, ЖК обладают холеретической активностью. Молекулы, которые поступают в каналикулы пассивно через межклеточные соединения, обозначаются как вторичные компоненты желчи. В их состав входят вода, электролиты, глюкоза, ионы кальция.
Ток желчи в каналикулях обеспечивается активной каналикулярной секрецией и сокращением периканаликулярных нитей актина, которые индуцируются конъюгированными ЖК. Из каналикул желчь через промежуточные канальцы Геринга поступает в экстралобулярные желчные протоки, и далее в долевые, общий печеночный и желчный проток.
Во время прохождения желчи по внутрипеченочным желчным протокам состав ее изменяется: через межклеточные соединения протокового эпителия в просвет диффундирует вода; холангиоцитами абсорбируются глюкоза и некоторые органические кислоты; происходит гидролиз глютатиона до аминокислот, которые частично всасываются. При появлении в желчи неконъюгированных ЖК последние всасываются пассивно холангиоцитами и поступают в гепатоцит через перидуктулярные капилляры (холегепатическая циркуляция ЖК). Под влиянием секретина и глюкагона происходит активная секреция бикарбонатов и отмечается увеличение содержания IgA и слизи.
Желчь представляет собой водный (коллоидный) раствор органических и неорганических веществ. В физиологических условиях желчь стерильна, имеет щелочную реакцию (рН - 7,3-8,0). Желчь содержит практически все составные компоненты организма: белки, липиды, углеводы, витамины, минеральные соли, но основными являются: вода, ЖК, желчные пигменты, фосфолипиды, холестерин, лецитин, большинство из которых синтезируются гепатоцитами. Основные компоненты желчи, секретируемые в билиарный тракт, и их функции представлены в таблице 1.
Таблица 1.
Основные компоненты желчи, как билиарного секрета, и их функции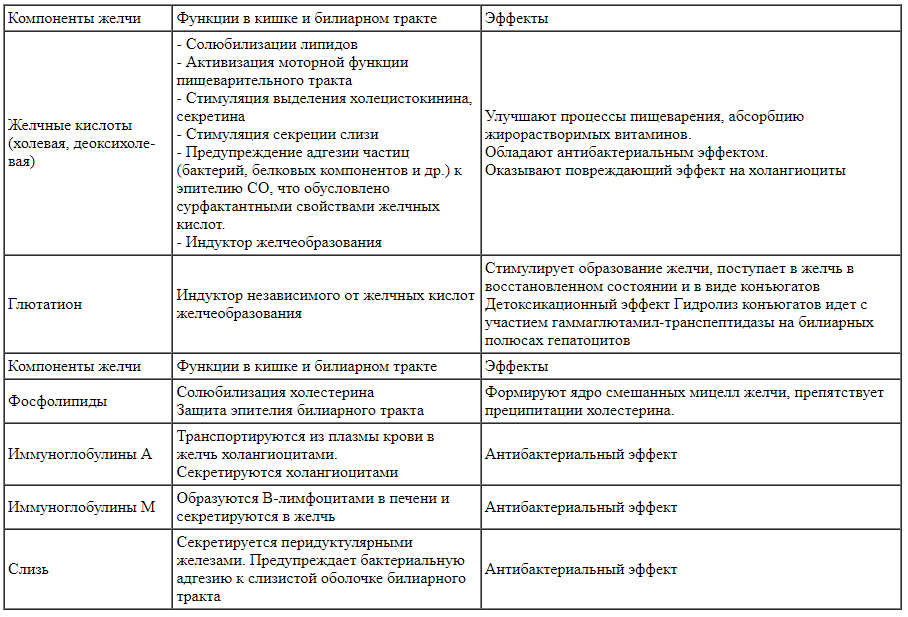 Желчь выполняет также экскреторную и детоксицирующую функции. Основные компоненты желчи, экскретируемые в билиарный тракт, представлены в таблице 2.
Желчь выполняет также экскреторную и детоксицирующую функции. Основные компоненты желчи, экскретируемые в билиарный тракт, представлены в таблице 2.
Таблица 2.
Основные компоненты желчи, как билиарного секрета, и их функции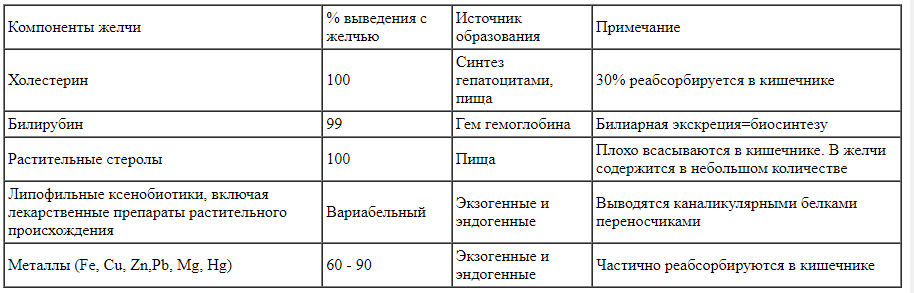 Билиарная экскреция является единственным путем выведения из организма растительных стеролов, таких как ситостерол, а также ксенобиотиков, присутствующих в растениях, препятствуя их накоплению в организме. Все они, а также ряд липофильных лекарств, метаболиты жирорастворимых витаминов и стероидных гормонов в гепатоците конъюгируются с глютатионом, сульфатами, глюкуроновой кислотой; реже с глюкозой, ксилозой, глицином или таурином и выделяются в желчь. Данные компоненты желчи и, в первую очередь, растительные стеролы, благодаря конъюгации с глютатионом, увеличивают концентрацию органических анионов в каналикулах и участвуют в формировании фракции желчи, независимой от ЖК и таким образом оказывают желчегонный эффект.
Билиарная экскреция является единственным путем выведения из организма растительных стеролов, таких как ситостерол, а также ксенобиотиков, присутствующих в растениях, препятствуя их накоплению в организме. Все они, а также ряд липофильных лекарств, метаболиты жирорастворимых витаминов и стероидных гормонов в гепатоците конъюгируются с глютатионом, сульфатами, глюкуроновой кислотой; реже с глюкозой, ксилозой, глицином или таурином и выделяются в желчь. Данные компоненты желчи и, в первую очередь, растительные стеролы, благодаря конъюгации с глютатионом, увеличивают концентрацию органических анионов в каналикулах и участвуют в формировании фракции желчи, независимой от ЖК и таким образом оказывают желчегонный эффект.
В межпищеварительный период основная масса желчи поступает в ЖП, где она концентрируется в результате абсорбции воды, электролитов, включая ионы кальция. Эта абсорбция приводит к активизации Na+/ Н+-обменника, в результате чего бикарбонаты замещаются на СО2 и снижается уровень рН желчи. В желчи сохраняются смешанные мицеллы, которые включают достаточно большое количество молекул, но они имеют такой же осмотический потенциал, как и мономеры. В результате пузырная желчь может содержать анионов в концентрации, превышающей 200 ммоль и оставаться изотоничной. При этом содержание главных компонентов в пузырной желчи: ЖК, желчных пигментов (билирубина, биливердина), холестерина и др. может увеличиваться в 5-10 раз по сравнению с печеночной. Состав печеночной и пузырной желчи представлен в таблице 3.
Таблица 3.
Состав печеночной и пузырной желчи
| Компоненты | Печеночная желчь | Пузырная желчь |
| Цвет | золотисто-желтый | темно-коричневый |
| Удельный вес | 1.008-1.015 | 1.026-1.048 |
| Реакция (рН) | 7.3-8 | 6.8 |
| Вода | 97.5% | 86% |
| Сухой остаток | 2.5% | 14% |
| Желчные кислоты | 0.6% | 7% |
| Желчные пигменты (билирубин, биливердин) | 0.5% | 4.1% |
| Холестерин | 0.15% | 0.6% |
| Муцин (слизь) | отсутствует | много |
Во время приема пищи ЖП опорожняется и в течение 30-45 минут остается в сокращенном, а СФО - в расслабленном состоянии. В этот период слизистой оболочкой в просвет ЖП секретируются вода и электролиты, что способствует вымыванию из него всех накопившихся субстанций, а в ДПК непрерывно поступает печеночная желчь. При отсутствии ЖП в межпищеварительный период печеночная желчь депонируется в проксимальных отделах тонкой кишки, главным образом, в ДПК, а после еды поступает в дистальные отделы. Избыточное содержание желчи в ДПК с развитием дуоденальной гипертензии является одним из механизмов развития болевого синдрома и диспепсических расстройств у больных, перенесших холецистэктомию.
После поступления желчи в тонкую кишку метаболизм и скорость транзита каждого из ее компонентов существенно различаются. Так, скорость транзита ЖК значительно ниже, чем других компонентов желчи. Лишь незначительная часть ЖК (не более 5%) теряется с калом, основная их масса всасывается и вступает в энтерогепатическую циркуляцию. В проксимальных отделах тонкой кишки часть конъюгированных с глицином ЖК всасывается пассивно. Основная масса ЖК абсорбируется активно с участием специфического белка-переносчика (илеальный транспортер для ЖК), который локализуется на апикальной поверхности энтероцитов. В дистальных отделах тонкой и в толстой кишке ЖК подвергаются микробной деконъюгации и легко абсорбируются пассивным способом.
Поступая в венозную кровь основная масса ЖК (70-90%) связывается с альбумином и возвращается в печень, где они захватываются гепатоцитами, конъюгируются и вновь транспортируются в билиарную систему и в кишечник. В результате вышеуказанной энтерогепатической циркуляции в организме формируется пул ЖК, равный приблизительно 5 ммоль с периодом полураспада в 2-3 дня.
В регуляции желчеобразования и желчевыведения. определенная роль принадлежит давлению в желчных протоках (N 150-200 мм водного столба). При повышении давления в протоках секреция желчи снижается, а при достижении уровня 350 мм водяного столба - полностью прекращается секреция билирубина, ЖК и воды.
Холекинез
Выделение образовавшейся в печени желчи в кишечник имеет сложный механизм, включающий согласованные функции печени, ЖП, желчных протоков, сфинктеров желчных путей. Направление движения желчи по желчным путям определяется созданием градиентов давления. В его формировании участвуют: печеночная секреция, ритмическая деятельность сфинктера холедоха в составе СФО, сфинктера ЖП (Люткенса), всасывательная функция слизистой оболочки ЖП и протоков билиарной системы, внутриполостное давление во внепеченочных желчных путях и ДПК.
В межпищеварительный период желчь, вырабатываемая печенью постоянно, поступает в ЖП, где происходит ее концентрация. Особую роль в регуляции направления тока печеночной желчи в ЖП играет пузырный проток со сфинктером Люткенса и клапанный аппарат Хайстера. В этот период сфинктеры Мирицции и Люткенса расслаблены, а СФО закрыт, с чем связано формирование минимального градиента давления. Для его поддержания происходит периодическое открытие СФО и небольшой сброс желчи в ДПК,что необходимо для нормального функционирования печени и системы желчевыделения.
После приема пищи (пищеварительный период) происходит синхронное сокращение ЖП и холедоха с повышением давления до 200-300 мм вод. ст. в ЖП и до 100-150 мм вод.ст. - в холедохе с последующем током желчи в ДПК. При этом в регуляции тока желчи по холедоху активно участвует сфинктер Мирицци, который препятствует регургитации желчи во внутрипеченочные желчные протоки.
СФО, обеспечивающий поступление желчи в ДПК, обладает двумя типами моторной активности: базальное давление и фазовая, периодическая сократительная активность. Базальное давление отвечает за регуляцию оттока секрета из желчных и панкреатических протоков. Фазовые сокращения СФО накладываются на базальное давление с частотой около 4 в минуту и перемещаются от проксимальных к дистальным отделам (антеградно). Моторная активность СФО регулируется сложными нейрогормональными взаимодействиями благодаря наличию пептидергических нейронов, реагирующих на различные нейропептиды: энкефалин/ эндорфин, субстанцию P, NO, VIP, нейропептид Y, холецистокинин, кальцитонин ген-связанный пептид. Например, окись азота уменьшает частоту фазовых сокращений и базальное давление СФО, а также угнетает моторику ДПК. При ингибировании синтеза окиси азота наблюдается увеличение спонтанных сокращений СФО.
Выделение желчи в просвет ДПК начинается в ответ на комплекс условных и безусловных раздражителей, включение которых связано с приемом определенного качества и количества пищи. Главным регулятором, обеспечивающим функционирование желчевыделительного аппарата, является ДПК. Ритм колебаний давления в полости ДПК полностью коррелирует с ритмом желчеотделения, т.е. периодика желчеотделения модулируется ДПК. Следует также подчеркнуть, что актин мышц СФО имеет больше сходства с актином продольного мышечного слоя ДПК, чем, например, с актином мышц нижнего пищеводного сфинктера, что подчеркивает общность строения ДПК и СФО. Через эфферентные волокна блуждающего нерва стимулируется моторика ЖП, общего желчного протока и расслабление СФО. Этот процесс обусловлен не только раздражением рецепторов желудка и ДПК химусом, но и влиянием на мускулатуру желчевыводящего аппарата гастроинтестинальных гормонов холецистокинина-панкреазимина, секретина, мотилина, глюкагона и др.
Ведущая роль в регуляции холереза и холекинеза принадлежит гастроинтестинальным гормонам - холецистокинину и секретину. Холецистокинин секретируется гормональными клетками ДПК. Основные эффекты холецистокинина сводятся к:
а) повышению тока печеночной желчи;
б) сокращению ЖП;
в) релаксации СФО;
г) повышению панкреатической секреции;
д) снижению давления в билиарной системе.
Продукцию холецистокинина стимулируют жиры, особенно с наличием жирных кислот с длинной цепью (жареные продукты), белки, кислоты, составные компоненты желчегонных трав (алкалоиды, протопин, сангвинарин, эфирные масла и др.), холинэргические стимулы. Секретин, продуцирующийся в ДПК, стимулирует секрецию воды, электролитов и бикарбонатов эпителием билиарных и панкреатических протоков и потенцирует эффекты холецистокинина. Основными стимуляторами выделения секретина являются соляная кислота, жиры, ЖК и, возможно, растительные алкалоиды и стеролы. В результате происходит сокращение ЖП, расслабление СФО и концентрированная пузырная желчь, к которой примешивается небольшая часть печеночной желчи, а также панкреатический секрет поступают в ДПК для участия в процессах пищеварения. Торможение желчевыведения происходит при раздражении симпатических нервов (расслабление мышц ЖП, общего желчного протока и сокращение СФО), а также под влиянием некоторых гормонов (ВИП, кальцитонина и др).
Таким образом, отток желчи и панкреатического секрета в ДПК осуществляется благодаря координированному функционированию ЖП, сфинктера Люткенса и СФО, при участии гастроинтестинальных гормонов и нейропептидов. Определенная роль в этом процессе принадлежит уровню секреции желчи и панкреатического сока, моторной функции желудочно-кишечного тракта, в первую очередь, ДПК и энтерогепатической циркуляции ЖК.
Понимание роли желчи в процессах пищеварения позволяет идентифицировать механизмы формирования симптомов при нарушениях ее поступлении в ДПК (таблица 4).
Таблица 4.
Роль желчи в пищеварительном тракте
| Участие в процессах пищеварения |
|
| Активизация моторной функции кишечника |
|
| Предупреждение избыточного бактериального роста в кишечнике |
|
| Увеличение циркуляции желчи в ЖП, что снижает ее литогенность, обеспечивает стерильность, стимулирует сократительную функцию ЖП и координирует тонус сфинктера Одди; | |
| Участие во всасывании жирорастворимых витаминов (A, D, Е, К) | |
| Экскреция из организма эндогенных и экзогенных ксенобиотиков (детоксикация организма), холестерина, билирубина, Cu, и др. | |
Функциональные расстройства билиарного тракта.
Классификация и определение.
В соответствии с IV Римским консенсусом по диагностике и лечению функциональных заболеваний органов желудочно-кишечного тракта (ЖКТ) функциональные расстройства билиарного тракта определяются как комплекс клинических симптомов, обусловленных нарушением сократительной функции ЖП и тонуса сфинктеров билиарной системы .
Функциональные расстройства билиарного тракта традиционно подразделяются:
по этиологии:
- первичные дисфункции
- вторичные дисфункции
по локализации:
- дисфункция ЖП
- дисфункция СФО
по функциональному состоянию:
- гиперкинетическая функция ЖП/СФО
- гипокинетическая функция ЖП/СФО
В МКБ - 10: К82.8.0 Дискинезия ЖП и желчных путей.
В соответствии с Римским консенсусом IV (2016г.), функциональные расстройства билиарного тракта включены в рубрику Е и подразделяются на:
Е1. Функциональное расстройство ЖП;
Е2. Функциональное расстройство СФО билиарного типа;
Е3 Функциональное расстройство СФО панкреатического типа
Распространенность функциональных расстройств билиарного тракта по разным оценкам колеблется от 12 до 58%. Среди женщин функциональные билиарные расстройства встречаются в 2-3 раза чаще, чем среди мужчин. Первичные функциональные расстройства регистрируется, почти в полтора раза реже вторичных. Наиболее часто в практике врача встречаются сочетание повышения тонуса СФО и гипокинетической дискинезии ЖП, и повышение тонуса СФО после удаления ЖП.
Первичные функциональные расстройства билиарного тракта определяются как комплекс клинических симптомов (болевой абдоминальный и диспепсический синдромы), которые обусловлены моторно-тоническими нарушениями ЖП и СФО, при отсутствии признаков органической патологии желчевыводящей системы. Данные симптомы могут быть постоянными или возникать периодически, по крайней мере, в течение не менее 3 последних месяцев с началом их проявлений не менее 6 месяцев перед диагностикой. (Рим IV. 2016).
Функциональные расстройства ЖП и СФО сочетающиеся с органическими, воспалительными изменениями или аномалиями билиарного тракта, а также сопровождающие заболевания других органов пищеварения и систем организма относятся к вторичным. Вторичные функциональные расстройства ЖП могут наблюдаться при следующих состояниях: воспалительные заболевания ЖП (острый и хронический холецистит), полипоз ЖП, заболевания печени (стеатоз, стеатогепатит, гепатит, цирроз печени и др.), желудка и ДПК (хронический гастрит, хронический дуоденит, язвенная болезнь 12пк и др.), заболевания поджелудочной железы (хронический панкреатит), заболевания, сопровождающиеся нарушением обмена холестерина (холестериновый холецистолитиаз, холестероз ЖП), заболевания кишечника (целиакия, болезнь Крона), оперативные вмешательства (ваготомия, резекция желудка и ДПК, обширные резекции тонкой кишки), длительное соблюдение строгой диеты, нерегулярный прием пищи с длительными интервалами, эндокринные заболевания (гипотиреоз, сахарный диабет), высокий уровень эстрогенов в крови (беременность, прием контрацептивных препаратов, вторая фаза менструального цикла), длительная терапия миотропными спазмолитиками и соматостатином, системные заболевания (системная красная волчанка, склеродермия) и другие причины.
Функциональное расстройство СФО чаще наблюдается у больных, после удаления ЖП. Экспериментальными и клиническими наблюдениями установлено, что отсутствие функционирующего ЖП отражается на работе СФО. В настоящее время преобладает точка зрения, что после удаления ЖП развивается гипертонус СФО. Механизм гипертонуса СФО связывают с выключением регулирующей роли сфинктера Люткенса и мышечной активности ЖП, так как тонус СФО рефлекторно понижается во время сокращения ЖП, что обеспечивает скоординированную деятельность всего сфинктерного аппарата желчных путей. У больных после холецистэктомии отмечается: повышение базового давления, увеличение частоты сокращений СФО, парадоксальный ответ на ХЦК (вместо нормального расслабления, он сокращается и замедляет отток желчи и панкреатического секрета). В первые месяцы после холецистэктомии спазм СФО отмечается у 85,7% больных. В дальнейшем под действием адаптационных процессов и при отсутствии патологических изменений в органах гепатодуоденопанкреатической системы возможна нормализация тонуса СФО. Так, через год после холецистэктомии спазм СФО отмечался у 63%, а через 2 года -у 30% пациентов. После удаления ЖП постепенно происходит адаптация билиарной системы к новым условиям функционирования, в частности, отмечается расширение («опузыривание») холедоха.
Диагностические критерии функциональных расстройств билиарного тракта
Функциональное расстройство желчного пузыря
Диагностические критерии функционального расстройства ЖП включают:
1. Наличие билиарной боли.
2. Отсутствие камней или других структурных изменений ЖП
Подтверждающими критериями являются:
1. Нормальные уровни печеночных ферментов, конъюгированного билирубина и амилазы/липазы крови
2. Низкая фракция выброса ЖП при сцинтиграфии.
Функциональные расстройства СФО билиарного типа
Диагностические критерии функционального расстройства СФО билиарного типа включают:
1.Наличие билиарной боли
2. Повышение уровня печеночных ферментов, щелочной фосфатазы >2 норм, связанное по времени, по крайней мере, с двумя эпизодами болей или дилатация холедоха, но не оба признака вместе
3. Отсутствие камней или органических изменений в протоке
Подтверждающими критериями являются:
Нормальные показатели амилазы /липазы
Изменение показателей манометрии СФО (является предиктором хорошего ответа на сфинктеротомию).
Патологические результаты гепатобилиарной сцинтиграфии.
Функциональные расстройства СФО панкреатического типа.
Диагностические критерии функционального расстройства СФО панкреатического типа включают:
1. Документально подтвержденные повторяющиеся эпизоды острого панкреатита с повышением амилазы/липазы >3 норм и/или инструментальные доказательства острого панкреатита (УЗИ).
2. Исключение другой этиологии панкреатита
3. Отсутствие органической патологии при эндоскопическом ультразвуковом исследовании (ЭУЗИ)
4. Патологические результаты при манометрии СФО (мало применимо в рутинной клинической практике)
(Альтернативные тесты: измерение панкреатического протока при мульти спиральной компьютерной томографии (МСКТ) или ЭУЗИ до и после в/в секретина - может подтверждать наличие дисфункции СФО панкреатического типа)
Билиарная боль.
Боль билиарного типа является одним из основных критериев функциональных расстройств ЖП и СФО билиарного типа. Экспертами Римских консенсусов сформулированы основные признаки билиарной боли, для которой характерно: приступы болей в эпигастрии и/или в правом верхнем квадранте живота в сочетании со всеми нижеследующими признаками:
- длительность болей 30 мин и более; постоянный уровень болей во время приступа;
- рецидивирование симптомов с различными интервалами (не обязательно ежедневно)
- боли умеренные или сильные, достаточно интенсивные, способные нарушить повседневную активность или приводить в отделение неотложной помощи;
- боли не уменьшаются после стула*
- боли не уменьшаются после приема антацидов или подавления кислоты* (* у 20% пациентов билиарная боль может уменьшаться)
Подтверждающие критерии билиарной боли:
Боли могут сочетаться с одним или более из нижеследующих симптомов:
- тошнота или рвота,
- иррадиация в спину и/или правую подлопаточную область,
- возникновение в ночные часы
При функциональном расстройстве СФО панкреатического типа отмечаются боли, характерные для панкреатита - локализуются в эпигастральной области с иррадиацией в спину и/или левое подреберье.
Роль дуоденальной гипертензии в формировании болевого и диспепсических расстройств при функциональных нарушениях билиарной системы.
Одной из составляющих болевого синдрома и причиной диспепсических симптомов при функциональных расстройствах билиарного тракта является формирование дуоденальной гипертензии. Причиной дуоденальной гипертензии является недостаточное поступление желчи для процесса пищеварения (билиарная недостаточность), приводящая к микробной контаминации ДПК и синдрому избыточного бактериального роста (СИБР) в тонкой кишке. Нарушение сократительной и концентрационной функции ЖП и/ или функциональное расстройство СФО сопровождаются нерегулярным и недостаточным поступлением желчи в кишечник для процессов пищеварения. Нарушается в первую очередь переваривание и всасывание жира и других веществ липидной природы, уменьшается бактерицидность дуоденального содержимого (дефицит ЖК), что приводит к микробному обсеменению (контаминации) ДПК, избыточному бактериальному росту в тонкой кишке, нарушению состава и функционирования толстокишечных бактерий - дисбиозу. СИБР в тонкой кишке характеризуется увеличением в ней количества нормальной, или появлением патологической микрофлоры, чаще фекальной. Под влиянием бактерий ДПК и проксимальных отделов тонкой кишки ЖК подвергаются преждевременной деконъюгации и исключаются из процессов пищеварения.Токсичные деконьюгированные ЖК, бактерии и эндотоксины бактерий могут повреждать слизистую оболочку ДПК, тонкой и толстой кишки с развитием дуоденита, энтерита и колита. Деконьюгированные ЖК активируют аденилатциклазу энтероцитов, что сопровождается развитием секреторной (холагенной) диареи, главным признаком которой является ее персистенция даже после 24 часового голодания. Бактерии, участвуют в ферментации нутриентов, приводя к формированию высокоосмолярного содержимого, с задержкой жидкости и образованием большого количества газа в просвете кишки. Эти процессы сопровождаются увеличением объема дуоденального содержимого, усугубляя проявления дуоденальной гипертензии.
О наличии дуоденальной гипертензии у пациентов с функциональными билиарными расстройствами могут свидетельствовать следующие симптомы:
- горечь во рту;
- чувство быстрого насыщения;
- тяжесть и боли в эпигастрии, усиливающиеся после еды часто становятся опоясывающими;
- обильные воздушные отрыжки или срыгивания горького содержимого;
- тошнота, реже - рвота желчью.
При пальпации могут определяться болезненность и урчание в проекции ДПК
Дуоденальная гипертензия сопровождается ретроградной перистальтикой с развитием дуодено-гастро-пищеводно-оральных рефлюксов. Последствиями рефлюкса желчи в желудок является формирование рефлюкс-гастрита, в пищевод - щелочного рефлюкс-эзофагита, и в ротовую полость - поражения слизистых ротовой полости, языка.
Высокое давление в ДПК рефлекторно повышает тонус СФО, что приводит к развитию или прогрессированию функциональных расстройств в билиарной системе и способствует функциональному расстройству панкреатического сфинктера, которое может являться этиологическим фактором развития острого и рецидива хронического панкреатита, и участвовать в механизмах формирования абдоминального болевого синдрома и относительной внешнесекреторной недостаточности поджелудочной железы. При СИБР могут разрушаться и инактивироваться панкреатические ферменты, усугубляющие абсолютную и/или относительную внешнесекреторную недостаточность поджелудочной железы.
Нарушаются процессы полостного гидролиза и всасывания в тонкой кишке в результате:
- асинхронизма между поступлением в ее просвет пищи и пищеварительных ферментов;
- относительной ферментной недостаточности поджелудочной железы и тонкой кишки;
- преждевременной деконюгации ЖК.
Токсины и продукты бактерий могут самостоятельно влиять на ускорение транзита по кишке. Диарея у больных при развитии СИБР в тонкой кишке имеет сложный генез: сочетаются секреторный, осмотический и в ряде случаев - гиперкинетический тип ее формирования. Нередко эти клинические проявления расцениваются в качестве синдрома раздраженного кишечника с диареей.
Поскольку слизистая оболочка ДПК лишена мощного защитного барьера и отличается высокой проницаемостью, при наличии микробной контаминации происходит транслокация кишечных бактерий за пределы кишечной стенки, что может приводить к формированию неспецифического мезаденита с лимфостазом и наличием лимфангиэктазий (симптом манной крупы), холецистита, папиллита.
Эндотоксины бактерий, поступая по портальной системе в печень нарушая работу купферовских клеток, мононуклеарных макрофагов и запуская продукцию провоспалительных цитокинов, способствуют формированию и прогрессированию стеатогепатита на фоне имеющегося стеатоза печени или реактивного гепатита.
При транслокации бактерий за пределы кишечной стенки могут наблюдаться и внекишечные проявления, включая интоксикационный синдром (утомляемость, головная боль иногда по типу мигрени, депрессия и др.), псевдоаллергические реакции, суставной синдром, кожные проявления, микробная контаминация мочевых путей и др.
Диагностические тесты при заболеваниях билиарного тракта
Экспертами, участвующими в создании Римских критериев, подчеркивается, что клиническая картина функциональных расстройств билиарной системы не позволяет исключить наличия органической патологии (желчнокаменной болезни или хронического панкреатита). Для исключения органической патологии, установления и подтверждения типа функциональных расстройств используется ряд скрининговых и уточняющих методов исследования билиарной системы и поджелудочной железы.
Скриннинговые методы:
- функциональные пробы печени, панкреатические ферменты в крови и моче;
-трансабдоминальное ультразвуковое исследование (УЗИ);
- эзофагогастродуоденоскопия (ЭГДС) с осмотром БДС (дуоденоскопия является обязательным тестом при заболеваниях билиарного тракта)
Уточняющие методы:
- УЗИ с оценкой функционального состояния желчного пузыря и/или СФО
- эндоскопическое ультразвуковое исследование(ЭУЗИ)
- динамическая гепатобилиосцинтиграфия (ГБСЦ)
- магнитно резонансная холангио-панкреаторграфия (МРХПГ)
- мультиспиральная компьютерная томография (МСКТ)
- эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ)
- эндоскопическая манометрия СФО
Исследования печеночных ферментов (АЛТ, АСТ, ГГТП, щелочной фосфатазы, общего и прямого билирубина) панкреатических ферментов (амилазы, липазы в крови, диастазы в моче) необходимо проводить во время или не позднее 6 часов после окончания болевого приступа, а также в динамике. Транзиторное повышение в 2 и более раз уровня печеночных или панкреатических ферментов не менее чем во время двух последовательных приступах болей является важным фактором в диагностике функционального расстройства СФО. Повышение уровня печеночных ферментов при наличии расширения холедоха требует более тщательного обследования для исключения органического поражения билиарного тракта.
Трансабдоминальное УЗИ включает исследование печени, желчевыделительной системы и поджелудочной железы. Площадь ЖП в норме составляет 15-18см2, длина ЖП 6-7 см., ширина в теле ЖП - 3 см, толщина стенки ЖП не более 3 мм, содержимое ЖП однородное. Важное значение придается расширению холедоха и главного панкреатического протока, которое свидетельствует о нарушении тока желчи и панкреатического секрета на уровне СФО. Верхняя граница нормы диаметра общего желчного протока составляет 6 мм, после удаления ЖП диаметр его не должен превышать 10мм. Расширение холедоха в сочетании с повышением уровня печеночных ферментов (особенно ЩФ и ГГТП) или панкреатического протока на фоне повышения амилазы или липазы требует тщательного обследования для исключения органической патологии. Поджелудочная железа в норме имеет ровные контуры, структура однородная, размеры головки, тела и хвоста не увеличены, диаметр главного панкреатического протока составляет в головке - 2,8 - 3,3 мм, в теле -2,4 - 2,6 мм, хвосте - 1,0 - 1,7 мм.
ЭГДС также относится к скрининговым методам обследования пациентов с патологией билиарной системы. Целью эндоскопического исследования является не только выявление эрозивно-язвенных поражений верхних отделов ЖКТ. Важен осмотр Фатерова соска для исключения папиллита, стеноза, парафатерального дивертикула. Обнаружение лимфангиэктазий в ДПК (симптом «манной крупы»), дистального дуоденита, косвенно указывают на наличии микробной контаминации ДПК с транслокацией бактерий за пределы кишечной стенки. При проведении эндоскопического исследования желудка и ДПК также можно обнаружить косвенные признаки дуоденальной гипертензии: наличие антрального рефлюкс-гастрита, в том числе и эрозивного на фоне дуоденогастрального рефлюкса; скопление желчи в нижней горизонтальной ветви.
Для исключения органических изменений в желчевыделительных путях могут потребоваться уточняющие методы исследования: ЭУЗИ, МРХПГ и ЭРХПГ. В настоящее время предпочтение отдается МРХПГ как достоверному и менее инвазивному методу исследования желчевыводящих путей в распознавании причин нарушения оттока желчи и секрета поджелудочной железы. МРХПГ позволяет оценить протоки билиарной системы без прямого введения в них контрастного средства: измерить их диаметр, выявить дефекты наполнения (камни), наличие стенозов и стриктур, оценить культю пузырного протока.
ЭУЗИ является высокоэффективным, перспективным методом для оценки зоны СФО и поджелудочной железы. Метод является инвазивным, требует анестезиологического сопровождения, проводится в крупных диагностических центрах и пока еще не так широко внедрен в повседневную практику.
ГБСГ с радиофармацевтическим препаратом на основе иминодиацетовой кислоты, меченой 99mTc-Тс-HIDA (гепато-НIDA,DISHIDA,меброфенин),имеет важные преимущества в оценке анатомического и функционального состояния билиарной системы. Метод позволяет получить сцинтиграфическую картину высокой разрешающей способности и визуализировать не только ЖП, но и желчные протоки. Новый метод радионуклидной диагностики - гепатобилигастросцинтиграфия (ГБГСГ) с технецием-99м-броммезидой позволяет проводить одновременное изучение поглотительно-выделительной функции гепатоцитов, концентрационной, сократительной функции ЖП, желчных протоков, моторно-эвакуаторной функции желудка и дуоденогастрального рефлюкса. Следует отметить, что исследовать ЖП и желчные протоки при ГБСГ возможно только при нормальной функции печени и отсутствии обструкции желчных путей.
ЭРХПГ в качестве диагностической процедуры используется только по специальным показаниям и чаще в настоящее время применяется как лечебное эндоскопическое пособие (экстракция и литотрисия конкрементов при холедохолитиазе, папиллотомия, установка стентов).
В качестве дополнительных методов следует указать рентгенологическое исследование ДПК для выявления дуоденостаза. В норме скорость транзита контрастной массы по ДПК составляет 10 - 12 сек. Признаками функционального дуоденостаза является: задержка контраста в ДПК свыше 30 секунд, усиление перистальтики в сочетании с антиперистальтическими волнами указывает на компенсированный дуоденостаз. Снижение перистальтической активности, эктазия кишки, скопление бария в нижней горизонтальной ветви ДПК являются признаками субкомпенсированного или декомпенсированного дуоденостаза (чаще указывает на органическую патологию ДПК).
Наличие дуоденостаза может быть выявлено также при УЗИ ДПК. Признаками дуоденостаза являются: увеличение диаметра ДПК натощак и после приема жидкости >2 см и замедление эвакуации жидкости из ДПК свыше 40 секунд.
Для подтверждения наличия СИБР тонкой кишки целесообразно проведение водородного дыхательного теста с нагрузкой глюкозой или лактулозой.
Исследование функционального состояния ЖП и СФО
Для оценки функционального состояния и типа моторных нарушений ЖП используется трансабдоминальное УЗИ до и после его сокращения. Сократительную функцию ЖП считают нормальной, если после приема пробного завтрака объем ЖП через 30-40 минут уменьшается на 1/2 от первоначального, а показатель коэффициента опорожнения находится в пределах 50-75%. Если коэффициент опорожнения составляет менее 50%, сократительную функцию ЖП следует считать сниженной (гипокинетическая дискинезия), а при коэффициенте опорожнения более 75% - повышенной (гиперкинетическая дискинезия).
Для стимуляции сокращения ЖП могут использоваться различные вещества. Внутривенное введение ХЦК в дозе 20 мг/кг массы тела является золотым стандартом для оценки функционального состояния ЖП. Однако, этот тест не используется в клинической практике из-за недоступности препарата. Широко распространены так называемые желчегонные завтраки, которые благодаря стимуляции выработки эндогенного холецистокинина вызывают сокращение ЖП: 20 г сорбита в 100 мл воды, 200 мл 10% сливок, или жирной сметаны, 50 мл растительного масла, 2 вареных желтка, банан, жирный йогурт. Предпочтение чаще отдают раствору сорбита, который является наиболее физиологичным. Исследование проводится в 2-3 этапа (по усмотрению врача): до и через 30 минут и 60 минут после желчегонного завтрака. Наиболее часто используется двухэтапный вариант: до и через 45 минут после стимуляции ЖП.
Для оценки функционального состояния СФО используется УЗИ диаметра общего желчного протока до и после приема желчегонного «завтрака». После пищевой нагрузки, включающей 20г сливочного масла, сыр, сладкий чай (6,5г сахара), белый хлеб, измерение диаметра холедоха проводится каждые 15 минут в течение 1 часа. Увеличение его диметра на 1 мм и более по сравнению с исходным, позволяет предположить наличие препятствия оттоку желчи в результате, как функционального расстройства СФО, так и органического генеза. Уменьшение диаметра общего желчного протока свидетельствует о нормальном функционировании СФО. Можно предположить невысокую чувствительность этого теста, поскольку при относительно небольшом диаметре холедоха незначительные колебания его диаметра в процессе исследования выявить трудно.
Наиболее точным методом, подтверждающим функциональные расстройства СФО, является эндоскопическая манометрия СФО. Данный метод успешно дополняет традиционную эндоскопию и включает прямое измерение давления СФО с помощью специального трехпросветного, или однопросветного тефлонового катетера, вводимого через дуоденоскоп в общий желчный или панкреатический проток. Проксимальный конец катетера соединен с наружным преобразователем и пишущим устройством, возможно использование водяного манометра. Манометрические показатели функционального состояния СФО отражают его тонус (базальное давление) и двигательную активность (амплитуду, частоту, продолжительность сокращения и направление распространения перистальтических волн). Данный метод позволяет оценивать функциональное состояние непосредственно СФО, а также точно определять длину зоны сфинктера, исследовать раздельно с шагом в 4 мм давление на дистальном, среднем и проксимальном участке СФО, дифференцировать стеноз и дисфункцию СФО. Следует учитывать, что проведение указанной манипуляции возможно только при отсутствии камней в общем желчном протоке. У здоровых людей базальное давление СФО колеблется на уровне 100-150 мм вод. ст. У больных с дисфункцией СФО базальное давление колеблется от 180 до 300 мм вод. ст. и выше. Для дифференциальной диагностики функционального спазма СФО от его органического поражения рекомендуется проведение во время исследования нитроглицериновой пробы (две таблетки нитроглицерина под язык). У пациентов с функциональной патологией после приема нитроглицерина спазм СФО купируется и давление нормализуется. Метод прост в выполнении, не сопровождается такими грозными осложнениями как при проведении ЭРХПГ. В настоящее время считается основным методом для оценки функционального расстройства СФО и дифференциальной диагностике функциональной патологии от органических нарушений.
Принципы лечения функциональных расстройств ЖП и СФО.
Диета
Общими принципами диеты являются:
- Режим питания с частыми приемами небольших количеств пищи (5-6 разовое питание), что способствует нормализации давления в ДПК и регулярному опорожнению ЖП и протоковой системы;
- Из рациона исключаются алкогольные напитки, газированная вода, копченые, жирные и жареные блюда и приправы в связи с тем, что они могут провоцировать спазм сфинктера СФО;
- Овощи, фрукты, травы предпочтительнее использовать термически обработанными (отварные, запеченные);
Принципы медикаментозной терапии включают:
- Купирование болевого синдрома, обусловленного повышением тонуса СФО, моторной активности ЖП и ДПК - показание для назначения спазмолитиков
- Разрешение симптомов дуоденальной гипертензии - показание для назначения спазмолитиков или прокинетиков, или нормокинетиков и антибиотиков для деконтаминации ДПК.
- Нормализация процессов переваривания и всасывания - показание для назначения препаратов УДХК и панкреатических ферментов без желчных кислот.
Купирование болевого синдрома
Для купирования болевого синдрома, обусловленного повышением тонуса СФО, ЖП и ДПК используют релаксанты гладкой мускулатуры, которые включают в себя несколько групп препаратов.
Нитраты (нитроглицерин, нитросорбит). Механизм действия нитратов сводится к образованию в гладких мышцах свободных радикалов оксида азота (NO), которые активируют гуанилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Однако выраженные кардиоваскулярные эффекты, побочные действия и развитие толерантности делают применение нитратов малоприемлемыми для длительной терапии функционального расстройства СФО. Используется нитроглицерин в режиме по требованию.
Антихолинергические средства блокируют мускариновые рецепторы на постсинаптических мембранах органов-мишеней, в результате чего происходит блокада кальциевых каналов и прекращается проникновение ионов кальция в цитоплазму гладкомышечных клеток и как следствие - снятие мышечного спазма. В качестве спазмолитиков используются как неселективные М-холиноблокаторы (препараты красавки, метацин, платифиллин и др.), так и селективные (гиосцина бутилбромид). Однако при приеме неселективных препаратов данной группы может наблюдаться достаточно широкий спектр побочных эффектов: сухость во рту, задержка мочеиспускания, нарушения зрения, повышение внутриглазного давления, тахикардия, запоры, сонливость. Сочетание довольно низкой эффективности с широким спектром побочных действий неселективных препаратов ограничивает их применение для курсового лечения. Неселективные миотропные спазмолитики (платифиллин) вводятся парентерально при выраженном болевом синдроме по требованию или коротким курсом. Гиосцина бутилбромид в таблетках и свечах используется в курсовом режиме и по требованию.
Блокаторы медленных кальциевых каналов.
К неселективным препаратам этой группы относятся фенилалкиламины (веропамил, галлопамил),1-4 дегидроперидины (нифедипин, амлодипин) и бензотиа-зепины (дилтиазем). Препараты этой группы закрывают кальциевые («медленные») каналы клеточных мембран, препятствуют входу ионов кальция в цитоплазму клеток гладкой мускулатуры и вызывают ее релаксацию. Препараты обладают многочисленными кардиоваскулярными эффектами, в первую очередь вазодилятирующими и в связи с этим используются только для лечения патологии сердечно-сосудистой системы. Имеются лишь единичные сообщения об использовании нифедипина при функциональном расстройстве СФО.
К группе неселективных миотропных спазмолитиков, механизм действия, которых заключается в ингибировании фосфодиэстеразы, или в активации аденилатциклазы, или в блокаде аденозиновых рецепторов, что приводит к снижению тонуса и двигательной активности гладкой мускулатуры, относятся: дротаверин, бенциклан (галидор); альверина цитрат и др. Основные их недостатки - существенные различия в эффективности терапии при билиарных расстройствах, отсутствие селективного воздействия на билиарный тракт, наличие нежелательных эффектов, обусловленных воздействием на гладкомышечные клетки сосудов, мочевыделительной системы и других отделов пищеварительного тракта; наличие побочных эффектов. Препараты дротаверина, папаверина (парентеральная форма и таблетки) назначаются короткими курсами или в режиме по требованию.
Более современный селективный миотропный спазмолитик Мебеверин - блокатор ионных каналов, избирательно действует на гладкие мышцы желудочнокишечного тракта. Экспериментальные исследования показали, что препарат обладает двумя эффектами. Первый из них сводится к блокаде быстрых натриевых каналов клеточной мембраны миоцита, что нарушает процессы поступление натрия в клетку, замедляет процессы деполяризации и прекращает вход кальция в клетку через медленные каналы. В результате снижаются процессы фосфорилирования миозина, и быстро снимается спазм мышечного волокна (антиспастический эффект). Второй эффект обусловлен снижением пополнения внутриклеточных кальциевых депо, что приводит лишь к кратковременному выходу ионов калия из клетки и ее гиперполяризации, предупреждающей развитие гипотонии мышечного волокна после купирования спазма. Этот эффект Мебеверина выгодно отличает его от действия других миотропных спазмолитиков, вызывающих длительную гипотонию. Мебеверин практически не всасывается и является селективным спазмолитиком, оказывающим выраженное спазмолитическое действие на кишку и СФО. Оказывая спазмолитический эффект на СФО препарат вторично улучшает опорожнение ЖП, устраняет симптомы функциональной дуоденальной гипертензии. Экспериментально установлено, что спазмолитический эффект мебеверина на СФО примерно в 40 раз превышает таковой при применении папаверина. Мебеверин в капсулах (200мг) используется в режиме по требованию и для курсового лечения.
Гимекромон (7-гидрокси-4-метил кумарин) - препарат химического синтеза, относится к группе «Желчегонные средства и препараты желчи». Оказывает селективное спазмолитическое действие в отношении желчных протоков и сфинктера Одди; улучшает отток желчи в ДПК, снижает давление во внутри- и внепеченочной билиарной системе; оказывает опосредованный желчегонный эффект. Препарат не влияет на гладкую мускулатуру кишечника; не оказывает влияния на секрецию пищеварительных желез и процессы всасывания. Усиливает эффекты непрямых антикоагулянтов. Таблетки 200 мг используются курсами 2 недели или в режиме по требованию.
На выбор спазмолитика и способ его введения оказывает влияние выраженность болевого синдрома. При наличии выраженного болевого синдрома используются препараты для парентерального введения М - холиноблокаторы (платифиллин 2-4 мг в/м) или миотропные спазмолитики дротаверин (но-шпа 2% раствор 2.0 - 4.0 мл в/м) с последующим переходом на селективные спазмолитики мебеверин - для курсового лечения. Дополнительно к спазмолитикам для купирования интенсивных болей (билиарная колика) могут вводиться анальгетики: метамизила натрия (баралгин, спазган) 5.0 в/м, реже в/в, или нестероидные противовоспалительные средства (диклофенак 50-75 мг в/м; кетопрофен 200 мг в/м; индометацин 50 мг в/м). При умеренном болевом синдроме применяются селективные спазмолитики.
Российская гастроэнтерологическая ассоциация и эксперты Римских критериев IV для купирования билиарных болей рекомендуют использовать следующие препараты:
- Гиосцина бутил бромид 10-20 мг внутрь, или в свечах 10-20 мг 3 раза в день, курс 10-30 дней,
- Мебеверина гидрохлорид 135 мг 3 раза в день, или 200 мг 2 раза в день за 20 мин до еды внутрь, курсом 10-30 дней
- Гимекромон 200-400 мг внутрь по требованию и 200-400мг х 3 раза в день внутрь за 30 мин до еды, курс 14 дней
- Тримебутин 200 мг 3 раза в день внутрь в течение 30 дней
- Нитроглицерин 1-2 таблетки под язык по требованию.
Одним из наиболее изученных и длительно используемых спазмолитических препаратов для купирования боли и лечения функциональных билиарных расстройств является мебеверин. В настоящее время в России в распоряжении врачей имеется лекарственное средство на основе мебеверина - Спарекс®. Капсулы Спарекс® пролонгированного действия содержат полимерную матрицу, в которой равномерно распределено лекарственное вещество. После приема капсулы на поверхности матрицы образуется гелевый слой, который регулирует высвобождение мебеверина с заданной скоростью за счет матричного высвобождения лекарственного средства. Спазмолитический эффект наступает через 15 минут и сохраняется на протяжении 12 часов. Спарекс® нормализует моторику двенадцатиперстной кишки, толстого кишечника - обладает эукинетическим действием, купирует спазм СФО и опосредовано улучшает опорожнение желчных путей. При этом гипотония гладкой мускулатуры не развивается даже при длительном приеме препарата. Спарекс® отличается хорошей переносимостью, отсутствием системных побочных эффектов, удобным способом приема - по 1 капсуле (200 мг) 2 раза в день, утром и вечером, до еды. В отличие от аналогов Спарекс® резрешен детям с 12 лет. Продолжительность курсового лечения 4-8 недель.
У значительной части больных с функциональными расстройствами ЖП по гипокинетическому типу нарушение опорожнения ЖП в большинстве случаев носит вторичный характер и обусловлено гипертонусом СФО. Таким пациентам назначение селективных спазмолитиков, в том числе Спарекс®, является также оправданным. Для нормализации функционального состояния ЖП при гипомоторной дискинезии после купирования болевого синдрома назначают холекинетики, стимулирующие выделение эндогенного холецистокинина, под влиянием которого происходит сокращение ЖП, открытие СФО и желчь поступает в кишку. Часто используемыми препаратам этой группы являются: сульфат магния, многоатомные спирты (ксилит, сорбит), масла (тыквеол), ряд лекарственных растений (бессмертник, мята перечная, пижма, дымянка, артишок и др.) и препаратов на их основе (фламин, танацехол, берберин, хофитол). Также к этой группе относятся желчегонные препараты, которые в своем составе содержат желчь (аллохол, холензим, фестал и др.). Применение препаратов, содержащих желчь, ограничено из-за токсического действия на гепатоциты и слизистые оболочки ЖКТ, их назначение противопоказанно при гепатитах и циррозах печени, язвенной болезни и эрозиях слизистой оболочки ЖКТ, панкреатитах и поносах, не связанных со стеатореей. Исключение составляет урсодезоксихолевая кислота, которая обладает гепатопротективным, иммуномодулирующим, гипохолестеринемическим, холеретическим и холекинетическим эффектом, и является единственным препаратом в терапии внутрипеченочного холестаза. Механизм действия УДХК при функциональных нарушениях билиарного тракта связан с угнетением синтеза ХС в печени, уменьшением ее секреции в желчь, снижением всасывания в кишечнике и повышением растворимости в пузырной желчи. Кроме того, УДХК участвует в процессах пищеварения, не подвергается микробной деконъюгации, не оказывает токсического влияния на кишечный эпителий и гепатоциты, усиливает бактерицидный эффект желчи, стимулирует моторную функцию ЖП. В 2015 г. на фармацевтический рынок РФ был выведен лекарственный препарат УДХК в дозе 500 мг - Эксхол®. Эксхол 500 мг (делимые таблетки, покрытые пленочной оболочкой), и Эксхол 250 мг (капсулы) производятся из субстанции, соответствующей Европейской фармакопее последнего 8-го выпуска.
Для нормализации гипомоторных нарушений ДПК и купирования симптомов, вызванных функциональной дуоденальной гипертензией могут быть назначены прокинетики: агонисты парасимпатических и дофаминовых рецепторов, агонисты 5HT4- и антагонисты 5HT3- серотониновых рецепторов. К препаратам, разрешенным для использования в России в настоящее время, относятся метоклопрамид, домперидон, итоприда гидрохлорид. Основными физиологическими эффектами перечисленных прокинетиков являются повышение тонуса нижнего пищеводного сфинктера, повышение эвакуаторной функции желудка, повышение антродуоденальной координации, повышение пропульсивной перистальтики ДПК. Кроме того, при применении прокинетиков восстанавливается координация взаимоотношений «желудок - ДПК », выравнивается градиент давления «ДПК - желудок» и «ДПК - желчные протоки», что способствует также и улучшению оттока желчи. Наиболее эффективным и безопасным препаратом из группы прокинетиков является итоприда гидрохлорид, который назначается по 50 мг за 30 минут до еды 3 раза в сутки в течение 4 недель и более. Препараты метоклопрамид и домперидон рекомендованы в настоящее время только в качестве симптоматической терапии тошноты и рвоты и ограничены для применения в курсовом лечении до 7 дней в дозе 10 мг 3 раза в день в связи с наличием побочных эффектов (развитие желудочковых аритмий и внезапной смерти).
Нифуроксазид высоко активен в отношении Campylobacter jejuni, Escherichia coli, Salmonella spp, Shigella spp; Clostridium perfringens, Vibriocholerae, патогенных Vibrions и Vibrioparahaemolytique, Staphylococcus spp. Резистентны к нифуроксазиду: Klebsiella spp., Proteus mirabilis, Providencia spp., Pseudomonas spp.
Деконтаминация ДПК
Важным компонентом разрешения дуоденальной гипертензии, сопровождающей функциональные билиарные расстройства, является деконтаминация ДПК и подавление СИБР в тонкой кишке. С этой целью проводится антибактериальная терапия. Основные антибактериальные препараты, используемые в терапии кишечного дисбактериоза представлены в таблице 5.
Таблица 5.
Антибактериальные препараты, используемые в терапии кишечного дисбактериоза
| Невсасывающиеся препараты | Всасывающиеся препараты | ||
| Нифуроксазид | 200 мг 4 раза в день | Фуразолидон | 0,1 г 3 р/день |
| Интетрикс | 1 капс 4 р/день или 2 капс 2 раза в день | Нифурател | 400 мг 2 р/ день |
| Неомицин | 500 мг 2 р/день | Ципрофлоксацин | 500 мг 2 р/день |
| Рифаксимин | 200 мг 4 р / д или 400 мг 2 раза в день | Метронидазол | 250 мг 3-4 р/день или 500 мг 2 р/день |
| Налидиксовая кислота | 0,5 г 3 р/день | ||
| Доксициклин | 0,1- 0,2 г / день | ||
| Амоксициллин с клавулоновой кислотой | 875 мг 2 р/день | ||
Следует отдельно остановиться на невсасывающемся препарате нифуроксазида Адисорд®. Как и другие нитрофураны, нифуроксазид блокирует активность дегидрогеназ и угнетает дыхательные цепи, цикл трикарбоновых кислот и ряд других биохимических процессов в клетках микроорганизмов. При применении в терапевтических дозах оказывает бактериостатическое действие, в высоких дозах — бактерицидное.
При инфицировании энтеротропными вирусами препятствует развитию бактериальной суперинфекции. Важно отметить, что в терапевтических дозах препарат практически не нарушает равновесие симбиотической бактериальной флоры кишечника; и не вызывает развития резистентности бактериальных штаммов. После перорального приема нифуроксазид практически не абсорбируется из ЖКТ. Продолжительность курсовой терапии 7-10 дней. При невозможности ликвидации этиологического фактора лечение проводится при появлении симптомов со сменой препаратов в очередном курсе. Частота проведения курсов антибактериальной терапии может колебаться от ежемесячного до 4 и более раз в год.
Одновременно или после окончания антибактериальной терапии целесообразно использовать метабиотики (бактистатин, хилак форте и др), содержащие продукты метаболизма или структурные компоненты пробиотических микроорганизмов, обладающие антибактериальной, ферментной и иммунологической активностью.
Что касается пробиотиков и пребиотиков, то назначение их при толстокишечном дисбиозе является, несомненно, обоснованным, в тоже время при СИБР - спорным. Вероятнее всего любое увеличение бактериальной нагрузки в тонкой кишке является нежелательным у пациентов с наличием факторов риска развития, не говоря о больных с уже имеющимся СИБР. Проведенные исследования эффективности терапии пробиотиками при СИРБ не выявили положительных как ближайших, так и отдаленных результатов.
Нормализация процессов пищеварения.
Для нормализации процессов пищеварения в режиме «по требованию» используются препараты панкреатических ферментов без желчных кислот, предпочтительнее в виде микросфер или микротаблеток (Креон, Эрмиталь, Микрозим и др) по 10 000 Ед во время основных приемов пищи.
Урсодезоксихолевая кислота (Эксхол®) используется при гипокинетической дискинезий ЖП в качестве желчегонного и холекинетического препарата и при наличии признаков билиарной недостаточности после удаления ЖП -для заместительной терапии из расчета 5-7 мг /кг массы тела, разделенные на 2-3 приема во время еды. Курс терапии продолжается 1-2 мес. Для растворения билиарного сладжа у пациентов с гипокинетической дискинезией ЖП препараты УДХК назначаются из расчета 10 мг/кг массы тела, вечером перед сном, в течение 1-3 месяцев, с ежемесячным контролем УЗИ .
Схема назначения препарата Эксхол® 500 мг (УДХК) при заболеваниях печени*.
Дозы и сроки лечения:
| 1. Для растворения холестериновых желчных камней | Суточная доза лечения: Эксхол® 500 мг 10 мг/кг Курс лечения: 6-12 месяцев. Профилактика несколько месяцев. |
| 2. При билиарном рефлюкс-гастрите | Суточная доза лечения: Эксхол® 500 мг 250 мг 1 раз в день Курс лечения: от 10-14 дней до 6 месяцев, при необходимости до 2 лет |
| 3. Терапия первичного билиарного цирроза | Суточная доза лечения: Эксхол® 500 мг 10-15 мг/кг Курс лечения: 6-12 месяцев и более |
| 4. При хронических гепатитах различного генеза | Суточная доза лечения: Эксхол® 500 мг 10-15 мг/кг в 2-3 приема в сутки Курс лечения: 6-12 месяцев и более |
| 5. При неалкогольном стеатогепатите, алкогольной болезни печени | Суточная доза лечения: Эксхол® 500 мг 10-15 мг/кг в 2-3 приема в сутки Курс лечения: 6-12 месяцев и более |
| б. При кистозном фиброзе (муковисцидозе) | Суточная доза лечения: Эксхол® 500 мг 12-15 мг/кг при необходимости 20-30 мг/кг Курс лечения: 6-12 месяцев и более |
| 7. При дискинезии желчевыводящих путей | Суточная доза лечения: Эксхол® 500 мг 10 мг/кг в 2 приема Курс лечения: от 2 недель до 2 месяцев |
| 8. При первичном склерозирующем холангите | Суточная доза лечения: Эксхол® 500 мг 12-15 мг/кг при необходимости 20-30 мг/кг Курс лечения: 6-12 месяцев и более |
Диагноз:
Функциональное расстройство желчного пузыря по гипокинетическому типу.
Лечение:
- Диета
- Спарекс® 200 мг 2 раза в сутки, до еды. Курс 4 недели.
- Эксхол® 500 мг 7 мг/кг/сут., доза разделяется на 2-3 приема, во время еды. Курс 2-4 недели
Диагноз:
Хронический холецистит в стадии ремиссии. Гипокинетическая дискинезия желчного пузыря. Хронический постбульбарный дуоденит с множественными лимфангиэктазиями, ассоциированный с избыточным бактериальным ростом в тонкой кишке.
Лечение:
- Диета
- Эксхол 500 мг 7 мг/кг/сут, доза, разделенная на 2-3 приема, во время еды; в течение 2-4 недель
- Спарекс 200 мг 2 раза в сутки, до еды. Курс 4-6 нед.
- Ципрофлоксацин 0,5 г 2 раза в день, или Доксициклин 100 мг 1 раз в день, или Фуразолидон 100 мг 3 раза в день, принимать один из препаратов в течение 7-10 дней.
- Бактистатин 1 капс. 2 раза в день 10 - 20 дней.
Диагноз:
Желчнокаменная болезнь: стадия билиарного сладжа. Функциональное расстройство СФО билиарного типа.
Лечение:
- Диета.
- Эксхол® 500 мг 10 мг/кг/сутки, вся доза принимается однократно вечером перед сном в течение (1-3 мес.). Если однократная доза равняется или превышает 750 мг она принимается вечером в 2 приема с интервалом в 1 час;
- Спарекс® 200 мг 2 раза в сутки, до еды. Курс 4-6 нед.
Контроль УЗИ желчного пузыря ежемесячно.
Диагноз:
Функциональное расстройство СФО по билиарному типу. Желчнокаменная болезнь (холецистэктомия в 2000году). Хронический постбульбарный дуоденит с множественными лимфангиэктазиями, ассоциированный с избыточным бактериальным ростом в тонкой кишке. Синдром раздраженного кишечника. Дисбактериоз толстой кишки с наличием условно-патогенной флоры
Лечение:
- Диета
- Спарекс 200 мг 2 раза в сутки, до еды. Курс 4-6 нед.
- Ципрофлоксацин 0,5 г 2 раза в день, или Доксициклин 100 мг 1 раз в день, принимать один из препаратов в течение 7 дней, далее Адисорд 200 мг 4 раза в день в течение 5 дней.
- Метабиотики курсом 10-14 дней
- Пробиолог по 1 капс. в течение14 дней (после окончания антибактериальной терапии)
- Ферментные препараты во время основных приемов пищи по требованию
