Двойное слепое, контролируемое исследование терапии умеренной и тяжелой шизофрении сертиндолом и рисперидоном
СтатьиЖ.-М. Азорин1, Н. Страб2, Н. Лофт2
1Франция, 2Дания
Введение
Атипичные антипсихотики в настоящее время являются препаратами первого выбора для лечения шизофрении, поскольку они имеют большую терапевтическую широту применения и переносятся лучше, чем традиционные нейролептики.
Производное фенилиндола сертиндол является неседативным антипсихотическим препаратом с высоким сродством к дофаминовым D2, серотониновым 5-HT2, и α1-адренергическим рецепторам (18). Он селективно связывается с дофаминовыми рецепторами преимущественно в лимбических, а не в стриарных структурах (18), что предполагает антипсихотическую активность с низким удельным весом экстрапирамидной симптоматики. Эффективность сертиндола в отношении как продуктивных, так и негативных расстройств была продемонстрирована несколькими крупными плацебо-контролируемыми исследованиями. Более того, частота экстрапирамидных расстройств была сопоставима с плацебо (19, 31. 33). При сравнении с галоперидолом, в равнозначных дозировках сертиндол оказался не менее эффективным в отношении облегчения продуктивной симптоматики и, при этом, вызывал гораздо меньше экстрапирамидных расстройств (14, 15, 19, 33). Он значительно уменьшал негативную симптоматику, по сравнению с плацебо, в то время как галоперидол не был эффективным (14, 19, 33). Долгосрочные исследования (12 месяцев) продемонстрировали, что как продуктивная, так и негативная симптоматика продолжала смягчаться на протяжении всего курса лечения, более того, сертиндол также положительно влиял на комплайенс и частоту обострений и регоспитализаций (10, 30). Во всех этих исследованиях сертиндол зарекомендовал себя как достаточно безопасный и хорошо переносимый препарат и не ассоциировался как с седацией, антихолинергическими и гистаминергическими побочными действиями, так и с увеличением массы тела. Также одно из наблюдений предполагает, что сертиндол улучшает когнитивные способности пациентов, однако это еще должно быть подтверждено клиническими испытаниями (14, 21).
Рисперидон является агонистом центральных D2-дофаминовых и 5-НТ2 рецепторов, а также потенцирует α1-адренергическую и H1-гисгаминовую антагонистическую активность. Исследования показали, что он, по крайней мере, так же эффективен в отношении острой и хронически протекающей шизофрении с продуктивной и/или негативной симптоматикой, как и классические нейролептики (7-9, 16, 17, 22, 28). Рисперидон демонстрирует большее сродство к нигростриарным дофаминергическим нейронам, чем сертиндол (1), и известен дозозависимой тенденцией к вызыванию экстрапирамидных побочных действий, но, тем не менее, он лучше переносится, чем традиционные нейролептики (12).
К настоящему времени эффективность и безопасность сертиндола сравнивалась напрямую только с галоперидолом. Хотя эффективность сертиндола по сравнению с другими атипичными антипсихотиками была проанализирована косвенно при помощи мета-анализа, прямых сравнений произведено не было. Целью настоящего исследования было сравнить эффективность и безопасность сертиндола в дозе 12-24 мг, назначавшейся однократно в сутки, с рисперидоном, назначавшимся дважды в сутки в дозе 4-10 мг у больных с шизофренией. Гибкая схема назначения была выбрана для того, чтобы позволить лечение пациентов оптимальными для них дозами, так как ответ на лечение зачастую зависит от индивидуальных особенностей пациента. Исследование было закончено досрочно, поскольку сертиндол был временно запрещен к применению на европейском рынке из-за сомнений в его безопасности в отношении возможных кардиотропных действий. Однако, после тщательного исследования всех фактических данных по безопасности сертиндола, запрет был снят в июне 2002 года.
Расширенный реферат статьи, опубликованной в Int. Clin. Psychopharmacol. - 2006. - Vol. 21. N 1. - P 49-56, предоставлен компанией Лундбек.
Методы
Пациенты. В исследование включались мужчины или женщины от 18 до 65 лет, страдающие параноидной, кататонической, недиффереицированной или дезорганизованной шизофренией по DSM-IV (2); они должны были насчитывать более 2-х баллов по, как минимум, 2-м из 4-х показателей шкалы PANSS (то есть концептуальная дезорганизация, галлюцинаторное поведение, подозрительность и необычное содержание мыслей), и сумма любых 2-х из этих 4-х параметров должна была быть большей или равной 8-ми; также они должны были быть по меньшей мере «умеренно больны» по Шкале общего клинического впечатления тяжести (CGI-S) (26); и они не должны были получать антипсихотического лечения, либо оно должно было быть эффективным на любом отрезке времени в течение 5-ти лет. Пациенты исключались из исследования, если по результатам скрининговой электрокардиографии интервал QT составлял ≥430 мс у мужчин и ≥450 мс у женщин. Пациенты могли быть исключены во время исследования, если интервал QT был ≥480 мс.
Дизайн. Данное двойное слепое, рандомизированное. мультицентровое исследование с параллельными группами и гибким дозированием состояло из двух последовательных этапов: 1) от 4-х до 7-ми дней плацебо-периода пациенты получали только плацебо и 2) 12 недель продолжался двойной слепой период, когда рандомизированные пациенты получали либо сертиндол, либо рисперидон. На протяжении титрации (дни 1-16) сертиндол назначался один раз и сутки; начальная доза 4 мг повышалась на 4 мг каждый четвертый день до 16 мг/сут, а рисперидон изначально назначался в дозе 1 мг дважды в сутки, и доза наращивалась на 2 мг ежедневно до 6 мг/сут; эти дозировки оставались до конца периода титрации неизменными. Для поддержания «слепого» метода, лечение этими препаратами проводилось двумя капсулами дважды в сутки независимо от дозы, для чего использовалось плацебо. После периода титрации (16-й день), схема могла становиться покой (12-24 мг/сут для сертиндола и 4-10 мг/сут для рисполепта), в зависимости от индивидуального ответа на лечение; лоза могла быть как увеличена при недостаточной эффективности, так и снижена при проблемах с переносимостью.
Допускалось использование лоразепама до 7,5 мг/ сут или оксазепама до 150 мг/сут при возбуждении и/или бессоннице, а также биперидена до 8 мг/сут для коррекции экстрапирамидной симптоматики. Если требовалось назначение диуретиков, было возможным использование калийсберегающих препаратов с целью сохранить калиевый баланс.
Оценка эффективности и безопасности. Оценка проводилась исследователями, которые перед началом испытаний участвовали в тренингах по стандартизированному применению шкал (PANSS).
Первичной эффективностью считалось изменение в сумме баллов по шкале PANSS от исходного уровня. Определяемые вторичные параметры эффективности складывались из: 1) данных позитивной и негативной подшкал PANSS; 2) пропорции пациентов, достигших 10%, 20%, 30%, 40%, 50% или более улучшения от исходного уровня по сумме баллов шкалы PANSS к концу исследования; 3) суммы баллов по подшкалам гяжести и улучшения Шкалы общего клинического впечатления CGI (CGI-S, CGI-I); 4) данных опросника Drug Attitude Inventory (DAI), выражающего субъективный ответ пациента на лечение (3, 4, 6); и 5) из данных шкалы Global Assessment of Functioning (GAF), оценивающей уровень психологического, социального функционирования и занятость. Шкала PANSS применялась в 1-й день (исходный уровень), 16-й, 28-й, 42-й, 56-й и 84-й дни. Общее клиническое впечатление оценивалось в те же дни, а также на 8-й и 21-й день; также шкала CGI-S применялась в период плацебо. Шкалы DAI и GAF применялись на исходном уровне и в конце исследования.
Безопасность оценивалась еженедельно. Сообщалось о побочных явлениях, жизненных показателях и массе тела. ЭКГ проводилась в период скрининга, на 16-й и 28-й дни, а также в конце исследования: интервал QT высчитывался при помощи коэффициента Баззета, и пациенты были разделены на группы: норма (мужчины <430 мсек; женщины <450 мсек), пограничные (мужчины 431-450 мсек; женщины 451-470 мсек), пролонгированные (мужчины >450 мсек, женщины >470 мсек). Кроме того, применялись следующие неврологические шкалы: Simpson-Angus Scale (SAS) (29) для оценки паркинсонических явлений, Barnes Akathisia Scale (BAS) (5) для оценки акатизии и Abnormal Involuntar) Movement Scale (AIMS) (27) для оценки дискинезии. Шкалы SAS и BAS применялись еженедельно, шкала AIMS - в начале и в конце исследования.
Статистический анализ. Количество пациентов в выборке основывалось на всех рандомизированных пациентах, получавших препараты (intention-to-treat ITT), в соответствии с целью исследования - оценка эффективности в двух терапевтических группах на основании улучшения суммы баллов шкалы PANSS на 6 единиц в течение 12-ти недель. Количественный подсчет выборки со значениями α=5% и 1-β=90% указывал на требуемое количество пациентов в группе равное 160 человек. Однако, набор в исследование был прекращен раньше по требованию французского агентства по контролю над лекарственными препаратами.
Тестирование гипотезы было двусторонним, статистически значимым при р≤0,05. Анализ эффективности базировался на всей рандомизированной популяции, получавшей лечение (по крайней мере, с одним промежуточным тестированием после исходного). За параметр первичной эффективности было принято изменение суммы баллов по шкале PANSS, обсчитываемое при помощи методики Last Observation Carried Forward (LOCF), позволяющей учитывать влияние недостающих данных; отдельно оценивались все завершенные случаи, Observed Cases (ОС). Безопасность и переносимость оценивалась с учетом всех пациентов, получавших лечение.
При анализе эффективности, за исключением шкалы CGI-I, использовалась модель ковариативности (ANCOVA), где терапевтическая группа выступала в качестве факторов, а исходные данные – в качестве коварианты. Также, в качестве вторичного анализа проводилось повторное сравнение двух групп по шкалам и подшкалам PANSS (с целью выявления разных моделей развития с течением времени). Для описания группы пациентов, сформировавших ответ на лечение (то есть улучшение по шкале PANSS ≥30% от исходного уровня), применялись показатели Каплана-Мейера (Kaplan-Meier survival estimates), а терапевтические группы сравнивались между собой при помощи логарифмического рангового критерия (log-rank test). Данные шкалы CGI-I обрабатывались при помощи теста Cochrane-Mantel-Haenszel.
Побочные действия кодировались при помощи словаря COSTART III (11). Момент исключения из-за побочных действий определялся при помощи модели Сох. Межгрупповое сопоставление пациентов с экстрапирамидными расстройствами как результат лечения приводилось при помощи точного критерия Фишера (Fisher's exact test); время начала проявления экстрапирамидных расстройств и их длительность обрабатывались при помощи показателей Каплана-Мейера и модели Сох. Исходные показатели двух групп оценивались при помощи тета-теста (t-test) или теста Вилкоксона (Wilcoxon rank sum test for continuous and ordered data), а также при помощи критерия хи-квадрат или точного критерия Фишера для качественных данных.
Результаты
Поскольку исследование было завершено преждевременно, только 263 пациента прошли скрининг и 187 из них были рандомизированы на лечение в 70 центрах во Франции. Один из рандомизированных пациентов не получал никакого из исследуемых препаратов и только 186 человек получали лечение сертиндолом (n=97) или рисперидоном (n=89); 172 паписта пыли включены в оцениваемую популяцию (сертиндол, n=90; рисперидон, n=82). Среднесуточная дозировка составила 16,6 мг для пациентов, получавших сертиндол, и 6,6 мг для пациентов, получавших рисперидон (55% которых получало рисперидон в дозе 4-6 мг/сут, а остальные - 8-10 мг/сут).
Из 186 рандомизированных пациентов, 120 (65%) полностью прошли через исследование (59 на сертиндоле и 61 на рисперидоне). Исключение из исследования в двух группах происходило по сходным причинам. Наиболее частыми были: побочное действие, несогласие (отказ от участия), недостаточная эффективность (табл. 1). Статистически значимых различий во времени наступления побочных действий в двух группах не наблюдалось.
Таблица 1
Выбывшие из исследования пациенты, получавшие лечение
| Причина исключения | Сертиндол (n=97) n (%) | Рисперидон (n=89) n (%) |
|---|---|---|
| Общее количество выбывших | 38 (39) | 28 (31) |
| Общее количество рандомизированной популяции | 90 (93) | 82 (92) |
| Побочные действия | 12 (12) | 9 (10) |
| Недостаточная эффективность | 8 (8) | 5 (6) |
| Некомплайентность | 2 (2) | 2 (2) |
| Нарушение протокола | 3 (3) | 3 (3) |
| Отзыв согласия | 8 (8) | 8 (9) |
| Не пришедшие на визиты | 1 (1) | 0 (0) |
| Административные причины | 0 (0) | 0 (0) |
| Другие причины | 4 (4) | 1 (1) |
Распределение по половому признаку оказалось неравным с меньшим количеством мужчин в группе сертиндола (56%) по сравнению с группой рисперидона (66%); эта разница не являлась статистически значимой. Все остальные характеристики в 2-х группах были сходными (табл. 2). Также не было обнаружено какой-либо статистической разницы в нозологических категориях.
Таблица 2
Исходные демографические и нозологические характеристики пациентов
| Характеристики | Группа сертиндола (n=97) | Группа рисперидона (n=89) |
|---|---|---|
| Пол, n (%) Мужской Женский | 54 (56) 43 (44) | 59 (66) 30 (34) |
| Возраст (средний в годах) Мужчины Женщины | 36,0±9,1 35,1±10,4 | 35,5±10,9 35,1±9,3 |
| Масса тела (средняя в кг) | 71,3±14,7 | 71,8±15,3 |
| Индекс массы тела (средний в кг/м²) | 24,9±4,5 | 24,5±4,8 |
| Раса, п (%) Европеоидная Негроидная Монголоидная Другая | 94 (97) 2 (2) 1 (1) 0 (0) | 86 (97) 2 (2) 0 (0) 1 (1) |
| Классификация, DSM-IV, n (%) Параноидная форма Дезорганизованная Кататоническая Недифференцированная | 55 (57) 19 (20) 3 (3) 20 (21) | 45 (51) 29 (33) 3 (3) 12 (13) |
Изменения в сумме баллов шкалы PAMSS. Средняя исходная сумма баллов по шкале PANSS была сходной у двух групп (сертиндол, 69,7; рисперидон 69,3). На протяжении исследования симптоматика смягчилась у пациентов в обеих группах (рис. 1). К концу исследования пациенты, получавшие сертиндол, продемонстрировали значительное уменьшение суммы баллов шкалы PANSS, по сравнению с пациентами, получавшими рисперидон (табл. 3). При помощи анализа ANCOVA данных LOCF, статистически значимых различий в дельте суммы баллов PANSS между двумя группами зарегистрировано не было. Однако, при анализе данных всех завершенных случаев (ОС) было выявлено статистически значимое различие в группе сертиндола. Также эта группа продемонстрировала статистически значимое (р≤0,001) уменьшение суммы баллов по шкале PANSS, по сравнению с группой, получавшей рисперидон; обнаруженная разница составила 7,5 баллов к 12-й неделе.
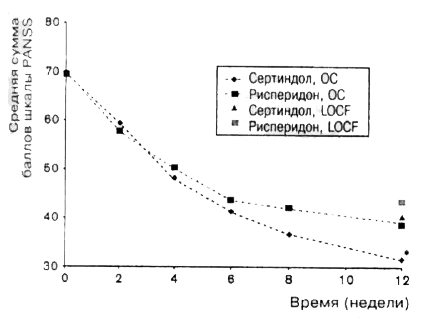
Рис 1. Средняя сумма баллов шкалы PANSS (для данных LOCF и ОС, при течении сертиндолом и рисперидоном; *р≤0,05 vs. рисперидон для модели ANCOVА
Когда респондеры были классифицированы исходя из процентного соотношения улучшений по шкале PANSS от исходного уровня к концу исследования, количество пациентов с 10- и 20-процентным улучшением было одинаковым для обеих групп, в то же время большее количество пациентов, получавших сертиндол, показало 30-, 40- и 50-процентное улучшение (рис. 2), по сравнению с пациентами, получавшими рисперидон. Кривые улучшения Каплана-Мейера по сумме баллов PANSS показывают сходную динамику для обеих групп на протяжении первых четырех недель. Позднее пропорция респондеров на сертиндол была больше, чем на рисперидон; различие, оцениваемое при помощи логарифмического рангового критерия, было статистически значимым в пользу группы сертиндола для ≥30% улучшения по шкале PANSS.
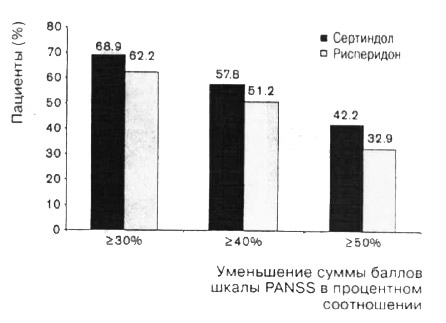
Рис. 2. Процентное соотношение респондеров с. как минимум. 30-, 40- и 50-процентным уменьшением показателей шкалы PANSS от начала к концу исследования
Переменные вторичной эффективности. Пациенты, получавшие сертиндол, продемонстрировали статистически значимое большее улучшение по субшкале негативных расстройств PANSS, чем пациенты на рисперидоне (табл. 3, рис. 3). Также. повторные анализы средних значений позитивной и негативной под шкал PANSS на протяжении исследования выявили статистически значимые различия в выборке посетивших все визиты пациентов (позитивная подшкала, р<0,01; негативная под-шкала, р<0,01). Никаких статистически значимых различий между двумя группами не было зарегистрировано для шкал CGI-S, DAI и GAF (табл. 3). Более того, количество пациентов, чье состояние улучшилось по шкале CGI-I, было одинаковым: пациентов на сертиндоле и 8,4% на рисперидоне достигли «очень значительного улучшения», и 58,2% на сертиндоле и 53,0% на рисперидоне достигли «значительного улучшения».
Таблица 3
Первичные и вторичные параметры эффективности: средние изменения от исходного уровня к концу исследования (рандомизированная, получавшая лечение популяция)
| Шкалы | ОС | LOCF | ||||
|---|---|---|---|---|---|---|
| Исходный уровень | Изменения | Изменения | ||||
| Сертиндол | Рисперидон | Сертиндол | Рисперидон | Сертиндол | Рисперидон | |
| n | 90 | 82 | 61 | 59 | 90 | 82 |
| PANSS сумма | 69,7±17,5 | 69,3±14,9 | -37,6±18,8* | -31,5±17,3 | -29,3±23,9 | -25,8±22,4 |
| PANSS позитивная | 16,7±4,7 | 15,9±5,8 | -10,7±5,6 | -8,5±5,7 | -8,0±7,9 | -7,2±6,5 |
| PANSS негативная | 19,6±7,2 | 20,0±6,1 | -9,3±5,6*** | -7,7±5,6 | -7,7±5,8* | -6,4±6,4 |
| CGI-S | 5,1*0,6 | 5,2±0,7 | -1,6*1,0 | -1,6*0,8 | -1,4±1,2 | -1,3±1,0 |
| n | 76 | 65 | 59 | 54 | ||
| DAIa | 29,8±5,8 | 31,0±6,1 | 2,2±6,9 | 1,4±7,0 | ||
| N | 80 | 70 | 59 | 55 | ||
| GAFa | 37,9±12,3 | 37,2±10,5 | 21,1±15,7 | 18,2±14,3 | ||
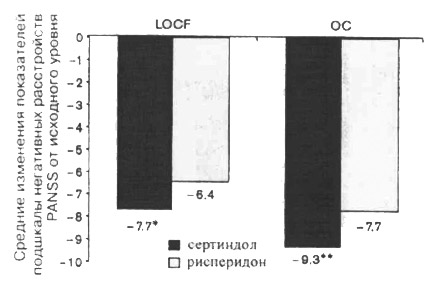
Рис. 3. Средние изменения показателей подшкалы негативных расстройств PANSS от исходного уровня; *р≤0,05 vs. pucneридон для модели ANCOVA; *p≤0,001 vs. рисперидон для модели ANCOVA
Анализ безопасности и переносимости. И сертиндол, и рисперидон хорошо переносились пациентами. Общее количество побочных эффектов было одинаковым в обеих группах: у 84 из 97 пациентов группы сертиндола (86,6%) и у 72 из 89 пациентов группы рисперидона (80,9%) наблюдался хотя бы один случай нежелательного действия; в таблице 4 приведены побочные действия, наблюдавшиеся, как минимум, у 5% пациентов из обеих групп. У значительно большего числа пациентов, получавших сертиндол, по сравнению с рисперидоном, наблюдалось удлинение интервала QT (22,7% vs. 4,5%) и нарушения эякуляции (18,5% vs. 3,4%) (р<0,05). Седативный эффект в виде сонливости наблюдался у 8% пациентов, получавших сертиндол, и у 8% пациентов, получавших рисперидон.
Таблица 4
Побочные действия, наблюдаемые, как минимум, у 5% пациентов, получавших сертиндол или рисперидон
| Побочное действие | Сертиндол (n=97) (%) | Рисперидон (n=89) (%) |
|---|---|---|
| Как минимум одно побочное действие | 84 (86,6) | 72 (80,9) |
| Удлинение QT a | 22 (22,7)* | 4 (4,5) |
| Увеличение массы тела | 20 (20,6) | 14 (15,7) |
| Тревога | 18 (18,6) | 20 (22,5) |
| Нарушение эякуляции b | 10 (18,5)* | 2 (3,4) |
| Бессонница | 9 (9,3) | 11 (12,4) |
| Сонливость | 8 (8,2) | 7 (7,9) |
| Нарушение внутрисердечной проводимости | 7 (7,2) | 4 (4,5) |
| Запор | 7 (7,2) | 6 (6,7) |
| Астения | 7 (7,2) | 10 (11,2) |
| Фарингит | 6 (6,2) | 7 (7,9) |
| Половая дисфункция b | 3 (5,6) | |
| Тремор | 5 (5,2) | 3 (3,4) |
| Головная боль | 5 (5,2) | 4 (4,5) |
| Гипотензия | 5 (5,2) | 5 (5,6) |
| Экстрапирамидные расстройства | 4 (4,1) | 9 (10,1) |
| Нарушения сна | 2 (2,1) | 5 (5,6) |
| Гиперсаливация | 1 (1,0) | 5 (5,6) |
| Аменорея c | 2 (6,7) |
У меньшего количества пациентов из группы сертиндола наблюдались экстрапирамидные расстройства (19% vs. 28%), хотя это различие не было статистически значимым. Также разница во времени наступления первого случая проявления экстрапирамидной симптоматики в обеих группах не была статистически значимой. Большее улучшение по шкалам SAS, BAS и AIMS (в особенности SAS и BAS) в числовом выражении наблюдалось в группе сертиндола (табл. 5), но статистически значимых различий зарегистрировано не было.
Таблица 5
Неврологические шкалы: средние изменения от исходного уровня к концу исследования у пациентов, получавших лечение
| Неврологические шкалы | Сертиндол | Рисперидон | ||||
|---|---|---|---|---|---|---|
| n | Исходный уровень | Изменения | n | Исходный уровень | Изменения | |
| SAS | 93 | 2,б±3,6 | -1,1±3,0 | 86 | 2,5±3,4 | -0,2±3,5 |
| BAS | 93 | 1,0±1,8 | -0,5±1,8 | 86 | 1,0±1,9 | -0,1±2,2 |
| AIMS | 82 | 5,4±3,8 | -0,8±3,0 | 74 | 5,4±3,4 | -0,7±3,3 |
Показатели ЭКГ, проведенной в начале исследования, свидетельствовали, что значительной разницы между группами не было. На протяжении исследования у большей пропорции пациентов из группы сертиндола наблюдалась пограничная (сертиндол, 34%; рисперидон, 26%) или пролонгированная (сертиндол, 19%; рисперидон, 5%) длина интервала QT (табл. 6). Прирост массы тела в обеих группах был небольшим (сертиндол, 2,1±3,9 кг; рисперидон, 1,5±3,7 кг), и индекс массы тела составлял для сертиндола 0,7±1,3, а для рисперидона 0,5±1,2. Каких-либо значимых изменений в витальных показателях в обеих группах зарегистрировано не было.
Таблица 6
Средние величины интервалов QTc на протяжении исследования у пациентов с высокими показателями QT или QTc на любом отрезке исследования
| Сертиндол | Рисперидон | ||||
|---|---|---|---|---|---|
| Средние величины | Общее количество | Средние величины | Общее количество | pa | |
| Средний исходный QTc | 407,7±20,8 | 95 | 409,3±18,2 | 87 | NS |
| Средний конечный QTc | 429,6±29,1 | 91 | 411,0±27,0 | 83 | <0,05 |
| n (%) | n (общее) | n (%) | n (общее) | pb | |
| Максимальный QT>500 мсек | 0 | 90 | 0 | 81 | - |
| Максимальный QTc>500 мсек | 2 (2,2) | 90 | 0 | 81 | NS |
| Изменения QT>60 мсек | 12 (13,3) | 90 | 1 (1,2) | 81 | <0,05 |
| Изменения QTc >60 мсек | 11 (12,2) | 90 | 8 (6,2) | 81 | NS |
Всего по вине побочных действий из исследования выбыл 21 пациент. Из 12 (12%) пациентов группы сертиндола, 6 – из-за удлинения интервала QT. Остальные случаи прерывания участия в испытаниях были обусловлены тревогой, сонливостью, увеличением массы тела, судорогами, нарушениями эякуляции и заболеваниями легких. Из 9 (10%) пациентов из группы рисперидона, выбывших досрочно, один – из-за удлинения интервала QT, одни – по причине тревоги, а остальные из-за гипертензии, судорог, галлюцинаций, сыпи, бреда, депрессии и гастроинтестинальных расстройств. Поскольку только один из пациентов с удлинением интервала QT получал большую, чем в среднем (24 мг сертиндола), дозировку антипсихотика, не похоже, чтобы это побочное действие было дозозависимым. На 13-й день исследования один из пациентов в группе рисперидона совершил суицид; статус пациента характеризовался как бредовый еще до начала рандомизации.
Обсуждение
Настоящее исследование является первым непосредственным сравнением сертиндола и рисперидона в популяции пациентов с шизофренией. Хотя оба препарата очевидно облегчали симптоматику, некоторые значительные различия несомненны. К концу исследования в группе данных ОС, сертиндол статистически более значимо влиял на улучшение показателей PANSS, чем рисперидон. Более того, сертиндол, по сравнению с рисперидоном, статистически значимо оказывал большее влияние на негативную симптоматику (PANSS, подшкала негативных симптомов) (р≤0,05), а также и на продуктивную (PANSS, подшкала позитивных симптомов), что выявилось при применении модели повторных измерений. С одинаковой эффективностью сертиндол и рисперидон улучшали показатели шкал CGI есть и улучшение), DAI и GAF.
Улучшение общих значении PANSS на протяжении исследования наблюдалось в обеих группах. Несомненно, существует клинический интерес в проведении долгосрочного исследования для определения влияний по окончании 12-недельного периода. Более того, возможно, различия в суммарных значениях PANSS достигли бы статистически значимых показателей, если бы исследование не было прервано досрочно.
Оба препарата продемонстрировали хорошую переносимость и безопасность применения. Единственными статистически значимыми различиями были удлинение интервала QT и нарушение эякуляции, отмеченные в группе сертиндола, по сравнению с рисперидоном. Эти побочные действия описаны при применении сертиндола (13). Несмотря на то, что удлинение интервала QT наблюдалось при сертиндоле, нет доказательств увеличения сердечной или общей смертности в большом количестве клинических и эпидемиологических исследований (23, 24). Уже докладывалось об уменьшении объема эякулята примерно в 20% случаев применения сертиндола, и это не было связано с низким либидо, эректильной дисфункцией и аноргазмиеи (13). К тому же, ни сертиндол, ни рисперидон не были причиной избыточного увеличения массы тела, что сопоставимо с ранними исследованиями (13, 25). Увеличение массы тела может быть значимым препятствием при применении некоторых антипсихотиков (32) и может явиться причиной нон-комплайенса.
В обеих группах наблюдались осложнения, связанные с экстрапирамидной симптоматикой, однако никаких статистически значимых различий зарегистрировано не было, хотя пропорция пациентов с такими побочными эффектами в группе рисперидона была больше. Поскольку экстрапирамидные расстройства ассоциируются с уровнями антипсихотиков в плазме, возможно, более частое возникновение подобной симптоматики отражает то, что средняя дозировка рисперидона 6,6 мг/сут несколько превышала лицензированную дозу 6 мг/ сут. Более того, баллы неврологических шкал уменьшались с ходом исследования, особенно у пациентов из группы сертиндола. Это перекликается с предыдущими клиническими испытаниями, продемонстрировавшими, что частота возникновения экстрапирамидной симптоматики у сертиндола сопоставима с плацебо (19, 31, 33). Оба препарата редко вызывали другие побочные действия. что выражалось в низком уровне исключений из исследования по этой причине.
Средние дозировки препаратов составили 16,7 мг/сут для сертиндола и 6,6 мг/сут для рисперидона. Обе эти дозировки отражают оптимальное клинически эффективное дозирование и, следовательно, сравнивать результаты лечения было вполне правомерно.
В заключение можно сказать, что сертиндол продемонстрировал некоторое клиническое превосходство над рисперидоном. Острота симптоматики пациентом, В соответствии с данными PANSS, лучше поддавалась терапии сертиндолом. Также сертиндол оказался статистически достоверно более эффективным в лечении негативной симптоматики. В сочетании с хорошими переносимостью и профилем безопасности, возможным положительным действием на когнитивную сферу, сертиндол предлагает пациентам эффективный и приемлемый способ справляться с болезнью и восстанавливать способность к функционированию.
Литература
- Arnt J., Skarsfeldt T. Do novel antipsychotic have similar pharmacological characteristics? A review of the evidence //Neuropsychopharmacol. - 1998. - Vol. 18. - P. 63-101.
- American Psychiatric Association. Diagnostic and statistical manual of mental disorders, 4th edn. - Washington, DC: American Psychiatric Association, 1994.
- Awad A.G. Subjective response to neuroleptics in schizophrenia //Schizophr. Bull. - 1993. – Vol. 19. – P.609-618
- Awad A.G., Hogan T.P. Subjective response to neuroleptics and the quality of life: implications for treatment outcome //Acta Psychiatr. Scand. - 1994 – Vol. 380. Suppl. - P. 27-32.
- Barnes T.R. A rating scale for drug-induced akathisia // Br. J. Psychiatry. - 1989 – Vol. 154. - P. 672-676.
- Bonsack C.H. Subjective response to antipsychotics in schizophrenic outsubjects preliminary results using a French version of the Drug Auiiude Inventory (DAI): London, AEP, 1996.
- Carman J., Peuskens J., Vangeneugden A. Risperidone in the treatment of negative symptoms of schizophrenia a meta-analysis // Int. Clin. Psychopharmacol. – 1995. – Vol. 10. – P. 207-213
- Chouinard G., Arnott W. Clinical review of risperidone//Can. J. Psychiatry. - 1993. -Vol. 38, Suppl. 3. - P.S89-S95
- Chouinard G., Jones В., Remington G. et al. A Canadian multicenter placebo-controlled study of fixed doses of risperidone and haloperidol in the treatment of chronic schizophrenic patients // J. Clin. Psychopharmacol. - 1993. - Vol. 13. - P. 25-40
- Daniel D.G., Wozniak P., Mack R.J., McCarthy B.G. Long-term efficacy and safely comparison of sertindole and haloperidol in the treatment of schizophrenia. The Sertindole Study Group //Psychopharmacol. Bull. - 1998. - Vol. 34. - P. 61-69.
- FDA. COSTART III coding symbols for thesaurus of adverse reaction terms. 5th edn. - Rockville, Maryland: Food and Drug Administration, 1989.
- Geddes J., Freemantle N., Harrison P., Bebbington P. Atypical antipsychotics in the treatment of schizophrenia systematic overview and meta analysis//B.M.J - 2000. – Vol. 321. -P. 371-1376.
- Hale A.S. A review of the safety and tolerability of sertindole// Int. Clin. Psychopharmacol. – 1998. –Vol. 13. Suppl. 3. – P. S65-S70.
- Hale A.S., Azorin J.-M., Kasper S. et al. Sertindole improves both the positive and negative symptoms of schizophrenia: results of a phase III trial //Int. J. Psych. Clin. Pract. - 2000. - Vol. 4. - P. 55-62.
- Hale A.S., Azorin J.-M., Kasper S. et al. Sertindole is associated with a low level of extrapyramidal symptoms in schizophrenic patients: results of base III trial // Int. J. Psych. Clin. Pract. – 2000. - Vol. 4. - P. 47-54
- Hoyberg O.J., Fensbo C., Remvig J. et al. Risperidone versus perphenazine in the treatment of chronic schizophrenic patients with acute exacerbations //Acta Psychiatr. Scand. - 1993 - Vol. 88. - P. 395-402.
- Huttunen M.О., Piepponen T., Rantanen H. et al. Risperidone versus zuclopenthixol in die treatment of acute schizophrenic episodes; a double-blind parallel-group trial //Acta Psychiatr Scand. - 1995. – Vol. 91.- P. 271-277.
- Hyttel J. Nielsen J.В., Nowak G. The acute effect of sertindole on brain 5-HT2. D2 and alpha 1 receptors (ex vivo radioreceptor binding studies) // J. Neural. Transm. Gen. Sect. - 1992 – Vol. 89 - P. 61-69
- Kane J.M. Sertindole a review of clinical efficacy // Int. Clin. Psychopharmacol. - 1997. – Vol. 13. Suppl. 3. - P SS9
- Kay S.R., Fiszbein A., Opler LA. The positive and negative syndrome scale (PANSS) for schizophrenia // Schizophr. Bull - 1987 -Vol. 13.- P. 261-276.
- Lis S., Krieger S., Gallhofer B. et al. Sertindole is superior to haloperidol in cognitive performance in patients with schizophrenia, a comparative study II Eur. Neuropsychopharmacol - 2003 – Vol. 13 Suppl. 4. – P. S323.
- Marder S.R., Meibach R.C. Risperidone in the treatment of schizophrenia //Am J. Psychiatry - 1994 - Vol. 151. - P. 825-835
- Moore N. Higher cardiovascular mortality with sertindole in ADROIT, a signal not confirmed/7 Int .1 Psychiatry Clin Prac.-2002 - Vol. 6. Suppl. 1 - P. 3-9.
- Moore N., Hall G., Sturkenboom M. et al. Biases affecting the proportional reporting ratio (PPR) in spontaneous reports pharmacovigilance databases the example of sertindole // Pharmacoepidemiol . Drug Saf. -2003. -Vol. 2 - P. 271-Z81
- Nasrallah H. A review of the effect of atypical antipsychotics on weight // Psychoneuroendocrinol - 2003. - Vol. 28 -P. 83
- NIMH. Clinical Global Impression // ECDEU assessment manual for psychopharmacology, rev, edn, / W. Guy (Ed.) - Rockville, Maryland National Institutes of Mental Health, 1976 - P. 212-222.
- NIMH. AIMS, Abnormal Involuntary Movement Scale // ECDEU assessment manual for psychopharmacology, rev. edn. / W. Guy (Ed.) - Rockville, Maryland: National Institutes of Mental Health. 1976 – P. 534-537.
- Peuskens J. Risperidone in the treatment of patients with chronic schizophrenia: a multi-national, multi-centre, double-blind, parallel-group study versus haloperidol Risperidone Study Group // Br. J. Psychiatry - 1995. - Vol. 166 - P. 712
- Simpson G.M., Angus J W. A rating scale for extrapyramidal side effects //Acta Psychiatr Scand - 1970. – Vol. 212, Suppl – P. 11-19
- Tamminga С A., Mack R.J.. Granneman G.R. et al. Sertindole in the treatment of psychosis in schizophrenia efficacy and satety // Int. Clin. Psychopharmacol. - 1997. – Vol. 12, Suppl. 1 - P. S29-S35
- van Kammen D.P., McEvoy J.P., Targum S.D. et al. A randomized, controlled, dose-ranging trial of sertindole in patients with schizophrenia // Psychopharmacol. - 1996 – Vol. 124. – P. 168-175
- Winning D.A., Wirshing W.C., Kysar L. et al. Novel antipsychotics: comparison of weight gain liabilities // J. Clin Psychiatry - 1999. – Vol. 60. - P. 358-363.
- Zimbroff D.L., Kane J.M., Tamminga С.A. el al for the Sertindole Study Group. Controlled, dose-response study of sertindole and haloperidol in the treatment of schizophrenia Sertindole Stud; Am J. Psychiatry - 1997 - Vol. 154, - P. 782-791.
A double-blind, controlled study of sertindole versus risperidone in the treatment of moderate-to-severe schizophrenia
J.-M. Azorin, N. Strub, H. Loft Sertindole is a non-sedating atypical antipsychotic effective in the management of schizophrenia and is associated with placebo-level incidence of extrapyramidal symptoms (EPS). In this randomized, double-blind. parallel-group, flexible-dose, multi-centre study, the efficacy and tolerability of sertindole was directly compared with another atypical antipsychotic in patients with schizophrenia. A total of 187 patients were randomly assigned to treatment with sertindole (12-24 mg/day, n=98) or risperidone (4-10 mg/day, n=89) for 12 weeks. Although early termination reduced the power of the study, some significant between-group differences were evident. Sertindole reduced the mean Positive and Negative Syndrome Scale total scores to a greater extent than risperidone. and the difference reached statistical significance al endpoint for the Observed Cases (ОС) dataset. Moreover, sertindole was superior for the treatment of negative symptoms compared to risperidone (p<0.05. Last Observation Carried Forward and ОС). Both treatment groups were similarly effective in improving Clinical Global Impression (Seventy and Improvement), the Drug Attitude Inventory and Global Assessment of Functioning scores. Sertindole and risperidone were both well tolerated Numerically, fewer patients in the sertindole group (19%) reported EPS-related adverse events than in the risperidone group (28%), although significantly more sertindole-treated patients reported QT prolongation and abnormal ejaculation volume (p<0.05). In conclusion, sertindole well tolerated and demonstrated clinically relevant efficacy advantages over risperidone.
