Когнитивные нарушения при артериальной гипертонии и возможности их коррекции
СтатьиОпубликовано в журнале:
Врач 14'2011
О. Остроумова, доктор медицинских наук, профессор, К. Резникова
МГМСУ Рассмотрены вопросы определения, диагностики и прогностической значимости когнитивных расстройств (КР) при артериальной гипертензии. Подробно проанализированы данные исследования PROGRESS о влиянии антигипертензивной терапии на риск развития деменции и КР. Приведены результаты собственного исследования эффективности препарата Нолипрел А/Нолипрел А форте в снижении АД и улучшении когнитивных функций.
Ключевые слова: артериальная гипертония, суточное мониторирование АД, когнитивные нарушения, антигипертензивная терапия, фиксированные комбинации антигипертензивных препаратов, периндоприл, индапамид.
Несмотря на усилия ученых, врачей и органов управления здравоохранением, артериальная гипертензия (АГ) в Российской Федерации остается одной из наиболее значимых медико-социальных проблем. Это обусловлено как ее широким распространением (около 40% взрослого населения РФ имеют повышенный уровень АД), так и тем, что АГ - важнейший фактор риска развития основных сердечно-сосудистых заболеваний — инфаркта миокарда и мозгового инсульта, главным образом определяющих высокую смертность в нашей стране [1, 2]. АГ — причина и других грозных осложнений, в том числе терминальной почечной недостаточности, требующей проведения гемодиализа, хронической сердечной недостаточности, внезапной смерти, инсульта (ишемического или геморрагического), а также сосудистой деменции [1, 3,4].
Развитию этих осложнений предшествует бессимптомное поражение соответствующих органов-мишеней: почек (микроальбуминурия), сердца (гипертрофия миокарда левого желудочка), головного мозга (ГМ) [1]. К сожалению, в стандартный план обследования больного АГ не входит оценка состояния ГМ как органа-мишени АГ, поэтому в клинической практике врач констатирует его поражение уже на этапе развития осложнений.
Субклинические поражения ГМ (поражения ГМ как органа-мишени АГ) отмечают у 44% больных гипертонической болезнью, что примерно в 2 раза превышает распространенность поражения сердца и почек как органов-мишеней АГ [6]. Проявлениями поражения ГМ как органа-мишени АГ считают когнитивные расстройства (КР) и феномены «немых» лакун и(или) лейкоареоза (по данным магнитно-резонансной томографии - МРТ) [6, 7]. В рекомендациях по диагностике и лечению АГ впервые на необходимость выявления субклинических поражений ГМ как органа-мишени АГ указано лишь в 2009 г. в так называемом согласительном документе Европейского общества по АГ [7].
Отметим, что из клинических симптомов наиболее тесную взаимосвязь со степенью поражения белого вещества ГМ (МРТ) имеют нарушения когнитивных функций (КФ) [8]. КФ (синонимы: высшие мозговые, высшие психические, высшие корковые, познавательные) - наиболее сложные функции ГМ, с помощью которых осуществляется процесс рационального познания мира и обеспечивается целенаправленное взаимодействие с ним [9].
К основным 5 КФ относят: гнозис (восприятие информации); праксис (произвольное/целенаправленное двигательное действие); речь, память и интеллект [9]. Гнозис - способность соединять элементарные ощущения в целостные образы. Пациент с тяжелыми нарушениями гнозиса (агнозия) видит предмет, может его описать, но не узнает его. Память - способность запечатлевать, сохранять и многократно воспроизводить полученную информацию. Интеллект - способность к анализу информации, выявлению сходств и различий, общего и частного, главного и второстепенного, способность к абстрагированию, решению задач, построению логических умозаключений. Подчеркнем, что субъективные жалобы больных на память не соответствуют истинным ее нарушениям, выявляемым с помощью специальных методов исследования. Речь - способность понимать обращенную речь и выражать свои мысли вербально (словами). Праксис - способность усваивать и удерживать разнообразные двигательные навыки, в основе которых лежат автоматические серии движений. Больные с тяжелыми нарушениями праксиса (апраксия) не могут выполнить то или иное действие вследствие утраты навыка («разучился»; например, больные разучаются ходить, несмотря на отсутствие пареза [10]).
Согласно классификации акад.Н. Яхно (2005), выделяют легкие, умеренные и тяжелые КР [9]. Легкие КР – снижение одной или нескольких КФ по сравнению с исходным более высоким уровнем (индивидуальной нормой), не влияющее на бытовую, профессиональную и социальную деятельность, в том числе на наиболее сложные ее формы. Умеренные КР - расстройства одного или нескольких КФ, выходящие за рамки среднестатистической возрастной нормы, но не вызывающие дезадаптацию, хотя они могут приводить к трудностям в сложных и непривычных для пациента ситуациях.
Необходимо понимать, что КР — прогрессирующее состояние, которое со временем трансформируется в деменцию. Так, через год у 5-15% пациентов с умеренными КР разовьется деменция (для сравнения: в общей популяции вероятность ее развития — 1—5%), а через 4 года таких пациентов будет уже 70%, и соответственно через 5 лет деменции будут подвержены все пациенты с КР [10, 11].
Тяжелые КР - расстройства КФ, приводящие к полной или частичной утрате пациентами независимости и самостоятельности, т.е. вызывающие профессиональную, социальную и(или) бытовую дезадаптацию. К тяжелым КР относится и деменция, в том числе сосудистая.
Сосудистая деменция, как и инсульт (ишемический и геморрагический), является уже осложнением АГ. Согласно МКБ-10, деменцию диагностируют при нарушении памяти и по крайней мере одного из других КФ (речь, праксис, гнозис, мышление), если этосостояние затрудняет профессиональную деятельность или социальную адаптацию и сохраняется не менее 6 мес. Принципиально отличается от легких и умеренных КР инвалидизация — невозможность сохранять профессиональную деятельность или социальную, в том числе бытовую, адаптацию [12]. Особенно часто деменция отмечается в пожилом возрасте. Согласно популяционным исследованиям, она наблюдается у 5-20% пожилых лиц [13]. Деменция и преддементные КР регулярно сочетаются с эмоциональными нарушениями, которые прежде всего носят характер депрессивных и тревожно-депрессивных расстройств [13].
Ведущую роль в формировании когнитивной недостаточности при АГ играет поражение глубинных отделов белого вещества ГМ и базальных ганглиев, что приводит к нарушению связи лобных структур ГМ с подкорковыми (феномен корково-подкоркового разобщения). Как считают, хроническая неконтролируемая АГ - причина вторичных изменений сосудистой стенки - липогиалиноза, который развивается преимущественно в сосудах микроциркуляторного русла. Формирующийся вследствие этого артериолосклероз ведет к изменению физиологической реактивности сосудов. В таких условиях снижение АД в результате, например, присоединения сердечной недостаточности со снижением сердечного выброса, или избыточной гипотензивной терапии, или циркадных изменений АД способствует возникновению гипоперфузии в зонах терминального кровообращения, к которым относятся указанные выше глубинные церебральные структуры [14-16].
Острые ишемические эпизоды в бассейне глубоких пенетрирующих (перфорантных) артерий вызывают небольшие по диаметру лакунарные инфаркты в глубинных отделах ГМ. При неблагоприятном течении АГ или неадекватном ее лечении повторные острые эпизоды способствуют возникновению так называемого лакунарного состояния — одного из вариантов мультиинфарктной сосудистой деменции [17, 18]. Помимо повторных острых нарушений, предполагается и наличие хронической ишемии в зонах терминального кровообращения. Маркером последней служит резрежение перивентрикулярного или субкортикального белого вещества - лейкоареозис, который патоморфологически представляет собой зону демиелинизации, глиоза и расширения периваскулярных пространств [14-16].
Жалоба пациентов на снижение памяти (или отсутствие таковой) не может служить критерием нарушения памяти. Для объективизации КР следует использовать психометрические методики (специальные опросники) [9].
В ряде многоцентровых рандомизированных исследований, например в исследовании PROGRESS (Perindopril Protection against Recurrent Stroke Study) [19], доказана способность антигипертензивной терапии снижать риск развития новых случаев деменции. Антигипертензивные препараты могут также улучшать или по крайней мере снижать темпы прогрессирования КР [19].
В исследовании PROGRESS под наблюдением находились больные (более 6 тыс. человек) с указаниями на мозговой инсульт или преходящее нарушение мозгового кровообращения в анамнезе (в предшествующие 5 лет) [19, 20]. Уровень АД не был критерием включения в исследование, в связи с чем в него отбирали не только больных АГ, но и больных с нормальным АД, ранее перенесших мозговой инсульт [20].
В течение подготовительного периода (4 нед) все больные получали терапию периндоприлом. Затем они были рандомизированы на группы и получали периндоприл (при необходимости - в комбинации с индапамидом, число таких больных составило 58%) или плацебо. Особо подчеркнем, что решение о назначении больному индапамида в комбинации с периндоприлом принимал лечащий врач: рандомизации пациентов в эти 2 подгруппы не проводили. Больные находились под наблюдением в течение 4 лет.
Несмотря на большое количество рандомизированных пациентов, включенных в группы активного лечения и плацебо, различия в их исходных показателях полностью отсутствовали. В группах активного лечения и плацебо средний возраст больных составил 64 года; мужчин было 70%, представителей европеоидной расы - 61%. Большинство больных названных групп (активного лечения и плацебо) перенесли мозговой инсульт (транзиторная ишемическая атака отмечена только у 22% включенных в исследование). Наиболее распространенной формой мозгового инсульта был инфаркт мозга, что указывает на большую частоту ишемического инсульта, чем геморрагического. Примерно у 20% пациентов были сахарный диабет (СД) или ишемическая болезнь сердца. На момент включения в исследование средний уровень АД составлял у больных обеих групп 147/86 мм рт. ст. Таким образом, в исследовании PROGRESS под наблюдением находились больные с анамнестическими указаниями на цереброваскулярные заболевания, имеющие как нормальное, так и высокое АД, т.е. АГ (примерно поровну) [20]. Перед началом исследования около 50% больных уже получали антигипертензивную терапию.
Различия в снижении уровня систолического и диастолического АД (САД и ДАД), наблюдавшиеся в ходе исследования у представителей групп активного лечения и плацебо, были статистически достоверны: снижение составило соответственно 9,0 и 4,0 мм рт. ст. [20] (табл. 1). Эти данные наглядно демонстрируют стойкое снижение уровня АД у больных, получавших периндоприл (+индапамид) в течение 4 лет.
Таблица 1
Различия показателей АД у больных основной и контрольной групп к моменту завершения исследования PROGRESS (M±m)
| Показатель | Снижение АД, мм рт. ст. | |
| систолическое | диастолическое | |
| Больные АГ | 9,5±0,6 | 3,9±0,3 |
| Больные без АГ | 8,8±0,5 | 4,2 ± 0,3 |
| Комбинация препаратов (периндоприл/индапамид) | 12,3±0,5 | 5,0 ± 0,3 |
| Монотерапия (периндоприл) | 4,9±0,6 | 2,8 + 0,3 |
| Все больные | 9,0±0,3 | 4,0 ± 0,2 |
Снижение как САД, так и ДАД было более выраженным в подгруппе пациентов, получавших комбинированную терапию (периндоприл+индапамид).
Особый интерес представлял анализ влияния периндоприла на уровень КР и развитие деменции. В исследовании PROGRESS сбор информации о состоянии КФ пациентов осуществляли исходно, через 6 и 12 мес, а затем — через каждый год с момента рандомизации больных. Во время каждого посещения пациент проходил тестирование с помощью Mini-Mental State Examination [21]. Помимо этого, наличие деменции определяли, исходя из мнения исследователя. Всем больным с баллом по шкале <25 и(или) положительным ответом исследователя на вопрос, имеет ли этот больной, на его взгляд, деменцию, проводили дальнейшее дообследование с верификацией деменции в соответствии с критериями Американской психиатрической ассоциации (DSM-IV) [22]. Деменцию, которая возникла после перенесенного в ходе наблюдения в исследовании PROGRESS инсульта, назвали «деменцией после повторного инсульта», а если деменция возникла у пациента, который в ходе наблюдения в PROGRESS избежал повторного нарушения мозгового кровообращения, - «деменцией без повторного инсульта» [19]. Кроме того, отдельно оценивали влияние антигипертензивной терапии на риск развития ухудшения КФ. В исследовании PROGRESS это рассчитывали как снижение количества баллов по шкале MMSE на 3 и более по сравнению с исходными данными [19]. Исходно в обеих группах средний балл по шкале MMSE составил 29, а число больных с количеством баллов по MMSE 25 и менее - по 15% в обеих группах. Если исходно у пациента количество баллов по MMSE составило 25 и менее и(или) был получен положительный ответ на вопрос, имеет ли этот больной, по мнению врача, деменцию, констатировали наличие исходных КР [19].
Всего в группе активного лечения деменция зарегистрирована у 6,4% больных, а в группе плацебо — у 7,1% (16 и 19 случаев на 1000 пациенто-лет соответственно) [19]. В группе активного лечения риск развития деменции оказался ниже на 12%, чем в группе плацебо (различия недостоверны; р=0,02) — рис. 1. При этом антигипертензивная терапия достоверно (р=0,03) снижала риск деменции после повторного инсульта - на 34% (см. рис. 1) [19]. Риск ухудшения КФ на фоне терапии комбинацией периндоприл+индапамид достоверно - на 19% - ниже, чем в группе плацебо (р=0,01), а риск ухудшения КФ после перенесенного повторного инсульта— на 45% (р=0,001) — рис. 2. При этом не выявлено никаких достоверных различий влияния комбинации периндоприл+индапамид на риск развития деменции или ухудшения КФ у больных АГ и без АГ (см. рис. 1, 2).
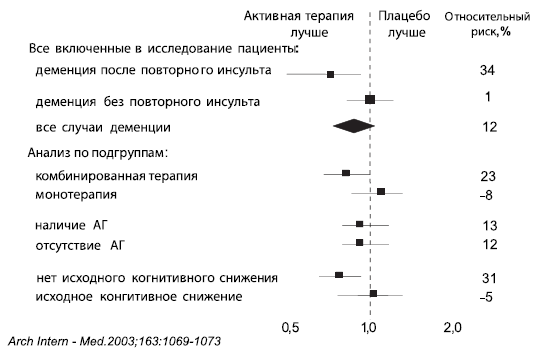
Рис. 1. PROGRESS: снижение риска развития деменции
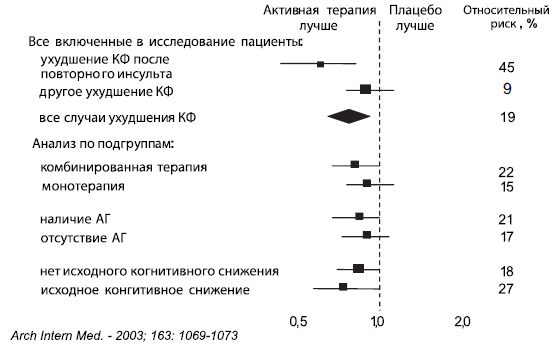
Рис. 2. PROGRESS: снижение риска развития КФ
Интересно, что в подгруппе больных, получавших комбинированную терапию (периндоприл+индапамид), отмечено большее снижение риска как деменции (на 23%; р=0,05), так и ухудшения КФ (на 22%; р=0,05), чем в подгруппе пациентов, получавших монотерапию (на 8 и 15% соответственно, недостоверно) - см. рис. 1 и 2. Кроме того, выявлено, что риск развития деменции достоверно (р=0,02) снизился в подгруппе пациентов без исходных КР — на 31%, что отличало их от больных с исходным наличием КР (см. рис. 1) [19].
Следовательно, в погруппе больных, получавших в исследовании PROGRESS комбинированную терапию периндоприлом и индапамидом, наблюдали достовернобольшее снижение АД (как САД, так и ДАД); у них также риск развития деменции или ухудшения КФ снизился больше, чем у пациентов на фоне монотерапии.
Исходя из изложенного, оценено влияние фиксированной комбинации Нолипрел А и Нолипрел А форте на уровень АД и КФ у больных с эссенциальной АГ. Обследовано 33 пациента (11 мужчин, 22 женщины) с впервые выявленной или нелеченой АГ I-II степени (17 больных АГ I степени и 16 - АГ II степени, средний возраст - 54,3+1,5 года) без метаболического синдрома и СД: у всех исходно отмечен нормальный уровень глюкозы натощак. 13 человек курили, средняя длительность АГ - 4,7+0,7 года.
Критерии включения в исследование: возраст 40-75 лет; установленный диагноз АГ II и III степени и АД 140-169 и(или) 90-109 мм рт. ст. (при визите для рандомизации).
Не включали в исследование лиц: с клинически значимым заболеванием сердца (в том числе с недавно перенесенным — менее 6 мес назад - кардиогенным шоком; инфарктом миокарда с осложнениями; атриовентрикулярной блокадой II и III степени без искусственного водителя ритма; синоатриальной блокадой, синдромом слабости синусового узла; хронической сердечной недостаточностью); брадикардией; клинически значимым заболеванием сосудов; бронхиальной астмой; клинически значимыми заболеваниями эндокринной системы (в том числе с СД), крови, печени, почек, обмена веществ, клинически значимыми иммунологическими, неврологическими заболеваниями (в том числе с острым нарушением мозгового кровообращения в анамнезе любой давности, транзиторной ишемической атакой в течение ближайших 6 мес). В ходе исследования не допускалось использования каких-либо других антигипертензивных лекарственных средств, кроме клофелина, и (или) каптоприла, и(или) нифедипина не чаще 1 раза в неделю по потребности.
Пациенты, не завершившие исследование и(или) преждевременно прекратившие участие в нем, были исключены из анализа данных.
Все пациенты получали комбинацию ингибитора ангиотензинпревращающего фермента периндоприла аргининовая соль - 2,5 мг и диуретика индапамида - 0,625 мг (Нолипрел А, Сервье, Франция) по 1 таблетке 1 раз в сутки утром. Через 4 нед при недостижении целевого АД (менее <140 и 90 мм рт. ст.) доза препарата на однократный прием была изменена - периндоприла аргининовая соль 5 мг и диуретика индапамида 1,25 мг(Нолипрел А форте, Сервье, Франция) по 1 таблетке 1 раз в сутки утром. Срок наблюдения - 12 нед с момента достижения целевого АД. Исследование было несравнительным, открытым.
Всем пациентам исходно и в конце периода наблюдения, помимо общеклинического обследования и измерения АД методом Короткова, выполняли суточное мониторирование (СМАД) с использованием комплекса АВРМ-04 фирмы Mediteck (Венгрия). Исходно и через 12 нед антигипертензивной терапии в стабильных дозах у пациентов исследовали состояние КФ.
Субъективную оценку внимания и памяти проводили по визуальным аналоговым шкалам (ВАШ) [23], длиной 100 мм. Отметка «0» на шкале соответствует самой плохой оценке внимания/памяти, «100» - максимально хорошей оценке, о чем информируют пациента. Пациенту задают 2 вопроса:
- трудно ли вам сосредоточиться на чем-либо? (шкала внимания);
- трудно ли вам вспомнить недавно произошедшие события? (шкала памяти);
Пациент отмечает на шкалах точки, соответствующие состоянию внимания и памяти на текущие сутки. При повторном тестировании пациенту не предоставляют результат предыдущего исследования. Измерение производят от точки «0» до точек, отмеченных пациентом на шкале в миллиметрах.
Объем непосредственной слухоречевой памяти оценивали по субтесту Векслера № 5 [24], внимание — по субтесту Векслера № 7, заключающемуся в воспроизведении символов, соответствующих определенным цифрам. После получения разъяснений и заполнения тренировочной части теста пациент в течение 90 с выполнял задание по расстановке соответствующих заданным числам символов [24].
Статистическую обработку данных проводили с помощью пакета программ STATISTICA 5.0. Рассчитывали средние величины, их средние стандартные ошибки и 95% доверительный интервал. Гипотезу о равенстве средних оценивали по F-критерию (дисперсионный анализ). Для изучения распределения дискретных признаков применяли стандартный метод анализа таблиц сопряженности с применением критерия χ² по Пирсону.
С помощью титрования дозы у всех 33 больных удалось достигнуть целевого уровня АД <140/90 мм рт. ст. (по данным рутинного измерения), при этом 22 (66,67%) пациента принимали по 1 таблетке Нолипрела А в сутки и 11 (33,33%) - по 1 таблетке Нолипрела форте 1 раз в сутки. Отмечено достоверное снижение САД и ДАД (табл. 2).
Таблица 2
Динамика показателей рутинного измерения АД у больных АГ, получавших Нолипрел А или Нолипрел А форте в течение 12 недель (М+м)
| Показатель | Группа Нолипрела (n=33) |
| САД, мм рт. ст.: исходно на фоне лечения Δ | 155,6±0,78 127,1±2,15* -28,5±3,06* |
| ДАД, мм рт. ст.: исходно на фоне лечения Δ | 96,5±3,06 77,3±0,86* -19,2±1,94* |
| Частота сердечных сокращений, в минуту: исходно на фоне лечения Δ | 73,5±2,07 72,8±2,04 -0,7±0,6 |
По данным СМАД, у больных, получавших в течение 12 нед Нолипрел А или Нолипрел А форте в стабильной дозе, выявлено достоверное уменьшение уровней САД и ДАД днем, ночью и в целом за сутки (табл. 3). На фоне 12 нед терапии в стабильной дозе целевых цифр среднесуточного АД (≤125/80 мм рт. ст.) по САД и ДАД достигли 20 (60,6%) больных, целевых цифр среднесуточного САД (≤125 мм рт. ст.) - 25 (75,8%), целевых цифр среднесуточного ДАД (≤80 мм рт. ст.) - 23 (69,7%), среднедневного АД (≤130/85 мм рт. ст.) по САД и ДАД - 24 (72,7%), среднедневного САД (≤130 мм рт. ст.) - 29 (87,9%), среднедневного ДАД (≤85 мм рт. ст.) - 25 (75,8%), средненочного АД (≤120/70 мм рт. ст.) по САД и ДАД - 22 (66,7%), средненочного САД (≤120 мм рт. ст.) - 23 (69,7%), средненочного ДАД (≤70 мм рт. ст.) - 21 (63,7%).
Таблица 3
Динамика показателей СМАД на фоне 12 недель лечения Нолипрелом А или Нолипрелом А форте в стабильной дозе (М±m)
| Показатель, мм рт. ст. | Группа Нолипрела (n=33) |
| Среднедневное САД: до лечения после лечения Δ | 158,0±2,14 129,1±1,73* -28,9±2,57* |
| Среднедневное ДАД: до лечения после лечения Δ | 96,5±1,18 76,9±1,34** -19,6±1,19** |
| Средненочное САД: до лечения после лечения Δ | 139,4±4,19 119,4±2,49* -20,0±3,35* |
| Средненочное ДАД: до лечения после лечения Δ | 85,8±2,44 69,8±3,29* -15,0±2,92* |
| Среднесуточное САД: до лечения после лечения Δ | 152,3±2,29 125,0±1,24* -27,3±2,74* |
| Среднесуточное ДАД: до лечения после лечения Δ | 94,0±1,96 77,8±1,57* -16,2±1,92* |
Анализ по ВАШ памяти и внимания выявил достоверное (р<0,001) улучшение в процессе лечения Нолипрелом А или Нолипрелом А форте субъективного восприятия больными АГ состояния указанных КФ. Так, исходно по шкале ВАШ «Память» значения составили 68,4+4,54 мм, тогда как в конце периода наблюдения - 82,7+2,78 мм, по шкале ВАШ «Внимание» - соответственно 39,3+3,15 и 72,4+5,67 мм. Безусловно, это означает улучшение самочувствия больных, качества их жизни, а следовательно, будет способствовать увеличению приверженности лечению.
На фоне лечения Нолипрелом А и Нолипрелом А форте отмечено также увеличение объема непосредственной слухо-речевой памяти (субтест Векслера № 5) с 13,4 до 16,9 балла (р<0,05) и концентрации внимания (субтест Векслера № 7) с 43,4 до 69,5 балла (р<0,01).
Таким образом, применение Нолипрела А/Нолипрела А форте в качестве средства антигипертензивной терапии 1-й линии у больных АГ с высоким и очень высоким риском сердечно-сосудистых осложнений позволяет не только добиться целевого уровня АД, в том числе в большом проценте случаев (по данным СМАД), но и благодаря его огранопротективным, в частности церебропротективным, свойствам значительно снизить риск сердечно-сосудистых осложнений и смертность. Выявленное положительное влияние препарата на КФ, кроме того, повышает качество жизни пациентов с АГ и способствует увеличению их приверженности лечению.
Недавно появилась новая дозировка Нолипрела А Би-форте - фиксированная комбинация полных доз периндоприл аргинина 10 мг и индапамида 2,5 мг. Эта комбинация рекомендуется в первую очередь больным, не достигшим контроля АД на фоне приема 2 антигипертензивных препаратов, включая диуретик, вместо ранее проводимой терапии. Такое лечение будет способствовать не только улучшению контроля за уровнем АД, но и позволит в полной мере реализовать органопротективный потенциал и благоприятное влияние на прогноз (снижение смертности) этой фиксированной комбинации.
Литература
Cognitive impairments in arterial hypertension and possibiliies of their correction
Professor O. Ostroumova, MD; K. Reznlkova
Moscow State Institute of Medicine and Dentistry The detection, diagnosis, and prognostic value of cognitive disorders (CD) are considered in arterial hypertension. The data of the PROGRESS study of the impact of antihypertensive therapy on the risk of dementia and CD are analyzed in detail. The paper gives the results of the authors' studies of the efficacy of Noliprel /V NoliprelA forte in lowering blood pressure and improving cognitive functions.
Keywords: arterial hypertension, 24-hour blood pressure monitoring, cognitive impairments, antihypertensive therapy, fixed-dose combinations of antihypertensive agents, perindopril, indapamide.
