Динамика вариабельности ритма сердца и желудочковой эктопической активности у больных хронической сердечной недостаточностью ишемической этиологии на фоне терапии ивабрадином
Статьи Опубликовано в журнале:
«Российский кардиологический журнал» № 6 (98), 2012г.
Суровцева М. В., Козиолова Н. А., Чернявина А. И.
ГБОУ ВПО Пермская государственная медицинская академия им. ак. Е. А. Вагнера Минздравсоцразвития России, Пермь, Россия.
Цель. Оценить динамику вариабельности ритма сердца (ВРС) и желудочковой эктопической активности на фоне терапии ивабрадином в комплексном лечении больных хронической сердечной недостаточностью (ХСН) ишемической этиологии.
Материал и методы. Обследовано 90 больных ХСН и стабильной стенокардией. В зависимости от антиишемической терапии пациенты были рандомизированы на 3 равные группы: 1-я группа – пациенты, получавшие периндоприл и ивабрадин в комплексной терапии, 2-я группа – получавшие периндоприл, бисопролол и ивабрадин, 3-я группа – пациенты, получавшие периндоприл и бисопролол. Длительность терапии составила 6 месяцев. До и после лечения оценивали показатели вариабельности ритма сердца (среднюю суточную частоту сердечных сокращений (ЧСС), SDNN, триангулярный индекс (HRVti) и средневзвешенную вариацию ритмограммы (СВВР)); среднесуточную длительность интервала QT, QTc, дисперсию интервала QTс (QTсd) и частоту желудочковой экстрасистолии (ЖЭ).
Результаты. На фоне лечения отмечено достоверно большее снижение среднесуточной ЧСС в 1 и 2 группах больных по сравнению с 3 группой (рmgmg1-2=0,091). В 3 группе СВВР также увеличилась достоверно меньше, чем в 1 и 2 группах больных (рmg1-2=0,065). HRVti увеличился во 2 группе достоверно больше, чем в 1 и 3 группах (рmgmg Заключение. Включение ивабрадина в комплексную терапию больных ХСН и стабильной стенокардией обеспечило благоприятное влияние на ВРС при отсутствии достоверных изменений среднесуточных показателей QTс и QTcd и умеренный антиаритмический эффект в отношении желудочковой экстрасистолии.
Ключевые слова: сердечная недостаточность, вариабельность ритма сердца, желудочковая эктопическая активность, комплексное лечение, ивабрадин.
Несмотря на успехи, достигнутые в лечении ишемической болезни сердца (ИБС) и хронической сердечной недостаточности (ХСН), эти заболевания по-прежнему остаются наиболее частыми причинами потери трудоспособности и смертности. ИБС, особенно в сочетании с артериальной гипертензией (АГ), является основной причиной развития и прогрессирования ХСН в России и во всем мире, частота которой неуклонно увеличивается в последнее время [1].
Снижение вариабельности ритма сердца (ВРС) у больных ИБС и ХСН позволяет не только подтвердить дисбаланс вегетативной нервной системы при данной сочетанной патологии, но и определить прогноз больных, особенно в отношении внезапной кардиальной смерти, инфаркта миокарда, прогрессирования сердечной недостаточности [2]. В настоящее время уделяется большое внимание изучению не только известных показателей ВРС, таких как SDNN, но и «новых» параметров – таких, как средневзвешенная вариация ритмограммы (СВВР).
Частота, особенности и негативное прогностическое значение желудочковой эктопической активности при ИБС хорошо изучены в многочисленных исследованиях. Известно, что развитие ХСН у больных ИБС значительно увеличивает частоту и тяжесть желудочковых нарушений ритма [3]. При этом использование многих антиаритмических препаратов для подавления аритмий при наличии ХСН, особенно III–IV функционального класса (ФК), противопоказано в силу их выраженного кардиодепрессивного действия и риска развития неблагоприятных сердечно-сосудистых событий [4]. Одним из негативных побочных эффектов антиаритмиков III класса, которые могут быть использованы при ХСН при наличии симптомных желудочковых нарушений ритма, ограничивающих их применение, являются удлинение интервала QTc и среднесуточной дисперсии QTc.
Поэтому в настоящее время продолжается активный поиск препаратов для лечения больных ИБС в сочетании с коморбидной патологией, которые, наряду с антиишемическим эффектом, оказывали бы лечебный эффект в отношении ХСН при хорошем профиле переносимости и безопасности, прежде всего – в отношении желудочковых нарушений ритма.
Tаблица 1
Сравнительная клинико-анамнестическая характеристика больных по группам (n=90)
| Показатель | 1 группа (n=30) | 2 группа (n=30) | 3 группа (n=30) | р1–2 | р2–3 | р1–3 | р mg |
|---|---|---|---|---|---|---|---|
| Средний возраст (год) | 55,7±4,8 | 54,9±5,6 | 57,5±4,8 | 0,555 | 0,058 | 0,152 | 0,134 |
| Пол, муж, абс. / % | 21/70,0 | 18/60,0 | 14/46,6 | 0,866 | 0,724 | 0,466 | 0,640 |
| Пол, жен, абс. / % | 9/30,0 | 12/40,0 | 16/53,4 | 0,756 | 0,347 | 0,692 | 0,456 |
| Продолжительность стенокардии, годы Ме [LQ; UQ] | 6,2 [2,4;8,9] | 6,6 [2,8;10,5] | 6,4 [2,1;11,8] | 0,456 | 0,723 | 0,748 | 0,784 |
| Продолжительность ХСН, годы Ме [LQ; UQ] | 6,6 [3,1;12,6] | 6,8 [4,5;10,0] | 6,7 [4,8;8,9] | 0,720 | 0,851 | 0,854 | 0,934 |
| Инфаркт миокарда в анамнезе, абс. / % | 12/40,0 | 13/43,3 | 9/30,0 | 0,944 | 0,631 | 0,756 | 0,753 |
| Средний ФК стенокардии, Ме [LQ; UQ] | 2,2 [1,8;2,6] | 2,3 [1,9;2,7] | 2,3 [1,8;2,7] | 0,278 | 0,772 | 0,446 | 0,563 |
| Средний ФК ХСН, Ме [LQ; UQ] | 2,4 [2.0;2,6] | 2,5 [2,1;2,7] | 2,5 [2,0;2,7] | 0,645 | 0,701 | 0,723 | 0,686 |
| Курящие пациенты абс. / % | 12/40,0 | 10/33,3 | 7/23,3 | 0,908 | 0,713 | 0,461 | 0,604 |
| ИMT, кг/м | 32,1±9,8 | 30,5±11,1 | 29,2±10,7 | 0,556 | 0,646 | 0,278 | 0,568 |
| Общий холестерин, ммоль/л | 6,2+1,6 | 6,4+1,8 | 6,3+1,5 | 0,651 | 0,816 | 0,804 | 0,781 |
| Наследственность по ИБС, абс. / % | 16/53,3 | 12/40,0 | 15/50,0 | 0,692 | 0,804 | 0,940 | 0,817 |
| СД 2 типа, абс. / % | 1/3,4 | 2/6,7 | 1/3,4 | 0,978 | 0,978 | 0,472 | 0,789 |
| АГ, абс/% | 28/93,3 | 27/90,0 | 25/83,3 | 0,929 | 0,839 | 0,764 | 0,812 |
| ХОБЛ, абс / % | 3/10,0 | 4/13,3 | 2/6,7 | 0,967 | 0,726 | 0,971 | 0,846 |
| Атеросклероз артерий нижних конечностей, абс./% | 2/6,7 | 3/10,0 | 2/6,7 | 0,971 | 0,971 | 0,606 | 0,788 |
| Атеросклероз сонных артерий, абс. / % | 1/3,3 | 3/10,0 | 2/6,6 | 0,651 | 0,971 | 0,978 | 0,625 |
Примечание: pmg – p multigroup – критерий множественного межгруппового сравнения.
Сокращения: ФК – функциональный класс, ХСН – хроническая сердечная недостаточность; ИМТ – индекс массы тела, ИБС – ишемическая болезнь сердца, АГ – артериальная гипертония, СД – сахарный диабет, ХОБЛ – хроническая обструктивная болезнь легких.
Исследования последних лет продемонстрировали не только высокую клиническую антиангинальную и антиишемическую эффективность нового препарата – ивабрадина – у больных стабильной стенокардией, но и показали его позитивное влияние на прогноз больных ИБС. Ивабрадин реализует свой антиишемический и антиангинальный эффект за счет ингибирования If-каналов клеток синусового узла, обеспечивая урежение ЧСС. На основании результатов многоцентрового клинического исследования SHIFT (the Systolic Heart Failure Treatment with the I (f) Inhibitor Ivabradine Trial) было обнаружено, что у больных хронической сердечной недостаточностью (ХСН), в том числе более чем у 50% ишемической этиологии с фракцией выброса левого желудочка менее 35% и ЧСС в покое более 70 ударов в минуту, на фоне приема ивабрадина отмечалось достоверное снижение частоты смертельных исходов от сердечнососудистых причин и количества госпитализаций в связи с усугублением течения ХСН [5].
В связи с этим, изучение патогенетических механизмов влияния современных лекарственных препаратов, в том числе ивабрадина, на течение и прогноз больных ИБС и ХСН, возможно, связанных с изменением ВРС или желудочковой эктопической активности, является актуальной и перспективной задачей кардиологии, требующей решения.
Цель исследования – оценка динамики вариабельности ритма сердца (ВРС) и желудочковой эктопической активности на фоне терапии ивабрадином в комплексном лечении больных хронической сердечной недостаточностью (ХСН) ишемической этиологии.
Материал и методы
Проведено сравнительное открытое клиническое исследование. Обследовано 205 пациентов стабильной стенокардией II–III ФК. Из них выделена когорта больных с ХСН II–III ФК – 90 человек. Средний возраст больных составил 56,2±6,4 лет, среди них 58,8% (53) мужчин, 41,1% (37) женщин. Продолжительность стенокардии среди обследованных составила 5,9±2,6 года, средний ФК – 2,27±0,37. Инфаркт миокарда в анамнезе выявлен у 37,7% (34) больных. Продолжительность ХСН – 6,2+2,1 лет.
Средний ФК ХСН составил 2,52±0,08. Критериями включения в исследование являлись: возраст от 30 до 65 лет; наличие стабильной стенокардии II–III ФК, подтвержденной клинически и/или диагностическими тестами; наличие ХСН II–III ФК, подтвержденной клинически в сочетании с дисфункцией миокарда левого желудочка по эхокардиоскопии или увеличением уровня N-терминального концевого фрагмента мозгового натрий-уретического пептида более 400 пг/дл согласно Рекомендациям Европейского общества кардиологов (2008); синусовый ритм на ЭКГ с ЧСС 70 ударов в минуту и более; получение информированного согласия на участие в исследовании. Критериями исключения из исследования были следующие: острый коронарный синдром; ХСН не ишемической этиологии; вторичная стенокардия; митральный стеноз; митральная и аортальная регур-гитация более II степени; тахикардия более 100 ударов в минуту в покое; другие клинически значимые сопутствующие заболевания и состояния, требующие постоянного лечения; онкологические заболевания; острые воспалительные и инфекционные заболевания; противопоказания к назначению ингибиторов ангиотензинпревращающего фермента (ИАПФ) и ивабрадина; деменция, психические заболевания и иные причины, препятствующие подписанию информированного согласия и дальнейшему адекватному контакту с больным в период наблюдения.
Tаблица 2
Показатели вариабельности ритма сердца, среднесуточной ЧСС, среднесуточных интервалов QT, QTc, QTсd
до лечения по группам обследуемых (n=90)
| Показатель | 1 группа (n=30) | 2 группа (n=30) | 3 группа (n=30) | р1–2 | р2-3 | р1–3 | рmg |
|---|---|---|---|---|---|---|---|
| SDNN, мс | 111,57±22,91 | 112,26±18,01 | 114,20±21,17 | 0,899tdd | 0,702 | 0,650 | 0,880 |
| HRVti, усл. ед. | 30,56±4,56 | 29,72±3,34 | 28,97±4,12 | 0,408 | 0,453 | 0,165 | 0,406 |
| CBBP, мс | 776,0±82,88 | 768,62±119,31 | 780,28±95,26 | 0,782 | 0,674 | 0,676 | 0,396 |
| Среднесуточный интервал QT, мс | 364,01±2,95 | 363,41±18,60 | 369,44±18,52 | 0,885 | 0,213 | 0,193 | 0,244 |
| Среднесуточный QTc, мс | 409,47±11,72 | 409,21±13,51 | 409,41±15,92 | 0,937 | 0,958 | 0,980 | 0,136 |
| Среднесуточная QTсd, мс | 29,8±1,77 | 29,60±1,40 | 29,80±2,01 | 0,629 | 0.656 | 1,0 | 0,529 |
| Среднесуточная ЧСС, уд/мин | 82,0±5,9 | 82,4±5,1 | 81,8±6,8 | 0,780 | 0,481 | 0,904 | 0,810 |
Примечание: pmg – p multigroup – критерий множественного межгруппового сравнения.
Tаблица 3
Bиды желудочковых нарушений ритма сердца по группам обследуемых до лечения (n=90)
| Показатель | 1 группа | 2 группа | 3 группа | р1–2 | р2-3 | р1–3 | рmg |
|---|---|---|---|---|---|---|---|
| Общее количество ЖЭ за сутки | n=18 1253,2±437,7 | n=19 1329,5±561,7 | n=15 1134,3±371,2 | 0,761 | 0,320 | 0,211 | 0,644 |
| Среднее количество единичных ЖЭ на одного больного | n=10 19,5±10,8 | n=11 22,0±10,1 | n=9 37,1±8,85 | 0,341 | 0,258 | 0,044 | 0,043 |
| Среднее количество парных ЖЭ на одного больного | n=4 12,75±3,45 | n=5 10,48±1,7 | n=4 9,1±0,82 | 0,754 | 0,806 | 0,110 | 0,058 |
| Среднее количество политопных ЖЭ на одного больного | n=4 99,4±18,9 | n=4 99,8±9,51 | n=4 99,2±8,56 | 1,0 | 0,020 | 0,014 | 0,025 |
Примечание: pmg – p multigroup – критерий множественного межгруппового сравнения.
Сокращение: ЖЭ – желудочковая экстрасистола.
В зависимости от выбора терапии пациенты были разделены на 3 равные группы: первая группа – пациенты, получавшие в комплексной терапии периндоприл (средняя доза – 5,9±1,8 мг в сутки) и ивабрадин (средняя доза – 11,6±1,9 мг в сутки), вторая группа – получавшие периндоприл (средняя доза – 5,7±1,6 мг в сутки), бисопролол (средняя доза –7,9±1,9 мг в сутки) и ивабрадин (средняя доза – 6,4±1,6 мг в сутки), третья группа – пациенты, получавшие периндоприл (средняя доза – 4,4±1,5 мг в сутки) и бисопролол (средняя доза – 7,2±1,6 мг в сутки). Достоверных различий между группами по использованию статинов, антиагрегантов, ситуационному использованию короткодействующих нитратов и препаратов для лечения ХСН не было выявлено. Длительность лечения составила 6 месяцев.
Всем пациентам до и после лечения было проведено суточное мониторирование (СМ) ЭКГ с помощью аппарата «Card (X)plore» («Meditech», Венгрия). По данным суточного мониторирования ЭКГ, оценивали следующие параметры: среднесуточная ЧСС; среднесуточный интервал QT (мс), корригированный интервал QTc (мс) и среднесуточная его дисперсия QTсd, желудочковая эктопическая активность в соответствии с классификацией B. Lown и M. Wolf (1971) в модификации M. Ryan et al. (1975), параметры вариабельности ритма сердца (SDNN – стандартное отклонение величин всех анализируемых интервалов NN за рассматриваемый период наблюдения, рефе-ренсные значения – 141±38 мс; HRVti – триангуляр-ный индекс интервальной гистограммы, референ-сные значения – 37±15 усл.ед;. СВВР – средневзвешенная вариация ритмограммы, референсные значения у лиц старше 40 лет – 1166 +322 мс).
Статистическую обработку полученных результатов осуществляли при помощи программы STATISTICA 6.0. Для количественных признаков были рассчитаны среднеарифметическое значение (M)± и среднеквадратичное отклонение среднего (М±sdd); медианы и нижнего и верхнего квартилей (Ме [LQ; UQ]). Для качественных признаков были рассчитаны абсолютная частота проявления признака (количество обследованных), частота проявления признака в процентах (%). Анализ вида распределения осуществлен с использованием критерия Шапиро-Уилка. Для ряда данных гипотеза о нормальности распределения была отвергнута. Для статистического сравнительного анализа данных трех групп при нормальном распределении использовали параметрические методы: для количественных показателей – однофакторный дисперсионный анализ (ANOVA), для качественных показателей – критерий χ2. Сравнение трех групп при ненормальном распределении по количественному показателю было проведено с помощью критерия Краскела-Уоллиса с поправкой Бонферрони p/3, по качественному признаку – при помощи критерия χ2. Критический уровень достоверности нулевой статистической гипотезы, свидетельствующий об отсутствии значимых различий или факторных влияний, принимали равным р ≤ 0,017.
Tаблица 4
Динамика желудочковых нарушений ритма сердца на фоне терапии по группам обследуемых (n=90)
| Параметр | 1 группа (n=30) | 2 группа (n=30) | 3 группа (n=30) | р1–2 | р2-3 | р1–3 | рmg |
|---|---|---|---|---|---|---|---|
| Δ общее количество ЖЭ за сутки,% | -33,00±0,64 | -33,50±0,36 | -7,50±0,17 | ||||
| Δ среднее количество единичных ЖЭ на одного больного,% | -18,6±5,3 | -16,0+6,1 | -14,1±7,7 | 0,083 | 0,294 | 0,011 | 0,029 |
| Δ среднее количество парных ЖЭ на одного больного,% | -30,0±3,4 | -28,1±4,1 | -2,7±1,6 | 0,056 | |||
| Δ среднее количество политопных ЖЭ на одного больного,% | -54,9±6,8 | -52,6±7,1 | -5,9±2,9 | 0,205 |
Примечание: рmg – достоверность различий между показателями в группах.
Сокращение: ЖЭ – желудочковая экстрасистола.
Результаты
Сравнительная клинико-анамнестическая характеристика больных по группам представлена в таблице 1.
Группа были сопоставимы по полу, возрасту, факторам риска ИБС, тяжести стенокардии и ХСН, структуре и тяжести сопутствующих заболеваний. У всех больных исходно отмечена низкая вариабельность ритма сердца: средняя величина SDNN составила 111,5±24,1 мс, HRVti – 28,8±9,1 усл. ед., СВВР – 782,9±109,7 мс. Достоверных различий показателей вариабельности ритма сердца, среднесуточной ЧСС, среднесуточных интервалов QT, QTc, QTсd по группам до лечения получено не было (табл. 2).
У 57,7% (52) пациентов выявлены желудочковые экстрасистолы (ЖЭ) по СМ ЭКГ. Из них у 33,3% (30) больных выявлены единичные ЖЭ, у 14,0% (13) пациентов – парные ЖЭ, у 13,3% (12) – обнаружены политопные ЖЭ (табл. 3).
На фоне комплексной терапии ХСН, по данным СМ ЭКГ, отмечено значимое снижение среднесуточной ЧСС в первой и второй группах больных, при этом урежение ЧСС не сопровождалось появлением побочных эффектов (р1–2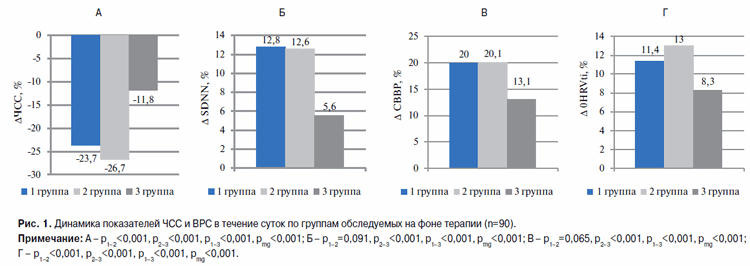
В третьей группе среднесуточная ЧСС снизилась достоверно меньше, чем в первой группе больных(р1–3mg1–32–31–2=0,091). В группе периндоприла и бисопролола СВВР также увеличился достоверно меньше, чем в группе больных, получающих ивабрадин и перин-доприл (р1–32–31–2=0,065). HRVti увеличился во второй группе достоверно больше, чем в первой (р1–22–31–3На фоне 6-месячного лечения отмечено снижение желудочковой эктопической активности во всех группах обследуемых (табл. 4).
Общее количество ЖЭ за сутки уменьшилось во второй группе достоверно больше, чем в первой (р1–322–31–3=0,011). Первая и вторая группы, а также вторая и третья группы по среднему количеству единичных ЖЭ на одного больного достоверно не различались. В третьей группе среднее количество парных и политопных ЖЭ на одного больного уменьшилось достоверно меньше, чем во второй (р2–31–3На фоне комплексной терапии с включением ивабрадина отмечено достоверное возрастание среднесуточного интервала QT в первой и второй группах по сравнению с третьей группой (р1–32–3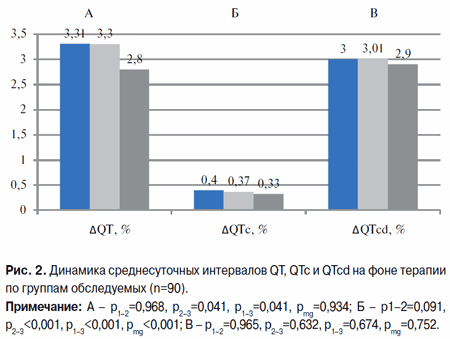
Обсуждение
По результатам нашего исследования у всех больных стабильной стенокардией II–III ФК и ХСН исходно выявлены: повышение среднесуточной ЧСС, низкая ВРС, у 57,7% пациентов – наличие желудочковой эктопической активности. В многочисленных исследованиях показано, что при развитии и прогрессировании ХСН повышение ЧСС является ведущим симптомом заболевания, в основе которого лежит дисбаланс нейрогуморальных систем [6]. Повышение ЧСС играет важную роль в снижении ВРС у больных ХСН [7]. Хорошо известно, что у больных ИБС при формировании ХСН, особенно при снижении фракции выброса левого желудочка, возрастает частота желудочковой эктопической активности с возникновением жизнеугрожающих нарушений ритма [8].
Наличие эктопической желудочковой активности и снижение ВРС у больных ИБС и ХСН связывают с непосредственным изменением электрофизиологических свойств миокарда вследствие его ремоделирования и фиброза, а также опосредованно – за счет снижения коронарного резерва, систолической и диастолической дисфункции, активации симпатической нервной системы. Большое значение в развитии жизнеугрожающих желудочковых нарушений ритма у больных ИБС и ХСН имеет длительность интервала QTc и его дисперсия в течение суток.
Доказано, что высокая ЧСС, снижение ВРС, наличие желудочковых аритмий у больных ИБС и ХСН являются предикторами неблагоприятного прогноза в плане развития внезапной кардиальной смерти, жизнеугрожающих нарушений ритма, инфаркта миокарда и других тромбоэмболических осложнений, острой сердечной недостаточности [9].
На фоне комплексной терапии ХСН с включением ивабрадина в нашем исследовании отмечено достоверное снижение среднесуточной ЧСС, благоприятная динамика показателей SDNN, HRVti и СВВР. Вероятно, действие ивабрадина на ВРС связано непосредственно с его механизмом снижения ЧСС в результате ингибирования If-каналов клеток синусового узла и уменьшения скорости медленной спонтанной диастолической деполяризации клетки, а также с опосредованным воздействием препарата на нейрогуморальные системы – прежде всего на РААС – за счет уменьшения экспрессии генов АПФ и АТ1-рецепторов к ангио-тензину II [10]. Известно также, что ивабрадин способен подавлять Ca2+-зависимую АТФ-азу в саркоплазматическом ретикулуме кардиомиоциотов у больных с постинфарктной сердечной недостаточностью, обеспечивая улучшение сократительной функции миокарда левого желудочка и, соответственно, снижение ЧСС.
При оценке динамики желудочковых нарушений ритма сердца в нашей работе было обнаружено, что при включении в терапию ивабрадина достоверно больше снижалось общее количество ЖЭ за сутки, уменьшалось среднее количество парных и политопных ЖЭ на одного больного. Известно, что в ремоделированном миокарде желудочков имеет место феномен “up-regulation” If тока и гиперэкспрессия HCN-каналов, которые рассматриваются как составная часть феномена «фетализации» фенотипа миокарда. Кардиопротективный эффект ивабрадина в отношении эктопической желудочковой активности, возможно, связан с устранением данного феномен, как одного из возможных механизмов аритмогенной активности желудочков [11]. В экспериментальной работе I. Koncz et al. было найдено, что ивабрадин с электрофизиологических позиций можно отнести с IC и III классу антиаримических препаратов по классификации Williams и Harrison (1983) [12]. Ряд авторов считают, что многие эффекты ивабрадина еще не изучены. Помимо снижения ЧСС, в некоторых исследованиях на животных получены плейотропные эффекты препарата, не связанные с его основным механизмом действия – такие, как иммуномодулилирующий, антиоксидантный, улучшение эндотелиальной дисфункции, антиатеросклеротический и другие [13]. Следует отметить важный момент, что применение ивабрадина в составе комплексной терапии у обследованных нами больных не сопровождалось такими негативными эффектами, которые проявляют антиаритмики III класса, как увеличение длительности QTc и QTcd в течение суток. Полученные нами результаты согласуются с данными литературы, что делает препарат ивабрадин безопасным при применении у больных стабильной стенокардией и ХСН при наличии желудочковых нарушений ритма [14, 15].
Заключение
Включение ивабрадина в комплексную терапию больных стабильной стенокардией II–III ФК в сочетании с ХСН оказывает благоприятное влияние на ВРС, подавляет желудочковую эктопическую активность при отсутствии достоверных изменений среднесуточных показателей QTс и QTcd , что может реально повлиять на улучшение прогноза пациентов данной категории.
Dynamics of heart rate variability and ventricular ectopic heart failure
Surovtseva M. V., Koziolova N. A., Chernyavina A. I.
Academician E. A. Vagner Perm State Medical Academy, Perm, Russia.
Aim. In patients with chronic heart failure (CHF) of ischemic aetiology, to assess the dynamics of heart rate variability (HRV) and ventricular ectopic activity during the complex, ivabradine-including therapy. material and methods. In total, 90 patients with CHF and stable angina pectoris were examined. All participants were randomised into three equally sized groups: Group 1, receiving perindopril and ivabradine, as a part of the complex treatment; Group 2, receiving perindopril, bisoprolol, and ivabradine; and Group 3, receiving perindopril and bisoprolol. The therapy duration was 6 months. At baseline and in the end of the treatment phase, the following parameters were assessed: HRV measures (mean 24-hour hear rate (HR), SDNN, triangular index (HRVti), and mean weighted variation of rhythmogram (MWVR)); mean 24-hour QT, QTc, QTc dispersion (QTcd), and ventricular extrasystolia (VE).
Results. The treatment was associated with a significantly greater reduction of mean 24-hour HR in Groups 1 and 2 vs. Group 3 (p Conclusion. Including ivabradine in the complex therapy of patients with CHF and stable angina pectoris was associated with improved HRV, no marked QTc or QTcd changes, and a moderate preventive effect on VE.
Russ J Cardiol 2012, 6 (98): 60-65
Key words: heart failure, heart rate variability, ventricular ectopic activity, complex treatment, ivabradine.
Сведения об авторах:
Суровцева М. В. – к. м.н., доцент кафедры внутренних болезней педиатрического и стоматологического факультетов,
Козиолова Н. А.* – д. м.н., профессор, заведующая кафедрой внутренних болезней педиатрического и стоматологического факультетов,
Чернявина А. И. – к. м.н., ассистент кафедры внутренних болезней педиатрического и стоматологического факультетов.
Список сокращений:
АГ – артериальная гипертензия, Литература
1. Fomin I. V. Epidemiology of chronic heart failure in Russian Federation. In. Belenkov Yu. N., Ageev F. T. , Arutjunov G. P. , Vasyuk Yu. A. Chronic heart failure. Moscow: Geotar-Media; 2010. pp. 7–77. Russian (Фомин И. В. Эпидемиология хронической сердечной недостаточности в Российской Федерации. В кн.: Хроническая сердечная недостаточность (Беленков Б. Н., Агеев Ф. Т. , Арутюнов Г. П., Васюк Ю. А.) М.: ГЕОТАР-Медиа 2010,7–77.
ВРС – вариабельность ритма сердца,
ЖЭ – желудочковая экстрасистолия,
ИАПФ – ингибиторы ангиотензинпревращающего фермента,
ИБС – ишемическая болезнь сердца,
РААС – ренинангиотен-зинальдостероновая система,
СВВР – средневзвешенная вариация ритмограммы,
ФК – функциональный класс, ХСН – хроническая сердечная недостаточность,
ЧСС – частота сердечных сокращений,
ЭКГ – электрокардиограмма,
HRVti – триангулярный индекс,
SHIFT – the Systolic Heart Failure Treatment with the I (f) Inhibitor Ivabradine Trial.
2. Huikuri H. V. , Stein P. K. Clinical application of heart rate variability after acute myocardial infarction. Front Physiol 2012; 3: 41.
3. Liu Y. H., Su J. Y., Wang L. J. et al. Impact of potentially lethal ventricular arrhythmias on long-term outcome in patients with chronic heart failure. Chin Med J (Engl) 2012; 125 (4):563–8.
4. Coons J. C., Plauger K. M., Seybert A. L. et al. Worsening heart failure in the setting of dronedarone initiation. Ann Pharmacother 2010; 44 (9):1496–500.
5. Swedberg K., Komajda M., Behm M. et al. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010; 376 (9744):875–85.
6. Tardif J. C. Heart rate as a treatable cardiovascular risk factor. Br Med Bull 2009; 90:71–84.
7. Tanindi A., Olgun H., Celik B. et al. Heart rate variability in patients hospitalized for decompensated diastolic heart failure at admission and after clinical stabilization. Future Cardiol 2012; 8 (3): 473–82.
8. Agarwal S. K., Simpson R. J. Jr., Rautaharju P. et al. Relation of ventricular premature complexes to heart failure (from the Atherosclerosis Risk In Communities (ARIC) Study). Am J Cardiol 2012; 109 (1):105–9.
9. Kapoor J. R., Heidenreich P. A. Role of heart rate as a marker and mediator of poor outcome for patients with heart failure. Curr Heart Fail Rep 2012; 9 (2):133–8.
10. Ulu N., Henning R. H., Goris M. et al. Effects of ivabradine and metoprolol on cardiac angiogenesis and endothelial dysfunction in rats with heart failure. J Cardiovasc Pharmacol 2009; 53 (1):9–17.
11. Hofmann F. , Fabritz L., Stieber J. et al. Ventricular HCN channels decrease the repolarization reserve in the hypertrophic heart. Cardiovasc Res 2012;95 (3):317–26.
12. Koncz I., Szйl T. , Bitay M. et al. Electrophysiological effects of ivabradine in dog and human cardiac preparations: potential antiarrhythmic action. Eur J Pharmacol 2011; 668 (3):419–26.
13. Speranza L., Franceschelli S., Riccioni G. The biological effects of ivabradine in cardiovascular disease. Molecules 2012; 17 (5):4924–35.
14. Lуpez-Bescуs.L, Filipova S., Martos R. on behalf of the studyinvestigators. Long-Term Safety and Efficacy of Ivabradine in Patients with Chronic Stable Angina. Cardiology 2007; 108:387–96.
15. Becher P. M., Lindner D., Miteva K. et al. Role of heart rate reduction in the prevention of experimental heart failure: comparison between If-channel blockade and β-receptor blockade. Hypertension 2012; 59 (5):949–57.
