Уровень преднагрузки и варианты гемодинамики у пациентов с острым инфарктом миокарда, осложненным кардиогенным шоком
СтатьиОпубликовано в журнале:
"Российский кардиологический журнал"
»» N 5 2004
Шевченко И.И.
Городская клиническая больница №10 («Электроника»), Воронеж
Резюме
В работе изучены параметры центральной гемодинамики у больных с острым ИМ, ослложненным кардиогенным шоком. Контрольная группа – 315 пациентов с острым инфарктом миокарда, отобранные методом случайной выборки. Основная группа – 306 пациентов с кардиогенным шоком (КШ). Уровень преднагрузки миокарда левого желудочка, определяемый по конечному диастолическому объему (КДО), оказался неоднородным. С учетом уровня преднагрузки, пациенты разделены на группы: со сниженной, нормальной, повышенной и резко повышенной преднагрузкой. При КШ значительно возрастает число пациентов с резко повышенным (КДО>200 см3) уровнем преднагрузки. Определена зависимость между значениями КДО и летальностью пациентов с КШ.
Ключевые слова: кардиогенный шок, центральная гемодинамика, конечный диастолический объем, уровень преднагрузки.
Ведение больных в клиниках неотложной кардиологии предполагает постоянный контроль объемных параметров центральной гемодинамики (ЦГ), что имеет несомненное значение для правильной диагностики и контроля над адекватностью проводимой терапии [1, 3, 7]. Особо значимо определение гемодинамического статуса в случае осложненного течения острого инфаркта миокарда – в частности, при кардиогенном шоке [11]. Проводимые ультразвуковым методом исследования обычно включают определение конечного диастолического (КДО) и конечного систолического объемов (КСО), ударного объема (УО), фракции выброса (ФВ) [12]. В ургентных ситуациях параметры ЦГ мониторируются при катетеризации правых отделов сердца [1, 7], определяемое при этом давление заклинивания в легочной артерии (ДЗЛА) приравнивается к конечному диастолическому давлению в левых отделах сердца [3]. В то же время, ряд авторов отмечает тесную корреляцию между конечным диастолическим давлением в левых отделах сердца (КДД) и конечным диастолическим объемом (КДО) левого желудочка сердца [8, 9]. Катетеризация правых отделов сердца, как любая инвазивная процедура, может сопровождаться осложнениями и, кроме того, предусматривает наличие высококлассных специалистов, что зачастую недоступно для большинства учреждений практического здравоохранения. Представляется актуальным новый подход в неинвазивном определении параметров ЦГ, позволяющий улучшить диагностику состояния пациентов в неотложной кардиологии, учесть уровень преднагрузки, а также обеспечить постоянный контроль над адекватностью проводимой терапии.
Материал и методы
Клинические исследования проводились на базе кардиологического отделения городской клинической больницы №10 («Электроника»), работающего круглосуточно в режиме скорой помощи и обслуживающего два крупных района г. Воронежа. В качестве контрольной группы были взяты 315 пациентов с ОИМ, не осложненным кардиогенным шоком. Отбор осуществлялся методом случайной выборки. Группу составили 175 мужчин (55,46%) и 140 женщин (44,54%). Средний возраст мужчин – 62,88 лет, женщин – 70,81 лет, средний возраст во всей группе – 66,42 года. Локализация ОИМ в указанной группе была следующей: трансмуральный передний – 48 пациентов (15,22%), крупноочаговый передний – 82 пациента (26,09%), крупноочаговый передний с распространением на боковые отделы – 29 пациентов (9,24%), мелкоочаговый и интрамуральный передний – 42 пациента (13,33%), трансмуральный и крупноочаговый нижний с распространением на заднебазальные отделы – 74 пациента (23,56%), нижний мелкоочаговый – 18 пациентов (5,67%), субэндокардиальный – 19 (5,98%). Впервые возникший ОИМ у 266 пациентов (84,44%), повторный – у 49 пациентов (15,56%).
Основную группу составили 306 пациентов с кардиогенным шоком, из них 112 мужчин (36,68%), 194 женщины (63,32%), возраст от 42 до 84 лет, средний возраст – 68,58 лет. Первичный ОИМ у 172 пациентов (56,08%), повторный – у 134 (44,01%). Локализация ОИМ следующая: передний трансмуральный и крупноочаговый – 164 пациента (53,72%), нижний трансмуральный и крупноочаговый с распространением на заднебазальные отделы – 53 (17,25%), передний с распространением на заднюю стенку – 44 (14,5%), нижний с распространением на правый желудочек – 30 (9,8%), циркулярный с распространением на правый желудочек – 14 (4,7%). Параметры центральной гемодинамики определялись неинвазивно электрокардиографическим компьютерным анализатором «Бианкор» [4,5], позволяющим определять КДО, КСО, УО, ФВ, а также целый ряд необъемных параметров. В контрольной группе параметры определены у 105 пациентов, в основной – у 103 пациентов.
Статистическая обработка материала осуществлялась с использованием программы STATISTICA (Статистический анализ и обработка данных в среде Windows) [2], позволившей провести многофакторный статистический анализ. Учитывая то, что распределение большинства анализируемых переменных оказалось ненормальным, использовали методы непараметрической статистики (медиана, квартили, ранговые критерии Манна-Уитни, Вилкоксона, критерий Колмогорова-Смирнова). С помощью модуля «Анализ длительности жизни» произведена оценка функции выживаемости (25% и 75% квартили, а также медиана выживаемости с построением экспоненциальной модели) [6].
Результаты
КДО в контрольной группе пациентов имел следующие значения: 803100 см3 – 8 пациентов (7,61%), 101-150 см3 – 43 пациента (40,95%), 151-200 см3– 39 пациентов (37,14%), больше 200 см3 – 15 пациентов (14,29%) (рис. 1).
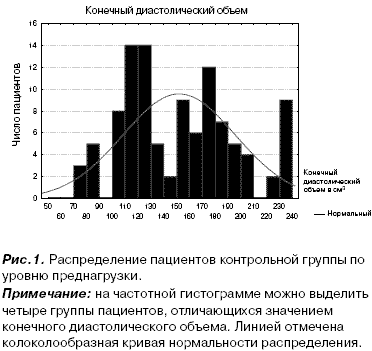
Дальнейший анализ параметров центральной гемодинамики, проведенный нами [10], выявил определенную особенность. С учетом значения КДО, отражающего уровень преднагрузки, были выделены следующие гемодинамические варианты в контрольной и основной группах (табл.1).
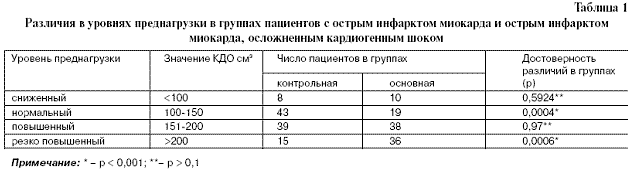
Группа пациентов со сниженной преднагрузкой (КДО<100 см3) оказалась самой малочисленной и в контрольной группе (7,61%), и в основной группе (9,7%); более того, различия в численности этих групп оказались недостоверными (р>0,4). Число пациентов с нормальным уровнем преднагрузки (150>КДО>100см3) в группе с КШ значительно снизилось по сравнению с контрольной группой (с 40,95% до 18,09%), уровень различий высоко значим (р< 0,001).
Число пациентов с повышенным уровнем преднагрузки и в контрольной, и в основной группе достоверно не различалось (37,14% и 36,89%, соответственно) (р>0,9). Высоко значимым (р<0,001) был уровень различий в группах с резко повышенной преднагрузкой (14,29% и 34,95%, соответственно). Таким образом, кардиогенный шок ведет к резкому повышению уровня преднагрузки миокарда левого желудочка.
Дополнительные исследования, проведенные с группой пациентов гастроэнтерологического отделения (98 человек) и группой амбулаторных больных кардиологического профиля (102 человека) с использованием ультразвукового метода и электрокардиографического компьютерного анализатора, подтвердили возможность выделения гемодинамических вариантов у всех пациентов (рис. 2).
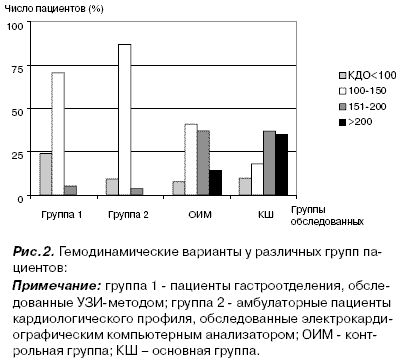
Следует отметить, что в группах пациентов, не имеющих острой коронарной патологии (первая и вторая группы) отсутствовал резко повышенный уровень преднагрузки, в то же время, наблюдался значительный рост удельного веса варианта с повышенной и резко повышенной преднагрузкой в группе пациентов с ОИМ и, особенно, с КШ, что подтверждается и ультразвуковым методом, и методом трансформации ЭКС.
Обсуждение
С целью учета особенностей течения, лечения и прогноза сочли целесообразным произвести разделение пациентов в обеих группах по типам гемодинамики. Анализ соотношения КДО, КСО, УО, ФВ и МО позволил выделить в контрольной группе пациентов следующие типы гемодинамики: гипокинетический – 60,44%, эукинетический – 29,33%, гиперкинетический – 10,22%. Критерии гипокинетического типа гемодинамики: ФВ менее 60%, УО менее 70 см3, при этом КДО, КСО, МО могут быть снижены, соответствовать норме или быть повышенными.
Подобный тип гемодинамики встречается наиболее часто при ОИМ и свидетельствует об обширности острого повреждения и/или выраженности рубцовых изменений в сердечной мышце. Нормальное соотношение КДО, КСО, УО, ФВ и МО свидетельствует о наличии у данного пациента эукинетического типа гемодинамики. Данный тип гемодинамики наблюдался в контрольной группе при первичных мелкоочаговых ОИМ, как правило, протекавших без осложнений или же с незначительными осложнениями, не приведшими к существенному нарушению гемодинамики.
У незначительного числа пациентов в связи с индивидуальными особенностями гемодинамики наблюдался гиперкинетический тип, критериями которого являются: ФВ более 70%; при этом УО может быть как нормальным, так и повышенным или сниженным, а МО нормален или снижен. Гиперкинетический тип гемодинамики, являясь вариантом нормы, исходно является гемодинамическим вариантом со сниженными резервными возможностями, а повреждение сердечной мышцы при ОИМ приводит к еще большему увеличению потребности миокарда в кислороде. В результате растет риск расширения зоны повреждения сердечной мышцы и, в конечном счете, ухудшается прогноз [10]. Кроме этих, обусловленных конституциональными особенностями случаев, гиперкинетический тип может быть транзиторной реакцией на выраженный болевой синдром, а также на неадекватное обезболивание.
Взаимоотношения типов и вариантов гемодинамики показывает, что при кардиогенном шоке гипокинетический тип гемодинамики преимущественно сочетается с вариантами с повышенной и резко повышенной преднагрузкой [10]. Анализ достоверности различий параметров центральной гемодинамики в основной и контрольной группе выявил высокий их уровень при всех вариантах гемодинамики, кроме того выявлена определенная зависимость роста КДО, КСО с показателями УО И ФВ (табл. 2).
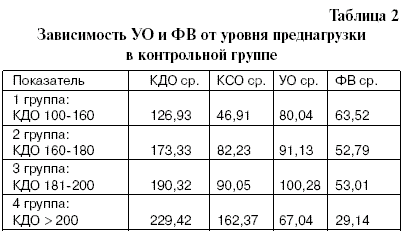
Увеличение уровня преднагрузки во второй группе на 46,4 см3 (36,55%) сопровождается ростом УО на 11,09 см3 (13,85%), и, в то же время, снижением интегрированного показателя насосной функции миокарда левого желудочка (ФВ) на 10,73%. Дальнейший рост преднагрузки в третьей группе (увеличение КДО на 63,39 см3 – 49,94%) все еще сопровождается ростом ударного объема до 100,28 см3, поэтому ФВ практически остается неизменной – 53,01%. Увеличение КДО до 200 см3 и более в третьей и четвертой группе ведет к снижению УО на 13 см3 (16,24%) и к еще более существенному снижению ФВ – на 34,38%, что свидетельствует о существенном нарушении систолической функции миокарда. Приведенные данные укладываются в закон Франка-Старлинга [8], согласно которому, с ростом преднагрузки происходит рост УО и ФВ, но эта зависимость сохраняется до определенного предела, а затем рост преднагрузки вызывает падение УО и ФВ вследствие истощения компенсаторных возможностей миокарда. В нашем примере увеличение преднагрузки до 200 см3 еще сопровождается ростом УО, однако в случае роста КДО свыше 200 см отмечается резкое снижение УО и еще более выраженное снижение ФВ, соответственно, 33,24 см3 и 23,87%. Следует отметить, что приведенные данные относятся к пациентам контрольной группы, у которых увеличение преднагрузки происходило постепенно в течение многих лет и было обусловлено ремоделированием, связанным с перенесенным ОИМ, артериальной гипертензией. Сравнительный анализ группы пациентов с кардиогенным шоком и контрольной группы пациентов с острым инфарктом миокарда, неосложненным кардиогенным шоком, проведенный с использованием непараметрических критериев (Mann-Whitney U test; Kolmogorov-Smirnov Test) [2,6] позволяет выявить существенные отличия параметров центральной гемодинамики. В группе пациентов с кардиогенным шоком, по сравнению с контрольной группой, отмечается прирост КДО, в среднем, на 19,7 см3 (12,74%) (U=848,5; р > 0,05), КСО – на 43,44 см3 (56,17%) (U=632,0; р < 0,05), ЦВД – на 10,7 см водного столба (133,75%) (р < 0,05), в то же время, снижены следующие показатели центральной гемодинамики: УО – на 23,73 см3 (30,59%) (U=421,5; р <0,001), ФВ – на 28,69% (U=454,5; р <0,001), СИ – на 0,73 л/м2 (23,47%) (р < 0,05). Значительно более выраженный прирост КСО, который, прежде всего, отражает состояние систолической функции левого желудочка, в основной группе, снижение ударного и минутного объемов и особенно значительное снижение ФВ, свидетельствуют о более существенном влиянии кардиогенного шока именно на систолическую функцию левого желудочка.
Клиническая значимость предложенного разделения пациентов на группы с учетом уровня преднагрузки заключается в том, что имеется определенная зависимость уровня летальности от уровня преднагрузки. Зависимость не носит линейного характера, максимальные цифры летальности отмечаются в группе пациентов со сниженным и резко повышенным уровнем преднагрузки (табл.3).
Различия летальности недостоверны при сравнении в группах с нормальной и повышенной преднагрузкой (р=0,58), в то же время, сравнение летальности в группах со сниженной и нормальной преднагрузкой оказалось значимым (р< 0,1). В группах с повышенной и резко повышенной преднагрузкой значимость выше (р< 0,05).
Выводы
1. При определении параметров центральной гемодинамики у пациентов можно выделить несколько вариантов уровня преднагрузки с учетом значения конечного диастолического объема.
2. Уровень преднагрузки увеличивается в зависимости от тяжести инфаркта миокарда; наиболее высокий уровень преднагрузки у пациентов с тяжелым кардиогенным шоком.
3. Летальность пациентов с кардиогенным шоком зависит от уровня преднагрузки, будучи максимальной в группе пациентов со сниженной и резко повышенной преднагрузкой.
Литература
1. Алперт Д., Френсис Г., Лечение инфаркта миокарда.3 М.: Практика,1994.3225 с.
2. Боровиков В.П., Боровиков И.П. STATISTICA. Статистический анализ и обработка данных в среде Windows. М: «Филинъ», 1998. 3 592 с.
3. Окороков А.Н. Лечение болезней внутренних органов. Т.3. Книга 1. Лечение заболеваний сердечно3сосудистой системы. Витебск, Белмедкнига,1998. - 445 с.
4. Сафонов М.Ю. Способ определения основных функциональных показателей миогемодинамики левого желудочка сердца. Патент 21074576 Россия, МПК6 А61в5/02, 5/0402. / № 97105501/ 14; -19989.
5. Сафонов М.Ю. Электрокардиографическая диагностика функционального состояния центральной гемодинамики Изд.ВГУ, Воронеж. 1998. - 101 с.
6. Стентон Г. Медико3биологическая статистика. М: Практика, 1999, 459 с.
7. Сыркин А.Л. Инфаркт миокарда. М.:МИА,1998. - 397 с.
8. Физиология человека. Том 3/ Под ред. Р. Шмидта и Г. Тевса. М.: «Мир», 1986.- 288 с.
9. Чазов Е.И.(ред.) Болезни органов кровообращения. 3 М.: Медицина,1997.- 832 с.
10. Шевченко И.И. Рационализация выбора методов противошоковой терапии при остром инфаркте миокарда: Автореф. дис…канд. мед. наук. - Воронеж, 2001.- 16 с.
11. Hollenberg SM, Kavinsky CJ, Parrillo JE: Cardiogenic shock//Ann. Intern. Med. 1999 Jul 6; 131(1): 47-59.
12. Picard M.H., Davidoff R., Sleeper L.A., et al. SHOCK Trial. Should we emergently revascularize Occluded Coronaries for cardiogenic shock// Circulation. 2003 Jan 21; 107 (2): 279-84.
Поступила 4/11 /2003
