Многоцентровое (пилотное) исследование эффективности глиатилина при остром ишемическом инсульте
Статьи Опубликовано в журнале:
« Анналы НЕВРОЛОГИИ » Том 4. № 1, 2010г. М.М, Одинак 1, И.А. Вознюк1, М.А. Пирадов2, С.А. Румянцева3, А.Н. Кузнецов4, С.Н. Янишевский1, С.Ю. Голохвасгов1, Н.В. Цыган1.
1 Военно-медицинская академия им. СМ. Кирова, Санкт-Петербург
2 Научный центр неврологии РАМИ, Москва
3 ГУЗ«ГКБ№ 15имениО.М. Филатова», Москва 4ФГУ «Национальный медико-хирургический центр им. Н.И. Пирогова Росздрава», Москва
В статье представлены результаты многоцентрового (пилотного) исследования эффективности применения глиатилина в лечении пациентов с острым ишемическим инсультом, проводившегося в 2906-2008 гг. в России. В состав исследуемой группы вошли 122 пациента, которые получали базисную терапию, а также глиатилин в течение 3 мес. после дебюта инсульта, который получали по схеме: по 2000 мг в сутки в течение 15 дней, затем по 1000 мг в сутки в течение 15 дней, затем по 800 мг в сутки в течение 60 дней. Всем пациентам исследуемой группы выполнялось неврологическое обследование с оценкой по шкале NIHSS, шкале Rankin, индексу Barihel в динамике, стандартное лабораторное обследование; комплексная сосудистая диагностика с применением церебральной допплерогра-фии и дуплексного сканирования брахиоцефальных артерий; компьютерная томография либо магнитно-резонансная томография головного мозга в течение 24 часов после дебюта заболевания. 25 пациентам была выполнена магнитно-резонансная томография в расширенном объеме (1-е, 3-й сут. после дебюта инсульта - T1-, Т2-, диффузионно-, перфузионно-взвешенная томография; 30-е сут. после дебюта инсульта - 77-, Т2-взвешенная томография).
Результаты исследования пациентов, получавших только базисную терапию, были получены из литературы. Применение глиатилина для лечения пациентов с ишемическим инсультом способствует уменьшению неврологического дефиците и увеличению способности пациентов к самообслуживанию, что, вероятно, связано с меньшим конечным объемом поражения мозга.
Ключевые слова: ишемический инсульт, глиатилин, объем инфаркта мозга, магнитно-резонансная томография, клинический исход.
Введение
Разнообразие факторов риска, этиологии, особенности церебральной ангиоархитектоники определяют "гетерогенность инсульта" и прогредиентность течения острой цереброваскулярной патологии. Существование областей с различной степенью повреждения в регионе нарушенного кровообращения - «ядерной» зоны ишемии и «ишемической полутени» - обусловлено тем, что помимо некротического распада, роль в регуляции клеточного гомеостаза играет процесс отсроченной, программированной гибели (апоптоз) нейронов и нейроглии [5, 9. 13, 14, 24, 27].
Экспериментальные модели с постоянной и преходящей окклюзией, ряд МРТ-исследований (с оценкой диффузионно-взвешенного изображения), выполненных на животных, демонстрируют, что после первоначального восстановления кровотока развивается отсроченное повреждение ткани мозга.
Совокупностью причин «реперфузионного» повреждения является высокая активность метаболических процессов, вызванных гипоксией, гипогликемией, метаболическим ацидозом. перифокальным (или диффузным) отеком мозгового вещества и вторичной гипоперфузией, а также продолжающимся воздействием факторов риска/патогенеза [10, 11, 13, 19].
Тем не менее церебральная ишемия в области обратимого повреждения, запушенная гипоксическим каскадом «кальциевой» гибели, имеет пространственные и временные границы. Длительность периода обратимости («терапевтическое окно») индивидуальна и учитывается современной тактикой лечения инсульта. Эта тактика подразумевает решение двух основных задач: максимально раннее восстановление мозгового кровотока и/или проведение нейропротективной терапии [1-4, 6, 9, 24, 27, 32]. Большинство специалистов по нейропротективной терапии выделяют несколько целей при борьбе за выживаемость нейроиитов при состоявшейся ишемии: снижение экспрессии глутамата, нормализация работы ионных насосов и активности Na+-К+-АТФазы, восстановление уровня фосфатидилхолина, ослабление активности фосфолипазы и снижение уровня арахидоновой кислоты и других медиаторов воспаления [15—18, 21.22,25,26,37].
Подтверждение способности фосфолипидов и деацитилированных фосфолипидов поддерживать целостность мембран нервных клеток путем восстановления синтеза фосфолипидов и нейротрансмиттера ацетилхолина в поврежденном мозге стало основанием в предположении, что эти соединения могут использоваться в качестве нейрозашитных агентов.
Центральные холиномиметики (глиатилин, холин альфосцерат), являясь источниками холина и фосфатидилхолина, поддерживая физиологический уровень ацетилхолина, обладают мембраностабилизирующими свойствами, служат средствами, восстанавливающими межнейрональную трансмиссию. Их цитопротективные свойства многократно изучались и были доказаны в эксперименте и в клинических условиях. В большинстве работ подчеркивается эффективность и дозозависимость терапевтического воздействия нейропротекторов.
Среди рассматриваемых препаратов, выдержавших более десятка рандомизированных и так называемых слепых исследований, уже с 1990-х гг. особое внимание уделяется препаратам экзогенного холина: CDP-холин (цитиколин), -GPS (холин альфосаерат, глиатилин), рекогнан. Центральные холиномиметики, являясь источниками холина и фосфатидилхолина, участвуют в поддержании физиологических уровней ацетилхолина, обладают мембраностабилизирующими свойствами, нормализуя энергетику митохондрий и восстанавливая функционирование Na+-К+-АТФазы, воздействуют (CDP-холин) на восстановление сниженного ишемией уровня АТФ, уменьшают выброс глутамата. Несмотря на снижение синтеза фосфолипидов в условиях острой ишемии, нейроны используют экзогенный холин и ускоренно синтезируют фосфолипиды. Использование экзогенного холина увеличивает доступность продуктов распада фосфолипидов мембран для синтеза ацетилхолина и снижает энергоемкий холинэргический синтез предшественников, контролирующих выработку трансмиттеров [15, 16, 20, 23, 28-31,33-36].
Метаанализ четырех крупных клинических исследований (1652 пациента), проведенный для уточнения способности CDP-холина, улучшает обший показатель восстановления функций через 3 мес. после начала терапии, подтвердил эффективность препарата. При лечении инсульта отмечен достоверно лучший исход в сравнении с плацебо при использовании дозы 2 г/сут - повышение шансов благоприятного исхода в сравнении с плацебо на 38%. Warach et al. (2000), объединив данные диффузионно-взвешенной магнитно-резонансной томографии двух клинических исследований, выявили значительное влияние дозы препарата на изменение объема очага поражения: если в группе плацебо размер очага увеличивался в среднем на 84,7%, то у пациентов, получавших цитиколин в дозе 0,5 г/сут, - на 34%, а у получавших препарат в дозе 2,0 г/сут - всего на 1,8% [20. 31].
Клиническая эффективность и переносимость холин альфоснерата была изучена в нескольких клинических исследованиях, наиболее крупным из которых было исследование Barbagallo S.G. et al. (1994), включавшее в себя 2058 пациентов. Лечение начиналось не позднее 10 дней после инсульта или транзиторной ишемической атаки. Вес результаты подтверждают эффективность холин альфоснерата при восстановлении неврологических и психических расстройств, являющихся следствием цереброваскулярных нарушений, что наиболее очевидно к 3-му месяцу наблюдений. Нами в период с 1997 по 2005 г. проводились сравнительные клинико-морфологические исследования эффективности применения глиатилина при острой церебральной ишемии, подтвердившие высокую клиническую эффективность препарата в достижении регресса как общемозговой, так и грубой очаговой неврологической патологии.
Собственные экспериментальные работы, сопровождавшиеся ультраструктурным и гистологическим контролем, позволили обнаружить подтверждения цитопротекторным свойствам глиатилина в момент гипоксического повреждения и стимуляции регенеративных/репаративных процессов в случае стабилизации энергетического гомеостаза мозгового вещества в регионе повреждения [7, 8, 12]. Однако рандомизированных исследований по изучению влияния глиатилина на область формирующегося ишемического инфаркта и сопоставлению с клиническими изменениями при начале лечения с первых суток возникновения симптомов острого заболевания не было.
Цель исследования
Цель данного исследования заключалась в оценке влияния холин альфоснерата (глиатилина) при парентеральном (внутривенном) и пероральном назначении на острое ише-мическое повреждение головного мозга и на его клинический исход.
Задачи:
Оценить влияние глиатилина на степень неврологического дефицита и способность пациентов к самообслуживанию к концу 3-го месяца наблюдения.
Количественно оценить динамику объема церебрального инфаркта в конце 30-дневного периода парентерального лечения.
Оценить уровень летальности в группе обследуемых спустя 6 месяцев после рандомизации,
Выявить наличие побочных действий препарата в процессе лечения.
Организация исследования
Исследование GL1A проводилось в 2006-2008 гг. в России на базе 5 клинических центров:
1. Государственное образовательное учреждение высшего профессионального образования «Военно-медицинская академия им. СМ. Кирова», г. Санкт-Петербург.
2. Государственное учреждение здравоохранения г. Москвы «Городская клиническая больница № 15 им. О.М. Филатова».
3. Федеральное государственное учреждение «Национальный медико-хирургический центр им. Н.И. Пирогова Росздрава». г. Москва.
4. Государственное учреждение «Научный центр неврологии РАМН», г. Москва.
Дизайн исследования
В ходе исследования было обследовано 800 больных.
Критериями включения пациентов в исследуемую группу явились:
- умеренный или значительный неврологический дефицит (по NIHSS -от 6 до 21 баллов) в течение первых суток после дебюта заболевания;
- исключение субарахноидального кровоизлияния, заболевания центральной нервной системы с псевдо инсультным течением, инфаркта мозга стволовой локализации по данным компьютерной томографии либо магнитно-резонансной томографии головного мозга в течение 24 часов после дебюта заболевания;
- функциональная независимость пациента до инсульта: при первичном инсульте - способность к самообслуживанию и повседневной деятельности по шкале Rankin менее 2 баллов, при повторном инсульте - менее 3 баллов;
- уровень образования не менее 5 классов школы.
- спонтанное исчезновение большинства неврологических симптомов в течение 24 часов после дебюта заболевания;
- кома;
- эпилепсия;
- деменция;
- черепно-мозговые травмы либо нейрохирургические вмешательства в течение последних 3 лет;
- онкологические заболевания;
- декомпенеированное течение соматических заболеваний;
- получение пациентом других ноотропных препаратов после дебюта заболевания;
- беременность;
- лактация.
GLIA-2 - пациенты с неврологическим дефицитом по NIHSS более 9 баллов в первые сутки после дебюта инсульта ( n= 46);
GLIA-3 - пациенты, которым было выполнено расширенное нейровизуализационное обследование с уточнением объема «обратимых» повреждений (n = 25);
GLIA-4 - пациенты группы GL1A-3, у которых не было выявлено дополнительных1 критериев исключения (11=15).
Дизайн исследования не включал формирования группы плацебо. В связи с этим при проведении статистического анализа были использованы представленные в литературе результаты клинико-инструментальных обследований пациентов групп плацебо в других клинических исследованиях.
Источники данных группы плацебо
В ходе анализа отечественной и зарубежной литературы были изучены 35 журнальных статей (1999-2008), содержавших информацию о результатах клинико-инструментального обследования пациентов с ишемическим инсультом, вошедших в состав групп плацебо. В результате анализа литературы было установлено, что по дизайну исследования и по степени неврологического дефицита в первые сутки после дебюта инсульта пациентам группы GLIA-1 в наибольшей степени соответствовали пациенты группы плацебо исследования Clark W.M. et at. (1999). При анализе результатов расширенного нейровизуализационного исследования в качестве данных группы плацебо были использованы результаты обследования пациентов группы плацебо исследования Warach S. et al. (2000) [19, 38].
Статистический анализ полученных результатов
Результаты клинико-инcтрументального обследования накапливались в электронной базе данных с помощью табличного редактора Microsoft Excel в составе Microsoft Office 2007 с последующим переводом в математико-статистический пакет StatSoft STATISTICA v. 6.0.
В ходе статистического анализа результатов исследования применялись следующие процедуры и методы:
- проверка гипотезы о происхождении групп, сформированных по качественному признаку, из одной и той же популяции, на основе построения таблиц наблюдаемых частоте применением критерия Pearson Chi-square;
- сравнение независимых групп по количественному признаку при помощи параметрического t-критерия Стьюдента (для двух групп);
- корреляционный анализ с использованием коэффициента ранговой корреляции &teta;-Кендалла.
Применение непараметрических методов сравнения независимых групп было затруднено в связи с тем, что при описании результатов обследования пациентов групп плацебо по данным литературы во всех случаях были представлены результаты, учитывающие только средние значения и стандартные отклонения показателей.
1 - Дополнительные критерии исключения, возраст пациентов менее 55 лет; наличие стенозируюшего атеросклеротического поражения магистральных артерий каротидного бассейна с формированием хронической гипоперфузии; объем диффузионно-взвешенной магнитно-резонансной томографии в дебюте инсульта более 120 см3 ; отношение объема перфузионно-диффузионной разницы к объему необратимо поврежденной нервной ткани по данным магнитно-резонансной томографии в дебюте инсульта более чем 17:1.
Назначение препарата
Все пациенты группы GLIA-1 получали глиатилин по сле¬дующей схеме:
-с 1-х по 15-е сутки после дебюта инсульта- 2000 мг внут¬ривенно капельно I раз в сутки;
- с 16-х по 30-е сутки после дебюта инсульта — 1000 мг внутривенно капельно либо внутримышечно 1 раз в сутки;
- с 31-х по 90-е сутки после дебюта инсульта - 400 мг внутрь 2 раза в сутки.
Также всем пациентам проводилась базисная терапия, направленная на коррекцию показателей гемодинами¬ки, реологических свойств крови, осложнений инсуль¬та,
Клинико-инструментальное обследование
Согласно протоколу исследования, клиническое обследо¬вание на 1-е, 30-е и 90-е сутки после дебюта инсульта включало в себя:
- неврологический осмотр;
- оценку неврологического дефицита по NIHSS;
- оценку способности пациентов к самообслуживанию и повседневной деятельности по индексу Barthel и шкале Rankin.
Всем пациентам группы GLIA-1 осуществлялись:
- стандартное лабораторное обследование;
- комплексная сосудистая диагностика с применением церебральной допплерографии и дуплексного сканирова¬ния брахиоцефальных артерий;
- компьютерная томография либо магнитно-резонансная томография головного мозга в течение 24 часов после дебюта заболевания.
Пациентам группы GLIA-3 было проведено расширенное нейровизуализационное обследование, направленное на оценку динамики ишемического повреждения головного мозга и включавшее:
- в 1-е и 3-й сутки после дебюта инсульта - Т1 - и Т2-взве-шенную магнитно-резонансную, диффузионно-взвешен-ную, перфузионно-взвешенную томографию;
- на 30-е сутки после дебюта инсульта - Т1- и Т2-взве-шенную магнитно-резонансную томографию.
Протокол выполнения магнитно-резонансной томогра¬фии включал получение Т2- и Т1-взвешенных изображе¬ний в аксиальной плоскости, Т1-взвешенных изображе¬ний в сагиттальной плоскости и Т2-взвешенных изображе¬ний в коронарной плоскости. В большинстве случаев объем сформировавшегося ишемического очага рассчитывался по данным Т2-взвешенных изображений в аксиальной плоскости.
По данным диффузионно-взвешенных изображений с фактором диффузионного взвешивания b = 1000 производился расчет объема выявленных изменений интенсивности магнитно-резонансного сигнала, соответствовавших ядру инфаркта мозга (рис. 1).
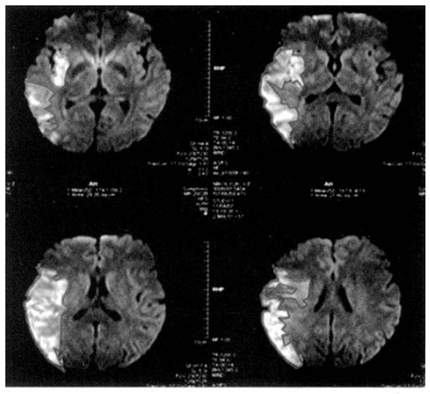
Рис.1. Пример выделения ядра инфаркта в каждом срезе для расчета объема
необратимо поврежденной нервной ткани по данным диффузионно-взвешенной МРТ.
По данным перфузионно-взвешенной магнитно-резонансной томографии оценивали объем и характер перфузионных нарушений, поданным диффузионно-взвешенной магнитно-резонансной томографии — объем необратимого повреждения нервной ткани, по данным Т2-взвешенной магнитно-резонансной томографии -объем инфаркта мозга. При построении перфузионных карт рассчитывали следующие показатели мозгового кровотока:
ТТР - время до прибытия контрастного вещества;
МТТ - среднее время прохождения контрастного вещества;
СВР - мозговой кровоток;
CBV - объем мозгового кровотока.
Расчет объема морфологических и перфузионных изменений проводили с использованием возможностей томографической станции и специально созданной программы, учитывая данные всей серии аксиальных срезов, число и шаг которых являлись постоянными для всех исследований у каждого пациента.
Оценка выживаемости выполнялась через 6 месяцев после дебюта заболевания.
Результаты исследования
В состав группы GLIA-1 вошли 122 человека (80 мужчин, 42 женщины), средний возраст - 63,78 ±11,1 года. В 1-е сутки после дебюта инсульта неврологический дефицит по NIHSS составил 10,78 ±4,13 балла, способность пациентов к самообслуживанию и повседневной деятельности по индексу Barthel - 45,92 ± 28.12 балла, по шкале Rankin — 3,6 ± 1,06 балла.
Наиболее адекватной для сравнения, сопоставимой по неврологическому дефициту в дебюте инсульта с группой плацебо (Clark W.M. et al., 1999) явилась подгруппа пациентов с неврологическим дефицитом по NIHSS более 9 баллов в дебюте заболевания (GLIA-2). В табл. 1 показана однородность сравниваемых групп пациентов по степени выраженности неврологических симптомов в 1-е сутки заболевания.
Tаблица 1.
Неврологический дефицит в 1 -е сутки после дебюта инсульта у пациентов группы GLIA-2 и группы плацебо исследования Clark W.M. et al. (1999).
| Показатель | Группа GLIA-2 | Группа плацебо | Достоверность различий |
|---|---|---|---|
| Количество пациентов | 46 | 306 | - |
| Неврологический дефицит по NIHSS в первые сутки | 12,35 ±4,2 | 11±5 | р > 0.1 |
В ходе анализа результатов клинического обследования с использованием N1HSS, индекса Barthel, шкалы Rankin изучались показатели в 1-е, 30-е и 90-е сутки после дебюта заболевания, их абсолютная и относительная динамика, а также частоты значений шкал менее пороговых уровней.
В результате проведенного анализа установлено, что к 30-м суткам после дебюта инсульта у пациентов группы GLIA-2 достоверно чаше отмечалось значимое клиническое улучшение, проявлявшееся уменьшением выраженности инвалидизирующнх симптомов, значимым повышением способности пациентов к самообслуживанию (менее 2 баллов по шкале Rankin) (рис. 2).
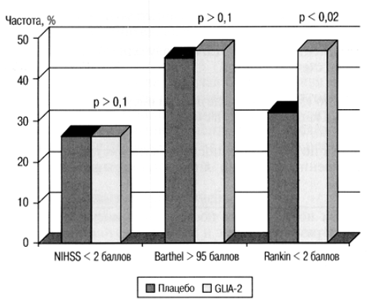
Pис. 2: Неврологический дефицит и способность пациентов к самообслуживанию на 30-е сутки
после дебюта инсульта у пациентов группы GUA-2 и группы плацебо исследования Clark W.M. et al. (1999).
Степень выраженности положительных изменений, наблюдавшаяся в остром периоде инсульта, существенно возрастала к концу 3-го месяца восстановительного лечения. На основании анализа можно было утверждать, что к 90-м суткам после дебюта инсульта у пациентов группы GLIA-2 не только формировалась высокая способность пациентов к самообслуживанию (менее 2 баллов по шкале Rankin), но и достоверно чаше, чем в группе плацебо, отмечался умеренный неврологический дефицит (менее 2 баллов по N1HSS) (рис. 3).
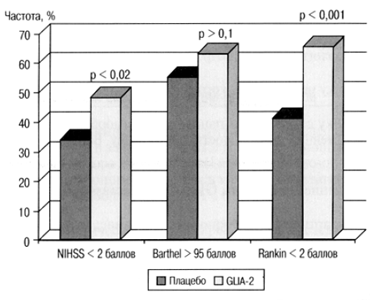
Pис. 3. Неврологический дефицит и способность к самообслуживанию на 90-е сутки после дебюта инсульта
у пациентов группы GLIA-2 и группы плацебо исследования Clark W.M. et al. (1999).
Таким образом, применение глиатилина для лечения пациентов с ишемическим инсультом способствовало уменьшению выраженности неврологических симптомов, увеличивало степень их независимости от помощи персонала и родственников, способствуя формированию самообслуживания.
При анализе результатов магнитно-резонансной томографии, полученных в группе пациентов GL1A-3, в качестве плацебо-контроля использовались результаты обследования пациентов плацебо-группы в исследовании Warach S. et al. (2000).
Для повышения достоверности полученных данных кроме фактических данных магнитно-резонансной томографии было проведено тщательное сопоставление характеристик пациентов по всевозможным параметрам, в том числе по возрасту и степени выраженности неврологических расстройств (табл. 3).
Tаблица 3.
Bозраст и неврологический дефицит в 1-е сутки после дебюта инсульта у пациентов группы Ш-3 и группы плацебо исследования Warach S. el al. (2000).
| Показатель | Группа GLIA-3 | Группа плацебо | Достоверность различий |
|---|---|---|---|
| Количество пациентов | 25 | 40 | - |
| Возраст пациентов на момент дебюта инсульта | 66,54 ± 9,74 | 72,1 ±1,9 | р |
| Неврологический дефицит no NIHSS в первые сутки после дебюта инсульта | 10,7 ±3,97 | 12,7 + 0,9 | р |
Как следует из таблицы, наличие достоверных различий в возрасте пациентов и степени неврологического дефицита в 1-е сутки после дебюта инсульта не позволило сравнивать результаты обследования пациентов группы GLIA-3 и группы плацебо-контроля. Кроме того, в исследование W/arach S. et al. (2000) были включены пациенты с объемом необратимого повреждения нервной ткани по данным диффузионно-взвешенной магнитно-резонансной томографии от I до 120 см1 в 1-е сутки после дебюта заболевания.
Для достижения большей однородности анализируемого материала и выделения группы, более сравнимой с группой плацебо-контроля, нами были установлены дополнительные критерии исключения:
- возраст пациентов менее 55 лет;
- наличие стенозирующего атероскл еретического поражения магистральных артерий каротидного бассейна с формированием хронической гипоперфузии;
- объем диффузионно-взвешенной магнитно-резонансной томографии в дебюте инсульта более 120 см3;
- отношение объема лерфузионно-диффузионной разницы к объему необратимо поврежденной нервной ткани по данным магнитно-резонансной томографии в дебюте инсульта более чем 17 : 1.
Таким образом, опираясь на дополнительные критерии, из числа пациентов группы GLIA-З была выделена группа GLIA-4, которая оказалась однородной с группой плацебо-контроля по основным клинико-неврологическим и инструментальным показателям. Проведенное сравнение позволило подтвердить отсутствие достоверных различий между пациентами выбранных для анализа групп (табл. 4).
Tаблица 4.
Основные показатели клинико-инструментального обследования пациентов группы GLIA-4 и группы плацебо исследования Warach S. etal. (2000).
| Показатель | Группа GLIA-4 | Группа плацебо | Достоверность различий |
|---|---|---|---|
| Количество пациентов | 15 | 40 | - |
| Возраст пациентов на момент дебюта инсульта | 68,27 ±8,8 | 72,1 ± 1,9 | р>0,1 |
| Неврологический дефицит no NIHSS в первые сутки после дебюта заболевания | 10,87 ±4,16 | 12,7 ±0,9 | р>0,05 |
| Объем необратимо поврежденной нервной ткани по данным диффузионно-взвешенной МРТ в первые сутки после дебюта инсульта (по картам с коэффициентом взвешивания b - 1000) | 25,4 ±33,05 | 31,9 ±5,7 | р>0,1 |
| Обьем перфузионных нарушений поданным перфузионно-взвешенной МРТ в первые сутки после дебюта инсульта (по картам гМТТ) | 111,84 ± 90.35 | 97,4 ±15,5* | Р>0,1 |
| Объем перфузионно-диффузионной разницы по данным перфузионно-взвешенной (карты гМТТ) и диффузионно-взвешенной (карты с коэффициентом взвешивания b = 1000) МРТ в первые сутки после дебюта инсульта | 86,43 ± 79,82 | 67,6 ±13,1* | р>0,1 |
Сравнительному анализу были подвергнуты объемные характеристики инфаркта мозговой ткани, полученные при исследовании в 1-е и 30-е сутки наблюдения. А именно для оценки степени изменений объема необратимого повреждения нервной ткани использовалась относительная разница между:
- объемом необратимого повреждения по данным диффузионно-взвешенной МРТ в 1-е сутки после дебюта инсульта по картам (ДВИ МРТ) с коэффициентом взвешивания b = 1000;
- объемом инфаркта мозга по данным Т2-взвешенной МРТ на 30-е сутки после дебюта инсульта (группа GLIA-4) и на 90-е сутки после дебюта инсульта (плацебо-группа). Указанная динамика в сравнении с данными плацебо представлена в табл.5.
Tаблица 5.
Динамика объемов необратимого повреждения головного мозга у пациентов группы GLIA-4 и группы плацебо Warach S. et al, (2000).
| Показатель | Группа GLIA-4 | Группа плацебо | Достоверность различий |
|---|---|---|---|
| Количество пациентов | 15 | 40 | - |
| Срок выполнения Т2-взвешенной MFT после дебюта инсульта(сутки) | 30 | 90 | - |
| Относительная разница между объемом необратимого повреждения по данным диффузной-no-взвешенной МРТ в первые сутки после дебюта инсульта (то картам с коэффициентом взвешивания b=1000) в объемом инфаркта мозга по данным повторной Т2-взвешенной MFT | 12,78% ±71,62% | 180,2% ±106.8% | р |
Примененный сравнительный анализ позволяет считать, что использование глиатилина по предложенной схеме оказалось эффективным. Лечение с применением глиатилина, начатое с 1-х суток острого периода ишемического инсульта, достоверно предотвращало ожидаемое (потенциально возможное) значительное увеличение конечных размеров мозгового инфаркта - морфологического дефекта мозговой ткани. В среднем у пациентов группы GL1A-4 к концу острого периода наблюдалось увеличение конечного объема инфаркта мозга по сравнению с объемом необратимого повреждения в 1-е сутки только на 13%, вто время как у пациентов плацебо-группы конечный объем повреждения к концу периода наблюдения достоверно возрастал на 180%.
Для выявления зависимостей, связанных с динамикой размеров необратимого повреждения нервной ткани, в группе GL1A-4 был проведен корреляционный анализ с использованием коэффициента ранговой корреляции &teta;-Кендалла. В ходе проведенного анализа не было установлено зависимостей, связанных с динамикой размеров необратимого повреждения нервной ткани. При анализе результатов обследования пациентов группы GL1A-3 были установлены корреляционные связи, отражающие зависимость клинического исхода от динамики объемов ишемического повреждения головного мозга:
- отрицательная умеренной силы (&teta; -0,3, р = 0,04) корреляционная связь между преобладанием конечного объема инфаркта над объемом необратимо поврежденной ткани в 1-е сутки после дебюта заболевания и относительной динамикой неврологического дефицита по NIHSSc 1-х по 30-е сутки после дебюта инсульта;
- отрицательная умеренной силы (т = -0,34, р = 0,035) корреляционная связь между преобладанием конечного объема инфаркта над объемом необратимо поврежденной ткани в I -с сутки после дебюта заболевания и относительной динамикой способности пациента к самообслуживанию и повседневной деятельности с 1-х по 90-е сутки после дебюта инсульта.
Нежелательные явления и клинические исходы
В ходе исследования было зарегистрировано 7 случаев нежелательных явлений (пароксизм мерцательной аритмии, острые эрозии желудка и двенадцатиперстной кишки, пневмония, гидроторакс), не связанных с приемом препарата глиатилин. Один пациент отказался от продолжения участия в исследовании, в 6 случаях отмечался летальный исход.
Заключение
Проведенное исследование позволило установить, что применение глиатидина для лечения пациентов с острым ишемическим инсультом способствует уменьшению неврологического дефицита и увеличению способности пациентов к самообслуживанию.
Количественная оценка конечного объема инфарктной зоны в группе обследованных больных дает возможность говорить об эффективном сохранении массы мозгового вещества в области обратимых изменений у больных с ишемическим инсультом средней степени тяжести. Полученные результаты также позволяют предположить, что большая степень восстановления нарушенных функций при использовании глиатилина в лечении пациентов с ишемическим инсультом может быть объяснена меньшим конечным объемом поражения мозга.
Для уточнения полученных результатов и более глубокой клинической и фармакологической оценки многогранного действия глиатилина при остром ишемическом повреждении головного мозга необходимы дальнейшие исследования. Список литературы 1. Верещагин И.В., Парадов М,А. Принципы ведения и лечения больных в острейшем периоде инсульта. Интенсивная терапия острых нарушений мозгового кровообращения. Орел. 1997: 3-11.
2. Виленскии Б.С. Инсульт: профилактика, диагностика и лечение. СПб.: Фолиант, 2002: 397.
3. Виленскии Б.С. Современная тактика борьбы с инсультом. СПб.: Фолиант, 2005: 2S8.
4. Вознюк И.А., Голохвастов С.Ю., Фокин В.А. и др. Нарушения церебрального кровотока и перфуэионные расстройства в остром периоде ишемического инсульта. Инсульт (Прилож. к Журн. неврологии и психиатрии им. С.С, Корсакова) 2007. Спец. вып. 242—243.
5. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. М.: Медицина, 2001:327.
6. Инсульт; диагностика, лечение, профилактика / Под рел. З.А. Суслиной, М.А. Пирадова. М.: МЕДпресс-информ, 2008: 283.
7. Одинак М.М., Вознюк И.А. Новое в терапии при острой и хронической патологии мозга, СПб.: ВМелА, 2000: 31.
8. Одинок М.М., Вознюк И.А.. Янишевскии СИ. Ишемия мозга (нейронротективная терапия, дифференцированный подход). СПб.: ВМсдА, 2002: 75.
9. Одинак W.W., Вознюк И.А. Ишемия мозга- преемственность врешении проблемы. Мед. акад. журн. 2006; т. 6: 3: 88-94,
10. Одинак М.М., Вознюк И.А., Ролохеастов СЮ. и др. Мониторинг псрфузионных нарушений в острейшую стадию ишемического инсульта. Всстн. Рос. воен.-мед. акад. 2005; 2: 25-30.
11. Одинак М.М., Вознюк И.А., Годохввшов С.Ю., и др. Особенности ранней нейровизуализационной диагностики при острых нарушениях мозговою кровообращения. Регионарное кровообращение и микроииркуляция. 2007: 1: 113—114.
12. Одинак М.М.. Вознюк И.А.. Янишевскии СИ. Инсульт. Вопросы этиологии, патогенеза. Алгоритмы лиагностики и терапии. СПб.: ВМедА, 2005: 192.
13. Труфанов Г.Е., Одинак М.М., Фокин В.А. Магнитно-резонансная томография в диагностике ишемического инсульта. СПб.:ЭЛБИ-СПб. 2008: 271.
14. Труфанов Г.Е., Фокин В.А., И.В. Пьяное и др. Рентгеновская компьютерная и магнитно-резонансная томография в диагностике ишемического инсульта. СПб.: ЭЛ БИ-СПб, 2005: 192.
15. Barbagallo S.G., Barbagalio М.. Giordano М. el el. Glycerophosphocholine in the menial recovery of cerebral ischemic attacks. An Italian mullicenler clinical trial. Pharmacology of Aging Process (Annals of the New York Academy of Sciences). 1994; 717: 253-269.
16. Bergamaschi M.. Piccolo O. Deacylated phospholipids: Chemistry and therapeutic potential. Phospholipids: characterization, metabolism, and novel biological applications / Ed. by G. Cvec, R Paltauf, AOCS Press, USA 1995: 228-247. n.Blusztajn J.K., Wurlman R.J. Choline and cholinergic neurons. Science 1983; 221: 19-22. H.Casamenii F., Mantovani P., Amaducci L., Pepeu G Effect of phosphatidylserine on Ach output from the cerebral cortex of the rat. J.Neurochem 1979;32:529-533.
19. Clark W.M., Wissman S., AlbersG.W. etal. Recombinant Tissue-Type Plasminogen Activator (Alteplasc) for Ischemic Stroke 3 to 5 Hours After Symptom Onset. The ATLANTIS Studv. J. Am. Med. Association 1999:282:21:2019-2026.
20. D'Ortando J.K., Sandage B.W. Cilicoline (CDP-choline): mechanism of action and effects in ischemic brain injury. Neurol. Res. 1995;17:281-284.
21. Delwaide P.J.. GyeselynckA.M., Muriel A., YlieffM. Double-blind randomized controlled study of phosphatidvlserine in senile patients. Acta Neurol. Scand 1986; 73:136-140.
22. Dorman P.J., Sandercock P.A. Considerations in the design of clinical trials of neuroprotective therapy in acute stroke. Stroke 1996; 27:9: 1507-1515.
23. Dross K., Kevitz M. Concentration and origin of choline in the rat brain. N.S.Arch. Pharmacol. 1972:274:91-10.
24. Fisher M., Takano K. The panumbra, therapeutic lime window and acute ischemic stroke. Baillieres Clin. Neurol. 1995; 4: 2: 279-295.
25. Flenige F.. Van Der Berg C.J. Choline administration and Ach in brain. J.Neurochem 1979; 32: 1331-1333.
26. Freeman J.J., Jendeti D.J. The source of choline for Ach synthesis in brain. Life Science 1976; 19: 949-962.
27. Heiss W.-D. Detection of the penumbra as a rationale for therapy of ischemic stroke. Журн. непрол. и неихиат. (Прилож. «Инсульт»). 2003; 9: 13-15.
28. Jope R.S. Effects of phosphatidylcholine administration to rats on choline in blood and choline and Ach in brain. J. PET 1982; 220: 322-328.
29. Jope R.5., Jenden D.J. Choline and phospholipid metabolism and synthesis of Ach in rat brain. J. Neuroscience Res. 1979; 4; 69-82.
30. Loffetholiz K. Receptor regulation of choline phospholipid hydrolysis. Biochemical Pharmacol. 1989; 38: 1543-1544.
31. Sandage Jr. et ai. Reduction of infarct volume using cilicoline. United States Patient 1999; 5: 872.
32. Schehr R.S. New treatments for acute stroke. Nature Biotcchnol. 1996; 14: 1549-1554.
33. Schmidt D.E., Wecker L. CNS effects of choline administration : evidence for temporal dependence. Neuropharmacol. 1981; 20: 535-539.
34.Seeades J.J., Frontera G. CDP-choline: Pharmacological and clinical review Methods Find Exp. Clin. Pharmacol. 1995; 17; Suppl. В.: 2-54.
35. Studies on the pharmacological and biochemical effects of alfa-glycerylphosphorylcholine in experimental animals. Report from Shionogy Research Laboratories.
36. TommasinaC, Manzino M., Novella P., Pasiorino P. Studio clin-ico dell'efficacia terapeutica e della tollerabilita della colina alfos-ccrato in 15 soggetti con compromissione delle funzioni cognitive successive ad ischemia cerebrale focale acuta. Rivista di Neuropsichiatria e Scienze Affini. 1991; 37: 21—28.
37. Wurtmann R.J.. Heft! F., Melamed E. Precursor control of neurotransmitter synthesis. Pharmacological Rev. 1981; 32; 331-335.
38. Warach S., Petligrew L.C., DasheJ.F. etal. Effect of cilicoline on ischemic lesions as measured by diffusion-weighted magnetic resonance imaging. Citicoline 010 Investigators. Ann. Neurol. 2000; 48: 5:713-722.
