akvion.ru
akvion.ru

Комбинированный препарат для повышения мужской фертильности
далее...
Больше информации на сайтах:
www.reproduction.info
www.plan-baby.ru
Роль гипербарической оксигенации в сочетании с антиоксидантами в лечении идиопатического мужского бесплодия
СтатьиОпубликовано в журнале:
«Андрология и генитальная хирургия», №4, Том 18, 2017
Д.Г. Кореньков1, С.Н. Калинина1, В.Н. Фесенко1, А.Л. Павлов2
1Кафедра урологии ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И. И. Мечникова» Минздрава России; Россия, 191015 Санкт-Петербург, ул. Кирочная, 41;
2Санкт-Петербургское ГБУЗ «Городская Александровская больница»; Россия, 193312 Санкт-Петербург, ул. Солидарности, 4
Введение. В андрологической практике причиной бесплодия в 40—70 % случаев является идиопатическое мужское бесплодие. Для его лечения применяется эмпирическая терапия, основанная на имеющихся знаниях о сперматогенезе. Последние несколько лет в качестве средств 1-й линии терапии мужской инфертильности часто используются биологически активные добавки. К таким многокомпонентным биологическим добавкам к пище относятся: комбинированный препарат для повышения мужской фертильности Сперотон и антиоксидантный комплекс Синергин (АКВИОН, Россия).
Цель исследования — оптимизация результатов применения гипербарической оксигенации (ГБО) в комбинированном лечении пациентов с идиопатическими нарушениями спермограммы.
Материалы и методы. В исследовании приняли участие 155 мужчин в возрасте от 20 до 45 лет. Из них у 120 мужчин установлено идиопатическое бесплодие, а 35 были практически здоровы (контрольная группа). Пациенты с бесплодием (n = 120) были разделены на 3 группы по 40 человек в каждой. Во всех 3 группах больные проходили лечение ГБО в сочетании с препаратами Сперотон и/или Синергин: в 1-й группе получали Сперотон (по 1 саше 1 раз в день), во 2-й группе — Синергин (по 2 капсулы 1 раз в сутки), в 3-й группе — Сперотон (по 1 саше 1 раз в день) и Синергин (по 2 капсулы 1 раз в день). Пациенты всех 3 групп по окончании терапии ГБО продолжали прием препаратов в течение 3 мес. Курс ГБО состоял из 10 ежедневных сеансов продолжительностью 60 мин. У всех больных 4 групп в плазме крови и эякуляте исследовали изменения уровня продуктов свободнорадикального окисления, активности антиоксидантной защиты, а также основные показатели спермограммы.
Результаты. Проведенная терапия способствовала нормализации тиол-дисульфидного обмена в плазме крови и эякуляте, антиоксидантной защиты, а также основных показателей спермограммы. У больных 1-й группы (ГБО + Сперотон) концентрация сперматозоидов в эякуляте после курса лечения увеличилась по сравнению с исходными значениями (до лечения) в 3 раза, а количество подвижных форм — в 2,4 раза, количество дегенеративных форм уменьшилось в 1,3 раза. У больных 2-й группы (ГБО + Синергин) концентрация сперматозоидов в эякуляте после курса лечения увеличилась в 2,2 раза, количество подвижных форм — в 2,7 раза, а количество дегенеративных форм уменьшилось в 1,4 раза. У больных 3-й группы (ГБО + Сперотон + Синергин) концентрация сперматозоидов в эякуляте увеличилась в 4,7 раза, количество подвижных форм — в 5,3 раза, а количество дегенеративных форм уменьшилось в 1,8 раза.
Вывод. Комбинированный прием Сперотона и Синергина в сочетании с проведением ГБО показал высокую эффективность в коррекции основных показателей эякулята и может быть рекомендован в качестве терапии различных форм патозооспермии.
Ключевые слова: бесплодие, гипербарическая оксигенация, сперматогенез, перекисное окисление липидов, свободнорадикальное окисление, Синергин, Сперотон
The role of hyperbaric oxygen therapy and antioxidant administration in treatment of idiopathic male infertility
D. G. Korenkov1, S. N. Kalinina1, V. N. Fesenko1, A.L. Pavlov2
1Department of Urology of the North-Western State Medical University named after I. I. Mechnikov, Ministry of Health of Russia; 41 Kirochnaya St., Saint Petersburg 191015, Russia;
2Saint-Petersburg City Aleksandrovskaya Hospital; 4 Solidarnosti St., Saint Petersburg 193312, Russia
Introduction. In clinical andrology practice, the cause of infertility in 40—70 % cases is idiopathic male infertility. The treatment involves empirical therapy based on the knowledge of spermatogenesis. In recent years, dietary supplements are used as the first line therapy of male infertility. Among these multicomponent dietary supplements are combination supplement for increasing male fertility Speroton and antioxidant complex Sinergin (Acvion, Russia).
The study objective is to optimize the results of hyperbaric oxygen therapy (HBOT) in combination treatment of patients with idiopathic abnormalities in semen analysis.
Materials and methods. The study included 155 males aged 20—45 years. Among them, 120 males were diagnosed with idiopathic infertility, 35 were practically healthy (control group). Patients with infertility (n = 120) were divided into 3 groups, 40 patients each. In all 3 groups, patients received HBOT in combination with Speroton and/or Sinergin: the 1st group (n = 40) received Speroton (1 sachet/day); the 2nd group (n = 40) received HBOT and Sinergin (2 capsules/day); patients in the 3rd group received combination of HBOT + Speroton (one sachet/day) + Sinergin (2 capsules/day). Patients in the 3 groups continued to receive the supplements 3 months after the completion of HBOT. The HBOT course consisted of 10 60-minute daily sessions. In patients of the 4 groups, including the control group, the levels of oxidative stress products and endogenous antioxidants activity in plasma and ejaculate were evaluated, as well as the main semen characteristics.
Results. The administered therapies normalized thiol-disulfide metabolism in plasma and semen, antioxidant protection, and the main semen characteristics. In patients of the 1st group (HBOT + Speroton), sperm count in the ejaculate increased 3-fold compared to the baseline (before treatment), motile sperm forms increased 2.4-fold, the number of degenerated sperm cells decreased 1.3-fold. In the 2nd group (HBOT + Sinergin), sperm count in the ejaculate increased 2.2-fold in the course of treatment, motile sperm count increased 2.7-fold, the number of degenerated sperm cells decreased 1.4-fold. In the 3rd group (HBOT + Speroton + Sinergin), sperm count in the ejaculate increased 4.7-fold, motile sperm count — 5.3-fold, the number of degenerated sperm cells decreased 1.8-fold.
Conclusion. Combined administration of Speroton and Sinergin in combination with HBOT has shown high effectiveness in correction of the main ejaculate characteristics and can be recommended as a therapy for various forms of asthenozoospermia.
Key words: infertility, hyperbaric oxygen therapy, spermatogenesis, lipid peroxidation, oxidative stress, Sinergin, Speroton
Введение
Частота бесплодных браков в России составляет 15—20 %, из них около 45 % — по причине мужской инфертильности. Актуальность мужского бесплодия не вызывает сомнений, а методы его диагностики и лечения остаются не до конца изученными. Прогрессирующее снижение мужской фертильности оценивают как состояние, которое может быть связано с воздействием эндо- и экзогенных факторов. Причинами мужского бесплодия помимо упомянутых могут быть инфекции, передающиеся половым путем и вызывающие заболевания репродуктивных органов, а также варикоцеле.
Наиболее затруднительно и малоэффективно лечение секреторного бесплодия, которое обусловлено первичным (гипергонадотропным) гипогонадизмом при поражении яичек и вторичным (гипогонадотроп ным) гипогонадизмом. Гормонотерапия таких состояний с известными серьезными осложнениями уже достаточно давно имеет альтернативные неспецифические методы лечения. Частая причина мужского бесплодия — воспалительные заболевания дополнительных половых желез, приводящие к патоспермии [1—4]. Лечение инфертильности у мужчин должно быть направлено на медикаментозную коррекцию выявленных причин патозооспермии.
В андрологической практике 40—70 % случаев па тоспермии приходится на идиопатическое мужское бесплодие, когда причину качественных и количественных нарушений эякулята установить не удается, так как при физикальном осмотре изменения не выявляются, гормональный статус в норме и т. д. В этом случае применяется эмпирическая терапия, основанная на имеющихся знаниях о сперматогенезе [5—11].
Нарушения сперматогенеза являются следствием существенных изменений гомеостаза в целом, а также нарушения биохимии клетки, клеточных структур и биологических мембран. Патогенетическими немедикаментозными методами, воздействующими на основные звенья патологического процесса, могут быть экстракорпоральные методы гемо- и иммунокоррекции, гипербарическая оксигенация (ГБО).
Проведенные нами ранее исследования [12—14] показали высокую эффективность ГБО у больных с секреторным бесплодием (патент № 2152210 РФ. Способ лечения бесплодия у мужчин. Заявл. 28.10.1996 г, опубл. 10.07.2000 г. Бюл. № 19). У пациентов нормализовался гормональный фон, улучшались показатели спермо граммы, репродуктивной и копулятивной функций (улучшение эрекции, оргазма). Незначительное и непостоянное положительное действие ГБО на сперматогенез у больных с бесплодием было связано, очевидно, с тяжелыми морфологическими и функциональными изменениями в яичках. ГБО обладает универсальным воздействием на организм на субклеточном, клеточном и тканевом уровнях. Ранее мы получили данные об активации продукции гонадотропных гормонов и тестостерона у мужчин с бесплодием под влиянием ГБО: о его положительном воздействии на энергетику сперматозоидов и процессы спермофагии, о снижении дегенеративных форм спермиев, усилении биохимического компонента антиоксидантной защиты.
Однако следует учитывать, что лечебное действие метода ГБО реализуется через механизмы гипероксии и, таким образом, мало отличается от токсического. В условиях исходного повреждения трофической и защитной функций гематотестикулярного барьера (морфологически — это оболочка семенных канатиков и цитоплазма сустентоцитов) лечебные эффекты гипероксии уступают повреждающим эффектам, а антиоксидантная защита организма оказывается несостоятельной.
В клинической практике имеется большой опыт использования препаратов-антиоксидантов в сочетании с ГБО при печеночной недостаточности и черепномозговых травмах [15, 16]. Резонно также предположить, что по мере утяжеления степени расстройств сперматогенеза необходимо усиление антиоксидантной защиты.
Участие оксидативного стресса в патогенезе мужского бесплодия предопределило изучение эффективности различных антиоксидантов (витаминов, микроэлементов) в лечении данного заболевания [17, 18]. Антиоксиданты защищают организм от свободных радикалов, которые образуются как в результате естественных физиологических процессов, так и при патологических изменениях [19—21].
Последние несколько лет в качестве средств 1-й линии терапии мужской инфертильности часто используются биологически активные добавки (БАД). По регистрационной форме эти препараты не являются лекарствами, но в своем составе часто содержат витамины, аминокислоты и микроэлементы в количестве, достаточном для восстановления качества эякулята. К таким БАДам относятся комбинированный препарат для повышения мужской фертильности Сперотон и антиоксидантный комплекс Синергин (оба — производства компании «АКВИОН», Россия).
Свойства компонентов, входящих в состав Сперотона
L-карнитин — наиболее важный биохимический маркер нормального созревания сперматозоидов, продуцируется придатком яичка [22, 23]. Также установлено, что L-карнитин обладает антиоксидантной активностью за счет удаления токсичного внутриклеточного ацетилкофермента А и стабилизации клеточной мембраны сперматозоидов, чья целостность нарушается под действием активных форм кислорода, гиперпродукция которых является важным патогенетическим фактором патоспермии у мужчин [24, 25]. Физиологическая роль L-карнитина достаточно полно изучена в последние десятилетия. Потребность в нем индивидуальна для каждого человека и зависит от физических и эмоциональных нагрузок. Известно, что эндогенная секреция L-карнитина составляет лишь 25 % от суточной потребности, в то время как 75 % L-карнитина должны поступать с пищей. Он содержится во многих тканях человека, но наибольшей концентрации достигает в эпидидимальном секрете (его присутствие необходимо для созревания сперматозоидов). Недостаточное потребление L-карнитина может являться одной из причин патозооспермии.
Витамин Е (а-токоферол) — наиболее распространенный антиоксидант в природе. Является липофильной молекулой, способной инактивировать свободные радикалы непосредственно в гидрофобном слое мембран и таким образом предотвращать развитие цепи перекисного окисления. Различают 8 типов токоферолов, но тип а наиболее активен. Витамин Е (а-токоферол) ингибирует свободнорадикальное окисление путем отдачи электрона, что приводит к инактивации радикала липида и превращению витамина Е в стабильный, полностью окисленный токоферолхинон.
Цинк — важный микроэлемент, металл, который необходим для нормального функционирования мужской репродуктивной системы, его дефицит приводит к снижению уровня тестостерона и, соответственно, патозооспермии. Цинк преимущественно секретируется в предстательной железе, в большом количестве содержится в созревающих сперматозоидах, поскольку его количество коррелирует с уровнем потребления кислорода и стабильностью ядерного хроматина. Цинк является кофактором большой группы ферментов и по этому необходим для протекания многих биохимических процессов. Он стимулирует производство у-интерферона, необходимого для правильного функционирования иммунной системы, снижает уровень свободных радикалов, обеспечивает общую защиту от старения, действуя как антиоксидант [26].
Селен является микроэлементом, способным уменьшать окислительный стресс. Он необходим для созревания сперматозоидов и нормального развития яичек. При дефиците селена процесс сперматогенеза нарушается за счет атрофии сперматогенного эпителия. Патологические изменения сперматозоида, по-видимому, локализуются преимущественно в средней части и головке клетки. Было показано, что прием добавок с селеном способствует увеличению подвижности сперматозоидов и снижению их повреждения свободными радикалами. Ведущий механизм развития последствий селенового дефицита заключается в повреждении клеточных мембран из-за перекисного окисления липидов (ПОЛ), обусловленного снижением активности фермента глутатионпероксидазы, активным центром которого является селен [27, 28].
Витамин B9 (фолиевая кислота) — водорастворимый витамин, хорошо растворяется в воде при щелочных значениях pH, легко разрушается при тепловой обработке и на свету. Витамины группы В составляют самую обширную группу отдельных витаминов. Они выполняют роль кофакторов, участвующих в работе ферментов, способствуют переносу метильных, метиленовых и формильных групп в клетку. Фолиевая кислота незаменима для синтеза ДНК и, следовательно, способствует усилению сперматогенеза и увеличению стабильности сперматозоидов, уменьшая фрагментацию ДНК. При низких уровнях этой кислоты наблюдается снижение количества и подвижности сперматозоидов. Она играет важную роль в сперматогенезе, влияя на объем эякулята и качество спермы. Прием фолиевой кислоты помогает уменьшить количество дефектных сперматозоидов, а следовательно, снижает риск рождения ребенка с генными аномалиями.
Свойства компонентов, входящих в состав Синергина
Убихинон (коэнзим Q10) — это кофермент, который синтезируется в организме человека и является одним из мощнейших антиоксидантов. Его антиокислительная активность фактически в 2 раза превышает активность других антиоксидантов. Главным преимуществом этого соединения является то, что он способен восстанавливаться из окисленной формы в отличие от других жирорастворимых антиоксидантов, например витамина A. Именно восстановленная форма коэнзима Q10 предотвращает разрушение мембран в липопротеинах низкой плотности, липосомах и ДНК. Защищая клетки от пагубного воздействия свободных радикалов, коэнзим Q10 обеспечивает нормальное протекание жизненно важных обменных процессов организма. Убихинон также участвует в выработке энергии в митохондриях и поэтому необходим сперматозоидам, энергетические потребности которых особенно высоки.
Ликопин — пигмент, относится к природным соединениям группы каротиноидов. Ликопин не синтезируется в человеческом организме, он поступает только с пищей. Биологическая активность ликопина связана прежде всего с его антиоксидантными свойствами, т. е. со способностью ингибировать свободнорадикальные процессы в клетках. Особый интерес представляют данные о том, что ликопин может прямо реагировать на перекисные радикалы, участвуя, таким образом, в процессе окисления липидов. Механизм действия этого пигмента заключается в его способности функционировать как антиоксидант, выводящий перекисные радикалы из сферы цепных свободнорадикальных реакций.
Рутин (витамин Р) является мощным природным антиоксидантом. Он защищает капилляры, уменьшает их повышенную проницаемость, укрепляет стенки сосудов, снижает их отечность и воспаление, что способствует улучшению кровоснабжения всего организма. Рутин обладает антиагрегационным действием, способствуя улучшению микроциркуляции во всех органах и тканях. Его прием снижает степень венозной недостаточности. Рутин полезен пациентам с сахарным диабетом и другими заболеваниями, связанными с ок сидативным стрессом [29].
Витамин С (аскорбиновая кислота, АК) — это антиоксидант, который участвует в ингибировании ПОЛ, реализуя 2 различных механизма: во-первых, восстанавливает окисленную форму витамина Е и таким образом поддерживает необходимую концентрацию этого антиоксиданта непосредственно в мембранах клеток, и, во-вторых, будучи водорастворимым витамином и сильным восстановителем, взаимодействует с водорастворимыми активными формами кислорода и инактивирует их.
β-каротин — предшественник витамина А, обладает антиоксидантным действием и ингибирует ПОЛ. β-каротин, а также каротиноиды, не способные к образованию витамина А, выполняют антиоксидантные функции за счет наличия изопреноидных участков. Они являются достаточно эффективными ловушками для синглетного кислорода (в особенности при низком парциальном давлении последнего). Кроме того, в этом случае они могут действовать иначе, выступая в качестве антиоксидантных соединений, обрывающих цепи ПОЛ. Эти вещества оказывают мощное антиоксидантное действие, стимулируют сперматогенез и увеличивают подвижность сперматозоидов. В то же время механизм их антиоксидантного эффекта недостаточно изучен. Представляется, что одну из ведущих ролей при этом играет нормализация тиол-дисульфидного и аскорбатного обменов в органах репродуктивной системы.
Цель настоящей работы — оптимизация результатов применения ГБО в комбинированном лечении пациентов с идиопатическими нарушениями спермограммы с проявлениями олигоастенотератозооспермии. При этом в задачи исследования входило изучение показателей тиол-дисульфидного и аскорбатного обменов, ПОЛ, супероксиддисмутазы (СОД) в плазме и эякуляте больных с бесплодием и изменений этих показателей при использовании ГБО в сочетании с препаратами Сперотон и Синергин в лечении патоспермии.
Материалы и методы
В исследовании приняли участие 155 мужчин в возрасте от 20 до 45 лет, из которых у 120 мужчин установлено идиопатическое бесплодие, а остальные 35 были практически здоровы.
Критериями включения в группы исследования являлись:
- ненаступление/отсутствие беременности у партнера в браке более 12 мес половой жизни без контрацепции;
- идиопатическая форма бесплодия (олигоастеноте ратозооспермия);
- неинфицированность (Chlamydia trachomatis, Mycoplasma hominis, Trichomonas vaginalis, Ureaplasma urealiticum) репродуктивного тракта, диагностированная методом полимеразной цепной реакции;
- отсутствие клинических и лабораторных признаков воспалительного процесса дополнительных половых желез;
- отсутствие аутоиммунных реакций против сперматозоидов, сопровождающихся выработкой анти спермальных антител;
- концентрация сперматозоидов не менее 10 млн/мл;
- отсутствие эякуляторных нарушений;
- отсутствие травм половых органов;
- отсутствие выраженной соматической патологии;
- способность пациента понять суть клинического исследования и дать письменное согласие на участие в нем.
- обтурационная (кроме варикоцеле) или иммунологическая форма бесплодия;
- наличие женского бесплодия у партнерши (непроходимость маточных труб, нарушения овуляции, распространенный эндометриоз и др.);
- возраст младше 20 и старше 45 лет;
- алкогольная или наркотическая зависимость;
- повышенная чувствительность к любому из компонентов препаратов;
- нарушения функции печени и почек;
- участие в другом клиническом исследовании в последние 3 мес.
Курс ГБО состоял из 10 ежедневных сеансов продолжительностью 60 мин. Каждый сеанс проводился при давлении 1,5—2,0 АТА (0,15198-0,20265 МПа). Использовалась одноместная терапевтическая барокамера «ОКА-МТ» («Технодинамика», Россия).
В качестве основного критерия оценки эффективности проводимой терапии использовали спермограм му. Исследование спермы проводили по стандартной методике до начала терапии и через 3 мес от начала приема препаратов, при этом ее основные параметры оценивали в соответствии с требованиями руководства Всемирной организации здравоохранения [30], объем эякулята, концентрацию, подвижность и морфологию сперматозоидов - по строгим критериям Крюгера.
У всех больных в каждой из 4 групп до лечения, через 1 и 3 мес исследовали в плазме крови и эякуляте изменения уровней:
- малонового диальдегида (МДА);
- окисленных дисульфидных (SS) групп тиоловых соединений;
- окисленных форм АК (ОФАК), служащих критерием интенсивности процессов ПОЛ и свободнорадикального окисления, а также СОД;
- АК;
- восстановленных сульфгидрильных (SH) групп тиолов, дающих информацию об активности антиоксидантной защиты.
Результаты и обсуждение
Полученные данные свидетельствуют о существенных изменениях состояния антиоксидантных процессов у пациентов, вошедших в исследование. Следует особо отметить, что изменения показателей тиол-дисульфидного и аскорбатного обменов оказались более выраженными в эякуляте по сравнению с аналогичными показателями в плазме крови. Так, у пациентов исходно (до лечения) уровень SH-групп в плазме крови был снижен в 1,7 раза по сравнению с нормальными показателями, коэффициент SH/SS был равен 1,10 ± 0,14 (при норме 2,16 ± 0,10) (табл. 1). В эякуляте содержание SH-групп было ниже нормальных значений в 2,5 раза, причем коэффициент SH/SS составлял 0,94 ± 0,15 (при норме 2,20 ± 0,12) (табл. 2).
Содержание АК в плазме крови у больных с пато спермией было ниже нормальных значений в 1,6 раза при увеличении ОФАК в 1,2 раза (коэффициент АК/ОФАК составлял 0,47 ± 0,04 при норме 0,95 ± 0,01). В эякуляте этот показатель был меньше в 2 раза (17,3 ± 1,51 при норме 36,2 ± 1,20), а коэффициент АК/ОФАК — ниже нормы в 2,8 раза (см. табл. 1 и 2).
Таблица 1.
Влияние терапии ГБО в сочетании с приемом препарата Сперотон на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в плазме крови у больных с бесплодием в 1-й группе, n = 40
Table 1.
Effect of HBOT in combination with Speroton administration on free radical oxidation, lipid peroxidation, and antioxidant activity in plasma of patients with infertility in the 1st group, n = 40
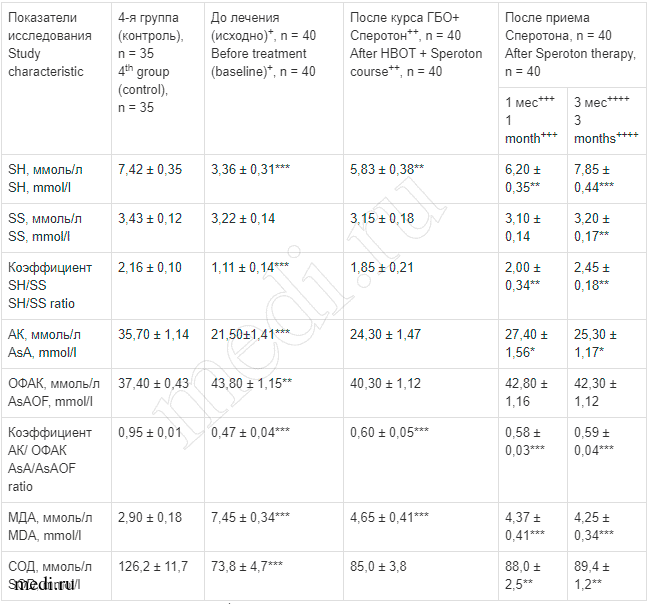 Примечание. Здесь и в табл. 2: знак «+» обозначает сравнение исследуемых показателей фона в 1-й группе с аналогичными показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Сперотон с исходными значениями в 1-й группе;«+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Сперотона с исходными значениями в 1-й группе.
Примечание. Здесь и в табл. 2: знак «+» обозначает сравнение исследуемых показателей фона в 1-й группе с аналогичными показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Сперотон с исходными значениями в 1-й группе;«+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Сперотона с исходными значениями в 1-й группе.Здесь и в табл. 2-7: * -р <0,05; ** - р <0,01; *** - р <0,001.
Здесь и в табл. 2 и 4-7: SS и SH- соответственно окисленные дисульфидные и восстановленные сульфгидрильные группы тиоловых соединений, АК - аскорбиновая кислота, ОФАК - окисленные формы АК, МДА - малоновый диальдегид, СОД -супероксиддисмутаза.
Note. Here and in Table 2:+ denotes comparison between the studied baseline characteristics in the 1st group with the characteristics in the control group(norm), ++ denotes comparison of the studied characteristics after HBOT + Speroton treatment with the baseline characteristics in the 1st group; +++ and ++++ denote comparison of the studied characteristics 1 and 3 months after Speroton administration, respectively, with the baseline characteristics in the 1st group. Here and in Tables 2-7: * - р <0.05; ** - р <0.01; *** - р <0.001.
Here and in Tables 2 and 4-7: SS and SH stand for oxidized disulfide and reduced sulfhydryl groups of thiol compounds, respectively; AsA - ascorbic acid; AsAOF - oxidized forms of ascorbic acid; MDA - malondialdehyde; SOD - superoxide dismutase.
Таблица 2.
Влияние терапии ГБО в сочетании с препаратом Сперотон на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в эякуляте у больных с бесплодием в 1-й группе, n = 40
Table 2.
Effect of HBOT in combination with Speroton on changes in free radical oxidation, lipid peroxidation, and antioxidant activity in ejaculate of patients with infertility in the 1st group, n = 40
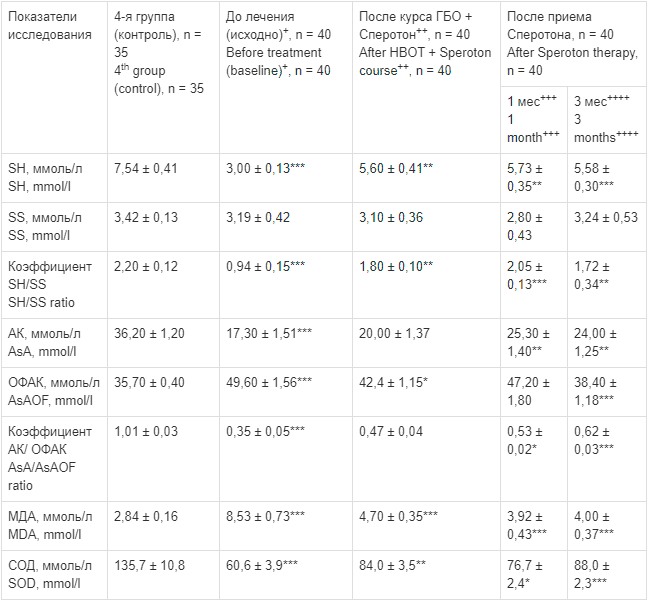
Таким образом, выраженные изменения тиолдисульфидного и аскорбатного обменов отмечались в эякуляте у пациентов с патоспермией. Исходно содержание МДА в плазме крови превышало норму в 2,5 раза, в эякуляте — в 3 раза при сниженном содержании СОД в плазме в 1,7 раза, а в эякуляте — в 2,26 раза.
После курса ГБО в сочетании с приемом антиоксиданта Сперотон уровень SH-групп в плазме крови повышался в 1,34 раза, через 1 мес приема препарата — в 1,42 раза. Через 3 мес данный уровень примерно в 2 раза превысил исходные показатели, достигнув практически нормальных значений (см. табл. 1). При этом содержание SS-групп достоверно снижалось как в плазме крови, так и в эякуляте, а изменения уровня SH-групп в эякуляте после применения Сперотона в системе с ГБО были значительными, достоверно положительными и особенно выраженными после 3 мес приема препарата (см. табл. 2).
По мере проведения курса лечения уровень МДА в плазме крови постепенно и достоверно снижался (уменьшился в 1,75 раза по сравнению с нормой), содержание СОД увеличилось (в 1,13 раза превысило нормальные значения), а в эякуляте уровень МДА снизился в 2,15 раза, а содержание СОД увеличилось в 1,5 раза.
Таким образом, прием препарата Сперотон во время проведения ГБО и затем в течение 3 мес значительно и высокодостоверно активирует тиол-дисульфидный обмен в репродуктивных органах и незначительно поднимает уровень АК, что приводит к повышению концентрации сперматозоидов, увеличению количества их подвижных форм и снижению количества их дегенеративных форм (табл. 3).
Таблица 3.
Основные показатели спермограммы у больных с бесплодием после применения ГБО в сочетании с препаратом Сперотон и комплексом Синергин, N = 120
Table 3.
The main sperm characteristics in patients with infertility after HBOT in combination with Speroton and Sinergine, N = 120
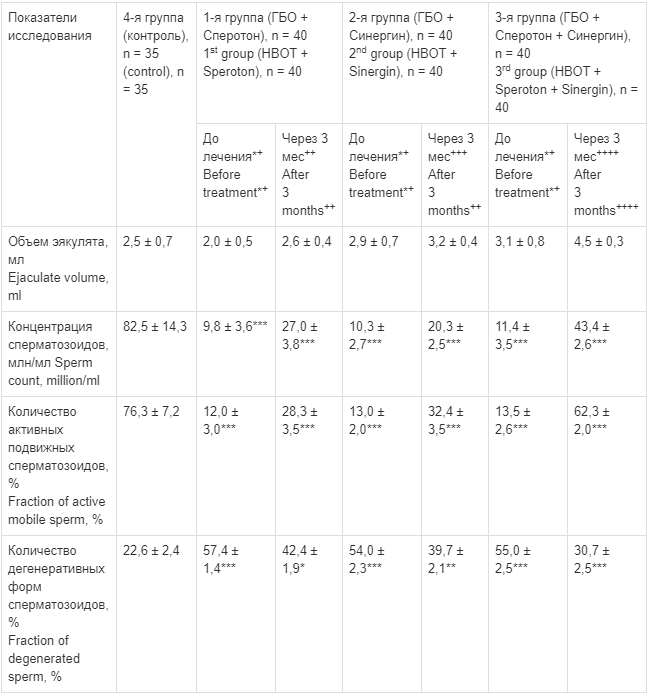 Примечание. Знак «+» обозначает сравнение исходных значений показателей спермограммы больных в каждой группе с показателями контрольной группы (норма), «++» — сравнение показателей спермограммы после курса ГБО + Сперотон с исходными значениями в 1-й группе, «+++» — сравнение показателей спермограммы после курса ГБО + Синергин с исходными значениями во 2-й группе, «++++» — сравнение показателей спермограммы после курса ГБО + Сперотон + Синергин с исходными значениями в 3-й группе.
Примечание. Знак «+» обозначает сравнение исходных значений показателей спермограммы больных в каждой группе с показателями контрольной группы (норма), «++» — сравнение показателей спермограммы после курса ГБО + Сперотон с исходными значениями в 1-й группе, «+++» — сравнение показателей спермограммы после курса ГБО + Синергин с исходными значениями во 2-й группе, «++++» — сравнение показателей спермограммы после курса ГБО + Сперотон + Синергин с исходными значениями в 3-й группе.Note. + denotes comparison of the baseline sperm characteristics of patients in each group with the control group (norm), ++ denotes comparison of the studied characteristics after HBOT + Speroton treatment with the baseline characteristics in the 1st group; +++ denotes comparison of the studied characteristics after HBOT + Sinergin treatment with the baseline characteristics in the 2st group, ++++ denotes comparison of the studied characteristics after HBOT + Speroton + Sinergin treatment with the baseline characteristics in the 3rd group.
После курса ГБО в сочетании с приемом антиоксидантного комплекса Синергин количество SH-групп в плазме крови увеличивалось по сравнению с исходным фоном, но малодостоверно (табл. 4). Через 1 мес приема Синергина уровень SH-групп в плазме крови практически не изменился, и только после 3-месячной терапии этим препаратом содержание SH-групп в плазме крови повышалось достоверно по сравнению с исходным фоном (6,20 ± 0,20 ммоль/л против 4,35 + 0,31 ммоль/л) (см. табл. 4). Содержание SS-групп в плазме крови практически не изменялось на всех этапах исследования, оставаясь на уровне исходного фона. В то же время уровень АК в плазме крови высокодостоверно повышался как после курса ГБО + Синергин, так и через 1 и 3 мес применения Синергина при столь же достоверном снижении содержания ОФАК, а коэффициент АК/ОФАК приближался к значениям контрольной группы (т. е. к норме) (см. табл. 4).
Таблица 4.
Влияние терапии ГБО в сочетании с антиоксидантным комплексом Синергин на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в плазме крови у больных с бесплодием во 2-й группе, n = 40
Table 4.
Effect of HBOT in combination with Sinergin antioxidant complex on changes in free radical oxidation, lipid peroxidation, and antioxidant activity in plasma of patients with infertility in the 2nl group, n = 40
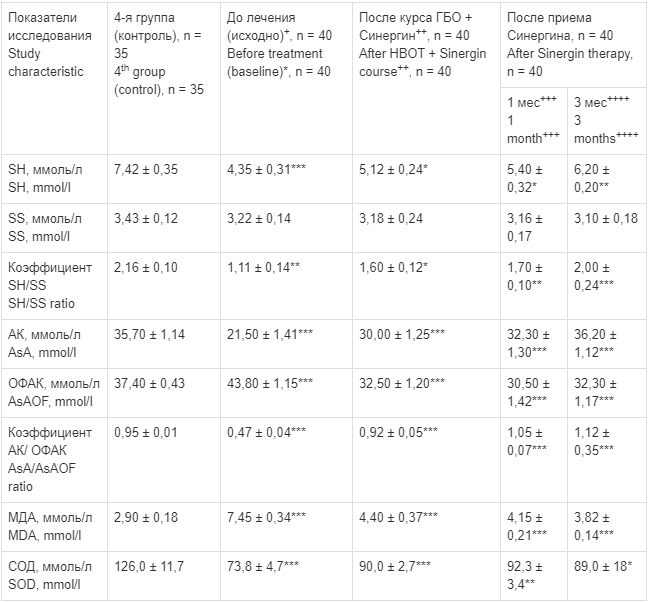 Примечание. Здесь и в табл. 5: знак «+» обозначает сравнение исходных значений исследуемых показателей во 2-й группе с показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Синергин с исходными значениями во 2-й группе, «+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Синергина с исходными значениями во 2-й группе.
Примечание. Здесь и в табл. 5: знак «+» обозначает сравнение исходных значений исследуемых показателей во 2-й группе с показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Синергин с исходными значениями во 2-й группе, «+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Синергина с исходными значениями во 2-й группе.Note. Here and in Table 5:+ denotes comparison between the studied baseline characteristics in the 2nd group with the characteristics in the control group (norm), ++ denotes comparison of the studied characteristics after HBOT + Sinergin treatment with the baseline characteristics in the 2nd group; +++ and ++++ denote comparison of the studied characteristics 1 and 3 months after Sinergin administration, respectively, with the baseline characteristics in the 2nd group.
У больных 2-й группы содержание МДА в плазме крови на всем протяжении терапии было достоверно снижено при высокодостоверном увеличении количества СОД (см. табл. 4). Уровень SH-групп в эякуляте после курса ГБО с антиоксидантным комплексом Синергин повышался, но малодостоверно. Только через 3 мес терапии количество SH-групп в эякуляте достоверно увеличивалось (с 3,00 ± 0,13 до 5,43 ± 0,38 ммоль/л). Содержание SS-групп в эякуляте на всем протяжении исследования при приеме Синергина практически не изменялось (табл. 5).
Таблица 5.
Влияние терапии ГБО в сочетании с антиоксидантным комплексом Синергин на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в эякуляте у больных с бесплодием во 2-й группе, n = 40
Table 5.
Effect of HBOT in combination with Sinergin antioxidant complex on changes in free radical oxidation, lipid peroxidation, and antioxidant activity in ejaculate of patients with infertility in the 2nd group, n = 40
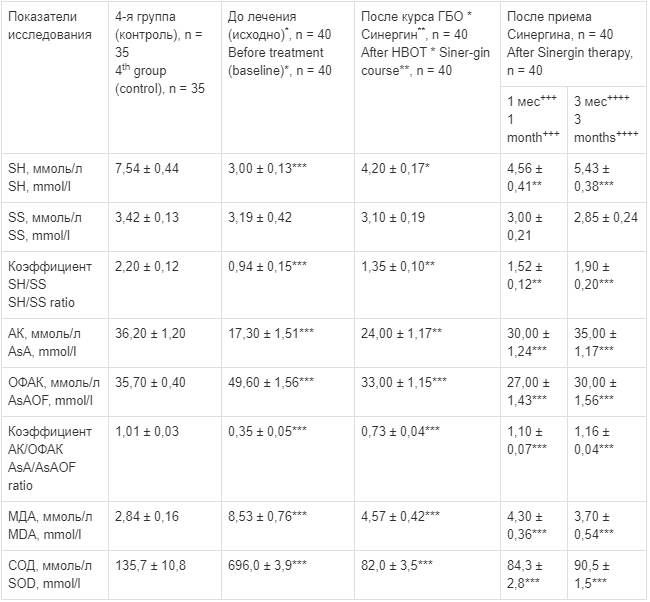
Следует особо подчеркнуть, что при приеме антиоксидантного комплекса Синергин значительно и высокодостоверно повышался уровень АК в эякуляте на всех этапах исследования (см. табл. 5), при этом резко и с высокой достоверностью уменьшалось содержание МДА и повышался уровень СОД. Так, после курса ГБО с Синергином содержание АК в эякуляте увеличивалось в 1,38 раза по сравнению с исходным значением, а через 1 и 3 мес терапии этим комплексом — в 1,78 и 2 раза соответственно. При этом уровень ОФАК по соответствующим этапам исследования снижался в 1,5, 1,86 и 1,65 раза (см. табл. 5).
После курса ГБО с антиоксидантным комплексом Синергин увеличивалось количество сперматозоидов в эякуляте высокодостоверно по сравнению с исходными значениями (до лечения) и возрастало число подвижных сперматозоидов при снижении уровня их дегенеративных форм (см. табл. 3).
Полученные данные позволяют сделать вывод о том, что использование Синергина в качестве антиоксиданта оказывает положительный эффект за счет повышения содержания АК как в плазме крови, так и в эякуляте.
Есть основания полагать, что для наиболее выраженного положительного результата в качестве антиоксидантной защиты при ГБО (и в последующем) следует применять комбинацию Сперотона с Синергином: Сперотон способствует повышению уровня SH-групп, а Синергин — повышению содержания АК как в плазме крови, так и в эякуляте, что особенно важно.
Результаты приема препаратов Сперотон и Синергин совместно с проведением ГБО и в последующие 3 мес показали, что именно такое сочетание антиоксидантов после курса ГБО обеспечивает надежную антиоксидантную защиту, достоверное увеличение содержания сперматозоидов в эякуляте, способствует повышению количества их подвижных форм и уменьшению количества дегенеративных форм (см. табл. 3).
Так, уровень SH-групп в плазме крови после курса ГБО в сочетании с Синергином и Сперотоном был выше исходного значения в 1,5 раза, через 1 мес использования антиоксидантов — в 1,7 раза, а через 3 мес — в 1,8 раза, значительно превышая показатели контрольной группы (см. табл. 5). При этом уровень SS-групп и величина коэффициента SH/SS были в пределах нормы (табл. 6).
Такие же положительные изменения в плазме крови у пациентов этой группы отмечались и в динамике колебания уровня АК: после курса ГБО в сочетании с антиоксидантами содержание АК увеличивалось, но незначительно (26,00 ± 1,37 ммоль/л при исходном значении 21,50 ± 1,41 ммоль/л), однако через 1 мес приема антиоксидантов содержание АК в плазме крови достоверно увеличивалось, достигая максимума через 3 мес проводимой терапии (см. табл. 6).
Таблица 6.
Влияние терапии ГБО в сочетании с приемом препаратов Сперотон и Синергин на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в плазме крови у больных с бесплодием в 3-й группе, n = 40
Table 6.
Effect of HBOT in combination with Speroton and Sinergin on changes in free radical oxidation, lipid peroxidation, and antioxidant activity in plasma of patients with infertility in the 3nd group, n = 40
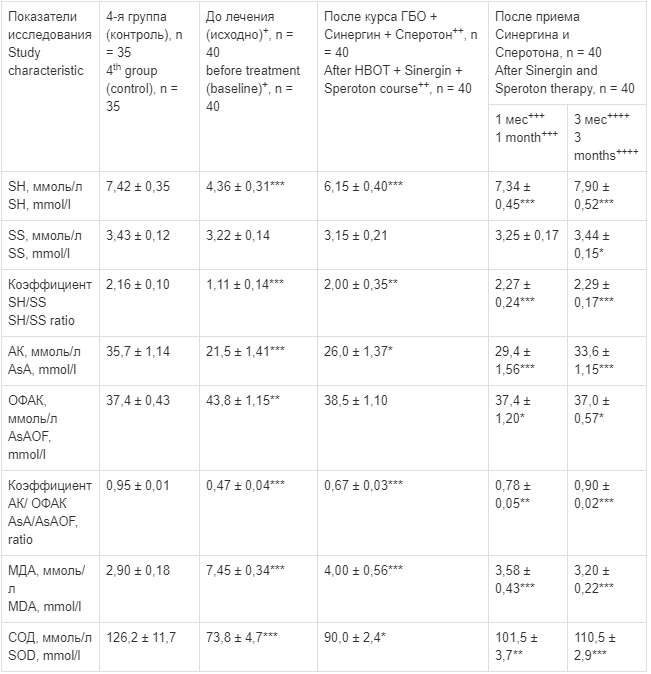 Примечание. Здесь и в табл. 7: знак «+» обозначает сравнение исходных значений исследуемых показателей у больных в 3-й группе с показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Синергин + Сперотон с исходными значениями в 3-й группе, «+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Синергина и Сперотона с исходными значениями в 3-й группе.
Примечание. Здесь и в табл. 7: знак «+» обозначает сравнение исходных значений исследуемых показателей у больных в 3-й группе с показателями в контрольной группе (норма), «++» — сравнение исследуемых показателей после курса ГБО + Синергин + Сперотон с исходными значениями в 3-й группе, «+++» и «++++» — сравнение исследуемых показателей соответственно через 1 и 3 мес приема Синергина и Сперотона с исходными значениями в 3-й группе.Note. Here and in Table 7: + denotes comparison between the studied baseline characteristics in the 3rd group with the characteristics in the control group (norm), ++ denotes comparison of the studied characteristics after HBOT + Sinergin + Speroton treatment with the baseline characteristics in the 3rd group; +++ and ++++ denote comparison of the studied characteristics 1 and 3 months after Sinergin and Speroton administration, respectively, with the baseline characteristics in the 3rd group.
Подобные положительные эффекты со стороны тиол-дисульфидного и аскорбатного обменов у больных этой группы отмечались и в эякуляте. Уровень SH-групп и содержание АК значительно и достоверно повышались по мере проведения терапии, а количество SS-групп достоверно уменьшалось. Как в плазме крови, так и в эякуляте на всех этапах терапии уровень МДА достоверно снижался, содержание СОД достоверно увеличивалось (табл. 7).
Таблица 7.
Влияние терапии ГБО в сочетании с приемом препаратов Сперотон и Синергин на изменения показателей свободнорадикального окисления, перекисного окисления липидов и антиоксидантной активности в эякуляте у больных с бесплодием в 3-й группе, n = 40
Table 7.
Effect of HBOT in combination with Speroton and Sinergin on changes in free radical oxidation, lipid peroxidation, and antioxidant activity in ejaculate of patients with infertility in the 3rd group, n = 40
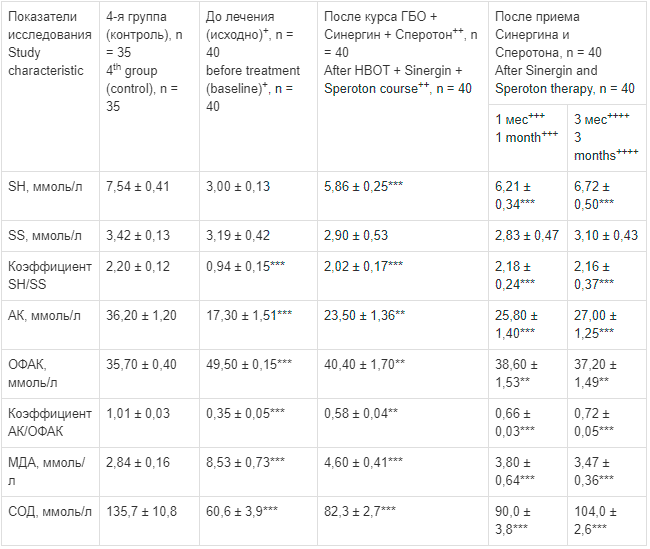
В 3-й группе объем эякулята у больных под влиянием проводимой терапии достоверно увеличился.
У больных в 1-й группе (ГБО + Сперотон) концентрация сперматозоидов в эякуляте после курса лечения увеличилась по сравнению с исходными значениями (до лечения) в 3 раза, количество подвижных форм сперматозоидов — в 2,4 раза, а количество их дегенеративных форм уменьшилось в 1,3 раза.
У больных 2-й группы (ГБО + Синергин) концентрация сперматозоидов в эякуляте после курса лечения увеличилась по сравнению с исходными значениями (до лечения) в 2,2 раза, количество подвижных форм сперматозоидов — в 2,7 раза, количество их дегенеративных форм уменьшилось в 1,4 раза.
Концентрация сперматозоидов в эякуляте больных в 3-й группе после курса ГБО в сочетании со Сперото ном и Синергином увеличилась по сравнению с исходными значениями (до лечения) в 4,7 раза, количество подвижных форм — в 5,3 раза, количество дегенеративных форм уменьшилось в 1,8 раза.
Выводы
1. В результате проведенного исследования достоверно установлено положительное влияние препарата Сперотон и антиоксидантного комплекса Синергин на функциональное состояние мужской репродуктивной системы, улучшение качественных и количественных показателей спермограммы (объем эякулята, концентрация сперматозоидов, количество подвижных и дегенеративных форм) у мужчин с идиопатической патозооспермией.
2. Применение препарата Сперотон в процессе курса ГБО и в последующие 3 мес способствует нормализации тиол-дисульфидного обмена как в плазме крови, так и в репродуктивных органах (уровень SН-групп в плазме крови и эякуляте после курса терапии приближается к нормальным значениям).
3. Применение Синергина значительно и высокодостоверно повышает уровень восстановленной формы АК в плазме крови и эякуляте на всех этапах исследования.
4. Совместный прием Сперотона и Синергина при проведении курса ГБО и в течение 3 мес после его окончания высокодостоверно повышает уровень SН-групп, АК, СОД при снижении содержания SS-групп и МДА, способствует нормализации показателей спер мограммы, достоверно увеличивает число сперматозоидов и их подвижных форм, снижает количество дегенеративных форм у пациентов с патоспермией.
5. Полученные при исследовании данные позволяют сделать вывод о том, что при идиопатическом мужском бесплодии одним из механизмов антиоксидантной защиты при сочетанном применении препаратов Сперотон и Синергин на фоне ГБО является активация тиол-дисульфидного и аскорбатного обменов как в плазме крови, так и на уровне репродуктивных органов. Можно предположить, что увеличение количества SH-групп и АК — результат синтеза этих биологических активных субстратов из эндотелия сосудов микроциркуляции и клеток белой крови, в том числе и из сосудов репродуктивных органов под воздействием компонентов препаратов Сперотон и Синергин. Комбинированный прием Сперотона и Синергина показал высокую эффективность в коррекции количественных и качественных показателей эякулята и может быть рекомендован в качестве терапии различных форм патозооспермии.
6. Прием Сперотона и Синергина не вызвал каких-либо нежелательных явлений.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Conflict of interests. Authors declare no conflict of interest.
ЛИТЕРАТУРА/REFERENCES
1. Сухих Г.Т., Божедомов В.А. Мужское бесплодие. М.: Эксмо, 2008. [Sukhikh G.T., Bozhedomov V.A. Male infertility. Moscow: Eksmo, 2008. (In Russ.)].
2. Божедомов В.А., Торопцева М.В., Ушакова И.В. Активные формы кислорода и репродуктивная функция мужчин. Фундаментальные и клинические аспекты (обзор литературы). Андроло гия и генитальная хирургия 2011;3:10-6. [Bozhedomov V.A., Toroptseva M.V., Ushakova I.V Reactive oxygen species and male reproductive function. Basic and clinical aspects (literature review). Andro logiya i genitalnaya khirurgiya = Andrology and Genital Surgery 2011;3:10-6. (In Russ.)].
3. Калинина С.Н. Роль заболеваний, передающихся половым путем, в бесплодном браке. Урология и нефрология 1997;1:37-9. [Kalinina S.N. The role of sexually transmitted diseases in infertile marriage. Urologiya i nefrologiya = Urology and Nephrology 1997;1:37-9. (In Russ.)].
4. Гамидов С.И., Иремашвили В.В., Тхагапсоева Р.А. Мужское бесплодие: современное состояние проблемы. Фар матека 2009;9:12-7. [Gamidov S.I., Irema shvili V.V., Tkhagapsoeva R.A. Male infertility: Current state of the problem. Farmateka = Pharmateca 2009;9:12-7. (In Russ.)].
5. Рутинский А.И. Особенности диагностики идиопатического мужского бесплодия (обзор литературы). Медикосоциальные проблемы семьи 2013;18(1):116-21. [Rutinsky A.I. Diagnostic features of idiopathic male infertility (literature review). Mediko-sotsialnie problemy semyi = Medical and Social Problems of Family 2013;18(1):116-21. (In Russ.)].
6. Sabanegh E.J., Agarwal A. Male infertility. In: Campbell-Walsh urology. 10th ed. Eds.: M.F. Campbell, P.C. Walsh, A.J. Wein. Philadelphia: Saunders Elsevier, 2012. P. 616-647.
7. Jung J.H., Seo J.T. Empirical medical therapy in idiopathic male infertility: Promise or panacea? Clin Exp Reprod Med 2014;41(3):108-14. DOI: 10.5653/ cerm.2014.41.3.108. PMID: 25309854.
8. Imamovic Kumalic S., Pinter B. Review of clinical trials on effects of oral antioxidants on basic semen and other parameters in idiopathic oligoasthenoteratozoo spermia. Biomed Res Int 2014;2014: 426951. DOI: 10.1155/2014/426951. PMID: 24800224.
9. Божедомов В.А., Николаева М.А., Теодорович О.В. Нормализация акро сомальной реакции сперматозоидов в результате комплексной терапии карнитином, фруктозой и лимонной кислотой. Проблемы репродукции 2005;4:84-7. [Bozhedomov V.A., Nikolaeva M.A., Teodorovich O.V Normalization of sperm acrosome reaction as a result of combination therapy with carnitine, fructose, and citric acid. Problemy re produktsii = Russian Journal of Human Reproduction 2005;4:84-7. (In Russ.)].
10. Lenzi A., Lombardo F., Sgro P. et al. Use of carnitine therapy in selected cases of male factor infertility: a double-blind crossover trial. Fertil Steril 2003;79(2): 292-300. PMID: 12568837.
11. Sigman M., Glass S., Compagnone J., Pryor J.L. Carnitine for the treatment of idiopathic asthenospermia: a randomized, double-blind, placebo-controlled trial. Fertil Steril 2006;85(5):1409-14. DOI: 10.1016/j.fertnstert.2005.10.055. PMID: 16600222.
12. Кореньков Д.Г. Применение гипербарической оксигенации у больных с бесплодием. В кн.: Сексология и андрология. Вып. 1. Киев, 1992. С 97-8. [Korerkov D.G. Use of hyperbaric oxygen therapy in infertile patients. In: Sexology and Andrology. Issue 1. Kiev, 1992. P. 97-98. (In Russ.)].
13. Кореньков Д.Г., Александров В. П., Марусанов В.Е. и др. Влияние гипербарической оксигенации (ГБО) на репродуктивную и копулятивную функции у мужчин. Андрология и генитальная хирургия 2000;1:37. [Korenkov D.G., Aleksandrov V. P., Maru sanov V.E. et al. Effect of hyperbaric oxygen therapy (HBOT) on reproductive and copulative function in men. Andrologiya i genitalnaya khirurgiya = Andrology and Genital Surgery 2000;1:37. (In Russ.)].
14. Кореньков Д.Г., Александров В.П., Марусанов В.Е. Гипербарическая оксигенация и антиоксиданты в лечении аутоиммунного бесплодия у мужчин. Скорая медицинская помощь 2003; 4(2):32-3. Доступно по: szgmu.ru/files/ smp/2003 %E2 %84 %962. pdf. [Korenkov D.G., Aleksandrov V.P., Marusanov V.E. Hyperbaric oxygen therapy and antioxidants in treatment of autoimmune infertility in men. Skoraya meditsinskaya po mosch = Emergency Medical Care 2003; 4(2):32-3. Available at: szgmu.ru/files/ smp/2003 %E2 %84 %962.pdf. (In Russ.)].
15. Андреев Г.Н., Сондорe А.А., Даугу лис Э.К., Тимофеева Б.Я. Некоторые вопросы применения ГБО в сочетании интенсивного лечения недостаточности печени. Современные проблемы. М.: Медицина, 1980. С. 228-36. [Andreev G.N., Sondore A.A., Daugu lis E.K., Timofeeva B.Ya. Selected questions of HBOT use in combination with intensive treatment of liver failure. Current problems. Moscow: Meditsina, 1980. P. 228-236. (In Russ.)].
16. Марусанов В.Е., Мирошниченко А.Г., Николау С.А. и др. Солкосерил в интенсивной терапии тяжелой черепномозговой травмы. Вестник хирургии им. И.И. Грекова 2000;3:37-9. [Marusanov V.E., Miroshnichenko A.G., Nikolau S.A. et al. Solkoseril in intensive care of traumatic brain injury. Vestnik khirurgii imeni I.I. Grekova = I.I. Grekov Surgery Bulletin 2000;3:37-9. (In Russ.)].
17. Нашивочникова Н.А., Крупин В.Н., Селиванова С.А. Антиоксидантная терапия бесплодного брака. Урология 2015;3:71-4. [Nashivochnikova N.A., Krupin V.N., Selivanova S.A. Antioxidant therapy for infertile couples. Urologiya = Urology 2015;3:71-4. (In Russ.)].
18. Сухих Г.Т., Попова А.Ю., Овчинников Р.И., Ушакова И.В. Влияние комплекса Сперотон на функциональные характеристики сперматозоидов у мужчин с идиопатической патоспермией. Проблемы репродукции 2016;40:106-10. [Sukhikh G.T., Popova A.Yu. Ovchinnikov R.I., Ushakova I.V The influence of Speroton on functional characteristics of sperm in men with idiopathic patozoospermia. Problemy Reproduktsii = Problems of Reproduction 2016;40:106-10. (In Russ.)].
19. Калинченко С.Ю., Тюзиков И.А. Практическая андрология. М.: Практическая медицина, 2009. [Kalinchen ko S.Yu., Tyuzikov I.A. Practical andrology. Moscow: Prakticheskaya meditsina, 2009. (In Russ.)].
20. Гамидов С., Авакян А. Идиопатическое бесплодие у мужчин: эпидемиология, этиология, патогенез, лечение. Врач 2013;7:2-4. [Gamidov S., Avakyan A. Idiopathic male infertility: Epidemiology, etiology, pathogenesis, treatment. Vrach = The Doctor 2013;7:2-4. (In Russ.)].
21. Marnett L.J., Riggins J.N., West J.D. Endogenous generation of reactive oxidants and electrophiles and their reactions with DNA and protein. Clin Invest 2003;111(5): 583-93. DOI: 10.1172/JCI18022.PMID: 12618510.
22. Jeulin C., Lewin L. Role of free L-carnitine and acetyl-L-carnitine in post-gonadal maturation of mammalian spermatozoa. Hum Reprod Update 1996;2(2):87-102. PMID: 9079406.
23. Vicari E., Calogero A.E. Effects of treatment with carnitines in infertile patients with prostato-vesiculo-epididymis. Hum Reprod 2001;16(11):2338-42. PMID: 11679516.
24. Loumbakis P., Anezinis P., Evangeliou A. et al. Effect of L-carnitine in patients withasthenospermia. Eur Urol 1996;30(2):255. Abstract 954.
25. Balercia G., Regoli F., Armeni T. et al. Placebo-controlled double blind randomized trial on the use of L-carnitine, L-ace tylcarnitine, or combined L-carnitine and L-acetylcarnitine in men with idiopathic asthenozoospermia. Fertil Steril 2005;84(3):662-71. DOI: 10.1016/ j.fertnstert.2005.03.064. PMID: 16169400.
26. Herzberg M., Lusky A., Blonder J., Frenkel Y. The effect of estrogen replacement therapy on zinc in serum and urine. Obstet Gynecol 1996;87(6):1035-40. PMID: 8649686.
27. Селен в жизни человека и животных. Под ред. Л.П. Никитиной, В.М. Иванова. М.: МП Союзинформбиоло гия,1995. [Selenium in human and animal life. Eds.L. P. Nikitina, V.M. Ivanov. Moscow: MP Soyuzinformbiologiya, 1995. (In Russ.)].
28. Steinbrenner Н., Al-Quraishy S., Dkhil МА et al. Dietary selenium in adjuvant therapy of viral and bacterial infections. Adv Nutr 2015;6(1):73-82. DOI: 10.3945/ an.114.007575. PMID: 25593145.
29. Ковальский И.В., Краснюк И.И., Краснюк И.И. (мл.) и др. Механизмы фармакологического действия рутина (обзор). Химико-фармацевтический журнал 2014;2:3-6. [Koval’skii I. V., Krasnyuk I.I., Krasnyuk I.I. Jr. et al. Pharmacological mechanisms of rutin action (a review). Khimiko-Farmatsevti cheskii Zhurnal = Pharmaceutical Chemistry Journal 2014;2:3-6. (In Russ.)].
30. WHO laboratory manual for the examination of human sperm and semen-cervical mucus interaction. 4nd ed. Cambridge: The Press Syndicate of the University of Cambridge, 1999.
31. Иванов Ю.И., Погорелик О.И. Обработка результатов медико-биологических исследований. М.: Медицина, 1999. [Ivanov Yu.I., Pogorelik O.I. Data analysis for medical and biological studies. Moscow: Meditsina, 1999. (In Russ.)].
Комментарии
ПРАКТИКА ПЕДИАТРА