akvion.ru
akvion.ru
Комбинированный препарат для прегравидарной подготовки женщин со сниженной фертильностью
далее...
Больше информации на сайтах:
www.reproduction.info
www.plan-baby.ru
Прегравидарная подготовка пары. Роль синергизма микронутриентов
СтатьиОпубликовано в журнале:
« Трудный пациент » № 8-9, ТОМ 13, 2015
О.А.Громова1,2, И.Ю.Торшин1, О.А.Лиманова1
1 Ивановская государственная медицинская академия, Иваново
2Российский сателлитный центр Института микроэлементов ЮНЕСКО
Современным трендом преконцептуальной подготовки к успешному зачатию и вынашиванию беременности является совместная подготовка и женщины, и мужчины. Преконцептуальная подготовка женщины к зачатию предполагает не только санацию очагов инфекции, но и обеспечение тонкой настройки гормонального баланса за счет поддержки микронутриентами и использования определенных стандартизированных фитоэкстрактов. Сочетание микронутриентов и фитоэкстрактов является «мягким», но эффективным средством модуляции гормонального баланса, исключающим возможность тератогенеза. Преконцептуальная подготовка мужчины направлена, в частности, на улучшение показателей репродуктивного качества сперматозоидов, на которые весьма влияет адекватная микронутриентная обеспеченность.
Ключевые слова: преконцептуальная подготовка мужчины и женщины к зачатию, стандартизованные экстракты Vitex Agnus-castus, репродуктивное здоровье, антиоксиданты.
Preconception Preparation Pair. The Role of the Synergy of Micronutrients
O.A.Gromova1,2, I.Yu.Torshin1, O.A.Limanowa1
1Ivanovsky National Medecal Academy, Ivanovo
2Russian Satellite Center Trace Element -Ibstitute for UNESCO
The modern trend of preconceptional preparation for successful conception and carrying of a pregnancy is the joint preparation of both the woman and the man. Preconceptional preparation of a woman to conceive implies not only the reorganization of foci of infection, but also providing fine-tuning of hormonal balance by supporting the use of certain micronutrients and standardized phytoextracts. The combination of micronu-trients and phytoextracts is «mild», but an effective means of modulation of hormonal balance, which excludes the possibility of teratogenesis. Preconceptional preparation of a man is directed at improving the quality of reproductive spermatozoa in particular which are highly influenced by adequate micronutrient provision.
Keywords: preconceptional preparation of a man and a woman to conceive, standardized extracts of Vitex Agnus-castus, reproductive health, antioxidants.
Введение
Обеспеченность организмов и будущей матери, и отца всеми необходимыми витаминами, витаминоподобными веществами и микроэлементами - бесспорный фактор, способствующий физиологическому зачатию и течению беременности. Витамины и минералы воздействуют на формирование и состояние яйцеклеток и сперматозоидов, контролируют оплодотворение, имплантацию, эмбриогенез, фетогенез, роды, лактацию и послеродовую реабилитацию [1].
Зачастую к моменту планирования беременности соматическое и репродуктивное здоровье пары требует реабилитационных мер. И «мужское», и «женское» здоровье (в смысле здоровья репродуктивной системы) не может быть рассматриваемо в отрыве от общего соматического здоровья и, прежде всего, от состояния сердечно-сосудистой системы и печени. Эссенциальные нутриенты и фитоэкстракты являются важнейшим фактором оздоровления как репродуктивного, так и соматического здоровья.
Для микронутриентной подготовки к беременности в парах в России была разработана линия из трех препаратов - «Прегнотон», «Сперотон» и «Синергин». Женщинам рекомендуется использовать комбинацию «Прегнотон» + «Синергин», а мужчинам - «Сперотон» + «Синергин», в течение 3 мес до зачатия [2].
Витаминно-минеральный комплекс «Прегнотон», обогащенный стандартизированным экстрактом витекса, особенно рекомендуется для прегравидарной подготовки женщин с гиперпролактинемией. Наряду со стандартизированным экстрактом Vitex Agnus-castus (40 мг), в состав препарата входят фолиевая кислота (520 мкг), цинк (12 мг), витамин С (90 мг), витамин Е (15 мг), селен (55 мкг), витамин В6 (2 мг), и L-аргинин (915 мг). Компоненты «Прегнотона» способствуют снижению риска пороков развития и патологии беременности на ранних сроках, предупреждают внутриутробную инфекцию, позволяют нормализовать менструальный цикл, улучшают состояние эмоциональной сферы.
Препарат «Сперотон» предназначен для повышения мужской фертильности за счет поддержания сперматогенеза и нормальных показателей сперматозоидов. В состав препарата входят L-карнитин (750 мг), фолиевая кислота (400 мкг), витамин Е (30 мг), цинк (21 мг), селен (70 мкг).
Для использования в преконцептуальной подготовке и мужчин, и женщин разработан комплекс «Синергин», включающий набор антиоксидантных витаминов и витаминоподобных веществ. В суточной дозировке (2 капсулы) содержится витамин С (180 мг), витамин Е (15 мг), убихинон (коэнзим Q10, 45 мг), ликопин (5 мг), рутин (30 мг), бета-каротин (5 мг). Данные микронутриенты являются не только антиоксидантами, но проявляют также и другие полезные свойства (например, витамин С участвует в синтезе нитей коллагена, убихинон участвует в процессах клеточного дыхания и др.).
Заметим, что поддержание антиоксидантного ресурса организма весьма важно для преконцептуальной подготовки, так как активные формы кислорода (АФК) приводят к нарастанию окислительного стресса, который крайне негативно сказывается на репродуктивной системе [3]. И сперматозоиды, и ооциты обеспечиваются энергией вследствие так называемого «окислительного фосфорилирования» в митохондриях - процесса, активность которого неизбежно сопровождается генерацией АФК [4]. Такие функции сперматозоидов, как созревание, капацитация, гиперактивация, акросомная реакция и слияние с яйцеклеткой осуществляются посредством поддержания физиологических уровней АФК [5], в то время как избыток АФК весьма вреден для функциональности сперматозоидов и может привести к мужскому бесплодию [6]. Репродуктивное «качество» ооцитов коррелирует с уровнями 8-гидрокси-2'-дезоксигуанозина (8-OHdG) - биомаркера окислительного стресса, указывающего на степень повреждения ДНК [7]. Избыток АФК в ооцитах приводит к нарушениям цитоскелета, функционирования микротрубочек, что приводит к формированию гаметоцитов с недостаточным или избыточным количеством хромосом, повреждениям хромосом и др. [4]. Далее, последовательно рассмотрены нутриентные компоненты препаратов «Прегнотон», «Сперотон» и «Синергин».
Аргинин
Аминокислота аргинин играет важную роль в поддержке репродуктивного здоровья. Результаты экспериментальных и клинических исследований аргинина указывают на практическую пользу от использования аргинина в профилактике и терапии гипертонии, нутрициальной поддержки беременности (в частности, для улучшения фетоплацентарного кровотока и лечения задержки внутриутробного развития), противоинфекционного иммунитета, лечении бесплодия. Дотации аргинина также участвуют в поддержке соматического здоровья, способствуя профилактике ожирения, диабета, нарушений функции печени и почек.
Метаанализ плацебо-контролируемых испытаний по использованию аргинина при гипертонических расстройствах у беременных женщин включил 5 исследований. Установлено, что прием аргинина снижает повышенное диастолическое АД, в среднем, на -3,07 мм рт. ст. (р=0,004), удлиняет вынашивание, в среднем, на +8,4 сут (р=0,002) [8] (рис. 1, 2).
Рис. 1. Метаанализ эффектов аргинина на диастолическое АД у беременных. Размеры маркеров указывают относительный вес каждого исследования
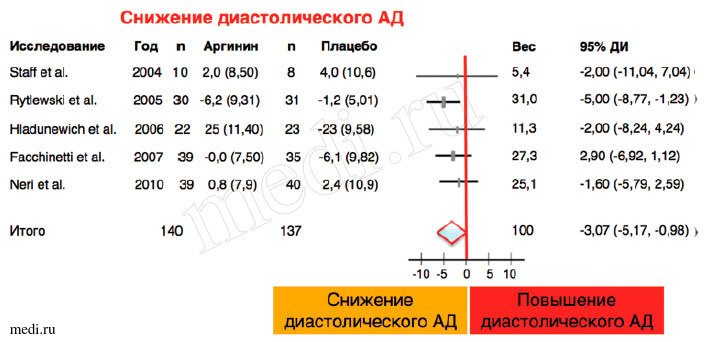
Рис. 2. Метаанализ эффектов аргинина на продолжительность беременности (в нед)
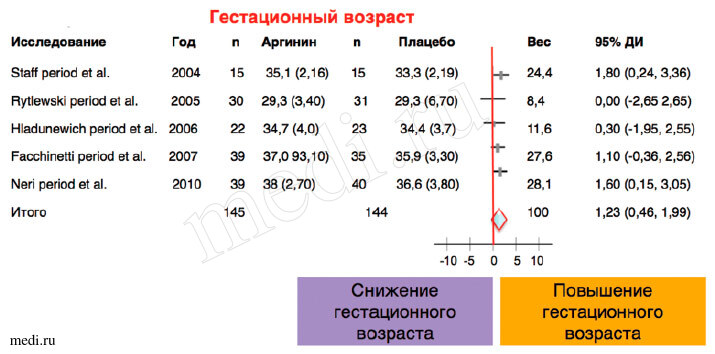
Долговременный (5-7 мес) прием аргинина представляется перспективным для нутрициальной поддержки беременных с высоким риском осложнений. Например, в группе 17 женщин с «двусторонней насечкой» и высокой сопротивляемостью маточной артерии, у 3 в анамнезе отмечена преэклампсия, у 2 - рождение мертвого плода, у 5 - необъяснимые привычные выкидыши, у 2 - изолированные спонтанные аборты, хотя ни у одной пациентки не была установлена тромбофилия. Прием аргинина (100 мг/кг/сут) был начат на 10-й неделе беременности и продолжался до родов. Среднее АД и индекс сопротивляемости маточной артерии достоверно снизились, все женщины родили в срок (38±1 нед) детей с нормальной массой тела (3227±371 г) и только у одной пациентки развилась умеренная форма преэклампсии. Благотворное влияние аргинина очевидно, так как в анамнезе у 9 пациенток из 17 отмечены серьезные осложнения беременности, которые, как правило, повторяются с вероятностью в 40-60% [9].
Продемонстрированные в экспериментальных и клинических исследованиях позитивные эффекты аргинина на поддержку беременности связаны не столько с ролью аргинина как «строительного материала», сколько с другими биологическими ролями этой аминокислоты (рис. 3). В организме аргинин метаболизируется в оксид азота (II), орнитин и пролин, необходимые для поддержки ряда физиологических процессов во время беременности. Оксид азота - вазодилататор и фактор ангиогенеза. Орнитин и пролин существенны для синтеза полиаминов, регулирующих экспрессию генов и синтез белка в матке и плаценте. Аргинин регулирует функцию гипофиза и увеличивает маточный кровоток. Пероральный прием аргинина ускоряет рост плода при ЗВУР [10, 11]. Поэтому, дотации аргинина будут способствовать поддержке нормального уровня артериального давления и снижать риск преэклампсии.
Рис. 3 Физиологические роли аргинина в улучшении выживания и роста плода
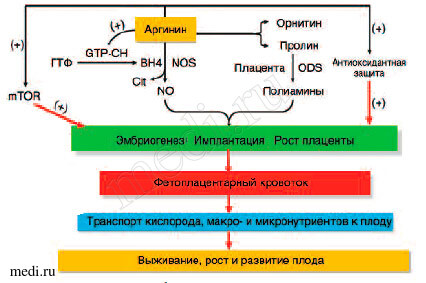
Дотации аргинина способствуют синтезу плацентарного NO и полиаминов, стимулируя маточно-плацентарный кровоток. BH4 -тетрагидробиоптерин, Cit - цитруллин, mTOR - сигнальный каскад клеточного выживания, GTP-CH - ГТФ-циклогидролаза 1, ODC -орнитиндекарбоксилаза, NO - оксид азота, NOS - синтаза окиси азота.
Аргинин используется синтетазой оксида азота для синтеза NO. Ингибирование синтетазы оксида азота нарушает оплодотворение яйцеклетки [12].
Стандартизированный экстракт Vitex Agnus-castus
Экстракты Vitex Agnus-castus применяются для регуляции менструального цикла, в терапии синдрома предменструального напряжения, лечения гиперпролактинемии и бесплодия. Стандартизированный экстракт витекса входит в состав препарата Прегнотон. Компоненты экстрактов витекса характеризуются противовоспалительным, антипролиферативным, антиоксидантным, противомикробным (в частности противогрибковым), вазопротекторным и обезболивающим действием. Для поддержки беременности наиболее актуальны эстрогенмодулируюшие и антигиперпролактиновые свойства экстрактов витекса.
Вещества в составе экстрактов Vitex Agnus-castus включают: (1) полифенолы, флавоноиды, O-дифенолы и антоцианы, (2) фитостероиды (ß-розастерол, ß-ситостерол, ß-даукостерол [15], в том числе такие экдистероиды как витикостерон E), (3) иридоидные гликозиды (например, аукубин и агнозид), (4) дитерпеноиды и лигнаны. Согласно анализу фармакологических свойств отдельных компонентов «нелетучей» и «летучей» фракций экстрактов Vitex Agnus-castus [16], эти вещества характеризуются, в первую очередь, противовоспалительным, антипролиферативным, антиоксидантным, противомикробным (в частности, противогрибковым), кардио- и вазопротекторным действием (рис. 4).
Рис. 4. Наиболее частые фармакологические свойства веществ, обнаруженных в составе экстрактов Vitex Agnus-castus.
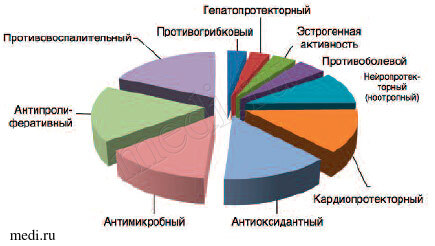
Экстракты Vitex Agnus-castus и других представителей Vitex характеризуются выраженной эстрогенмодулирующей активностью. Это обусловлено как вхождением в состав экстрактов фитоэстрогенов витикостерона, ß-розатерола, ß-ситостерола, ß-даукостерола, так и эстрогеноподобными эффектами флавонов апигенина, витексина, кемпферола и др. Эстрогенное действие экстракта Vitex Agnus-castus осуществляется посредством взаимодействий с рецепторами эстрогенов (ERa, ERb). Воздействие экстрактов витекса на эстрогеновую активность (в частности, повышение уровней рецепторов эстрогена и прогестерона) позволяет использовать эти растительные экстракты при дисбалансе эстроген-прогестерон [17].
Антигиперпролактиновый эффект экстрактов витекса связан, в частности, с торможением избыточного высвобождения пролактина вследствие блокировки дофаминовых рецепторов 2-го типа в клетках гипофиза [18]. Эти эффекты стимулируются компонентами флавоновой фракции экстракта: флавоновая фракция показала более высокую степень обезболивания и более выраженное снижение уровня пролактина. Дальнейшее разделение (фракционирование) экстрактов показало, что флавоноид кастицин сам по себе может снижать аномальные высокие уровни пролактина сыворотки (на 50%, р<0,01) [19].
Фолиевая кислота (витамин В9)
Фолиевая кислота - один из самых изученных микронутриентов, имеющий прямое отношение к профилактике врожденных пороков развития. Витамин В9 необходим для предотвращения анемии у беременных и дефектов развития плода, в том числе развития дефектов нервной трубки (ДНТ) через свое влияние на рост и дифференциацию клеток. Влияя на метилирование ДНК, фолиевая кислота играет важное значение в процессах деления клеток, что особенно важно для тканей, клетки которых активно делятся и дифференцируются (кровь, эпителий). Так как адекватная обеспеченность фолиевой кислотой и фолатами обеспечивают физиологическое деление и нормальный рост клеток, их уровень в организме должен быть оптимальным. При недостатке фолатов замедляется рост клеток, возникает фолиеводефицитная анемия и замедляется заживление ран.
Роль препаратов фолиевой кислоты в снижении риска ДНТ (дефекты нервной трубки плода) была многократно доказана в многочисленных клинических исследованиях [20]. У беременных дефицит фолиевой кислоты и фолатов увеличивает риск невынашивания, частичной или полной отслойки плаценты, спонтанного аборта [21]. В последующем у детей, матери которых испытывали дефицит фолатов во время беременности, повышается риск задержки умственного развития. Изучение 324 случаев детей с дефектами конечностей и 4982 здоровых младенцев показало, что низкое диетарное потребление фолиевой кислоты соответствовало 4-кратному увеличению риска дефектов (ОШ 3,9, 95% ДИ 1,08-13,78). Прием фолиевой кислоты предупреждает синдром Дауна и врожденные пороки сердца [22].
В настоящее время пересматривается та догматичная точка зрения, что фолиевая кислота важна только для профилактики пороков развития и должна назначаться только женщинам при подготовке к беременности. Как у женщин, так и мужчин, препараты фолиевой кислоты способствуют преодолению гипергомоцистеинемии. Гипергомоцистеинемия является одним из наиболее важных факторов сердечно-сосудистого риска и эректильной дисфункции
[23]. Как известно, основным физиологическим эффектом Т-варианта полиморфизма MTHFR 677C>T является снижение уровней эндогенных фолатов и повышения уровней гомоцистеина. В исследовании 342 человек, генотип 677TT соответствовал 3-кратному повышению риска эректильной дисфункции [24].
Ассоциированная с низкими уровнями фолатов гипергомоцистеинемия может являться одним из основных факторов, вызывающих у пациентов резистентность к ингибиторам фосфодиэстеразы-5 (ФДЭ-5), используемым в терапии эректильной дисфункции. В эксперименте прием фолиевой кислоты улучшал эректильную функцию и снижал интракавернозный окислительный стресс на фоне снижения общего гомоцистеина плазмы [25]. Прием витамина B6 (600 мг/сут) и фолиевой кислоты (15 мг/сут) в течение 6 нед показал улучшение баллов по шкале МИЭФ у 89% пациентов [26].
Витамин В6 (пиридоксин)
Витамин В6 входит в препарат «Прегнотон». Пиридоксин участвует в процессах трансаминирования, дезаминирования и декарбоксилирования аминокислот; превращения триптофана, серосодержащих аминокислот. Пиридоксин улучшает использование организмом ненасыщенных жирных кислот, благотворно влияет на функции нервной системы, печени, кроветворение. Эти эффекты важны для лечения женщин, страдающих предменструальным синдромом, особенно с выраженными нарушениями психоэмоциональной сферы [27].
Дефицит пиридоксина сопряжен с повышенной частотой судорог, парестезий, с тревожным состоянием психики, рвотой, кариесом зубов (категория доказательности «А») [28]. Метаанализ 5 исследований, включивший более 1600 женщин, показал, что регулярное употребление витамина В6 уменьшает риск рассасывания эмали зубов у беременных и риск низкой массы тела плода при рождении [29]. Вхождение в беременность на фоне недостаточности пиридоксина способствует развитию дефектов нервной трубки плода и может способствовать развитию гестозов [30]. Изучение 324 случаев детей с дефектами конечностей и 4982 здоровых младенцев показало, что самое низкое диетарное потребление витамина B6 соответствовало 4-кратному увеличению риска дефектов конечностей (ОШ 3,9, 95% ДИ 1,08-13,78) [31].
Витамин В2
Витамин В2 (рибофлавин) является исходной молекулой для биосинтеза флавиновых кофакторов энергетического метаболизма всех клеток, в том числе ооцитов. Флавинаденин динуклеотид (ФАД) и флавин мононуклеотид (ФМН) имеют принципиальное значение для энергетического метаболизма и фертильности ооцитов. В частности, кофакторы ФАД, ФМН и синтезируемого из витамина РР никотинамид динуклеотида (НАД) необходимы для поддержания оптимальных уровней восстановленного глутатиона в ооците. Снижение антиоксидантного потенциала вследствие дефицита этих витаминов нарушает раннее развитие эмбриона [32].
Карнитин
L-карнитин стимулирует энергетический метаболизм за счет участия в биосинтезе кофермента А (КоА). Фармакологически L-карнитин оказывает анаболическое, антигипоксическое действие, т.к. КоА необходим для ß-окисления, катаболизма аминокислот и работы цикла трикарбоновых кислот. Антиапоптотическое действие L-карнитина важно для повышения выживаемости и фертильности сперматозоидов.
Витамин С (аскорбиновая кислота) и рутин
Обеспеченность аскорбиновой кислотой является важным фактором в поддержании гормонального баланса. Витамин С также участвует в образовании кортикостероидов, обмене тирозина, биотрансформациях фолатов. При недостаточности аскорбиновой кислоты снижается иммунитет, увеличивается риск развития простудных заболеваний. Аскорбиновая кислота является антиоксидантом. Совместно с биофлавоноидом рутином аскорбиновая кислота принимает участие в образовании мукополисахаридов соединительной ткани (гиалуроновая и хондроитинсерная кислоты); синтезе коллагена, который «скрепляет» клетки сосудов, костной ткани, способствует репарации кожи, способствует укреплению стенки вен [34].
Важно подчеркнуть, что витамин С является синергистом фолатов и обеспечивает превращение фолиевой кислоты в ее активную форму - тетрагидрофолиевую кислоту. Исследование более 5000 беременных показало, что низкое диетарное потребление витамина С ассоциировано с тяжелыми формами гестозов и эклампсии [35]. Частота пороков развития плода у беременных с сахарным диабетом заметно сокращается при использовании витаминов Е и С [36]. По данным мексиканского исследования, ежедневный прием по крайней мере 100 мг аскорбиновой кислоты способствует уменьшению инфекций мочевыделительной системы и улучшает общее соматическое здоровье [37].
У женщин прием аскорбиновой кислоты во время подготовки к ЭКО или при наличии нарушений лютеальной фазы менструального цикла, способствует увеличению частоты наступления беременности [38].
У мужчин пероральный прием аскорбиновой кислоты улучшает качество сперматозоидов [39] и повышает выживаемость сперматозоидов при замораживании [40], что также важно для успешного проведения ЭКО.
Витамин Е (токоферол)
Витамин Е - жирорастворимый антиоксидант, предотвращающий повреждение гаметоцитов при окислительном стрессе или избыточном воспалении. Также витамин Е способствует сохранению в организме витамина С. В доказательной медицине витамин Е используется в лечении дисменореи (категория доказательности «А») и угрожающего аборта. Витамин Е снижает риск дефектов нервной трубки, индуцированных вальпроевой кислотой [41].
Гиповитаминоз Е проявляется медленно нарастающей общей слабостью, мышечными болями. При тяжелой физической нагрузке и при регулярных занятиях спортом потребность в витамине Е повышается. Поэтому в комплексах «Сперотон» содержится 30 мг витамина Е, а в комплексах «Прегнотон» и «Синергин» - по 15 мг.
Антиоксидантная терапия с витамином Е способствует компенсации возрастной эректильной дисфункции: в эксперименте витамин Е (α-токоферол) увеличивает продукцию оксида азота в кавернозных телах [46]. Витамин Е также компенсирует связанное с возрастом снижение уровней секреции оксида азота и активности фермента супероксиддисмутазы [47]. Пероральный прием витамина Е повышает подвижность сперматозоидов, улучшает оплодотворение и частоту наступления беременности в паре [48].
Йод
Йод принципиально необходим для биосинтеза гормонов тироидной железы. Как известно, дефицит йода во время ранней беременности приводит к тяжелым аномалиям развития плода и, впоследствии, к зобу и йодному кретинизму. Дефицит йода в преконцепции приводит не только к снижению активности щитовидной железы, но и к формированию кист в яичниках, медленному фолликулогенезу, гипотрофии желтого тела, утолщению теки кавернозных фолликулов и снижению фертильности ооцитов, в среднем на 20% [49].
Цинк
Цинк - эссенциальный микронутриент, необходимый для активации процессов экспрессии генов, поэтому недостаток цинка приводит к нарушениям процессов роста клеток и гормонального баланса и женщин, и мужчин. Дефицит цинка следует устранять до наступления беременности, так как дефицит цинка во время беременности повышает риск пороков развития плода (сращение 5 и 4-го пальцев, тремы, аномалии прорезывания зубов и др.) [50]. В эксперименте цинк противодействовал тератогенному воздействию дефицита фолатов и повышенного уровня гомоцистеина [51]. Исследование случай-контроль, включившее 116 матерей, родивших детей с изолированной расщелиной губы и 64 матерей, родивших детей без дефектов (контрольная группа) показало, что концентрация цинка плазмы крови менее 47,1 мкмоль/л приводила к 2,5-кратному повышению риска рождения ребенка с небной расщелиной (95% ДИ 1,03-6,23, р<0,05) [52]. Кохрейновский метаанализ 20 рандомизированных контролируемых испытаний включил более 15000 женщин и их детей. Прием препаратов цинка во время беременности приводил к достоверному уменьшению риска преждевременных родов на 14% (отношение шансов 0,86, 95% ДИ 0,76-0,97, 16 испытаний, 7637 женщин) [53].
Более высокая потребность в цинке у мужчин обусловлена как большей пропорцией мышечной ткани, так и специфическим накоплением цинка в простате. Простата - один из немногих органов с самым высоким уровнем цинка - содержит цинк в количестве более 10 мкмоль/г сухой массы. В простате цинк необходим для поддержания баланса гормональной регуляции. Пониженные уровни цитрата и цинка в секрете простаты соответствуют повышенному риску простатита [54], который, как известно, снижает фертильность. Обеспеченность организма мужчины цинком необходима для защиты от аденомы простаты [55]. И у женщин, и у мужчин, дотации цинка улучшают антиоксидантную защиту, повышая уровни антиоксиданта глутатиона и защищая гаметы от АФК [56].
Селен
Вследствие участия в активном центре глутатионпероксидазы (фермента биосинтеза основного эндогенного антиоксиданта - глутатиона) селен имеет отчетливый антиоксидантный эффект, защищая женские и мужские гаметоциты от повреждения и способствуя их созреванию [57]. Дефицит селена усугубляется к 3-му триместру беременности. Наиболее глубокий дефицит отмечается у женщин, вошедших в период беременности с изначально низкой обеспеченостью селеном.
У мужчин уровни селена, глутатиона и глутатионпероксидазы значительно ниже в эритроцитах и ткани простаты у пациентов с гиперплазией простаты [58]. В эксперименте дефицит активности селенобелков способствовал повышению риска злокачественных новообразований простаты [59]. И наоборот, селен тормозил развитие процессов воспаления в простате и останавливал пролиферативные процессы в клетках, ведущие к развитию рака [60].
Селен действует в синергизме с витамином Е, осуществляя защиту сперматозоидов от АФК, повышая подвижность и фертильность сперматозоидов. Высокие концентрации селена найдены в ткани яичка, где селен необходим для синтеза тестостерона и сперматогенеза [61]. Терапия 690 бесплодных мужчин с астенотератозооспермией, проводимая с применением селена в течение 14 недель, способствовала улучшению подвижности и морфологии сперматозоидов [62].
Ликопин и ß-каротин
Ликопин - каротиноидный пигмент, определяющий окраску плодов некоторых растений (например, томатов, гуавы, арбуза). Как микронутриент, ликопин является антиоксидантом и проявляет другие положительные эффекты за счет модуляции экспрессии генов, регуляции клеточного цикла и иммуномодуляции [63, 64]. Ликопин проявляет гипохолестеренемические свойства, т.к. ингибирует фермент гидроксиметилглутарил-кофермент А-редуктазу - важный фермент биосинтеза холестерина [65]. При пероральном приеме ликопин способствует уменьшению перекисного окисления липидов и окислительного стресса, являясь ярко выраженным синергистом селена.
Механизмы положительного воздействия ликопина на поддержание репродуктивного здоровья мужчины и функцию простаты включают ингибирование сигналов инсулиноподобного фактора роста, снижение экспрессии провоспалительного интерлейкина-6 и снижение передачи андрогеновых сигналов внутри клетки [66]. Кроме того, ликопин стимулирует ферменты 2-й фазы детоксикации и гены антиоксидантной защиты, ингибирует рост клеток эпителия простаты [67].
Ликопин препятствует эректильной дисфункции при диабете. В эксперименте, ликопин (10, 30, 60 мг/кг/сут) вводился посредством зондирования в течение 8 нед. Результаты показали, что прием ликопина значительно и дозозависимо восстанавливал эректильную функцию, способствовал снижению глюкозы в крови, снижению окислительного стресса и увеличивал уровни экспрессии эндотелиальной синтетазы окиси азота (eNOS) [68]. Ликопин оказывает положительное влияние на подвижность сперматозоидов у пациентов, принимавших 4 мг/сут ликопина в течение 3 мес [69].
ß-Каротин является одним из витамеров витамина А и необходим для процессов клеточного роста. Более высокие уровни ß-каротина в фолликулярной жидкости соответствуют повышению антиоксидантного потенциала и качества ооцита. В эксперименте повышение содержания ß-каротина в пище приводит к улучшению функционирования яичников, размеров желтого тела и синтезу прогестерона даже при приеме в течение нескольких недель [70].
Убихинон (Коэнзим Q10) является неотъемлемым компонентом митохондриальной дыхательной цепи. Хорошо известно, что гаметоциты - одни из самых насыщенных митохондриями типов клеток. У женщин более высокие уровни кофермента Q10 в фолликулярной жидкости будут способствовать созреванию ооцита [71]. У мужчин пероральный прием кофермента Q10 увеливает концентрацию и подвижность сперматозоидов [72]. Прием кофермента Q10 при идиопатическом мужском бесплодии был ассоциирован с более низкими уровнями перекисного окисления липидов и окислительного стресса в семенной плазме, повышением ферментативной антиоксидантной активности [73], улучшением акросомной реакции и повышением частоты наступления беременности [74].
Например, в исследовании [75] 212 бесплодных мужчин с идиопатической олигоастенотератоспермией были рандомизированы для получения 300 мг коэнзима Q10 ежедневно (n=106) или плацебо (n=106) в течение 26-недельного периода. Отмечено значительное улучшение плотности и подвижности сперматозоидов на фоне приема коэнзима Q10 (р=0,01). Установлена положительная корреляция между продолжительностью лечения коэнзимом Q10 и количеством сперматозоидов (r=0,46, р=0,03), подвижностью сперматозоидов (r=0,45, р=0,04) и их морфологией (r=0,34, р=0,04). К концу лечения в группе принимавших коэнзим Q10 акросомная реакция увеличилась от 14±8% до 31±11% (р=0,01 при сравнении с плацебо).
Заключение
Адекватная поддержка организма эссенциальными микронутриентами есть необходимое условие для формирования, созревания и защиты жизнеспособности гамет. Преконцептуальная подготовка пары к успешному зачатию включает обязательную коррекцию повсеместно распространенных микронутриентных дефицитов (рис. 5).
Рис. 5. Принципы синергизма при подготовке пары к зачатию и рождению ребенка при комбинировании комплексов «Прегнотон»+«Синергин» у женщин и «Сперотон»+«Синергин» у мужчин
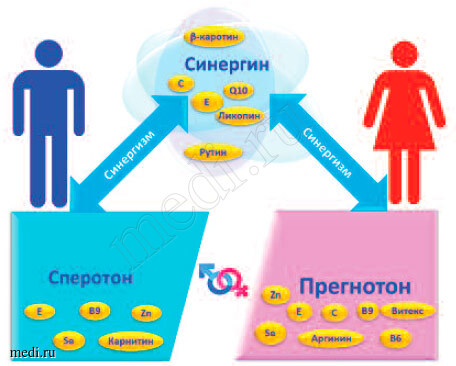
Наличие синергизма между принципиально важными для поддержки фертильности микронутриентами привело к созданию линии специализированных препаратов «Прегнотон», «Сперотон» и «Синергин», способствующих нормализации гормонального баланса и снижения риска формирования пороков развития плода.
ЛИТЕРАТУРА
- Громова О.А., Торшин И.Ю. Витамины и микронутриенты: между Сциллой и Харибдой. МЦНМО, 2013; 869. / Gromova O.A., Torshin I.Ju. Vitaminy i mikronutrienty: mezhdu Scilloj i Haribdoj. MCNMO, 2013; 869. [in Russian]
- Справочник лекарственных средств «Видаль», М.: 2015.
- Agarwal A., Durairajanayagam D., du Plessis S.S. Utility of antioxidants during assisted reproductive techniques: an evidence based review. Reprod Biol Endocrinol. 2014 Nov 24; 12: 112.
- du Plessis S.S., Makker K., Desai N.R., Agarwal A. Impact of oxidative stress on IVF. Expet Rev Obstet Gynecol. 2008; 3: 539-554.
- de Lamirande E, Gagnon C: A positive role for the superoxide anion in triggering hyperactivation and capacitation of human spermatozoa. Int J Androl. 1993; 16:21-25.
- Agarwal A, Virk G, Ong C, du Plessis S.S.: Effect of oxidative stress on male reproduction. World J Men's Health. 2014; 32: 1-17.
- Seino T., Saito H., Kaneko T., Takahashi T., Kawachiya S., Kurachi H. Eight-hydroxy-2'-deoxyguanosine in granulosa cells is correlated with the quality of oocytes and embryos in an in vitro fertilization-embryo transfer program. Fertil Steril. 2002; 77: 1184-1190.
- Zhu Q., Yue X., Tian Q.Y, Saren G., Wu M.H., Zhang Y, Liu T.T. Effect of L-arginine supplementation on blood pressure in pregnant women: a meta-analysis of placebo-controlled trials. Hypertens Pregnancy. 2013; 32 (1): 32-41 doi.
- Germain A.M., Valdes G., Romanik M.C., Reyes M.S.. Evidence Supporting a Beneficial Role for Long-Term L-Arginine Supplementation in High-Risk Pregnancies. Hypertension. 2004; 44 (1): e1.
- Wu G., Bazer F.W., Satterfield M.C., Li X., Wang X., Johnson G.A., Burghardt R.C., Dai Z., Wang J., Wu Z. Impacts of arginine nutrition on embryonic and fetal development in mammals. Amino Acids. 2013; 45 (2): 241-56 doi.
- Zeng X., Mao X., Huang Z., Wang F., Wu G., Qiao S. Arginine enhances embryo implantation in rats through PI3K/PKB/mTOR/NO signaling pathway during early pregnancy. Reproduction. 2013; 145 (1): 1-7 doi.
- Romero-Aguirregomezcorta J, Santa AP, Garcia-Vazquez FA, Coy P, Matas C. Nitric Oxide Synthase (NOS) Inhibition during Porcine In Vitro Maturation Modifies Oocyte Protein S-Nitrosylation and In Vitro Fertilization. PLoS One. 2014; 9 (12): e115044.
- Arcaniolo D., Favilla V., Tiscione D., Pisano F., Bozzini G., Creta M., Gentile G., Menchini Fabris F., Pavan N., Veneziano I.A., Cai T. Is there a place for nutritional supplements in the treatment of idiopathic male infertility? Arch Ital Urol Androl. 2014; 86 (3): 164-70 doi.
- Srivastava S., Agarwal A. Effect of anion channel blockers on L-arginine action in spermatozoa from asthenospermic men. Andrologia. 2010; 42 (2): 76-82 doi.
- Liu Q.Y, Chen YS., Wang F., Chen S.W., Zhang YH. Chemical of Vitex trifolia. Zhongguo Zhong Yao Za Zhi. 2014 Jun; 39(11):2024-8. PMID: 25272835
- Торшин И.Ю., Громова О.А., Лиманова О.А.. Систематический анализ состава и механизмов молекулярного воздействия стандартизированных экстрактов Vitex Agnus-castus. Трудный пациент. 2015; 1-2:13: 19-28. /Torshin I.Ju., Gromova O.A., Limanova O.A.. Sistematicheskij analiz sostava i mehanizmov molekuljarnogo vozdejstvija standartizirovannyh jekstraktov Vitex Agnus-castus. Trudnyj pacient. 2015; 1-2:13: 19-28. [in Russian]
- Liu J., Burdette J.E., Xu H., Gu C., van Breemen R.B., Bhat K.P., Booth N., Constantinou A.I., Pezzuto J.M., Fong H.H., Farnsworth N.R., Bolton J.L. Evaluation of estrogenic activity of plant extracts for the potential treatment of menopausal symptoms. J Agric Food Chem. 2001 May; 49 (5): 2472-9. PMID: 11368622
- Carmichael A.R.. Can Vitex Agnus Castus be Used for the Treatment of Mastalgia? What is the Current Evidence? Evid Based Complement Alternat Med. 2008 Sep; 5(3): 247-50. PMID: 18830450
- Hu Y,Xin H.L.,Zhang Q.Y, Zheng H.C., Rahman K., Qin L.P. Antinociceptive and anti-hyperprolactinemia activities of Fructus Viticis and its effective fractions and chemical constituents. Phytomedicine. 2007 Oct; 14 (10): 668-74. PMID: 17350238
- Smith A.D., Kim YI., Refsum H. Is folic acid good for everyone? Am J Clin Nutr. 2008; 87 (3): 517-533.
- Christian P., West K.P., Khatry S.K. Effects of maternal micronutrient supplementation on fetal loss and infant mortality: a cluster-randomized trial in Nepal.Am J Clin Nutr. 2003 Dec; 78 (6): 1194-202.
- Bailey LB, Berry RJ.Folic acid supplementation and the occurrence of congenital heart defects, orofacial clefts, multiple births, and miscarriage.Am J Clin Nutr. 2005 May; 81 (5): 1213S-1217S.
- Wang C.H., Huang YF. Hyperhomocysteinemia and erectile dysfunction: an update. Zhonghua Nan Ke Xue. 2011;17 (11):1019-1022.
- Safarinejad M.R., Safarinejad S., Shafiei N. Role of methylenete-trahydrofolate reductase gene polymorphisms (C677T, A1298C, and G1793A) in the development of early onset vasculogenic erectile dysfunction. Arch Med Res. 2010; 41 (6): 410-422.
- Shukla N., Hotston M., Persad R., Angelini G.D., Jeremy J.Y The administration of folic acid improves erectile function and reduces intracavernosal oxidative stress in the diabetic rabbit. BJU Int. 2009; 103 (1): 98-103.
- Lombardo F., Tsamatropoulos P., Piroli E., Culasso F., Jannini E.A., Dondero F., Lenzi A., Gandini L. Treatment of erectile dysfunction due to C677T mutation of the MTHFR gene with vitamin B6 and folic acid in patients non responders to PDE5i. J Sex Med. 2010; 7 (1 Pt 1): 216-23 Epub 2009 Au.
- Громова О.А., Лиманова О.А., Торшин И.Ю. Систематический анализ фундаментальных и клинических исследований, как обоснование необходимости совместного использования эстрогенсодержащих препаратов с препаратами магния и пиридоксина. Акушерство, гинекология и репродукция. 2013; 3: 35-50. / Gromova O.A., Limanova O.A., Torshin I.Ju. Sistematicheskij analiz fundamental'nyh i klinicheskih issledovanij, kak obosnovanie neobhodimosti sovmestnogo ispol'zovanija jestrogensoderzhashhih preparatov s preparatami magnija i piridoksina. Akusherstvo, ginekologija i reprodukcija. 2013; 3: 35-50. [in Russian]
- Формулярная система. Федеральное руководство, ГеотарМед, М.: 2010; 996.
- Thaver D., Saeed M.A., Bhutta Z.A.Pyridoxine (vitamin B6) supplementation in pregnancy.Cochrane Database Syst Rev. 2006 Apr 19; 2: CD000179.
- Ronnenberg A.G., Venners S.A., Xu X., Chen C., Wang L., Guang W., Huang A., Wang X. Preconception B-vitamin and homocysteine status, conception, and early pregnancy loss. Am J Epidemiol. 2007 Aug 1; 166 (3): 304-12.
- Robitaille J., Carmichael S.L., Shaw G.M., Olney R.S. Maternal nutrient intake and risks for transverse and longitudinal limb deficiencies: data from the National Birth Defects Prevention Study, 19972003. Birth Defects Res A Clin Mol Teratol. 2009; 85 (9): 773-779.
- Dumollard R., Ward Z., Carroll J., Duchen M.R. Regulation of redox metabolism in the mouse oocyte and embryo. Development. 2007 Feb; 134 (3): 455-65.
- Zare Z., Masteri Farahani R., Salehi M., Piryaei A., Ghaffari Novin M., Fadaei Fathabadi F., Mohammadi M., Dehghani-Mohammadabadi M. Effect of L-carnitine supplementation on maturation and early embryo development of immature mouse oocytes selected by brilliant cresyle blue staining. J Assist Reprod Genet. 2015; 32 (4): 635-643.
- Hara K., Akiyama Y Collagen-related abnormalities, reduction in bone quality, and effects of menatetrenone in rats with a congenital ascorbic acid deficiency. J Bone Miner Metab. 2009; 27 (3): 324-32.
- Dheen S.T, Tay S.S. Recent studies on neural tube defects in embryos of diabetic pregnancy: an overview. Curr Med Chem. 2009; 16 (18): 2345-2354.
- Klemmensen A., Tabor A., Osterdal M.L. Intake of vitamin C and E in pregnancy and risk of preeclampsia: prospective study among 57346 women. BJOG. 2009 Jun; 116 (7): 964-74.
- Ochoa-Brust G.J., Fernandez A.R., Villanueva-Ruiz G.J. Daily intake of 100 mg ascorbic acid as urinary tract infection prophylactic agent during pregnancy.Acta Obstet Gynecol Scand. 2007; 86 (7): 783-7.
- Jenkins T.G., Aston K.I., Carrell D.T. Supplementation of cryomedium with ascorbic acid-2-glucoside (AA2G) improves human sperm post-thaw motility. Fertil Steril. 2011; 95: 2001-2004.
- Dawson E.B., Harris W.A., Teter M.C., Powell L.C. Effect of ascorbic acid supplementation on the sperm quality of smokers. Fertil Steril. 1992; 58: 1034-1039.
- Henmi H., Endo T., Kitajima Y., Manase K., Hata H., Kudo R. Effects of ascorbic acid supplementation on serum progesterone levels in patients with a luteal phase defect. Fertil Steril. 2003; 80: 459-461.
- Al Deeb S., Al Moutaery K., Arshaduddin M., Tariq M. Vitamin E decreases valproic acid induced neural tube defects in mice. Neurosci Lett. 2000; 292 (3): 179-182.
- Viana M., Castro M., Barbas C., Herrera E., Bonet B. Effect of different doses of vitamin E on the incidence of malformations in pregnant diabetic rats. Ann Nutr Metab. 2003; 47 (1): 6-10.
- Siman C.M. Malformations in offspring of diabetic rats: morphometric analysis of neural crest-derived organs and effects of maternal vitamin E treatment. Teratology. 2000; 61 (5): 355.
- Torfs C.P., Lam P.K., Schaffer D.M., Brand R.J. Association between mothers' nutrient intake and their offspring's risk of gastroschisis.Teratology. 1998 Dec; 58 (6): 241-50.
- Chen K., Zhang X., Wei X.P. Antioxidant vitamin status during pregnancy in relation to cognitive development in the first two years of life. Early Hum Dev. 2009 Jul; 85 (7): 421-7.
- Tronchini E.A., de Miranda Neto M.H., Zanoni J.N. Vitamin E (alpha-tocopherol) supplementation enhances nitric oxide production in penile tissue of diabetic rats. BJU Int. 2010; 106 (11): 1788-93.
- Helmy M.M., Senbel A.M. Evaluation of vitamin E in the treatment of erectile dysfunction in aged rats. Life Sci. 2012; 90 (13-14): 489—94.
- Geva E., Bartoov B., Zabludovsky N., Lessing J.B., Lerner-Geva L., Amit A. The effect of antioxidant treatment on human spermatozoa and fertilization rate in an in vitro fertilization program. Fertil Steril. 1996; 66: 430-434.
- Rodzaevskaia E.B. Morphological impairment of oogenesis in experimental iodinedependent thyroid transformation. Arkh Patol. 2002 Mar-Apr; 64 (2): 10-3.
- Donangelo C.M., King J.C. Maternal zinc intakes and homeostatic adjustments during pregnancy and lactation.Nutrients. 2012 Jul;4(7):782-98. doi: 10.3390/nu4070782. Epub 2012 Jul 24.
- He X., Hong X., Zeng F., Kang F., Li L., Sun Q. Zinc antagonizes homocysteine-induced fetal heart defects in rats.Cardiovasc Toxicol. 2009 Sep; 9 (3): 151-9.
- Hozyasz K.K., Kaczmarczyk M., Dudzik J., Bulska E., Dudkiewicz Z., Szymanski M. Relation between the concentration of zinc in maternal whole blood and the risk of an infant being born with an orofacial cleft.Br J Oral Maxillofac Surg. 2009 Sep; 47 (6): 466-9.
- Mori R., Ota E., Middleton P., Tobe-Gai R., Mahomed K., Bhutta Z.A. Zinc supplementation for improving pregnancy and infant o come.Cochrane Database Syst Rev. 2012 Jul 11; 7: CD000230.
- Gomez Y, Arocha F., Espinoza F., Fernandez D., Vasquez A., Granadillo V. Zinc levels in prostatic fluid of patients with prostate pathologies. Invest Clin. 2007; 48 (3): 287-294.
- Christudoss P., Selvakumar R., Fleming J.J., Gopalakrishnan G. Zinc status of patients with benign prostatic hyperplasia and prostate carcinoma. Indian J Urol. 2011; 27 (1): 14-18.
- Banudevi S., Elumalai P., Arunkumar R., Senthilkumar K., Gunadharini D.N., Sharmila G., Arunakaran J. Chemopreventive effects of zinc on prostate carcinogenesis induced by N-methyl-N-nitrosourea and testosterone in adult male Sprague-Dawley rats. J Cancer Res Clin Oncol. 2011; 137 (4): 677-86 Epub 2010 Ju.
- Mirone M., Giannetta E., Isidori A.M. Selenium and reproductive function. A systematic review. J Endocrinol Invest. 2013 Nov; 36 (10): Suppl: 28-36.
- Zachara B.A., Szewczyk-Golec K., Tyloch J., Wolski Z., Szylberg T., Stepien S., Kwiatkowski S., Bloch-Boguslawska E., Wasowicz W. Blood and tissue selenium concentrations and glutathione peroxidase activities in patients with prostate cancer and benign prostate hyperplasia. Neoplasma. 2005; 52 (3): 248-254.
- Muecke R., Klotz T., Giedl J., Buentzel J., Kundt G., Kisters K., Prott F.J., Micke O. Whole blood selenium levels (WBSL) in patients with prostate cancer (PC), benign prostatic hyperplasia (BPH) and healthy male inhabitants (HMI) and prostatic tissue selenium levels (PTSL) in patients with PC and BPH. Acta Oncol. 2009; 48 (3): 452-456.
- Kandas N.O., Randolph C., Bosland M.C. Differential effects of selenium on benign and malignant prostate epithelial cells: stimulation of LNCaP cell growth by noncytotoxic, low selenite concentrations. Nutr Cancer. 2009; 61 (2): 251-264.
- Moslemi M.K., Tavanbakhsh S. Selenium-vitamin E supplementation in infertile men: effects on semen parameters and pregnancy rate. Int J Gen Med. 2011; 4: 99-104.
- Mistry H.D., Broughton Pipkin F., Redman C.W., Poston L. Selenium in reproductive health. Am J Obstet Gynecol. 2012; 206: 21-30.
- Chauhan K.., Sharma S., Agarwal N., Chauhan B. Lycopene of tomato fame: its role in health and disease. IJPSR. 2011; 10: 99-115.
- Palozza P., Catalano A., Simone R., Cittadini A. Lycopene as aguardian of redox signalling. Acta Biochim Pol. 2012; 59: 21-5.
- Heber D., Lu Q.Y Overview of mechanisms of action of lycopene. Exp Biol Med (Maywood). 2002; 227: 920-3.
- Durairajanayagam D., Agarwal A., Ong C., Prashast P. Lycopene and male infertility. Asian Journal of Andrology. 2014; 16: 420-425.
- Obermuller-Jevic U.C., Olano-Martin E., Corbacho A.M., Eiserich J.P., van der Vliet A., Valacchi G., Cross C.E., Packer L. Lycopene inhibits the growth of normal human prostate epithelial cells in vitro. J Nutr. 2003; 133 (11): 3356-3360.
- Gao J.X., Li Y, Zhang H.Y, He X.L., Bai A.S. Lycopene ameliorates erectile dysfunction in streptozotocin-induced diabetic rats. Pharmazie. 2012; 67 (3): 256-259.
- Hekimoglu A., Kurcer Z., Aral F., Baba F., Sahna E. et al. Lycopene, an antioxidant carotenoid, attenuates testicular injury caused by ischemia/reperfusion in rats. Tohoku J Exp Med. 2009; 218: 141-7.
- Arellano-Rodriguez G.1., Meza-Herrera C.A., Rodriguez-Martinez R., Dionisio-Tapia R., Hallford D.M., Mellado M., Gonzalez-Bulnes A. Shortterm intake of beta-carotene-supplemented diets enhances ovarian function and progesterone synthesis in goats. J Anim Physiol Anim Nutr (Berl). 2009 Dec; 93 (6): 710-5.
- Turi A.1., Giannubilo S.R., Bruge F., Principi F., Battistoni S., Santoni F., Tranquilli A.L., Littarru G., Tiano L. Coenzyme Q10 content in follicular fluid and its relationship with oocyte fertilization and embryo grading. Arch Gynecol Obstet. 2012 Apr; 285 (4): 1173-6.
- Lafuente R., Gonzalez-Comadran M., Sola I., Lopez G., Brassesco M., Carreras R., Checa M.A. Coenzyme Q10 and male infertility: a meta-analysis. J Assist Reprod Genet. 2013; 30: 1147-1156.
- Nadjarzadeh A., Shidfar F., Amirjannati N., Vafa M.R., Motevalian S.A., Gohari M.R., Nazeri Kakhki S.A., Akhondi M.M., Sadeghi M.R. Effect of Coenzyme Q10 supplementation on antioxidant enzymes activity and oxidative stress of seminal plasma: a double-blind randomised clinical trial. Andrologia. 2014; 46: 177-183.
- Safarinejad M.R. The effect of coenzyme Q10 supplementation on partner pregnancy rate in infertile men with idiopathic oligoas-thenoteratozoospermia: an open-label prospective study. Int Urol Nephrol. 2012; 44: 689-700.
- Safarinejad M.R. Efficacy of coenzyme Q10 on semen parameters, sperm function and reproductive hormones in infertile men. J Urol. 2009 Jul; 182 (1): 237-48.
Сведения об авторах:
Торшин Иван Юрьевич - к.м.н., консультант Российского центра института микроэлементов ЮНЕСКО, Москва
Громова Ольга Алексеевна - д.м.н., профессор кафедры фармакологии с клинической фармакологией, заведующая курсом клинической фармакологии ГБОУ ВПО «Ивановская государственная медицинская академия Минсоцздравразвития РФ», заместитель директора по научной работе РСЦ Института Микроэлементов ЮНЕСКО, Москва