Уважаемый посетитель!
Эта информация для специалистов здравоохранения
Нажимая «ПРОДОЛЖИТЬ», Вы подтверждаете, что им являетесь
Клиническая эффективность и антиоксидантная активность Мексидола при хронических цереброваскулярных заболеваниях
СтатьиОпубликовано в журнале:
АтмосферА. Нервные болезни, 1, 2006
И.Н. Смирнова, Т.Н. Фёдорова, М.М. Танашян, З.А. Суслина
ГУ НИИ неврологии РАМН, Москва.
Сосудистые заболевания головного мозга из-за высокой распространенности и тяжелых последствий для состояния здоровья населения остаются в настоящее время важнейшей медицинской и социальной проблемой. Предотвращение их прогрессирования и улучшение качества жизни больных является одной из ключевых задач неврологии. В связи с этим представляется важным поиск новых направлений воздействия на различные звенья патогенеза ишемических повреждений мозга, а также расширение представлений о механизмах действия уже известных лекарственных препаратов.
В ряде экспериментальных работ [1, 15, 16, 20] было показано существенное значение окислительного стресса в патогенезе ишемических нарушений мозгового кровообращения (НМК). Ишемия мозга инициирует каскад биохимических реакций, лежащих в основе тканевого повреждения. Основные механизмы нейронального повреждения включают истощение энергетических ресурсов в условиях ацидоза ткани мозга, нарушение ионного гомеостаза, избыточное накопление возбуждающих аминокислот и гиперпродукцию активных форм кислорода. Последние индуцируют развитие окислительного стресса, который характеризуется повышенным образованием свободных радикалов и снижением активности антиоксидантной системы [2, 18]. Ткань мозга особенно чувствительна к окислительному стрессу, так как чрезвычайно богата ненасыщенными липидами, входящими в состав мембранных фосфолипидов и являющимися основными субстратами свободнорадикального (перекисного) окисления.
Как показали наши данные, традиционная лекарственная терапия, направленная на улучшение кровоснабжения мозга, не всегда препятствует нарастанию окислительных повреждений в организме пациентов с сосудистыми заболеваниями головного мозга, что определило необходимость поиска препаратов, избирательно корригирующих эти процессы [12, 14]. В течение последних 15 лет в НИИ неврологии РАМН разрабатываются принципы антиоксидантной терапии у пациентов как с острыми, так и с хроническими формами сосудистой мозговой недостаточности – дисциркуляторной энцефалопатией (ДЭ) и последствиями НМК. В результате этих исследований была определена антиоксидантная активность ряда лекарственных препаратов при лечении цереброваскулярных заболеваний [6, 11–13].
Наиболее широкое применение в клинической практике нашли отечественные препараты эмоксипин и Мексидол – производные 3-оксипиридина, относящиеся к водорастворимым антиоксидантам биогенного типа и являющиеся структурными аналогами соединений группы витамина В6 [4]. Важным положительным свойством антиоксидантов этой группы является способность проникать через гематоэнцефалический барьер. Впервые клиническая эффективность и антиоксидантная активность эмоксипина при лечении больных с различными формами НМК были доказаны в 90-х годах прошлого столетия [6, 12].
Препарат Мексидол (3-окси-6метил-2-этилпиридин сукцинат) был создан на основе эмоксипина с включением в его молекулу янтарной кислоты, что обеспечило расширение терапевтических возможностей препарата. Действие Мексидола заключается в антиоксидантном и мембранопротекторном эффектах, которые обеспечиваются ингибированием свободнорадикального окисления липидов клеточных мембран и модулированием синтеза простагландинов, повышением активности антиоксидантных ферментов организма, повышением содержания полярных фракций липидов и снижением соотношения холестерин/фосфолипиды, модулированием активности ферментов и рецепторных комплексов мембран клеток мозга и крови (эритроцитов и тромбоцитов), а также активацией энергосинтезирующих функций митохондрий [3, 4].
В настоящее время накоплен достаточно большой опыт применения Мексидола в неврологической практике, однако некоторые вопросы, связанные с применением этого препарата у больных с хроническими цереброваскулярными заболеваниями, остаются недостаточно изученными. Целью нашей работы явилось проведение комплексного клинико-биохимического исследования эффективности Мексидола у больных с хроническими цереброваскулярными заболеваниями, с детальным анализом взаимосвязи между клинической эффективностью препарата и количественными характеристиками окислительного стресса. Соответственно, в задачи нашего исследования входили:
- оценка динамики основных клинических синдромов у больных с дисциркуляторной энцефалопатией и последствиями ишемических НМК на фоне лечения Мексидолом;
- оценка влияния терапии Мексидолом на состояние процессов перекисного окисления липидов (ПОЛ) и антиоксидантной защиты, характеризующих степень выраженности окислительного стресса;
- проведение сопоставления между вышеуказанными параметрами окислительного стресса и клиническими характеристиками заболевания (в том числе их динамикой) на фоне терапии Мексидолом.
Клиническая характеристика больных и методы исследования
В исследование были включены 43 пациента (19 мужчин и 24 женщин) в возрасте от 42 до 75 лет (средний возраст составил 61,2±8,8 лет), страдающих дисциркуляторной энцефалопатией I–II стадии или имеющих последствия НМК ишемического характера с легкой либо умеренно выраженной неврологической симптоматикой. Основными сосудистыми заболеваниями, обусловившими развитие неврологических расстройств у обследованных больных, были артериальная гипертония и атеросклероз (в том числе в сочетании друг с другом).
Эффективность Мексидола исследовалась открытым способом. 23 пациента получали препарат в суточной дозе 300 мг в сутки (утром по 4,0 мл 5% раствора на 250,0 мл физиологического раствора внутривенно капельно и вечером – 2,0 мл 5% раствора внутримышечно) в течение 10 дней. При необходимости больные получали базовую гипотензивную, кардиальную и антидиабетическую терапию. Группу сравнения составили 20 пациентов, сопоставимых по полу, возрасту и характеру заболевания, получавших в течение 10 дней лишь вышеуказанную базовую терапию. На протяжении всего курса лечения пациентам обеих групп не назначались вазоактивные, ноотропные, психотропные, антиагрегантные и антикоагулянтные препараты.
Для оценки эффективности терапии до начала лечения и после его окончания определяли выраженность основных субъективных проявлений заболевания (головной боли, головокружения, шума в голове, нарушений сна, утомляемости, снижения памяти и настроения, эмоциональной лабильности), а также показателей неврологического статуса (вестибуло-мозжечковых, двигательных, экстрапирамидных, чувствительных и псевдобульбарных расстройств) с помощью 5-балльной рейтинговой шкалы со стандартизированными критериями оценки выраженности каждого симптома (0 – симптом отсутствует, 1 – легкие проявления, 2 – умеренные проявления, 3 – значительные проявления, 4 – грубые проявления). Общая эффективность лечения оценивалась исследователем и пациентом по 5-ступенчатой шкале: 0 – ухудшение, 1 – без динамики, 2 – удовлетворительно (небольшое улучшение), 3 – хорошо (заметное улучшение), 4 – отлично (исчезновение симптомов).
Количественную характеристику окислительного стресса в динамике до и после курса лечения осуществляли с помощью метода железоиндуцированной хемилюминесценции суммарной фракции липопротеинов низкой и очень низкой плотности, выделенных из сыворотки крови пациентов [17]. Этот метод отличается высокой специфичностью к свободнорадикальным процессам. В работе регистрировали ряд информативных кинетических параметров: уровень первичных продуктов перекисного окисления липидов, преимущественно гидроперекисей липидов (h), устойчивость липопротеиновых структур к окислению (τ) и максимальную способность липидов к перекисному окислению (Н). Полученные результаты подвергались статистической обработке на основе пакета программ Statistica 99 (StatSoft, США).
Результаты исследования и их обсуждение
При общей оценке эффекта лечения было выявлено четкое превалирование положительных результатов при использовании Мексидола (95,7%) по сравнению с группой сравнения (65%) (табл. 1).
Таблица 1. Субъективная оценка эффективности терапии Мексидолом больными в группе Мексидола (N = 23) и в группе сравнения (N = 20)
| Эффект | Мексидол, n (%) | Группа сравнения, n (%) | |
| Положительный | 22 (95,7%)* | 13 (65%) | |
| в том числе | хороший и отличный | 12 (52,2%) | 4 (20%) |
| удовлетворительный | 10 (43,5%) | 9 (45%) | |
| Отрицательный | 1 (4,3%)* | 7 (35%) | |
| в том числе | без эффекта | 1 (4,3%) | 5 (25%) |
| ухудшение | 0 | 2 (10%) | |
* р <0,05.
Разница суммарного балла, отражающая динамику субъективных проявлений заболевания до и после лечения, в группе больных, получавших Мексидол, оказалась достоверно большей, чем в группе сравнения (5,7±2,9 и 2,9±2,1 соответственно, р = 0,0045) (рис. 1). При лечении Мексидолом достоверно чаще наблюдалось уменьшение выраженности эмоциональной лабильности, тревоги и депрессивных реакций, утомляемости, шума в голове, нарушений сна (рис. 2). Однако по отношению к таким частым при дисциркуляторной энцефалопатии симптомам, как головная боль и головокружение, улучшение при лечении Мексидолом оказалось статистически недостоверным. В трех наблюдениях на фоне лечения Мексидолом отмечалось уменьшение степени выраженности подкорковой симптоматики: у двоих больных – тремора при статическом напряжении и у одного – атетоидного гиперкинеза.
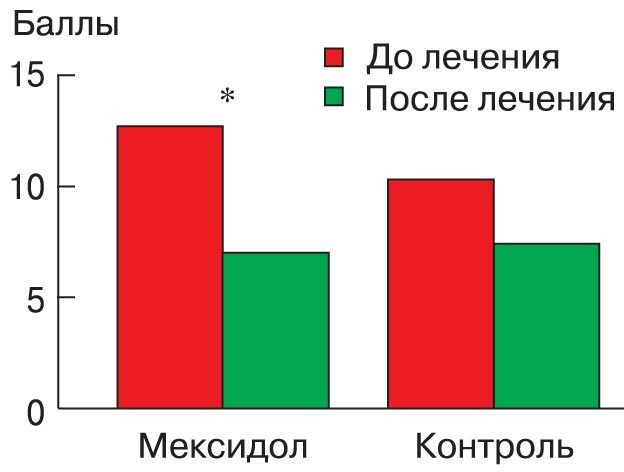
Рис. 1. Динамика выраженности основных субъективных симптомов до и после лечения в баллах. * р = 0,0045.
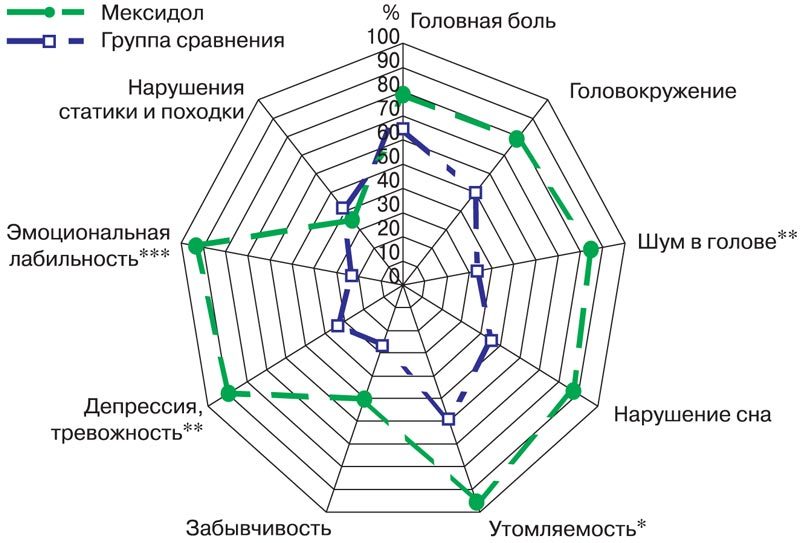
Рис. 2. Частота положительной динамики (%) со стороны отдельных симптомов заболевания на фоне лечения Мексидолом. * р <0,05, ** р <0,01, *** р <0,005.
Объяснить избирательное действие препарата на те или иные симптомы можно исходя из его фармакологических свойств. Транквилизирующее действие Мексидола связывают с взаимодействием 3-оксипиридинов с ГАМК-бензодиазепиновым хлор-ионофорным рецепторным комплексом нейрональных мембран [3, 4]; клинически этот эффект был подтвержден у больных с неврозами [8] и у пациентов с органическими эмоционально-лабильными расстройствами [10]. Описано положительное влияние Мексидола на подкорковую симптоматику у больных с хроническим нейролептическим синдромом [9], а в экспериментальных работах на животных было показано, что благодаря антиоксидантным свойствам Мексидол защищает нигростриарные дофаминергические нейроны от повреждения и гибели, в результате чего увеличивается синтез дофамина в стриатуме [5, 7].
Результаты хемилюминесцентного анализа показали, что исходно у обследованных больных наблюдалось значительное, почти в 2 раза по сравнению с контролем, снижение устойчивости липопротеиновых структур к окислению (54,6±23,1 с, норма – 93,6±18,0 с), что свидетельствует о недостаточной эффективности эндогенной антиоксидантной защиты. В то же время средние величины показателей, отражающих уровень гидроперекисей липидов и максимальную способность липопротеинов к окислению, не выходили за рамки нормальных значений. Отсутствие выраженного повышения содержания в крови перекисных продуктов, по видимому, можно объяснить тем, что в исследование были включены больные с легкой формой дисциркуляторной энцефалопатии (I–II стадии) или негрубыми остаточными явлениями НМК в поздние сроки (не менее 1 мес после перенесенного сосудистого эпизода). Это согласуется с полученными нами ранее данными о взаимосвязи между тяжестью сосудистого поражения головного мозга и степенью окислительных повреждений липопротеинов [15].
После курса лечения у больных, получавших Мексидол, произошло достоверное повышение резистентности липопротеиновых структур к перекисному окислению (до нормальных значений, или на 44% от исходного уровня), что свидетельствует о восстановлении активности эндогенной антиоксидантной системы. В группе сравнения данный показатель остался сниженным. Важным результатом нашего исследования явилось статистически значимое (на 12,7%) снижение уровня гидроперекисей липидов у пациентов, получавших лечение Мексидолом (табл. 2), в то время как в группе больных, получавших лишь базисную терапию, каких-либо изменений в параметрах перекисного окисления липидов не произошло. На основании полученных данных можно заключить, что Мексидол обладает выраженной антиоксидантной активностью, существенно увеличивает резистентность липопротеиновых структур к окислению, проявляя таким образом у больных с цереброваскулярными заболеваниями свойства мембранопротектора.
Таблица 2. Интенсивность процессов перекисного окисления липидов и их динамика под влиянием антиоксидантной терапии
| Группа лечения |
Параметры Fe2+-индуцированной хемилюминесценции | |||||
| гидроперекиси липидов, мВ |
эндогенная антиоксидантная защита, с |
окисляемость липидов, мВ |
||||
| до лечения |
после лечения |
до лечения |
после лечения |
до лечения |
после лечения |
|
| Мексидол (n = 19) |
100,4±22,4 | 87,6±19,6** | 58,4±19,7* | 103,5±40,3#*** | 1156±243 | 1141±249 |
| Группа сравнения (n = 15) |
93,6±8,4 | 93,6±8,4 | 52,9±19,7* | 52,8±20,9* | 1121±238 | 1222±205 |
| Норма (n = 11) |
92,9±10,7 | 93,6±18,0 | 1229±185 | |||
* р = 0,000 (достоверные различия с нормой).
** р <0,05.
*** p = 0,0008 (достоверные различия до и после лечения Мексидолом).
# p = 0,0002 (достоверные различия с группой сравнения).
Нам удалось установить зависимость клинической эффективности препарата от исходного состояния процессов перекисного окисления липидов при проведении корреляционного анализа. Оказалось, что у больных, получавших лечение Мексидолом, имеется статистически значимая зависимость между степенью регресса неврологических симптомов в баллах и исходным уровнем гидроперекисей липидов (r = 0,41, p = 0,019), в то время как в группе сравнения аналогичной зависимости выявлено не было (рис. 3). Отмечена также тенденция к обратной корреляции между степенью клинического улучшения в результате лечения Мексидолом и эндогенной антиоксидантной активностью (r = –0,35, p = 0,058). Другими словами, чем выше у больных была исходная активность перекисного окисления липидов, тем отчетливее было клиническое улучшение после проведенного курса лечения Мексидолом, что указывает на патогенетическую роль окислительного стресса и необходимость коррекции этих нарушений при хронических цереброваскулярных заболеваниях.
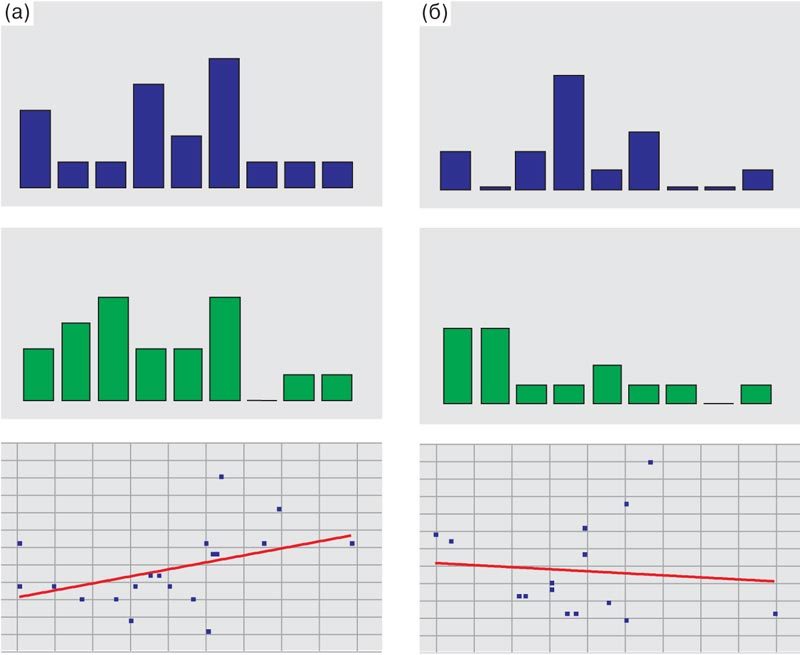
Рис. 3. Корреляция между исходным уровнем гидроперекисей липидов (синие гистограммы) и динамикой неврологических симптомов в баллах (зеленые гистограммы) под действием Мексидола. а – группа терапии Мексидолом, корреляция достоверна (r = 0,41, p = 0,02). б – контрольная группа, корреляция отсутствует (r = –0,08, p > 0,05).
На основании проведенной работы можно сделать следующие выводы.
- Применение Мексидола у больных с хроническими цереброваскулярными заболеваниями приводит к улучшению состояния пациентов и уменьшению выраженности наиболее часто встречающихся клинических проявлений данной патологии – астенического синдрома, психоэмоциональных расстройств и кохлеовестибулярных нарушений.
- Биохимической основой терапевтического действия Мексидола является его антиоксидантная активность: Мексидол существенно уменьшает повреждение липопротеиновых структур, восстанавливая активность эндогенной антиоксидантной системы.
- Максимальный терапевтический эффект Мексидола наблюдается у больных с изначально повышенным содержанием продуктов перекисного окисления липидов и истощенной антиоксидантной защитой, что указывает на значение окислительного стресса в патогенезе хронических цереброваскулярных заболеваний.
Полученные данные демонстрируют перспективу применения Мексидола в качестве нейропротектора при сосудистых заболеваниях головного мозга.
Со списком литературы вы можете ознакомиться на нашем сайте www.atmosphereph.ru
Ирина Николаевна Смирнова – канд. мед. наук, врач 2-го сосудистого отделения.
Татьяна Николаевна Фёдорова – докт. биол. наук, вед. сотр. лаборатории биохимии.
Маринэ Мовсесовна Танашян – докт. мед. наук, ученый секретарь института.
Зинаида Александровна Суслина – член-корр. РАМН, директор института.
