Диагностика и лечение диабетической дистальной полинейропатии у больных сахарным диабетом в амбулаторной практике
Статьи Опубликовано в журнале:РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ, ТОМ 16, № 15, 2008
Профессор М.Б. Анциферов, к.м.н. А.К. Волковой
Эндокринологический диспансер Департамента здравоохранения Москвы
В настоящее время диабетическая периферическая нейропатия (ДПН) определяется наличием симптомов и/или признаков нарушения функции периферических нервов у больных сахарным диабетом после исключения других причин [1]. ДПН является наиболее частым осложнением у больных сахарным диабетом (СД). По современным оценкам, частота диабетической полинейропатии у больных СД колеблется от 8 до 100%. Различия в частоте встречаемости ДПН обусловлены использованием различных критериев ее диагностики. При целенаправленном исследовании с использованием средств диагностики (камертона, монофиламента, тип-терма) нарушения функционального состояния периферической нервной системы регистрируются у 60-80% больных СД. Есть данные, что при проведении электромиографии ДПН обнаруживается у 100% больных диабетом [2]. ДПН, являясь поздним осложнением СД, не только значительно снижает качество жизни больного, но и способствует развитию других осложнений СД, таких как язвенные дефекты стоп (нейропатическая форма синдрома диабетической стопы) и нейроостеоартропатия (стопа Шарко). ДПН лежит в основе 50-75% всех нетравматических ампутаций при СД.
Эндокринолог и невропатолог занимающиеся лечением осложнений СД, чаще всего встречаются с сенсомоторной нейропатией. Клинически это проявляется покалыванием, чувством "ползанья мурашек", онемением, зябкостью стоп или чувством жжения, колющими, режущими болями в области стоп, в основном в состоянии покоя, ближе к вечеру. Дистальная симметричная локализация болей - характерный признак ДПН. При физической активности интенсивность жалоб уменьшается, что является характерным диагностическим признаком. Со временем жалобы принимают постоянный и упорный характер. Нередко уже на стадии постановки диагноза СД 2 типа, у больного имеются те или иные нарушения чувствительности, снижение рефлексов на нижних конечностях (ахилловых, коленных).
На приеме врач может столкнуться как с болевыми, так и безболевыми вариантами поражений [3]. Среди болевых форм нейропатий выделяют острую и хроническую [4]. Продолжительность острой болевой формы составляет 6 месяцев. Появляются колющие, стреляющие, ноющие боли в стопах и голенях; чувство жжения, онемения, стягивания стоп. Интенсивность болевого синдрома может усиливаться в вечернее и ночное время. Для хронической нейропатии характерно наличие болевой симптоматики более полугода. Клиническая картина болевого синдрома разнообразна по интенсивности и частоте.
Компенсация СД может приводить к регрессу субъективных симптомов, в то время как ненадлежащий контроль уровня глюкозы в крови, напротив, ухудшает чувствительность и усиливает чувство онемения, жжение, покалывание, парестезии. В случае если пациент не проявляет активных жалоб, диагноз ставится на основании результатов осмотра и диагностического исследования.
Характерные жалобы больного, данные анамнеза (давность симптоматики, наличие сопутствующей патологии), данные объективного осмотра помогают диагностировать ДПН. Одним из основных исследований, проводимых врачом на амбулаторном приеме, является определение нарушения различных видов чувствительности.
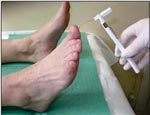
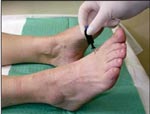
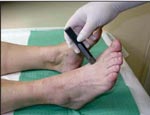
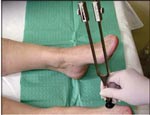
Для оценки наличия изменений тактильной чувствительности применяется монофиламент весом 10 г (5,07 Semmens-Weinstein) (рис. 1); болевой - укол тыльной поверхности большого пальца специальной иглой с притупленным концом (рис. 2); температурной - при помощи определения разницы в ощущениях тепла и холода инструментом "Tip-therm" (рис. 3), вибрационной - с использованием камертона либо биотезиометра (рис 4). Для оценки нарушенной моторной функции исследуются ахилловы и коленные рефлексы.
| Рис. 1. Исследование тактильной чувствительности с помощью монофиламента весом 10 г | Рис. 2. Исследование болевой чувствительности с помощью специальной иглы с притупленным концом (нейро-типс) | Рис. 3. Исследование температурной чувствительности с помощью инструмента "Тип-терм" | Рис. 4. Исследование вибрационной чувствительности с помощью камертона |
 |  |  |  |
Таким образом, для полноценной диагностики ДПН в кабинете врача необходимо наличие камертона, монофиламента, специальной иглы с притупленным концом, инструмента "Тип-терм" и неврологического молотка. Полное определение чувствительности и рефлексов у больного СД занимает не более 5-8 минут. Это позволяет врачу-эндокринологу самостоятельно поставить диагноз ДПН и соответственно определить подходы к лечению полинейропатии.
Для более раннего выявления и углубленного исследования ДПН выполняется электромиография с определением скорости проведения импульса по нервному волокну. Биопсия нерва с последующим морфологическим исследованием является наиболее точным методом диагностики полинейропатии. Однако в повседневной практике этот метод применяется нечасто. Для дифференциального диагноза ДПН и нарушения магистрального кровотока нижних конечностей проводится ультразвуковое дуплексное сканирование артерий голеней и стоп.
После установления диагноза ДПН врач должен определить, с чего следует начинать лечение этого осложнения. Для этого необходимо четко представлять, что лежит в основе патогенеза нейропатии. Согласно современным представлениям основная роль в развитии ДПН принадлежит хронической гипергликемии. Гипергликемия, недостаток инсулина и С-пептида запускают каскад метаболических и сосудистых нарушений, таких как:
Все вышеуказанные механизмы приводят к структурным изменениям нервных волокон у больного СД, вызывая гибель нервных клеткок и замедление проведения импульса по нервным волокнам.
Клинически это проявляется появлением болевой симптоматики, нарушением разных видов чувствительности. Понимая, какую роль имеет хроническая гипергликемия в развитии полинейропатии, становится очевидным, что достижение стойкой компенсации СД является основным направлением в профилактике и лечении ДПН. В ходе исследования DCCT продемонстрировано, что через 5 лет наблюдения на фоне интенсивной инсулинотерапии и достижения компенсации углеводного обмена частота развития нейропатии снижается на 64%, а частота выявления нарушений проводимости по нервным волокнам и развития автономной дисфункции - на 44 и 53% соответственно [5].
В 1998-1999 гг. были сформулированы основные терапевтические цели для больных СД 1 и 2 типа (табл. 1 и 2) [6].
Таблица 1. Терапевтические цели при СД 1. Показатели углеводного обмена (European Diabetes Policy Group, 1998)
| показатели | Адекватный уровень | Неадекватный уровень | |
| 2HbA1c (%) при норме 4,0-6,0 | 6,1-7,5 | >7,5 | |
| Самоконтроль глюкозы крови, ммоль/л | Натощак/перед едой | 5,1-6,5 | >6,5 |
| Через 2 часа после еды | 7,6-9,0 | >9,0 | |
| Перед сном | 6,0-7,5 | >7,5 | |
Таблица 2. Терапевтические цели при СД 2 (риск развития микро- и макрососудистых осложнений). Показатели углеводного обмена (European Diabetes Policy Group, 1998-1999)
| показатель | Низкий риск развития ангиопатии (целевые значения) | Риск макроангиопатии | Риск микроангиопатии |
| HbA1c(%) | ≤6,5 | >6,5 | >7,5 |
| Гликемия натощак/перед едой, ммоль/л: - в плазме венозной крови - цельная капиллярная кровь (самоконтроль) |   ≤6,0 ≤5,5 |   >6,0 >5,5 |   ≥7,0 >6,0 |
| Постпрандиальная гликемия (2 часа после еды), ммоль/л: - в плазме венозной крови и цельной капиллярной крови | <7,5 | ≥7,5 | >9,0 |
В то же время у ряда больных, несмотря на длительную компенсацию СД, клинические проявления ДПН сохраняются. Это является основанием для назначения дополнительной лекарственной терапии с учетом знаний о патогенезе полинейропатии. На сегодняшний день основанием для проведения медикаментозной терапии является наличие болевой формы ДПН с активными жалобами больного на онемение, жжение, боли, покалывание, судороги, ощущение "ползанья мурашек". Как правило, больной без болевой формы полинейропатии (острой или хронической) не нуждается в назначении подобной терапии. При отсутствии жалоб у больного врач должен делать основной акцент в лечении на поддержание оптимальной компенсации СД. Нормализация гликемии часто приводит к устранению нейропатических болей, в то время как лекарственная терапия на фоне декомпенсации углеводного обмена может быть мало- или вовсе неэффективной.
Сегодня из всех видов патогенетической терапии, прошедших многоцентровые клинические испытания (ингибиторы альдозоредуктазы, γ-линолевая кислота, вазодилататоры (ингибиторы АПФ или аналоги простациклина), фактор роста нерва, аминогуанидин, миоинозитол) в клинической практике применяются только препараты α-липоевой кислоты. Серьезные побочные эффекты, а также недостаточная клиническая эффективность ограничили применение других (вышеуказанных) препаратов.
Учитывая ведущую роль окислительного стресса в развитии ДПН, назначение антиоксиданта - α-липоевой кислоты - патогенетически оправдано. Основные механизмы патогенетического действия этого препарата включают: подавление образования свободных радикалов; улучшение энергетического метаболизма нейронов; восстановление окисленных антиоксидантных систем организма, в частности, витамина Е; улучшение нарушенного эндоневрального кровотока и, как результат, увеличение проводимости по сенсорным и моторным нервным волокнам. Эффективность применения α-липоевой кислоты в качестве средства для лечения периферической полинейропатии подтверждено несколькими рандомизированными двойными слепыми плацебо-контролируемыми испытаниями, такими как ALADIN, DEKAN, ORPIL, SYDNEY Так, в исследовании ALADIN (Alpha-Lipoic Acid in Diabetic Neuropathy) была подтверждена высокая клиническая безопасность этого препарата и определена его эффективная дозировка - 600 мг/сут. [7]. Было отмечено, что кратковременная (3 недели) в/в инфузионная терапия α-липоевой кислотой в указанной дозе способствует клиническому регрессу основных проявлений ДПН. В исследовании ALADIN II (1999) продемонстрировано, что длительная пероральная терапия α-липоевой кислотой статистически значимо улучшает нейрофизиологические показатели, повышая, в частности, скорость проведения по сенсорным и моторным нервным волокнам [8]. По результатам исследования ALADIN III, длительный пероральный прием α-липоевой кислоты в суточной дозе 1800 мг в течение 6 месяцев приводит к достоверному уменьшению объективных симптомов сенсомоторной полинейропатии у больных СД 2 типа [9]. Эффективность α-липоевой кислоты в качестве средства терапии и профилактики автономной кардиальной нейропатии была доказана в исследовании DEKAN (Deutsche Kardiale Autonome Neuropathie) [10].
Положительный терапевтический эффект перорального приема α-липоевой кислоты (1800 мг/сут.) на течение ДПН у больных СД отмечен в исследовании ORPIL ("Oral Pilot...") [11]. В исследовании SYDNEY (SYmptomatic Diabetic NEuropathY trial) было показано, что 3-недельный курс в/в введения α-липоевой кислоты быстро уменьшает клинические проявления полинейропатии и улучшает электрофизиологические показатели проводимости нервов [12].
В исследовании, проведенном на базе отделения диабетической стопы Эндокринологического диспансера города Москвы, продемонстрирована эффективность приема α-липоевой кислоты как высокой дозировки препарата в течение короткого периода времени (1800 мг в стуки в течение 4 недель), так и невысокой дозировки в течение длительного времени (600 мг в сутки в течение 3 месяцев) приема [13].
Таким образом, проведенные контролируемые исследования показали, что применение препаратов α-липоевой кислоты позволяет уменьшить как субъективные, так и объективные проявления диабетической полинейропатии, уменьшает болевой синдром, улучшает чувствительность, что подтверждается данными электрофизиологических исследований. Также показана хорошая переносимость и безопасность α-липоевой кислоты как при парентеральном введении, так и при приеме внутрь.
В настоящее время выпускаются несколько препаратов, содержащих различные соли α-липоевой кислоты (этилендиаминовую, трометамоловую, меглюминовую). При введении меглюминовой соли α-липоевой кислоты -препарат Тиогамма ("Верваг Фарма", Германия) частота побочных эффектов ниже, чем при инфузии других солей α-липоевой кислоты [К. Lehman, 2000]. Кроме этого, из всех препаратов только Тиогамма выпускается во флаконах, защищенных от света. Каждый флакон содержит 600 мг меглюминовой соли α-липоевой кислоты в виде готового раствора, не требующего дополнительного разведения. Инфузии проводятся непосредственно из флаконов, что существенно повышает безопасность проводимой терапии.
При выраженных симптомах полинейропатии препараты α-липоевой кислоты первоначально назначают в/в в дозе 600 мг ежедневно в течение 2-3 недель. В наиболее тяжелых случаях внутривенные инфузии проводят более длительно - до 3-4 недель. Препарат вводят в/в капельно в течение 20-30 минут. Так как α-липоевая кислота -фоточувствительное соединение, разведенный препарат должен быть защищен от света в процессе инфузии. После внутривенного введения больного переводят на пероральный прием Тиогаммы (в течение 2-3 месяцев) в суточной дозе 600 мг Таблетки принимают за 30-40 минут до завтрака.
В амбулаторных условиях внутривенные инъекции α-липоевой кислоты возможно делать в условиях "дневного стационара" на базе окружных эндокринологических или неврологических отделений, то есть без госпитализации в стационар. Врач должен помнить, что перед назначением в/в введения α-липоевой кислоты необходима консультация окулиста, так как наличие у больного свежих кровоизлияний на глазном дне у больного СД является противопоказанием для парентерального введения препарата.
Водорастворимые витамины группы В применяются при лечении ДПН в течение нескольких десятилетий. Механизм действия тиамина при ДПН связан прежде всего со способностью препарата тормозить гликолиз, образование лактата и конечных продуктов гликозилирования, тем самым ослабляя токсический эффект хронической гипергликемии. Снижая гликирование белков, тиамин и его активный метаболит - тиамин пирофосфат блокируют прогрессирование полинейропатии у больных СД.
Учитывая, что у больных ДПН отмечено снижение концентрации тиамина [14], восстановление его уровня должно привести к улучшению энергетического метаболизма нервной ткани. Однако терапевтическая эффективность водорастворимых тиаминов выражена слабо из-за крайне низкой биодоступности и плохой абсорбционной способности этих препаратов в желудочно-кишечном тракте. Открытие бенфотиамина позволило отрыть новую эру в лечении диабетической невропатии. Бенфотиамин в 10 раз лучше всасывается в ЖКТ и в значительных концентрациях обнаруживается в тканях [15]. Применение бенфотиамина в рандомизированном плацебо-контролированном исследовании привело к улучшению как показателей вибрационной чувствительности, так и скорости прохождения нервного импульса по малоберцовому нерву [16]. В работе [Schmidt J., 2002] показано, что прием бенфотиамина (у 1154 больных с симптоматической полинейропатией) привел к достоверному снижению клинической симптоматики у 2/3 больных [17]. При этом отмечалось явная зависимость от дозировки: прием перорально 2 раза в день по 150 мг бенфотиамина принес значительно лучшие результаты, чем однократный прием по 150 мг в день. Показано, что по сравнению с аминогуанидином бенфотиамин в большей мере подавляет образование конечных продуктов гликозилирования [18]. Повышение активности транскетолазы (аутогенного фермента, обезвреживающего продукты ускоренного гликозилирования) в 400 раз на фоне приема бенфотиамина отмечено в исследовании [Hammes H.P. et al., 2003] [19]. Ряд авторов отметили преимущество пероральной терапии бенфотиамином над парентеральной водорастворимой формой тиамина [20,21]. Соответственно, прием бенфотиамина внутрь устраняет необходимость парентерального введения тиамина, что более доступно и приемлемо для больных СД. Все вышеуказанное позволяет рассматривать применение бенфотиамина в качестве важного элемента патогенетической терапии ДПН.
На сегодняшний день бенфотиамин назначают в форме монотерапии (Бенфогамма 150) или комбинации с другими витаминами группы В. Комбинация бенфотиамина (100 мг) и пиридоксида (100 мг) содержится в препарате Мильгамма композитум ("Верваг Фарма", Германия) для приема внутрь. Мильгамма композитум назначается по 1 драже 3 раза в сутки в течение 2 месяцев. В тяжелых случаях и при болевой форме нейропатии лечение начинают с внутримышечных инъекций мильгаммы (2 мл раствора для инъекций содержит 100 мг тиамина, 100 мг пиридоксина, 1000 мкг цианокобаламина, 20 мг лидокаина) один раз в сутки в течение 10 дней, а в дальнейшем переходят на прием Мильгаммы композитум.
Достижение и поддержание нормогликемии у больных СД, применение препаратов с патогенетической направленностью позволяют добиться хорошего клинического эффекта в лечении ДПН. В то же время, несмотря на вышеуказанные меры, у ряда пациентов сохраняются активные жалобы, характерные для полинейропатии: боли, жжение, покалывание. Сохранение болевого синдрома у больных СД является основанием для назначения так называемого симптоматического лечения, главной целью которого является устранение или уменьшение болевой симптоматики (табл. 3).
Таблица 3. Симптоматическая терапия болевой формы диабетической периферической нейропатии
| Фармакологическая группа, лечебные подходы | Лечебный препарат, метод лечения | Дозировка |
| Трициклические антидепрессанты | Амитриптиллин | 25-150 мг |
| Имипрамин | 25-150 мг | |
| Кломипрамин | 25-150 мг | |
| Блокаторы ионных каналов | Карбамазепин | 200-800 мг |
| Габапентин | 900-3600 мг | |
| Мексилетин | 675 мг | |
| Селективные ингибиторы обратного захвата серотонина | Циталопрам | 40 мг |
| Пароксетин | 40 мг | |
| Опиоиды | Трамадол | 50-400 мг |
| Оксикодон | 10-30 мг | |
| Нестероидные противовоспалительные средства | Ибупрофен | 400-800 мг |
| Напроксен | 250-1750 мг | |
| Средства местной терапии | Крем, содержащий капсаицин (0,075%) | Применяется местно, не более 8 недель |
| Кремы, пластыри и гели с 5%-ным содержанием лидокаина | Применяется местно 3-5 раз в сутки | |
| Немедикаментозные методы лечения | Магнитотерапия Чрескожная электро-нейростимуляция Медицинская гимнастика Бальнеотерапия Расслабляющая терапия Акупунктура Электростимуляция спинного мозга | - |
Хорошо известно, что эффективность патогенетической терапии у больных ДПН, находящихся в состоянии неудовлетворительной компенсации СД, крайне мала. Достижение стойкой нормогликемии является длительным процессом, поэтому назначение симптоматической терапии позволяет снизить выраженность болевого синдрома на данный период, а следовательно, улучшить качество жизни больного.
На сегодняшний день во всем мире из всех средств симптоматической терапии препаратами выбора при лечении болевой формы ДПН являются трициклические антидепрессанты (ТЦА - амитриптиллин, имипрамин) и блокаторы ионных каналов (габапентин, карбамазепин, мексилетин) [22]. Симптоматические средства не влияют на механизмы развития полинейропатии. Тем не менее они хорошо зарекомендовали себя как препараты, надежно купирующие болевой синдром у больных с ДПН.
Назначение антидепрессантов больным с болевой формой ДПН может быть также оправдано при наличии депрессии, признаки которой отмечаются у значительной части больных с хронической нейропатической болью. Механизм обезболивающего действия антидепрессантов до конца не ясен, но считается, что ингибирование ими обратного захвата серотонина и норадреналина активизирует нисходящий путь торможения боли. Эффективность ТЦА показана в ряде плацебо-контролируемых исследований. Рекомендуется начинать применение препаратов с низких доз (10 или 24 мг/сут.), преимущественно вечером. Максимальная доза 150 мг/сут.
В то же время нельзя забывать о целом ряде противопоказаний и побочных эффектов, ограничивающих применение ТЦА в повседневной практике. Это прежде всего острый и подострый инфаркт миокарда с нарушением внутрижелудочковой проводимости и закрытоугольная глаукома. С осторожностью препарат следует применять больным с ИБС, аритмией, артериальной гипертонией, вегетативной недостаточностью. Американское общество геронтологов в терапевтическом руководстве (2002 г.) не рекомендует назначать эти препараты пациентам пожилого возраста.
В настоящее время габапентин (Габагамма) - антиконвульсант второго поколения - является препаратом, успешно купирующим все виды нейропатической боли. Механизм его действия основан на способности связываться с добавочной субъединицей альфа-2-дельта потенциалзависимых Са2+-каналов, которая расположена на внеклеточной стороне канала. Это приводит к уменьшению притока Са2+ к нервным окончаниями, следовательно, тормозит высвобождение ряда нейротрансмиттеров, включая глутамат и субстанцию Р. Таким образом, блокируется распространение импульса в синаптической щели на следующий нейрон.
Габагамма принимается независимо от приема пищи. Начальная доза 300 мг/сут. Период титрации дозы до максимально допустимой (3600 мг/сут.) длится 12-14 дней. К побочным эффектам препарата можно отнести головокружение, сонливость, атаксию, нистагм, тошноту, периферические отеки. Все это несколько ограничивает применение препарата у пожилых людей.
Антиконвульсант первого поколения - карбамазепин по химическому строению близок к ТЦА. Наибольшую эффективность препарат показал у пациентов с невралгией тройничного и языкоглоточного нервов. Вместе с тем ряд клинических исследований подтверждают эффективность применения препарата у больных с болевой формой ДПН. Начальная доза препарата 100-200 мг/сут. Титрование дозы идет до 800-1200 мг/сут. Многочисленные побочные эффекты препарата (такие как агранулоцитоз, апластическая анемия, гепатит, нарушение почечной функции, головокружение, атаксия, сонливость, отеки) позволяют применять его в клинической практике только при условии регулярного врачебного контроля. Необходимо контролировать печеночные ферменты и показатели развернутого анализа крови сначала еженедельно, потом ежемесячно.
Селективные ингибиторы обратного захвата серотонина (пароксетин, циталопрам) по сравнению с ТЦА имеют меньшее количество побочных эффектов. Однако контролируемые исследования, проведенные у пациентов с нейропатической болью, показывают ограниченную эффективность этих препаратов [23]. Средняя суточная доза препарата составляет 20-40 мг
В случае неэффективности терапии болевого синдрома вышеуказанными лекарственными средствами, возможно назначение опиоидных анальгетиков (трамадол, оксикодон). Следует помнить, что в настоящее время нет данных о долгосрочной эффективности опиоидных анальгетиков в терапии нейропатической боли. Из их главных побочных эффектов необходимо отметить угнетение дыхательного центра, сонливость, нарушения сна, спутанность сознания, ортостатическую гипотензию, коллапс, а также побочные явления со стороны ЖКТ (возбуждение пусковой зоны рвотного центра). При продолжительном применении возможно развитие толерантности к лекарственным препаратам. Трамадол - препарат, обладающий низкой аффинностью к опиоидным μ-рецепторам и являющийся ингибитором обратного захвата серотонина, сначала назначают в низких дозах (50 мг 1-2 раза в сутки), а затем титруют до максимальной дозы (100 мг 4 раза в сутки).
Применение других препаратов с анальгетической активностью, таких как нестероидные противоспалительные средства (ибупрофен, напроксен), ограничено как значительными побочными явлениями (риск агранулоцитоза, нарушения со стороны ЖКТ), так и в связи с низкой эффективностью.
К анестетикам местного действия относят кремы, пластыри и гели с 5%-ым содержанием лидокаина, а также крем на основе капсаицина. Механизм действия лидокаина основан на блокировании транспорта ионов Na+ через клеточную мембрану периферичеких нейронов. За счет стабилизации клеточной мембраны замедляется распространение потенциала действия, что приводит к уменьшению боли.
Другой местный анестетик - капсаицин получают из стручков красного жгучего перца. Воздействуя на ваниллоидные рецепторы, капсаицин уменьшает выброс субстанции Р из окончания чувствительных нервов. Эффект наступает через 2 недели регулярного применения крема. Длительность лечения данным препаратом не должна превышать 8 недель. Как капсаицин, так и лидокаин при местной терапии могут вызывать жжение, покалывание, покраснение [23,24]. Поэтому необходимо тщательно подбирать дозу препарата.
Несмотря на отсутствие с точки зрения доказательной медицины убедительных данных эффективности немедикаментозных методов лечения (магнитотерапии, психофизиологической релаксации, рефлексотерапии, бальнеотерапии, чрескожной электронейростимуляции и других физиотерапевтических процедур), нельзя полностью отказываться от использования данных методов терапии. Эти виды лечения становятся актуальными, особенно тогда, когда фармакотерапия болевого синдрома при ДПН противопоказана или вызывает непереносимые побочные эффекты.
На сегодняшний день только комплексный подход (сочетание патогенетической и симптоматической терапии) в лечении болевой формы ДПН может дать максимальный клинический эффект и улучшить качество жизни пациента.
Таким образом, в современных условиях в амбулаторной практике у врача есть все возможности для своевременной диагностики и эффективного лечения диабетической периферической полинейропатии. Литература
1. International guidelines on the out-patient management of diabetic peripheral neuropathy, 1996
2. Dyck P.J., Ltchy W.J. et al. Variables influences neuropathic endpoints. The Rochester Diabetic Neuropathy Study of Health Subjects. Neurology, 1995,45: 1115-1121
3. International Guidelines on the Out-patient Management of Dabetic Peripheral neuropathy. Abingdon: The Medicine Group (Education) Ltd., 1998
4. Kempler P. Neuropathies. Springer. Budapest. 2002.
5. The Diabetes Control and Complication Trial Research Group. The effect of intensive diabetes therapy on the development and progression of diabetic neuropathy. Ann Intern Med 1995; 122:561-8
6. Дедов И.И., Шестакова М.В. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. М. 2006. стр.11-18
7. Ziegler D, Hanefeld M, Ruhnau K.J, et al. Treatment of symptomatic diabetic peripheral neuropathy with the anti-oxidant alpha -lipoc acid. A 3-week multicentre randomized controlled trial (ALADIN study). Diabetologia 1995;38:1425-33.
8. Reljanovic M, Reichel G., Rett K. Et all. Treatment of diabetic polyneuropathy with the antioxidant thioctic acid (alpha-lipoic acid): a two-year multicenter randomized double-blind placebo-controlled tral (ALADIN I) // Free Radc Res.-1999. - Vol.31. - P. 171-179.
9. Ziegler D, Hanefeld M, Ruhnau K.J, et al. Treatment of symptomatic diabetic polyneuropathy with the anti-oxidant alpha-lipoic acid: a 7-month multicenter randomized controlled trial (ALADIN III Study). ALADIN III Study Group. Alpha-Lipoic A in Diabetic neuropathy. Diabetes Care 1999 Aug;22(8):1296-301.
10. Ziegler D, Schatz H, Conrad F, et al. Effects of threatment with the antioxidant alpha -lipoic acid on cardiac autonomic neuropathy in NIDDM patients. A 4-month randomized controlled multicenter trial (DEKAN Study). Dab Care 1997;20:369-73.
11. Zyegler D, Reljanovic M, Mehnert H, et all. Alfa-Lipoic acid in the treatment of diabetic polyneuropathy in Germany current evidence front clinical trails. Exp Clin Endocrinol Diabetes 1999;107:421-30.
12. AmetovA, BarinovA, O Brien P. et al. The sensory symptoms of diabetic polyneuropathy are improved with alpha - lipolc acid: the SYDNEY trial. /Diabetes Care. - 2003. - Vol.26. - P. 770-776.
13. Комелягина Е.Ю., Волковой А.К., Мыскина Н.А., Анциферов М.Б. Сравнительная эффективность различных режимов перорального приема тиоктовой кислоты (Тиоктацид БВ) в терапии болевой формы диабетической дистальной нейропатии. Фарматека. 2006, 17:89- 94
14. Jermendy G. The effectiveness of Milgamma in treatment of diabetic polyneuropathy. Medicuc Universalis 1995.
15. Greb A., Bitsch R.: Int.J.Cin. Pharmacol. Therapy 36, (1998) 214-221
16. Stracke H. Et al.: Exp. Clin. Endocrin.& Dabetes: 104(1996) 311-316
17. Schmidt J.: Der Kassenarzt 14/15 (2002) 40-43
18. Booth. A.A., et al.: Biochem. And Biophy. Res. Comm. 220 (1996) 1084-1088
19. Hammes H.P. et al.: Nature Medicine 9, №3 (2003) 294-299)
20. Schreeb K.H. rtal: Eur.J.Clin. Pharmacol. 52,4(1997) 319-320
21. Маркина О.А. Клиническая фармакология и терапия №12(2), 2003, с. 6-9
22. Atta N, Cruccu G, Haanp M, Hansson P, Jensen TS, Nurmikko T, Sampao C, Sindrup S, Wiffen P; EFNS Task Force. EFNS guidelines on pharmacological treatment of neuropathic pan. Eur J Neurol, 2006; 13 (11): 1153-69
23. Spruce M.C., Potter D.V. et al. The pathogenesis and management of painful diabetic neuropathy: a review. Diabetic Medicine 2003, Vol.20, 2: 88-99
24. Ziegler D. Treatment of neuropathic pain. In: Textbook of Diabetic Neuropathy, Thieme 2002, pg.211- 224
