akvion.ru
akvion.ru

Комбинированный препарат для повышения мужской фертильности
далее...
Больше информации на сайтах:
www.reproduction.info
www.plan-baby.ru
Влияние комплекса Сперотон на функциональные характеристики сперматозоидов у мужчин с идиопатической патозооспермией
СтатьиОпубликовано в журнале:
«ПРОБЛЕМЫ РЕПРОДУКЦИИ»; № 4; 2016; стр. 106-110.
Акад. РАН Г.Т. Сухих, А.Ю. Попова, Р.И. Овчинников, И.В. Ушакова
ФГБУ «Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова» Минздрава России, Москва, Россия, 117997
Представлен обзор современных данных литературы по вопросу функциональных изменений сперматозоидов и их роли в бесплодном браке. Приведены результаты исследования влияния комплекса Сперотон на функциональные характеристики сперматозоидов и реальную фертильность мужчин с идиопатической патозооспермией. Полученные данные позволяют селективно подходить к диагностике и терапии пациентов с идиопатической патозооспермией.
Ключевые слова: бесплодный брак, идиопатическая патозооспермия, оксидативный стресс, акросомальная реакция.
The influence of Speroton on functional characteristics of sperm in men with idiopathic patozoospermia
G.T. Sukhikh, A.Yu. Popova, R.I. Ovchinnikov, I.V. Ushakova
Academician V.I. Kulakov Research Center for Obstetrics, Gynecology, and Perinatology (dir. — professor G.T. Sukhikh, MD, PhD, Academician of the RAS) Ministry of Healthcare of Russia, Moscow, Russia, 117997
This article presents a review of modern literature data on the functional changes in sperm cells and their role in a barren marriage. The study results assessing the impact of Speroton on functional characteristics of sperm and actual fertility of men with idiopathic patozoospermia are presented. The data present a selective approach to the diagnosis and treatment of patients with idiopathic patozoospermiа.
Keywords: infertility, idiopathic patozoospermia, oxidative stress, reaction of acrosome.
Бесплодие является болезнью репродуктивной системы, характеризующейся неспособностью к зачатию по причине мужского или женского фактора [ВОЗ, 2011]. Настоящая проблема носит пандемический характер, так как отмечено четырехкратное увеличение заболеваемости начиная с 1980 г. [1]. На сегодняшний день мужской фактор является причиной бесплодия почти в половине случаев [2, 3]. Данный факт не только имеет серьезное негативное влияние на качество жизни пациентов, но также приводит к огромным социально-экономическим катастрофам. Известно, что оплодотворяющая способность сперматозоидов зависит от секреторной активности вспомогательных половых желез: придатков яичек, предстательной железы и семенных пузырьков [4]. Нарушение функции этих органов способно приводить к снижению количественных и функциональных показателей эякулята: концентрации, подвижности, морфологии сперматозоидов, нарушению акросомальной реакции (АР), образованию антиспермальных антител (АСАТ). Одной из основных причин, приводящих к нарушению мужской репродуктивной функции, считают избыточную продукцию активных форм кислорода (АФК) [5]. Активные формы кислорода — это окислители с высокой реакционной способностью, принадлежащие к классу свободных радикалов (ROS). Они очень неустойчивые окислители, поэтому реагируют со многими биохимическими веществами, такими как липиды, аминокислоты, углеводы, белки и ДНК. Хотя наличие ROS в сперматозоидах было обнаружено еще в 1943 г. [6], однако их роль в мужской репродуктивной физиологии начали изучать лишь в 1989 г. [7]. Известно, что в результате воздействия на организм мужчины различных негативных внутренних и внешних факторов происходит повышение генерации АФК. Так, низкий уровень АФК необходим для нормальной функции сперматозоидов, что обеспечивает капацитацию, гиперактивацию, АР, а также слияние и оплодотворение с ооцитами [8, 9]. А повышение уровня ROS запускает капацитацию и АР в более ранние сроки, что приводит к нарушению их оплодотворяющей способности [10]. Другими словами, при повышении уровня АФК возникает каскад патологических состояний, которые отрицательно влияют на функцию сперматозоидов [11]. Примерно от 40 до 80% пациентов с бесплодием имеют высокие уровни АФК [4].
Примечательно, что выявление повышенного уровня АФК в некоторых случаях может являться важным методом для обработки спермы с целью искусственного оплодотворения.
Появляется все больше доказательств того, что мощные антиоксиданты, содержащиеся в семенной плазме, защищают сперматозоиды от пагубных эффектов ROS. Защитные способности семенной плазмы имеют значительные индивидуальные колебания. И в том случае, когда производство АФК переполняет антиоксидантную защиту, возникает окислительный стресс (ОС). Последний существенно ухудшает сперматогенез и функцию спермы, что может привести к мужскому бесплодию [12, 13]. ОС может привести к денатурации ДНК в одноцепочечной ДНК и двунитевым разрывам ДНК [14]. В семенной плазме бесплодных мужчин уровень антиоксидантов значительно ниже, чем у фертильных мужчин. При бесплодии, связанном с повышенным уровнем кислородных радикалов в сперме, отмечается терапевтический эффект антиоксидантов, влияющих на уровень ROS. Поэтому тщательная диагностика нарушений функциональной способности сперматозоидов, а также выявление и успешное лечение пациентов с идиопатической патозооспермией — путь к восстановлению утраченной способности к зачатию.
Наиболее важным биохимическим маркером нормального созревания сперматозоидов является L-карнитин, продуцируемый придатком яичка. Физиологическая роль придатка яичка заключается в создании условий для нормального развития сперматозоидов путем секреции ряда соединений, в том числе L-карнитина, участвующего в переносе ацил-группы и окислительном фосфорилировании жирных кислот в митохондриях и, как следствие, обеспечении энергией, используемой сперматозоидами для созревания и приобретения ими подвижности.
L-карнитин, играющий большую роль в защите клеточной мембраны от ROS, все шире используется в лечении мужского бесплодия в последнее время [4, 5]. Помимо L-карнитина качество спермы также зависит от поступления в организм витаминов и некоторых аминокислот.
Селен влияет как на адаптивный, так и на врожденный иммунитет, способствует пролиферации и дифференциации CD4+ Т-лимфоцитов в сторону Т-хелперов, поддерживая тем самым острый клеточный иммунный ответ [15]. Также потенциальной антивирусной активностью обладает витамин Е [16]. Доказано, что прием витамина Е снижает «тяжесть» ОС в ткани яичек, повышает подвижность сперматозоидов и положительно влияет на их способность проникать в яйцеклетку. Витамин E обладает синергизмом с селеном, т.е. при одновременном приеме эти вещества проявляют выраженную эффективность в более низких дозах, чем при употреблении по отдельности, за счет взаимного предотвращения окисления (разрушения) как в кишечнике, так и в тканях. Цинк — жизненно важный микроэлемент, который можно обнаружить практически в любых тканях организма. Цинк абсолютно необходим для клеточного дыхания, утилизации кислорода, воспроизведения генетического материала (ДНК и РНК), поддержания целости клеточных стенок и обезвреживания ROS. В организме человека цинк концентрируется во всех органах и тканях, в том числе в яичках, придатках яичек, предстательной железе, в достаточно большом количестве содержится в сперме. Он запускает и поддерживает процессы производства мужского полового гормона — тестостерона и активизирует сперматогенез. Цинк активирует глутатионпероксидазу, которая необходима для нормального созревания и подвижности сперматозоидов, а также участвует в регуляции активности других ферментов спермоплазмы, способствует регуляции процессов коагуляции и разжижения эякулята.
Цель настоящей работы — оценка влияния комплекса Сперотон на функциональные характеристики сперматозоидов и реальную фертильность мужчин с идиопатической патозооспермией.
Материал и методы
В исследование включены 40 инфертильных мужчин в возрасте от 26 до 45 лет с различными идиопатическими нарушениями спермограммы. Средний возраст составил 34±3,2 года. Все пациенты случайным образом были разделены на две группы: 1-я, основная группа — 20 пациентов, получавших препарат Сперотон по 1 саше 1 раз в день в течение 3 мес; 2-я, контрольная группа — 20 пациентов, получавших плацебо по 1 саше 1 раз в день на протяжении 3 мес. Исследование показателей спермограммы осуществлялось в соответствии с требованиями ВОЗ до лечения и через 3 мес от начала приема препарата. Оценивались концентрация, подвижность, морфология сперматозоидов по строгим критериям Крюгера, объем эякулята. Согласно концепции оксидативного стресса, АФК появляются, когда естественные антиоксиданты не способны блокировать АФК. В нашем исследовании уровень АФК оценивался методом OxiSperm — метод оценки повышенного количества супероксидных радикалов, присутствующих в эякуляте. Тест основан на химических свойствах нитросинего тетразолия, который находится в наборе 0хiSрегm в виде реакционного геля. Результаты оценивали в процентах. Оценка АР сперматозоидов была проведена методом проточной цитофлуорометрии. После обработки сперматозоидов определяли процент сперматозоидов, у которых прошла АР.
Критерии включения: мужчины с бесплодием (отсутствие беременности у партнерши в браке более 12 мес половой жизни без контрацепции) в возрасте от 20 до 45 лет; наличие в анализе спермограммы идиопатической патозооспермии (олигозооспермия, астенозооспермия, тератозооспермия), нарушений АР сперматозоидов и повышения уровня АФК; отсутствие клинических и лабораторных признаков воспалительных изменений придаточных половых желез; отсутствие при пальпации варикоцеле и других негативно влияющих на сперматогенез заболеваний органов мошонки, подтвержденное результатами ультразвукового исследования (УЗИ) и допплерографией; отсутствие иммунной формы бесплодия (MAR-testIgG<10%); отсутствие выраженной соматической патологии.
Критерии исключения: обструктивная или необструктивная азооспермия или иммунологическая форма бесплодия; наличие женского бесплодия у партнерши (непроходимость маточных труб, нарушения овуляции, распространенный эндометриоз и др.); возраст моложе 20 и старше 47 лет; алкогольная или наркотическая зависимость; повышенная чувствительность к любому из компонентов препарата; нарушения функции печени и почек.
Статистические тесты проводились как двусторонние с уровнем а=5%. Для описания количественных переменных были использованы следующие статистические характеристики: количество пациентов, среднее значение, стандартное отклонение, стандартная ошибка, медиана, экстремальные значения. Статистическая достоверность изменений количественных переменных оценивалась с использованием парного t-теста Стьюдента или знакового критерия Уилкоксона.
Результаты
Сбор анамнеза показал, что ни один из пациентов не подвергался воздействиям ионизирующих излучений и не употреблял наркотических средств, а также не наблюдалось систематического употребления алкоголя. К сожалению, с помощью сбора анамнеза и подробного изучения медицинской документации выяснить этиологию заболевания не представлялось возможным. При осмотре у больных не отмечались внешние признаки гипогонадизма. При пальпации органов мошонки отмечался нормальный объем яичек. По данным УЗИ предстательной железы, у 62,7% больных были выявлены ультразвуковые признаки хронического простатита. Результаты УЗИ органов мошонки патологических изменений не показали. При цветовом допплеровском картировании сосудов органов мошонки патологический рефлюкс на высоте пробы Вальсальвы не был регистрирован. При стандартном спермиологическом исследовании был поставлен диагноз патозооспермии. Причем 42% больных имели астенозооспермию, 20% — астенотератозооспермию, 9% — тератозооспермию, 11% —олигоастенозооспермию, 12% — олиастенотератозооспермию. По данным гормонального анализа крови, изменений в средних показателях гормонов (ФСГ, ЛГ, тестостерон, пролактин) не отмечено.
Сравнительное изучение динамики основных показателей спермограмм до лечения и через 3 мес приема препарата выявило достоверное увеличение количества сперматозоидов с поступательным движением (А+Б) в 1-й группе пациентов (с 29,2±1,2 до 43,6±0,8%) по сравнению с пациентами 2-й группы (с 28,2±0,8 до 31,3±1,2%; р<0,05) (рис. 1).
Рис. 1. Сравнительная динамика значений подвижности (А+В) сперматозоидов (%).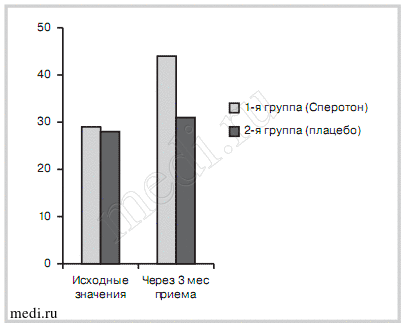
Также достоверно более значительное увеличение концентрации сперматозоидов в эякуляте наблюдалось у пациентов 1-й группы (с 13,2±0,5 до 18,9±0,8 млн/мл) по сравнению с пациентами 2-й группы (с 11,3±0,5 до 12,7±0,5 млн/мл; р<0,05) (рис. 2).
Рис. 2. Сравнительная динамика значений концентрации сперматозоидов (млн/мл).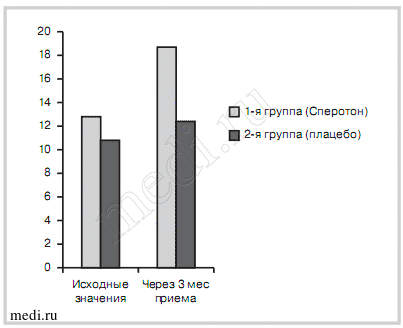
Отмечалось увеличение количества морфологически нормальных форм сперматозоидов через 3 мес лечения — более значительное в 1-й группе (с 2±0,7 до 4,2±0,8%) по сравнению со 2-й группой (с 2,3±0,7 до 3,0±0,5%).
Также выявлены положительные изменения физических и химических показателей спермы (АФК, АР). По результатам лечения в основной группе показатели OxiSperm-теста значимо улучшились после 3 мес приема препарата. Снижение показателей окислительного стресса ROS (по данным OxiSperm-теста) в основной группе составило 27,3% по сравнению с исходным значением, при этом в контрольной группе показатели ухудшились на 6,5% (табл. 1).
Таблица 1.
Сравнительная динамика показателей АФК (в %)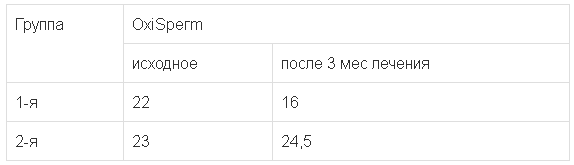
Доля пациентов с улучшением показателей АР через 3 мес после исходного анализа в основной группе была значимо выше, чем в контрольной. Так, спонтанная АР в основной группе составила 16,2±2,3 и 21,1±5,3% соответственно, тогда как индуцируемая реакция — 31,6±1,3 и 28,9±1,6% соответственно (р<0,05), что в свою очередь демонстрирует положительную динамику индекса АР (табл. 2).
Таблица 2.
АР сперматозоидов в основной и контрольной группах (в %)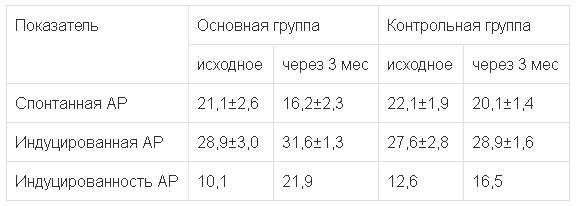
На фоне приема Сперотона ни у одного пациента не наблюдалось нежелательных эффектов. У 3 семейных пар из 1-й группы была зафиксирована клиническая беременность.
Обсуждение
В настоящее время имеется достаточное количество работ, посвященных роли антиоксидантов в мужской фертильности. Известно, что различные антиоксиданты являются некой системой обороны, которая включает как ферментативные, так и неферментативные молекулы. Как правило, антиоксиданты семенной плазмы производятся против АФК, чтобы поддерживать их нормальный уровень, необходимый для выполнения ими своей физиологической функции [16]. Другими словами, антиоксиданты в семенной плазме и сперматозоидах поддерживают устойчивое состояние уровня ROS в сперме путем преобразования свободных радикалов в нереагирующие вещества. Эта способность определяется зрелостью сперматозоида, имеющего цитоплазму. Другими словами, цитоплазма является основным источником антиоксидантов, ее отсутствие в зрелом сперматозоиде вызывает дефицит как антиоксидантной защиты, так и эндогенного механизма восстановления. В последнее время L-карнитин благодаря роли в защите клеточной мембраны от ROS приобрел большое значение в лечении мужского бесплодия [4, 5]. Карнитин обеспечивает сперматозоидам энергию для подвижности и созревания через бета-окисление длинноцепочечных жирных кислот в митохондрии. Учитывая данные факты, пациентам, имеющим идиопатическое нарушение сперматогенеза и желающим сохранить или максимально быстро восстановить свою фертильность, в комплексной терапии рекомендовано использование антиоксидантов. Антиоксидантные комплексы позволят восстановить дисбаланс между АФК и антиоксидантной емкостью спермы, что в свою очередь восстанавливает моторику и дефекты ДНК сперматозоидов. Таким образом, у мужчин с идиопатическим бесплодием, получавших антиоксидантный комплекс Сперотон, отмечалась положительная динамика показателей спермограммы, а также индуцируемости АР и снижение уровня АФК, что в свою очередь позволяет говорить об увеличении вероятности благоприятных исходов относительно как естественного зачатия, так и программ ВРТ. Однако требуются дополнительные исследования для получения более подробных данных.
Заключение
Комплекс Сперотон является перспективным видом терапии, которая, улучшая функциональные характеристики сперматозоидов, способствует естественному зачатию у супружеских пар с исходным идиопатическим бесплодием у мужчин. На основании полученных данных можно сделать вывод, что комплексная консервативная терапия, включающая антиоксиданты, является эффективной в коррекции различных форм патозооспермии. Рекомендуются дальнейшие исследования в этой области для достижения высокой эффективности лечения бесплодия у мужчин, а также уменьшения сроков восстановления фертильности для пациентов, прибегающих к экстракорпоральному оплодотворению.
1. Maheshwari A, Hamilton M, Bhattchary S. Effect offemale age on the diagnostic categories of infertility. Hum Reprod. 2008;23(3):538-542.
2. Bronte AS, Allyse A, Lawrence BW, Marrs RP. Age thresholds for changes in semen parameters in men. Fertil and Steril. 2013 0ctober;100:lssue 4:952-958.
3. Irvine DS. Epidemiology and aetiology of male infertility. Hum Reprod. 1998;13:Suppl. 1:33-44.
4. Lenzi A, Lombardo F, Sgro P, et al. Use of carnitine therapy in selected cases of male factor infertility: a double-blind crossover trial. Fertil Steril. 2003;79(2):292-300.
5. Lenzi A, Sgro P, Salacone P, Paoli D, Gilio B, Lombardo F, et al. A placebo-controlled double-blind randomized trial of the use of combined l-carnitine and l-acetyl-carnitine treatment in men with asthenozoospermia. Fertil Steril. 2004;81:1578-1584.
6. Olayemi FO. A review on some causes ofmale infertility. Afr J Biotechnol. 2010;9:2834-3842.
7. Abd-Allah AR, Aly HA, Moustafa AM, Abdel-Aziz AA, Hamada FM. Adverse testicular effects of some quinolone members in rats. Pharmacol Res. 2000;41:211-219a.
8. Khaki A, Heidari M, Ghaffari Novin M, Khaki AA. Adverse effects of ciprofloxacin on testis apoptosis and sperm parameters in rats. Iran J Reprod Med. 2008;6:71-76.
9. Aral F, Karacal F, Baba F. The effect of enrofloxacin on sperm quality in male mice. Res Vet Sci. 2008;84:95-99.
10. El-Bahrawy K, El-Hassanein ES, Kamel YM. Comparison of gentamycin and ciprofloxacin in dromedary camels’ semen extender. World J Agric Sci. 2010;6:419-424.
11. Sies H. Strategies of antioxidant defense. Eur J Biochem. 1993;215:213-219.
12. Tremellen K. Oxidative stress and male infertility — a clinical perspective. Hum Reprod Update. 2008;14:243-258.
13. Agarwal A, Makker K, Sharma R. Clinical relevance of oxidative stress in male factor infertility: an update. Am J Reprod Immunol. 2008;59:2-11.
14. Agarwal A, Prabakaran SA, Sikka C. Clinical relevance of oxidative stress in patients with male factor infertility: Evidence based analysis. American Urological Association Update Ser. 2007;26:1-11.
15. St. Steinbrenner H, Al-Quraishy S, Dkhil MA, Wunderlich F, Sies H. Dietary selenium in adjuvant therapy of viral and bacterial infections. Adv Nutr. 2015;6(1):73-82.
16. Fiorino S, Bacchi-Reggiani L, Sabbatani S, Grizzi F, di Tommaso L, Masetti M, Fornelli A, Bondi A, de Biase D, Visani M, Cuppini A, Jovine E, Pession A. Possible role of tocopherols in the modulation of host microRNA with potential antiviral activity in patients with hepatitis B virus-related persistent infection: a systematic review. Br J Nutr. 2014;112(11):1751-1768.
Комментарии
ПРАКТИКА ПЕДИАТРА