Оптимизация ведения пациентов с диабетической полиневропатией с помощью междисциплинарного подхода
СтатьиОпубликовано в журнале:
Неврология, 2017
В.А. Парфенов, д.м.н., профессор, В.А. Головачева, к.м.н., В.В. Фадеев, д.м.н., профессор, чл.-корр. РАН, А.Ю. Воловик, А.А. Головачева
Первый Московский государственный медицинский университет им. И.М. Сеченова
Введение. Ведущее значение в ведении пациентов с диабетической полиневропатией (ДПН) имеет междисциплинарный подход, включающий фармакотерапию, образовательную терапию, когнитивно-поведенческую терапию (КПТ). Отсутствует отечественный опыт междисциплинарного лечения пациентов с ДПН.
Цель исследования – изучение эффективности лечения пациентов с ДПН с использованием междисциплинарного подхода.
Пациенты и методы. В исследование было включено 50 пациентов (29 женщин и 21 мужчина) в возрасте от 20 до 78 лет (средний возраст 57,6 ± 10,2 года) с сахарным диабетом (СД) 1-го и 2-го типов и ДПН. Все пациенты получали междисциплинарное лечение, состоящее из фармакотерапии, образовательной программы, КПТ. Всем пациентам проводилась лекарственная коррекция уровня гликемии (постоянно) и терапия Кокарнитом (в течение 9 дней). Период наблюдения за пациентами составил 12 недель. У всех пациентов проводилась оценка невропатических и астенических симптомов.
Результаты. У многих пациентов были впервые диагностированы сочетанные неврологические (люмбоишиалгия, цервикалгия, туннельные синдромы, головные боли, инсомния) и эмоциональные (тревога, депрессия) расстройства. Достоверно значимые снижения средних показателей позитивных невропатических и астенических симптомов, улучшение среднего показателя болевой чувствительности наблюдалось с 10-го дня и сохранялось до 12-й недели наблюдения. Наилучшие показатели эффективности междисциплинарного лечения отмечены у пациентов с 2а-стадией ДПН.
Заключение. Наблюдается низкий уровень диагностики сочетанных неврологических и эмоциональных расстройств у пациентов с СД и ДПН. Междисциплинарное лечение позволяет относительно быстро и стойко снизить выраженность невропатических и астенических симптомов у пациентов с ДПН, наиболее эффективно – на 2а-стадии ДПН. Применение Кокарнита эффективно и безопасно в комплексной терапии пациентов с ДПН.
Ключевые слова: диабетическая полиневропатия, лечение, междисциплинарный подход, поведенческая терапия, когнитивно-поведенческая терапия, витамины группы В, Кокарнит.
Optimization diabetic polyneuropathy patients management using a multidisciplinary approach
V.A. Parfenov, MD, Prof., V.A. Golovacheva, PhD in medicine, V.V. Fadeev, MD, Prof., Corresponding Member of RAS, A.Y. Volovik, А.А. Golovacheva,
Moscow First Moscow State Medical University
Introduction. The multidisciplinary approach, including pharmacological therapy, educational therapy, cognitive-behavioral therapy (CBT) has the leading role in management of patients with diabetic polyneuropathy (DPN). There is no domestic experience in the multidisciplinary treatment of DPN patients.
Study purpose – study of efficiency of DPN patients management using a multidisciplinary approach.
Patients and methods. The study included 50 patients (29 women and 21 men) aged 20 to 78 years (mean age = 57.6 ± 10.2 years) with diabetes mellitus (DM) of type 1 and 2 and DPN. All patients received multidisciplinary treatment consisting of pharmacotherapy, educational programs, KPT. All patients by Cocarnit (for 9 days). The observation period for the patients was 12 weeks. All the patients underwent assessment of neuropathic and asthenic symptoms.
Results. Many patients were newly diagnosed with concomitant neurological (lumboischalgia, cervicalgia, tunnel syndromes, headaches, insomnia) and emotional (anxiety, depression) disorders. Authentically significant reduction in the average positive neuropathic and asthenic symptoms, improvement in average pain sensitivity was observed from Day 10 and persisted until 12 weeks of observation. Best value of effectiveness of interdisciplinary treatment was observed in patients with Stage 2 DPN.
Conclusion. There is a low level of diagnostics of combined neurological and emotional disorders in patients with diabetes and DPN. The multidisciplinary treatment allows relatively quickly and firmly to reduce the severity of neuropathic and asthenic symptoms in DPN patients, most effectively – at the Stage 2A of DPN. The use of Cocarnit is effective and safe in complex therapy of DPN patients.
Keywords: diabetic polyneuropathy, treatment, multidisciplinary approach, behavioral therapy, cognitive-behavioral therapy, Group B vitamins, Cocarnit.
Эффективные способы оптимизации ведения пациентов с сахарным диабетом (СД) и диабетической полиневропатией (ДПН) – достижение оптимального уровня гликемии, образовательная программа, образ жизни (диета, поддержание или достижение нормального веса, лечебная гимнастика, поддержание повседневной активности) и, при наличии показаний, когнитивно-поведенческая терапия (КПТ) [1]. В симптоматической терапии невропатической боли при ДПН достигнуты значимые успехи, однако данная терапия не замедляет процесс повреждения периферических нервов [2]. В настоящее время продолжается поиск патогенетической фармакотерапии ДПН, эффективно воздействующий на невропатические симптомы [1]. В России обсуждается эффективность препаратов группы В [3]. Ряд авторов указывает на целесообразность назначения пациентам с ДПН не одного из витаминов группы В, а их комплекса. Полагают, что нейротропные витамины дополняют действия друг друга в биохимических процессах, происходящих в нервной ткани [4]. Для лечения ДПН разработаны препараты, представляющие собой комплекс витаминов и метаболически активных веществ. К данной категории лекарственных средств относится Кокарнит [5–7].
Один из ключевых компонентов лечения ДПН – коррекция и адекватный контроль уровня гликемии с помощью диеты, снижения массы тела и сахароснижающей терапии
В мировой практике разработаны и эффективно применяются междисциплинарные программы лечения пациентов с СД, ДПН, сочетанными болевыми синдромами и эмоциональными расстройствами [1, 2, 8, 9]. Междисциплинарное лечение состоит из фармакотерапии (СД, невропатической боли, сочетанных расстройств), образовательной программы, КПТ, физиотерапии (лечебной гимнастики). В нашей стране не проводились исследования по применению КПТ в лечении СД и ДПН, отсутствует опыт междисциплинарного лечения данной категории пациентов.
В Клинику нервных болезней, клинику эндокринологии Первого Московского государственного медицинского университета им. И.М. Сеченова обращаются большое количество пациентов, страдающих ДПН, что и послужило основанием для проведения исследования с целью анализа типичной врачебной практики и ее оптимизации.
Цель исследования – повышение эффективности лечения пациентов с ДПН с использованием междисциплинарного подхода.
Пациенты и методы
В исследование включались пациенты, которые соответствовали всем следующим критериям: 1) мужчины и женщины в возрасте от 18 лет; 2) наличие СД1 или СД2; 3) наличие ДПН.
Исключались пациенты, у которых выявлялся хотя бы один из следующих критериев: 1) тяжелое соматическое заболевание; 2) онкологическое заболевание; 3) тяжелое психическое заболевание, требующее лечения в психиатрическом стационаре; 4) хроническое или тяжелое инфекционное заболевание; 5) патология печени; 6) нарушение ритма сердца; 7) беременность.
Диагноз СД устанавливался эндокринологом, диагноз ДПН – неврологом. У всех пациентов была определена стадия ДПН в соответствии с классификацией P. Dyck и P. Thomas [10]. Стадия 2а ДПН устанавливалась при наличии жалоб пациентов на типичные позитивные невропатические симптомы (боль, жжение, онемение, парестезии) и негативные невропатические симптомы (снижение чувствительности и рефлексов), но при отсутствии слабости в стопах. Стадия 2б ДПН ставилась при наличии указанных невропатических симптомов в сочетании со слабостью в стопах, а стадия 3 ДПН устанавливалась пациентам, имеющим социальную дезадаптацию и сниженную трудоспособность. У всех пациентов, включенных в исследование, оценивались кожные покровы стоп и голеней на наличие трофических нарушений. Для определения степени язвенных дефектов кожи стоп и голеней использовалась классификация Техасского университета [11].
В исследование было включено 50 пациентов (29 женщин и 21 мужчина) в возрасте от 20 до 78 лет (средний возраст 57,6 ± 10,2 года) с СД и ДПН. Все пациенты наблюдались эндокринологом, неврологом в течение 12 недель. СД2 страдали 45 пациентов, СД1 – 5 пациентов. Средняя продолжительность СД у пациентов составила 9,7 ± 5,23 года, средняя продолжительность клинически выраженной ДПН – 4,6 ± 3,51 года. Средний индекс массы тела пациентов равнялся 30,2 ± 4,32 кг/м² (ожирение I степени). По заключению эндокринологов, у большинства пациентов (N = 36, 72%) наблюдалась суб- и декомпенсация СД и требовалась коррекция сахароснижающей терапии. Средний уровень гликированного гемоглобина (HbA1c) до лечения составлял 7,92 ± 1,74%. В соответствии с классификацией P. Dyck и P. Thomas пациенты, включенные в исследование, распределялись следующим образом: 2a – N = 35, 70% пациентов, 2б – N = 10, 20% пациентов, 3 – N = 5, 10%. Характеристика трофических нарушений у пациентов с тремя указанными стадиями ДПН представлена в таблице 1.
Таблица 1. Наличие трофических нарушений голеней и стоп у пациентов с 2а-, 2б- и 3-й стадиями ДПН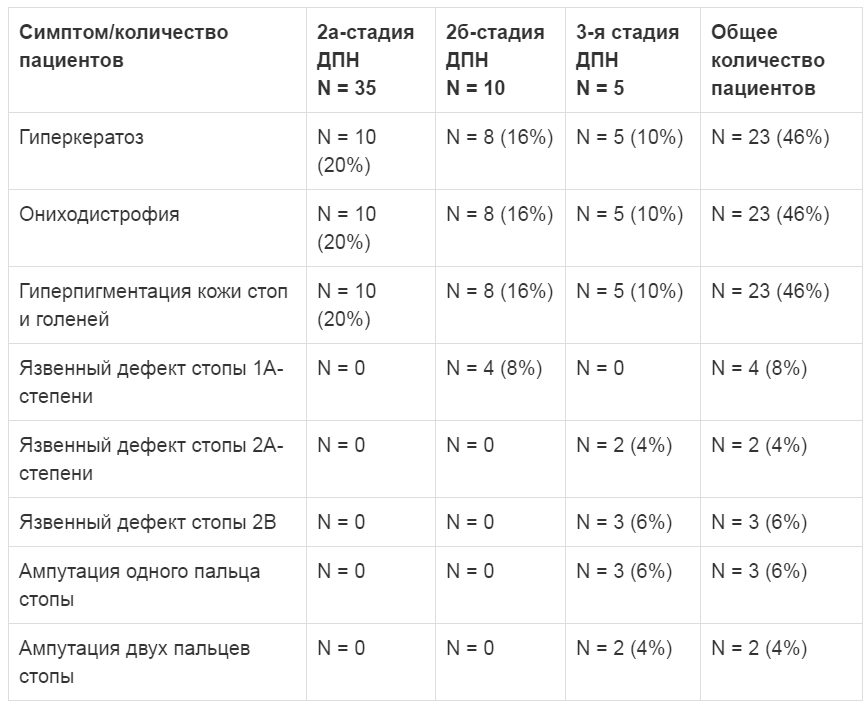
Все пациенты были клинически обследованы неврологом на предмет наличия сочетанных неврологических и эмоциональных расстройств. Оценивалось наличие болевого синдрома другой локализации. Эндокринолог, терапевт диагностировали сочетанные соматические заболевания.Для оценки выраженности позитивных невропатических симптомов у всех пациентов, включенных в исследование, использовалась шкала TSS (Total Symptom Score – Общий Счет Симптомов). Данная шкала была разработана немецким ученым D. Ziegler [12]; на сегодняшний день широко применяется в клинических исследованиях для количественной оценки динамики невропатических симптомов у пациентов с ДПН [13]. По шкале TSS оценивается выраженность основных симптомов ДПН – боль, жжение, парестезии, онемение. Для оценки выраженности негативных невропатических симптомов у всех пациентов, включенных в исследование, применялась модифицированная шкала NIS LL (Neuropathy Impairment Score Low Limbs – Шкала невропатических нарушений в ногах). По данной шкале оценивают мышечную силу, сухожильные рефлексы, чувствительность [14]. У всех пациентов оценивалась выраженность астении по шкале MFI-20 (Multidimensional Fatigue Inventory – Субъективная Шкала Оценки Астении). Данная шкала позволяет оценить несколько составляющих астенического синдрома: общую астению, физическую астению, пониженную активность, снижение мотивации и психическую астению [15]. Для определения клинического впечатления об эффективности и переносимости проведенного лечения использовалась шкала CGIC (Clinical Global Impression Scale – Шкала оценки общего клинического впечатления). Данная шкала позволяет оценить наличие и выраженность терапевтического эффекта (минимальный, умеренный, выраженный) и побочных эффектов (незначительные, значительные, превышающие терапевтический эффект) [16].
Пациентам, предъявляющим жалобы на нарушения памяти, проводилась оценка когнитивных функций по Монреальской когнитивной шкале (МКШ – Montreal cognitive assessment). Пациенты, которые предъявляли жалобы на головокружение, ощущение неустойчивости и шаткости при ходьбе, отмечали эпизоды системного головокружения в анамнезе и/или за период наблюдения, проходили нейровестибулярное исследование.
В течение 9 дней все пациенты получали стационарное междисциплинарное лечение, состоящее из оптимальной фармакотерапии, образовательной программы, КПТ. До начала лечения (на 1-м визите) всем пациентам проводилось тестирование по шкалам TSS, NIS LL, MFI-20.
Все пациенты получали сахароснижающую терапию в виде таблетированных сахароснижающих препаратов или препаратов инсулина. У всех пациентов проводилась стационарная коррекция указанной фармакотерапии. Все пациенты получали Кокарнит (2,0 мл в/м № 9). Пациентам, страдающим выраженной формой болевой ДПН, назначались антиконвульсанты (карбамазепин, габапентин или прегабалин).
Образовательная программа проводилась в форме 4 бесед продолжительностью по 30 мин. Две образовательные беседы были посвящены СД, навыкам коррекции уровня гликемии, уходу за кожей ног. Другие 2 образовательные беседы были посвящены ДПН.
КПТ проводилась в форме 2 индивидуальных сессий продолжительностью по 60 мин в соответствии с последними рекомендациями Американского руководства КПТ Бостонского университета [9].
Проводилось лечение сочетанных расстройств, выявленных неврологом, эндокринологом, терапевтом.
При наличии сочетанной соматической патологии – артериальной гипертензии, атеросклероза артерий, гиперлипидемии – пациенты получали соответствующую терапию: антигипертензивную, антиагрегантную (ацетилсалициловая кислота) и гиполипидемическую (статины).
Кокарнит содержит ряд активных веществ – производных витаминов В: трифосаденин, кокарбоксилаза, цианкобаламин и никотинамид, каждое из которых выполняет определенную функцию в процессах метаболизма
Всем пациентам, страдающим неспецифической люмбоишиалгией и цервикалгией, была показана техника выполнения упражнений по лечебной гимнастике и рекомендованы ежедневные занятия по 15-20 мин, а также назначен препарат из группы нестероидных противовоспалительных средств в течение 5 дней.
Консервативное лечение синдромов карпального и кубитального канала у пациентов с СД заключалось в снижении отеков и массы тела: коррекция антигипертензивной терапии, уровня гликемии, соблюдение диеты. Рекомендовалось ношение ортеза на области запястья и локтевого сустава (особенно в ночное время), при пользовании компьютером – эргономическая клавиатура. В дальнейшем, при неэффективности или недостаточной эффективности предложенного лечения через 12 недель, рекомендовалось нейрохирургическое лечение в виде невролиза.
Всем пациентам, страдающим инсомнией, были разъяснены правила гигиены сна, назначены мелатонинсодержащие препараты.
При наличии депрессивного и тревожного расстройства со всеми пациентами была проведена образовательная беседа по поводу текущего эмоционального состояния и нелекарственных методов лечения данных расстройств, показана техника прогрессирующей мышечной релаксации. Также данной категории пациентов назначалась фармакотерапия в виде одного из препаратов: пароксетин, тофизопам или миансерин, которые не обладают противоболевым эффектом.
При наличии лекарственно-индуцированной головной боли была проведена образовательная беседа по поводу данного состояния, рекомендована отмена обезболивающих препаратов, предложены эффективные средства для купирования мигрени или головной боли напряжения. Пациентам с хронической мигренью назначался метопролол, вазобрал. При наличии эпизодической мигрени, головной боли напряжения также была проведена образовательная беседа, рекомендованы эффективные средства для купирования головной боли.
Когнитивный тренинг был рекомендован пациентам, имеющим легкие и умеренные когнитивные нарушения.
Для оценки эффективности и переносимости лечения проводились повторные встречи с пациентами: на 10-й день наблюдения, стационарно (2-й визит), на 4-й неделе наблюдения, амбулаторно (3-й визит), на 12-й неделе наблюдения, амбулаторно (4-й визит). На всех перечисленных визитах проводилось тестирование пациентов по шкалам TSS, NIS LL, MFI-20. На заключительном (4-й визит) проводилось дополнительное тестирование по шкале CGIC.
Ранее проведенные исследования продемонстрировали снижение выраженности позитивных невропатических симптомов (боль, жжение, парестезии), улучшение показателей проведения по чувствительным и двигательным волокнам периферических нервов по результатам стимуляционной электромиографии
Полученные данные до лечения, а также через 10 дней, 4 и 12 недель от начала лечения обрабатывались методами описательной и сравнительной статистики. Описательная статистика была выполнена для всех анализируемых показателей в зависимости от типа переменной: при анализе количественных переменных вычислялись среднее арифметическое, стандартное отклонение, среднеквадратичное отклонение, минимальное и максимальное значение, а при анализе качественных переменных – частота и доля (в %) от общего числа. Ряд полученных данных был представлен в виде M ± SD, где M – среднее арифметическое, SD – среднеквадратичное отклонение, которое описывает характерный разброс величины. Статистический анализ осуществлялся с использованием дисперсионного анализа ANOVA, t-теста Стьюдента для количественных показателей с нормальным распределением и критерия суммы рангов/знаков Уилкоксона, Манна – Уитни для количественных показателей с распределением, отличным от нормального. Для всех пациентов разность значений средних показателей между визитами рассчитывали с помощью вычитания из значения показателя при предыдущем визите значения показателя при следующем визите. Статистическую обработку проводили с использованием пакета статистических программ SPSS 11,5 для Windows. Также с помощью SPSS рассчитывались точные величины соответствующей доверительной вероятности (р), достоверные различия средних арифметических.
Результаты и обсуждение
Большинство пациентов ДПН страдали сопутствующими и сочетанными заболеваниями: ожирением (N = 35, 70%), артериальной гипертензией (N = 38, 76%), ишемической болезнью сердца (N = 18, 36%), хроническим холециститом и панкреатитом. У многих пациентов впервые были диагностированы неврологические заболевания, эмоциональные расстройства: неспецифическая люмбоишиалгия (N = 31,62%) и цервикалгия (N = 29,58%), инсомния (N = 10,20%), паническое расстройство (N = 4,8%), депрессивное расстройство (N = 6,12%), синдром карпального канала (N = 8,16%), синдром кубитального канала (N = 5,10%), головная боль напряжения (N = 9,18%), мигрень без ауры (N = 4,8%), лекарственно-индуцированная головная боль (N = 2,4%), синдром легких когнитивных нарушений (N = 5,10%), синдром умеренных когнитивных нарушений (N = 2,4%). Ранее наблюдалась ошибочная интерпретация предъявляемых жалоб и симптомов, связанных вышеперечисленными расстройствами. Так, невропатические симптомы, связанные с указанными туннельными синдромами, ранее у всех пациентов расценивались как клинические проявления заболевания суставов, остеохондроза и межпозвонковых грыж шейного отдела позвоночника. Головные боли ошибочно расценивались как проявления синдрома вегетативной дистонии, хронической ишемии головного мозга, а также остеохондроза шейного отдела позвоночника. Схожая ситуация наблюдалась с интерпретацией болей в спине, которые ошибочно расценивались как клинические проявления остеохондроза и грыж межпозвонковых дисков пояснично-крестцового отдела позвоночника. У 8% (N = 4) пациентов определялся эпизод или эпизоды доброкачественного пароксизмального позиционного головокружения, которые ранее ошибочно расценивались как проявления хронической ишемии головного мозга и остеохондроза шейного отдела позвоночника (у 3 пациентов) или ишемического инсульта в вертебро-базилярном бассейне (у 1 пациента).
В ходе лечения у всех пациентов был скорректирован уровень гликемии.
10 (20%) пациентам с выраженной невропатической болью (7–8 баллов по визуально-аналоговой шкале – ВАШ) назначены антиконвульсанты (карбамазепин или прегабалин). 6 из 10 пациентов хорошо переносили терапию антиконвульсантами. У 3 пациентов наблюдалось легкое несистемное головокружение, не оказывающее значимого влияния на повседневную активность, у 1 пациента выраженность побочного эффекта антиконвульсанта (ощущения неустойчивости при ходьбе, несистемного головокружения) была выраженной, превышала терапевтический эффект, в связи с чем антиконвульсант был отменен через 7 дней от начала приема.
Все пациенты хорошо переносили терапию Кокарнитом, побочных эффектов не наблюдалось.
До лечения средняя общая оценка симптомов по шкале TSS составляла 9,24 ± 1,56 балла, что соответствует выраженному уровню позитивных невропатических симптомов. Через 10 дней от начала лечения наблюдалось достоверно значимое снижение средних значений по показателям «общая оценка симптомов», «стреляющая боль», «жжение», «парестезии», «онемение» (p < 0,001). Ко 2-й и 4-й неделям наблюдения отмечалось сохранение терапевтического эффекта и тенденция к дальнейшему уменьшению выраженности невропатических симптомов (табл. 2, рис. 1).
Таблица 2. Динамика позитивных невропатических симптомов по шкале TSS на фоне лечения (баллы, M ± SD, 95% ДИ)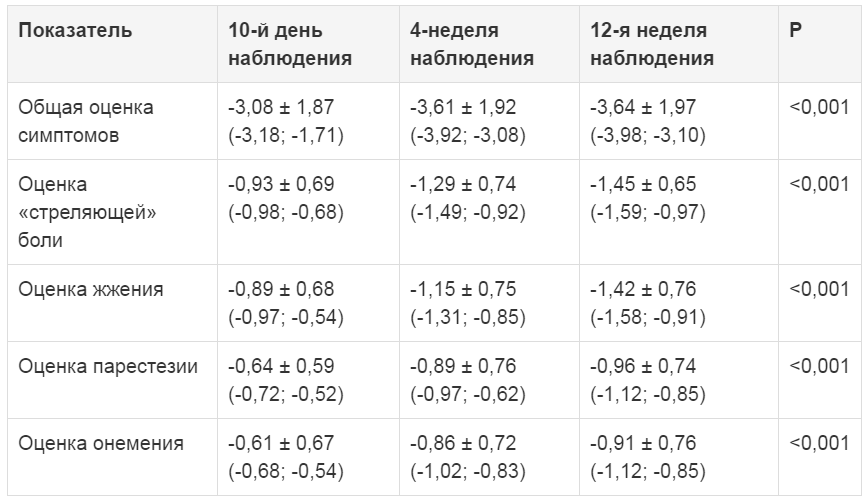
Средний показатель «болевая чувствительность» по шкале NIS LL составлял 2,68 ± 0,81 до лечения. На 10-й день от начала лечения наблюдалось достоверно значимое улучшение данного показателя (p < 0,001), при этом на 4-й и 12-й неделях наблюдения отмечалась тенденция к его дальнейшему улучшению. Также в результате лечения к 10-му дню наблюдалось улучшение других средний показателей по шкале NIS LL – «общая оценка», «мышечная сила», «рефлексы», с тенденцией к их дальнейшему улучшению к 4-й и 12-й неделям, однако данные изменения не были достоверно значимыми (табл. 3, рис. 2).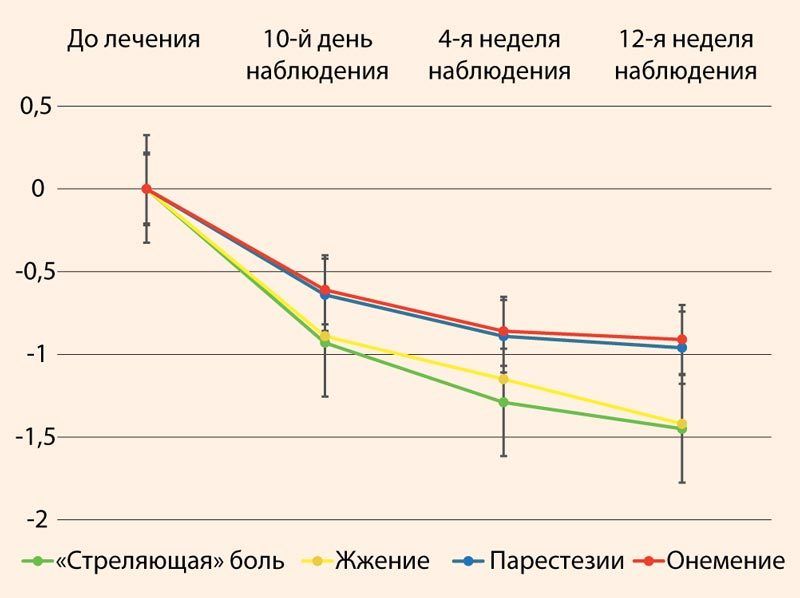
Рисунок 1. Уменьшение позитивных невропатических симптомов по шкале TSS в результате лечения (динамика разницы между исходным значением и значением в указанный период наблюдения)
Таблица 3. Динамика негативных невропатических симптомов по шкале NIS LL (баллы, M ± SD, 95% ДИ)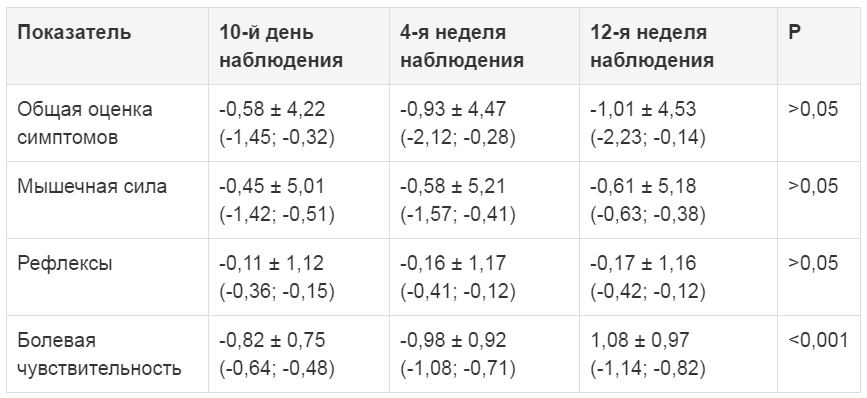
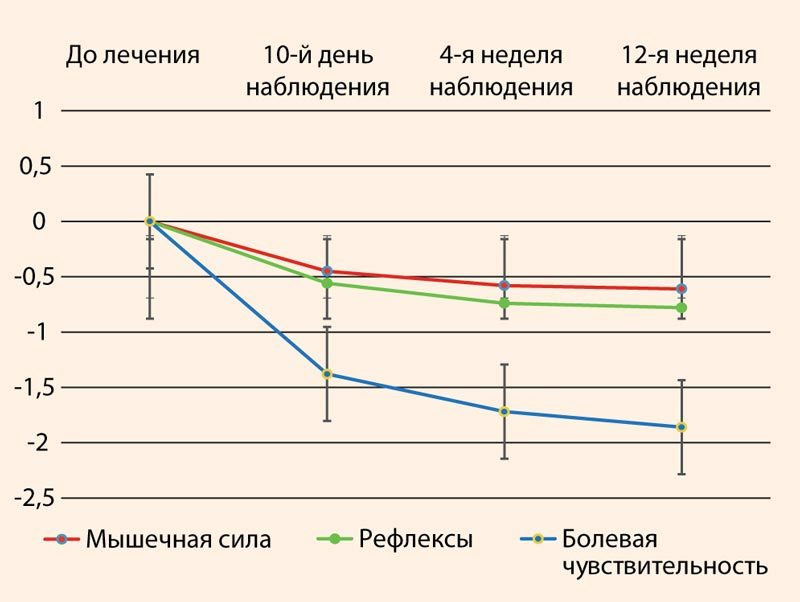
Рисунок 2. Уменьшение негативных невропатических симптомов по шкале NIS LL в результате лечения (динамика разницы между исходным значением и значением в указанный период наблюдения)
На фоне предложенного междисциплинарного лечения, наряду с уменьшением выраженности позитивных и негативных невропатических симптомов, установлено снижение выраженности астенического синдрома. Так, к 10-му дню наблюдалось достоверно значимое снижение средних значений всех показателей по шкале MFI-20: «общая астения», «пониженная активность», «снижение мотивации», «физическая астения», «психическая астения» (p < 0,001). К 4-й и 12-й неделям наблюдения отмечалась дальнейшая тенденция к улучшению перечисленных показателей (табл. 4).
Таблица 4. Динамика показателей астении по шкале MFI (баллы, M ± SD, 95% ДИ)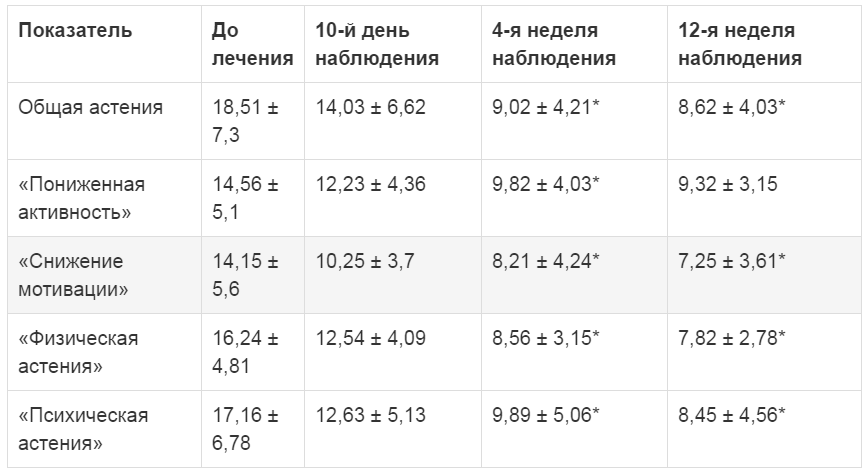
К 10-му дню наблюдения средний индекс эффективности предлагаемого лечения по шкале CGIC был достаточно высоким и составлял 2,7. При последующем наблюдении средний индекс эффективности лечения имел тенденцию к повышению (рис. 3).*p < 0,001 – при сравнении с соответствующим исходным показателем.
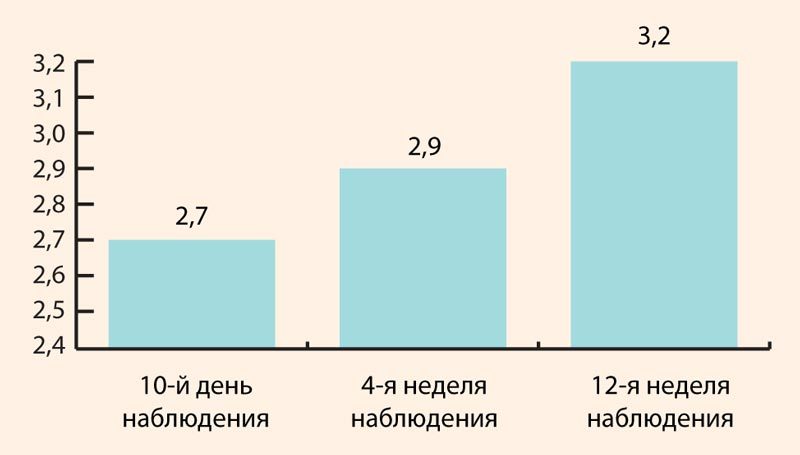
Рисунок 3. Показатели терапевтической эффективности проведенного лечения по шкале CGIC (баллы, M ± SD)
При анализе эффективности лечения пациентов с тремя различными стадиями ДПН было получено следующее. В группе пациентов с 2а-стадией ДПН наблюдалось достоверно значимое улучшение всех средних показателей по шкале TSS (p < 0,001), среднего показателя болевой чувствительности по шкале NIS LL (p < 0,001), всех средних показателей по шкале MFI-20 (p < 0,001). В группе пациентов с 2б-стадией ДПН отмечалось достоверно значимое улучшение средних показателей «стреляющая боль», «жжение» по шкале TSS (p < 0,001), достоверно значимое улучшение показателей всех сред них показателей по шкале MFI-20 (p < 0,001). У пациентов с 3-й стадией ДПН не выявлено достоверно значимых улучшений по предложенным шкалам.
У всех пациентов, включенных в исследование, наблюдалось уменьшение выраженности симптомов вышеперечисленных сочетанных и сопутствующих расстройств.
19 пациентов с ДПН (38%), страдавших люмбоишиалгией, отметили существенное (на 30–40%) снижение выраженности боли в течение первых дней применения препарата Кокарнит. Данный эффект позволил пациентам начать лечебную гимнастику, составляющую основу лечения подострых и хронических болей в спине.
Несомненно, что один из ключевых компонентов лечения ДПН – коррекция и адекватный контроль уровня гликемии с помощью диеты, снижения массы тела и сахароснижающей терапии. По результатам ранее проведенных исследований поддержание нормального уровня гликемии у пациентов с СД1 предупреждает развитие ДПН [17], но в отношении пациентов с СД2 и прогнозом развития ДПН выводы неоднозначны [2, 18, 19]. Данные одних исследований поддерживают гипотезу о том, что контроль уровня гликемии предупреждает развитие ДСПН, но большинство других свидетельствуют о несостоятельности этой гипотезы. У многих пациентов недостаточный контроль уровня гликемии связан с трудностями соблюдения рекомендаций по образу жизни, активности в течение дня и питанию [2, 18, 19]. В связи с этим организуются междисциплинарные центры ведения пациентов с СД и ДПН, разрабатываются междисциплинарные программы лечения, включающие оптимальную фармакотерапию и нелекарственные методы лечения – образовательную программу, КПТ, физиотерапию [2]. В России необходима разработка и активное внедрение в практическую деятельность подобных междисциплинарных программ.
Результаты проведенного исследования представляют первый российский опыт междисциплинарного (эндокринологи и неврологи) ведения пациентов с СД и ДПН. Рациональное сочетание фармакотерапии, образовательной программы, КПТ и физиотерапии легло в основу предлагаемого междисциплинарного лечения. Рас смотрим практическое значение каждого терапевтического метода, который применялся в данном исследовании для лечения пациентов с ДПН.
Поиск патогенетической фармакотерапии ДПН – актуальная медицинская задача [1]. На сегодняшний день одни из самых обсуждаемых кандидатов патогенетической терапии ДПН в России – альфа-липоевая кислота и витамины группы В [3, 4]. При этом современный фармакологический рынок содержит несколько вариантов препаратов, содержащих витамины группы В, и перед врачом стоит непростая задача – выбрать наиболее эффективный, безопасный и экономически выгодный препарат для пациента с ДПН. Безусловно, эффективность и хорошая переносимость препарата в лечении ДПН должна быть подтверждена данными его клинических исследований [3, 13]. Распространена практика суждений об эффективности и переносимости препаратов, являющихся дженериками, на основании результатов исследований по оригинальному препарату. Однако эффективность и переносимость дженериков и оригинальных препаратов может отличаться ввиду различий в фармакодинамике и фармакокинетике [3]. Необходимо проведение собственных постмаркетинговых исследований эффективности и переносимости препаратов, в частности препаратов группы В. Только часть препаратов с витаминами группы В имеет клинические данные, полученные в результате проведения собственных исследований.
Наибольшая эффективность терапии Кокарнитом достигается у пациентов с непродолжительным течением клинически выраженной ДПН (в среднем 2,3 года)
На сегодняшний день особый интерес представляет новый оригинальный препарат витаминов группы В Кокарнит [5]. Препарат Кокарнит отличается от других лекарственных средств с витаминами группы В тем, что содержит ряд активных веществ – производных витаминов В: трифосаденин, кокарбоксилаза, цианокобаламин и никотинамид [6]. Каждый из указанных компонентов Кокарнита выполняет определенную функцию в процессах метаболизма. Трифосаденин – производное аденозина, один из ключевых компонентов физиологического процесса энергообеспечения клеток. Кокарбо ксилаза – кофермент, образующийся в организме из поступающего извне тиамина (витамина В1). Кокарбоксилаза входит в состав фермента карбоксилазы, катализирующего карбоксилирование и декарбоксилирование альфа-кетокислот, участвует в синтезе нуклеиновых кислот, белков и липидов, в процессах усвоения глюкозы. Цианокоба ламин (витамин В12) при введении в организм превращается в метилкобаламин и 5-дезоксиаденозилкобаламин. Метил кобаламин участвует в реакции превращения гомоцистеина в метионин и S-аденозилметионин – ключевых реакциях метаболизма пиримидиновых и пуриновых оснований. 5-дезоксиаденозилкобаламин служит кофактором при изомеризации L-метилмалонил-КоА в сукцинил-КоА – важной реакции метаболизма углеводов и липидов. Дефицит витамина В12 приводит к нарушению образования миелиновой оболочки нейронов. Никотинамид – одна из форм витамина РР, участвует в окислительно-восстановительных процессах в клетке, тканевом дыхании.
Эффективность и хорошая переносимость Кокарнита при ДПН отмечены в ряде клинических исследований. Авторы ранее проведенных исследований продемонстрировали снижение выраженности позитивных невропатических симптомов (боль, жжение, парестезии) [5–7, 22–24, 26], улучшение показателей проведения по чувствительным и двигательным волокнам периферических нервов по результатам стимуляционной электромиографии [7, 22]. Также было показано улучшение функции проведения симпатических волокон периферических нервов (по данным исследования вызванных кожных симпатических потенциалов) [22], повышение вариабельности сердечного ритма (по результатам кардиоваскулярных тестов), свидетельствующее об улучшении функции проведения кардинальных автономных волокон [25]. Влияние препарата Кокарнит на функцию проведения соматических и вегетативных волокон продолжает активно изучаться [27]. Отмечено, что наибольшая эффективность терапии Кокарнитом достигается у пациентов с непродолжительным течением клинически выраженной ДПН (в среднем 2,3 года) [23]. Установлено, добавление Кокарнита к стандартной терапии СД и ДПН повышает эффективность проводимого лечения [5]. Авторы предшествующих работ наблюдали улучшение эмоционального состояния, повышение повседневной активности, улучшение качества жизни при уменьшении выраженности невропатических симптомов у пациентов с ДПН на фоне лечения Кокарнитом [22, 24, 26]. В связи с вышеперечисленными данными, наряду с тщательным подбором сахароснижающей терапии, всем пациентам, включенным в наше исследование, был назначен препарат Кокарнит. У всех пациентов отмечены хорошая переносимость Кокарнита и отсутствие существенных побочных эффектов. Только у 4 пациентов, включенных в исследование, наблюдались побочные эффекты, связанные с приемом антиконвульсантов.
Только 10 (20%) пациентов с ДПН, включенных в настоящее исследование, имели выраженную (7–8 баллов по ВАШ) невропатическую боль, поэтому стали получать терапию антиконвульсантами. Остальные 40 (80%) пациентов с ДПН не получали какой-либо специфической противоболевой фармакотерапии, и препарат Кокарнит был единственным лекарственным препаратом, направленным на уменьшение невропатических симптомов ДПН.
Проведение сессий КПТ в настоящем исследовании позволило изменить неправильные представления пациентов о «вреде инсулинотерапии», «невозможности предупредить осложнения СД», «неизбежности инвалидности», «ограниченности в личной и социальной жизни» и обучить пациентов адаптивному поведению, направленному на повышение приверженности к соблюдению медицинских рекомендаций
Авторы ранее проведенных исследований указывают на важность своевременной диагностики сочетанных эмоциональных расстройств и болевых синдромов другой локализации, что повышает эффективность лечения болевой ДПН [2]. Результаты проведенного нами исследования показывают недостаточный уровень диагностики сочетанных неврологических и эмоциональных расстройств у пациентов с СД и ДПН. Ошибочная интерпретация сочетанных расстройств, отсутствие своевременного лечения болевых расстройств другой локализации и эмоциональных расстройств способствуют повышению выраженности невропатических симптомов ДПН. У многих пациентов мы впервые диагностировали головные боли, туннельные синдромы, люмбоишиалгию, цервикалгию, тревожные и депрессивные расстройства. Назначение оптимального лечения сочетанных заболеваний уменьшило их проявления, что повысило эффективность терапии ДПН.
Образовательные беседы с пациентами включали рассмотрение широкого круга проблем – СД, ДПН, сочетанных расстройств, что имеет большое практическое значение и также повышает эффективность лечения ДПН.
В соответствии с последними рекомендациями национального руководства США по лечению СД, КПТ – эффективный поведенческий метод лечения пациентов с СД, который помогает им принять болезнь без формирования психологических и психических проблем и следовать рекомендациям врача в отношении образа жизни (уровень рекомендаций А) [20]. С помощью метода КПТ врач мотивирует пациентов на лечение и поддержание повседневной активности, что улучшает течение СД. Проведение сессий КПТ в настоящем исследовании позволило изменить неправильные представления пациентов о «вреде инсулинотерапии», «невозможности предупредить осложнения СД», «неизбежности инвалидности», «ограниченности в личной и социальной жизни» и обучить пациентов адаптивному поведению, направленному на повешение приверженности к соблюдению медицинских рекомендаций.
Известно, что КПТ эффективна в лечении ряда болевых расстройств [9]. Интересен тот факт, что в последние годы обсуждается эффективность КПТ в лечении невропатической боли при ДПН. По результатам американского пилотного рандомизированного контролируемого исследования, проводимого под руководством известного когнитивно-поведенческого терапевта J.D. Otis, добавление КПТ к стандартной терапии ДПН повышает эффективность проводимого лечения: у пациентов, получающих комбинированное лечение, в достоверно большей степени уменьшается интенсивность боли и ее влияние на повседневную активность. [8]. Всем пациентам, включенным в наше исследование, проводились сессии КПТ, направленные на изменение ошибочных представлений пациентов о ДПН и обучение навыкам преодоления боли, негативных эмоций. Нам не известно о публикации подобного практического опыта применения КПТ у пациентов с ДПН в нашей стране. В соответствии с данными шкалы TSS предлагаемое междисциплинарное лечение привело к быстрому (на 10-й день лечения) и устойчивому (к 12-й неделе наблюдения), достоверно значимому уменьшению средних показателей выраженности позитивных невропатических симптомов. Тенденция к улучшению мышечной силы и сухожильных рефлексов, достоверно значимое улучшение болевой чувствительности по шкале NIS LL свидетельствует об улучшении функции проведения по двигательным и чувствительным волокнам в течение всего периода наблюдения за пациентами. Благодаря комбинации фармакотерапии с образовательной программой и КПТ, у пациентов повышалась мотивация к изменению образа жизни и приверженность к медицинским рекомендациям, что способствовало достоверно значимому снижению всех показателей астении по шкале MFI-20.
Предлагаемое междисциплинарное лечение наиболее эффективно при ранней стадии ДПН – 2а, что согласуется с данными предшествующих работ [1, 21]. Вовлечение двигательных волокон в патологический процесс свидетельствует о более тяжелом повреждении периферических нервов и ухудшает терапевтический прогноз [21]. Практически значимо, что применение междисциплинарного лечения, включающего терапию Кокарнитом, позволило достоверно уменьшить интенсивность невропатический боли и выраженность симптомов астении у пациентов с 2б-стадией ДПН, в большинстве случаев – без применения антиконвульсантов и антидепрессантов. Данное наблюдение позволяет обсуждать междисциплинарное лечение, включающее Кокарнит, как альтернативную терапию невропатических симптомов при 2а- и 2б-стадии ДПН. У части пациентов терапия антиконвульсантами приводила к развитию побочных эффектов в виде ощущения несистемного головокружения и неустойчивости при ходьбе. Терапия Кокарнитом ни в одном случае не сопровождалась побочными эффектами. Указанное положение имеет большое практическое значение в ведении пожилых пациентов с СД и ДПН, среди которых исходно распространены жалобы на ощущения головокружения и неустойчивости при ходьбе.
Применение междисциплинарного лечения, включающее терапию Кокарнитом, позволило достоверно уменьшить интенсивность невропатический боли и выраженность симптомов астении у пациентов с 2б стадией ДПН, в большинстве случаев – без применения антиконвульсантов и антидепрессантов
Таким образом, отмечен неудовлетворительный уровень диагностики сочетанных неврологических и эмоциональных расстройств у пациентов с СД и ДПН. Диагностика и рациональное лечение указанных расстройств позволяют улучшить состояние пациентов и повышают эффективность лечения ДПН. Междисциплинарное лечение пациентов с СД и ДПН позволяет относительно быстро и устойчиво уменьшить выраженность невропатических и астенических симптомов. Для ведения пациентов с СД и ДПН в отечественной практической деятельности продемонстрирована эффективность междисциплинарного лечения, включающего: 1) фармакологическую коррекцию уровня гликемии, 2) патогенетическую фармакотерапию ДПН (Кокарнит), 3) специфическую противоболевую терапию (антиконвульсанты, у пациентов с выраженной болевой ДПН), 4) образовательную программу, 5) КПТ. Продемонстрирована хорошая переносимость и терапевтическая эффективность препарата Кокарнит. Предложенная междисциплинарная программа эффективна в лечении пациентов с 2а- и 2б-стадией ДПН, при этом наибольший терапевтический эффект наблюдается при 2а-стадии ДПН.
Литература
- Ziegler D. Современные принципы ведения больных с диабетической полинейропатией. Нервно-мышечные болезни, 2012, 2: 7-19.
- Tesfaye S, Vileikyte L, Rayman G et al. Painful diabetic peripheral neuropathy: consensus recommendations on diagnosis, assessment and management. Diabetes Metab Res Rev, 2011, 27: 629-638.
- Строков И.А. Место нейротропных комплексов в терапии неврологических осложнений сахарного диабета. РМЖ, 2013, 30: 1535-1539.
- Строков И.А., Ахмеджанова Л.Т., Солоха О.А. Применение высоких доз витаминов группы В в неврологии. Трудный пациент, 2009, 10: 17-22.
- Мкртумян А.М., Подачина С.В., Доскина Е.В. и др. Эффективное лечение диабетической нейропатии комплексным препаратом Кокарнит. Эффективная фармакотерапия. Эндокринология, 2015, 5(43) Available at: (Accessed 27 December 2015). (in Russian)
- Литвиненко Л.А., Короленко Г.Г. Использование Кокарнита в комплексном лечении диабетической полинейропатии. Медицинские новости, 2009, 3: 67-68.
- Романов И.П., Казаков А.В., Олейникова С.П. и др. Современный подход к лечению диабетической полиневропатии. Проблемы эндокринной патологии, 2012, 3: 56-59.
- Otis JD, Sanderson K, Hardway C et al. A randomized controlled pilot study of a cognitivebehavioral therapy approach for painful diabetic peripheral neuropathy. J Pain, 2013, 14(5): 475-482.
- Otis JD. Managing chronic pain: a cognitivebehavioral therapy: therapist guide, 1st ed. New York, Oxford University Press, 2007. 114 p.
- Dyck PJ, Thomas PK. Diabetic neuropathy, 2nd ed., Philadelphia: W.B. Saunders, 1999, 720.
- Оболенский В.Н., Семенова Т.В., Леваль П.Ш., Плотников А.А. Синдром диабетической стопы в клинической практике. РМЖ, 2010, 18(2): 45-54.
- Ziegler D, Hanefeld M, Ruhnau KJ et al. Treatment of symptomatic diabetic peripheral neuropathy with the antioxidant alfa-lipoic acid. A 3-week multicentre randomized controlled trial (ALADIN Study). Diabetologia, 1995, 38: 1425-1433.
- Stracke H, Gaus W, Achenbach U et al. Benfotiamine in diabetic polyneuropathy (BENDIP): results of a randomized, double blind, placebo-controlled clinical trial. Exp Clin Endocrinil Diabetes, 2008, 116: 1-6.
- Строков И.А., Фокина А.С., Головачева В.А. Эффективность тиолепты при диабетической полинейропатии (по данным исследования ЭТИКА). Журнал неврологии и психиатрии, 2013, 113(5): 36-41.
- Smets EM, Garssen B, Bonke B, De Haes JC. The Multidimensional Fatigue Inventory (MFI) psychometric qualities of an instrument to assess fatigue. J Psychosom Res, 1995, 39(3): 315-325.
- Busner J, Targum SD. The Clinical Global Impressions Scale. Psychiatry (Edgmont), 2007, 4(7): 28-37.
- Martin CL, Albers J, Herman WH et al.; DCCT/ EDIC Research Group. Neuropathy among the diabetes control and complications trial cohort 8 years after trial completion. Diabetes Care, 2006, 29: 340-344.
- Tesfaye S, Boulton AJM, Dyck PJ et al. Diabetic Neuropathies: update on definitions, diagnostic criteria, estimation of severity, and treatments on behalf of the Toronto Diabetic Neuropathy Expert Group. Diabetes Care, 2010, 33: 2285-2293.
- Kasznicki J. Advances in the diagnosis and management of diabetic distal symmetric polyneuropathy. Arch Med Sci, 2014, 10(2): 345-354.
- Management of diabetes. A national clinical guideline. U.S. Department of Health & Human Services. Available at: http://guideline.gov.
- Строков И.А., Фокина А.С., Строков К.И. и др. Современные принципы диагностики и лечения диабетической полинейропатии. Медицинский совет, 2014, 5: 38-42.
- Девликамова Ф.И. Применение препарата кокарнит при лечении пациентов с диабетической полинейропатией. Журнал неврологии и психиатрии им. С.С. Корсакова, 2016, 116(11): 64-68.
- Ховасова Н.О., Наумов А.В., Магомедова А.Ю. и др. Диабетическая нейропатия: что должен знать терапевт поликлиники. Амбулаторный прием, 2016, 2(2): 67-71.
- Каракулова Ю.В., Филимонова Т.А. Новые возможности патогенетического лечения диабетической полинейропатии. Manage pain, 2016, 4: 46-49.
- Крутиков Е.С., Цветков В.А., Чистякова С.И. Автономная нейропатия сердца у больных сахарным диабетом типа 2. Consilium medicum, 2016, 18(9): 98-102.
- Мкртумян А.М., Маркова Т.Н., Подачина С.В. Возможность применения препарата Кокарнит при лечении диабетической полинейропатии. Эффективная фармакотерапия. Эндокринология, 2016, 4: 6-10.
- Радоуцкая Е.Ю., Кругликова Н.В. Кокарнит в лечении профессиональных полиневропатий. Нервные болезни, 2016, 2: 32-36.
