Клиническая эффективность и безопасность схем лечения синдрома раздраженного кишечника
Статьи(результаты сравнительного исследования)
Опубликовано в Consilium Medicum. 2016; 18 (8): 19–26.
И.В.Маев, А.А.Самсонов, А.В.Яшина, Д.Н.Андреев, В.А.Шестаков, С.А.Караулов
ГБОУ ВПО Московский государственный медико-стоматологический университет им. А.И.Евдокимова Минздрава России. 127473, Россия, Москва, ул. Делегатская, д. 20, стр. 1
Приведены результаты сравнительного неинтервенционного наблюдательного исследования по оценке эффективности и безопасности применения препарата Колофорт в лечении синдрома раздраженного кишечника в сравнении с препаратом тримебутина.
Ключевые слова: синдром раздраженного кишечника, Колофорт, тримебутин.
aleksey.samsonov@gmail.com
Для цитирования: И.В.Маев, Самсонов А.А., Яшина А.В. и др. Клиническая эффективность и безопасность схем лечения синдрома раздраженного кишечника (результаты сравнительного исследования). Consilium Medicum. 2016; 18 (8): 19–26.
Clinical efficacy and safety of treatment regimens for irritable bowel syndrome (a comparative study)
I.V.Maev, A.A.Samsonov, A.V.Yashina, D.N.Andreev, V.A.Shestakov, S.A.Karaulov
A.I.Evdokimov Moscow State University of Medicine and Dentistry of the Ministry of Health of the Russian Federation. 127473, Russian Federation, Moscow, ul. Delegatskaia, d. 20, str. 1
The results of the comparative non-interventional observational study held to evaluate the efficacy and safety of Kolofort in the treatment of irritable bowel syndrome in comparison with trimebutine are given below.Key words: irritable bowel syndrome, Kolofort, trimebutine.
For citation: I.V.Maev, Samsonov A.A., Yashina A.V. et al. Clinical efficacy and safety of treatment regimens for irritable bowel syndrome (a comparative study). Consilium Medicum. 2016; 18 (8): 19–26.
aleksey.samsonov@gmail.com
Синдром раздраженного кишечника (СРК) – наиболее распространенная и изученная патология среди функциональных расстройств желудочно-кишечного тракта (ЖКТ), затрагивающая до 25% популяции [1]. Доля пациентов с СРК, обращающихся за амбулаторной медицинской помощью, составляет 12% и на сегодняшний день является самой большой подгруппой больных в гастроэнтерологических клиниках [2]. Одна из причин пристального внимания к проблеме СРК – несоответствие тяжести состояния пациента и благоприятного прогноза течения заболевания предъявляемым жалобам и субъективной тяжести симптоматики, существенно снижающим качество жизни пациентов и их трудоспособность [3].
Согласно недавно опубликованным Римским критериям IV пересмотра, СРК определяется как функциональное расстройство, при котором периодические боли в животе наблюдаются в среднем по крайней мере 1 день в неделю за последние 3 мес и связаны с 2 или более критериями:
1) дефекацией;
2) изменением частоты стула;
3) изменением формы стула на протяжении последних
3 мес при общей продолжительности жалоб не менее 6 мес.
Римские критерии IV не противоречат Римским критериям III, но исключают термин «дискомфорт» и еще более уточняют временные рамки наличия симптомов [4].
Клинические проявления СРК характеризуются наличием болевого синдрома, что отличает СРК от других функциональных расстройств, и нарушением стула разного характера – запор, диарея и их сочетание.
В зависимости от типа стула выделяют 4 вида (типа) СРК – с преобладанием запоров (СРК-З), с преобладанием диареи (СРК-Д), смешанный (СРК-С) и неспецифический (СРК-Н). Однако в практике часто наблюдается гетерогенность симптомов и «перемещение» одного и того же пациента из одного вида СРК в другой [4].
 СРК – всегда диагноз исключения, что означает не только четкое соблюдение Римских критериев IV, но и необходимость тщательного обследования пациента для исключения органической патологии кишечника. В помощь этому существуют так называемые «симптомы тревоги»: дебют симптомов в пожилом возрасте, снижение уровня гемоглобина и железа в крови, лейкоцитоз, повышение СОЭ, гематохезия, ночная симптоматика, потеря массы тела, семейный анамнез органического заболевания кишечника. СРК – полиэтиологичное заболевание. Несмотря на широкую распространенность СРК, его этиопатогенез до конца не расшифрован [5, 6]. В связи с этим отсутствует и единая схема терапии заболевания, обеспечивающая эффективный контроль над ним.
СРК – всегда диагноз исключения, что означает не только четкое соблюдение Римских критериев IV, но и необходимость тщательного обследования пациента для исключения органической патологии кишечника. В помощь этому существуют так называемые «симптомы тревоги»: дебют симптомов в пожилом возрасте, снижение уровня гемоглобина и железа в крови, лейкоцитоз, повышение СОЭ, гематохезия, ночная симптоматика, потеря массы тела, семейный анамнез органического заболевания кишечника. СРК – полиэтиологичное заболевание. Несмотря на широкую распространенность СРК, его этиопатогенез до конца не расшифрован [5, 6]. В связи с этим отсутствует и единая схема терапии заболевания, обеспечивающая эффективный контроль над ним.К факторам, вызывающим или провоцирующим развитие симптомов, относят феномен висцеральной гиперчувствительности, перенесенную острую кишечную инфекцию или не связанное с ней нарушение микрофлоры кишечника, наследственную предрасположенность, средовые факторы и стрессовые воздействия [5, 6]. Также к факторам риска СРК относят молодой возраст и женский пол [3]. Данные компоненты этиопатогенеза СРК отдельно или в совокупности ведут к нарушению по оси «мозг–кишечник» – регуляции между центральной нервной системой (ЦНС) и энтеральной нервной системой (ЭНС) [7]. Ключевая задача последней – регуляция основных функций кишечника, в частности ритмической моторной активности тонкой и толстой кишки. В настоящее время большое значение в патогенезе уделяется процессам воспаления в кишечнике, дисбалансу иммунных процессов в кишечнике [8, 9]. В частности, установлена роль мастоцитов, энтероэндокринных клеток в кишечнике и дисбаланса ряда цитокинов, включая фактор некроза опухоли a (ФНО-a), гистамин, серотонин, интерлейкины (ИЛ-1b, 6, 10), что проявляется персистирующим субклиническим воспалением [10].
 Медиаторы воспаления, вырабатываемые тучными клетками (гистамин, протеазы и серотонин) и Т-клетками (цитокины), влияют на ЭНС и ЦНС, активность гладкомышечных клеток кишечника, что, в свою очередь, приводит к усугублению изменений кишечного транзита и боли в животе. Также известно, что серотониновые 5-НТ-рецепторы в кишечнике играют важную роль в регуляции моторики и болевой чувствительности. И показанное при СРК увеличение количества серотонинсодержащих энтерохромаффинных клеток – еще один важный фактор формирования клинических симптомов [6].
Медиаторы воспаления, вырабатываемые тучными клетками (гистамин, протеазы и серотонин) и Т-клетками (цитокины), влияют на ЭНС и ЦНС, активность гладкомышечных клеток кишечника, что, в свою очередь, приводит к усугублению изменений кишечного транзита и боли в животе. Также известно, что серотониновые 5-НТ-рецепторы в кишечнике играют важную роль в регуляции моторики и болевой чувствительности. И показанное при СРК увеличение количества серотонинсодержащих энтерохромаффинных клеток – еще один важный фактор формирования клинических симптомов [6].Терапия пациентов с СРК является трудной задачей, несмотря на обилие лекарственных препаратов. В настоящее время используются спазмолитики, слабительные средства, препараты для купирования диареи, ветрогонные, комбинированные препараты, про- и пребиотики, антибиотики, антидепрессанты и нейролептики [11, 12]. Эффективность препаратов указанных групп показана во множестве клинических исследований с разным уровнем доказательности. Тем не менее до настоящего времени не существует универсальной схемы терапии СРК, которая одинаково хорошо подходила бы ко всем его типам. Гетерогенность клинических проявлений, «перемещение» пациентов из одного типа в другой обусловливают необходимость приема нескольких препаратов, что существенно снижает приверженность пациентов лечению, эффективность терапии и, следовательно, качество жизни [13, 14]. В связи с этим представляются важным поиск и применение препаратов для лечения СРК, не только обладающих симптоматическим действием, но и влияющих на его патогенетические механизмы, что позволило бы обеспечить высокую терапевтическую эффективность вне зависимости от типа СРК.
Недавно в арсенале врача появился новый отечественный комбинированный лекарственный препарат для лечения СРК – Колофорт, созданный на основе антител к мозгоспецифическому белку S-100, ФНО-a и гистамину, прошедших технологическую обработку в процессе производства. В результате в состав Колофорта входят релиз-активные антитела, которые оказывают воздействие на молекулы-мишени – не блокируют, а модифицируют активность белка S-100, рецепторов к гистамину и ФНО-a. Сочетание трех активных компонентов позволяет осуществлять комплексное воздействие на центральные и периферические звенья патогенеза функциональных нарушений кишечника и, в частности, СРК [15].
Полученные в ходе экспериментальных и клинических исследований данные о влиянии Колофорта на функциональное состояние ЖКТ показали, что благодаря нормализующему действию на его моторику, противовоспалительному и успокаивающему эффектам препарат обладает достоверной терапевтической эффективностью при СРК. Колофорт уменьшает боль и висцеральную гиперчувствительность, нормализует паттерн стула, улучшает качество жизни пациентов, положительно влияет на эмоциональные нарушения [16, 17].
Наиболее часто при СРК для купирования болевого синдрома используются спазмолитики. Их применение терапевтически оправдано как в отношении боли в животе, поскольку одна из ее причин – аномальное сокращение гладких мышц в ЖКТ, так и спазма как причины нарушенного кишечного транзита. Широко применяемый спазмолитик при СРК – синтетический холиноблокатор тримебутин (торговое название Тримедат), относящийся к эфирам с третичной аминогруппой и фармакодинамически оказывающий агонистическое действие на энкефалиновую систему кишечника – периферические опиатные рецепторы. Согласно данным официальной инструкции по применению, тримебутин регулирует моторику ЖКТ без влияния на ЦНС, восстанавливая нормальную физиологическую активность мускулатуры кишечника [18]. Нормализуя висцеральную чувствительность, он обеспечивает анальгетический эффект при абдоминальном болевом синдроме. Клинические исследования и лечебная практика демонстрируют успешное применение тримебутина в лечении пациентов с СРК [19].С учетом изложенного представляется интересным клиническое изучение сравнительной эффективности и безопасности терапии СРК препаратами Колофорт и Тримедат в рутинной практике.
Целью исследования явилась оценка эффективности и безопасности применения препарата Колофорт в терапии СРК в сравнении с Тримедатом.
Неинтервенционное сравнительное клиническое исследование в параллельных группах проводилось с октября 2014 г. по июнь 2016 г. на базе клиники кафедры пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО «МГМСУ им. А.И.Евдокимова».
В исследование включались амбулаторные пациенты обоего пола в возрасте от 18 до 60 лет с установленным диагнозом СРК всех подтипов, который соответствовал Римским критериям III (2006 г.), согласно которым СРК – функциональное расстройство, при котором боль или дискомфорт в животе уменьшается после дефекации, связаны с изменением частоты и консистенции стула, возникают не менее 3 дней в месяц на протяжении последних 3 мес при общей продолжительности жалоб не менее 6 мес [20].
Поскольку исследование носило неинтервенционный характер, до включения в исследование лечащим врачом была назначена терапия препаратом Колофорт или Тримедат. В зависимости от этого пациенты были распределены в одну из двух групп – 1-я группа (основная, группа Колофорта) и 2-я группа (сравнения, группа Тримедата). Колофорт был назначен врачом по схеме: первые 2 нед приема 2 таблетки 3 раза в сутки, начиная с 15-го дня – по 2 таблетки 2 раза в сутки. Тримедат был назначен по 1 таблетке (200 мг) 3 раза в день. Длительность лечения – 12 нед.
Помимо объективного обследования в данном исследовании для оценки клинической динамики симптомов СРК использовались визуальная аналоговая шкала (ВАШ) при СРК, Бристольская шкала формы стула, расчет суммарного индекса висцеральной чувствительности по шкале VSI (Visceral Sensitivity Index) и опросник для оценки качества жизни при СРК (IBS-QoL).
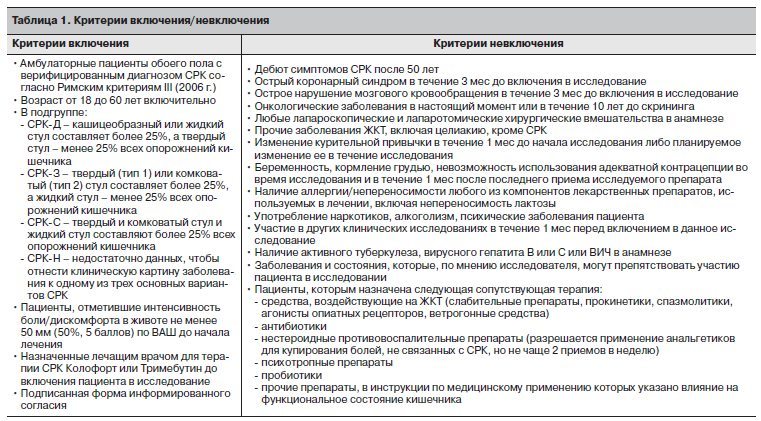
После подписания пациентом информированного согласия на визите 1 подтверждалась возможность его участия в исследовании в соответствии с критериями включения/невключения (табл. 1). В течение последующего периода лечения (12 нед) пациенты совершали еще 4 визита в медицинский центр, в ходе которых проводились объективное обследование, тестирование по указанным опросникам и шкалам, регистрировались сопутствующая терапия (если такая применялась), а также возможные нежелательные явления.
Для оценки эффективности лечения использовались следующие критерии:
• Первичные:
1. Доли пациентов, у которых отмечается снижение выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5.
2. Доли пациентов, у которых отмечается снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5.
• Вторичные:
1. Доля пациентов в подгруппе СРК-Д с изменением типа стула по Бристольской шкале формы стула до 5 и менее (в среднем за 1 нед).
2. Динамика изменения типа стула по Бристольской шкале.
3. Доля пациентов в подгруппе СРК-З, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем.
4. Динамика количества актов дефекации у пациентов с СРК-З.
5. Динамика результатов оценки по ВАШ.
6. Динамика значений суммарного балла индекса висцеральной чувствительности по опроснику VSI.
7. Динамика значений суммарного балла опросника качества жизни IBS-QоL.
В процессе исследования выполнялись 5 визитов пациента к врачу: визит 1 (день 0), визит 2 (день 14±3), визит 3 (день 28±3), визит 4 (день 56±3), визит 5 (день 84±3). На каждом визите проводились объективное обследование пациента, включающее измерение массы тела, артериального давления, частоты сердечных сокращений, температуры тела, и оценка безопасности, заполнение опросников ВАШ, VSI, IBS-QoL и определение типа стула по Бристольской шкале. Кроме этого, на визите 1 пациенты подписывали форму информированного согласия, а также проводилась проверка соответствия критериям включения/невключения. Определение критериев безопасности было связано с наличием, характером и продолжительностью нежелательных явлений, их связью с приемом препарата, выраженностью и другими характеристиками, в связи с чем проводилось заполнение соответствующей формы для оповещения отдела клинической безопасности компании-производителя. Для обработки полученных данных использовались стандартные методы описательной статистики, включая дисперсионный анализ, метод Generalized estimating equations (GEE), расчет t-критерия Стъюдента, точного критерия Фишера, критерий χ2, критерий Кохрана–Мантеля–Хенсзеля (модификация критерия χ2 для множественных сравнений), критерий Фаррингтона–Мэннинга.
Результаты исследования
 В исследование были включены 149 пациентов обоего пола (53 мужчины – 35,6% и 96 женщин – 64,4%) в возрасте от 18 до 60 лет (средний возраст составил 33,3±0,8 года) с СРК, диагноз которого соответствовал Римским критериям III (2006 г.).
В исследование были включены 149 пациентов обоего пола (53 мужчины – 35,6% и 96 женщин – 64,4%) в возрасте от 18 до 60 лет (средний возраст составил 33,3±0,8 года) с СРК, диагноз которого соответствовал Римским критериям III (2006 г.).Все рекрутированные пациенты полностью соответствовали критериям включения/невключения в исследование и завершили участие в нем через 12 нед наблюдения. В окончательный анализ эффективности и безопасности включены данные всех 149 пациентов, принимавших участие в исследовании.
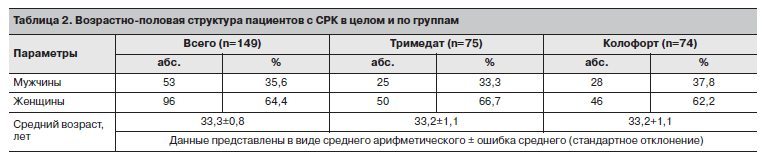
В соответствии с назначенной лечащим врачом терапией пациенты были распределены в 2 группы: 74 пациента составили группу Колофорта, 75 – группу Тримедата. Возрастно-половая структура пациентов с СРК в целом и по группам представлена в табл. 2.
Соотношение мужчин и женщин среди пациентов, включенных в исследование, составило примерно 1:2, что согласуется с данными мировой литературы о примерно двукратном преобладании женщин среди лиц, страдающих СРК [3]. Средний возраст по группам был одинаков и составил 33,2±1,1 года.
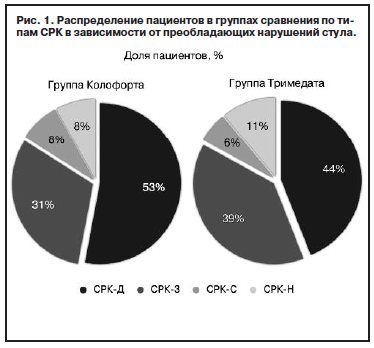
Согласно классификации СРК по типам в зависимости от преобладающих нарушений стула, пациенты распределились следующим образом: в группе, принимавшей Колофорт, пациенты с СРК-Д составили 39 (53%) человек, СРК-З – 23 (31%), СРК-С и СРК-Н – по 6 (8%) в каждой подгруппе. Аналогичное распределение по субтипам СРК наблюдалось и в группе Тримедата: пациенты с СРК-Д составили 33 (44%) человека, СРК-З – 29 (39%), СРК-С – 5 (6%), СРК-Н – 8 (11%); рис. 1. В целом в сравниваемых группах отмечено доминирование пациентов с СРК-Д и СРК-З. Полученные результаты несколько противоречат эпидемиологическим данным о частоте встречаемости типов СРК с примерно равным распределением по подгруппам СРК-З, СРК-Д, СРК-С, что в данном исследовании, вероятно, связано с переходом одной формы СРК в другую у одного и того же пациента.
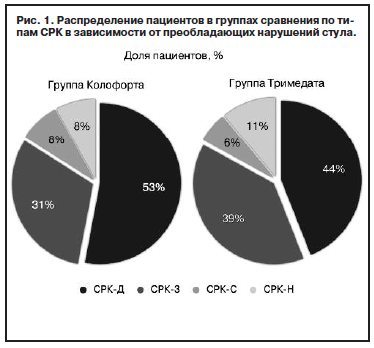
Таким образом, по возрастному, половому составу и исходным клиническим характеристикам исследуемые группы были сопоставимы.
Влияние сравниваемой терапии на болевой синдром
В соответствии с выбранными первичными критериями эффективности оценивалась доля пациентов со снижением выраженности боли/дискомфорта по ВАШ на 30% и более от исходного значения на визитах 3 и 5. Выбор данного значения был сделан в соответствии с существующими подходами к проведению клинических исследований при СРК – снижение боли в животе на 30% по сравнению с исходным уровнем считается клинически значимым [20].
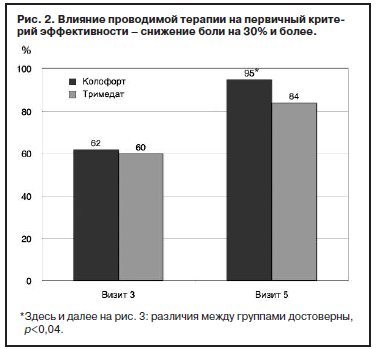
Через 4 нед терапии, к визиту 3, доля пациентов со снижением боли по ВАШ на 30% и более была сопоставима в обеих группах: 62% пациентов в группе Колофорта и 60% – в группе Тримедата [критерий χ2: χ2=0,07; p=0,7867; критерий Фаррингтона–Мэннинга (nonferiority test): z=1,53; p=0,0633]; рис. 2.
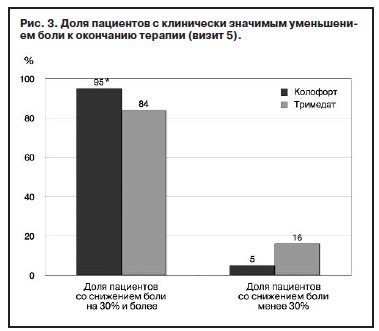
Однако к визиту 5, окончанию курса наблюдения и терапии сравниваемыми препаратами, продемонстрировано статистически значимое превосходство терапии Колофортом по сравнению с Тримедатом: уменьшение выраженности боли на 30% и более отмечено у 95% пациентов основной группы против 84% пациентов в группе сравнения [критерий χ2: χ2=4,4; p=0,0368; критерий Фаррингтона–Мэннинга (nonferiority test): z=3,7; p=0,0001]; рис. 2, 3.
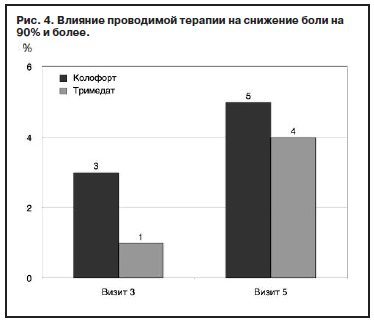
При оценке доли пациентов, у которых отмечено снижение выраженности боли/дискомфорта по ВАШ на 90% и более от исходного значения на визитах 3 и 5, получены сопоставимые данные в сравниваемых группах с тенденцией к лучшим показателям в группе Колофорта, что может говорить о необходимости более длительной терапии СРК (рис. 4).
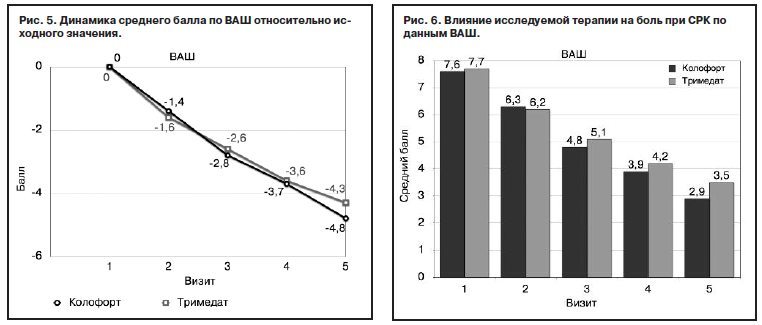
В целом под действием обоих препаратов в течение всего периода наблюдения отмечалась отчетливая сопоставимая положительная динамика в отношении купирования болевого синдрома с тенденцией к несколько большей эффективности в группе Колофорта (дисперсионный анализ: фактор «Группа» F1/145=0,7, p=0,4122; фактор «Визит» F3/435=2,2, p=0,1115; фактор «Группа*Визит» F3/435=3,7, p=0,0229; ковариата «Визит 1» F1/145=100, p=0,0001); рис. 5.
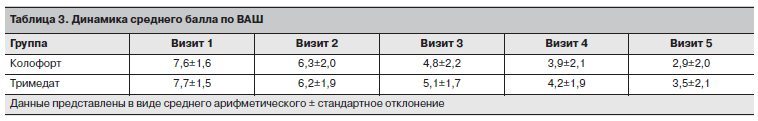
 Более выраженная тенденция к уменьшению болевого синдрома по ВАШ при приеме Колофорта по сравнению с Тримедатом, несмотря на сопоставимую эффективность проводимой терапии в целом, выявлена уже к визиту 3, через 4 нед терапии (табл. 3; рис. 6).
Более выраженная тенденция к уменьшению болевого синдрома по ВАШ при приеме Колофорта по сравнению с Тримедатом, несмотря на сопоставимую эффективность проводимой терапии в целом, выявлена уже к визиту 3, через 4 нед терапии (табл. 3; рис. 6).Выявленная тенденция к большей выраженности купирования боли в животе демонстрировала нарастание до конца исследования.
Таким образом, к окончанию 3-месячного курса Колофорт продемонстрировал более выраженное влияние на уменьшение болевого синдрома.
Влияние сравниваемой терапии на паттерн стула
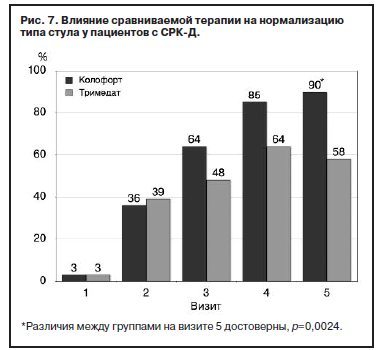
При анализе динамики изменений типа стула по Бристольской шкале формы кала получены результаты, свидетельствующие о существенном превосходстве терапии Колофортом по сравнению с Тримедатом. У пациентов с СРК-Д уже через 4 нед терапии нормальный стул наблюдался у 90% пациентов, получавших Колофорт, против 58% пациентов, получавших Тримедат (критерий Кохрана– Мантеля–Хенсзеля: χ2=8,4; p=0,0038; для визита 5 точный критерий Фишера: p=0,0024); рис. 7.Таким образом, Колофорт продемонстрировал достоверно превосходящую Тримедат эффективность во влиянии на нормализацию типа стула по Бристольской шкале у пациентов с СРК-Д. Причем эффективность Колофорта была более выраженной как по срокам, так и по стабильности изменений. Полученные результаты позволяют сделать вывод о более быстром и стабильном действии Колофорта в отношении нормализации типа стула у пациентов с СРК-Д по сравнению с Тримедатом. Различия в динамике влияния исследуемых препаратов на нормализацию типа стула при СРК-Д, вероятно, связаны с особенностями механизма действия препаратов и подтверждают регуляторное, патогенетическое действие Колофорта [13, 21].
Оценка динамики типа стула по Бристольской шкале у пациентов с СРК-З также продемонстрировала статистически значимое преимущество Колофорта по сравнению с Тримедатом (критерий Кохрана–Мантеля–Хенсзеля: χ2=29,1; p=0,0001).
Оба препарата продемонстрировали положительную динамику, но уже через 4 нед терапии доля пациентов с нормальным типом стула в группе Колофорта была более чем в 4 раза больше, чем в группе сравнения. А к концу наблюдения нормальный тип стула отмечен у всех пациентов группы Колофорта, тогда как данный параметр на фоне терапии Тримедатом был на 1/4 меньше и достиг значения лишь в 76% (точный критерий Фишера: визит 3 – p=0,0001, визит 5 – p=0,0135); рис. 8.
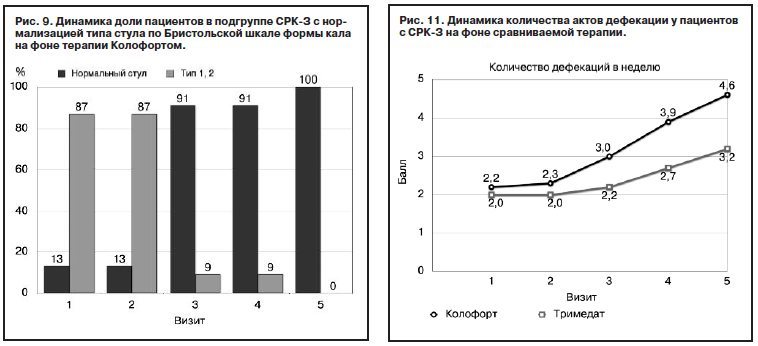
Стоит отметить, что, несмотря на одинаковую долю пациентов с типом стула 1, 2 (87%) на визите 1 и 2 в группе Колофорта, выраженность запора между двумя визитами в течение 2 нед терапии существенно уменьшилась. Так, к визиту 2 по сравнению с визитом 1 доля пациентов с типом стула 2 увеличилась более чем в 2 раза, а доля пациентов с типом стула 1 уменьшилась в 5,5 раза. В дальнейшем к визиту 3 доля пациентов с нормальным типом стула увеличилась в 7 раз, продемонстрировав нормализацию стула у 100% пациентов с СРК-З через 3 мес (рис. 9).
Полученные результаты позволяют сделать вывод о достоверном превосходстве Колофорта по сравнению с Тримедатом в отношении нормализации типа стула у пациентов с СРК-З. Превосходство заключалось в более быстром наступлении эффекта и большей его выраженности. Очевидно, выявленные различия в терапевтической эффективности связаны с особенностями действия Колофорта – его регуляторным влиянием как на центральные, так и на периферические звенья патогенеза заболевания [15–17].
При оценке динамики частоты дефекаций в подгруппе СРК-З определялась доля пациентов, у которых число актов дефекации увеличилось в среднем на 1 раз в неделю по сравнению с исходным уровнем. Было установлено, что результаты, полученные в группе Колофорта, значимо превосходят таковые в группе Тримедата, начиная уже с визита 2, 3-й недели терапии, достигнув максимума к 8-й неделе (метод Generalized estimating equations – GEE): Z=4,8; p=0,0001); рис. 10.
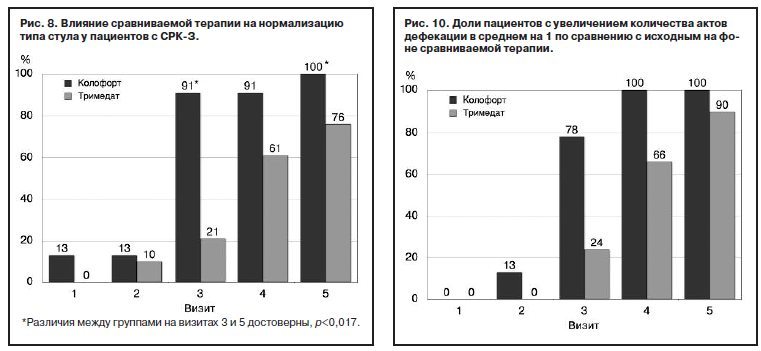
В группе Тримедата увеличение частоты стула происходило значительно медленнее, начавшись только с визита 3, через 4 нед лечения. На визите 4 улучшения по данному критерию достигли на 1/3 меньше пациентов, чем в группе Колофорта, а к окончанию исследования – 90% пациентов, тогда как в группе Колофорта уже на визите 4 отмечалась его нормализация у 100% пациентов.
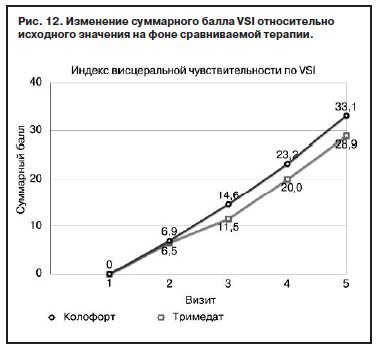
Средняя динамика количества актов дефекации у пациентов с СРК-З также свидетельствовала в пользу большей эффективности Колофорта, достигнув к окончанию наблюдения в среднем 4,6±0,9 раза в неделю против 3,2±0,6 раза в неделю в группе сравнения. Под действием Колофорта улучшение отмечалось уже с визита 2, тогда как на фоне приема Тримедата первые результаты получены на 4 нед позже, к визиту 3 (рис. 11).
Данные, полученные при оценке влияния сравниваемой терапии на паттерн стула, позволяют сделать вывод о достоверно более быстром наступлении эффекта Колофорта, его большей выраженности и стабильности по сравнению с Тримедатом у пациентов с СРК.
Влияние сравниваемой терапии на висцеральную гиперчувствительность
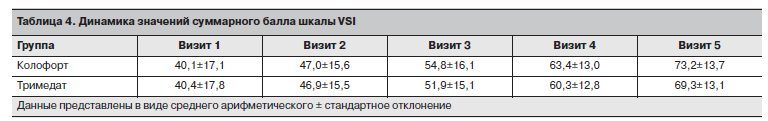
При анализе динамики значений данного критерия эффективности по шкале VSI в ходе исследования установлена статистически значимая тенденция к превосходству терапии Колофортом по сравнению с Тримедатом согласно результатам дисперсионного анализа (фактор «Группа» F1/146=4,3, p=0,0411; фактор «Визит» F3/438=306, p=0,0001; фактор «Группа*Визит» F3/438=2.8, p=0,0725; ковариата «Визит 1» F1/146=263, p=0,0001); табл. 4.
Несмотря на очевидно прослеживаемую в течение всего периода наблюдения тенденцию к преимуществу Колофорта по сравнению с Тримедатом, оценка изменений суммарного балла VSI относительно исходного значения на фоне сравниваемой терапии в целом свидетельствует о сопоставимой эффективности сравниваемых препаратов (дисперсионный анализ: фактор «Группа» F1/147=2,5, p=0,1147; фактор «Визит» F3/441=317, p=0,0001; фактор «Группа*Визит» F3/441=1,9, p=0,1701); рис. 12.
Полученные результаты позволяют сделать вывод о способности как Колофорта, так и Тримедата нормализовывать висцеральную гиперчувствительность, что подтверждают ранее описанные данные о влиянии препаратов на основные клинические проявления СРК. Прослеживаемая на протяжении всего периода наблюдения устойчивая тенденция к несколько большему, хотя и статистически незначимому влиянию Колофорта на изменение висцеральной чувствительности относительно исходного значения, что согласуется с продемонстрированной в данном исследовании его более выраженной терапевтической эффективностью в отношении клинической симптоматики.
Полученные в исследовании положительные результаты по влиянию проводимой терапии на клиническую симптоматику, висцеральную гиперчувствительность нашли свое отражение и в динамике значений суммарного балла опросника качества жизни IBS-QoL. Влияние изучаемой терапии СРК на качество жизни пациентов было сопоставимым в обеих группах при более выраженном его улучшении по сравнению с исходным уровнем в группе пациентов, получавших Колофорт.
В ходе данного исследования какого-либо неблагоприятного влияния на витальные функции и параметры, включая частоту сердечных сокращений, артериальное давление, а также нежелательных явлений в обеих группах зарегистрировано не было.
Исследуемые препараты характеризовались хорошей переносимостью, что наряду с продемонстрированной эффективностью обеспечило высокий уровень приверженности пациентов назначенной им терапии.
Выводы
Проведенное неинтервенционное сравнительное клиническое исследование в параллельных группах для оценки эффективности и безопасности применения препарата Колофорт в терапии СРК в сравнении с Тримедатом продемонстрировало соответствие применяемых препаратов основным клиническим задачам, решаемым при терапии данного заболевания, и в первую очередь – необходимости купирования его ведущих проявлений. При сопоставимой в целом эффективности рассматриваемых препаратов полученные в ходе исследования результаты позволяют сделать следующие выводы:1. Колофорт более выраженно влияет на уменьшение болевого синдрома – к окончанию исследования установлено статистически значимое превосходство по первичному критерию исследования с уменьшением выраженности боли на 30% и более у 95% пациентов основной группы против 84% пациентов в группе сравнения.
2. Колофорт достоверно более быстро, выраженно и стабильно способствует нормализации паттерна стула при СРК по сравнению с Тримедатом.
3. Колофорт достоверно превосходит Тримедат в эффективности нормализации типа стула по Бристольской шкале у пациентов с СРК, это заключается в более быстром наступлении эффекта и большей его выраженности.
4. Колофорт способствует нормализации висцеральной гиперчувствительности с устойчивой тенденцией на протяжении всего периода наблюдения к несколько большему по сравнению с Тримедатом, хотя и статистически незначимому, влиянию на ее изменение относительно исходного значения.
5. Влияние изучаемой терапии СРК на качество жизни пациентов было сопоставимым в обеих группах при более выраженном его улучшении по сравнению с исходным уровнем в группе пациентов, получавших Колофорт.
6. При сопоставимо высоком уровне безопасности применения сравниваемых препаратов также подтверждена высокая безопасность длительного использования Колофорта в терапии СРК, что иллюстрируют отсутствие зарегистрированных в ходе исследования нежелательных явлений и результаты мониторинга витальных функций пациентов.
Совокупность хорошей переносимости и продемонстрированной эффективности обеспечила высокий уровень приверженности пациентов назначенной терапии.
Таким образом, полученные данные позволяют рекомендовать препарат к широкому применению в терапии СРК вне зависимости от его подтипа и тяжести течения.
Литература
1. Canavan C, West J, Card T. The epidemiology of irritable bowel syndrome. Clin Epidemiol 2014; 6: 71–80.
2. Saha L. Irritable bowel syndrome: Pathogenesis, diagnosis, treatment, and evidence-based medicine. World Journal of Gastroenterology : WJG 2014; 20 (22): 6759–73.
3. Enck P, Aziz Q, Barbara G et al. Irritable bowel syndrome. Nat Rev Dis Primers 2016; 2: 16014.
4. Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features, and Rome IV. Gastroenterology 2016; 150 (6): 1262–79.
5. Lee YJ, Park KS. Irritable bowel syndrome: Emerging paradigm in pathophysiology. World J Gastroenterol 2014; 20 (10): 2456–69.
6. El-Salhy M. Recent developments in the pathophysiology of irritable bowel syndrome. World Journal of Gastroenterology. WJG 2015; 21 (25): 7621–36.
7. Drossman DA, Hasler WL. Rome IV – Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology 2016; 150 (6): 1257–61.
8. Ohman L, Simrén M. Pathogenesis of IBS: role of inflammation, immunity and neuroimmune interactions. Nat Rev Gastroenterol Hepatol 2010; 7 (3): 163–73.
9. Sinagra E, Pompei G, Tomasello G et al. Inflammation in irritable bowel syndrome: Myth or new treatment target? World J Gastroenterol 2016; 22 (7): 2242–55.
10. Bashashati M, Rezaei N, Shafieyoun A et al. Cytokine imbalance in irritable bowel syndrome: a systematic review and meta-analysis. Neurogastroenterol Motil 2014; 26 (7): 1036–48.
11. Маев И.В., Кучерявый Ю.А., Черемушкин С.В. Эволюция представлений о синдроме раздраженного кишечника. М.: Форте Принт, 2013. / Maev I.V., Kucheria-vyi Iu.A., Cheremushkin S.V. Evoliutsiia predstavlenii o sindrome razdrazhennogo kishechnika. M.: Forte Print, 2013. [in Russian]
12. Malagelada JR, Malagelada C. Mechanism-Oriented Therapy of Irritable Bowel Syndrome. Adv Ther 2016; p. 1–17. URL:link.springer.com/article/10.1007/s12325-016-0336-….
13. Самсонов А.А., Андреев Д.Н., Дичева Д.Т. Синдром раздраженного кишечника с позиций современной гастроэнтерологии. Фарматека. 2014; 18: 7–14. / Samsonov A.A., Andreev D.N., Dicheva D.T. Sindrom razdrazhennogo kishechnika s pozitsii sovremennoi gastroenterologii. Farmateka. 2014; 18: 7–14. [in Russian]
14. Андреев Д.Н., Самсонов А.А., Черемушкин С.В. Синдром раздраженного кишечника: критерии диагностики и подходы к терапии. Фарматека. 2014; 14: 6–11. / Andreev D.N., Samsonov A.A., Cheremushkin S.V. Sindrom razdrazhennogo kishechnika: kriterii diagnostiki i podkhody k terapii. Farmateka. 2014; 14: 6–11. [in Russian]
15. Инструкция по медицинскому применению препарата Колофорт. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx / Instruktsiia po meditsinskomu primeneniiu preparata Kolofort. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx [in Russian]
16. Авалуева Е.Б., Адашева Т.В., Бабаева А.Р. и др. Эффективность и безопасность применения Колофорта при синдроме раздраженного кишечника: итоги многоцентрового двойного слепого плацебо-контролируемого рандомизированного клинического исследования. Гастроэнтерология. 2014; 1: 36–43. / Avalue-va E.B., Adasheva T.V., Babaeva A.R. i dr. Effektivnost' i bezopasnost' primeneniia Koloforta pri sindrome razdrazhennogo kishechnika: itogi mnogotsentrovogo dvoinogo slepogo platsebo-kontroliruemogo randomizirovannogo klinicheskogo issledovaniia. Gastroenterologiia. 2014; 1: 36–43. [in Russian]
17. Осадчук М.А., Бурдина В.О. Новые патогенетические подходы к терапии синдрома раздраженного кишечника, основанные на морфофункциональных особенностях данной патологии. Практическая медицина. 2014; 1 (77): 12–20. / Osadchuk M.A., Burdina V.O. Novye patogeneticheskie podkhody k terapii sindroma razdrazhennogo kishechnika, osnovannye na morfofunktsional'nykh osobennostiakh dannoi patologii. Prakticheskaia meditsina. 2014; 1 (77): 12–20. [in Russian]
18. Инструкция по медицинскому применению препарата Тримедат. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx / Instruktsiia po meditsinskomu primeneniiu preparata Trimedat. URL: grls.rosminzdrav.ru/Grls_View_v2.aspx [in Russian]
19. Ивашкин В.Т., Драпкина О.М. Возможности применения тримебутина в лечении больных с синдромом раздраженного кишечника. РЖГГК. 2008; 18 (5): 12–6. / Ivashkin V.T., Drapkina O.M. Vozmozhnosti primeneniia trimebutina v lechenii bol'nykh s sindromom razdrazhennogo kishechnika. RZhGGK. 2008; 18 (5): 12–6. [in Russian]
20. Miller LE. Study design considerations for irritable bowel syndrome clinical trials. Annals of Gastroenterology: Quarterly Publication of the Hellenic Society of Gastroenterology. 2014; 27 (4): 338–45.
21. Казюлин А.Н. Колофорт: механизм действия и возможности патогенетической терапии заболеваний желудочно-кишечного тракта. Гастроэнтерология Санкт-Петербурга. 2016; 1–2: 19–23. / Kaziulin A.N. Kolofort: mekhanizm deistviia i vozmozhnosti patogeneticheskoi terapii zabolevanii zheludochno-kishechnogo trakta. Gastroenterologiia Sankt-Peterburga. 2016; 1–2: 19–23. [in Russian]
22. Ивашкин В.Т., Шелыгин Ю.А., Баранская Е.К. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации, Ассоциации колопроктологов России по диагностике и лечению больных с синдромом раздраженного кишечника. Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. 2014; 2: 92–9. / Ivashkin V.T., Shelygin Iu.A., Baranskaia E.K. i dr. Klinicheskie rekomendatsii Rossiiskoi gastroenterologicheskoi assotsiatsii, Assotsiatsii koloproktologov Rossii po diagnostike i lecheniiu bol'nykh s sindromom razdrazhennogo kishechnika. Ros. zhurn. gastroenterologii, gepatologii, koloproktologii 2014; 2: 92–9. [in Russian]
СВЕДЕНИЯ ОБ АВТОРАХ
Маев Игорь Вениаминович – чл.-кор. РАН, д-р мед. наук, проф., зав. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Самсонов Алексей Андреевич – д-р мед. наук, проф. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова. E-mail: aleksey.samsonov@gmail.com
Андреев Дмитрий Николаевич – ассистент каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Шестаков Вячеслав Александрович – д-р мед. наук, проф. каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Яшина Александра Валерьевна – аспирант каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Караулов Сергей Алексеевич – канд. мед. наук, ассистент каф. пропедевтики внутренних болезней и гастроэнтерологии ГБОУ ВПО МГМСУ им. А.И.Евдокимова
Портал Consilium Medicum:
con-med.ru/eprint/234435
