Изучение эффективности обеззараживателя воздуха нового типа — генератора диоксида хлора на примере вируса гриппа A (H1N1)pdm09 в составе аэрозоля
СтатьиЛЕЧАЩИЙ ВРАЧ, НОЯБРЬ 2016, № 11,
Скачать репринт статьи в формате pdf
В. В. Зарубаев* кандидат биологических наук
А. А. Штро*, кандидат биологических наук
Е. Н. Свентицкий**, доктор технических наук, профессор
* ФГБУ НИИ гриппа МЗ РФ, Санкт-Петербург ** ГосНИИ ОЧБ ФМБА России, Санкт-Петербург
Резюме. Рассмотрены подходы к профилактике респираторных вирусных инфекций, включая применение средств инактивации внеклеточного вируса на поверхностях и в объеме помещений, что позволяет предотвратить инфицирование людей в местах их скоплений.
Ключевые слова: респираторные вирусные инфекции, грипп, инфекционная активность, санитарные меры, профилактика.
Abstract. Approaches to prevention of respiratory viral infections were considered, including application of inactivation drugs for extracellular virus on the surfaces and inside the facilities, which allows to prevent contamination in gathering of people. Keywords: respiratory viral infections, influenza, infectious activity, sanitary measures, prophylaxis.
Грипп представляет собой широко распространенную во всем мире респираторную инфекцию. Он является наиболее тяжелым заболеванием, вызываемым респираторными вирусами человека. Грипп вызывает ежегодные эпидемии, быстро распространяющиеся из страны в страну, вовлекая в тяжелых случаях (пандемии) значительную часть человеческой популяции земного шара. Он также является причиной 20 000—40 000 смертельных исходов в США в год [1]. Он остается трудно контролируемой инфекцией, несмотря на успехи, достигнутые в области химиотерапии, вакцинопрофилактики и иммунологии. Это обусловлено высокой генетической изменчивостью возбудителя и долговременными осложнениями после острой стадии, приводящими к «скрытой», или вторичной, смертности [2, 3].
Наиболее эффективным средством профилактики гриппа является вакцинация. Однако вследствие постоянной смены антигенных свойств возбудителя требуется постоянный мониторинг и разработка новых вакцинных штаммов, соответствующих циркулирующим в человеческой популяции в каждый конкретный эпидемический сезон.
Наряду с вакцинацией для предотвращения и лечения заболевания применяются химиопрофилактика и химиотерапия гриппа. В настоящее время для этих целей доступен широкий спектр патогенетических, иммуномодули-рующих, общеукрепляющих препаратов наряду со средствами специфической противогриппозной терапии. Этиотропные препараты для лечения гриппа представлены соединениями двух групп, отличающимся по механизму действия и вирусным мишеням. Ремантадин и амантадин блокируют белок М2 вируса гриппа, препятствуя тем самым процессу расщепления гемагглютинина и слияния мембран вируса и лизосомальной вакуоли [4]. Препараты второй группы ингибируют вирусную нейраминидазу, необходимую для почкования и распространения вирусных частиц. Сюда относятся занамивир (Реленца®), осельтамивир (Тамифлю®), перамивир (Рапиваб®) и ланинамивир (Инавир®) [5], последние два в России не зарегистрированы. Кроме того, в Японии, Корее и Китае используется препарат T-705 (Фавипиравир), являющийся нуклеозидным аналогом [6-8], направленный на вирусную полимеразу и обладающий, активностью не только против вируса гриппа, но и против широкого круга других вирусов [9].
В отношении группы производных адамантана можно отметить сравнительно высокую токсичность и узкий спектр действия (препараты активны против гриппа А, но не против гриппа В, не имеющего белка M2). Для ингибиторов нейраминидазы характерна высокая стоимость синтеза, что делает эти препараты менее доступными для широкого использования. Кроме того, к препаратам обеих групп вирус гриппа способен вырабатывать устойчивость [10, 11].
Однако для более надежного контроля заболеваемости наряду с вакцинопрофилактикой и химиотерапией важную роль играют средства инактивации внеклеточного вируса на поверхностях и в объеме помещений. Такие меры позволяют во многом предотвратить инфицирование людей в местах их скоплений, таких как общественные места, массовые мероприятия и т. п. Для обеззараживания поверхностей и объемов помещений используются ультрафиолетовые лампы различного спектрального диапазона и химические средства дезинфекции.
Преимуществом ультрафиолетового облучения является его комплексный механизм. Эффективность такого воздействия на патогены обусловлена как прямым воздействием излучения, так и реакционно-способными молекулами озона О3, генерируемыми при взаимодействии ультрафиолетовых квантов с кислородом воздуха. Следует, однако, отметить, что доза облучения падает пропорционально квадрату расстояния от источника и для инактивации вируса на поверхностях в помещениях потребуется время, также пропорциональное квадрату линейных размеров помещения. Кроме того, для эффективного обеззараживания поверхностей требуется прямая их экспозиция к облучению, что не всегда достижимо в помещениях сложного профиля и с установленным оборудованием и мебелью. В этом случае основной эффект дезинфекции достигается за счет диффузии молекул озона, имеющей меньшую эффективность.
В России в настоящее время для обеззараживания помещений из дезинфицирующих средств в форме аэрозоля применяют [12]:
- 37%-е растворы формальдегида;
- 20%-й раствор параформальдегида с добавлением 1% едкой щелочи;
- 24%-й раствор глутарового альдегида;
- 30%-й раствор алкамона;
- препарат надуксусной кислоты;
- 10%-й раствор перекиси водорода с добавлением 1% муравьиной кислоты.
Для дезинфекции воздуха и поверхностей помещений в присутствии животных в форме аэрозоля применяют молочную кислоту, йод, триэ-тиленгликоль и гипохлорит натрия. Следует указать на такие недостатки этих препаратов, как:
- высокая токсичность для человека;
- необходимость направленного распыления при обработке поверхностей;
- необходимость дополнительной очистки или нейтрализации после обработки деконтаминантом (например, 25% аммиак после обработки формальдегидом и глутаральдегидом, раствор железосинероди-стого калия после обработки алкамоном и пр.);
- высокие нормы расхода препарата дезинфектанта (15-90 мл/м3 или 100-200 мл/м2 при обработке поверхностей).
Грипп представляет собой наиболее тяжелое и опасное заболевание из группы острых респираторных вирусных инфекций. Список химических дезинфицирующих агентов [14], активных в отношении вируса гриппа птиц H5N1, на 13 марта 2008 г. включает более 100 зарегистрированных коммерческих препаратов, содержащих химические соединения нескольких классов. Активные компоненты дезинфектантов могут быть подразделены на несколько типов по механизму действия.
1. Химические окислители. Сюда входят такие соединения, как кислоты (фосфорная, соляная, лимонная и др.), соли хлорсодержа-щих кислот (хлориты, гипохлориты), перекись водорода, йод и пр. Такие вещества оказывают неспецифическое разрушающее действие на все материалы, и степень этого разрушения зависит от устойчивости материала к окисляющим агентам, при этом биологические соединения, составляющие бактерии и вирусы, оказываются более уязвимыми по сравнению с материалами самих помещений, мебели и оборудования, чем и обусловлен эффект дезинфекции. Окислители могут применяться как для протирания поверхностей, так и для обеззараживания воздуха посредством аэрозолирования. В любом случае, однако, лишь некоторые из них (перекись водорода) впоследствии распадаются при взаимодействии с компонентами воздуха. Многие другие дезинфектанты этой группы (кислоты, йод и пр.), напротив, сохраняют свою химическую активность и реакционную способность, чем создают потенциальную опасность для человека и животных, находящихся в дальнейшем в обработанных помещениях. В особенности актуален этот аспект при аэрозольной обработке и с учетом летучести активных соединений. Например, пары йода представляют опасность для слизистых оболочек ротовой полости, глаз и носоглотки и при попадании на них могут привести к побочным последствиям. Кроме того, соединения, действующие при помощи активного хлора (например, препараты Хлорокс (компания Clorox), Жавель солид (компания Жазол) и др.), имеют ограниченный срок действия вследствие малой стабильности хлора. Поэтому при проведении дезинфекционных мероприятий следует либо готовить рабочие растворы непосредственно перед дезинфекцией, либо контролировать концентрацию активного хлора, что дополнительно усложняет процедуру деконтаминации [15].
2. Поверхностно-активные вещества. Как правило, аммониевые производные жирных кислот (С12-С18). Их активность обусловлена воздействием на липидные оболочки и белковые капсиды вирусов, и их использование ограничивается в основном дезинфекцией поверхностей. Эти соединения не распадаются со временем, поэтому после обработки требуется дополнительная процедура промывки дезинфицированных поверхностей водой или другим дезинфектантом.
3. Фиксирующие и денатурирующие агенты. Сюда относятся этанол, фенол, формальдегид, глутаральдегид и пр. Активность соединений этого класса является следствием их способности к дегидратации (этанол), денатурации (фенол) или образованию перекрестных сшивок (формальдегид) в биологических молекулах. К характерным особенностям этих соединений относится их высокая летучесть, с одной стороны, обеспечивающая их высокую проникающую способность, а с другой — представляющая потенциальную опасность при контакте с органами дыхания.
К примеру, одним из основных средств деконтаминации против гриппа птиц за рубежом является препарат Виркон (Virkon®S) производства DupontAnimalHealthiSolutjons или KRKA, представляющий собой смесь соединений перекиси, поверхностно-активных веществ, органических кислот и неорганических буферных систем [13]. Главным компонентом состава является калия персульфат 50%. Препарат обладает антимикробной активностью в отношении грамотрицательных и грамположительных бактерий (кроме микобактерий туберкулеза), вирусов (включая ВИЧ, гепатит В, герпес, грипп, полиомиелит, ротавирус, энтеровирусы и др.), грибов рода Candida, дермато-фитов. В отношении спор бактерий препарат не проявляет активности.
С целью оценки дезинфицирующих свойств персонального обез-зараживателя воздуха нового типа (генератора диоксида хлора) как средства инактивации возбудителей воздушно-капельных вирусных инфекций было проведено исследование его вирулицидного действия в аэрозольной камере с распыленным вируссодержащим аэрозолем, содержащим вирус гриппа А. После активации средства (извлечения кассеты из герметичной алюминиевой упаковки) запускается медленное испарение активного компонента (диоксида хлора), который уничтожает болезнетворные вирусы и бактерии в окружающем воздухе.
Материалы и методы исследования
Подготовка обеззараживателя воздуха для тестирования
Обеззараживатель воздуха индивидуальный (генератор диоксида хлора производства Global Product Planning Co., Ltd.) извлекали из защитного пакета, выдерживали в течение 1 часа в открытом состоянии и помещали в аэрозольную камеру в воздухонепроницаемый пакет. Момент открывания пакета считали нулевой временной точкой эксперимента.
Исследование защитных свойств обеззараживателя воздуха индивидуального (генератора диоксида хлора) 3,0 мл суспензии вируса (5 х 107 ЕЮ50/мл) распыляли в течение 10 минут в камере объемом 0,4 м3 с помощью вихревого пневматического генератора аэрозоля типа ВАГ-2, расположенного в центре камеры и обеспечивающего получение аэрозоля с расчетной концентрацией 3,8 х 104 ЕЮ50/л с массовым медианным диаметром частиц 3,6 мкм. Для равномерного распределения аэрозоля в объеме камеры использовали постоянно работающий вентилятор. Система для отбора проб воздуха включала насос, измеритель скорости потока и микроциклон для улавливания частиц аэрозоля, содержащий 10 мл физиологического раствора.
Отбор проб воздуха в микроциклоны для определения концентрации вируса, находящегося в воздушной фазе объема камеры, проводили в течение 2 минут при скорости потока 7,2 л/мин, что приблизительно соответствует режиму дыхания человека. Забор материала проводили в периоды 1-3, 3-5 и 10-12 мин после начала экспозиции обеззаражи-вателя воздуха индивидуального (генератора диоксида хлора).
В контрольной серии экспериментов те же манипуляции проводили в отсутствие изучаемого обеззараживателя воздуха индивидуального (генератора диоксида хлора).
Вирус
В работе использовали вирус гриппа A/California/07/09 (H1N1)pdm09. Вирус культивировали в течение 48 часов при 36 °С в аллантоисной полости 10-12-дневных куриных эмбрионов. В качестве исходного инфекционного материала использовалась аллантоисная жидкость.
Подготовка инфекционного материала
Вируссодержащую аллантоисную жидкость центрифугировали в течение 30 минут при 4 °С и 4000 об./мин. После осаждения фрагментов мембран и крупных контаминирующих частиц надосадок центрифугировали при 36 000 g и 4 °С в течение 1 часа. Осажденные вирионы ресуспендировали в физиологическом растворе, равном по объему исходному количеству аллантоисной жидкости. Полученная вирусная суспензия имела физические характеристики, близкие к таковым для воды. Это позволило использовать ее для создания аэрозоля, что было затруднительно при использовании аллантоисной жидкости с высоким содержанием белков и, как следствие, большой вязкостью. Для замедления высыхания частиц аэрозоля, приводящего к быстрой потере инфекционной активности, к вирусной суспензии добавляли глицерин до конечной концентрации 5%.
Титрование инфекционной активности вируса
Аликвоты физиологического раствора отбирали из микроциклонов и готовили из них серию десятикратных разведений на фосфатном буфере. 10-12-дневные куриные эмбрионы заражали серийными десятикратными разведениями вирусного материала от 100 до 10-6 по 0,2 мл на эмбрион и инкубировали в термостате при 36 °C в течение 48 часов. По окончании срока инкубации эмбрионы охлаждали, вскрывали и переносили аллантоисную жидкость (0,1 мл) в лунки планшета для иммунологических реакций, после чего добавляли равный объем 1% куриных эритроцитов в физиологическом растворе.
Уровень репродукции вируса в эмбрионах оценивали по реакции гемагглютинации эритроцитов. За титр вируса принимали величину, обратную наибольшему разведению вируса, способного вызвать положительную реакцию гемагглютинации, и выражали в логарифмах 50% инфекционной дозы вируса (lgID50). На основании полученных результатов на каждом сроке эксперимента оценивали эффективность инактивации — снижение титра вируса в% от контроля.
Статистическая обработка результатов
Статистическую обработку результатов оценки активности проводили с помощью непараметрического U-критерия Манна-Уитни. Различия считали значимыми при р < 0,05.
Результаты
Данные по титрованию проб воздуха на инфекционную активность вируса гриппа суммированы в табл. (для наглядности представлены на рис.).
|
Таблица. |
|||
|
Интервал отбора проб воздуха, мин |
Титр вируса в пробах воздуха, lgID50/0,2 мл |
||
|
Без обеззараживателя |
С обеззараживателем |
Эффективность, % |
|
|
1-3 |
3,0 ± 0,5 |
2,0 ± 0,5 |
90 |
|
3-5 |
2,5 ± 1,0 |
1,0 ± 0,5 |
97 |
|
10-12 |
2,0 ± 0,5 |
0,0 ± 0,0* |
99 |
|
Контроль заражающего вируса |
7,0 ± 0,0 |
||
|
Примечание. * Различия с группой контроля значимы при р < 0,05. |
|||
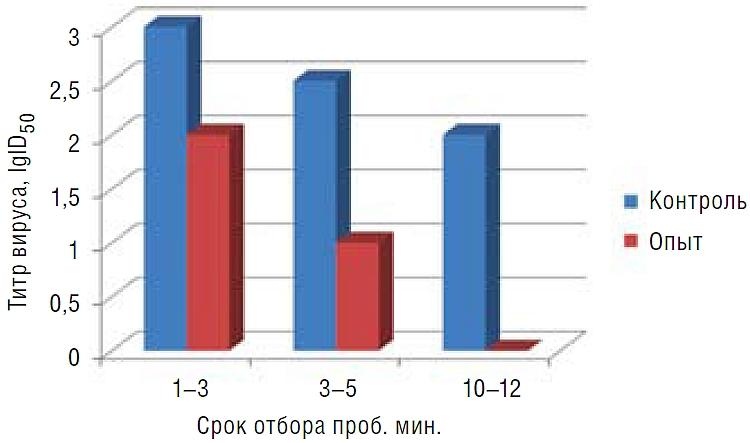
Как следует из представленных данных, титр вируса в аэрозоле в начале эксперимента составлял 3,0 lgID50/0,2 мл, что примерно на порядок ниже, чем следует из расчетных данных. Такое падение инфекционной активности вируса следует объяснять его инактивацией при высыхании частиц аэрозоля, негативно влияющей на биологические свойства вирионов.
С течением времени от 1 до 10 мин эксперимента отмечалось некоторое снижение инфекционной активности вируса в составе аэрозоля, что можно объяснить коагуляцией его частиц и последующей их седиментацией, что приводит к снижению количества инфекционного вируса в воздушной фазе. Тем не менее, на каждом из этапов эксперимента воздействие обеззара-живателя воздуха индивидуального (генератора диоксида хлора) снижало инфекционный титр вируса на 1-2 порядка. При 10-минутной экспозиции инфекционный вирус в воздухе не обнаруживался.
Выводы
Таким образом, в условиях аэрозольной камеры применение обез-зараживателя воздуха индивидуального (генератора диоксида хлора) приводит к инактивации вируса гриппа в составе аэрозоля, что позволяет прогнозировать его использование в качестве средства инактивации вируса гриппа в воздухе. Более детальные исследования спектра активности, механизма и кинетики обеззараживания являются главными направляющими будущих экспериментов для объективной оценки перспективности данной новой технологии. ■
Литература
1. Киселев О.И., Маринич И.Г, Соминина А.А. (ред.). Грипп и другие респираторные инфекции: эпидемиология, профилактика, диагностика и терапия. СПб, 2003. 244 с.2. Покровский В.И. (ред.). Грипп птиц: происхождение инфекционных биокатастроф. СПб, 2005. 269 с.
3. Киселев О.И. Геном пандемического вируса гриппа A/H1N1 v-2009. СПб-М., 2011. 163 с.
4. Scholtissek C., Quack G., Klenk H.D, Webster R.G. How to overcome resistance of influenza A viruses against adamantane derivatives // Antiviral Res. 1998; 37: 83-95.
5. Fiore A.E, Fry A, Shay D. et al. Antiviral agents for the treatment and chemoprophylaxis of influenza // Recomm. Rep. 2011; 60 (1): 1-26.
6. Kiso M. , Takahashi K., Sakai-Tagawa Y. et al. T-705 (favipiravir) activity against lethal H5N1 influenza A viruses // Proc. Natl. Acad. Sci. USA. 2010; 107:
882-887.
7. Sleeman K, Mishin V. P., Deyde V. M. et al. In vitro antiviral activity of favipiravir (T-705) against drug-resistant influenza and 2009 A (H1N1) viruses // Antimicrob. Agents Chemother. 2010; 54: 2517-2524.
8. Smee D.F., Hurst B.L., Wong M.H. et al. Effects of the combination of favipiravir (T-705) and oseltamivir on influenza A virus infections in mice // Antimicrob. Agents Chemother. 2010; 54: 126-133.
9. Furuta Y., Takahashi K., Shiraki K. et al. T-705 (favipiravir) and related compounds: Novel broad-spectrum inhibitors of RNA viral infections // Antiviral Res. 2009; 82: 95-102.
10. Pizzorno A., Abed Y, Boivin G. Influenza drug resistance//Semin. Respir. Crit. Care Med. 2011; 32: 409-422.
11. Thorlund K., Awad T., Boivin G., Thabane L. Systematic review of influenza resistance to the neuraminidase inhibitors // BMC Infect. Dis. 2011; 11: 134.
12. Проведение ветеринарной дезинфекции объектов животноводства (инструкция ^агропромышленного Комитета СССР). М., 1988.
13. thepoultrysite.com/articles/124/avian-influenza-de…procedures-for-the-cleaning-and-disinfection-of-farm-premises.
14. epa.gov/pesticides/factsheets/avian_flu_products.h….
15. who.int/csr/resources/publications/surveillance/An….
1 Контактная информация: vladimir.zarubaev@influenza.spb.ru


