Микроэлементные и микрогемодинамические нарушения у пациентов с дисциркуляторной энцефалопатией при использовании Мексидола в комплексном лечении
Статьи Опубликовано в журнале, "Неврология и нейрохирургия в Беларуси" № 1 (09), 2011 Нечипуренко Н.И., Верес А.И., Василевская Л.А., Пашковская И.Д.РНПЦ неврологии и нейрохирургии МЗ РБ
|
Выполнена оценка нейропротективной эффективности Мексидола в составе комплексной терапии с изучением результатов количественной характеристики клинического статуса, ряда химических элементов в крови (кальций, магний, железо, медь, цинк, алюминий и литий) и кожной микрогемодинамики у пациентов с дисциркуляторной энцефалопатией (ДЭ). При ДЭ установлены дефицит некоторых эссенциальных макро- и микроэлементов (кальция, железа, цинка и лития), снижение цереброваскулярной реактивности с ограничением резервов вазоконстрикции и вазодилатации, что имеет существенное значение в механизмах формирования хронического гипоксического повреждения головного мозга. Использование Мексидола в составе комплексного лечения у пациентов основной группы по сравнению с результатами базисной терапии в контрольной группе способствует коррекции содержания ряда микроэлементов, микрогемодинамики и цереброваскулярной реактивности, что подтверждает целесообразность применения этого препарата для лечения больных с ДЭ. Ключевые слова: Мексидол, микроэлементы, кожная микрогемодинамика, дисциркуляторная энцефалопатия. Blood trace elements content and the condition of the dermal microhaemodynamic in patients with dyscirculatory encephalopathy after the complex treatment with Mexidol
Nechipurenko N.I., Veres A.I., Vasilevskaya L.A., Pashkovskaya I.D. The blood trace elements concentration (Ca, Mg, Fe, Cu, Zn, Li and Al), the dermal microhaemodynamic, the climical codition in patients with dyscirculatory encephalopathy (DE) after the treatment with Mexidol were investigated. There were registered Ca, Fe, Zn and Li concentration decreasing, the cerebrovascular reactivity decreasing with limitation of vasoconstriction and vasodilatation reserve in connection with the pathogenesis of the chronicle cerebral ischemia. The treatment with Mexidol in patients with DE of the main group lead to correction the content some trace elements concentration (Fe, Zn, Li), the dermal microhaemodynamic and cerebrovascular reactivity. Key words: Mexidol, trace elements, dermal microhaemodynamic, dyscirculatory encephalopathy. Введение Дисциркуляторная энцефалопатия (ДЭ) относится к широко распространенным заболеваниям, нередко сопровождающимся развитием инфаркта мозга и когнитивными нарушениями, которые приводят пациентов к трудовой и социальной дезадаптации. Это обусловливает медико-социальную значимость изучения патогенеза, диагностики и терапии хронических форм цереброваскулярных заболеваний ишемического генеза. | |
| Сложность патогенетической структуры ишемии головного мозга, включающей в себя нарушения процессов свободнорадикального окисления, макро- и микроэлементного гомеостаза, микрогемоциркуляции, развитие дисфункции эндотелия, предполагает включение в фармакологическую терапию ДЭ препаратов, корригирующих эти сдвиги. Одним из таких средств является Мексидол - синтетический препарат, выпускаемый фирмой "Фармасофт" (Россия), который представляет собой соль янтарной кислоты (2-этил-6-метил-3-гидроксипиридина сукцинат). Препарат обладает антигипоксическим и антиоксидантным действием. Он тормозит процессы перекисного окисления липидов (ПОЛ), активирует супероксиддисмутазу (СОД), оказывает влияние на физико-химические свойства мембраны и улучшает энергетический обмен в клетке. Известно, что от особенностей обмена макро- и микроэлементов во многом зависят процессы синтеза и деградации многочисленных медиаторов, гормонов и нейропептидов, регуляция трансмембранного потенциала клеток, нервной проводимости, сосудистого тонуса, функциональное состояние эндотелия сосудов, все этапы свертывания крови [10]. Существенное место в оценке компенсаторно-адаптивных возможностей организма при сосудистых заболеваниях головного мозга занимает взаимосвязь между микроэлементным и антиоксидантным статусом организма, что обусловлено каталитическими реакциями инициирования, развития и затухания процессов свободнорадикального окисления [4]. | Мексидол оказывает церебропротекторное, ноотропное, вегетотропное действие. Обладает способностью улучшать мозговое кровообращение, ингибировать агрегацию тромбоцитов, снижать уровень общего холестерина, оказывать антиатеросклеротическое действие [1]. |
Показано, что отдельные микроэлементы участвуют в про- или антиоксидантных реакциях и проявляют свои свойства в зависимости от концентрации [10]. Большую роль в несостоятельности ферментативной антиоксидантной системы (АОС) играет дефицит микроэлементов - меди и цинка, входящих в каталитические центры СОД, а усиление реакций ПОЛ приводит в свою очередь к изменению состава клеточных мембран, нарушению их проницаемости и ионному дисбалансу, особенно электролитов - калия, натрия, кальция и магния [4]. Магнийсодержащие ферменты и ионы магния обеспечивают поддержание энергетических и пластических процессов в нервной ткани. Его уровень влияет на регуляцию баланса фракций липопротеидов высокой и низкой плотности и триглицеридов [2]. Железо, обладая выраженными окислительно-восстановительными свойствами, участвует в переносе кислорода гемоглобином, синтезе ДНК, работе многочисленных митохондриальных энзимов, но в то же время оно может инициировать ПОЛ и повреждать макромолекулярные компоненты клеток [12]. Цинк способен защищать эндотелий сосудов при атеросклерозе и ишемии мозга, а также обладает антиокислительным эффектом. Он является кофактором процессов репарации и регенерации вследствие своих антиоксидантных свойств. В неврологической практике дефицит цинка встречается чаще, чем его избыток. Литий участвует в обмене нейромедиаторов (норадреналина, дофамина, серотонина). В больших дозах он снижает активность эксайтотоксичных аминокислот глутамата и аспартата в центральной нервной системе (ЦНС). В экспериментальных исследованиях было показано, что литий тормозит апоптоз стволовых клеток мозга [4]. Учитывая функциональную роль биоэлементов в организме и характер изменения их содержания при острой ишемии головного мозга, выявленный нами ранее [9], можно предположить позитивное влияние Мексидола и на макро-, микроэлементный гомеостаз в организме при ДЭ. | Алюминий известен более широко как генотоксичный металл, так как вследствие высокого аффинитета к фосфатным группам ДНК легко с ней связывается и токсически действует на процесс митоза [11]. |
| В ранее выполненной нами работе была изучена нейропротективная эффективность Мексидола на модели локальной ишемии головного мозга у кроликов. Применение препарата в раннем постишемическом периоде способствовало снижению первичных и вторичных продуктов ПОЛ с увеличением активности ферментативного звена АОС, улучшению снабжения тканей головного мозга кислородом, а также оказало позитивный эффект на показатели кислородтранспортной функции крови и микрогемодинамических процессов в тканях [6]. Полученные данные послужили патогенетическим обоснованием использования Мексидола в комплексной фармакотерапии больных с ДЭ - хронической ишемией мозга (ХИМ). Цель Целью настоящего исследования явилось изучение влияния Мексидола в составе комплексной терапии на состояние клинического статуса, кожной микрогемодинамики (МГД) и содержание ряда микроэлементов в крови у пациентов с ДЭ. Материалы и методы исследований Обследовано 34 пациента со 2-й стадией ДЭ и 19 практически здоровых добровольцев (доноры). Критериями включения в исследование явились наличие у больных неврологической микросимптоматики, в т.ч. когнитивных нарушений при системном поражении сосудов (стенозирующий атеросклероз, артериальная гипертензия, гиперхолестеринемия, экстравазальная компрессия позвоночных артерий) и характерных изменений при выполнении компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) и ультразвуковой допплерографии (УЗДГ) брахиоцефальных артерий. Критериями исключения служили острые нарушения мозгового кровообращения, тяжелые сопутствующие поражения легких и сердца, указания в анамнезе на наличие тяжелой печеночной и почечной недостаточности, интоксикаций различного генеза. Анализ эффективности Мексидола в составе комплексной терапии у больных с ДЭ проведен в двух группах обследованных, сформированных рандомизированно. Основную группу составили 23 пациента (11 мужчин и 12 женщин, средний возраст 68,2 ± 9,7 года), в контрольную группу вошли 11 больных (5 мужчин и 6 женщин, средний возраст 67,4 ± 10,3 года; р>0,05), получавших базисную терапию. Пациенты основной группы получали Мексидол по 4,0 мл 5%-го раствора внутривенно струйно ежедневно в течение 10 дней. Базисная терапия включала Полокард, или Кардиомагнил, или Аспирин по 75 мг внутрь ежедневно, 20%-й раствор пирацетама по 10 мл внутримышечно в течение 10 дней ежедневно; при необходимости назначали вазодилататоры, гипотензивные средства и симптоматическую терапию. Забор крови осуществляли из кубитальной вены натощак. В качестве антикоагулянта использовали гепарин. Концентрации химических элементов (кальций, магний, железо, медь, цинк, алюминий и литий) в цельной крови определяли методом атомно-эмиссионной спектрометрии [3]. Функциональное состояние кожной МГД изучали неинвазивным спекл-оптическим методом с помощью лазерного диагностического аппарата "Спеклометр". С помощью осветительно-приемного датчика излучением лазера освещался участок кожного покрова в области лба. Расчет спектра производили в диапазонах 1-1000 Гц. Оценивали наиболее информативный показатель спектров динамического спекл-поля - мощность спектра (МС), равную площади под спектральной кривой. Разработаны способы оценки и информативные критерии васкулярной реактивности у здоровых лиц и у больных с ХИМ при церебральной микроангиопатии. Один из способов - методика спеклоптического исследования реактивности микроциркуляторного русла кожных покровов головы с оценкой вазодилататорного резерва. С этой целью проводили гиперкапническую функциональную пробу с задержкой дыхания (ЗД). Алгоритм обследования включал запись параметров кожной МГД при спокойном дыхании, через 12-15 с после ЗД, продолжающейся 25 с, а также через 30 с после восстановления дыхания. Данные представлены с учетом типа реакций на проведение функциональной пробы:
Не менее информативной оказалась оценка времени и степени восстановления изучаемых параметров в периоде восстановления дыхания. Второй способ - исследование реактивности микрогемоциркуляторного русла кожных покровов головы с оценкой вазоконстрикторного резерва. Алгоритм проведения гипокапнической функциональной пробы с гипервентиляцией (ГВ) включал запись параметров кожной МГД при спокойном дыхании, затем через 1 мин после начала ГВ, продолжающейся 3 мин, а также спустя 1 мин после восстановления дыхания. Данные представлены с учетом типа реакций на проведение функциональной пробы:
При статистической обработке результатов применяли программу Statistica 6.0. Проводили проверку данных на нормальность с помощью критерия Шапиро - Уилка. При нормальном распределении вычисляли среднюю арифметическую и стандартное отклонение (M ± SD). Результаты и их обсуждение | |
Как правило, ХИМ начиналась с цефалгического или неврастенического синдрома: головные боли, раздражительность, утомляемость, головокружение, снижение памяти, нарушение сна. С течением времени симптомы постепенно прогрессировали, усугублялись когнитивные нарушения, присоединялись пирамидные симптомы (микрознаки, гемисиндром), координаторные и мышечно-тонические нарушения, псевдобульбарный синдром. Поражения сосудов становились распространенными с вовлечением в процесс как вертебрально-базилярного, так и каротидного бассейнов. В большинстве случаев в клинических проявлениях ДЭ диагностированы несколько синдромов одновременно. Наиболее часто сочетались когнитивные нарушения, неврастенический и атактический синдромы, пирамидные знаки. Особенностью цефалгического синдрома являлась его полиморфность, непостоянство, отсутствие в большинстве случаев связи с конкретными сосудистыми и гемодинамическими факторами. Часто прослеживалась связь с эмоциональными, астеническими и тревожно-депрессивными расстройствами, а также вегетативными нарушениями. Когнитивные нарушения у больных с ХИМ были наиболее частым синдромом. 67% обследованных отмечали снижение памяти, особенно на близкие события (расстройство памяти по закону Рибо), нарушения способности концентрации внимания, восприятия новой информации, анализа происходящих событий, быструю истощаемость при запоминании нового. Пирамидные нарушения при ДЭ, как правило, были слабо выражены и у 43% больных представлены рассеянными микрознаками, гемисиндромом, пирамидной недостаточностью, легким гемипарезом. Особенностью пирамидного синдрома часто являлась его умеренная клиническая манифестация - анизорефлексия, минимально выраженные парезы. Заболевание в 19% случаев сопровождалось возникновением амиостатических расстройств в виде акинезии (олигобрадикинезия, гипомимия, сложность инициации движений) и негрубой мышечной ригидности, чаще в нижних конечностях с положительным феноменом "противодействия". При КТ и МРТ визуализировались смешанная церебральная атрофия и лейкоареоз. Заболевание обычно прогрессировало ступенеобразно, что обусловлено возникновением острых эпизодов дисгемии. Среди пароксизмальных расстройств при ХИМ в 4,7% случаев наблюдали дроп-атаки (внезапные падения без нарушения сознания) и в 9,5% - синкопальные состояния (приступы потери сознания). По мере прогрессирования заболевания частота пароксизмальных состояний нарастала. Чаще они наблюдались у больных с клиническими проявлениями недостаточности кровообращения в сосудах вертебрально-базилярной системы. Нередко данные состояния были обусловлены сочетанным или изолированным воздействием на позвоночные артерии компрессионных факторов, связанных с изменениями шейного отдела позвоночника (остеохондроз, остеоартроз, спондилез). У 47,6% пациентов наблюдались вестибулярные нарушения, которые при дисциркуляции в вертебрально-базилярном бассейне артерий проявлялись системным головокружением, иногда с тошнотой. У этих больных отмечалась неустойчивость при ходьбе, определялся нистагм и координаторные нарушения. | Анализ статистически значимых зависимостей осуществляли с помощью параметрического t-критерия Стьюдента для зависимых и независимых групп. При ненормальном распределении вычисляли медиану и квартили. Сравнение этих данных проведено с использованием критериев Вилкоксона и Манна - Уитни. Различия считали статистически значимыми при р<0,05. |
| Большое значение в диагностике ДЭ имеют результаты МРТ- или КТ-исследования. При этом визуализировалась атрофия белого вещества головного мозга, особенно в подкорковой области и лобных долях, с формированием гидроцефалии, преимущественно внутренней с расширением объема желудочков мозга. Часто выявлялись рассеянные очаги глиоза и демиелинизации: в начале заболевания - единичные, при выраженном процессе - множественные с формированием перивентрикулярного лейкоареоза. Нередко просматривались лакуны после перенесенных микроинфарктов мозга и криблюры. При УЗДГ определялась извитость артерий, стенозы различной степени выраженности, аномалии расположения крупных артерий шеи и головного мозга. | Клинически псевдобульбарный синдром проявлялся у 28,6% обследованных больных нарушениями речи по типу дизартрии, дисфагией, эпизодами насильственного смеха или плача, оживлением нижнечелюстного рефлекса, симптомом Маринеску - Радовичи, слюнотечением. Голос становился тихим, глухим, монотонным, с носовым оттенком. |
| Экспертным методом на основании результатов клинико-статистических исследований частоты встречаемости признаков ДЭ у больных с тяжелым и легким течением заболевания разработана шкала количественной оценки заболевания, которая включает 20 признаков (каждый со значением от 3 до 15 баллов). В шкалу включены органические признаки: пирамидные, когнитивные, координаторные, зрительные, амиостатические нарушения, гиперкинетический, вестибулярный, синкопальный, бульбарный и неврастенический синдромы, степень артериальной гипертенизии, а также данные нейровизуализации и УЗДГ. При этом учитывали клиническое значение признаков. Наибольшую оценку получили такие наиболее значимые клинические признаки, как когнитивные нарушения (15 баллов), пирамидные и экстрапирамидные симптомы (14 баллов) и нарушения функции тазовых органов (15 баллов). Следует отметить, что в процессе лечения такие синдромы, как гипертензивный, неврастенический, атактический, вестибулярный и амиостатический, лучше корригировались. Однако степень выраженности пирамидного и псевдобульбарного синдромов, когнитивных нарушений и КТ-, МРТ-признаков практически не менялась. Кроме частоты встречаемости признаков у больных до и после проводимого лечения нами определена количественная оценка выраженности ДЭ в процессе лечения с помощью разработанной шкалы. Общая клиническая оценка выраженности ДЭ у больных основной группы в процессе лечения снизилась с 22 ± 3,1 балла до 14 ± 2,7 балла (р<0,01), в контрольной - с 21 ± 2,6 балла до 18 ± 2,1 балла (р<0,05). Исследования микроэлементного состава крови выполнены у 11 пациентов основной и 10 - контрольной группы. Как видно на рис. 1, в цельной крови пациентов с ДЭ в обеих группах на момент госпитализации установлено существенное снижение содержания кальция, железа, цинка и лития по сравнению со здоровыми лицами, что может усугублять напряженность антиокислительных систем и поддерживать состояние эндотелиальной дисфункции при ХИМ. | Шкала количественной оценки заболевания позволяет оценить выраженность ДЭ, а также проводить сравнительную оценку эффективности методов лечения с вычислением статистических показателей. |
| Уменьшение содержания кальция в крови приводит к нарушению его трансмембранного транспорта и изменению функциональной активности митохондрий с последующим развитием энергодефицита и индукцией апоптоза [5]. В то же время сохранение у больных с ДЭ нормального уровня магния, конкурирующего с кальцием за места связывания со структурами мишеней, поддерживает, скорее всего, адаптивно-компенсаторные процессы в организме, направленные на активацию механизмов нейропротекции. Известно, что существенно сниженный или повышенный уровень железа способствует усилению процессов свободнорадикального окисления в мозге. Выраженное снижение содержания железа в крови больных ДЭ, с одной стороны, может приводить к снижению энергетического потенциала клеток и повышенному риску развития инсульта, а с другой - способствовать избыточному накоплению нейротоксичных металлов (алюминия, марганца, свинца, кадмия) в ЦНС, что во многом определяет патогенетическую структуру развития нейродегенерации, когнитивных нарушений и деменции у больных ДЭ [11]. У всех обследованных больных ДЭ обраружено снижение уровня цинка в крови. Так как цинк и медь формируют металл-содержащие кластеры в каталитическом центре СОД, то уменьшение их концентрации в организме способствует падению антиокислительного потенциала. Снижение содержания лития в крови у больных с ДЭ может свидетельствовать о нарушении обмена нейромедиаторов при ХИМ. Анализ данных, полученных в основной группе больных ДЭ после комплексной терапии с включением Мексидола, указывает на тенденцию к возрастанию содержания железа, цинка и лития в крови относительно данных, полученных до лечения (рис. 1). |
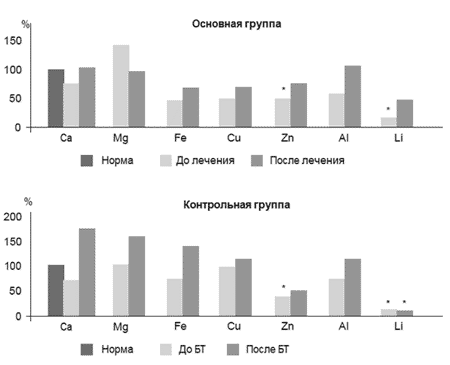
Рис. 1. Изменения содержания микроэлементов в крови у пациентов с ДЭ в основной и контрольной группах
Примечания:
* - различия статистически значимы по сравнению со здоровыми лицами (р<0,05);
БТ - базисная терапия.
| Так, уровень железа достигал 67%, цинка - 75%, лития - 43% от нормы. В то же время в контрольной группе больных ДЭ, получавших базисную терапию, не выявлено значимых изменений в содержании цинка и лития в крови. Можно предположить, что один из механизмов действия Мексидола, обеспечивающих увеличение содержания цинка и лития в крови при церебральной гипоксии, обусловлен способностью этого препарата стабилизировать биологические мембраны, повышать активность ферментов антиокислительной системы и снижать агрессивное действие окислителей на ткани. Это подтверждается результатами не только экспериментальных, но и наших предыдущих клинических исследований. Анализ данных, полученных после лечения, показал позитивный вклад Мексидола в составе комплексной терапии в динамику показателей АОС, что подтверждает не только важную роль развития окислительного стресса в патогенезе ХИМ, но и возможность эффективной коррекции дефицита эндогенных антиоксидантов при использовании указанного препарата [7]. Как было установлено нами ранее, применение Мексидола у кроликов в реперфузионном периоде после моделирования острой церебральной ишемии также оказывало положительное влияние на содержание ряда биоэлементов крови, скорее всего, благодаря его антигипоксическому и антиоксидантному свойствам [8]. Показано, что для исследования цереброваскулярной реактивности оптимальной областью регистрации являются кожные покровы лба, что обусловлено наличием анастомозов между сосудами наружной и внутренней сонных артерий. Это позволяет по изменениям кожного кровотока, регистрируемого в лобной области, косвенно судить о динамике церебральной микрогемоциркуляции. При проведении функциональной пробы с ЗД у 23 больных с ДЭ в 43% случаев (10 человек) установлена адекватная, но недостаточная реакция на гиперкапнию с возрастанием МС спекл-оптической кривой на 12% во время ЗД (в норме не менее 20%) и тенденцией к уменьшению этого показателя кожной МГД до 17% после окончания пробы в течение 30 с (рис. 2). |
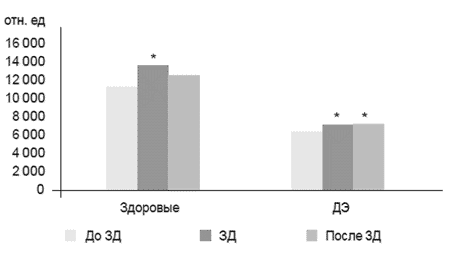
Примечание: * - достоверность различий по отношению к исходным данным.
| В 57% случаев (13 человек) реакция на ЗД оценивалась как неадекватная со снижением МС на 19%. В периоде восстановления дыхания у этих больных регресс МС уменьшился до 13%. Позитивное влияние комплексной терапии с включением Мексидола проявлялось возрастанием количества больных ДЭ с адекватной реакцией кожного кровотока на гиперкапнию до 70% (16 человек) при тенденции к улучшению фоновой микрогемоциркуляции кожных покровов лба, что выражалось в возрастании МС на 12%. При этом показатели сосудистой реактивности улучшались, приближаясь к нормальным данным и составляя 19% прироста значений МС во время ЗД с тенденцией к незначительному снижению в периоде восстановления дыхания (табл. 1). |
Таблица 1 Спекл-оптическая характеристика кожного кровотока у больных ДЭ с адекватной реакцией на проведение пробы с ЗД до и после лечения (медиана и квартили)
| Функциональные пробы | До ЗД | Во время ЗД | После ЗД |
| Контрольная группа | |||
| До лечения, n=11 | 9406 (7842; 12698) | 10552 (8544; 11341) р=0,03 | 8777 (8210; 9399) |
| После лечения, n=11 | 11943 (11780; 12343) | 12279 (10477; 13365) р=0,04 | 12173 (11026; 12490) |
| Основная группа | |||
| До лечения, n=10 | 6320 (4890; 9177) | 7113 (5721; 10065) р=0,00014 | 7111 (5281; 10585) р=0,004 |
| После лечения, n=16 | 7081 (5519; 8594) | 8451 (6650; 10776) р=0,0033 | 8347 (5920; 10047) р=0,0003 |
| В отличие от пациентов основной группы у 11 больных с адекватной реакцией на ЗД после базисной терапии наблюдали только тенденцию к улучшению фоновой МГД с увеличением МС на 12% (р>0,05) без существенного влияния на состояние вазодилататорных механизмов сосудистой реактивности (табл. 1). Cпекл-оптическими исследованиями реактивности сосудов кожных покровов с оценкой вазоконстрикторного резерва при проведении функциональной пробы с ГВ адекватная сосудистая реакция на гипокапнию выявлена у всех пациентов с ДЭ, из которых в 32% наблюдений реакция была достаточной (значения МС были снижены от 20% до 45%), в остальных случаях (68%) - недостаточной (сдвиг значений МС колебался от 4% до 18%). Установлено, что до проведения базисной терапии в ответ на ГВ при суммарной оценке изменений МС снизилась на 16% с последующим возрастанием показателя до исходных значений в постгипервентиляционном периоде. После лечения не наблюдали нормализации сосудистых эффектов на гипокапнию: регресс значений МС в ответ на ГВ после лечения составил всего 8% (табл. 2). | У лиц с неадекватной реакцией сосудов на гиперкапнию не установлено изменений спекл-оптических показателей фонового кровотока и сосудистой реактивности после лечения, что может свидетельствовать о формировании у них более выраженных функционально-структурных изменений и регуляторных нарушений с развитием парадоксальных сосудистых реакций и снижением эффекта от проводимого лечения. |
Таблица 2 Спекл-оптическая характеристика кожного кровотока у больных ДЭ с адекватной реакцией на проведение пробы с ГВ до и после лечения (медиана и квартили)
| Функциональные пробы | До ГВ | Во время ГВ | После ГВ |
| Контрольная группа | |||
| До лечения, n=11 | 7455 (6381; 8283) | 6385 (5599; 7075) p=0,0001 | 7009 (5460; 7696) |
| После лечения, n=11 | 6637 (6200; 8048) | 6123 (5671; 7327) p=0,0006 | 6712 (6145; 7194) |
| Основная группа | |||
| До лечения, n=21 | 8946 (8013; 9781) | 7957 (7453; 8051) p=0,018 | 7765 (7217; 10248) |
| После лечения, n=21 | 8304 (6962; 10063) | 5724 (5489; 8453) р=0,037 | 6895 (5474; 7446) р=0,037 |
| У 21 больного основной группы до лечения регресс значений МС во время ГВ составил 11% с дальнейшим уменьшением показателя после окончания пробы до 13%. В 2 случаях динамики исследуемых показателей при проведении теста с ГВ не отмечено. После комплексной терапии с включением Мексидола при суммарной оценке сосудистой реактивности на гипокапнию в целом наблюдалась достаточная реакция со снижением МС во время ГВ на 31%. Причем в 44% случаев диапазон изменений колебался в пределах 20-46%, а в 56% случаев реакция оценена как адекватная недостаточная: регресс значений МС во время ГВ составил 10,68 ± 4,34%. При оценке динамики изучаемых параметров во время проведения теста выявлено, что направленность изменений МС в периоде восстановления дыхания была аналогична той, которая регистрировалась у здоровых лиц. Следовательно, выявленные особенности сосудистых реакций кожных покровов области лба на функциональные дыхательные пробы у пациентов с ДЭ косвенно отражают снижение цереброваскулярной реактивности с ограничением резервов вазоконстрикции и особенно вазодилатации. Это свидетельствует о нарушении механизмов ауторегуляции мозгового кровообращения у больных ДЭ. Использование в комплексной терапии Мексидола улучшало МГД с увеличением емкости микрогемоциркуляторного русла и оказывало позитивный эффект на вазодилататорный и вазоконстрикторный компоненты цереброваскулярной реактивности, что проявилось не только нормализацией изучаемых реакций в большинстве случаев, но и увеличением лиц с адекватными и достаточными реакциями на гипер- и гипокапнию. Заключение Применение Мексидола в комплексной терапии больных с ДЭ способствует коррекции содержания железа, цинка и лития в крови, увеличению емкости микроциркуляторного русла с позитивным влиянием на состояние цереброваскулярной реактивности, что уменьшает выраженность неврологической симптоматики. ЛИТЕРАТУРА |
