Оценка эффективности вакцины Ваксигрип у школьников в период одного прививочного сезона
Статьи

Ваксигрип
Пневмо 23
|
№4 (22) Июль-август 2002 г.
Оценка эффективности вакцины Ваксигрип у школьников в период одного прививочного сезона Е.И. Бурцева1, А.Л. Заплатников2, Л.Н. Власова1, В.Т.Иванова1, Е.С. Шевченко1, В.И. Далечин2, Г.А. Мингалимова2, Н.А. Коровина2, А.Н. Слепушкин1 Как известно, в структуре заболеваемости гриппом и ОРВИ дети школьного возраста составляют большинство. Они также играют ведущую роль в распространении вирусных инфекций среди контактирующих с ними лиц [5, 9]. В ряде стран именно эта возрастная группа является приоритетной для проведения профилактики гриппа с помощью вакцин [8]. В последние годы и в России тактика вакцинации была переориентирована на особо нуждающиеся в защите категории лиц, среди которых школьники отнесены к группе населения "высокого риска заражения" гриппом. В России имеется широкий выбор гриппозных вакцин, представленный как отечественными (живые и инактивированные), так и зарубежными препаратами (инактивированные), среди которых расщепленная вакцина Ваксигрип (Авентис Пастер, Франция) входит в число наиболее иммунногенных препаратов [3]. Однако при оценке эпидемиологической эффективности вакцин авторам не всегда удавалось использовать весь спектр диагностических подходов для подтверждения гриппозной инфекции, в том числе вирусологические и серологические исследования. Кроме того, еще недостаточно изучен защитный потенциал поствакцинального иммунитета в течение одного календарного года после завершенной прививки, что имеет значение в условиях современного эпидемического процесса при гриппе. Цель данного исследования заключалась в определении защитной эффективности вакцины Ваксигрип у детей школьного возраста в периоды различной активности вирусов гриппа А и В. Настоящее наблюдение является продолжением исследования, начатого в сезоне 2000-2001 гг. Организационно-методическая часть подробно была описана ранее [4]. В коллективе детей одной из школ были сформированы 2 группы наблюдения: часть из них была привита вакциной Ваксигрип, другая была отнесена к контрольной группе. К моменту продолжения работы численность групп составляла 42 и 40 человек соответственно.
Таблица 1. Степень инфицированности детей школьного возраста в течение 1 года после иммунизации вакциной Ваксигрип
При оценке эффективности вакцинации был рассмотрен ряд показателей, включающих заболеваемость по данным клинических диагнозов и лабораторной диагностики гриппозной инфекции. Изучена также динамика изменений и уровни поствакцинального иммунитета. Клинический диагноз "грипп" ставили при наличии у заболевшего ряда симптомов: повышения температуры выше 38,0oС, головной боли, общего недомогания, последующего развития катаральных явлений и др. Изоляцию вирусов гриппа из носоглоточных смывов заболевших детей проводили в культуре клеток МДСК по ранее описанной методике [1]. При типировании выделенных изолятов использовали стандартный метод - реакцию торможения гемагглютинации (РТГА) с набором специфических иммунных сывороток. Для изучения уровня и динамики специфических антител к вирусам гриппа у детей были взяты парные образцы крови через 1 и 12 месяцев после вакцинации. Обработку и титрование сывороток проводили общепринятыми методами в РТГА и лектин-тесте, которыми определяли уровень специфических антител к гемагглютинину (анти-ГА) и нейраминидазе (анти-НА) соответственно. В реакциях были использованы антигены вирусов гриппа, подобные вакцинным штаммам эпидемического сезона 2000-2001 гг. - А/Новая Каледония/20/99 (H1N1), А/Панама/2007/99 (H3N2) и В/Сычуань/379/99.
Таблица 2. Динамика специфических антител к поверхностным белкам вирусов гриппа А и В у детей школьного возраста с различным прививочным анамнезом
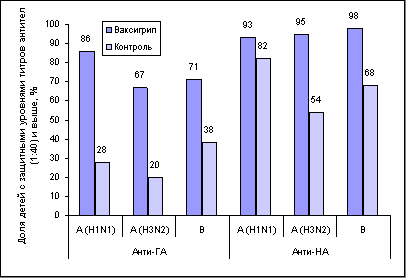
Проводили расчет уровней средних геометрических титров антител (СГТ), удельный вес детей с защитными титрами антител (1:40 и выше), а также выявляли диагностические приросты титров антител в парных сыворотках. Результаты, полученные в группах наблюдения, сравнивали расчетом показателей среднего квадратичного отклонения (M±2m) и критерия достоверности Стьюдента (t). В представленных ранее результатах изучения иммуногенных возможностей вакцины Ваксигрип в отношении гемагглютининов и нейраминидаз вакцинных вирусов нами была подтверждена ее высокая активность и комплексность ответа [4]. Наблюдение, начатое в эпидемическом сезоне 2000-2001 гг., было продолжено до следующего сезона с изучением анализа заболеваемости детей на протяжении 1 года после вакцинации. В период эпидемического подъема заболеваемости среди детей обеих групп наблюдения был зарегистрирован 21 (17,7%) эпизод респираторной инфекции, 5 (4,2%) из которых были подтверждены с помощью лабораторных методов как гриппозная инфекция. От 14 детей были взяты носоглоточные смывы для изоляции вирусов гриппа и определения их штаммовой принадлежности. В середине апреля было выделено 3 штамма вируса гриппа В, подобных вакцинному (В/Сычуань/379/99). При этом результаты распределились следующим образом: в группе привитых вакциной Ваксигрип вирусы были выделены в 2 случаях из 10, у детей контрольной группы - у 1 из 4 детей. Все случаи были подтверждены серологически. Таким образом, показатели заболеваемости гриппозной инфекцией регистрировали не часто, и в целом в группах наблюдения они составили: у привитых вакциной Ваксигрип - 3,0% и детей контрольной группы - 3,8%. Учитывая низкую интенсивность эпидемической заболеваемости гриппом в коллективе, в определенной степени обусловленной наличием высокой иммунной прослойки (более 80%), возникшей вследствие вакцинации, а также циркуляцией разновидности вируса гриппа В предшествующих 2 сезонов, представляло интерес оценить уровни инфицированности детей в обеих группах. В табл. 1 представлены показатели инфицированности детей за два временных промежутка - периоды эпидемической активности и межэпидемической циркуляции вирусов гриппа. При предшествующем титровании парных сывороток в период с января по апрель 2001 г. в группе детей, привитых вакциной Ваксигрип, серологические маркеры инфицирования вирусами гриппа были отмечены у 8 (12,1%) детей. Практически у всех из них (7 случаев) была диагностирована В-вирусная инфекция, а в 1 случае - инфицирование вирусом гриппа А(H1N1). В то же время, среди непривитых детей этот показатель был значительно выше и составил 30,8%. У 11 детей имели место диагностические приросты титров антител к вирусу гриппа В, у 4 - к вирусу гриппа А(H1N1) и у одного школьника регистрировали микст-инфекцию обоими вирусами гриппа. В период межэпидемической циркуляции вирусов гриппа были также получены некоторые различия по уровню инфицированности привитых и непривитых детей, показатели в которых составили 2,4% и 10,0% соответственно. В этот период диагностические приросты титров антител регистрировали ко всем 3 циркулирующим вирусам гриппа, что очень характерно при смене эпидемической активности вирусов гриппа А(H1N1) и В в сезоне 2000-2001 гг. на В и А(H3N2) - в сезоне 2001-2002 гг. Таким образом, уровни инфицированности привитых и детей контрольной группы за весь период наблюдения составили в целом 14,5% и 40,8% соответственно. Индекс эффективности вакцины Ваксигрип в отношении защиты от инфицирования составил 2,8, коэффициент эффективности - 64,0%, при достоверной разнице полученных показателей (t - 3,3). Определенный интерес представляло сравнить уровни специфических антител у детей с клинически выраженным гриппом, детей только с лабораторными признаками перенесенной инфекции и средними показателями в целом в наблюдаемых группах. Так среди привитых вакциной Ваксигрип уровни анти-ГА составили 1:80 у детей с клинически выраженной инфекцией и 1:193 у детей только с серологическими признаками перенесенной инфекции, а уровни анти-НА - 1:60 и 1:300 соответственно. В целом по группе эти показатели составили 1:223 - 1:338 и 1:75 - 1:479 соответственно. Таким образом, можно предположить корреляцию форм инфекции (клинически выраженная и инфицирование) с уровнями специфических антител к обоим поверхностным белкам. Рис. Уровни защищенности к вирусам гриппа А и В детей с различным прививочным анамнезом
В контрольной группе прослеживаются те же тенденции, однако уровни показателей были значительно ниже, чем в группе вакцинированных. Это могло послужить причиной большей инфицированности гриппом этих детей в период его циркуляции в коллективе. Уровни анти-ГА и анти-НА у детей с клинически выраженными формами составляли 1:120 и 1:22, у детей с бессимптомной инфекцией - 1:49 и 1:80 соответственно. Средние показатели в целом по группе были 1:56 - 1:91 и 1:53- 1:91. Изучение динамики специфических антител в течение года после вакцинации позволило оценить длительность и эффективность поствакцинального иммунитета у привитых. В табл. 2 представлены показатели уровней СГТ анти-ГА и анти-НА парных сывороток через 1 и 12 месяцев после вакцинации. Из общего числа обследованных сывороток при подсчете были исключены образцы, ранее имевшие диагностические приросты титров антител. В группе привитых вакциной Ваксигрип наметилась явная тенденция к статистически значимому снижению показателей СГТ, более выраженная в отношении антинейраминидазных антител. В тоже время, в контрольной группе регистрировали даже некоторое повышение показателей СГТ к вирусам гриппа А(H1N1) и A(H3N2), что косвенно подтверждает циркуляцию этих вирусов за анализируемый период и о чем уже упоминалось ранее. При этом разница между показателями СГТ в сравниваемых группах оставалась статистически достоверной. Обращают на себя внимание более высокие титры антинейраминидазных антител, чем антител к гемагглютинину в обеих группах наблюдения, что, возможно, обусловило выявленные различия между показателями инфицированности и частоте клинически выраженных форм заболевания. Как известно, нейраминидазные антитела препятствуют развитию инфекционного процесса, снижая тяжесть заболевания и развитие осложнений [6]. При этом, необходимо учесть, что в последние годы вирусы гриппа в меньшей степени подвержены антигенной изменчивости и соответственно число лиц, имеющих специфические антитела к эпидемическим или вакцинным вирусам, с годами накапливается, обеспечивая высокую иммунную прослойку. Этим можно объяснить и небольшую разницу по уровням анти-НА к вирусу гриппа А(H1N1) между сравниваемыми группами. Кроме того, в межэпидемический период были зарегистрированы случаи инфицирования этим вирусом детей контрольной группы, в которой наметился рост уровней СГТ антител к обоим поверхностным белкам. В обсуждении полученных результатов следует также учесть ряд особенностей эпидемического процесса гриппозной инфекции, которые могли повлиять на результативность оценки эффективности вакцинации. Как отмечалось ранее, у детей в течение года наблюдения были выявлены диагностические приросты титров антител ко всем 3 циркулирующим вирусам гриппа. Это является подтверждением одной из особенностей эпидемического процесса при гриппе. В последние годы более часто подъемы заболеваемости были обусловлены одновременной или последовательной циркуляцией штаммов вируса гриппа 2-3 серотипов в пределах одного сезона, что и определяло растянутость и невысокий уровень эпидемий. При этом, выделенные от заболевших детей вирусы являлись ранее циркулировавшими антигенными вариантами (все эталоны были зарегистрированы в 1999 г.), а значит, дети школьного возраста, вероятнее всего, уже имели контакт с ними до проведения настоящих исследований. Этим можно объяснить достаточно высокие уровни антител к нейраминидазному белку как менее подверженному изменчивости и высокие показатели инфицированности детей по сравнению с числом случаев клинических форм заболеваний. По показателям контрольной группы это соотношение составило 8:1. В ряде работ, в которых также обсуждается этот вопрос, авторы указывают, что только в 19-34% случаев инфицирование вирусом гриппа В приводит к развитию заболевания [10]. При этом, отмечается тот факт, что размножение вируса может не происходить у лиц с "пограничным" иммунным статусом, уровень которого определяется индивидуально. Обобщая полученные результаты, можно сделать вывод о том, что вакцина Ваксигрип является высокоиммуногенным препаратом и обеспечивает сохранение специфических титров антител к обоим поверхностным белкам в течение одного года после прививки. Статистически значимое снижение уровней СГТ анти-ГА и анти-НА у детей через один год после вакцинации в некоторой степени определяет целесообразность ежегодной вакцинации. Особенно это важно при смене штаммового состава гриппозных вакцин, проводимой при появлении новых антигенных вариантов вирусов гриппа. Так в рекомендованном ВОЗ составе гриппозных вакцин на эпидемический сезон 2002-2003 гг. вирус гриппа В/Сычуань/379/99-подобный заменен на В/Гонконг/330/2001- подобный. Как показали предварительные исследования, у детей раннего возраста и школьников практически отсутствуют антитела к этому вирусу, что необходимо учитывать при подготовке к следующему эпидемическому сезону. Важно также отметить, что защитная эффективность вакцины Ваксигрип была подтверждена в отношении 3-х циркулировавших вирусов гриппа в периоды их эпидемической и межэпидемической активности: суммарный индекс эффективности составил 2,8; коэффициент эффективности - 64,0%.
Литература
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||