Место Кеторолака в терапии острых болевых синдромов на догоспитальном этапе
СтатьиОпубликовано в журнале:
«Врач Скорой помощи», 2006, № 6, с. 1-6
А.Л.Верткин, А.В.Тополянский, Е.И.Вовк, А.В.Наумов
Наиболее частой причиной обращения больных за неотложной медицинской помощью, в том числе требующей проведения обезболивания, остается болевой синдром. Так, по данным S.McLean и соавт. (2002 г.), среди 14,5 млн. экстренных обращений умеренный болевой синдром был выявлен у двух млн. пациентов (14% случаев), выраженный - у 2,9 (20%). W.Cordell и соавт. (2002 г.) считают, что именно боль является причиной обращения пациентов за неотложной медицинской помощью в 52% случаев. В России, по данным Национального научно-практического общества скорой медицинской помощи (ННПОСМП), за последние 3 года количество вызовов скорой медицинской помощи (СМП) по поводу острых и хронических болевых синдромов возросло почти на 25%.
В то же время, согласно данным литературы, обезболивание получают не все пациенты, которые в нем нуждаются. J.Wilson и J.Pendleton (1989 г.), при ретроспективном исследовании обнаружили, что из 198 пациентов, обратившихся за помощью в связи с острой болью, только 44% получили аналгезию в отделении неотложной терапии. Из них 62% ждали обезболивания больше 1 ч и в 32% случаев анальгетики применялись в недостаточных дозах. Поданным S.McLean и соавт. (2002 г.), адекватное лечение проведено только 21% пациентов, нуждавшихся в экстренном обезболивании. И даже в тех случаях, когда обезболивание проводят в рамках неотложной терапии, оно далеко не всегда оказывается эффективным. Причинами этого могут быть использование малоэффективных лекарственных средств, стандартные, либо устаревшие схемы их применения, рефрактерность пациентов, особенно часто использующих анальгетики, побочные эффекты и др. (А.Е.Жуков и соавт., 2002).
Врач скорой помощи чаще всего является первым врачом, к которому обращается больной с болью. Традиционно обезболивание на догоспитальном этапе проводят метамизолом натрия (анальгин). Так в Москве частота его использования при купировании боли составила 86%, а в других регионах России - 88%. При этом применение метамизола натрия, особенно повторное, может вызывать развитие тяжелых нежелательных эффектов, таких как гематотоксический, развитие анафилактического шока, что значительно повышает риск лечения. Другие нестероидные противовоспалительные препараты (НПВП), а их только на российском рынке представлено 570 наименований («Федеральное руководство по использованию лекарственных средств», выпуск 5, 2004), используются значительно реже.
В данной публикации мы осветим дифференцированный подход к назначению современных лекарственных препаратов для терапии острой боли на догоспитальном этапе.
Боль - это субъективный феномен, включающий ощущение, указывающее на повреждение или угрозу повреждения тканей и аффективную реакцию на это ощущение.
Неприятные ощущения приводят к специфическому поведению больного и появлению вегетативных реакций, что позволяет врачу заключить, что пациент испытывает боль. Эмоциональная же реакция больного вызывает страдания, которые в зависимости от длительности болевого ощущения имеют разную клиническую характеристику (табл.1).
Таблица 1. Клиническая характеристика боли.
| Боль | Определение | Вегетативные реакции | Эмоциональные реакции |
| Острая | Необходимый биологический сигнал о нарушении целостности организма; кратковременна | Бледность или покраснение лица, холодный пот, расширенные зрачки, тахикардия, повышение АД, изменение ритма дыхания, рвота | Агрессия, тревога |
| Хроническая | Сохраняется более 3-6 мес, теряет свое приспособительное биологическое значение | Утомляемость, нарушение сна, снижение аппетита, потеря массы тела, снижение либидо, запоры | Депрессия |
Выраженность болевого синдрома определяется рядом факторов: длительностью влияния травмирующего агента на психическую и соматическую сферы; конституциональными, генетическими и психологическими особенностями пациентов; чувством страха и тревоги; степенью самоконтроля пациентом боли и болезни; качеством социальной поддержки; знанием пациентом признаков реакции на боль, причин ее вызвавших, ее значения и последствии; депрессивными реакциями (возникающими как результат протекающего хронического заболевания)и др.
ДИАГНОСТИКА БОЛИ
Несмотря на объективность ее существования, боль всегда субъективна. Поэтому если пациент предъявляя жалобы на боль, не делает никаких попыток (явных или скрытых) избавится от нее, стоит усомниться в ее присутствии. Напротив, если пациент страдает от боли, он всегда это демонстрирует: либо окружающим, либо самому себе, либо стремится обратиться к врачу (IASP, 1992).
Для оценки интенсивности болевого синдрома и эффективности проводимой терапии существует несколько способов (табл.2). Наиболее распространенными являются визуально-аналоговая шкала (ВАШ) и шкала облегчения боли. При применении ВАШ больной отмечает уровень выраженности болевого синдрома на 100 мм шкале (где «0» - отсутствие боли, «100» - максимальная боль) до и через 20 мин после введения препарата.
Таблица 2. Способы градации интенсивности болевого синдрома.
| Способ | Градации боли | Когда используется |
| Пятизначная общая шкала | 0=нет боли 1=слабая (чуть-чуть) 2=умеренная(болит) 3=сильная(очень болит) 4=невыносимая (нельзя терпеть) | При оценке/обследовании в обычных условиях |
| Словесная количественная шкала | 0 5 10 Нет боли - невыносимая (Какое число соответствует вашей боли?) |
При оценке/обследовании в обычных условиях |
| Визуальная аналоговая шкала (линия 10 см, скользящая линейка | Нет боли - невыносимая (Отметьте на линии, насколько сильна ваша боль) | При оценке/обследовании в обычных условиях Может применяться у детей старше 6 лет |
| Поведенческие и психологические параметры (эти признаки следует принимать во внимание с осторожностью, т.к. они не являются специфичными) | Мимические гримасы, повышение голоса, бледность, потливость, слезотечение, расширение зрачка, тахикардия, гипертензия, дискоординация дыхания, др. | При оценке/обследовании больных в бессознательном состоянии, аутичных, критически больных пациентов |
| Оценка жизненно важных функций больного врачом | Может ли пациент осуществлять самостоятельно основные функции (например, кашель, глубокое дыхание) - Да/Нет | Соотнести с субъективными оценками. Следует использовать у всех |
Для оценки эффективности проведенного обезболивания используют шкалу облегчения боли. Через 20 мин после введения препарата пациенту задают вопрос: «Уменьшилась ли интенсивность боли у Вас после введения препарата, по сравнению с болью до введения препарата?». Возможные варианты ответа оценивают в баллах: 0 - боль нисколько не уменьшилась, 1 - немного уменьшилась, 2 - уменьшилась, 3 - сильно уменьшилась, 4 - исчезла полностью. Важно также оценивать время наступления отчетливого обезболивающего эффекта.
ЛЕЧЕНИЕ БОЛИ
Согласно современной стратегии лечения боли существуют несколько принципов назначения лекарственных средств:
- индивидуализированный - доза, способ введения, лекарственная форма определяются индивидуально (особенно у детей), с учетом интенсивности боли и на основании регулярного мониторинга;
- «лестницы» - ступенчатое обезболивание, при соблюдении унифицированных диагностических подходов;
- своевременности введения - интервал между введениями определяется степенью боли и фармакокинетическими особенностями действия препаратов и его лекарственной формы; возможно использование лекарственных средств длительного действия, которые, при необходимости, можно дополнять препаратами быстрого действия;
- адекватности способа введения - предпочтение оральному введению (наиболее простой, эффективный и наименее болезненный). Для выбора оптимального средства для обезболивания необходимо понимание принципиальной характеристики НПВП, учитывающей обезболивающую активность, избирательность в отношении циклооксигеназ (ЦОГ), биодоступность, возможность различных путей введения, быстроту достижения эффекта, отсутствие активных метаболитов, сбалансированное выведение и безопасность.
Согласно современной классификации (табл. 3) все НПВП делятся на анальгетики-антипиретики, производные парааминофенола, гетероарилуксусной, салициловой, фенилуксусной, пропионовой, антониловой кислот, оксикамы, коксибы и комбинированные препараты.
Таблица 3. Классификация НПВС (D.Laurens, P.Bennet, 1992 с дополнениями).
| Группа НПВС | Препараты |
| анальгетики - антипиретики | пиразолоны - метамизол натрия, аминофеназол |
| парааминофенола | фенацетин, парацетамол |
| гетероарилуксусной кислоты | кеторолак |
| салициловой кислоты | ацетилсалициловая кислота, дифлунисал, салицилат натрия |
| арилуксусной кислоты | диклофенак |
| арилпропионовой кислоты | ибупрофен, кетопрофен, флурбипрофен, индометацин |
| эноликовой кислоты | пироксикам, лорноксикам, мелоксикам |
| фенамовой кислоты | мефенамовая кислота |
| другие: набуметон,коксибы | целекоксиб |
| комбинированные препараты | артротек(диклофенак\мисопростол) |
Согласно принятым положениям, все НПВП обладают обезболивающим, жаропонижающим, противовоспалительным и антиагрегантным действием. При этом они существенно отличаются по профилю безопасности, поскольку могут обладать гастротоксическим, гепатотоксическим, нефротоксическим, гематотоксическим, неиротоксическим эффектами, вызывать аллергические реакции, оказывать негативное влияние на иммунную систему и гемостаз. Главным, определяющим действие НПВП является их специфичность в отношении ЦОГ При этом имеетзначениие возможность НПВП усиливать продукцию эндогенных опиоидов и прерывать проведение болевых импульсов в спинном мозге.
КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ НПВП ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ
Лекарственные формы для парентерального применения, именно те, которые используются в экстренной службе, имеют метамизол натрия, его комбинации со спазмолитиками и холиноблокаторами, диклофенак натрия, кеторолак и лорноксикам.
Сегодня мы обсудим использование кеторолака для лечения острых болевых синдромов на догоспитальном этапе.
Кеторолак - производное арилуксусной кислоты. Используется в виде трометаминовой соли, что увеличивает его растворимость в воде, при этом трометаминовая соль легко расщепляется, высвобождая кеторолак.
В Северной Америке, Великобритании, некоторых других европейских странах и Гонконге кеторолак является единственным парентеральным НПВП, используемым для лечения острого болевого синдрома. Показано, что при внутримышечном введении 30 мг препарат оказывает действие, сопоставимое с эффектом 10-12 мг морфина или 50 мг меперидина (C.Brown и соавт, 1990., D.Dula и соавт, 2001, S.Henderson и соавт, 2002., C.Kenny и соавт, 1990). Преимуществом кеторолака по сравнению с наркотическими анальгетиками является отсутствие влияния на функцию дыхания, седативного и психомоторного действия. Так, при послеоперационной боли кеторолак оказался в некоторых случаях даже эффективнее морфина и мепередина (D.McGuire и соавт, 1993), а такие побочные эффекты как тошнота и рвота встречались реже. По данным F.Barber, D.GIadu (1998 г.), кеторолак при внутримышечном введении по эффективности сравним с кодеином, но реже вызывает явления диспепсии. Аналогичные результаты получены и в ряде других исследований (C.Eberson и соавт, 1999, M.Lieh-Lai и соавт, 1999).
Кеторолак продемонстрировал высокую обезболивающую эффективность в целом ряде исследований (F.Barber, D.GIadu, 1998., D.McGuire и соавт, 1993, G.Larkin и соавт, 1999, C.Eberson и соавт, 1999, J.Perez-Urizar и соавт, 2000). По сравнению с другими НПВП, кеторолак по-видимому, оказывает более выраженное обезболивающее действие (V.Swadia, M.Shah, 1999).
Кеторолак является препаратом выбора для купирования интенсивной боли, особенно при травме, однако кратковременное его использование возможно и при обострении хронической боли: у пациентов с дегенеративно-дистрофическими заболеваниями позвоночника, ревматоидным артритом, остеоартрозом и т.д. Так, при выраженной боли в спине, по данным двойного-слепого, проспективного исследования, проведенного K.Veenema и соавт. (2000 г), эффективность кеторолака была сравнима с эффектами меперидина, а седативное действие и побочные эффекты были менее выражены.
В многоцентровом исследовании, проведенном G.lnnes и соавт. (1998 г.), обезболивающее действие кеторолака при боли в спине оказалось сравнимо с эффектами кодеина при значительно меньшем количестве неблагоприятных явлений. В то же время, по данным М.Neighbor и соавт. (1998 г.), однократное внутримышечное введение кеторолака в дозе 60 мг при острой боли сопоставимо по эффективности с приемом 800 мг ибупрофена.
При почечной колике внутривенное введение 30 мг кеторолака оказывало такой же обезболивающий эффект, как и внутривенное введение 2,5 г метамизола в комбинации со спазмолитиками при меньшем количестве побочных эффектов (C.Martin Carrasco и соавт., 1993). По данным E.Cohen и соавт. (1998 г.), проведших двойное слепое рандомизированное исследование, включавшее 57 пациентов с почечной коликой, обезболивающая активность кеторолака (30 мг внутримышечно) и диклофенака (75 мг внутримышечно) оказалась сопоставимой по выраженности и продолжительности.
В проспективном рандомизированном исследовании J.Nicolas Torralba и соавт. (1999 г.), включавшем 48 пациентов с почечной коликой, внутримышечное введение 30 мг кеторолака оказалось более эффективным, чем подкожное применение трамадола в дозе 1 мг/кг массы тела.
Согласно экспериментальным данным, кеторолак, блокируя синтез простагландинов в почке, уменьшает перистальтику мочевых путей и спазм, снижает давление в них, а также уменьшает почечный кровоток (A.Perlmutter и соавт, 1993 г.).
Кеторолак оказывает анальгетическое и жаропонижающее действие, противоспалительный эффект выражен незначительно. Его действие связано с подавлением активности циклооксигеназы, фермента, регулирующего синтез простагландинов, простациклина, тромбоксана А2 из арахидоновой кислоты. Кеторолак подавляет активность обеих форм циклооксигеназы (ЦОГ-1 и ЦОГ-2). Он не действует на опиатные рецепторы, поэтому не вызывает побочных реакций со стороны ЦНС, угнетения дыхания и пареза гладкой мускулатуры.
Препарат быстро всасывается, обладает высокой биодоступностью (80 - 100%), что обеспечивает быстрое наступление анальгезии. После приема внутрь 10 мг эффект развивается через 10 - 60 минут, после внутримышечного введения 30 мг - через 15 - 75 минут. Продолжительность действия у кеторолака до 10 часов.
Кеторолак связывается с белками плазмы крови на 90 - 99%. Он подвергается печеночному метаболизму, выводится почками (90%) и кишечником (6%). Период полувыведения у пожилых пациентов больше чем у молодых (4,7 - 8,6 часов и 3,8 - 6,3 часов, соответственно). Выведение препарата замедляется у больных с нарушенной функцией почек.
Применение кеторолака противопоказано при реакциях гиперчувствительности, гиповолемии, тяжелой почечной и печеночной недостаточности, пептических язвах, язвенной болезни желудка и двенадцатиперстной кишки, нарушениях гемостаза, беременности, родах, кормлении грудью, детям до 16 лет.
Частота развития побочных эффектов при применении кеторолака составляет 2,7%. Наиболее часто встречаются диспепсические симптомы. Тяжелые побочные симптомы: геморрагические осложнения, нарушение функции почек, острая анафилаксия - встречаются значительно реже.
Кеторолак выпускается в 2-х формах: таблетки для приема внутрь по 10 мг и раствор для парентерального введения в ампулах по 30 мг/1 мл.
СРАВНИТЕЛЬНАЯ ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ПРИМЕНЕНИЯ РАЗЛИЧНЫХ НПВП НА ДОГОСПИТАЛЬНОМ ЭТАПЕ
Систематического сравнительного анализа эффективности и безопасности парентерального применения на догоспитальном этапе НПВП не проводилось. Поэтому в рамках программы ННПОСМП было проведено первое сравнительное открытое многоцентровое контролируемое клиническое исследование эффективности и безопасности парентерального применения на догоспитальном этапе метамизола натрия, диклофенака натрия, кеторолака и лорноксикама при болевых синдромах различного происхождения.
В исследование включали пациентов старше 18 лет с острой болью или обострением хронического болевого синдрома при воспалительных заболеваниях суставов, дегенеративно-дистрофических заболеваниях позвоночника (артралгии, люмбаго, ишалгия и т.д.), посттравматическими болевыми синдромами, почечной коликой.
Критериями исключения были возраст менее 18 лет, беременность, лактация, реакция гиперчувствительности на НПВП (в том числе на анальгин, аспирин) в анамнезе, заболевания системы кроветворения, язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения, застойная сердечная недостаточность, бронхиальная астма, выраженные нарушения функции печени и/или почек, систолическое артериальное давление ниже 100 мм рт. ст., проводимая в момент исследования антибиотикотерапия фторхинолонами или макролидами.
Всего в исследовании приняли участие 1011 больных, средний возраст которых составил 54,1 ±0,46 года, в том числе 498 мужчин и 513 женщин. На догоспитальном этапе внутримышечно вводили метамизол натрия (2 мл 50% раствора внутримышечно), диклофенак (3 мл - 75 мг внутримышечно), или кеторолак (препарат Кеторол производства компании «Д-р Редди'с Лабораторис Лтд»30мг/1 мл внутримышечно), или лорноксикам (8 мг/2 мл внутримышечно).
В зависимости от проведенной терапии больные были разделены на 5 сопоставимых групп: 240 больных (средний возраст 57,51 ±0,9 года) составили группу приема метамизола, 153 пациента (средний возраст - 54,17±1,1 года) - диклофенака натрия, 318 пациентов (средний возраст 51,68±0,9 года) - кеторолака, 95 пациентов (средний возраст 58,94±1,3 года) - лорноксикама.
Из принявших участие в исследовании 553 пациента (54,7%) обратились за неотложной помощью в связи со скелетно-мышечной болью, 244 (24,1 %) - по поводу травмы, 214 (21,2%) - с почечной коликой.
При скелетно-мышечной боли ее уменьшение наступало через 20 мин после внутримышечного введения НПВП. Средняя разница интенсивности боли до и после лечения, оцененная с помощью ВАШ, в группе метамизола составила 52,7±1,8, диклофенака - 57,7±4,6, кеторолака - 69,3±1,9, лорноксикама - 70,8±4,7.
По критериям ВАШ лучшей эффективностью обладал лорноксикам и кеторолак, худшей - метамизол; диклофенак занял промежуточное положение. Метамизол достоверно уступал диклофенаку (рРис. 1. Динамика интенсивности болевого синдрома через 20 мин после введения различных НПВП при использовании ВАШ (средняя разница показателей).
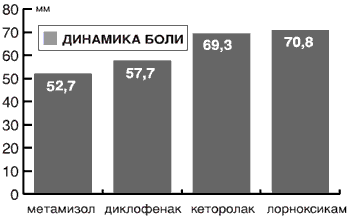
Согласно результатам оценки динамики болевого синдрома с использованием ВАШ кеторолак превосходит метамизол натрия в 1,3 раза.
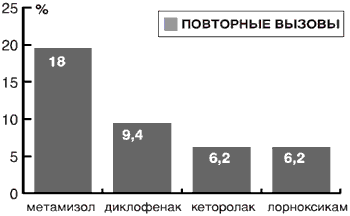
Повторные вызовы по поводу скелетно-мышечной боли были отмечены в 18% случаев в группе метамизола, в 9,4% - диклофенака, в 6,2%- кеторолака и лорноксикама (рис. 2). По количеству повторных вызовов препараты расположились следующим образом:
метамизол > диклофенак > кеторолак=лорноксикам.
Рис. 2. Частота повторных вызовов СМП при неэффективности НПВС
Важно отметить, что эффективность всех НПВП была одинаковой у больных моложе и старше 60 лет.
Метамизол приносил заметное уменьшение боли через 26,9±0,47 мин., диклофенак - 20,0±0,5 мин., кеторолак - 12,4±0,33 мин, лорноксикам -12,3±0,6 мин (рис. 3). По этому показателю метамизол достоверно (рРис. 3. Время развития отчетливого обезболивающего действия после внутримышечного введения НПВП.
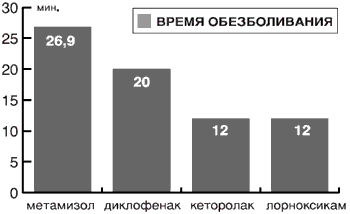
Таким образом, по скорости наступления отчетливого обезболивающего действия препараты распределились так:
лорноксикам = кеторолак > диклофенак > метамизол.
Средняя разница интенсивности боли, возникшей в связи с травмой до и после лечения, оцененная с помощью ВАШ, в группе метамизола составила 58,9±3,0, диклофенака - 60,0±4,6, кеторолака - 77,8±1,9, лорноксикама - 68,0±4,7 (рис. 4). По этому показателю метамизол достоверно не отличался от диклофенака, но достоверно уступал кеторолаку и лорноксикаму (РРис. 4. Динамика интенсивности посттравматической боли через 20 мин после введения различных НПВП при использовании ВАШ (средняя разница показателей).
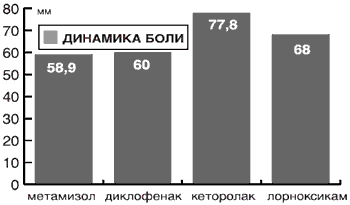
Таким образом, согласно оценке динамики боли с помощью ВАШ, по силе обезболивающего действия при травме исследуемые препараты можно расположить так:
кеторолак > лорноксикам > диклофенак = метамизол.
Оценка снижения интенсивности болевого синдрома при почечной колике с использованием ВАШ также показала преимущество использования кеторолака перед метамизолом.
Таким образом, по силе обезболивающего действия при почечной колике исследуемые препараты можно расположить так:
кеторолак > метамизол.
Различные обезболивающие средства по-разному переносились больными. Среди системных нежелательных явлений наиболее часто встречались дискомфорт в эпигастрии, сонливость, головокружение, анорексия, чаще они наблюдались после использования метамизола. Следует отметить, что случаев аллергических реакций и повышения кровоточивости (естественно без учета возможных побочных явлений на отдаленном этапе) в нашем исследовании не зарегистрировано, т.е. однократное применение всех исследуемых препаратов представляется вполне безопасным. В то же время, применение метамизола в 32 случаях и диклофенака - в 11 случаях вызывало местные реакции - боль в месте инъекции. Кроме того, зарегистрирован один случай развития некроза в месте инъекции после применения диклофенака и два случая возникновения инфильтратов после инъекций метамизола. После введения метамизола 5 пациентов беспокоила тошнота, у 4 отмечалась сонливость, у 5 - дискомфорт в эпигастрии.
Рис. 5. Динамика интенсивности боли при почечной колике через 20 мин после введения различных НПВП при использовании ВАШ (средняя разница показателей).
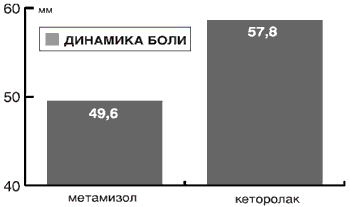
ВЫВОДЫ.
Приведённые результаты свидетельствуют о целесообразности использования кеторолака на догоспитальном этапе лечения острой боли, причём кеторолак (Кеторол) является наиболее эффективным при травме и острой скелетно-мышечной боли в сравнении с другими анальгетиками и НПВП. Применение метамизола не оправдано с позиций эффективность/безопасность.
Фармакоэкономический анализ применения различных обезболивающих средств на догоспитальном этапе.
| Показатель | Метамизол (анальгин) n=240 | Диклофенак (вольтарен) n=153 | Кеторолак (кеторол) n=318 | Лорноксикам(ксефокам) n=95 |
| Количество единиц лекарства | 1 амп. (2 мл 50% раствора) | 1 амп. (3 мл, 75 мг) | 1 амп. (1 мл, 30 мг) | 1 фл. (8 мг) |
| Стоимость единицы лекарства (руб.) | 0,63 | 36,36 | 10,86 | 97,23 |
| Количество повторных вызовов | 32 | 9 | 11 | 3 |
| Стоимость повторных вызовов, руб. | 25600 | 7200 | 8800 | 2700 |
| Общая стоимость лечения, руб. | 25751,2 | 12763,08 | 12253,48 | 11936,85 |
| Средние затраты на одного пациента (С), руб. |
107,29 | 83,42 | 38,53 | 125,65 |
| Эффективность (Ef)* | 67,9% | 69,9% | 82,4% | 87% |
| Затраты на единицу эффективности (СЕА=С/Ef), руб |
1,58 | 1,19 | 0,46 | 1,44 |
Примечания: * – критерий эффективности лечения – уменьшение интенсивности болевого синдрома не менее, чем на 50%.


