Эффективность внутрипортальных инфузий мексидола при лечении механической желтухи
Статьи Опубликовано в журнале:«Хирургия» »» №9, 2009
А.Н. БЕЛЯЕВ, Е.И. МОКШИНА, С.А. БЕЛЯЕВ, Д.В. МЕЛЬНИКОВА, С.В. КОСТИН, С.И. ХВОСТУНОВ, М.Н. БУХАРКИН
Кафедра общей хирургии и анестезиологии им. Н.И. Атясова (зав. - проф. А.Н. Беляев) Мордовского государственного университета им. Н.П. Огарева, Саранск
Ключевые слова: механическая желтуха, внутрипортальные инфузии, мексидол.
A.N. BELYAEV, E.I. MOKSHINA, S.A. BELYAEV, D.V. MELNIKOVA, S.V. KOSTIN, S.I. KHVOSTUNOV, M.N. BUKHARKIN
Key words: obstructive jaundice, intraportal infusions, mexidols:
Большая частота осложнений и значительная летальность при механической желтухе (МЖ), достигающая в послеоперационном периоде 20-40% [7], составляют важную проблему современной хирургии.
У больных с обтурационной желтухой наиболее опасным и частым осложнением в послеоперационном периоде является печеночная недостаточность. Исследования последних лет в гепатологии заметно улучшили понимание процессов, происходящих в печени при механической желтухе [8, 10, 12] и на их основе предложено новые методы медикаментозной коррекции ее морфо-функционального состояния. С этой целью применяют широкий арсенал медикаментозных препаратов, влияющие на белковосинтезирующую, детоксицирующую, гемостатическую и другие функции печени [5, 6, 11, 13].
В профилактике и комплексной терапии острой печеночной недостаточности находят применение антиоксиданты, в частности мексидол, обладающий широким спектром биологической активности. Он эффективен при разных видах гипоксии, повышая устойчивость организма к кислородзависимым патологическим состояниям [2], стабилизирует липидный бислой сарколеммы гепатоцитов в условиях активации ПОЛ и лимитирует трансмембранный перенос ионов кальция из внеклеточного пространства.
Однако при тяжелой интоксикации комплексная терапия, включающая антиоксиданты, не всегда оказывается эффективной, что в немалой степени связана с недостаточной концентрацией лекарственных препаратов, попадающих в поврежденный орган. Это касается и печени, когда при внутривенной инфузионной терапии лекарственные препараты, пройдя через легочный капиллярный фильтр, достигают точку приложения эффекта в недостаточной лечебной концентрации. Одним из эффективных и доступных методов регионарной медикаментозной коррекции нарушений морфофункционального состояния печени при МЖ является внутри -портальный метод инфузионной терапии, позволяющий доставлять в печень лекарственные препараты высокой концентрации [3, 4, 9].
Целью настоящей работы была оценка процессов перекисного окисления липидов и функциональной активности печени при системном (внутривенном) и регионарном (внутрипортальном) введении мексидола в лечении механической желтухи.
Материал и методы
Выполнены эксперименты на 40 беспородных собаках под тиопентал-натриевым наркозом (45 мг/кг). В зависимости от характера проведенного лечения и состава инфузионных сред экспериментальные животные были распределены на 5 серий (табл. 1).
В 1-й серии экспериментов проводили моделирование механической желтухи путём наложения лигатурной перетяжки на общий желчный проток. Удаление лигатуры (декомпрессия холедоха) проводилось на 3-и сутки после моделирования механической желтухи.
Таблица 1. Краткое содержание экспериментального материала
| Серия | Количество животных | Инфузионная среда и способ введения |
| 1-я | 8 | Моделирование механической желтухи (без лечения) |
| 2-я | 8 | Внутривенно 0,9% раствор хлорида натрия (ФР), 20 мл/кг |
| 3-я | 8 | Внутривенно ФР (10 мл/кг) и внутрипортально ФР (10 мл /кг) |
| 4-я | 8 | Внутривенно ФР (20 мл/кг) + мексидол (7 мг/кг) |
| 5-я | 8 | Внутривенно ФР (10 мл/кг) и внутрипортально ФР (10 мл/кг) + мексидол (7 мг/кг) |
Во 2-й серии сразу после выполнения декомпрессии желчевыводящих путей проводили внутривенное введение 0,9% раствора натрия хлорида (физиологического раствора - ФР) в объеме 20 мл/кг. В 3-й серии экспериментов, после декомпрессии холедоха, инфузионная терапия включала внутривенное (10 мл/кг) и внутрипортальное (10 мл/кг) введение ФР.
В 4-й и 5-й сериях проводилось изучение влияния внутривенного и внутрипортального введения мексидола (7 мг/кг). Препарат растворяли в 0,9% растворе натрия хлорида, при этом способы его введения и общий объем вводимых сред (20 мл/кг) был сопоставим с предыдущими сериями.
В асептических условиях при ревизии подпеченочного пространства в толще печеночно-двенадцатиперстной связке находили общий желчный проток и с помощью лигатурной иглы проводили под ним лигатуру. Концы лигатуры продевали через полихлорвиниловую трубку и затягивали на перпендикулярно расположенной второй трубке до такой степени, чтобы полностью перекрыть просвет холедоха, моделируя, таким образом, механическую желтуху.
На 3-и сутки эксперимента (на высоте биохимических изменений), после выполнения релапаратомии проводили удаление лигатурной перетяжки, восстанавливая тем самым пассаж желчи в двенадцатиперстную кишку. Затем катетеризировали портальную вену через ветвь брыжеечной вены (рацпредложение №101 от 01.04.03). Экспериментальных животных наблюдали в течение 10 дней. Для проведения биохимических исследований кровь забирали ежедневно. Выведение животных из эксперимента осуществлялось путём струйного введения тиопентала натрия.
Определение активности аспартатаминотранферазы (АсАТ) и аланинаминотрансферазы (АлАТ), щелочной фосфатазы (ЩФ), содержание общего билирубина и его фракций, мочевины, общего белка и его фракций, креатинина, общих липидов, три-ацилглицеридов (ТАГ), общего холестерина, α-холестерина и ß-липопротеидов (ß-ЛП) плазмы крови проводили стандартными унифицированными методами, принятыми в клинической и лабораторной практике (В.В. Меньшиков, 1987; А.И. Карпищенко, 1999). Активность каталазы плазмы определяли по М.А. Королюк (1988). Уровень малонового диальдегида (МДА) в плазме крови определяли по С.Г. Конюховой (1989). Про- и антиоксидантный статус организма изучали на основании анализа показателей интенсивности свечения индуцированной хемилюминесценции плазмы крови (S, Imax и I /Smax).
Свечение регистрировали на биохемилюминометре БХЛ-06 (НПФ аналитического приборостроения «Люмекс», Санкт-Петербург). При этом Imax отражает потенциальную способность биологического объекта к ПОЛ, а площадь под кривой (S) - буферную емкость антиоксидантной системы.
Полученные при исследовании данные обрабатывали методом вариационной статистики с использованием критерия Фишера-Стьюдента. Для изучавшихся параметров вычисляли среднее арифметическое выборочной совокупности (М), ошибку средней арифметической (m). Достоверность различий определяли в каждой серии по отношению к значению на 3-и сутки эксперимента (р). При этом различия средних величин признавались статистически достоверными при уровне значимости 95% (р<0,05).
Результаты и обсуждение
У всех экспериментальных животных с первых суток обтурации холедоха наблюдалось повышение уровня общего билирубина. На 3-и сутки содержание его в плазме возрастало с 7,08±0,47 до 288,33±6,99 мкмоль/л (что в 40,7 раза больше исходного значения; р<0,001). Было также отмечено значительное нарушение белоксинтезирующей функции печени со снижением уровня общего белка на 37,4%. Наряду с этим наблюдалось повышение активности внутриклеточных энзимов: величины АсАТ, АлАТ возрастали в 11 и 23 раза, ЩФ - в 4,9 раза по сравнению с исходными данными. Выявляемые изменения позволяют утверждать о развитии выраженного холестатического, цитолитического и мезенхимально-воспалительного синдромов, характеризующие данное состояние как механическую желтуху.
При исследовании прооксидантно-антиоксидантного статуса организма отмечена резкая интенсификация процессов свободнорадикального окисления, подтверждаемая данными биохемилюминометрического анализа плазмы. Показатель максимальной интенсивности индуцированной биохемилюминисценции (Imax) прогрессивно возрастал, составляя на 3-и сутки 286,05% (p<0,001) относительно исходного уровня. Содержание МДА на 3-и сутки увеличивалось в 4,3 раза (р<0,001).Реакцией на усиление липопероксидации явилось повышение на 3-и сутки показателя S - до 265,65% (p<0,001)
Высокий уровень реакций пероксидации сопровождался выраженными нарушениями липидного обмена. Уровень общих липидов плазмы крови значительно повышался, составляя на 3-и сутки 199,1% (p<0,05). Увеличение содержания липидной фракции крови происходило в основном за счет повышения концентрации общего холестерина и р-ЛП. В целом выявляемые изменения гомеостаза позволяли утверждать о развитии в организме состояния, характеризующегося как оксидативный стресс, требующего соответствующей фармакологической коррекции.
Выполнение 2-й и 3-й серий экспериментов было обусловлено необходимостью изучения влияния инфузии 0,9% раствора NaCl (растворителя мексидола, используемого для его парентерального введения) на функциональное состояние печени и процессы липопероксидации при механической желтухе (с целью сравнения эффективности применения мексидола).
Выявлено, что применение 0,9% раствора NaCl в объеме 20 мл/кг в обеих сериях в основном корригировало волемические расстройства гомеостаза. По сравнению с результатами 1-й серии экспериментов на 7-е сутки значимо уменьшалось содержание общего билирубина (в 3,6 раза; p<0,001), АсАТ (в 3,1 раза; p<0,01), АлАТ (в 3,0 раза; p<0,001), ЩФ (в 2,1 раза; p<0,01). Состояние внутренней среды организма характеризовалось незначительным снижением интенсивности липопероксидации с одновременным прогрессирующим истощением активности антиоксидантной системы. Содержание МДА снижалось до уровня 375,2%, Imax - до уровня 192,9% (p<0,001) относительно исходных величин, Активность каталазы на 7-е сутки составляла 79,6%, величина S увеличивалось до 282% (p<0,001). При сравнительном анализе эффективности внутривенного и внутрипортального путей введения ФР при механической желтухе выявлено отсутствие каких либо значительных и достоверных различий. Таким образом, анализ изучаемых показателей позволяет сделать вывод о том, что при применении ФР (внутривенно и внутрипортально) не достигалось значимого восстановления функциональной активности печени.
Внутривенное введение мексидола при внепеченочном холестазе сопровождалось существенной положительной динамикой большинства исследуемых показателей. Исходя из результатов проводимого лечения в четыре серии экспериментов, отмечена выраженная способность мексидола снижать интенсивность холестатического (снижение уровня ЩФ в 2,8 раза, билирубина - в 30,2 раза (p<0,001), холестерина - в 1,6 раза, (p<0,05) и цитолитического синдромов (понижение активности АсАТ и АлАТ - в 6,4 раза; p<0,001)
Проведение внутривенных инфузий мексидола существенно угнетало процессы перекисного окисления липидов (уменьшение значений МДА и Imax в 1,7 раза) (см. рисунок). Одновременно с этим значительно повышались величины показателя S - в 1,7 раза (p<0,01), активности каталазы - в 1,6 раза (p<0,05). Содержание общих липидов снижалось в 1,3 раза (p<0,05), общего холестерина - в 1,6 раза, при этом оставаясь на уровне 201 и 155,8% относительно исходных значений. Отмечалось однонаправленное уменьшение концентрации р-ЛП и ТАГ до уровня 114,8% (p>0,05) и 150,8% (p<0,05).
Смена пути введения мексидола с внутривенного на внутрипортальный характеризовалась большей степенью нормализации большинства изучаемых показателей. Наиболее существенному изменению подверглось содержание общего билирубина, которое к концу эксперимента приближалось к исходному уровню (табл. 2). Ликвидация холестаза и проведение инфузионной терапии в 5-й серии сопровождались уменьшением в 4,6 раза активности ЩФ, концентрация которой соответствовала нормальным величинам.
На фоне проводимой внутрипортальной терапии мексидолом происходило значительное восстановление трансаминазной активности крови со снижением уровня АлАТ в 16,07 раза, АсАТ - в 10 раз (см. табл. 2).
Важным моментом в лечении явилось восстановление баланса прооксидантно-антиоксидантного статуса организма. В ответ на внутрипортальное введение мексидола содержание каталазы в печени увеличивалась с 52,6 до 166,5% (p<0,001) относительно исходного состояния, что приводило к повышению ее активности в системном кровотоке до 83,0% (p<0,001). При хемолюминесцентном анализе гомогената печени выявлено снижение значения Imax в 3,5 раза (p<0,05), в системном кровотоке - в 1,7 раза (p<0,01). Концентрация МДА в ткани печени снижалась в 1,8 раза, в оттекающей крови - в 2,1 раза (p<0,01).
Рисунок. Сравнительная динамика концентрации малонового диальдегида
при внепеченочном холестазе на фоне внутривенной и внутрипортальной
инфузии мексидола
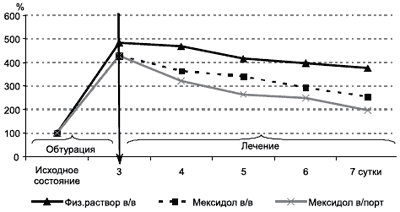
Снижение свободнорадикальной активности и активация антиоксидантной системы сочетались с нормализацией показателей липидного обмена. При внутрипортальном введении мексидола содержание липидной фракции венозной крови уменьшалось в 1,7 раза (p<0,05) в основном за счет снижения концентрации общей фракции холестерина (в 2,1 раза) и ß-ЛП (в 1,5 раза). Содержание липидных фракций в крови после проведения внутрипортальной терапии мексидолом приближалось к исходным значениям
Таблица 2. Показатели функциональной активности печени при внепеченочном холестазе и после внутрипортальных инфузий мексидола, n=8 (М±m)
| Показатель | Этапы эксперимента, сутки | |||||
| Исходно | 3-и | 4-е | 5-е | 6-е | 7-е | |
| ЩФ, нмоль/с·л | 331,25±20,04 | 1575,00±82,07 | 1275,19±74,91 (р<0,05) |
812,17±93,92 (р<0,001) |
578,12±105,43 (р<0,001) |
341,12±99,20 (р<0,001) |
| АсАТ, мкмоль/мл·ч | 0,20±0,03 | 2,29±0,19 | 1,23±0,23 (р<0,01) |
0,86±0,09 (р<0,001) |
0,41±0,21 (р<0,001) |
0,23±0,15 (р<0,001) |
| АлАТ, мкмоль/мл·ч | 0,21±0,03 | 4,34±0,32 | 2,45±0,20 (р<0,001) |
1,21±0,14 (р<0,001) |
0,78±0,16 (р<0,001) |
0,27±0,11 (р<0,001) |
| Общий билирубин, мкмоль/л | 7,36±0,57 | 298,75±2,99 | 122,81±48,11 (р<0,01) |
29,76±15,73 (р<0,001) |
10,34±1,84 (р<0,001) |
8,01±0,96 (р<0,001) |
| Прямой билирубин, мкмоль/л | 6,09±0,06 | 257,50±0,78 | 106,26±7,58 (р<0,001) |
25,51±2,50 (р<0,001) |
8,89±0,16 (р<0,001) |
6,61±0,07 (р<0,001) |
Полученные результаты позволяют говорить о высокой способности мексидола корригировать нарушения гомеостаза, развивающиеся при синдроме механической желтухи. Наиболее существенным фармакологическим действием мексидола является блокада процессов перекисного окисления липидов и активация антиоксидантных ферментов с улучшением физико-химических свойств клеточной мембраны и возрастанием ее текучести. Эти изменения при механической желтухе способствуют значительному уменьшению цитолитических процессов и повышению функциональной активности гепатоцитов. В большей степени ингибирующее влияние на свободнорадикальные реакции в печени мексидол оказывает при внутрипортальном пути его введения, что проявляется более значительным гепатопротекторным эффектом и повышением ее функциональной активности.
Список использованной литературы
