Оптимизация терапии энтеровирусного менингита на фоне герпетических инфекций у детей
Статьи Опубликовано в журнале:«Детские инфекции»; № 3; 2009; стр. 62-67.
Э. Н. Симованьян, Л. Ф. Бовтало, В. Б. Денисенко, М. А. Ким, И. Г. Крюкчиева, В. А. Новиков
ГОУ ВПО Ростовский государственный медицинский университет Росздрава Ростов-на-Дону
Обследованы 50 детей в возрасте от 1 месяца до 10 лет с энтеровирусным менингитом. У больных с активной формой герпес-вирусных инфекций (22 человека; 44%) энтеровирусный менингит характеруется тяжелым продолжительным течением, частым развитием осложнений и остаточных явлений. Назначение изопринозина (инозина пранобекс) способствовует сокращению длительности заболевания, уменьшению частоты осложнений и остаточных явлений.
Ключевые слова: энтеровирусный менингит, герпесвирусные инфекции, дети, изопринозин (инозин пранобекс)
УДК 616.022:578.833.26-08
Optimization therapy of enteroviral meningitis with herpetic infections in children
E. N. Simovanian, L. F. Bovtalo, V. B. Denisenko, M. A. Kim, I. G. Kriukchiyeva, V. A. Novikov
State Educational Institution of Higher Professional Education Rostov State Medical University of Roszdrav, Rostov-on-Don
50 children aged 1 month — 10 years old with enteroviral meningitis were examined. In patients with active viral herpes infections (22 patients, 44%) enteroviral meningitis was characterized by aggravated prolonged clinical course, frequent complications and residual effects. Prescription of inosine pranobex helps to reduce the clinical course of the disease, to lower the frequency of complications and residual effects.
Key words: enteroviral meningitis, viral herpes infections, children, inosine pranobex
Удельный вес серозных менингитов в структуре инфекционных заболеваний нервной системы достигает 70% [1,2]. Наиболее частыми этиологическими агентами серозных менингитов являются энтеровирусы (60—90%) [3, 4]. В последние годы в нашей стране наблюдается увеличение заболеваемости энтеровирусными менингитами (ЭМ), которые регистрируются в виде локальных вспышек или спорадических заболеваний, преимущественно в летне-осенний сезон [5]. Клинически ЭМ характеризуются преобладанием общемозговых и менингеальных симптомов, волнообразным течением, длительной санацией ликвора, частым развитием осложнений и остаточных явлений (до 30%) [1, 3, 4]. Одним из факторов, определяющих негладкое течение ЭМ, является формирование микст-инфекции. Широкое эпидемическое распространение герпесвирусных инфекций (ГВИ), пожизненная персистенция возбудителей в организме человека с возможной реактивацией, иммунодепрессивная активность, нейротропизм дают основание предположить участие этих возбудителей в развитии ассоциированной инфекции [1, 6, 7]. Вместе с тем, частота, особенности клинического течения, исходы энтеровирусно-герпесвирусной микст-инфекции до настоящего времени остаются неизученными.
Неблагоприятное течение ЭМ, частое развитие осложнений и остаточных явлений диктуют необходимость разработки новых подходов к лечению данного заболевания [1, 3, 4]. Перспективным направлением совершенствования этиотропной терапии ЭМ, протекающего в форме моно- и микст-инфекции, представляется использование препарата изопринозин (инозин пранобекс) производства Teva Pharmaceutical Industries Ltd. ИП обладает широким спектром противовирусной активности, оказывает положительное влияние на параметры иммунного ответа по клеточному и гуморальному типам, функциональную активность факторов врожденной резистентности, улучшает обменные процессы в пораженных клетках, хорошо проникает через гематоэнцефалический барьер [7, 8]. В последние годы доказана противовирусная активность изопринозина в отношении энтеровирусов и герпесвирусов [7, 9].
Цель исследования — охарактеризовать влияние герпесвирусных инфекций на особенности течения энтеровирусного менингита у детей и оценить эффективность программы комплексной терапии с использованием инозина пранобекс (изопринозина).
Материалы и методы исследования
Под нашим наблюдением находились 50 детей от 1 месяца до 10 лет с ЭМ. Критериями диагностики заболевания являлись клинико-лабораторные данные, обнаружение РНК энтеровирусов в ликворе методом полимеразной цепной реакции (ПЦР, тест-системы «Амплисенс Enterovirus 207», Россия), достоверное нарастание титра антител к энтеровирусам в парных сыворотках в реакции нейтрализации.
Клинические методы включали анализ анамнестических данных и осмотр больных в динамике. У всех пациентов методом иммуноферментного анализа (ИФА) исследовали серологические маркеры ГВИ, в том числе для вируса простого герпеса (ВПГ) 1 и 2 типов — IgM, IgG, авидность IgG, для вируса Эпштейна-Барр (ВЭБ) — IgM к VCA, IgG к EA, IgG к EBNA, авидность IgG, для цитомегаловируса (ЦМВ) — IgM и IgG к ЦМВ, IgM и IgG к IEA-антигену, авидность IgG. Мочу и слюну тестировали на наличие цитомегалических клеток (ЦМК). В крови и ликворе методом ПЦР определяли ДНК ВПГ, ВЭБ, ЦМВ (тест-системы «Ампли-сенс», Россия). У всех детей были получены отрицательные результаты обследования ликвора на ДНК герпесвирусов, что свидетельствовало об участии только энтеровирусов в поражении мягких мозговых оболочек. Маркерами активности ГВИ считали наличие цитомегалических клеток (ЦМК) в моче и слюне, ДНК герпесвирусов в крови, IgM и низкую авидность IgG (индекс авидности менее 30%) ко всем герпесвирусам, IgM и IgG к IEA-антигену ЦМВ, IgM к VCA- и IgG к EA-антигенам ВЭБ.
С учетом результатов обследования все больные были разделены на три группы. В первую группу вошли 22 ребенка (44%) с маркерами активной ГВИ (50%). У 16 пациентов этой группы (72,7%) имели место маркеры активности ЦМВ, у 13 — ВПГ (59,1%), у 11 человек — ВЭБ (50%). Активная герпесвирусная моноинфекция выявлена у 6 детей (27,3%), смешанная ГВИ — у 16 больных (72,7%). Вторую группу составили 10 пациентов (20%) с неактивной формой ГВИ, третью группу — 1 8 больных без лабораторных маркеров ГВИ (36%).
Всем детям назначали комплексное лечение, включавшее строгий постельный режим до санации ликвора, лечебное питание, дезинтоксикационную терапию, мочегонные препараты, вазоактивные нейрометаболиты, ноотропы, витамины группы В, рекомбинантный интерферон α-2 в форме ректальных свечей в возрастной дозе в течение 7—10 дней. Методом случайной выборки все пациенты были разделены на две группы, оказавшиеся сопоставимыми по возрасту и клинико-лабораторным показателям на момент начала лечения. Больным опытной группы (25 человек; 50%) помимо стандартной терапии назначали изопринозин в дозе 50—100 мг/кг/сут в 3—4 приема внутрь в течение 10 дней. Дети контрольной группы (25 пациентов; 50%) получали только стандартную терапию.
Статистическую обработку полученных данных проводили с помощью компьютерной программы «Statistica 6.0». Для оценки достоверности различий абсолютных величин использовали критерий Манна-Уитни, для относительных показателей использовали метод Фишера.
Результаты и их обсуждение
Среди больных ЭМ преобладали пациенты в возрасте 3 — 10 лет — 35 человек (70%). У детей в возрасте от 1 месяца до 3 лет заболевание возникало значительно реже (15 больных, 30%; р <0,05). Вместе с тем, именно в этой группе маркеры активной ГВИ встречались наиболее часто (табл. 1).
Таблица 1.
Возрастной состав и состояние преморбидного фона больных энтеровирусным менингитом с учетом активности герпесвирусных инфекций
| Показатели | Активная ГВИ | Неактивная ГВИ | Без ГВИ | |||
| n | % | n | % | n | % | |
| Возраст: | ||||||
| 1—3 года | 10 | 45,5* | 3 | 30 | 2 | 11 |
| 3 — 10 лет | 12 | 54,5* | 7 | 70 | 16 | 88,9 |
| Фоновые состояния: | ||||||
| Отягощенный акушерский анамнез | 19 | 86,4* | 6 | 60 | 10 | 55,5 |
| Внутриутробные инфекции | 9 | 40,9* | 3 | 30 | — | — |
| Перинатальное поражение ЦНС | 18 | 81,8* | 5 | 50 | 9 | 50 |
| Частые ОРЗ | 16 | 72,7* | 5 | 50 | 7 | 38,9 |
| Аллергические заболевания | 11 | 50* | 2 | 20 | 3 | 16,7 |
| Всего | 22 | 100 | 10 | 100 | 18 | 100 |
ЭМ у большинства больных развивался на отягощенном преморбидном фоне. У 70% матерей имел место отягощенный акушерский анамнез (хроническая гинекологическая патология, гестоз, угроза прерывания беременности, гестационный пиелонефрит, преждевременные роды и др.). У 24% пациентов в постнатальном периоде диагностирована внутриутробная инфекция, у 62% — перинатальное поражение ЦНС. К группе часто болеющих относились 56% детей, аллергической патологией страдали 32% больных. Частота фоновых состояний в группе с активной ГВИ была более высокой.
У большинства детей (76%) ЭМ начинался остро, реже — постепенно (24%). Основной симптомокомплекс включал сочетание общеинфекционного, общемозгового, менингеального, катарального и лимфопролиферативного синдромов. Лихорадка имела место у подавляющего большинства больных (94%). У 76% пациентов она имела фебрильный характер, у 18% детей отмечался субфебрилитет. В клинической симптоматике доминировал общемозговой синдром. Головная боль наблюдалась у 88% больных, рвота — у 80%, гиперестезия — у 68%, различная степень нарушения сознания — у 60% пациентов. У 32% детей на догоспитальном этапе возникли кратковременные тонико-клонические судороги. У всех пациентов выявлен менингеальный синдром, однако развернутый характер он имел только у 66% больных, в то время как у остальных детей он был неполным или диссоциированным. При неврологическом обследовании у 36% больных обнаружены кратковременные очаговые знаки — анизорефлексия, клонусоид, поражение лицевого и глазодвигательных нервов. У 82% пациентов имел место катаральный синдром по типу ринофарингита, герпангины. У 64% детей выявлен лимфопролиферативный синдром, включавший генерализованную лимфаденопатию (64%), реже — увеличение печени (26%) и селезенки (4%). Отек головного мозга (ОГМ) 2—3 степени развился у 42% пациентов. При исследовании ликворограммы у 74% детей обнаружен лимфоцитарный плеоцитоз (в среднем 205,5 ± 43,3 кл/мкл). У 26% больных он имел нейтрофильный или смешанный характер, однако в дальнейшем среди клеток преобладали лимфоциты. У 60% пациентов обнаружено умеренное увеличение содержания белка в ликворе (в среднем 0,6 ± 0,1 г/л), у остальных детей этот показатель оставался в пределах нормы или был сниженным.
У больных с активной формой ГВИ имела место более яркая клиническая симптоматика ЭМ по сравнению с детьми, не инфицированными герпесвирусами (табл. 2). Этих пациентов чаще беспокоили фебрильная лихорадка, головная боль, рвота, гиперестезия. На догоспитальном этапе у половины больных возникали судороги. При поступлении в стационар состояние большинства детей расценено как тяжелое, при объективном обследовании выявлены нарушение сознания, развернутый менингеальный синдром, очаговые знаки. У всех больных обнаружена генерализованная лимфаденопатия, у 36,4% — гепатомегалия, у 9,1% — увеличение селезенки. К особенностям клинической симптоматики относилось наличие кардиального (врожденные пороки сердца, вегето-сосудистая дистония и др.) и гастроинтестинального синдромов (аномалии развития и функциональные заболевания желудочно-кишечного тракта). У более половины детей развился ОГМ 2—3 степени. Уровень плеоцитоза (399,1 ± 36,7 кл/мкл) превышал аналогичные показатели у детей с неактивной ГВИ и у не инфицированных герпесвирусами (221,4 ± 71,6 кл/мкл и 104,7 ± 20,6 кл/мкл соответственно; р < 0,05). Среднее содержание белка в ликворе (0,6 ± 0,1 г/л) было более высоким, чем у больных с неактивной ГВИ и у пациентов без ГВИ (0,3 ± 0,03 г/л и 0,2 ± 0,05 г/л соответственно; р < 0,05).
Таблица 2.
Клиническая характеристика энтеровирусного менингита с учетом активности герпесвирусных инфекций
| Показатели | Активная ГВИ | Неактивная ГВИ | Без ГВИ | |||
| n | % | n | % | n | % | |
| Начало заболевания: | ||||||
| Острое | 16 | 72,7 | 7 | 70 | 15 | 83,3 |
| Постепенное | 6 | 27,3 | 3 | 30 | 3 | 16,7 |
| Состояние при поступлении: | ||||||
| Среднетяжелое | 5 | 22,7* | 6 | 60 | 10 | 55,6 |
| Тяжелое | 17 | 77,3* | 4 | 40 | 8 | 44,4 |
| Лихорадка | 21 | 95,4 | 9 | 90 | 17 | 94,4 |
| Субфебрильная | 1 | 4,5* | 2 | 20 | 6 | 33,3 |
| Фебрильная | 20 | 90,9* | 7 | 70 | 11 | 61,1 |
| Головная боль | 22 | 100* | 8 | 80 | 14 | 77,8 |
| Рвота | 21 | 95,4* | 7 | 70 | 12 | 66,7 |
| Гиперестезия | 18 | 81,8* | 7 | 70 | 9 | 50 |
| Нарушение сознания | 18 | 81,8* | 5 | 50 | 7 | 38,8 |
| Менингеальный синдром | 22 | 100 | 10 | 100 | 18 | 100 |
| Развернутый | 18 | 81,8* | 6 | 60 | 9 | 50 |
| Неполный, диссоциированный | 4 | 18,2* | 4 | 40 | 9 | 50 |
| Судороги | 11 | 50* | 3 | 30 | 2 | 11,1 |
| Очаговые знаки | 13 | 59,1* | 3 | 30 | 2 | 11,1 |
| Катаральный синдром | 18 | 81,8 | 8 | 80 | 15 | 83,3 |
| Лимфопролиферативный синдром | 22 | 100* | 6 | 40 | 4 | 22,2 |
| Кардиальный синдром | 7 | 31,8* | 1 | 10 | 1 | 5,5 |
| Гастроинтестинальный синдром | 8 | 36,4* | 1 | 10 | 1 | 5,5 |
| Осложнения: | 13 | 59,1* | 5 | 50 | 3 | 16,7 |
| Отек мозга 2—3 степени | 13 | 59,1* | 5 | 50 | 3 | 16,7 |
| Всего | 22 | 100 | 10 | 100 | 18 | 100 |
Динамическое наблюдение за детьми, получавшими стандартную терапию, показало, что у пациентов с активной ГВИ происходило увеличение продолжительности лихорадки, менингеального и катарального синдромов, сроков санации ликвора (табл. 3). Поздние осложнения (отит, синусит, нейропатия лицевого нерва и др.) чаще возникали при активной ГВИ (у 4-х из 1 1 пациентов), реже — у больных с неактивной ГВИ (у 1 -го из 5-ти больных) и у не инфицированных герпесвирусами (у 2-х из 9-ти человек). К моменту выписки из стационара остаточные явления имели место у 6-ти детей с активной ГВИ. У 5-ти пациентов диагностирован церебрастенический синдром, у 3-х— гипертензионный синдром, у 1-го ребенка — синдром очаговых нарушений. У остальных пациентов остаточные явления возникали реже — у 2-х человек с неактивной ГВИ и у 2-х больных, не инфицированных герпесвирусами. У детей этих групп развивался только церебрастенический синдром.
Таблица 3.
Продолжительность симптомов энтеровирусного менингита у детей, получавших стандартную терапию, с учетом активности герпесвирусной инфекции (дней)
| Показатели | Активная ГВИ | Неактивная ГВИ | Без ГВИ |
| Лихорадка | 8,6 ± 1* | 6,3 ± 0,8 | 5 ± 0,5 |
| Головная боль | 3,6 ± 0,6 | 3,1 ± 0,4 | 3 ± 0,4 |
| Рвота | 2,5 ± 0,4 | 2 ± 0,5 | 2,1 ± 0,5 |
| Гиперестезия | 2,2 ± 0,4 | 1,9 ± 0,5 | 1,8 ± 0,4 |
| Нарушение сознания | 2 ± 0,5 | 1,6 ± 0,4 | 1,5 ± 0,5 |
| Менингеальный синдром | 5,7 ± 0,5* | 4 ± 0,7 | 3,1 ± 0,2 |
| Катаральный синдром | 8,4 ± 1* | 4,7 ± 0,5 | 3,6 ± 0,5 |
| Изменения в ликворограмме | 16,8 ± 1,5* | 12,3 ± 1 | 1 1,1 ± 1,5 |
Сопоставление динамики клинических симптомов у детей, получавших различные схемы терапии, показало, что при использовании изопринозина происходило заметное сокращение продолжительности лихорадки, проявлений общемозгового синдрома (головной боли, рвоты, гиперестезии, нарушения сознания), менингеальных знаков, катаральных изменений в ротоглотке, отмечалась более быстрая санация ликвора (табл. 4). Частота поздних осложнений в этой группе (4%) была более низкой по сравнению со стандартной терапией (28%; р< 0,05). Назначение изопринозина способствовало снижению частоты остаточных явлений до 8% (в контрольной группе — 40%; р< 0,05). Побочные эффекты при использовании изопринозина отсутствовали.
Таблица 4.
Продолжительность симптомов энтеровирусного менингита у детей с учетом схемы терапии (дней)
| Показатели | Стандартная терапия + изопринозин | Стандартная терапия |
| Лихорадка | 3,5 ± 0,7* | 6,5 ± 0,5 |
| Головная боль | 2,3 ± 0,3* | 3,3 ± 0,3 |
| Рвота | 1,2 ± 0,3* | 2,2 ± 0,4 |
| Гиперестезия | 1 ± 0,2* | 2,1 ± 0,4 |
| Нарушение сознания | 0,8 ± 0,2* | 1,8 ± 0,3 |
| Менингеальный синдром | 3 ± 0,4* | 4,5 ± 0,5 |
| Катаральный синдром | 4,1 ± 0,4* | 6,7 ± 0,5 |
| Изменения в ликворограмме | 10,3 ± 1,1* | 14,3 ± 1 |
Таким образом, результаты проведенного исследования свидетельствуют о том, что основными факторами, определяющими неблагоприятное течение ЭМ у детей, являются высокая частота групп риска и наличие активной формы ГВИ (рис. 1). Они приводят к снижению системного и местного иммунитета, структурным нарушениям в ЦНС, повышению проницаемости гемато-энцефалического барьера [1, 7]. В результате при заражении энтеровирусами увеличивается продолжительность вирусемии, облегчается проникновение возбудителей через гемато-энцефалический барьер, развиваются значительные воспалительные изменения в мягких мозговых оболочках, отек головного мозга, гиперпродукция ликвора. Заболевание характеризуется появлением выраженных симптомов интоксикации, общемозговых симптомов, развернутого менингеального синдрома, судорог и очаговых знаков. Инфекционный процесс приобретает неблагоприятное течение, сопровождается увеличением продолжительности основных симптомов заболевания, сроков санации ликвора, частым развитием осложнений и остаточных явлений. В связи с этим больные из групп риска, с тяжелым негладким течением ЭМ, наличием полиорганной патологии нуждаются в углубленном обследовании с использованием методов ИФА, ПЦР и, при выявлении маркеров активной формы ГВИ, в назначении соответствующего лечения.
Рисунок 1. Патогенез энтеровирусного менингита у детей с активной формой герпесвирусной инфекции и механизм эффективности изопринозина
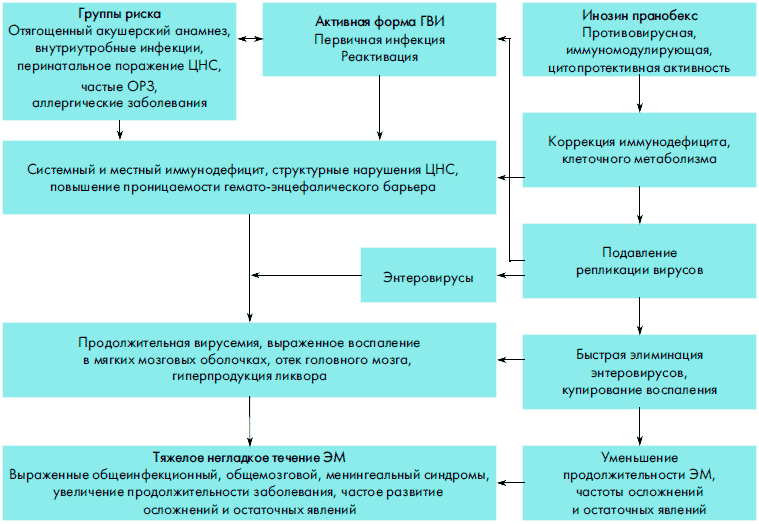
Перспективным направлением совершенствования терапии ЭМ у детей является использование изопринозина, который оказывает комплексное действие на основные этиопатогенетические механизмы заболевания. Изопринозин является препаратом с широким спектром противовирусной активности, тормозит репликацию ДНК- и РНК-содержащих вирусов, в том числе герпесвирусов, энтеровирусов [7, 9]. С другой стороны, изопринозин модулирует иммунный ответ по клеточному типу, павышает продукцию антител, функциональную активность факторов врожденной резистентности (нейтрофилов, макрофагов, естественных киллерных клеток), стимулирует выработку интерферона и других цитокинов [7, 8]. Включение иммунных механизмов ведет к подавлению активности ГВИ, быстрой элиминации энтеровирусов из организма, предупреждает развитие микст-инфекции. Третьим механизмом является улучшение обменных процессов в пораженных клетках, что приводит к снижению проницаемости гематоэнцефалического барьера, уменьшению отека и структурных нарушений головного мозга. О высокой клинической эффективности изопринозина свидетельствуют сокращение продолжительности общеинфекционного, общемозгового, менингеального синдромов, сроков санации ликвора, частоты осложнений и остаточных явлений.
Выводы
1. ЭМ на современном этапе сохраняет свойственные ему особенности — чаще возникает у детей старше 3-х лет жизни, характеризуется сочетанием общеинфекционного, общемозгового, менингеального, катарального, лимфопролиферативного синдромов, лимфоцитарным плеоцитозом, у части пациентов сопровождается развитием осложнений и остаточных явлений.
2. Активная форма ГВИ у детей из групп риска служит причиной тяжелого негладкого течения ЭМ, увеличения продолжительности заболевания, частого развития осложнений и остаточных явлений.
3. Противовирусная, иммуномодулирующая и цитопротективная активность изопринозина способствует сокращению продолжительности симптомов ЭМ, уменьшению частоты осложнений и остаточных явлений, что позволяет рекомендовать включение этого препарата в протокол лечения этого заболевания у детей.
Литература:
1. Сорокина М. Н. Вирусные энцефалиты и менингиты у детей: Руководство для врачей / М. Н. Сорокина, Н. В. Скрипченко. — М.: Медицина, 2004. — 416с.
2. Impact of rapid enterovirus molecular diagnosis on the management of infants, children, and adults with aseptic meningitis / С. Archim-baut et al. // J. Med. Virol. — 2009. — V. 81. — № 1. — P. 42—48.
3. Шевцова Н. П. Неврологические проявления энтеровирусной инфекции / Н. П. Шевцова, М. В. Голубева // Детские инфекции. — 2004. — № 3. — С. 49—52.
4. Куприна Н. П. Рабочий протокол ведения больных энтеровирусными менингитами / Н. П. Куприна, С. П. Кокорева // Детские инфекции. — 2005. — №2. — С. 53—56.
5. Черкасский Б. Л. Глобальная эпидемиология. — М.: Практическая медицина, 2008. — 447 с.
6. Szychowska Z. Herpes simplex meningoencephalitis in an infants observed during an epidemic of enterovial infections of the nervous system / Z. Szychowska, E. Kuchar, M. Sasiadek // Pediatr. Pol. — 1996. — V. 71. — № 8. — P. 721—725.
7. Исаков В. А. Герпесвирусные инфекции человека: Руководство для врачей / В. А. Исаков, Е. И. Архипова, Д. В. Исаков. — СПб.: Спецлит, 2006. — 303 с.
8. Immunological and clinical study on therapeutic efficiacy of inosine pranobex / М. Golebiowska-Wawrzyniak et al. // Pol. Merkuriusc. Lek. — 2005. — V. 19. — P. 379—382.
9. Попова О. В. Клиника, диагностика и лечение внутриутробных (TORCH) инфекций новорожденных и детей первого года жизни. — Минск, 2006. — 41 с.
