Изучение состава микробной флоры и местного иммунитета у больных с острым риносинуситом при лечении новой формой биопарокса
СтатьиК. Г. Добрецов1, О. А. Коленчукова2, А. В. Сипкин1
2НИИ Медицинских проблем севера СО РАН, г. Красноярск (Директор - член-корр. РАМН В. Т. Манчук)
Настоящее исследование посвящено изучению эффективности применения новой формы Биопарокса («Лаборатории Сервье», Франция) при лечении острого риносинусита. Было пролечено 52 больных с острым риносинуситом средней и тяжелой степени тяжести, из них 25 пациентов местно применяли аэрозоль Биопарокса в новой дозировке (по 2 ингаляции в каждый носовой ход 4 раза в день, 7 дней). В результате, на 5 сутки лечения выраженность эндоскопических критериев воспаления у больных, леченных Биопароксом, была меньше (2,4±0,5 балла), чем при традиционной терапии (3,6±0,4 балла); бактериальная обсемененность на 7-е сутки скуднее (Staphylococcus - 103КОЕ/мл, против 105КОЕ/мл в контроле, Streptococcus - 5,5х 103КОЕ/мл, против 108КОЕ/мл в контроле и отсутствие бактерий рода Enterococcus, против 5,5х102КОЕ/мл в контроле). Применение Биопарокса способствовало также улучшению местных иммунологических критериев (ИЛ-7β на 7-е сутки равнялся 2,6 пг/мг, против 3650 пг/мг -в контроле; ФНО-α - 1,0 пг/мг, против 10,0 пг/мг - в группе сравнения). Таким образом, результаты клинического исследования подтвердили эффективность применения новой формы Биопарокса при лечении острого риносинусита.
Ключевые слова: острый риносинусит, Биопарокс, микрофлора, иммунитет, местная терапия.
Библиография: 11 источников.
RESEARCH OF MICROFLORA STRUCTURE AND LOCAL IMMUNITY IN PATIENTS WITH ACUTE RHINOSINUSITIS IN TREATMENTS BY NEW FORM OF BIOPAROX
K. G. Dobretsov1, O. A. Kolenchukova 2, A. V. Sipkin 1
The paper presents the study of effectiveness of Bioparox new form (Servier, France) in the treatment of acute rhinosinusitis. 52 patients with severe and middle acute rhinosinusitis were treated: 25 patients - local use of aerosol Bioparox (new dose: 2 inhalations in each nasal passage, for times daily, during 7 days). Results: endoscopic inflammation criteria were less expressed in Bioparox treatment (2,4±0,5 points) in comparison with traditional method (3,6±0,4 points); bacterial number on 7 day: Staphylococcus - 103/ml versus 105/ml in control, Streptococcus - 5,5х103/ml versus 108/ml in control and absence of Enterococcus versus 5,5х102/ml in control. The use of Bioparox improved local immunological criteria (IL-1β on 7 day - 2,6 pg/mg versus 3650 pg/mg - control; TNFa - 1,0 pg/pg versus 10,0 pg/mg - comparison group). Thus, results confirmed effectiveness of new form of Bioparox in the treatment of acute rhinosinusitis.
Key words: acute rhinosinusitis, Bioparox, microflora, immunity, local therapy.
Bibliography: 11 articles
В последнее время, наряду с сердечно-сосудистой и онкологической патологиями, отмечается заметный рост воспалительных заболеваний дыхательного тракта [8]. Однако, современная фарминдустрия, в большинстве случаев, не может обеспечить потребности практической медицины в лекарственных средствах. Как отмечают аналитики, несмотря на постоянный рост финансирования научных работ, нацеленных на получение новых препаратов, количество разрабатываемых новых лекарств, тем не менее, постоянно уменьшается [2]. В частности, библиотека создаваемых новых химических соединений пополняется в среднем на 150000 образцов в год. В то же время реальное количество вновь синтезированных веществ, претендующих на роль потенциальных лекарственных средств, за последнее десятилетие значительно снизилось и составляет менее, чем один препарат в год на одну компанию [1]. Достаточно многообещающим видится использование лекарственных форм на основе наночастиц [10, 11]. Однако, в настоящее время таких зарегистрированных препаратов как за рубежом, так и в России нет.
На этом фоне появление новой формы препарата Биопарокс (фузафунгин) является уникальным событием и подтверждает высокий научно-практический потенциал французской фармацевтической компании «Лаборатории Сервье». Благодаря инновационным решениям компания сохранила форму препарата, улучшила его дизайн, уменьшила дозировку, не потеряв, при этом, уникальные фармакологические свойства активного компонента [9].
Быстрый эффект Биопарокса при остром риносинусите основан на сочетании антибактериального и противовоспалительного действия [6]. Элиминация возбудителя из очага воспаления снижает антигенную бактериальную нагрузку и восстанавливает местный иммунитет [3]. Таким образом, анализ микробной флоры и местного иммунитета позволяет судить об эффективности той или иной терапии при остром риносинусите.
Цель работы: исследовать эффективность новой формы Биопарокса при лечении острого риносинусита на основе изучения состава микробной флоры и местного иммунитета.
Характеристика больных и методы исследования
На базе ЛОР отделения Дорожной клинической больницы на станции Красноярск нами было пролечено 52 человека с острым риносинуситом средней и тяжелой степени тяжести: 31 мужчина (59,6%) и 21 женщина (40,4%).
По возрасту преобладали больные от 20 до 29 лет (28 человек; 53,8%). Наиболее типичным оказалось двухстороннее гнойное поражение верхнечелюстных пазух и клеток решетчатого лабиринта (33 человека; 63,5%), одностороннее воспаление верхнечелюстной пазухи наблюдалось у 13 пациентов (25,0%), одностороннее поражение лобной пазухи - у 5 человек (9,6%) и двухстороннее - у 1 пациента (1,9%). У 3 больных (5,8%) был диагностирован пансинусит. Установлено, что до начала лечебных мероприятий патологический процесс имел риногенный, бактериальный, неосложненный характер.
Социально-бытовые условия у всех больных были расценены ими как относительно удовлетворительные, т. е. они имели постоянную работу и место жительства, материальное состояние семьи позволяло поддерживать достаточный уровень питания.
В исследование не включались пациенты с гиперпластическими процессами в пазухах, с риногенными внутриглазничными и внутричерепными осложнениями, пациенты с сахарным диабетом, получавшие курсы антибиотикотерапии в течение последнего месяца или курсы лучевой, системной кортикостероидной и химиотерапии в течение последнего года, имеющие в анамнезе аллергические реакции на антибиотики группы цефалоспоринов и пенициллинов, лабораторно подтвержденными иммунодефицитными состояниями, а также беременные и кормящие женщины.
Всем 52 больным с риносинуситами проводилась системная антибактериальная терапия (внутримышечные инъекции цефалоспоринов II-III поколения в течение 7 дней), назальные деконгестанты (нафтизин 0,05% по 2 капли 2 раза в день - 7 дней), а также промывание полости носа по Проетцу (1 раз в день - 7-10 дней).
В зависимости от методов местного лечения все больные были распределены на 2 примерно равные группы:
Группа I - состояла из 25 человек с острым риносинуситом, которым применялось местное лечение новой формой Биопарокса (по 2 ингаляции в каждый носовой ход 4 раза в день, 7 дней).
Группа сравнения - состояла из 27 больных с острым риносинуситом, которые не получали Биопарокс.
В качестве оценки результатов лечения нами применялись учет жалоб с помощью анкетирования, эндоскопия полости носа, бактериологическое исследование и определение иммунного статуса.
Кроме этого, критериями эффективности проводимой терапии являлось проведение и количество пункций и/или трепанопункций, которые выполнялись больным через 7 дней лечения. Показаниями для проведения манипуляций после недельного курса консервативной терапии было наличие не менее двух критериев:
1. боли в области щеки и/или лба 5 баллов и выше;
2. гнойное отделяемое из носа;
3. сохранение температуры тела 37,5 град, и выше.
Интенсивность болей оценивалась больным при помощи 10-балльной визуально-ана логовой шкалы (ВАШ). При этом ответы пациентов характеризовались следующим образом: от 0 баллов - отсутствие боли, до 10 баллов - мучительная (нестерпимая) боль.
При бактериологическом исследовании выделение микроорганизмов проводили на трех питательных дифференциально-диагностических средах. Для выделения микрофлоры использовали желточно-солевой агар, кровяной агар и агар Эндо. При микроскопии нативного материала использовали окраску по Граму. Выросшие колонии изолировали в чистую куль туру для дальнейшей идентификации. О чистоте культуры судили с помощью визуального и микроскопического контроля [5]. Бактериологическое исследование проводилось путем забора носового секрета на 1-е и 7-е сутки лечения.
Оценка иммунологического статуса включала определение уровня иммуноглобулинов, сывороточных и секреторных провоспалительных цитокинов.
Определение иммуноглобулинов проводили методом радиальной иммунодиффузии в геле по Манчини [7].
Готовили три двухкратных разведения стандартной сыворотки в физиологическом растворе (0,9% раствор хлорида натрия) 1:2, 1:4, 1:8 (по 0,05 мл каждого разведения). Инкубацию проводили при комнатной температуре во влажной камере. При определении IgG срок инкубации составлял 24 часа, при определении IgA 24/18 часов, при определении IgM -48 часов. Затем измеряли диаметры колец преципитации. По результатам измерения диаметров колец стандартной сыворотки строили калибровочную кривую в полулогарифмических координатах.
При определении цитокинового статуса оценивали уровень концентрации ФНО-α и ИЛ-1|3 в сыворотке крови и носовом секрете методом твердофазного иммуноферментного анализа с помощью тест-систем «Вектор-Бест» ЗАО «Вектор-Бест» (Новосибирск, Россия) [4].
Иммунологическое исследование проводилось в 1-е и 7-е сутки лечения.
Статистическая обработка осуществлялась при помощи электронных таблиц «Excel» на базе персонального компьютера IBM Р-700, где проводилась первичная математическая обработка с вычислением средних значений полученных данных. Достоверность различий определялась по критериям Стьюдента и Фишера при нормальном распределении сравнительных рядов, и по критериям Вилкоксона-Манна-Уитни и Хи-квадрат при рядах, отличающихся нормальным распределением.
Результаты и обсуждение. Все больные исследуемой группы I при поступлении, как и в группе сравнения, предъявляли жалобы на выделения из носа, заложенность носа, боль/давление в области лица, ухудшение или потерю обоняния, слабость. На 5 сутки лечения жалобы на выделения из носа и заложенность носа у больных группы сравнения регистрировались у 18 (66,7%) и 16 (59,2%) больных соответственно. Аналогичные жалобы больные I группы в этот период предъявляли реже - 9 (36,0%) и 7 (28,0%) пациентов (р<0,05). На 10 сутки традиционного лечения жалобы сохранялись у 1/3 больных (8 человек; 29,6%). В группе I на 10 день жалобы на выделения из носа и заложенность носа предъявляли лишь 3 пациента (12,0%) (р<0,01).
Учитывая сохранение болей в области щеки и/или лба (6,1±0,8 балла) и наличие гнойного отделяемого из носа, 4 пациентам (14,8%) группы сравнения после 7-ми дневного курса терапии проводись пункции верхнечелюстных пазух. Повторные пункции верхнечелюстных пазух понадобились 2 пациентам (7,4%). У больных группы I однократная пункция верхнечелюстной пазухи проводилась только одному больному (4,0%) (р<0,01). Манипуляция проводилась в связи с наличием боли в области щеки (7,0 баллов) и гнойного отделяемого из носа после недельного курса терапии. Показаний для проведении трепанопункций лобных пазух больным обеих групп исследования отмечено не было.
При эндоскопическом исследовании полости носа в первые сутки болезни у всех больных с риносинуситом отмечались гиперемия, отек, влажность слизистой оболочки, обильные слизисто-гнойные выделения из носа. Интенсивность этих критериев оценивалась в баллах. Таким образом, в 1-е сутки терапии сумма баллов у больных обеих групп была максимальной: 4,2±0,5балла - в группе сравнения, 4,6±0,2 балла - в группе I. На 5 сутки лечения выраженность эндоскопической картины у больных I группы значительно уменьшилась и составила 2,4±0,5 балла, а в группе сравнения - 3,6±0,4 балла (р<0,05). К 10 суткам явления воспаления в полости носа купировались практически у всех больных группы I, интенсивность эндоскопических критериев равнялась 0,5±0,4 балла. У пациентов группы сравнения явления воспаления сохранялись и на 10 сутки (1,2±0,4 балла, р<0,05).
При микробиологическом исследовании у больных обеих групп исследования в первые сутки доминирующим родом были грамм положительные бактерий. Использование Биопарокса в новой дозировке сохранило выраженный антибактериальный эффект, что привело к обеднению микробного пейзажа на седьмые сутки лечения у больных I группы исследования. Так, в группе I бактерии рода Staphylococcus определялись в титре 1000 КОЕ/мл, против 100000 КОЕ/мл в группе сравнения (р<0,01); Streptococcus - 55000 КОЕ/мл, против 100000000 КОЕ/мл в группе сравнения (р<0,001); Enterococcus - не определялись, против 5500 КОЕ/мл в контроле (р<0,001) (табл. 1).
Таблица 1
Бактериологический анализ отделяемого из носа у больных с острым риносинуситом (N=52, median С25-С75)
|
Микроорганизмы (КОЕ/мл) |
1 сутки |
7 сутки | ||
| Группа сравнения | Группа Биопарокса | Группа сравнения | Группа Биопарокса | |
| Staphylococcus | 50500100,0 (200,0-101000000,0) | 50000000,0 (10000,0-100000000,0) | 100000,0 (1051,0-1000000,0) | 1000,0 (100,0-1000,0)* |
| Streptococcus | 505,0 (10,0-1000,0) | 100000,0 (1000,0-1000000,0) | 100000000,0 (100000000,0-100000000,0) | 55000 (10000-100000)** |
| Enterococcus | 0 | 0 | 5500,0 (1000,0-10000,0) | 0** |
| Micrococcus | 1000,0 (1000,0-1000,0) | 5000,0 (1000,0-10000,0) | 100,0 (100,0-100,0) | 10000,0 (10000,0-10000,0) |
| Enterobacteriaceae | 5005,0 (10,0-10000,0) | 3000,0 (500,0-5000,0) | 10000,0 (10000,0-1000000,0) | 10000,0 (10000,0-10000,0) |
Кроме антибактериального эффекта Биопарокс обладает еще и выраженным противовоспалительным действием. Это проявляется в уменьшении медиаторов воспаления и восстановлении иммунологических показателей.
При изучении уровня иммуноглобулинов на 7-е сутки достоверных отличий в группах лечения получено не было. Так, в группе I уровень IgM составит 10,15±1,3г/л; а в группе сравнения -13,90±3,5г/л; IgM в группе I - 0,78±0,3 г/л; в контроле - 1,48±0,5 г/л; IgA в группе I - 3,85±1,1г/л; в группе сравнения 1,19±0,6 г/л. Концентрация slgA в обеих группах была одинаковой (30,0 г/л). Отсутствие изменений специфических показателей гуморального иммунитета у пациентов с острым риносинуситом на 7-сутки свидетельствует об эффективности, в первую очередь, системной антибактериальной терапии. Однако, при дальнейшем изучении провоспалительных иммунологических показателей определено, что для полного купирования воспалительной реакции этого недостаточно. С этой точки зрения новая форма Биопарокса позволяет восстановить уровни цитокинов и повысить иммунный ответ на воспаление, как местно, так и всего организма в целом.
Таким образом, на 7-е сутки лечения сывороточная концентрация ИЛ-1β у пациентов, леченных Биопароксом, была 4,0±1,5 пг/мл, против 25,0±2,6 пг/мл в группе сравнения (р<0,01). При изучении секреторного ИЛ-1β было получено, что в группе I этот показатель равнялся 2,6±0,5 пг/мл; а в группе сравнения - 3650±25,5пг/мл (р<0,01) (рис. 1). Уровень секреторного ФНО-α у пациентов группы I был также лучше: 1,0±0,5пг/мг; против 10,0±2,5пг/мг в группе сравнения (р<0,01) (рис. 2).
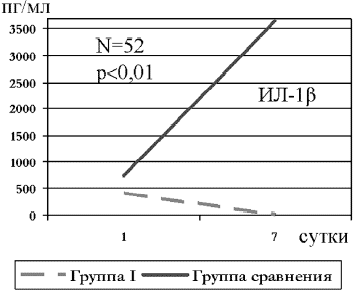
Рис. 1. Динамика уровня провоспалительного секреторного цитокина ИЛ- 1β у больных с острым риносинуситом (N=52, М±m).
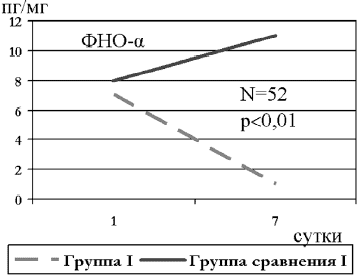
Рис. 2. Динамика уровня провоспалительного секреторного цитокина ФНО-α у больных с острым риносинуситом (N=52, М±m).
Нормализация иммунного барьера в носовом секрете у больных группы I объясняется снижением острой воспалительной реакции в слизистой оболочке. Это происходило за счет как антибактериального, так и противовоспалительного действия Биопарокса, чего при традиционной терапии не отмечалось.
Выводы:
Результаты клинического исследования подтвердили эффективность применения новой формы Биопарокса при лечении острого риносинусита. Использование Биопарокса привело к значительному снижению микробной флоры и восстановлению местного иммунитета у больных с воспалением носа и околоносовых пазух.
Таким образом, необходимость применения новой формы Биопарокса при лечении острого риносинусита не вызывает сомнений, а уменьшение частоты введения препарата увеличивает его комплаентность.
ЛИТЕРАТУРА
1. Бондарь В. С., Поздняков И. О., Пузырь А. П. Применение наноалмазов для разделения и очистки белков. Физика твердого тела 2004; 4: 737-739.
2. Васильев А. Е. Наноносители лекарственных веществ // Новая аптека 2003; 1: 64-67.
3. Воробьев А. А. Основы микробиологии, вирусологии и иммунологии. М.: Мастерство 2002; 224.
4. Завгородняя Е. Г. Цитокины и их место в диагностике и лечении ряда заболеваний ЛОРорганов. //Вестн. оторинолар. 2008; 3: 74-76.
5. Зубков М. Н. Сбор биологического материала для бактериологического исследования //Клинич. микробиология и антимикробная химиотерапия 2004; 2: 144-148.
6. Козлов В. С., Шиленкова В. В., Державина Л. Л. Влияние препарата биопарокс на слизистую оболочку полости носа при остром катаральном риносинусите // Вестн. оторинолар. 2007; 4: 45-74.
7. Лебедев К. А. Иммунология в клинической практике. М.: Медицинская электронная библиотека 1996; 387.
8. Овчинников А. Ю., Дженжера Г. Е., Лопатин А. С. Острый бактериальный риносинусит: в поисках оптимального антибиотика. Рос. ринология 2009; 1: 4-7.
9. German-Fattal М., Mosges R. How to improve current therapeutic standards in upper respiratory infections: value of fusafungine // Curr. Med. Res. Opin. 2004; 20(11): 1769-1776.
10. Lu A. H., Salabas E. L., Schuth F. Magnetic nanoparticles: synthesis, protection, functionalization, and application //Angew. Chem. Int. Ed. Engl. 2007; 46 (8): 1222-1244.
11. Yao L., Xu S. Long-range, high-resolution magnetic imaging of nanoparticles //. Angew. Chem. Int. Ed. Engl. 2009; 48 (31): 5679-5682.
