Диабетическая невропатия
Статьи3. Диабетическая невропатия
3.1. "Народная болезнь", которую раньше недооценивали
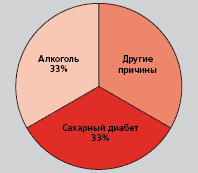
В западных индустриально развитых странах сахарный диабет наряду с алкоголизмом является наиболее частой причиной развития невропатии (рис. 3). При этом в проспективном многоцентровом исследовании показана тесная взаимосвязь между состоянием обмена веществ и невропатией (The Diabetes Control and Complications Trial (DCCT) - Исследование по контролю за сахарным диабетом и его осложнениями, 1993 и 1995 гг.). В течение 5-летнего периода наблюдения оценивался эффект интенсивной инсулинотерапии в отношении возникновения и развития диабетической полиневропатии у 1441 больного сахарным диабетом 1 типа. Посредством достижения оптимального уровня глюкозы в крови риск развития невропатических осложнений уменьшался независимо от возраста, длительности заболевания сахарным диабетом и пола на 64% по сравнению с обычной инсулинотерапией.
Рис. 3. Распределение невропатии по частоте встречаемости (изменено в сравнении с Neunddrfer, 1986)
В то же время, данные интервенционного исследования сахарного диабета по методике Киссинджера (Kissinger) (Haupt, 1996) свидетельствуют о том, насколько неудовлетворительно выглядит ситуация на практике. Выявление средних значений НЬА1с у 9,7% из 274 обследованных больных сахарным диабетом 1 типа и у 10,1% из 681 больного сахарным диабетом 2 типа позволяет судить о том, насколько трудно оптимизировать обмен веществ.
Установлено, что значительная часть больных сахарным диабетом со временем начинает страдать диабетической полиневропатией. Новейшие оценки (Haupt, 2005) исходят из того, что от 60% до 90% больных сахарным диабетом страдают периферической и/или автономной невропатией. Тем не менее, в литературе часто присутствуют противоречивые сведения. Неоднозначность данных, помимо всего прочего, может быть результатом разноплановой и даже неадекватной диагностики при выраженном разнообразии клинической симптоматики, отсутствием унифицированных методов выявления периферической невропатии, а также исследований, проводимых у различных контингентов пациентов.
В рамках многоцентрового исследования, проведенного в 118 диабетических клиниках Великобритании, были получены данные о распространенности диабетической полиневропатии в группе, включавшей 6487 больных сахарным диабетом 1 и 2 типа (Young, 1993). У больных сахарным диабетом 1 типа, независимо от продолжительности заболевания, распространенность составляла в среднем 32%, у больных диабетом 2 типа - 23%. С увеличивающимся временем заболеванием сахарным диабетом, а также повышением возраста пациентов частота возникновения диабетической полиневропатии возрастала. У пациентов со сроком давности сахарного диабета менее 5 лет распространенность составляла 21%, а у пациентов со сроком сахарного диабета более 10 лет - 37%. В то время как в возрастной группе 20-29 лет диабетическая полиневропатия диагностировалась лишь у 5% пациентов, ее распространенность в возрастной группе 70-79 лет составляла уже 44%
В ходе интервенционного исследования сахарного диабета по методике Киссинджера были получены обширные данные по частоте осложнений диабетической полиневропатии и сопутствующих заболеваний у 1050 больных сахарным диабетом 1 и 2 типов в одной из клиник Германии (Haupt, 1996). По истечении срока давности диабета 1 типа, равного 20 годам, 63% больных страдали диабетическими осложнениями, в то время как у 47% больных сахарным диабетом 2 типа, осложнения наблюдались уже по истечении 9-летнего срока давности заболевания. В обеих группах распространенность диабетической полиневропатии составляла примерно 26%.
Автономная невропатия также имеет существенное клиническое значение. Результаты исследования DiaCAN касаются эпидемиологии автономной кардиальной невропатии (Ziegler, 1992). В целом в 22 клиниках Германии, Австрии и Швейцарии в рамках многоцентрового исследования, включавшего 11 71 пациента, была изучена распространенность сахарного диабета 1 и 2 типов. Наличие автономной кардиальной невропатии устанавливалось и определялось при помощи специального автономного функционального теста. В то время как доля больных с автономной кардиальной невропатией при сахарном диабете 1 типа составляла 17%, это осложнение было диагностировано у 22% больных сахарным диабетом 2 типа.
Большое значение, которое свойственно диабетической полиневропатии не только с медицинской, но и с общесоциальной точки зрения, станет очевидным, если иметь в виду, что около 1 0% всех немцев (это число почти удвоилось в течение последних 10 лет!) страдают сахарным диабетом. Данные цифры соответствуют общему числу, равному приблизительно 8 миллионам больных сахарным диабетом в Германии, а к 2010 году в стране будет насчитываться 1 0 миллионов больных сахарным диабетом 2 типа. Основываясь на данных интервенционного исследования диабета по методике Киссинджера, согласно которым распространенность диабетической полиневропатии составляет 26%, можно судить о том, что уже более 2 миллионов больных сахарным диабетом в Германии страдают диабетической полиневропатией, причем в этот расчет не включены статистические данные по больным автономной невропатией.
Прогрессирующее течение заболевания при отсутствии адекватной терапии приводит в итоге к возникновению синдрома диабетической стопы. Приведенные ниже данные эпидемиологического исследования подтверждают высокий риск подобного рода поздних осложнений.
Средние финансовые затраты на пациентов с синдромом диабетической стопы составляют при 6-недельном пребывании в стационаре более 10000 евро (без учета затрат на компенсацию дней нетрудоспособности, суточных расходов и т.д.).
Обычно 5-летняя выживаемость после ампутации составляет 39-68% (Reiber, 1996).
3.2. Возникновение: комплекс патогенетических механизмов
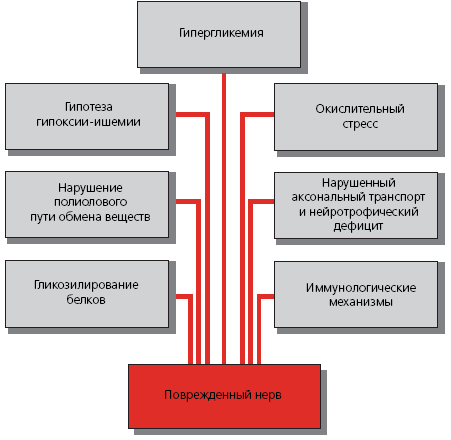
В настоящее время обсуждается комплекс частично связанных между собой различных патофизиологических и патобиохимических механизмов, которые имеют значение в патогенезе диабетической невропатии (рис. 4). Они приводят к метаболическим или сосудистым изменениям, которые первоначально проявляются обратимыми функциональными повреждениями нервов, а впоследствии - серьезными морфологическими дефектами вплоть до необратимых изменений.
Рис. 4. Патогенез диабетической невропатии
Не подлежит сомнению, что в патогенезе диабетической полиневропатии первостепенное значение имеет гипергликемия, которая способна повреждать как сами нервы, так и эндонейральные кровеносные сосуды. Повышенное содержание глюкозы выявляется не только в крови, но и в поврежденных органах-мишенях, например в нервных клетках. У крыс с индуцированным сахарным диабетом внутриклеточное накопление глюкозы выявлялось в N.ischiadicus (седалищный нерв) (Thurston, 1995). Так как глюкоза способна проникать в нервную клетку независимо от инсулина, она может не в полной мере включаться в процесс гликолиза, следствием чего является активация полиолового пути обмена веществ. В результате повышения активности ключевого фермента альдозоредуктаза образуется повышенное количество сорбитола. Он медленно диффундирует из нервных клеток или окисляется сорбитолдегидрогеназой с образованием фруктозы. Именно внутриклеточное накопление сорбитола является причиной различных повреждений нервов. Так, при активации полиолового пути обмена веществ происходит истощение запасов "вторичного мессенджера" миоинозитола. Кроме того, обсуждается возможность нарушения образования оксида азота (NO) как одного из патогенных последствий накопления сорбитола. Сужение сосудов с последующим пониженным давлением кислорода в периферических нервах обусловлено, возможно, уменьшением содержания этого сосудорасширяющего вещества.
Следующим важным моментом в патогенезе диабетической полиневропатии является накопление в тканях свободных радикалов. Обычно в организме окислительные и антиоксидантные процессы сбалансированы, поэтому постоянно образующиеся при окислительном стрессе свободные радикалы нейтрализуются. У больного сахарным диабетом данное равновесие сдвигается в сторону повышенной продукции свободных радикалов. Следовательно, функции антиокси-дантных защитных механизмов ослаблены (Low, 1991). Значение свободных радикалов заключается в их повышенной способности к химическим реакциям. Из-за реакций с ненасыщенными соединениями они нарушают структуру ферментных белков, липидов клеточных мембран и ДНК. При экспериментально воспроизведенной диабетической невропатии седалищных нервов установлены повышенные концентрации малонового диальдегида, являющегося маркером окислительного стресса (Low, 1991).
Кроме этого, повышенный окислительный стресс рассматривается как причина дегенерации аксонов (Reichel, 1996).
Дегенерация аксонов и атрофия нервных волокон при диабетической полиневропатии сопровождаются эндоневральными микрососудистыми изменениями, что составляет основу гипотезы гипоксии-ишемии. Исходные предпосылки заключаются в том, что первоначальное нарушение кровоснабжения происходит в области микрососудистого русла; оно обусловливает развитие гипоксии и влечет за собой атрофию нервных волокон.
Важную роль в патогенезе диабетической полиневропатии играет неферментное гликозилирование. В процессе реакции Майлларда (Maillard) между молекулами различных сахаров (включая глюкозу) и аминогруппами белков, липидов и ДНК происходит образование обратимых Шиффовых оснований. Из них образуются продукты Амадори (Amadori), и пройдя через комплексную серию реакций химических превращений, получаются конечные продукты ускоренного гликозилирования (AGE-продукты - advanced glycosylation end products) (Bierhaus, 2004). Они могут образовываться на промежуточной ступени реактивных дикарбониловых соединений в процессе окисления углеводов. AGE-продукты - класс чрезвычайно гетерогенных веществ, которые обладают характерной флюоресценцией. In vivo до настоящего времени лишь незначительную часть таких соединений смогли идентифицировать с помощью определения их химической структуры. Некоторые AGE-продукты являются субстанциями, обладающими повышенной способностью к химическим реакциям. Помимо всего прочего, с помощью внутримолекулярных и межмолекулярных поперечных связей они вызывают необратимые изменения структур, в т.ч. белков, и приводят к нарушениям их функций. В результате присоединения к рецепторным белкам образуются RAGEs (receptor agglutinat glucosulation) - продукты, которые вызывают ухудшение различных клеточных функций, в том числе экспрессию генов и внутриклеточную сигнальную трансдукцию (Rashi, 2004).
Вследствие гликозилирования базальных мембран кровеносных сосудов развиваются функциональные сосудистые нарушения (ретинопатия, нефропатия). Микроангиопатии, вызываемые AGE-продуктами в Vasa nervorum (нервные сосуды, ведут к нарушению питания нервов и являются дополнительным фактором возникновения полиневропатии (Ziegler, 1993).
Миелиновые оболочки также могут подвергаться процессу гликозилирования и впоследствии дегенерировать. У крыс и собак с индуцированным сахарным диабетом происходит усиленное гликозилирование белков в периферических нервах (Vlassara, 1981 и 1984 (1)). У крыс с сахарным диабетом выявлены в 5,2 раза более высокие концентрации гликозилированных миелиновых белков по сравнению со здоровыми животными (Vlassara, 1983). Из этого следует,что гликозилирования могут происходить на миелиновых оболочках нервов, и, возможно,таким образом способствовать функциональным нарушениям нейронов, которые встречаются при сахарном диабете. В одном из исследований in vitro было показано, что гликозилированный миелин из периферических нервов у больных сахарным диабетом избирательно распознается и утилизируется макрофагами (Vlassara, 1984 (2)). Возможно, этот феномен способствует сегментарной демиелинизации, которая, наряду с аксональными повреждениями, наблюдается при диабетической полиневропатии.
Проницаемость барьера кровь-нерв для гликозилированного альбумина, который образуется у пациентов с диабетической невропатией, может быть повышенной (Poduslo, 1992). Гликозилированные макромолекулы, повышенные концентрации которых отмечаются в эндоневрии, способны посредством прямого токсического эффекта, осмотических изменений или иммунологических механизмов приводить к возникновению невропатии.
Процессу гликозилирования подвергаются также белки цитоскелета в периферических нервах, что приводит к нарушению аксонального транспорта. В седалищных нервах больных сахарным диабетом крыс было выявлено более чем четырехкратное усиление гликозилирования тубулина, являющегося белком микроканалец. Такие изменения происходили уже спустя 14 дней от момента выявления сахарного диабета (Cullum, 1991). Микроканальцы, важные составные части цитоскелета, участвуют в антеро- и ретроградных транспортных процессах в нервной клетке. С помощью этих транспортных процессов переносятся в т.ч. факторы роста нервов, ферменты, нейромедиаторы и составные части мембран. Результаты этих экспериментальных исследований подтверждаются более новыми сведениями, указывающими на то, что у больного сахарным диабетом процессы гликозилирования также происходят в различных отделах периферических нервов.
Из ампутатов пациентов с сахарным диабетом и не имевших диабета извлекался N.suralis (икроножный нерв), причем число больных сахарным диабетом 1 и 2 типа было почти одинаковым. В белковых фракциях миелиновой оболочки и цитоскелета извлеченного нерва у больных сахарным диабетом выявлялись повышенные концентрации AGE-продуктов. Это свидетельствует о том, что наряду с неблагоприятным влиянием на аксональный транспорт создаются условия для формирования дегенерации аксонов, которая часто встречается при диабетической полиневропатии (Ryle, 1995).
Исходя из этого, важная роль в патогенезе диабетической невропатии отводится эндогенному фактору роста нервной ткани (ФРН) (Ziegler, 1993). Этот нейротрофический белок синтезируется в различных тканях, воспринимается через специфические рецепторы в нервных волокнах и переносится посредством ретроградного транспорта в перикарион нервной клетки. ФРН имеет ключевое значение для роста и функции нейронов. У животных с сахарным диабетом выявлен дефицит ФРН и замедленная скорость его переноса (Hellweg, 1990). Причинно-следственная связь с гипергликемией позволяет предполагать, что пониженный уровень ФРН может быть нормализован при помощи инсулинотерапии или аллотрансплантации островковых клеток (Hellweg, 1991; Fernyhough, 1994).
В патогенезе диабетической полиневропатии обсуждается участие также и иммунологических процессов. У больных сахарным диабетом с невропатией часто обнаруживаются антитела против симпатических нервных ганглиев, надпочечников и N.vagus (блуждающий нерв) (Rabinowe, 1990). Однако патогенетическое значение этих антител пока остается еще неясным.
Представленные патогенетические модели указывают на то, что развитие диабетической полиневропатии не имеет только одну причину. Она является следствием многофакторных событий, в которых центральную роль играет глюкозотоксичность.
3.3. Каким образом и где проявляется заболевание?
Клиническая картина диабетической невропатии может быть очень разнообразной. Различные формы ее проявления можно классифицировать следующим образом.
Taблица 2. Классификация диабетической невропатии (изменено в сравнении с Wiefels и Gries, 1988)
| Симметричные формы: | преимущественно дистальные, сенсорные или сенсорно-двигательные симптомы раздражения и расстройства |
| Асимметричные формы: | преимущественно проксимальные двигательные расстройства; особая форма -"диабетическая амиотрофия" |
| Мононевропатии: | изолированные расстройства, затрагивающие небольшое число нервов, преимущественно нервы головного мозга |
| Автономная невропатия: | симптоматика зависит от пораженного органа |
Наиболее частой формой является дистальная симметричная сенсорная полиневропатия, которая встречается приблизительно в 2/3 случаев, в то время как асимметричные формы и мононевропатии имеют в количественном отношении второстепенное значение. Нарушения вегетативных функций часто связаны с наличием дистальной симметричной полиневропатии, но могут встречаться также и как единственный ранний симптом диабетической невропатии.
Морфологически при полиневропатии различают следующие формы, которые дифференцируются в зависимости от видов поражений. Во-первых, это демиелинизирующая форма, при которой повреждена миелиновая оболочка нейрона, но аксон, тем не менее, остается нетронутым. При такой форме поражения отчетливо снижена сенсорная скорость проведения нервного импульса. Прогноз благоприятен, так как поврежденные фрагменты миелиновой оболочки могут регенерировать в процессе деления клеток.
И наоборот, при аксональной невропатии происходит дегенерация аксонального цилиндра. Это означает, что вследствие нарушения аксоплазматического транспорта, важные структурные элементы не могут больше перемещаться, и дисталь-ные участки нейронов погибают. Вначале скорость проведения нервного импульса не снижается или снижается медленно, но только до тех пор, пока еще не затронута миелиновая оболочка. Прогноз неблагоприятен, так как регенерация аксона может происходить вплоть до самого поражения, и процесс происходит очень медленно. При идеальных условиях аксон в человеческом нерве за 1 день вырастает примерно на 1 мм. Следовательно, если дегенерации подвержено волокно длиной 30 см, то на регенерацию необходимо около 1 года - за это время могут произойти тяжелые вторичные изменения, такие, как атрофия мышц и изменения суставов, поэтому исходное состояние уже не может быть достигнуто.
При диабетической полиневропатии речь в основном идет о смешанной форме повреждений. Соответственно различным бывает и прогноз. В любом случае тяжесть заболевания по мере увеличения его срока прогрессирует и соответственно ухудшается прогноз. По этой причине первостепенное значение имеет ранняя диагностика и своевременное начало лечения.
3.3 От клинической картины к ранней диагностике.
a. Дистальная симметричная полиневропатия -наиболее частое проявление на практике
При дистальной симметричной полиневропатии наиболее распространена сенсорная форма проявления (50-70%), в то время как симметрично-паретический тип наблюдается в 5-20% случаев (Neundorfer, 1993). В зависимости от типов пораженного нервного волокна отмечаются различные симптомы сенсорного раздражения и разные по характеру нарушения.
При вовлечении крупных волокон ухудшаются ощущения вибрации, прикосновения (тактильное чувство) и положения. Наоборот, если затронуты тонкие нервные волокна, то наблюдаются нарушения болевых и температурных ощущений. В большинстве случаев затронуты все типы волокон.
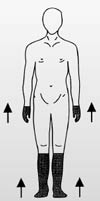
Дистальная симметричная полиневропатия неуклонно прогрессирует и находится в тесной взаимосвязи с состоянием обмена веществ. Жалобы, как правило, при этом тем выраженнее, чем дольше болеет пациент и чем хуже отрегулирован его обмен веществ. Развиваются нарушения чувствительности кожи конечностей, распространение которых в большинстве случаев начинается с пальцев стоп, а позднее они охватывают также пальцы и кисти рук. Прогрессирование нарушений чувствительности по типу "носок", "чулок" или "перчатка" имеет проксимальную направленность (рис. 5).
Рис. 5. Схема распространения нарушений чувствительности
К наиболее типичным симптомам относятся парестезия с ощущением "ползания мурашек", нарушение тактильной чувствительности и ощущение "ворсистости". При нарушении ощущений положения у пациентов дополнительно наблюдается атаксическая неустойчивость походки.
Особенно типичным симптомом является появление жгучих болей в стопах, так называемые "горящие ступни". Поэтому пациенты жалуются на симптом дизестезии - например, по ночам одеяло ощущается на ногах как болезненный и невыносимо тяжелый груз. Наблюдается характерное обострение упомянутых жалоб в ночное время и, прежде всего, в горизонтальном положении; в то же время при ходьбе пациенты предъявляют меньшее число жалоб.
Дополнительно могут наблюдаться мышечные судороги, повышенная чувствительность к холоду и болевые ощущения. У большого процента пациентов с дистальной симметричной сенсорной полиневропатией отмечаются жалобы на хронические боли достоверно различного характера. Варианты - от "жгучих поверхностных" до "глубоких сверлящих" болей. Прогноз болей является неопределенным. Если к нарушениям чувствительности прибавляются двигательные расстройства, они также в большинстве случаев имеют подчеркнуто симметричный и дистальный характер, как, например паралич мышцы, поднимающей ногу.
Типичным симптомом для более редких асимметричных форм невропатии являются острые боли с благоприятным прогнозом. При диабетической амиотрофии затрагивается Plexus lumbosacralis (пояснично-крестцовое сплетение) и, в частности, N.femoralis (бедренный нерв). У пациентов наблюдаются сильные боли, которые могут распространяться из поясничного отдела позвоночника к бедру и колену. Формируется парез затронутых мышц, которые быстро подвергаются атрофическим изменениям. При мононевропатии в области черепно-мозговых нервов затрагиваются преимущественно N.oculo-motorius (нерв глазодвигательный) и N.abducens. Клиническая картина проявляется изолированным или сочетанным парезом глазодвигательных мышц и парезом отводящего нерва. Кроме того, может развиваться поражение N.femoralis или N.medianus.
Встречаются также субклинические формы диабетической полиневропатии, которые выявляются при проведении электрофизиологических исследований и/или вегетативной или сенсорной функциональной проб. На практике начальные признаки невропатии могут быть выявлены своевременно при регулярном обследовании, и прогноз при этом существенно улучшается (Valk, 2002).
Диагноз симметричной дистальной полиневропатии основывается на подробных данных анамнеза, симптоматике и клинико-неврологическом обследовании, включающем постановку тестов на определение чувствительности, анализ проприоцептивных мышечных рефлексов, порога вибрации и, возможно, моторики, а также на результатах последующего проведения электро-физиологических исследований.
В связи с высокой распространенностью диабетической полиневропатии и большим значением, которое придается терапии этой патологии, каждый больной сахарным диабетом должен проходить профилактическое обследование по меньшей мере один раз в год. Описанный в табл. 3 базовый скрининг может проводиться семейным врачом с использованием минимального инструментария. Диагностический комплекс для выявления полиневропатии включает важнейшие функциональные пробы. Если необходимы специальные исследования, то их можно провести у соответствующих врачей-специалистов.
Таблица 3. Основная диагностика дистальной симметричной невропатии
Исследование чувствительности может выполняться посредством восприятия прикосновения, положения и боли. Для этого используются функциональные пробы, которые могут проводиться повседневно простыми средствами, и с их помощью можно выявлять проксимальное распространение нарушений чувствительности в конечностях.
Фото 1. Устройство Тип-Терм®

Необходимо обращать внимание на то, чтобы в каждом случае двигался только исследуемый сустав; при этом конечность поддерживается сбоку, чтобы облегчить восприятие путем надавливания в направлении движения. На находящиеся рядом пальцы ног или рук нажимают сбоку свободной рукой. Пациент с закрытыми глазами должен указать, в каком направлении произошло пассивное движение.
Ранними симптомами дистальной симметричной полиневропатии являются нарушение рефлекса ахиллова сухожилия и нарушенная вибрационная чувствительность. При исследовании вибрационной чувствительности оценивается состояние волокна А крупного калибра. С помощью калиброванного по Rydel-Seiffer камертона можно проводить полуколичественное измерение вибрационных волн, используя измерительные шкалы, разделенные на 8 делений (фото 2а).
Фото 2а и 2б. Исследование вибрационных ощущений в головке Os metatarsale l (первой плюсневой кости) с помощью калиброванного камертона Rydel-Seiffer
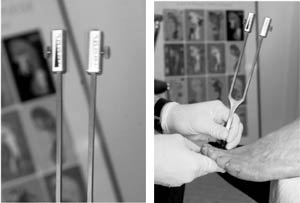
Участками, предназначенными для измерения, являются головка Os metatarsale l (1-й плюсневой кости) в проксимальном суставе большого пальца стопы (фото 2б), разгибающая сторона Os metatarsale l (или Os metacarpale I - первой пястной кости), внутренняя лодыжка, а также середина большеберцовой кости (или середина лучевой кости). Рекомендуется проводить несколько измерений, сравнивать полученные результаты и использовать их среднее значение. Порог вибрации указывает на зависимость от возраста пациента. У более пожилых людей ощущение вибрации часто бывает снижено, и это не следует рассматривать как патологическое изменение. Так, у пациентов в возрасте до 40 лет патологическими считаются значения менее 6, а у пациентов в возрасте свыше 40 лет значения ниже 5 (Ziegler и Gries, 1 996). Ощущение вибрации ухудшено тем сильнее, чем более дистально выбираются места для измерения. Если обнаруживается отчетливый вектор проксимального нарушения вибрационного ощущения, это говорит о наличии полиневропатии.
Регулярный осмотр стоп имеет важнейшее значение для раннего выявления синдрома диабетической стопы, при этом необходимо личное участие пациента.
Повреждения и деформации устанавливаются при внешнем осмотре, отсутствие пульса на нижней конечности является важным диагностическим критерием наличия облитерирующего заболевания периферических артерий.
Помимо клинико-неврологического обследования дополнительно может проводиться аппаратурная функциональная проба. При этом выбор подходящих методов измерения в каждом конкретном случае зависит от клинической симптоматики и дифференциально-диагностических соображений. При помощи электронейрографии может измеряться скорость проведения по нерву чувствительных и/или двигательных импульсов. Посредством измерения этих скоростей оцениваются функции быстропроводящих нервных волокон крупного калибра. Вовлечение двигательных волокон может быть предварительно подтверждено электромиографией. Количественное определение вибрационных ощущений может также проводиться с использованием измерительных приборов (виброметр, биотезиометр).
Для количественной оценки повышенной температурной чувствительности также имеются специальные устройства. Особенно хорошо зарекомендовало себя применение контактного термодинамического прибора.
Наиболее удобным для диагноза полиневропатии и контроля его развития является специальный диагностический комплекс - Polyneuropathie-Diagnose-Set. С его помощью на практике можно просто и оперативно выполнить важнейшие функциональные пробы:
В качестве дополнения при двигательных расстройствах может проводиться исследование мышечной силы. При этом пациента просят совершить определенное движение, при котором тот должен встретить сопротивление (например сгибание локтевого сустава). Затем оценивается мышечная сила посредством полуколичественной балльной шкалы. Важным признаком наличия пареза является атрофия мышц. Исследования проводятся путем осмотра рельефа мышцы и сравнительного измерения мышечного объема. Место измерений должно быть точно установлено, чтобы обеспечить объективный контроль динамики заболевания.
б. Опасные последствия: диабетическая стопа
Синдром диабетической стопы относится к наиболее серьезным осложнениям сахарного диабета. В ведущих индустриальных государствах частота ампутаций нижней конечности у больных сахарным диабетом составляет 6-8/1000 в год (Lechleitner, 2004). В 85% таких случаев выявляется предшествующее язвенное поражение. В целом ампутации ног у больных сахарным диабетом проводятся в 10 раз чаще, чем у пациентов, не страдающих данным заболеванием, долговременный прогноз для таких пациентов крайне неблагоприятный. В Сент-Винсентской декларации, принятой еще в 1989 году, среди других было выдвинуто требование вдвое снизить процент ампутаций в течение последующих 5 лет. Но с тех пор ситуация лишь усугубилась: при нынешних 30 000 ампутаций в год (округленно) частота ампутаций у больных сахарным диабетом существенно повысилась.
При синдроме диабетической стопы различаются 3 формы: невропатическая стопа, ишемически обусловленная диабетическая стопа и смешанная форма, объединяющая обе предыдущих. Приблизительно в 70% случаев причиной является невропатия (Boulton, 1990 и 2004). При этом в патогенезе важную роль играют как автономная (вегетативная), так и дистальная симметричная сенсорная или сенсорно-двигательная невропатия.
На основе поражения вегетативных нервных волокон происходит нарушение моторики сосудов. В результате ухудшения секреции потовых желез кожа становится сухой, ломкой и более восприимчивой для повреждений. Вследствие нарушенной регуляции тонуса кровеносного сосуда происходит расширение сосудов, которое приводит к возникновению отеков. Типичными являются необычная гладкость и напряженность кожи, которая может стать тонкой, как бумага, а также неотчетливый рельеф сухожилий. В отличие от сердечных отеков трофические отеки не устраняются при постельном режиме. Распространение отека в ряде случаев достигает голени. Трофические изменения, наряду с кожей, затрагивают также связки, сухожилия и суставы и могут вызывать остеопатию или остеоартропатию. Двигательные расстройства (нарушения походки) влекут за собой ошибочные нагрузки на туловище и приводят к типичным деформациям плюсневых костей, что является преимущественной локализацией поражения.
Так как при одновременном наличии нарушений чувствительности, обусловленных сенсорной невропатией, интенсивность болевых раздражителей уменьшается, либо они вовсе не воспринимаются, пациент перестает ощущать, "где у него болит". Возникают гиперкератозы, а при последующих нагрузках (надавливании) формируется невропатическая язва (Malum perforans). Это поначалу в большинстве случаев протекает бессимптомно и имеет характерную локализацию в областях повышенной нагрузки (прежде всего, на подушечках больших пальцев стопы). Обычно такая язва имеет круглую форму, похожую на "тавро", часто инфицируется и может быстро распространяться до кости. Вследствие инфицирования мягких тканей впоследствии могут развиваться такие осложнения, как остеомиелит и даже генерализованная септическая инфекция. Характерный признак - отсутствие боли в области поражения, что является важным дифференциально-диагностическим критерием макроангиопатической язвы как последствие облитерирующего заболевания перириферических артерий.
При проведении дифференциальной диагностики ишемически обусловленную диабетическую стопу отличают по клинической симптоматике от невропатически обусловленной язвы (табл. 4). При нарушении кровоснабжения отсутствует пульс на нижней конечности, кожа холодная, бледная с оттенком синюшности. При облитерирующих сосудистых поражениях, в отличие от невропатической язвы, ощущение боли и чувствительность сохранены. Важную информацию дает анамнез - в то время как при сосудистых поражениях пациенты предъявляют жалобы преимущественно при нагрузках, при невропатии происходит ухудшение симптомов в состоянии покоя, особенно в ночное время. Характерна различная локализация поражений. Так, трофические невропатические язвы образуются главным образом на участках, подверженных давлению, в то время как появляющуюся при нарушениях кровоснабжения гангрену обнаруживают в большинстве случаев в области плюсны. Разумеется, при проведении дифференциальной диагностики необходимо учитывать, что часто встречается и смешанный тип невропатически и ишемически обусловленной диабетической стопы.
Полиневропатия причиняет дополнительные страдания и приводит к существенному ухудшению качества жизни.
Таблица 4. Дифференциальная диагностика при диабетической стопе
|   | Невропатическая стопа | Ишемическая стопа |
| Анамнез | Сахарный диабет (нефропатия, ретинопатия). Жалобы в состоянии покоя (особенно ночью). | Дополнительные факторы риска (нарушения жирового обмена, хроническая ишемическая болезнь сердца, злоупотребление курением). Значительное усиление болей при нагрузке (перемежающаяся хромота). |
| Внешний осмотр | Розовая кожа. Костные и мышечные деформации. Безболезненная невропатическая подошвенная язва. Редко встречающиеся на тыльной стороне синяки и мозоли. | Атрофичная бледно-синюшная кожа. Гангрена пальцев ног, пяточной области. |
| Пальпация | Теплая, сухая кожа. Отчетливый пульс на нижних конечностях. | Холодная стопа. Отсутствие пульса стопы. |
| Базовая диагностика | Чувствительность снижена (часто повышена). Нарушения рефлексов. Ощущение вибрации нарушено. Допплеровский индекс > 0,9. | Чувствительность сохранена. Рефлексы сохранены. Ощущение вибрации не нарушено. Допплеровский индекс < 0,9 |
| Рентген | Деструкция / Остеолиз | Изменения отсутствуют |
в. Наибольший профиль риска: автономная невропатия
Сообщения о наличии вегетативно-автономных нарушений у больных сахарным диабетом впервые появились почти 200 лет назад (Rollo, 1798). В настоящее время следует исходить из того, что нарушениями вегетативной нервной системы страдают как минимум 20% больных сахарным диабетом 1 и 2 типов (Neundorfer, 1995). Согласно данным крупномасштабного научного исследования Euro-DIAB IDDM (исследование осложнений), распространенность автономной невропатии составляла больше 36,6% (Kempler, 2002). При этом автономная невропатия в большинстве случаев ассоциирована с сенсорной и сенсорно-двигательной формой, но может проявляться также и в виде единственного раннего симптома.
Наряду с эфферентными волокнами, которые сопровождают черепно-мозговые и соматические нервы, а также висцеральные периферические нервы, при автономной невропатии могут быть затронуты и афферентные волокна. Последние передают раздражения от болевых, механо- и хеморецепторов различным органам и системам. Нарушение афферентации приводит к опасным клиническим осложнениям (Kempler, 1997). Это, прежде всего, отсутствие боли при коронарной ишемии, которая может привести к "немому" инфаркту миокарда, а также отсутствие ощущения гипогликемии.
Автономная невропатия во многих случаях выявляется лишь на более поздних стадиях, так как даже при наличии нескольких функциональных нарушений часто не наблюдается никаких клинических симптомов. Функциональные нарушения являются органоспецифичными и поэтому должны отличаться от клинического синдрома заболеваний соответствующих органов. Различные формы автономной невропатии имеют преимущественно клиническое значение и часто неудовлетворительный прогноз. Систематизация автономной невропатии производится на основании клинических критериев, исходя из вовлеченных систем органов и их функций (табл. 5).
Наиболее серьезным осложнением сахарного диабета является невропатия сердечно-сосудистой системы. Поэтому продолжительность жизни больного сахарным диабетом определяется автономной кардиальной невропатией (Kempler, 2003).
Таблица 5. Автономная диабетическая невропатия - ведущие нарушения и симптомы (Haslbeck, 1993)
Сердечно-сосудистая система:
тахикардия покоя, ослабленное/отсутствующее восприятие боли, ограниченная вариабельность частоты сердечных сокращений, аритмия, удлиненный QT - интервал на ЭКГ, ортостатическая гипотензия, тахикардия.
Желудочно-кишечный тракт:
парез желудка, диспептические симптомы, "лабильный диабет", диарея, запор, недержание кала.
Урогенитальная система:
диабетическая цистопатия, увеличение количества мочи, нарушенное восприятие наполнения мочевого пузыря, остаточная моча, недержание мочи, эректильная дисфункция.
Трофика конечностей:
ангидроз, гиперкератоз, отеки, пониженная/отсутствующая чувствительность, патологическая нагрузка, язвы, остеопатия, остеоартропатия, гангрена.
Эндокринная система:
отсутствующее/ограниченное восприятие гипогликемии.
Для прогноза автономной невропатии необходимо принять во внимание результаты мета-анализа 9 важнейших исследований (Ziegler, 1994). При средней продолжительности наблюдения 5,8 лет, уровень смертности пациентов с автономной невропатией составлял 29%. В отличие от них, уровень смертности пациентов с нормальными результатами тестирования сердечно-сосудистой системы составлял всего 6%. Таким образом, при наличии автономной невропатии смертность возрастает в пять раз.
Автономная невропатия проявляется у больных сахарным диабетом в форме тахикардии покоя, аритмии, ограниченной вариабельностью частоты сердечных сокращений, ортостатической дисрегуляцией; на ЭКГ признаком автономной кардиальной невропатии является удлиненный интервал QT (Kempler, 1994).
Клинически автономная невропатия в большинстве случаев протекает без особенностей, так как вначале от пациента не поступает никаких жалоб. В качестве явного симптома можно отметить лишь нарушение регуляции артериального давления, например, в форме головокружения, потемнения перед глазами или общей слабости пациента. Опасным последствием пониженного или утраченного восприятия боли при ишемической болезни сердца является развитие "немого" инфаркта. Его признаки или предшествующего приступа стенокардии не распознаются больным сахарным диабетом из-за повреждения чувствительных афферентных нервных волокон или также в результате прогрессирующего атеросклероза, поэтому, как правило, не принимаются своевременные меры (Airaksinen, 2001). Показано, что сахарный диабету мужчин протекает с 3,5-кратным, а у женщин с 5,7-кратным риском развития инфаркта миокарда (Lowel, 1996), причем из этого следует, что у больных сахарным диабетом как минимум одна треть инфарктов миокарда протекает как "немой" (Soler, 1975).
Больных диабетом следует рассматривать в качестве пациентов риска также при получении ими наркоза. Они находятся в особой опасности, т.к. при наличии у них автономной кардиальной невропатии происходит накопление событий, которые могут представлять угрозу для жизни.
В целях диагностики автономной кардиальной невропатии разработаны и используются различные несложные функциональные тесты (табл. 6).
Таблица 6. Несложные функциональные тесты для диагностики автономной кардиальной невропатии
| Тест | Значение | Патологические величины |
| Вариабельность частоты сердечных сокращений при глубоком дыхании | Различия частоты сердечных сокращений в минуту | ≤ 10 |
| Ортостатический тест оценки артериального давления | Различия систолического артериального давления (мм рт. ст.) | ≥ 30 |
| Проба Вальсальвы | Отношение самого длинного RR-интервала к самому короткому RR-интервалу | ≤ 1,20 |
При этом с помощью тестов для оценки вариабельности сердечного ритма выявляют парасимпатические, а с помощью тестов по оценке артериального давления -симпатические повреждения.
Ранним признаком вагусного нарушения считается ослабление дыхательной синусовой аритмии, которое может приводить к почти полной ригидности частоты сердечных сокращений (рис. 6). Исследование проводится посредством регистрации ЭКГ при глубоком дыхании. Пациента, находящегося в горизонтальном положении, просят в течение одной минуты с ритмом в 5 секунд производить вдохи и выдохи. Затем рассчитывается разность между максимальной и минимальной частотой сердечных сокращений. С возрастом степень дыхательной аритмии усиливается. Величины до 10 расцениваются как патологические (Haslbeck, 1993). Ортостатический тест оценки артериального давления проводится путем определения уровня снижения систолического артериального давления при принятии вертикального положения. После 5-минутного нахождения в горизонтальном положении пациенту предлагают встать в течение 5 секунд. Самое низкое значение после подъема сравнивается с последним измерением при нахождении в положении лежа и определяется разность между этими величинами. Падение систолического артериального давления более чем на 30 мм рт. ст. считается патологией (Haslbeck, 1993).
Рис. 6. Вариабельность частоты сердечных сокращений как ведущий симптом автономной кардиальной невропатии (изменено в сравнении с Mackey, 1983)
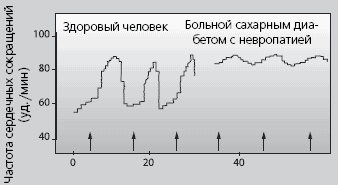
Для выявления ограничения вариабельности сердечного ритма проводится опыт Вальсальвы (Valsalva). Для этого пациента просят в положении сидя дуть в мундштук с определенной силой, чтобы поддерживать постоянное давление 40 мм рт. ст. продолжительностью свыше 15 секунд. Во время процесса дутья и далее в течение последующих 15 секунд производят регистрацию ЭКГ. Коэффициент Вальсальвы определяется как отношение значения самого длинного PR-интервала после эксперимента и самого короткого - во время эксперимента. Если получаемые величины оказываются ниже 1,20, то это рассматривается как признак нарушения вегетативной функции (Haslbeck, 1993).
При наличии желудочно-кишечных жалоб, которые особенно часто появляются у больных диабетом 2 типа, возникает подозрение на автономную невропатию желудочно-кишечного тракта. В случае вовлечения афферентных и эфферентных автономных нервных волокон происходит нарушение желудочно-кишечной моторики, секреции, всасывания, а также перцепции. Вследствие неудовлетворительной перистальтики характерным признаком является атония желудка, которая влечет за собой его замедленное опорожнение. Пациенты предъявляют жалобы на чувство переполнения, боли в животе, тошноту, позывы на рвоту, которая возникает после приема пищи или по утрам. Однако диабетический парез желудка может протекать также и без каких-либо симптомов. Энтеропатия обычно проявляется в виде "диабетической диареи". При этом наблюдается учащенный водянистый стул обычно после приема пищи и часто - в ночное время. Продолжительность диареи может быть различной, причем она может сменяться запорами. Удивление вызывает то, что общее состояние пациентов ухудшается лишь незначительно. Возникает опасность осложнения в виде энтерального размножения бактерий. При нарушении функции М.sphincter ani internus (внутренняя запирающая анус мышца) развивается недержание стула, о котором пациенты из чувства стыдливости чаще всего не говорят. Вполне очевидно, что симптомы желудочно-кишечной невропатии могут в значительной степени ухудшать качество жизни пациентов. Кроме того, нарушения всасывания еще больше усугубляют нарушения обмена веществ у больного сахарным диабетом. Таким образом, последствием желудочно-кишечной невропатии можно объяснить ранее непонятную нестабильность обмена веществ.
Для специфической диагностики желудочно-кишечной невропатии должны проводиться специальные исследования. В настоящее время методом выбора диагностики диабетического пареза желудка является радиоизотопное медицинское исследование опорожнения желудка, проводимое с помощью маркировки изотопами различных тестовых приемов пищи (сцинтиграфия функции желудка). Определенное практическое диагностическое значение имеет рентгенологическое исследование с использованием контрастного вещества. Ультразвуковое исследование дает возможность определить частоту и скорость антральных сокращений желудка.
Возникающая на фоне развития невропатии урогенитальной системы диабетическая цистопатия является распространенным и весьма серьезным осложнением. У пациентов молодого возраста с сахарным диабетом в 80% случаев наблюдались нарушения функции мочевого пузыря (Faerman, 1971). Данные нарушения клинически развиваются медленно. Наблюдаются аномально большие объемы утренней мочи со слабой струей и последующим эвентуальным мочеиспусканием (каплями). Следствием атонии мочевого пузыря является задержка мочи с образованием остаточной мочи. Характерно отсутствие ощущений переполненности мочевого пузыря. В качестве осложнений могут развиваться восходящие инфекции мочевых путей вплоть до пиелонефрита.
В процессе диагностики выявляется патологически увеличенный объем мочевого пузыря (от 800 до 1000 мл), а с помощью ультразвукового исследования -появление остаточной мочи (патологический уровень - от 50 до 90 мл). При необходимости проводятся специальные исследования (урография, урофлоуметрия). У мужчин должна проводиться дифференциальная диагностика для исключения увеличения предстательной железы.
Существенную проблему для больных сахарным диабетом представляет эректильная дисфункция. У 59% мужчин, больных сахарным диабетом могут развиваться нарушения потенции (Ellenberg, 1971), причем нужно исходить из того, что это "темное" число может быть завышено. С другой стороны, именно автономную невропатию следует рассматривать как наиболее частую причину импотенции у мужчин, страдающих сахарным диабетом (Strian, 1987; Haslbeck, 1986).
По мере увеличения возраста сексуальные расстройства у больных сахарным диабетом усугубляются. Эти нарушения в свою очередь приводят к серьезным психическим расстройствам. С ними связано значительное ухудшение качества жизни пациентов.
Характерный ранний симптом автономной урогенитальной невропатии у мужчин - отсутствие болевых ощущений при надавливании на яички, что обусловлено повреждениями афферентных волокон. С помощью дифференциально-диагностических методов нужно разграничивать нейрогенную и психогенную формы импотенции. Невропатическая импотенция, в отличие от психогенной, развивается медленно и часто связана с недостаточной утренней спонтанной эрекцией. В качестве последующих симптомов могут наблюдаться ретроградные эякуляции.
При психогенной импотенции могут наблюдаться нарушения либидо, которые присутствуют в случае развития автономных функциональных нарушений. Посредством тщательного сбора анамнеза можно в основном дифференцировать обе эти формы. В случае необходимости проводятся специальные исследования (SKAT-тестирование и т.п.). При постановке диагноза "нейрогенная импотенция" необходимо удостовериться, нет ли нарушений функции мочевого пузыря, так как обе формы проявления автономной невропатии часто бывают взаимосвязаны.
Развивающиеся при автономной невропатии трофические поражения конечностей приводят к возникновению невропатических язв.
Следующее серьезное осложнение при автономной диабетической невропатии -пониженное восприятие гипогликемии. Своими типичными признаками, такими как "сердцебиение, потливость", гипогликемия не проявляется, поэтому пациентам может угрожать внезапное коматозное состояние. У таких пациентов дополнительно затрудняется обмен веществ.
Таким образом полиневропатия может серьезно нарушить деятельность систем жизненно важных органов у больных сахарным диабетом. При этом автономные функциональные расстройства затрудняют обмен веществ и повышают риск летальности (Kempler, 2003).
