Бенфотиамин в лечении диабетической полинейропатии (BENDIP study)
Статьи
Опубликовано в журнале:
Медицинский вестник № 36-37 (463-464), 21 ноября 2008 г.
Результаты рандомизированного двойного слепого плацебоконтролируемого многоцентрового клинического исследования Hilmar Stracke* et al., клиника и поликлиника III больницы при Университете Гессена и Марбурга. Гессен, Германия Karlheinz Reiners, неврологическое отделение больницы при Университете Вюрцбурга. Вюрцбург, Германия
Введение
Полинейропатия является главным осложнением диабета, наблюдаемым у 30-50% пациентов. Гипергликемия вызывает активизацию разнообразных вредных метаболических путей. Повышенная выработка супероксидных радикалов в электронно-транспортной цепочке митохондрий, активация полиольного и гексозаминового путей метаболизма, активация протеинкиназы C и формирование высших конечных продуктов гликации приводят к ухудшению нейрональной и сосудистой деятельности. Было установлено, что у пациентов с нарушенной переносимостью глюкозы активация рецептора высших конечных продуктов гликации является одним из первых этапов патогенеза диабетической полинейропатии. Этим также может объясняться то наблюдение, что полинейропатия может возникнуть у пациентов с нарушенной переносимостью глюкозы, не обнаруживающих симптомов диабета, предшествуя, таким образом, выраженному сахарному диабету.
Недавно было продемонстрировано, что у страдающих диабетом пациентов наблюдается дефицит тиамина, вызванный его повышенным выведением почками. В ходе экспериментальных испытаний бенфотиамин оказал положительное воздействие на основные патофизиологические пути, ведущие к развитию осложнений диабета. Кроме того, в клиническую эффективность бенфотиамина могут вносить вклад его прямые антиоксидантные свойства. В ходе пилотного исследования монотерапия бенфотиамином значительно ослабила симптомы диабетической полинейропатии. Исследование BENDIP (БЕНфотиамин в лечении ДИабетической Полинейропатии) было проведено с целью подтверждения этих результатов в рамках рандомизированного двойного слепого плацебоконтролируемого исследования.
Характеристики исследования
Многоцентровое исследование (10 центров в Германии) Рандомизированное двойное слепое плацебоконтролируемое исследование. Из 181 отобранного пациента 165 были рандомизированно распределены по трем экспериментальным группам (фаза выведения), 133 и 124 пациента соответственно были подвергнуты анализу ITT и PP. Критерии включенияКлинически выраженная симметричная дистальная диабетическая нейропатия в течение как минимум 3-х месяцев Показатель по NSS (шкале нейропатических симптомов) и NDS (шкале нейропатического дисфункционального счета) >5 Стабильные симптомы (изменение показателей NSS и NDS между отбором и рандомизацией <1) Гликированный гемоглобин (HbA1c) ≤9,5% Возраст 18-70 лет. Критерии исключенияПродолжительность заболевания (полинейропатии) более 2 лет Прием витаминов (особенно группы B) в течение предшествующих 4 недель Продолжение лечения альфа-липоевой кислотой или иными препаратами, воздействующими на нейропатические симптомы (например, антидепрессантами, противоэпилептическими средствами) Предшествующее продолжительное (3 месяца) лечение психотропными препаратами Необходимость в мощных анальгетиках (опиоидах). Экспериментальные группы (ITT/PP) Группа A, по 200 мг бенфотиамина 3 раза в день (600 мг) (n = 47/43) Группа B, по 100 мг бенфотиамина 3 раза в день (300 мг) (n = 45/42) Группа C, плацебо (n = 41/39) Рис. 1. ITT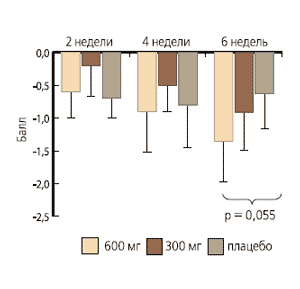 Рис. 2. РР
Рис. 2. РР Продолжительность лечения6 недель с контрольными посещениями врача через 2 и 4 недели. РезультатыИзмерение первичного результатаИзменение показателя NSS по сравнению с исходным:
Продолжительность лечения6 недель с контрольными посещениями врача через 2 и 4 недели. РезультатыИзмерение первичного результатаИзменение показателя NSS по сравнению с исходным:
Показатель NSS снизился на 1,35 балла в группе A, на 0,91 балла в группе B и на 0,63 балла в группе C (популяция ITT).
Различие было чуть выше уровня значимости (p = 0,055), однако в случае анализа PP различие между группами было значимым, p=0,033. Измерение вторичных результатовTSS: показатель TSS снизился на 1,12 балла в группе A, на 0,98 балла в группе B и лишь на 0,26 балла в группе C (без значимого различия между группами). Отдельные симптомы, составляющие показатель TSS, при приеме 600 мг бенфотиамина: Симптом "боль" ослабел больше всего, в то время как на "парестезию" бенфотиамин не оказал воздействия. NDS: Показатель NDS проявил тенденцию к устойчивому улучшению с течением времени без значимых различий между группами. Порог восприятия вибрации: при тестировании с камертоном между группами были обнаружены лишь минимальные различия. Демографические и диабетические характеристики| Группа | ITT (n = 133) | PP (n = 124) |
A
(n = 47) | B
(n = 45) | C
(n = 41) | A
(n = 43) | B
(n = 42) | C
(n = 39) |
| Ежедневная доза бенфотиамина | 600 мг | 300 мг | плацебо | 600 мг | 300 мг | плацебо |
| Возраст | Средний (лет) | 62 | 59 | 61 | | 58 | 61 |
| (Мин.-макс.) | (47-73) | (46-72) | (42-72) | (47-71) | (46-69) | (42-70) |
| Пол |
Мужской | 25 | 25 | 24 | 24 | 24 | 22 |
| Женский | 22 | 20 | 17 | 19 | 18 | 17 |
| Вес |
Средний (кг) | 87,8 | 86,5 | 85,6 | 88,9 | 85 | 85,9 |
| (Мин.-макс.) | (62-131) | (53-140) | (60-180) | (62-131) | (53-140) | (60-180) |
| Рост | Средний (см) | 171,4 | 172,0 | 171,9 | 171,6 | 172,0 | 171,6 |
| (Мин.-макс.) | (155-189) | (155-192) | (149-189) | (155-189) | (155-192) | (149-188) |
| Сахарный диабет |
Типа 1 | 8 | 6 | 2 | 7 | 6 | 1 |
| Типа 2 | 39 | 39 | 39 | 36 | 36 | 38 |
| Продолжительность заболевания | Средняя (лет) | 13,2 | 12,0 | 11,7 | 13,1 | 12,0 | 11,3 |
| (Мин.-макс.) | (0,75-41) | (0,25-37) | (0,5-37) | (0,75-41) | (0,25-51) | (0,5-37) |
| HbA1c | Средний (%) | 7,8 | 7,7 | 7,6 | 7,8 | 7,7 | 7,6 |
| (Мин.-макс.) | (6,0-10,1) | (6,2-9,4) | (5,5-9,7) | (6,0-10,1) | (6,2-9,4) | (5,5-9,7) |
Исходные значения для измерения результатов| Группа | ITT (n = 133) | PP (n = 124) |
A
(n = 47) | B
(n = 45) | C
(n = 41) | A
(n = 43) | B
(n = 42) | C
(n = 39) |
| Показатель NSS |
7,7 | 7,6 | 7,6 | 7,8 | 7,6 | 7,8 |
| (5-9) | (5-9) | (5-9) | (5-9) | (5-9) | (5-9) |
| Показатель TSS (общая шкала симптомов) |
6,2 | 6,0 | 4,9 | 6,1 | 5,8 | 4,9 |
| (1-14,64) | (0-14,64) | (0-13,98) | (1-14,64) | (0-14,64) | (0-13,98) |
| Показатель NDS | 7,6 | 8,3 | 7,9 | 7,6 | 8,3 | 7,9 |
| (5-10) | (5-10) | (5-10) | (5-10) | (5-10) | (5-10) |
| Тест с камертоном: - Левая сторона - Правая сторона |
3,4 | 3,0 | 3,5 | 3,4 | 2,9 | 3,4 |
| 3,4 | 3,0 | 3,5 | 3,3 | 3,0 | 3,4 |
Рис. 4. TSS (отдельные симптомы) при приеме 600 мг бенфотиамина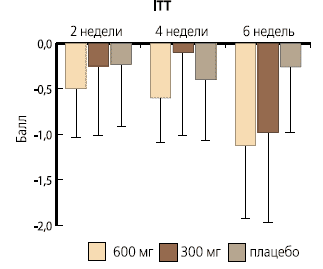 Рис. 3. TSS (различие с исходными данными)
Рис. 3. TSS (различие с исходными данными) 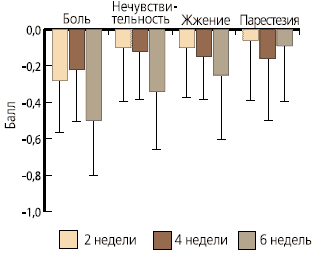 БезопасностьОтсутствие значимых изменений показателя HbA1c Отсутствие клинически значимых изменений метаболизма глюкозы, других лабораторных показателей, химического состава мочи, артериального давления или сердечного ритма 21 случай проявления отрицательных побочных эффектов у 14 пациентов (8,5% пациентов, принимавших исследуемый препарат) при сопоставимых долях среди получавших бенфотиамин (9,4%) и плацебо (8,0%) Наиболее часто сообщалось о желудочно-кишечных симптомах (6 пациентов, 5 получали бенфотиамин, 1 - плацебо) Аллергические кожные реакции у 2 пациентов, получавших бенфотиамин Прочие жалобы были неспецифичными Отсутствие неблагоприятных эффектов, связанных с лечением. ВыводыВ отношении двух показателей, NSS и TSS, был установлен положительный эффект 6-недельного лечения бенфотиамином пациентов с клинически выраженной диабетической полинейропатией. При анализе PP показателя NSS была достигнута статистическая значимость. Улучшение было более выражено при более высокой дозе бенфотиамина и усиливалось с течением времени лечения. К проблемам исследования BENDIP можно отнести значительный положительный эффект плацебо, несогласующиеся исходные характеристики для NSS, NDS и TSS (с большими межиндивидуальными различиями в TSS) и неравномерная реакция на лечение с точки зрения отдельных симптомов. Тем не менее клиническое испытание бенфотиамина подтверждает положительное воздействие препарата, продемонстрированное на экспериментальной модели. Благодаря каузальному улучшению нарушенного метаболизма глюкозы и другому (например, антиоксидантному) воздействию бенфотиамин расширяет возможности лечения пациентов с диабетической полинейропатией. *Stracke H., Gaus W, Federlin K., Achenbach U., Bretzel R. Benfotiamine in diabetic polyneuropathy (BENDIP): Results of a randomised, double blind, placebo-controlled clinical study. Exp Gin Endocrinol Diabetes 2008; DOI 10.I055/S-2008-1065351.
БезопасностьОтсутствие значимых изменений показателя HbA1c Отсутствие клинически значимых изменений метаболизма глюкозы, других лабораторных показателей, химического состава мочи, артериального давления или сердечного ритма 21 случай проявления отрицательных побочных эффектов у 14 пациентов (8,5% пациентов, принимавших исследуемый препарат) при сопоставимых долях среди получавших бенфотиамин (9,4%) и плацебо (8,0%) Наиболее часто сообщалось о желудочно-кишечных симптомах (6 пациентов, 5 получали бенфотиамин, 1 - плацебо) Аллергические кожные реакции у 2 пациентов, получавших бенфотиамин Прочие жалобы были неспецифичными Отсутствие неблагоприятных эффектов, связанных с лечением. ВыводыВ отношении двух показателей, NSS и TSS, был установлен положительный эффект 6-недельного лечения бенфотиамином пациентов с клинически выраженной диабетической полинейропатией. При анализе PP показателя NSS была достигнута статистическая значимость. Улучшение было более выражено при более высокой дозе бенфотиамина и усиливалось с течением времени лечения. К проблемам исследования BENDIP можно отнести значительный положительный эффект плацебо, несогласующиеся исходные характеристики для NSS, NDS и TSS (с большими межиндивидуальными различиями в TSS) и неравномерная реакция на лечение с точки зрения отдельных симптомов. Тем не менее клиническое испытание бенфотиамина подтверждает положительное воздействие препарата, продемонстрированное на экспериментальной модели. Благодаря каузальному улучшению нарушенного метаболизма глюкозы и другому (например, антиоксидантному) воздействию бенфотиамин расширяет возможности лечения пациентов с диабетической полинейропатией. *Stracke H., Gaus W, Federlin K., Achenbach U., Bretzel R. Benfotiamine in diabetic polyneuropathy (BENDIP): Results of a randomised, double blind, placebo-controlled clinical study. Exp Gin Endocrinol Diabetes 2008; DOI 10.I055/S-2008-1065351.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
 Рис. 2. РР
Рис. 2. РР Продолжительность лечения
Продолжительность лечения Рис. 3. TSS (различие с исходными данными)
Рис. 3. TSS (различие с исходными данными)  Безопасность
Безопасность