ХОБЛ: комплексное заболевание: Роль бронхиального и системного воспаления в патогенезе хронической обструктивной болезни легких
СтатьиПредыдущая статья | Оглавление | Следующая статья
Роль бронхиального и системного воспаления в патогенезе хронической обструктивной болезни легких
John R. Hurst
Реферат
Хроническая обструктивная болезнь легких (ХОБЛ) характеризуется, помимо прочего, наличием патологического воспалительного ответа в легких. Воспаление качественно и количественно отличается от такового у курильщиков и лиц с ненарушенной легочной функцией и сохраняется после прекращения курения. Имеются также данные в пользу наличия при ХОБЛ системного воспаления, которое, вероятно, берет начало в легких. По-видимому, системное воспаление играет немаловажную роль в патогенезе сопутствующих ХОБЛ заболеваний, в частности, сердечно-сосудистой системы. Для прогнозирования исходов и ответа на терапию представляется перспективным количественное определение так называемых маркеров воспаления, однако прежде чем результаты исследований можно будет вводить в клиническую практику, необходима их дальнейшая оценка и подтверждение.
Согласно современному определению, хроническая обструктивная болезнь легких (ХОБЛ) характеризуется, помимо прочего, наличием в легких «патологического воспалительного ответа на вредные частицы или газы» [1]. Таким образом, ХОБЛ определяется как заболевание отчасти воспалительного генеза. В настоящее время общепризнано, что воспаление при ХОБЛ не ограничивается легкими, а распространяется также на системный кровоток, где может участвовать в развитии сопутствующих ХОБЛ патологий. В периоды обострений легочное и системное воспаление нарастает. В обзоре подытоживаются данные в пользу этой концепции и обсуждаются перспективы применения в клинической практике тестов на так называемые маркеры воспаления.
Хроническая обструктивная болезнь легких как хроническое воспалительное заболевание
В развитых странах главной по частоте причиной ХОБЛ, несомненно, является вдыхание сигаретного дыма. В нем содержится большое число токсинов, способных провоцировать воспалительный ответ в дыхательных путях. Важно понимать, что по своему характеру этот ответ является нормальным. Согласно современным данным, характер воспалительных процессов у больных ХОБЛ - курящих лиц с наследственно обусловленной чувствительностью к влиянию сигаретного дыма - отличается как по количественным, так и по качественным показателям и сохраняется даже после прекращения курения.
Это хорошо видно на примере данных, полученных Saetta с соавт. [2] в ходе изучения гистологии бронхов у курильщиков, страдающих ХОБЛ и с нормальной легочной функцией. У страдающих ХОБЛ курильщиков отмечена более высокая плотность Т-лимфоцитов CD8+ бронхиальной стенки, чем у курящих лиц с сохранной функцией легких (при этом плотность Т-лимфоцитов CD4+, нейтрофилов и макрофагов не отличалась). Напротив, Vachier с соавт. [3] выявили качественные различия бронхиального воспаления в зависимости от наличия ХОБЛ у курящего. Так, у больных ХОБЛ Т-лимфоциты CD8+ обнаружены вместе с нейтрофилами и макрофагами, а у лиц со здоровой легочной функцией - вместе с эозинофилами. Анализ биоптатов с внутренней стенки бронхов более 100 больных ХОБЛ одинаковой степени тяжести -курильщиков и бывших курильщиков - не показал различий ни по числу клеток воспаления каждого типа, ни и по концентрации медиаторов воспаления [4]. Эти данные показывают, что характер воспаления у больных ХОБЛ сохраняется и после прекращения курения.
Большинство исследований бронхиального воспаления посвящены изучению эндобронхиальных биоптатов, анализу мокроты и составу выдыхаемых маркеров. Вместе с тем, основное место локализации характерной для ХОБЛ дыхательной обструкции - это мелкие бронхи и бронхиолы (внутренним диаметром менее 2 мм). Статья Hogg с соавт. [5] - первая и основополагающая работа, в которой воспаление в этой части легких всесторонне изучено у больных на всех стадиях ХОБЛ. По мере возрастания тяжести ХОБЛ авторы наблюдали прогрессирующее утолщение стенки бронха, вызванное аккумуляцией клеток воспаления, а также накопление избытка слизи в просвете бронха. Инфильтрат стенки бронха преимущественно состоял из нейтрофилов, макрофагов и Т-лимфоцитов (CD4 и CD8). В случае тяжелой и крайне тяжелой степени (III и IV стадии по классификации Международной инициативной группы по проблемам хронических обструктивных заболеваний легких - GOLD) лимфоциты были организованы в фолликулы, что указывает на развитие адаптивного иммунного ответа-вероятно, как реакции на колонизацию дыхательных путей микрофлорой, что характерно для поздних стадий ХОБЛ. Уровень маркеров воспаления выше у пациентов с более низкими показателями бактериального заселения и зависит как от состава патогенной флоры, так и от ее количества [6].
Показана эффективность ингаляционных кортикостероидов (ИКС) в снижении частоты обострений ХОБЛ. Некоторые данные указывают на то, что в мелких бронхах и бронхиолах ИКС оказывают противовоспалительное действие. Так, в ограниченном по масштабу трехмесячном рандомизированном плацебо-контролируемом клиническом испытании ингаляционного флутиказона показано снижение индекса CD8:CD4 и числа субэпителиальных тучных клеток, хотя изменение числа лимфоцитов CD8+ и нейтрофилов отсутствовало [7].
Системное воспаление
При ХОБЛ воспаление не ограничивается легкими, его признаки обнаруживаются также и в крови. Взгляды автора на воспалительные процессы, протекающие у больных ХОБЛ, представлены на Рис. 1. В статье, посвященной систематическому обзору и метаанализу данных 14 научных работ, Gan с соавт. [8] сообщают о подъеме концентрации С-реактивного белка, фибриногена и альфа-фактора некроза опухоли (ФНО), а также более высоком числе лейкоцитов в крови больныхХОБЛ (включая и бывших курильщиков) по сравнению с контрольными пациентами. Важно подчеркнуть, что системное воспаление имеет место не у всех пациентов. Причины и следствия этого требуют дальнейшего изучения.
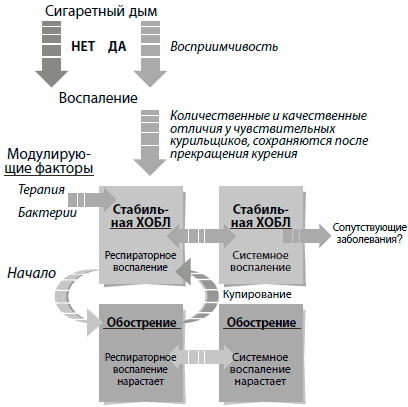
Рис. 1. Воспаление при хронической обструктивной болезни легких (ХОБЛ): схема.
Невыясненными остаются также истоки наблюдаемого при ХОБЛ системного воспаления. Чаще других в литературе упоминается гипотезао его «перетекании» (spillover) из легких. Не исключено также, что системное воспаление возникает в результате действия сигаретного дыма на другие ткани, в частности, эндотелий сосудов. Для гена, кодирующего С-реактивный белок, характерен полиморфизм, связанный с увеличением его концентрации в крови, однако у лиц с такими генетическими вариантами увеличения риска развития ХОБЛ, по-видимому, не происходит. Эти данные свидетельствуют против «обратной» гипотезы о том, что системное воспаление провоцирует воспаление в легких [9]. Прямая связь между тяжестью бронхиального и системного воспаления у лиц со стабильной ХОБЛ не доказана, но последние данные указывают на то, что бронхиальное воспаление возникает раньше системного, что, по-видимому, свидетельствует в пользу гипотезы «перетекания» [10].
В настоящее время изучение системного воспаления при ХОБЛ сосредоточено на двух аспектах. Во-первых, учитывая практические трудности обнаружения и количественного измерения бронхиального воспаления таким способом, который позволял бы при необходимости воспроизвести результат, представляется перспективной оценка воспалительной нагрузки путем определения содержания в крови маркеров воспаления. Эта методика обсуждается ниже в части, посвященной маркерам воспаления. Во-вторых, в настоящее время общепризнано, что ХОБЛ чревата развитием целого ряда внелегочных патологий и сопутствующих заболеваний, в том числе таких, как возрастание риска сердечно-сосудистых заболеваний, остеопороз, дисфункция скелетной мускулатуры и истощение. Предполагается, что отчасти в их основе лежат системные воспалительные механизмы (хотя, опять-таки, не исключено, что данные патологии - одно из проявлений генетически обусловленной чувствительности к действию сигаретного дыма на различные ткани-мишени). Решение этого вопроса представляет собой трудную задачу. Хотя связь между системным воспалением и сердечнососудистыми заболеваниями, несомненно, существует [11], гаплотипы, связанные с подъемом концентрации С-реактивного белка, сами по себе не сопряжены с риском сердечно-сосудистых патологий [12]. Поэтому более вероятно, что С-реактивный белок-это маркер, а не причина таких сопутствующих заболеваний. Риск сердечно-сосудистых заболеваний возрастает также при хронических воспалительных процессах, в частности, ревматоидном артрите. При ХОБЛ имеется прямая связь между величиной системного воспалительного ответа и жесткостью артерий [14]. Некоторые авторы также связывают жесткость аорты и системное воспаление с остеопорозом.
Ингаляционные кортикостероиды не снижают концентрацию маркеров системного воспаления [15] (однако, не исключено, влияют на содержание легочного сурфактанта D и других легочных маркеров). В клиническом испытании не показано также улучшение исхода ХОБЛ на фоне терапии инфликсимабом - препаратом моноклональных антител к альфа-фактору некроза опухоли [16]. Более того, данные этой работы указывают на возможное возрастание риска злокачественных новообразований и пневмонии на фоне инфликсимаба. Отметим, что в терапии ревматической болезни препаратами этого типа получен противоположный, резко положительный эффект.
Таким образом, для ХОБЛ характерно развитие системного воспаления, однако лежащие в его основе механизмы, связь с сопутствующими патологиями, а также целесообразность и практическая возможность подавления воспалительных процессов требуют глубокого изучения.
Воспаление дыхательных путей и системное воспаление в фазе обострения
Провоцирующим фактором обострений ХОБЛ обычно оказывается эпизод трахеобронхиальной вирусной или бактериальной инфекции [17], неизбежно приводящий к активизации воспаления в дыхательных путях. Схема этих процессов показана на Рис. 2. Так как самочувствие пациента в эти периоды резко ухудшается, проведение биопсии затруднительно. Поэтому исследования, посвященные обострениям ХОБЛ, проводятся главным образом на материале бронхиального секрета и выдыхаемого воздуха. Такой подход приводит к существенному разбросу результатов, поскольку стандартной методики анализа подобных образцов нет. Тем не менее, подытоженные в недавнем обзоре [18] данные ряда исследований указывают на активизацию воспалительных процессов в дыхательных путях во время обострений ХОБЛ.
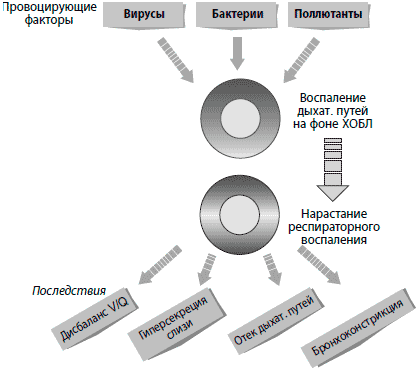
Рис. 2. Патофизиология и этиология обострений хронической обструктивной болезни легких (ХОБЛ). Сокращение: V/Q - вентиляция и перфузия.
Показана прямая, слабая, но статистически достоверная корреляция между степенью респираторного и системного воспаления, отсутствующая до начала обострения [19].
В ряде работ (их обзор приводится в [18]) показано также нарастание системного воспаления на фоне обострения ХОБЛ. Остается неясной связь этих явлений с увеличением риска инфаркта миокарда в период сразу после обострения [20].
Клиническое купирование обострения в ответ на соответствующую терапию приводит к падению уровня системных и респираторных маркеров воспаления.
Практическое значение количественного измерения степени активности воспаления: биологические маркеры
Обозначив ХОБЛ как воспалительное заболевание дыхательных путей, при котором признаки воспаления обнаруживаются также в крови, а респираторное и системное воспаление нарастают во время обострений, попытаемся ответить на вопрос, имеют ли эти знания практическое значение для врача-клинициста. В настоящее время с некоторой осторожностью можно утверждать, что да, имеют.
Под биологическим маркером понимается «показатель, объективно измеряемый и оцениваемый, служащий индикатором нормальных биологических или патологических процессов либо индикатором фармакологического ответа на терапевтическое вмешательство» [21]. В последнее время большой интерес вызывает изучение маркеров воспаления в дыхательных путях и крови больных ХОБЛ в качестве возможных биологических маркеров. Ввиду трудностей, связанных со взятием и обработкой биологических образцов из дыхательных путей и оценкой воспаления в них, большая часть работ в этой области проводилась на материале сыворотки и плазмы крови.
Изучение биомаркеров воспаления у больных ХОБЛ перспективно в нескольких отношениях. Предполагается, что информативный биомаркер позволит судить о прогнозе, определять фенотип заболевания и предсказывать ответ на терапию. Особенно много работ посвящено поиску и анализу биомаркеров обострения как способа объективно дифференцировать его от базового состояния и от других причин нарастания симптоматики (пневмонии, тромбоэмболии легочной артерии), а также в целях выяснения этиологии и тяжести обострений и прогнозирования следующих за ними событий. Стоит отметить крайне гетерогенный характер как самой ХОБЛ, так и ее обострений, поэтому выделение единственного универсального биомаркера, пригодного для прогнозирования исходов во всех случаях, - весьма трудная задача.
Из биомаркеров, имеющих клиническое значение в терапии ХОБЛ, широко используется только α1-антитрипсин [22]. Выявление полиморфных вариантов соответствующего гена среди пациентов с ранним началом и/или высокой тяжестью ХОБЛ имеет значение как для ведения самого пациента и прогноза заболевания, так и для наблюдения других членов семьи. Ниже приводятся другие примеры использования биомаркеров для решения конкретных задач терапии ХОБЛ, но в целом накопленных данных пока недостаточно для внедрения методики в клиническую практику.
По итогам весьма непредвзято проведенного анализа, предпринятого Nicholas с соавт. [23], сообщается о перспективности использования липокалина и аполипопротеина А1 для дифференциации больных ХОБЛ в стабильной фазе от здоровых курильщиков. С подъемом концентрации С-реактивного белка на фоне стабильной ХОБЛ связывают возрастание риска связанной с ХОБЛ смерти и госпитализации по поводу ХОБЛ [24].
В крупнейшем на сегодня исследовании, посвященном методам дифференциации обострений от стабильного состояния, изучены 36 маркеров плазмы у 90 пациентов. Наиболее полезным из изученных маркеров оказался С-реактивный белок, как отдельно, так и в комбинации с другими маркерами, однако чувствительность и специфичность этого метода недостаточны для клинического применения [25]. Чувствительность клинического порога 5 мг/л, широко применяемого для дифференцирования обострений от стабильного состояния, составляет 74%, специфичность - 58%. Это связано с тем, что у многих больных концентрация С-реактивного белка в стабильном состоянии превышает 5 мг/л, аобострения, напротив, не всегда сопровождаются существенным подъемом уровня системных маркеров воспаления.
По данным Stolz с соавт. [26], проба на прокальцитонин служит ориентиром при проведении антибактериальной терапии обострений ХОБЛ. Прокальцитонин является маркером бактериальной инфекции. В упомянутом рандомизированном исследовании врачи получали инструкцию не назначать антибиотики, если концентрация прокальцитонина была низкой. Показано, что проведение терапии с контролем уровня прокальцитонина позволяет снизить антибиотиковую нагрузку на пациента без ухудшения клинического исхода. Эти данные представляют большой интерес, поскольку на сегодняшний день это единственное рандомизированное клиническое испытание у больных ХОБЛ, показавшее возможность влиять на клинический исход, используя биомаркеры.
Тяжесть обострения представляет собой сложное и плохо определенное понятие, включающее в себя тяжесть фонового заболевания (ХОБЛ) и нагрузку обострения, однако имеются данные (также требующие проверки), указывающие на возможную связь между уровнем копептина и длительностью госпитализации [27], а также между уровнем натрийуретического пептида типа В (НУП-В) и необходимостью в проведении интенсивной терапии [28]. Согласно данным одного из исследований, уровень предшественника адреномедуллина позволяет судить о вероятности наступления смерти в течение 2 лет [29].
Сейчас не вызывает сомнений тот факт, что обострения наступают не случайно, а группируются во времени таким образом, что в период после обострения риск наступления следующего повышен [30]. Возможно, неудачи при попытках купировать системный воспалительный ответ после первого обострения объясняются именно этим обстоятельством. У больных с повышенным уровнем С-реактивного белка в первые 2 недели после обострения риск его рецидива более высок, чем в последующие [31]. Если эти данные подтвердятся в дальнейших работах, они станут основанием для принятия мер по усиленному наблюдению больных и раннему вмешательству в следующие за обострениями «опасные» периоды. Принятая сейчас концепция избирательной постановки на контроль пациентов, подверженных «частым» обострениям, в этом случае также потребует пересмотра.
Выводы
Для хронической обструктивной болезни легких характерно респираторное и системное воспаление, интенсивность которого нарастает в периоды обострений. Системное воспаление сопряжено с развитием сопутствующих патологий. Уровень маркеров воспаления является перспективным показателем, который позволит судить о статусе заболевания, его тяжести, фенотипе, исходе и вероятном ответе на терапию. Связь данных параметров с уровнем маркеров воспаления показана в ряде работ. Проверка этих предварительных выводов представляет собой неотложную задачу, так как только в этом случае возможно внедрение методики оценки воспаления в повседневную практику терапии ХОБЛ.
ЛИТЕРАТУРА
1. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management and prevention of chronic obstructive lung disease. Updated December 2009.
2. Saetta M, Di Stefano A, Turato G, et al. CD8+ T-lymphocytes in the peripheral airways of smokers with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1998;157.822-826.
3. Vachier I, Vignola AM, Chiappara G, et al. Inflammatory features of nasal mucosa in smokers with and without COPD. Thorax 2004;59:303-307.
4. Gamble E, Grootendorst DC, Hattotuwa K, et al. Airway mucosal inflammation in COPD is similar in smokers and ex-smokers: a pooled analysis. Eur Respir J 2007;30:467-471.
5. Hogg JC, Chu F, Utokaparch S, et al. The nature of small-airway obstruction in chronic obstructive pulmonary disease. N Engl J Med 2004;350:2645-2653.
6. Hill AT, Campbell EJ, Hill SL, Bayley DL, Stockley RA. Association between airway bacterial load and markers of airway inflammation in patients with stable chronic bronchitis. Am J Med 2000;109: 288-295.
7. Hattotuwa KL, Gizycki MJ, Ansari TW, Jeffery PK, Barnes NC. The effects of inhaled fluticasone on airway inflammation in chronic obstructive pulmonary disease: a double-blind, placebo-controlled biopsy study. Am J Respir Crit Care Med 2002;165:1592-1596.
8. Gan WQ, Man SF, Senthilselvan A, Sin DD. Association between chronic obstructive pulmonary disease and systemic inflammation: a systematic review and a meta-analysis. Thorax 2004;59:574-580.
9. van Durme YM, Verhamme KM, Aarnoudse AJ, et al. C-reactive protein levels, haplotypes, and the risk of incident chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2009;179:375-382.
10. He Z, Chen Y, Chen P, Wu G, Cai S. Local inflammation occurs before systemic inflammation in patients with COPD. Respirology 2010;15:478-484.
11. Kaptoge S, Di Angelantonio E, Lowe G, et al; Emerging Risk Factors Collaboration. C-reactive protein concentration and risk of coronary heart disease, stroke, and mortality: an individual participant meta-analysis. Lancet 2010;375:132-140.
12. Zacho J, Tybjaerg-Hansen A, Jensen JS, Grande P, Sillesen H, Nordestgaard BG. Genetically elevated C-reactive protein and ischemic vascular disease. N Engl J Med 2008;359:1897-1908.
13. del Rincon ID, Williams K, Stern MP, Freeman GL, Escalante A. High incidence of cardiovascular events in a rheumatoid arthritis cohort not explained by traditional cardiac risk factors. Arthritis Rheum 2001 ;44:2737-2745.
14. Sabit R, Bolton CE, Edwards PH, et al. Arterial stiffness and osteoporosis in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2007;175:1259-1265.
15. Sin DD, Man SF, Marciniuk DD, et al. The effects of fluticasone with or without salmeterol on systemic biomarkers of inflammation in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2008;177:1207-1214.
16. Rennard SI, Fogarty C, Kelsen S, et al. The safety and efficacy of infliximab in moderate to severe chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2007;175:926-934.
17. Hurst JR, Wedzicha JA. The biology of a chronic obstructive pulmonary disease exacerbation. Clin Chest Med 2007;28:525-536.
18. Hurst JR. Airway and systemic markers at exacerbation. In: Wedzicha JA, Martinez FJ (eds). Chronic Obstructive Pulmonary Disease Exacerbations. Lung Biology in Health and Disease, vol 228. New York: Informa Healthcare. 2009; pp 61 -73.
19. Hurst JR, Perera WR, Wilkinson TM, Donaldson GC, Wedzicha JA. Systemic and upper and lower airway inflammation at exacerbation of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2006;173:71-78.
20. Donaldson GC, Hurst JR, Smith CJ, Hubbard RB, Wedzicha JA. Increased risk of myocardial infarction and stroke following exacerbation of COPD. Chest 2010;137:1091 -1097.
21. Biomarkers Definitions Working Group. Biomarkers and surrogate endpoints: preferred definitions and conceptual framework. Clin Pharmacol Ther 2001 ;69:89-95.
22. Kohnlein T, Welte T. Alpha-1 antitrypsin deficiency: pathogenesis, clinical presentation, diagnosis and treatment. Am J Med 2008;121:3-9.
23. Nicholas BL, Skipp P, Barton S, et al. Identification of lipocalin and apolipoprotein A1 as biomarkers of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2010;181:1049-1060.
24. Dahl M, Vestbo J, Lange P, Bojesen SE, Tybjaerg-Hansen A, Nordestgaard BG, C-reactive protein as a predictor of prognosis in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2007;175:250-255.
25. Hurst JR, Donaldson GC, Perera WR, et al. Use of plasma biomarkers at exacerbation of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2006;174:867-874.
26. Stolz D, Christ-Crain M, Bingisser R, et al. Antibiotic treatment of exacerbations of COPD: a randomized, controlled trial comparing procalcitonin-guidance with standard therapy. Chest 2007;131:9-19.
27. Stolz D, Christ-Crain M, Morgenthaler NG, et al. Copeptin, C-reactive protein, and procalcitonin as prognostic biomarkers in acute exacerbation of COPD. Chest 2007;131:1058-1067.
28. Stolz D, Breidthardt T, Christ-Crain M, et al. Use of В-type natriuretic peptide in the risk stratification of acute exacerbations of COPD. Chest 2008;133:1088-1094.
29. Stolz D, Christ-Crain M, Morgenthaler NG, et al. Plasma pro-adrenomedullin but not plasma pro-endothelin predicts survival in exacerbations of COPD. Chest 2008;134:263-272.
30. Hurst JR, Donaldson GC, Quint JK, Goldring JJ, Baghai-Ravary R, Wedzicha JA. Temporal clustering of exacerbations in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2009;179:369-374.
31. Perera WR, Hurst JR, Wilkinson TM, et al. Inflammatory changes, recovery and recurrence at COPD exacerbation. Eur Respir J 2007;29:527-534.
Предыдущая статья | Оглавление | Следующая статья
