Легочная гипертензия: взгляд детского пульмонолога
СтатьиОпубликовано в журнале: «ПРАКТИКА ПЕДИАТРА»; июнь; 2016; стр. 10-15.
С.Э. Дьякова, к. м. н., в. н. с. отдела хронических воспалительных и аллергических болезней легких ОСП НИКИ педиатрии им. Ю.Е. Вельтищева
ГБОУ ВПО РНИМУ им.Н.И. Пирогова Минздрава России, г. Москва
Ключевые слова: легочная гипертензия, пульмонология, дети
Keywords: pulmonary hypertension, pulmonology, children
В практике детского пульмонолога пациенты с легочной гипертензией (ЛГ) встречаются относительно нечасто: по статистике, ЛГ имеют примерно 1,9 на 1000 рождающихся ежегодно детей, а распространенность легочной артериальной гипертензии составляет 15 случаев на 1 млн человек [5, 11, 18].
Хронические заболевания легких в 80-90% случаев являются причиной формирования хронического легочного сердца и сопровождаются развитием ЛГ у 30-50% больных. При отсутствии своевременной адекватной диагностики и лечения эта патология может быстро приводить к фатальному исходу. Установлено, что декомпенсированное хроническое легочное сердце в 30-37% случаев служит причиной смерти от недостаточности кровообращения и составляет 12,6% в структуре причин летальности от сердечно-сосудистых заболеваний. Причем многие причины ЛГ у детей значительно отличаются от таковых у взрослых пациентов [3, 5].
Известно, что малый круг кровообращения состоит из сосудистых элементов, которые находятся в анатомической и функциональной взаимосвязи. Разветвленная сеть артериовенозных анастомозов соединяет терминальные артериолы с легочными венами. В норме объем кровотока, минующего капилляры, невелик. Изменения тонуса стенки анастомозов обеспечивает расширение и сужение их просвета вплоть до полного закрытия. При повышении легочного артериального давления анастомозы, обеспечивая кровоток в обход капилляров, ограничивают этим дальнейшее повышение давления и предотвращают перегрузку давлением правого желудочка (ПЖ) [3, 6].
При этом малый круг кровообращения (МКК) осуществляет депонирование крови, обеспечение питанием респираторной ткани легких, реабсорбцию альвеолярной жидкости (дренажная функция) и нейтрализацию эмболов в венозной крови (фильтрационная функция), а также отвечает за транспортировку крови и газообмен.
Нормальные легочные сосуды оказывают малое сопротивление кровотоку. Разница средних давлений в легочной артерии (ЛА) и легочной вене составляет около 10 мм рт. ст. При физической нагрузке легочной кровоток увеличивается до 30-40 л/мин, что повышает среднее давление в МКК. В норме такое повышение незначительно, так как при этом снижается сопротивление в легких в результате расширения функционирующих и раскрытия закрытых капилляров. В патологических условиях увеличение кровотока может вызвать выраженную ЛГ с повышением легочного сосудистого сопротивления. К вазоспазму также приводят уменьшение напряжения кислорода в альвеолах (ангиоспастический рефлекс Савицкого - Эйлера -Лильестранда), нарушение кислотно-основного состояния крови, возрастание концентрации в крови биологически активных веществ (ангиотензина II, серотонина и т. д.) [3, 6].
В зависимости от локализации сопротивления кровотоку различают прекапиллярную, капиллярную и посткапиллярную ЛГ. Прекапиллярная ЛГ характеризуется нарастанием сопротивления в артериальном отделе МКК, что обусловлено падением парциального давления кислорода в альвеолах при обструктивных заболеваниях легких, системных васкулитах и тромбоэмболических осложнениях, а также при ограничении подвижности грудной клетки при кифосколиозе, ожирении и пневмофиброзе. Капиллярная ЛГ возникает при несоответствии объема кровотока и капиллярного русла. При заболеваниях легких эта форма гипертензии часто сочетается с прекапиллярной, поэтому условно объединяется с ней. Посткапиллярная ЛГ развивается при повышении давления в левом предсердии более 20 мм рт. ст. и наблюдается при митральных пороках и левожелудочковой недостаточности. Длительное повышение давления способствует развитию необратимых органических изменений сосудистого русла МКК, которые и становятся причиной стойкой и прогрессирующей ЛГ [3, 6].
Существующие современные международные рекомендации по диагностике и лечению ЛГ, созданные в 2009 году объединенной рабочей группой Европейского кардиологического (ESC) и Европейского респираторного обществ (ERS), одобрены различными авторитетными профессиональными врачебными Ассоциациями и дополнены в 2015 году экспертами Американской кардиологической ассоциации (AHA) и Американского общества специалистов в области торакальной медицины [1, 5, 11, 18, 20].
Согласно этим документам, под легочной гипертензией (ЛГ) понимают повышение среднего давления в легочной артерии (ЛА) в покое (по данным катетеризации правых отделов сердца) до ≥25 мм рт. ст. и ≥30 мм рт. ст. при физической нагрузке, хотя часто легочная гипертензия у детей сопряжена со значительно более высокими показателями. Различают артериальную ЛГ (при ней капиллярное давление или давление в левом предсердии менее 15 мм рт. ст.), венозную и смешанную формы (при этих формах повышено давление и в левом предсердии) ЛГ. По уровню среднего артериального давления в ЛА выделяют 4 степени ЛГ: первая - 25-40 мм рт. ст., вторая - 41-75 мм рт. ст., третья - 76-110 мм рт. ст., четвертая -выше 110 мм рт. ст. [5, 11, 20].
ЛГ представляет собой патофизиологическое явление, к которому может приводить целый ряд клинических состояний, в частности, она может осложнять большинство сердечно-сосудистых заболеваний и болезней дыхательной системы. Согласно классификации ЛГ 2008 года, выделяют пять основных типов ЛГ:
1. Легочная артериальная гипертензия (включающая два подтипа: веноокклюзивная болезнь легких и/или легочный капиллярный гемангиоматоз и персистирующая ЛГ у новорожденных).
2. ЛГ вследствие патологии левых отделов сердца.
3. ЛГ вследствие болезней легких и/или гипоксии.
4. Хроническая тромбоэмболическая ЛГ и прочие варианты обструкции легочной артерии.
5. ЛГ с неясными и/или многофакторными механизмами.
У детей наиболее часто встречается легочная артериальная гипертензия и ЛГ, ассоциированная с патологией дыхательной системы и/или гипоксией [1, 5].
Среди причин ЛГ, ассоциированной с патологией дыхательной системы и/или гипоксией, основными являются хронические обструктивные заболевания легких; к более редким этиологическим факторам ЛГ этого типа в детском возрасте относятся пороки развития бронхолегочной системы, интерстициальные заболевания легких, легочная патология со смешанными обструктивно-рестриктивными нарушениями, нарушения дыхания во время сна, альвеолярная гиповентиляция, высокогорная легочная гипертензия, легочная гипертензия вследствие хронических тромботических и/или эмболических заболеваний, а также системные заболевания с поражением легких (саркоидоз, гистиоцитоз легочных клеток Лангерганса, лимфангиоматоз, васкулиты).
Принципиально в развитии ЛГ можно выделить три стадии. На первой стадии увеличенное легочное давление является единственной гемодинамической аномалией: больные не имеют отчетливых симптомов заболевания, но может отмечаться одышка при физической нагрузке. На второй стадии при уменьшении сердечного выброса появляется развернутая клиническая симптоматика в виде гипоксемии, одышки, синкопальных состояний, при этом давление в ЛА сохраняется на стабильно высоком уровне. С появлением правожелудочковой недостаточности наступает третья стадия заболевания: несмотря на стабильно высокие значения легочного давления, резко падает сердечный выброс, появляются венозный застой и периферические отеки. Продолжительность каждой стадии может быть различной; течение ЛГ может быть острым и хроническим; быстро, умеренно и медленно прогрессирующим; крайне редко встречаются случаи спонтанного регресса заболевания.
Начальные признаки ЛГ при заболеваниях легких обычно маскируются проявлениями основного заболевания (приступный период бронхиальной астмы, спонтанный пневмоторакс, выраженный плевральный выпот и т. д.). Иначе протекает ЛГ при хронических обструктивных болезнях легких: ЛГ и вызванная ею патология сердца и недостаточность кровообращения занимают первое место среди осложнений этих заболеваний, определяют жизненный прогноз пациентов и эффективность их лечения.
Основной жалобой у детей с ЛГ бывает одышка. Именно поэтому нередко первым специалистом, к кому могут обращаться пациенты с ЛГ, является пульмонолог. В дебюте заболевания одышка возникает только при физической нагрузке, по мере прогрессирования заболевания одышка появляется в покое, иногда сопровождается приступами удушья. Чем выше давление в легочной артерии, тем ярче выражена одышка.
Другим характерным проявлением ЛГ у детей являются обморочные состояния (синкопе), которые могут присутствовать уже на ранних стадиях заболевания и учащаться по мере его прогрессирования при физической нагрузке, во время игр, эмоционального перенапряжения, реже - в покое. Причинами возникновения синкопе при ЛГ считают снижение церебрального кровотока, вазовагальный рефлекс с ЛА, острую правожелудочковую недостаточность, снижение минутного объема кровообращения [1, 2, 4]. Возможны приступы болей в грудной клетке, которые связывают с ишемией правого желудочка под влиянием общей гипоксии на миокард, относительной недостаточностью коронарного кровотока при гипертрофии миокарда правого желудочка и снижении сердечного выброса, рефлекторным спазмом коронарных артерий из-за расширения ствола ЛА. Для пациентов с ЛГ характерна усиленная пульсация во II межреберье слева и в эпигастральной области, обусловленная гипертрофией правого желудочка (ПЖ), при аускультации определяется расщепление I тона на верхушке (запаздывание закрытия трехстворчатого клапана в условиях ЛГ) и усиление II тона над ЛА. При появлении правожелудочковой недостаточности справа от грудины выслушивается III тон, а также диастолический шум во II межреберье слева из-за недостаточности клапанов ЛА (шум Грехэма - Стилла). При возникновении признаков правожелудочковой недостаточности появляются периферические отеки, гепатомегалия, периферический цианоз. Из-за сдавления гортанного нерва расширенной ЛА может появиться осиплость голоса [3-5].
При рентгенографии органов грудной клетки у детей с ЛГ могут быть не только диагностированы заболевания легких, при которых характерна ЛГ (эмфизема легких, пневмосклероз, туберкулез, саркоидоз, пороки легких и т. д.), но и выявлены патогномоничные признаки ЛГ, такие как расширение корней легких, усиление легочного рисунка, общее или неравномерное повышение прозрачности легочных полей, интерстициальный отек, выбухание дуги ЛА по левому контуру, увеличение коэффициента Мура (процентное отношение поперечника дуги ЛА к половине диаметра грудной клетки на уровне диафрагмы (норма до 30%)), расширение нисходящей ветви правой ЛА (рис.). При этом индекс Мура и ширина правой ЛА коррелируют с высотой давления в ЛА и могут быть использованы в качестве критериев наличия и выраженности ЛГ. На ранних стадиях ЛГ до развития дилатации ПЖ размеры сердца могут не изменяться; по мере нарастания ЛГ и увеличения ПЖ на рентгенограмме грудной клетки в боковой проекции ретростернальное пространство выполняется тенью ПЖ. Еще большей информационной ценностью для верификации диагноза обладает компьютерная томография легких [1, 4, 6].
Рисунок
Повышение прозрачности легочной ткани, усиление легочного рисунка и выбухание дуги легочной артерии у ребенка 12 лет с ЛГ 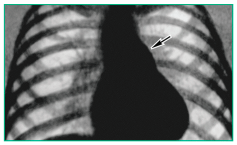
При электрокардиографии ЛГ можно заподозрить по наличию признаков перегрузки и гипертрофии правых отделов сердца: отклонение электрической оси сердца вправо, перегрузка правого предсердия и правого желудочка, отрицательный зубец Т в грудных отведениях, транзиторная блокада правой ножки пучка Гиса [1, 3, 6].
Тем не менее, электрокардиография и рентгенография дают возможность лишь косвенно судить о наличии ЛГ. В течение длительного времени единственным методом исследования, позволявшим оценивать состояние правых отделов сердца, получать характеристики внутрисердечного кровотока и определять давление в правых отделах сердца и ЛА, была катетеризация правых отделов сердца и ЛА, которая на сегодняшний день продолжает использоваться для исключения кардиальных причин ЛГ (врожденные пороки сердца), определения основных параметров легочной и центральной гемодинамики, а также для подбора эффективных вазодилататоров. Однако, в силу инвазивности и высоких рисков осложнений, эта методика не может быть рекомендована для динамического наблюдения детей с ЛГ [11, 18].
С этой целью успешно используется допплерэхокардиографический метод диагностики (ЭхоКГ), позволяющий неинвазивно в режиме реального времени оценивать размеры и движение сердечных структур, получать характеристики внутрисердечной гемодинамики и определять давление в камерах сердца и давления в ЛА [1, 4, 14]. Кроме этого, ЭхоКГ необходима для исключения врожденных аномалий сердца и оценки тяжести гемодинамических нарушений. Помимо неинвазивного определения систолического, диастолического и среднего давления в ЛА, с помощью ЭхоКГ можно оценить общее легочное сосудистое сопротивление. В ответ на перегрузку давлением, развиваются изменения конфигурации и функциональных характеристик ПЖ сердца, выявляется его дилатация, в последующем по мере прогрессирования ЛГ - дилатация ствола и ветвей ЛА. При длительно существующей ЛГ в ответ на перегрузку давлением развивается гипертрофия стенки ПЖ и межжелудочковой перегородки.
Достоверно установлено, что показатели легочной гемодинамики при проведении ЭхоКГ сопоставимы с данными, полученными при катетеризации ЛА. В связи с этим всем младенцам с бронхолегочной дисплазией в анамнезе рекомендовано проведение эхокардиографического скрининга для исключения формирования ЛГ. При обследовании детей с ЛГ с помощью ЭхоКГ рекомендуется проведение теста с физической нагрузкой, который позволяет уточнять степень функциональных нарушений.
Немаловажным для дифференциальной диагностики ЛГ является определение газового состава крови, в частности, определение насыщения ее кислородом: снижение этого показателя наблюдается при сбросе крови справа налево, а также при ЛГ, сочетающейся с дыхательной недостаточностью (хронические обструктивные заболевания легких, массивная тромбоэмболия легочной артерии и т. д.) [1, 5, 11].
Исследование функции легких позволяет выявить вид и степень выраженности вентиляционных нарушений (обструктивные, рестриктивные смешанные). В целях дифференциальной диагностики, наряду со спирометрией, целесообразно проведение бодиплетизмографии и оценки диффузионной способности легких. У детей старше 6 лет для контроля переносимости нагрузок должна использоваться проба с 6-минутной ходьбой. Если ребенок относится к группе риска нарушений дыхания во сне, то в план его обследования должна включаться полисомнография.
Для верификации диагноза ЛГ в детской практике редко прибегают к открытой биопсии легких с последующим морфометрическим исследованием мелких сосудов, поскольку она сопряжена со значительными рисками и не обладает высокой информативностью в связи с неравномерным поражением сосудов легких.
Таким образом, диагностика ЛГ у детей предполагает проведение комплексного обследования с целью установления диагноза, оценки клинического класса и типа ЛГ, уровня давления в ЛА и оценки функционального и гемодинамического статуса пациентов с определением стадии заболевания.
У детей с хроническими бронхолегочными заболеваниями необходимо регулярное проведение комплексного кардиологического обследования (ЭКГ, ЭхоКГ) с целью диагностики патологии легочной гемодинамики и предупреждения формирования легочного сердца. Раннее выявление ЛГ позволяет начать своевременное лечение и предупредить развитие сердечной декомпенсации.
Основные подходы к лечению детей с ЛГ включают в себя ежедневные физические нагрузки по переносимости, что способствует улучшению качества жизни и уменьшению клинической симптоматики [16], а также профилактику инфекционных заболеваний (вакцинирование от гриппа и пневмококковой инфекции), исключение активного и пассивного курения. Наибольшее внимание должно быть уделено лечению основного заболевания, ликвидации гипоксии, снижению давления в малом круге кровообращения, профилактике дистрофической гипоксии миокарда и лечению правожелудочковой недостаточности [7].
Хотя гипоксия не является единственным этиологическим фактором ЛГ, однако развивающаяся гипоксемия у больных с хронической бронхолегочной патологией обусловливает необходимость применения кислорода в качестве терапевтического средства [21].
Специфическая терапия ЛГ у детей включает в себя несколько групп препаратов. Антагонист эндотелиновых рецепторов бозентан является наиболее изученными и приоритетными в лечении ЛГ у детей старше 3 лет [8, 12, 19]. В качестве одних из наиболее перспективных препаратов рассматриваются ингибиторы фосфодиэстеразы - силденафил и тадалафил [7, 9]. При лечении ЛГ у детей активно изучаются простагландины и их аналоги - простаноиды (илопрост, берапрост, эпопростенол и т. д.) [13, 15]. Хорошо известные блокаторы кальциевых каналов могут использоваться только у пациентов с положительным острым вазореактивным тестом [10]. В последние годы формируется представление, что применение ингибиторов АПФ целесообразно в лечении ЛГ при хронических бронхолегочных заболеваниях [17].
Тем не менее, специфической терапии ЛГ при хронической бронхолегочной патологии не разработано. В любом случае решение о назначении специфической терапии ЛГ у детей должно приниматься коллегиально, с учетом возрастных особенностей, тяжести течения и быстроты прогрессирования заболевания. В лечении больных с бронхиальной обструкцией, осложненной ЛГ, применение адреналина, норадреналина, эфедрина требует особой осторожности, так как они, помимо бронходилатирующего действия, вызывают гипертензивные реакции в малом круге кровообращения.
При неэффективности медикаментозного лечения проводится трансплантация легкого; в большинстве случаев для снижения давления в легочной артерии достаточно пересадки одного легкого. Двухлетняя выживаемость при трансплантации легкого составляет 60%, однако в отдаленные сроки у 50% больных развивается облитерирующий бронхиолит (проявление хронической реакции отторжения). На конечных стадиях высокой легочной гипертензии, особенно при сочетании с врожденными пороками сердца или кардиомиопатией, показана легочно-сердечная трансплантация; на начальных стадиях заболевания даже успешно выполненная операция не увеличивает продолжительность жизни таких больных [7].
Наибольшая эффективность лечения ЛГ у детей достигается в случае, если оно начато в ранний период болезни с применением средств, повышающих реактивность организма (лечебная физкультура, массаж, использование климатических факторов, иммуномодуляторов).
Комплексное лечение детей с ЛГ проводится непрерывно с соблюдением преемственности между стационаром, поликлиникой и санаторием-профилакторием; важность этого принципа вытекает из особенностей течения хронических бронхолегочных заболеваний, для которых и в фазе ремиссии необходима постоянная поддерживающая терапия.
СПИСОК ЛИТЕРАТУРЫ:
1. Л.И. Агапитов, Ю.М. Белозеров. Диагностика легочной гипертензии у детей // Российский вестник перинатологии и педиатрии, 2009; 4: 24-32.
2. Л.И. Агапитов. Обмороки у детей. Лекция для врачей. М., 2003, 52 с.
3. Ю.М. Белозеров. Детская кардиология. М., 2004, 400 с.
4. Ю.М. Белозеров. Клинические симптомы и синдромы в кардиологии детского возраста. Казань, 1994, 110 с.
5. Л.А. Бокерия, С.В. Горбачевский, М.А. Школьникова. Руководство по легочной гипертензии у детей. Москва, 2013, 416 с.
6. В.С. Задионченко, И.В. Погонченкова, З.О. Гринева и др. Хроническое легочное сердце // Российский кардиологический журнал, 2003; 4: 5-10.
7. И.Е. Чазова. Современные подходы к лечению хронического легочного сердца // РМЖ, 2000; 2: 83-86.
8. R. Barst, D. Ivy, AC. Widlitz et al. Pharmacokinetics, safety, and efficacy of bosentan in pediatric patients with pulmonary arterial hypertension // Clin. Pharmacol. Ther., 2003, 73: 372-382.
9. H.R. Collard, K.J. Anstrom, M.I. Schwarz, D.A Zisman. Sildenafil improves walk distance in idiopathic pulmonary fibrosis // Chest, 2007; 131: 897-899.
10. I.W. Franz, Van Der Meyden J., S. Schaupp, U. Tonnesmann. The effect of amlodipine on exercise-induced pulmonary hypertension and right heart function in patients with chronic obstructive pulmonary disease // Z. Kardiol., 2002; 91 (10): 833-839.
11. N. Galie, M. Hoeper, M. Humbert. Guidelines for the diagnosis and treatment of pulmonary hypertension // European Heart Journal, 2009; 30 (20): 2493-2537.
12. A Gunther, B. Enke, P. Markart et al. Safety and tolerability of bosentan in idiopathic pulmonary fibrosis: an open label study // Eur. Respir. J., 2007; 29: 713-719.
13. D.D. Ivy, A.K. Doran, K.J. Smith et al. Short- and long-term effects of inhaled iloprost therapy in children with pulmonary arterial hypertension // J. Am. Coll. Cardiol., 2008, 51: 161-169.
14. A Kitabatake, M. Inoue, M. Asao et al. Noninvasive evaluation of pulmonary hypertension by a pulsed Doppler technique // Circulation, 1983, vol. 68: 302-303.
15. AE. Lammers, AA Hislop, Y. Flynn, S.G. Haworth. Epoprostenol treatment in children with severe pulmonary hypertension // Heart, 2007, 93: 739-743.
16. D. Mereles, N. Ehlken, S. Kreuscher et al. Exercise and respiratory training improve exercise capacity and quality of life in patients with severe chronic pulmonary hypertension // Circulation, 2006, 114: 1482-1489.
17. N.W. Morrell, S.M. Danilov, K.B. Satyan et al. Right ventricular angiotension converting enzyme activity and expression is increased during hypoxic pulmonary hypertension // Cardiovasc. Res., 1997; 34: 393-403.
18. E.B. Rosenzweig, A. Widlitz, R. Barst Pulmonary arterial hypertension in children // Pediatr. Pulmon., 2004; 38: 2-22. National Pulmonary Hypertension Centres of the UK and Ireland. Consensus statement on the management of pulmonary hypertension in clinical practice in the UK and Ireland // Heart, 2008, 94: 11-141.
19. E.B. Rosenzweig, D.D. Ivy, A Widlitz et al. Effects of long-term bosentan in children with pulmonary arterial hypertension // J. Am. Coll. Cardiol., 2005, 46: 697-704.
20. G. Simonneau, I. Robbins, M. Beghetti Updated clinical classification of pulmonary hypertension // J. Am. Coll. Cardiol., 2009; 54: S43-S54.
21. E. Weitzenblum, A Sautegeau, M. Ehrhart et al. Long-term oxygen therapy can reverse the progression of pulmonary hypertension in patients with chronic obstructive pulmonary disease // Am. Rev. Respir. Dis., 1985, 131: 493-498.
Комментарии
ПРАКТИКА ПЕДИАТРА

