Клинико-генетические характеристики и тактика ведения больных с синдромом удлиненного интервала QT с функциональной АВ-блокадой с проведением 2:1
СтатьиР.А.-Г. Ильдарова, канд. мед. наук, В.В. Березницкая, канд. мед. наук
ОСП «Научно-исследовательский клинический институт педиатрии и детской хирургии им. акад. Ю.Е. Вельтищева» ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, г. Москва.
Ключевые слова: внезапная сердечная смерть, функциональная АВ-блокада, удлинение интервала QT, полиморфная желудочковая тахикардия, дети
Keywords: sudden cardiac death, functional AV block, QT interval prolongation, polymorphic ventricular tachycardia, children
Резюме. Синдром удлиненного интервала QT - наследственное заболевание, ассоциированное с высоким риском внезапной сердечной смерти. Крайне редкие и наиболее тяжелые случаи заболевания манифестируют в раннем возрасте, характеризуются выраженным удлинением интервала QT и рецидивирующими синкопе, обусловленными полиморфной желудочковой тахикардией. При этом экстремально длинный интервал QT приводит к развитию функциональной АВ-блокады 2 степени с проведением 2:1, что затрудняет своевременную диагностику причин синкопе и как следствие приводит к неверной тактике ведения этой группы больных. В данной статье приведен опыт аритмологического центра в диагностике и ведении пациентов с редкой формой синдрома удлиненного интервала QT. На основании данных катамнестическо-го наблюдения за 12 пациентами с первичным синдромом удлиненного интервала QT и функциональной АВ-блокадой 2 степени рассмотрены особенности течения заболевания и электрокардиографические характеристики больных. Генетическими причинами заболевания были преимущественно гетерозиготные мутации в генах KCNH2 и SCN5A. Учитывая тяжесть течения данного варианта СУИQT, рекомендована терапия бета-адреноблокаторами в максимально переносимых дозах. Использование гибридной медикаментозной, интервенционной (имплантация кардиовертера-дефибриллятора) и хирургической (левосторонняя симпатэктомия) терапии позволяет эффективно курировать пациентов с редкой, но крайне тяжелой формой СУИQT.
Summary. Long QT syndrome is an inherited disease associated with a high risk of sudden cardiac death. Extremely rare and most severe cases of the disease manifest at an early age and are characterized by significant prolongation of the QT interval and recurrent syncope caused by polymorphic ventricular tachycardia. At the same time, an extremely long QT interval leads to the development of functional 2:1 AV block, which complicates the timely diagnosis of the causes of syncope and, as a consequence, leads to incorrect management of this group of patients. This article describes the experience of a single arrhythmological center in the diagnosis and management of patients with the rare form of long QT syndrome. Based on the follow-up observation data for 12 patients with primary long QT syndrome and functional 2:1 AV block, the features of the disease course and electrocardiographic characteristics of the patients are considered. The genetic causes of the disease were predominantly heterozygous mutations in the KCNH2 and SCN5A genes. Given the severity of this variant of LQTS, therapy with beta-blockers in maximum tolerated doses is recommended. The use of hybrid treatment combining drug, interventional (implantation of a cardioverter-defibrillator) and surgical (left cardiac sympathetic denervation) therapy allows for the effective management of patients with a rare but extremely severe form of QT syndrome.
Для цитирования: Ильдарова Р.А.-Г., Березницкая В.В. Клинико-генетические характеристики и тактика ведения больных с синдромом удлиненного интервала QT с функциональной АВ-блокадой с проведением 2:1 // Практика педиатра. 2025. № 2. С.12-22.
For citation: Ildarova R.A.-G., Bereznitskaya V.V. Clinical and genetic characteristics and management tactics of patients with prolonged QT syndrome with functional AV block with 2:1 // Pediatrician's Practice. 2025;(2): 12-22. (in Russ.)
Синдром удлиненного интервала QT (СУИQT) -заболевание из группы сердечных каналопатий преимущественно с аутосомно-доминантным типом наследования. Клинический синдром удлиненного интервала QT проявляется синкопальными состояниями, обусловленными пароксизмами полиморфной желудочковой тахикардии типа «пируэт» [1, 2]. При трансформации желудочковой тахикардии в фибрилляцию желудочков может развиться внезапная остановка кровообращения и внезапная сердечная смерть (ВСС). Это заболевание относится к орфанным патологиям, отдельные и наиболее злокачественные формы которого, такие как синдром Тимоти, синдром Джервелла - Ланге-Нильсена, встречаются с частотой не более 1 : 1000 000 000 [2-4].
Одним из маркеров тяжелого течения заболевания является ранний возраст манифестации аритмических событий. Так, у больных со злокачественными формами синдрома, которые характеризуются высокой летальностью, синкопальные состояния могут впервые развиться в возрасте до 3 лет [2, 3]. Самая ранняя манифестация - в перинатальном периоде - описана у больных с СУИQT и функциональной атриовентрикулярной (АВ) блокадой [5]. Прогноз таких больных крайне неблагоприятный, что обусловлено не только тяжестью собственно заболевания, но и в большинстве случаев неправильной интерпретацией причин атриовентрикулярной блокады и соответственно неверным выбором тактики ведения. Вместо назначения бета-блокатора и снижения частоты синусового ритма имплантируется кардиостимулятор и навязывается высокая частота стимуляции, что способствует увеличению частоты рецидивов жизнеугрожающего нарушения ритма.
Цель настоящего исследования - оценить исходы первичного синдрома удлиненного интервала QT с функциональной блокадой АВ проведения в зависимости от генетических и клинических характеристик заболевания, а также тактики ведения.
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективный анализ данных 12 пациентов, обратившихся в детское кардиологическое отделение нарушений сердечного ритма (ДКО НСР) Научно-исследовательского клинического института педиатрии и детской хирургии имени академика Ю.Е. Вельтище-ва за период с апреля 2010 г. по октябрь 2022 г. для получения телемедицинской консультации. Впоследствии были госпитализированы 9 больных, период наблюдения за которыми составил 5,9 ± 3,9 года (от 2 до 13 лет), а трем больным были проведены телемедицинские консультации два и более раз. Возраст пациентов во время последнего визита составил 5,4 ± 4,8 года (от 1 мес до 15 лет). В группе преобладали пациенты мужского пола - 8 (67%).
Пациентам, находившимся под наблюдением в ДКО НСР, проведено комплексное обследование при первичном обследовании, которое включало стандартную электрокардиографию (ЭКГ) в 12 отведениях, суточное (холтеровское) мониторирование ЭКГ с автоматическим анализом интервала QT, в возрасте более 7 лет проводился тест с физической нагрузкой (тредмил-тест). У всех пациентов исключены структурные заболевания сердца на основании эхокардиографии с допплерографией, а также электролитные нарушения и дисфункция щитовидной железы как причины вторичного удлинения интервала QT. На основании клинических критериев в соответствии с отечественными рекомендациями всем пациентам при первичной госпитализации установлен диагноз «I45.8. Первичный синдром удлиненного интервала QT, синкопальная форма, функциональная блокада АВ проведения». Генетическое исследование (секвенирование панели генов и отдельных генов) проведено девяти пациентам.
Катамнестическое обследование проводилось два раза в год, в ходе которого осуществлялся мониторинг факторов риска внезапной сердечной смерти: наличие рецидивов аритмических событий (т. е. аритмогенных синкопе, эпизодов документированной желудочковой тахикардии и/или фибрилляции желудочков, у пациентов с имплантированным кардиовертером-дефибриллятором - наличие мотивированных срабатываний), оценка продолжительности корригированного интервала QT (QTc), наличие эпизодов альтернации зубца Т, периодов функциональной атриовентрикулярной и/или внутрижелудочковой блокады и их длительность. В соответствии с результатом мониторинга осуществлялась коррекция антиаритмической терапии.
РЕЗУЛЬТАТ
Особенности течения перинатального периода. В пяти случаях в третьем триместре у плода была документирована брадикардия (табл. 1). В одном из них (пациент № 3) на основании ультразвукового обследования плода было установлено, что брадикардия обусловлена атриовентрикулярной блокадой 2 степени. Нарушения ритма сердца во внутриутробном периоде отсутствовали в шести случаях. В одном случае нет информации о состоянии плода (пациент №12).
Данные о состоянии ребенка при рождении были доступны в 11 случаях (табл. 1). При рождении состояние пациентов расценивалось как удовлетворительное у 6/11 больных (55%); масса тела при рождении составляла 3201 ± 196 г, рост - 52,5 ± 0,4 см, что соответствовало норме. Среднетяжелое состояние было отмечено в двух случаях (20%). При этом у одного больного имели место дыхательные нарушения на фоне морфофункциональной незрелости, находился на лечении в отделении реанимации и интенсивной терапии (ОРИТН). Во втором случае у девочки диагностирована умеренная асфиксия в родах (обвитие пуповиной), церебральная депрессия, дыхательная недостаточность; осуществлялось дыхание с респираторной поддержкой NCPAP в течение первых двух дней жизни; на 25-й день была выписана в удовлетворительном состоянии. У трех мальчиков состояние при рождении расценено как тяжелое: в двух случаях в связи с дыхательными нарушениями (респираторный дистресс-синдром), в одном -за счет признаков сердечной недостаточности.
Таблица 1. Клинические и электрокардиографические характеристики пациентов в перинатальном периоде
|
Пациент №/пол |
Брадикардия внутриутробно |
Состояние при рождении |
Масса тела при рождении, г |
ЭКГ: ЧСС (уд/мин) |
ЭКГ: АВБ 2:1 |
ЭКГ: QTc (мс) |
|
№ 1/м |
да |
удовлетворительное |
3160 |
75 |
да |
н/д |
|
№ 2/д |
нет |
удовлетворительное |
2867 |
70 |
да |
н/д |
|
№ 3/м |
да (+АВб) |
удовлетворительное |
3330 |
65 |
да |
н/д |
|
№ 4/м |
да |
среднетяжелое |
1950 |
90 |
да |
581 |
|
№ 5/д |
нет |
удовлетворительное |
3200 |
80 |
да |
598 |
|
№ 6/м |
нет |
удовлетворительное |
3450 |
н/д |
да |
н/д |
|
№ 7/м |
нет |
тяжелое |
2332 |
60 |
да |
748 |
|
№ 8/д |
нет |
среднетяжелое |
2145 |
80 |
да |
н/д |
|
№ 9/м |
нет |
удовлетворительное |
3200 |
н/д |
нет |
н/д |
|
№ 10/м |
да |
тяжелое |
2260 |
77 |
да |
663 |
|
№ 11/м |
да |
тяжелое |
н/д |
н/д |
да |
568 |
|
№ 12/д |
н/д |
н/д |
н/д |
н/д |
да |
н/д |
Примечание: н/д - нет данных; м - мальчик; д - девочка.
На ЭКГ в первый день жизни выраженная брадикардия за счет АВ-блокады 2 степени с проведением 2:1 регистрировалась у 11 пациентов (рис. 1), средняя ЧСС составила 74,6 ± 8,8 уд/мин (от 60 до 90 уд/мин), что менее 2%о возрастного распределения ЧСС (табл. 1). Продолжительность интервала QTc была оценена лишь в 5 случаях и составила 632 ± 67 мс (от 568 до 748 мс). В одном случае нарушений ритма ни внутриутробно, ни после рождения при осмотре не отмечалось, поэтому ЭКГ не проводилась (пациент № 9).
Варианты манифестации и возраст диагностики заболевания. Были выписаны из роддома в удовлетворительном состоянии с диагнозом «врожденная АВ-блокада» 6 пациентов. Синкопальные состояния либо их эквиваленты в виде приступов апноэ, замирания, эпизодов внезапной кратковременной вялости развили трое больных (пациенты № 1, № 6, № 8 в табл. 2). Один ребенок развил внезапную остановку кровообращения в возрасте 2,5 мес (пациентка № 2).
После аритмических событий пациенты были обследованы по месту жительства и консультированы в ДКО НСР, где диагностирован первичный синдром удлиненного интервала QT, констатирован функциональный характер АВ-блокады, назначена терапия бета-блокатором.
В связи с наличием АВ-блокады пациентка № 5 в возрасте 1 мес была консультирована детским кардиологом. Выявлен функциональный характер блокады и диагностирован первичный синдром удлиненного интервала QT (табл. 2). Также в связи с наличием АВ-блокады пациентке № 12 проведено контрольное холтеровское мониторирование в возрасте 1,5 мес, при котором были документированы пароксизмы неустойчивой желудочковой тахикардии, диагностирован синдром удлиненного интервала QT и функциональная АВ-блокада с проведением 2:1. В обоих случаях сразу назначена терапия бета-блокатором.
Пациент № 4 в связи с отягощенным семейным анамнезом (мама ребенка, его дядя и тетя по м/л имеют II молекулярно-генетический вариант синдрома удлиненного интервала QT) сразу после рождения консультирован в ДКО НСР, назначена терапия бета-блокатором.
Пациент № 9, не имевший аускультативно нарушений ритма при рождении, был также выписан из роддома в удовлетворительном состоянии, ЭКГ не проводилось. В возрасте 4 лет развил аритмическое событие во время сна, ретроспективно расцененное как внезапная остановка кровообращения (проводились реанимационные мероприятия дедушкой). В течение следующего года дважды в похожих об-
Таблица 2. Клинические проявления и возраст манифестации синдрома удлиненного интервала QT
Пациент №/пол | Катамнез, лет | Синкопе/ возраст | ЖТ/ФЖ возраст | ВОК/ возраст | ВСС/ возраст |
№ 1/м | 13,0 | да/1,5 мес | +++ | нет | нет |
№ 2/д | 2,0 | нет | — | да/2,5 мес | нет |
№ 3/м | 1,0 | да/2 дня | +++ | да/2 дня | нет |
№ 4/м | 9,0 | нет | +++ | нет | нет |
№ 5/д | 11,0 | нет | + | нет | нет |
№ 6/м | 4,0 | да/11 дней | +++ | да/3 года | да/4 года |
№ 7/м | 3,0 | да/1,5 мес | +++ | да/1,5 мес | нет |
№ 8/д | 4,0 | да/2 года | — | нет | нет |
№ 9/м | 6,0 | да/4 года | — | да/4 года | да/10 лет |
№ 10/м | 0,1 | да/2 дня | +++ | нет | да/1 месяц |
№ 11/м | 0,5 | да/2 дня | +++ | нет | да/6 месяцев |
№ 12/д | 0,5 | да/1,5 мес | ++ | нет | нет? |
Примечание: ЖТ/ФЖ - рецидивирующие пароксизмы желудочковой тахикардии/фибрилляции желудочков по данным ХМ в первые дни жизни; ВОК - внезапная остановка кровообращения; ВСС - внезапная сердечная смерть стоятельствах рецидивировали приступы потери сознания. После третьего эпизода ребенок консультирован кардиологом и при последующем обследовании впервые зарегистрировано выраженное удлинение интервала QT (QTc, по данным стандартной ЭКГ, до 540 мс и при ХМ до 681 мс), функциональная АВ-блокада 2 степени с проведением 2:1, в связи с чем направлен в ДКО НСР.
Четыре пациента (№ 3, № 7, № 10 и № 11) были переведены в ОРИТН в связи с выраженной брадикардией (№ 3) и по тяжести состояния (№ 7, № 10, № 11) сразу после рождения (табл. 1 и 2). Со второго дня жизни, по данным холтеровского мониторирования ЭКГ и/или прикроватного мониторирования в ОРИТН, регистрировалась рецидивирующая полиморфная желудочковая тахикардия, пароксизмы неустойчивой и устойчивой фибрилляции желудочков на фоне АВ-блокады с проведением 2:1, экстремально длинный интервал QT - QTc свыше 550 мс (рис. 2). В связи с неэффективностью симптоматической терапии и сохранением рецидивов устойчивой желудочковой полиморфной тахикардии пациенты были консультированы в федеральном аритмологическом центре, где диагностирована тяжелая форма первичного синдрома удлиненного интервала QT, определен функциональный характер АВ-блокады.
Рис. 1. Электрокардиограмма девочки с III типом СУИQT (пациент № 5) в возрасте 1 мес: регистрируется синусовый ритм, АВ-блокада с проведением 2:1 - частота сокращения предсердий - 166-176 уд/мин, интервал QT = 560-580 мс, QTc = 659 мс.
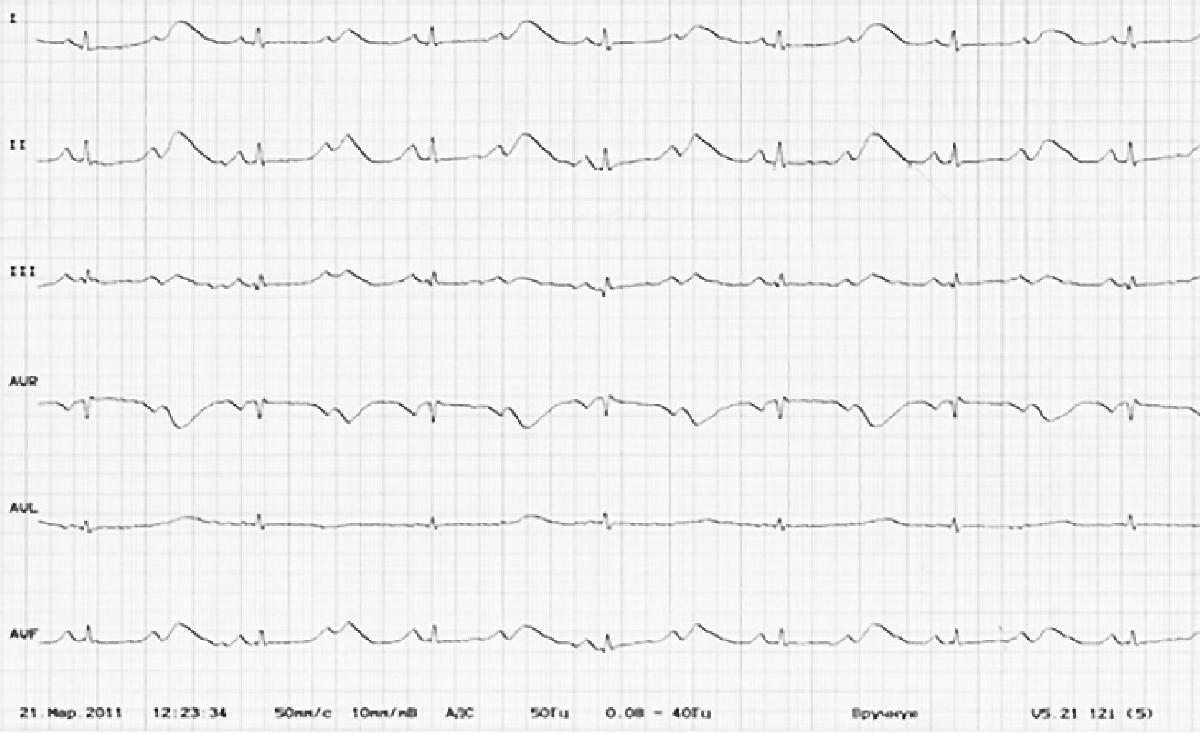
Таблица 3. Генетические характеристики пациентов
Пациент №/пол | Генетическое исследование | Мутация в гене | Состояние | Замена нуклеотида | Замена амино-кислоты |
№ 1/м | секвенирование панели генов | KCNH2 | гетерозиготное | 1838C>T | Thr613Met |
№ 2/д | экзомное секвенирование | SCN5A | гетерозиготное | T2821A | S941T |
№ 3/м | экзомное секвенирование | SCN5A | гетерозиготное | 4414T>A | Phe1472Ile |
№ 4/м | секвенирование панели генов | KCNH2 | гетерозиготное | 1501G>T | D501Y |
№ 5/д | экзомное секвенирование | SCN5A | гетерозиготное | 4489G>C | Ala497Pro |
№ 6/м | экзомное секвенирование | KCNH2 | гомозиготное | 3176A>C | Asp1059Ala |
№ 7/м | секвенирование панели генов | SCN5A | гетерозиготное | 4459A>G | Thr1487Ala |
№ 8/д | нет | — | — | — | — |
№ 9/м | нет | — | — | — | — |
№ 10/м | нет | — | — | — | — |
№ 11/м | нет | — | — | — | — |
№ 12/д | секвенирование гена SCN5A | не выявлено | — | — | — |
Генетические причины заболевания. Из 8 гено-типированных пациентов получен положительный результат у 7 (88%), в одном случае, когда анализ ограничен был исследованием одного гена (SCN5A), тест был отрицательный (табл. 3). У 4/7 больных были выявлены патогенные варианты в гене SCN5A в гетерозиготном состоянии. У 2/7 детей были выявлены патогенные варианты в гене KCNH2, в гетерозиготном состоянии, в области поры (область белка с 550 по 650 аминокислоту). В одном случае определялся вариант в гене KCNH2 вне поры, но в гомозиготном состоянии.
Секвенирование по Сэнгеру на вариант, выявленный у пациентов, проведено в двух семьях. В одном случае у обоих родителей искомый вариант в гене SCN5A не выявлен; в другом случае у ребенка с наследственным синдромом удлиненного интервала QT был подтвержден тот же вариант в гене KCNH2, что и у остальных членов семьи (пациент № 4). Клинических проявлений синдрома удлиненного интервала QT ни у одного из родителей не выявлено, за исключением единственного случая наследственного синдрома удлиненного интервала QT. Таким образом, на основании преимущественно клинических данных в пяти случаях можно предположить спорадический характер заболевания, что требует подтверждения; в одном случае вариант de novo подтвержден генетическим исследованием родителей.
Медикаментозная терапия и результаты динамического наблюдения. Пациенты с гетерозиготными мутациями в гене KCNH2 получали с рождения пропранолол. При этом пациенту № 1 пропранолол был назначен под контролем временного электрокардиостимулятора, в начальной дозе 1,0 мг/кг. Только по достижении дозы 3,3 мг/кг удалось достигнуть контроля над желудочковой тахикардией. В возрасте двух лет ребенок был переведен на пролонгированный бета-блокатор атенолол и за период наблюдения в 13 лет сохраняется стойкая ремиссия. Пациенту № 4 пропранолол назначен с первого дня жизни в дозе 3,0 мг/кг в сочетании с карбамазепином в дозе 11 мг/кг. С 6 дня жизни и по настоящее время (катамнез 9 лет) желудочковые нарушения ритма не рецидивировали, в возрасте 2 лет в связи со стабильным состоянием карбамазепин был отменен, находится на монотерапии бета-блокатором. В обоих случаях показаний для имплантации антиаритмических устройств при наблюдении в динамике не было.
Рис. 2. Фрагмент холтеровского мониторирования мальчика с II типом СУИQT: после ритма с АВ-блокадой 2 степени и проведением 2:1 регистрируется полиморфная желудочковая тахикардия типа «пируэт»

Пациент № 6 с гомозиготным вариантом в гене KCNH2 на 11 день жизни манифестировал эпизодами апноэ, во время которых была документирована полиморфная желудочковая тахикардия. Назначена комбинированная антиаритмическая терапия пропранололом в дозе до 4,2 мг/кг и карбамазепином в дозе 10 мг/кг, желудочковые нарушения ритма не рецидивировали, уменьшилась продолжительность интервала QT и представленность ритма с АВ-бло-кадой 2:1. С возраста 1,5 лет у ребенка на фоне регулярной антиаритмической терапии адекватными дозами бета-блокатора и карбамазепина отмечались рецидивы аритмических событий (синкопе), провоцированные вирусными респираторными инфекциями. При повторном анализе данных экзомного секвенирования у больного были выявлены варианты в генах СРТ2, SLC2A9 и CASR, ассоциированных с различными метаболическими нарушениями. Ребенок консультирован генетиком, было высказано предположение, что интеркуррентная инфекция провоцирует метаболические изменения, приводящие к электролитным нарушениям, в том числе гипокалиемии, что в свою очередь провоцирует рецидив желудочковой тахикардии. Учитывая крайне высокий риск внезапной сердечной смерти, у больного были выполнены имплантация кардиовертера-дефибриллятора для профилактики ВСС, а также для усиления антиадренергической терапии - левосторонняя симпатэктомия; была продолжена терапия пролонгированным бета-блокатором в дозе до 3,7 мг/кг и карбамазепином - до 10 мг/кг, постоянно получал препараты калия. Несмотря на проводимую гибридную терапию, у ребенка сохранялись рецидивы желудочковой тахикардии и мотивированные срабатывания кардиовертера-дефибриллятора на фоне интеркуррентных инфекций. Во время очередного эпизода развился электрический шторм, приведший к внезапной сердечной смерти.
Девочки с мутациями в гене SCN5A получают комбинированную антиаритмическую терапию, обеим имплантирован кардиовертер-дефибриллятор. У пациентки № 5 мутация не чувствительная к блокатору натриевых каналов (проба с аллапинином отрицательная), получала с возраста 1 мес атенолол в дозе 1,2 мг/кг, на фоне нерегулярного приема которого были документированы эпизоды устойчивой фибрилляции желудочков во сне в возрасте 4 мес. С этого времени получает атенолол в дозе до 2,3 мг/кг в сочетании с карбамазепином. При контрольных электрокардиографических исследованиях рецидивов желудочковой тахикардии, эпизодов АВ-блока-ды 2:1 не регистрировалось, синкопе отсутствовали (рис. 3). Кардиофертер-дефибриллятор был имплантирован в возрасте 11 лет в связи с сохраняющимся высоким риском внезапной сердечной смерти. Пациентка № 2 манифестировала с внезапной остановки кровообращения, получала трехкомпонентную терапию (пропранолол 3,3 мг/кг + аллапинин 1,0 мг/кг + карбамазепин 8,3 мг/кг). Учитывая возраст и вес пациентки и положительную динамику электрокардиографических показателей, от имплантации кардиовертера-дефибриллятора было решено временно воздержаться. Однако в течение следующего года на фоне регулярной терапии рецидивировал эпизод внезапной остановки кровообращения и кардиовертер-дефибриллятор был имплантирован.
Мальчики с мутациями в гене SCN5A манифестировали со второго дня жизни непрерывно-реци-дивирующими пароксизмами полиморфной желудочковой тахикардии - фибрилляции желудочков. Обоим пациентам (№ 3 и № 7) диагностировали первоначально врожденную АВ-блокаду и имплантировали постоянный кардиостимулятор с высокой базовой частотой желудочковой стимуляции -120 уд/мин и 125 уд/мин соответственно, что усугубляло проявления синдрома удлиненного интервала QT. Пациенту № 3 осуществлялся хаотический подбор антиаритмической терапии для контроля желудочковой тахиаритмии, а у пациента № 7 желудочковую тахиаритмию пытались контролировать пропранололом в низких дозах (менее 2 мг/кг). Дети были консультированы в аритмологическом центре; только после перепрограммирования кардиостимулятора (снижение базовой частоты до 40 уд/мин) и назначения адекватной дозы пропранолола (4,0 мг/кг) был достигнут положительный эффект в виде отсутствия желудочковых нарушений ритма. У пациента № 3 сохранялась АВ-блока-да 2:1 на фоне экстремально длинного интервала QT и эпизоды альтернации зубца Т, в связи с чем была назначена трехкомпонентная антиаритмическая терапия (атенолол до 4 мг/кг, аллапинин 1,2 мг/кг и карбамазепин 10 мг/кг), на фоне которой значительно уменьшилась продолжительность QTc, отсутствовали АВ-блокада и альтернация зубца Т. При динамическом наблюдении у пациента № 3 в возрасте около года на фоне интеркуррентных инфекций отмечались повторные синкопе, после назначения высоких доз препаратов (пропранолол до 6 мг/кг + карбамазепин до 17 мг/кг + аллапинин 1,6 мг/кг) аритмических события не рецидивировали.
У пациента № 7 на фоне относительно низкой дозы бета-блокатора (<2 мг/кг) отмечался рецидив синкопе и кардиостимулятор был заменен на кардиовертер-дефибриллятор. После этого повторно консультирован в ДКО НСР, назначена трехкомпонентная антиаритмическая терапия (надолол до 4,6 мг/кг, аллапинин 1,1 мг/кг и карбамазепин до 12 мг/кг). В возрасте 2,5 лет были выявлены эпизоды неустойчивой желудочковой тахикардии при контроле системы кардиовертера-дефибриллятора, которые были провоцированы интеркуррентной инфекцией; с целью усиления антиадренергической терапии ребенку проведена левосторонняя симпатэктомия, сохраняются единичные эпизоды неустойчивой желудочковой тахикардии.
Пациентка № 8 с фенотипически LQT3 манифестировала синкопальным состоянием в возрасте 2 лет. В ДКО НСР подобрана трехкомпонентная ан-тиаритмическая терапия под контролем электрокардиографических маркеров: атенолол 1,8 мг/кг + карбамазепин 10 мг/кг + аллапинин 0,9 мг/кг (предварительная проба с блокатором натриевых каналов была положительной). За период наблюдения в 4 года аритмические события не рецидивировали, уменьшились значения интервала QTc, отсутствует АВ-блокада 2:1.
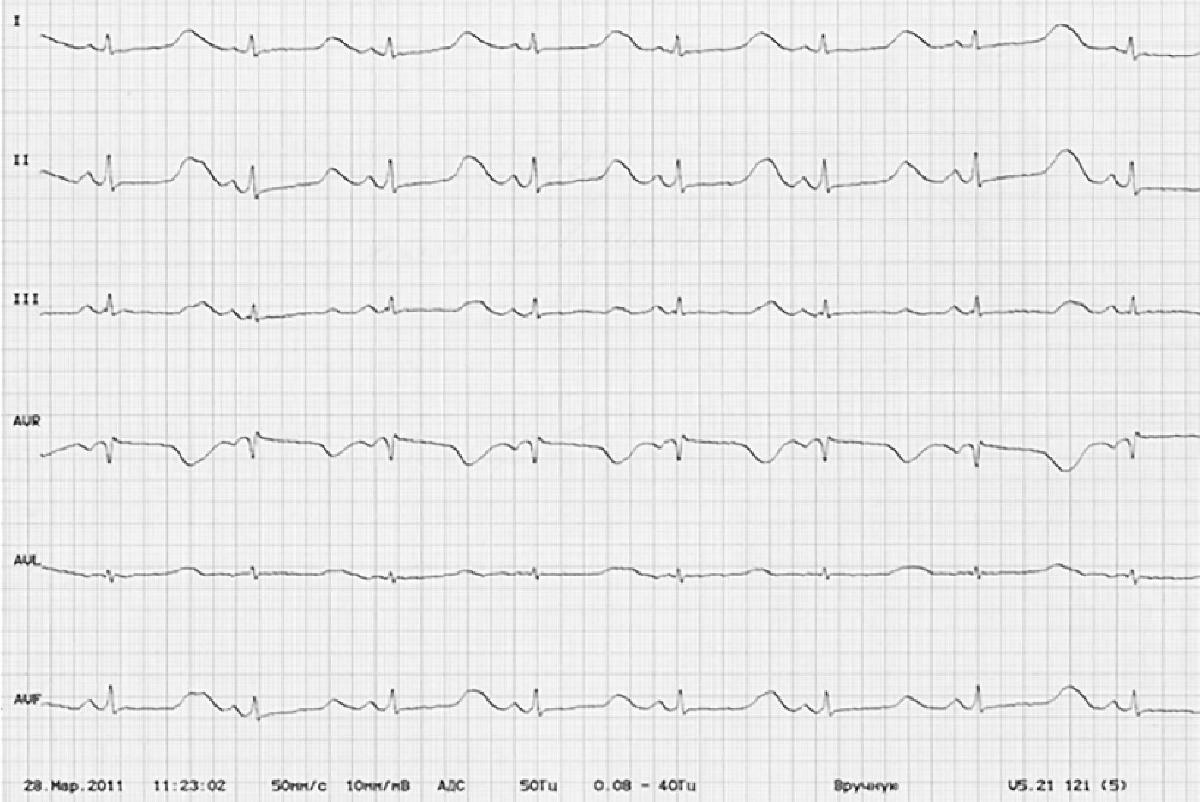
Рис. 3. Электрокардиограмма девочки с III типом СУИQT (пациент № 5) после назначения бета-блокатора: регистрируется синусовый ритм, снижение частоты синусового ритма до 90-100 уд/мин, отсутствует АВ-блокада, QT = 480 мс, QTc = 607 мс
Пациент № 9 впервые после трех синкопе в возрасте 4 лет получал комбинированную антиаритми-ческую терапию бета-блокатором (начали с пропранолола в дозе 2 мг/кг, впоследствии был заменен на надолол в дозе 1,9 мг/кг) и карбамазепином в дозе 10 мг/кг. В связи с внезапной остановкой кровообращения в анамнезе, с высоким риском ВСС, по данным электрокардиографического обследования, неоднократно была рекомендована имплантация кардиовертера-дефибриллятора, от которой родители отказывались. При наблюдении в динамике в течение 6 лет синкопе не рецидивировали, терапию получал регулярно, проводилась коррекция доз препаратов по весу; в возрасте 10 лет - внезапная сердечная смерть во сне.
Пациенты № 10, № 11 и № 12 наблюдались амбулаторно (телемедицинские консультации). Пациенту № 10 назначена терапия пропранололом в дозе не менее 3,0 мг/кг и карбамазепином в дозе не менее 10 мг/кг, была рекомендована целевая ЧСС синусового ритма менее 110 уд/мин, которая, по данным предоставленных заключений холтеровского мониторирования ЭКГ, не была достигнута. От госпитализации в ДКО НСР родители отказались; пациент наблюдался по месту жительства. Желудочковая тахикардия рецидивировала неоднократно, данных о регулярности терапии и дозах препаратов нет; во время одного из эпизодов полиморфная желудочковая тахикардия трансформировалась в фибрилляцию желудочков и привела к остановке сердца в возрасте 2 мес. Пациенту № 11 был имплантирован кардиостимулятор сразу после рождения в связи с АВ-блокадой с базовой частотой 130 имп/мин, на фоне которой сохранялись частые рецидивы фибрилляция желудочков, купированные повторными дефибрилляциями. После консультации в ДКО НСР была снижена частота стимуляции до 50 уд/мин, назначен пропранолол в дозе 3 мг/кг, рекомендован снижение ЧСС синусового ритма менее 100 уд/мин. Был достигнут контроль над желудочковой тахиаритмией, однако пациент развил по-лиорганную недостаточность и летальный исход в возрасте 5 мес. Пациентке № 12 установлен диагноз и подобрана трехкомпонентная антиаритмическая терапия амбулаторно. При последнем катамнести-ческом обследовании в возрасте 6 мес отсутствовали желудочковые нарушения ритма, не регистрировалась АВ-блокада, уменьшились значения QTc. От дальнейшего наблюдения родители отказались.
ОБСУЖДЕНИЕ
В исследовании представлены данные катамнести-ческого наблюдения за группой больных с СУИQT с очень редким фенотипом, когда экстремально длинный интервал QT приводит к развитию функциональной АВ-блокады с проведением 2:1. Доля таких больных составила 3% среди всех больных с первичным СУИQT, наблюдающихся в ЦНСР, что в целом соотносится с данными исследований больших групп больных с СУИQT в 1990-х гг., согласно которым в 4-4,5% случаев была документирована функциональная АВ-блокада 2 степени. Более современные исследования сосредоточены на анализе групп больных, у которых СУИQT диагностирован в перинатальном периоде и среди которых функциональная блокада документирована уже в 25% случаев [6-8].
Обращает на себя внимание, что выраженная брадикардия за счет АВ-блокады с проведением 2:1, которую прежде всего отмечают неонатологи, не влияет на общее состояние новорожденных. Более половины из них имели удовлетворительное состояние при рождении, у остальных тяжесть состояния была обусловлена дыхательными расстройствами, патогенетически не связанными с редким пульсом. Тем не менее СУИQT с функциональной АВ-бло-кадой ассоциирован с высоким риском ВСС в раннем возрасте, жизнеугрожающие нарушения ритма у этих больных манифестируют в перинатальном периоде [5, 7, 9]. В нашей группе больных в пяти случаях рецидивирующая полиморфная желудочковая тахикардия манифестировала в перинатальном периоде, еще у шести пациентов аритмические события впервые развились в раннем возрасте.
Пик манифестации аритмических событий у больных с СУИQT приходится на возраст от 12 до 20 лет [10]. Манифестация полиморфной желудочковой тахикардии в раннем возрасте ассоциирована с тяжестью заболевания и резистентностью к терапии. Такая картина наблюдается при редких вариантах синдрома, имеющих специфический фенотип, таких как, например, синдром Джервелла - Ланге-Нильсена с манифестацией синкопе в среднем в 1,2-2 года и высокой летальностью (50%) в детском возрасте в отсутствие терапии [2]. Единичные описания случаев СУИQT с функциональной блокадой 2:1 как специфического варианта СУИQТ с высокой летальностью встречается в литературе с 1980-х гг., при этом у некоторых больных желудочковая тахикардия возникала впервые внутриутробно. У большинства детей была документирована рецидивирующая желудочковая тахикардия или фибрилляция желудочков в неонатальном периоде. Несмотря на антиаритмическую терапию, пациенты погибали в раннем возрасте [9, 11]. Прогноз больных с первичным СУИQT и функциональной АВ-блокадой 2:1 крайне неблагоприятный, а тактика ведения требует глубокого понимания электрофизиологических механизмов развития атриовентрикулярной блокады и желудочковой тахикардии.
Увеличение длительности потенциала действия при первичном синдроме удлиненного интервала QT приводит к увеличению продолжительности абсолютного рефрактерного периода в миокарде желудочков. В данной группе пациентов рефрактерный период настолько длинный, что превышает длительность кардиоцикла, на ЭКГ при этом интервал QT (т. е. процесс реполяризации, во время которого кардиомиоциты рефрактерны) длительнее, чем интервал PP (отражает длительность одного кардиоцикла), что приводит к развитию функциональной атриовентрикулярной блокады, когда каждый второй стимул синусового узла приходится на период рефрактерности и не проводится [9, 12, 13]. На стандартной электрокардиограмме при этом каждый второй зубец Р регистрируется перед началом зубца Т (рис. 1). Это особенно актуально для новорожденных, частота синусового ритма которых в покое свыше 120 уд/мин, а при минимальной нагрузке может достигать 200 уд/мин. Функциональный характер блокады становится очевидным после снижения частоты синусового ритма с помощью бета-блокаторов, когда интервал PP превышает по длительности интервал QT и АВ проведение нормализуется.
При исследовании особенностей диагностики заболевания в зависимости от генотипа заболевания среди новорожденных было установлено, что в перинатальном периоде СУИQT проявляется преимущественно синусовой брадикардией у больных с I молекулярно-генетическим вариантом и функциональной АВ-блокадой 2:1 у больных с II и III вариантами синдрома [11]. Это наблюдение подтверждается нашими данными, так как при генетическом исследовании у наших пациентов были выявлены варианты в генах KCNH2 и SCN5A. При этом гетерозиготные варианты в гене SCN5A преобладали, что соотносится с данными других исследователей [5, 11].
Известно, что генетически детерминированные заболевания, обусловленные мутациями de novo, протекают тяжелее. Также было установлено, что описываемый фенотип СУИQT чаще спорадический, чем наследственный, при этом не отягощенный по СУИQT и ВСС семейный анамнез оказался одним из прогностически неблагоприятных факторов при оценке риска ВСС [9, 13]. В наблюдаемой нами когорте 11 из 12 пациентов были пробандами, при анализе родословной случаев СУИQT и ВСС в молодом возрасте отмечено не было. Только у одного пациента был подтвержден генетически спорадический характер аритмии - проведено секвенирование по Сэнгеру родителям и не был обнаружен вариант, выявленный у ребенка. В остальных случаях было установлено, что у обоих родителей отсутствуют синкопе, на стандартной ЭКГ регистрируется нормальная продолжительность интервала QTc, таким образом, предположен спорадический характер заболевания у ребенка.
В соответствии с современными клиническими рекомендациями пациенту с генетически и/или клинически подтвержденным синдромом удлиненного интервала QT показана терапия бета-адреноблокатором, при этом наиболее эффективным бета-блокатором в контроле желудочковых тахиаритмий является надолол, что также отражено в рекомендациях [10, 14]. В качестве медикаментозной терапии у больных с перинатальной манифестацией желудочковой тахикардии в дополнение к бета-блокаторам применяют блокаторы натриевых каналов (мексилетин) [3, 12, 13]. Блокаторы натриевых каналов также являются геноспецифической терапией для больных с III вариантом СУИQT [10, 14].
В исследуемой группе контроль над желудочковой тахикардией был достигнут при назначении высоких доз бета-блокаторов: для пропранолола -выше 3 мг/сут (средняя доза 3,4 ± 0,6 мг/кг), для пролонгированных бета-блокаторов (атенолол, надо-лол) - около 2 мг/кг (в среднем 2,0 ± 0,1 мг\кг). После назначения бета-блокатора в эффективной дозе отмечалось снижение частоты синусового ритма и пропорционально сокращение продолжительности QTc; кроме того, либо отсутствовали, либо сохранялись в небольшом объеме периоды ритма с функциональной блокадой проведения и периоды альтернации зубца Т. В тех случаях, когда имплантировался постоянный электрокардиостимулятор и программировалась высокая частота импульса-ции, клинически состояние больного ухудшалось и полиморфная желудочковая тахикардия сохранялась до тех пор, пока не снижали значительно частоту импульсации и не назначали высокую дозу бета-блокатора.
Эффективность медикаментозной терапии оценивалась на основании наличия или отсутствия аритмических событий, а также косвенных критериев, таких как выраженность электрокардиографических проявлений, то есть динамика продолжительности интервала QTc и ассоциированных со значением QTc признаков - альтернации зубца Т, транзиторного нарушения атриовентрикулярного и внутрижелудочкового проведения. Для усиления антиаритмической терапии большинству пациентов (75%) в дополнение к бета-блокатору назначался карбамазепин, обладаю-щийкакантиаритмическимдействиемзасчетблокады натриевого тока, так и антиаффективным (нормотимическим) действием, что актуально при лечении желудочковой тахикардии, провоцированной эмоциональной нагрузкой [15]. Пациентам с III вариантом после лекарственной пробы для подтверждения чувствительности мутации к препарату дополнительно к бета-блокатору назначалась геноспецифическая терапия блокатором натриевых каналов аллапинином в средней дозе 1,0 мг/кг.
При анализе эффективности медикаментозной терапии в зависимости от генетического варианта синдрома установлено, что несмотря на то что гетерозиготные варианты в гене KCNH2 локализовались в поре, то есть являлись более тяжелыми мутациями, контроль желудочковой тахикардии у обоих пациентов достигался монотерапией высокими дозами бета-блокаторов, тогда как трое из четырех пациентов (75%) с мутациями в гене SCN5A получали трехкомпонентную терапию, на фоне которой отсутствовали рецидивы аритмических событий.
При анализе летальных исходов в данной группе можно утверждать, что адекватная терапия способна была предотвратить ВСС, за единственным исключением, когда причиной резистентности к терапии с высокой степенью вероятности было по-лигенное поражение: сочетание гомозиготного варианта с вариантами, ассоциированными с метаболическими нарушениями. В остальных трех случаях летальных исходов нами констатирована недостаточно интенсивная, преимущественно медикаментозная терапия. Так, отказ родителей от имплантации кардиовертера-дефибриллятора не позволил предупредить ВСС в одном случае, при этом благодаря медикаментозной терапии ремиссия длилась 6 лет, а у пациентов с ВСС в возрасте до года назначались недостаточные дозы препаратов. Использование гибридной медикаментозной (анти-аритмической, геноспецифической с максимальной переносимыми дозами препаратов), интервенционной (имплантация аритмических устройств) и хирургической (левосторонняя симпатэктомия) терапии позволяет эффективно курировать пациентов с редкой, но крайне тяжелой формой СУИQT.
ВЫВОДЫ
1. Синдром удлиненного интервала QT с функциональной АВ-блокадой 2:1 относится к редким, но прогностически неблагоприятным формам заболевания, характеризуется высоким риском ВСС и манифестацией в перинатальном периоде.
2. Генетическими причинами являются преимущественно гетерозиготные мутации de novo в генах KCNH2 и SCN5A, с преобладанием поражений гена SCN5A.
3. Учитывая тяжесть клинической картины при данном варианте СУИQT, бета-адреноблокаторы (пропранолол, надолол, атенолол) должны назначаться в максимально переносимых дозах, при этом ориентиром при повышении дозы бета-блокатора должна быть целевая частота сердечных сокращений <100 уд/мин.
4. При синдроме удлиненного интервала QT с функциональной АВ-блокадой 2:1, обусловленном мутациями гена SCN5A, контроль желудочковой тахикардии достигался назначением трехкомпонентной антиаритмической терапии.
Литература
1. LongQT Syndrome: Genetics and Future Perspective/ L.Wallace [et al.] // Pediatric Cardiology. 2019. Vol. 40, No. 7. P. 14191430. DOI: 10.1007/s00246-019-02151-x.
2. The Jervell and Lange-Nielsen Syndrome. Natural history, molecular basis, and clinical outcome / P.J. Schwartz [et al.] // Circulation. 2006. Vol. 113, No. 6. P. 783-790. DOI: 10.1161/ CIRCULATIONAHA.105.592899.
3. Bauer R., Timothy K.W., Golden A. Update on the Molecular Genetics of Timothy Syndrome // Frontiers of Pediatric. 2021. No. 9. P. 668546. DOI: 10.3389/fped.2021.668546.
4. Orphanet. The portal for rare diseases and orphan drugs // Available at: orpha.net/consor/cgi-bin/Disease_ Search_Simple.php?lng=EN&diseaseGroup=long+qt+syn-drome (accessed: 25.01.2024).
5. Clinical characteristics and genetic background of congenital long-QT syndrome diagnosed in fetal, neonatal, and infantile life: a nationwide questionnaire survey in Japan / H. Horigome [et al.] // Circulation Arrhythmia and Electrophysiology. 2010. Vol. 3, No. 1. P. 10-17. DOI: 10.1161/CIRCEP.109.882159.
6. The long QT syndrome in children. An international study of 287 patients / A. Jr. Garson [et al.] // Circulation. 1993. Vol. 87, No. 6. P. 1866-1872. DOI: 10.1161/01.cir.87.6.1866.
7. Trippel D.L., Parsons M.K., Gillette P.C. Infants with long-QT syndrome and 2:1 atrioventricular block // American Heart Journal. 1995. No. 130. P. 1130-1134. DOI: 10.1016/0002-8703(95)90222-8.
8. Arrhythmia phenotype during fetal life suggests long-QT syndrome genotype: risk stratification of perinatal long-QT syndrome / B.F. Cuneo [et al.] // Circulation Arrhythmia and Electrophysiology. 2013. Vol. 6, No. 5. P. 946-951. DOI: 10.1161/CIRCEP.113.000618.
9. Systematic review of long QT syndrome identified during fetal life / S. Chivers [et al.] // Heart Rhythm. 2023. Vol. 20, No. 4. P. 596-606. DOI: 10.1016/j.hrthm.2022.12.026.
10. ESC Scientific Document Group. 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death / K. Zeppenfeld [et al.] // European Heart Journal. 2022. Vol. 43, No. 40. P. 3997-4126. DOI: 10.1093/eurheartj/ehac262.
11. Long QT syndrome in neonates: conduction disorders associated with HERG mutations and sinus bradycardia with KCNQ1 mutations / J.M. Lupoglazoff [et al.] // Journal of the American College of Cardiology. 2004. Vol. 43, No. 5. P. 826830. DOI: 10.1016/j.jacc.2003.09.049.
12. Two-to-One AV Block Associated with the Congenital Long QT Syndrome / E. Pruvot [et al.] // Journal of Cardiovasc Electrophysiol. 1999. Vol. 10, No. 1. P. 108-113. DOI: 10.1111/ j.1540-8167.1999.tb00647.x.
13. The long QT syndrome with impaired atrioventricular conduction: a malignant variant in infants / A.P. Gorgels [et al.] // Journal of Cardiovascular Electrophysiology. 1998. Vol. 9, No. 11. P. 1225-1232. DOI: 10.1111/j.1540-8167.1998. tb00096.x.
14. Желудочковые нарушения ритма. Желудочковые тахикардии и внезапная сердечная смерть : клинические рекомендации 2020 / Д.С. Лебедев [и др.] // Российский кардиологический журнал. 2021. Т. 26, № 7. С. 4600. DOI: org/10.15829/1560-4071-2021-4600.
15. Гордеев Л.С., Кульбачинская Е.К., Березницкая В.В. Влияние карбамазепина на сердечно-сосудистую систему : обзор литературы // Педиатрическая фармакология. 2022. Т. 19, № 6. С. 484-491.

