Перспективы повышения эффективности комплексной терапии ОРВИ у детей в возрасте 6–12 лет
СтатьиИ.Н.Захарова1, д-р мед. наук, профессор, Э.Р. Самитова2, канд. мед. наук, Н.Г. Сугян1,3, канд. мед. наук, В.И. Барыкин3, О.А.Тунгулова1, Д.Р. Хальметова1, Т.А. Алтыбаева1, М.С. Терехов1
1 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, г. Москва
2 ГБУЗ «Детская городская клиническая больница им. З.К. Башляевой Департамента здравоохранения г. Москвы»
3 ГБУЗ МО «Химкинская клиническая больница», г. Химки, Российская Федерация
Резюме.
Цель. Оценить эффективность комплексной терапии, включающей ректальные суппозитории Галавит® при ОРВИ у детей в возрасте от 6 до 12 лет по сравнению со стандартной схемой терапии.
Материалы и методы. Проведено сравнительное наблюдательное исследование, включившее 83 ребенка 6-12 лет, находившихся на стационарном и амбулаторном лечении с ОРВИ. Все включенные пациенты получали комплексную терапию основного заболевания. Пациентам основной группы дополнительно назначался препарат Галавит® по одному суппозиторию 50 мг ежедневно в течение 5 дней, затем по 1 суппозиторию 50 мг через день в течение 10 дней. При включении в исследование и на 15 день наблюдения у всех участников проводилось лабораторное обследование (ОАК, иммунологический анализ крови, исследование yровня витaминa D). Длительность наблюдения составила 30 дней.
Результаты. В исследовании участвовало 83 ребенка (01 в основной группе, 32 - в контрольной). В основной группе выявлено статистически значимое укорочение срока купирования ОРВИ по сравнению с контрольной (р = 0,033). Инфекционно-воспалительные осложнения, л также другие осложнения не были зарегистрированы (0%) ни в одной из групп сравнения. На 10 день наблюдения в основной группе отмечено статистически значимое повышение доли клеток CD3+CD19+ (р = 0,041), соотношения CD3+CD4+/CD3+CD8+ (p = 0,036), концентрации IFNy, (р = 0,010). Кроме того, произошло статистически значимое снижение концентрации и доли CDЗ-CD06+CD40+(р = 0,018 и р = 0,006 соответственно) по сравнению с контрольной группой. Препарат характеризовался хорошей переносимостью. Нежелательных явлений в процессе приема препарата Галавит® в течение 10 дней и 30 дней наблюдения не отмечалось.
Выводы. Данные клинической практики подтвердили эффективность ректальных суппозиториев Галавит® дия лечения ОРВИ при применении в составе комплексной терапии в сравнении со стандартной схемой терапии у детей 6-12 лет.
Ключевые слова: ОРВИ, дети, Галавит® суппозитории, антибиотикорезистентность, иммуномодуляторы
Summary.
Objective. To evaluate the effectiveness of complex therapy, including Galavit® rectal suppositories for acute respiratory viral infections (ARVI) in children aged 6 to 12 years compared with the standard therapy.
Methods. An observational study was conducted, which included the results of an examination of. 83 children aged 6-12 years who were hospitalized with ARVI. All patients received complex therapy for the underlying disease. Galavit® was additionally prescribed to patients of the study group one 00 mg suppository daily for 0 days, then 1 suppository every other day for 10 days. Upon the study and on the 10th day of follow-up, all participants underwent a laboratory examination (CBC, immunological blood test, vitamin D level study). The duration of the observation was 30 days.
Results. 81 children participated in the study (01 - study group, 32-control group). In the study group, a statissically significant shortening of the period of ARVI relief was revealed compared with the control group (p = 0.033). Infectious Inflammatory and other complications were not reported (0%) in any of the groups. On day 15 of follow-up, a statisticaIly significant increase in the proportion of CD3+CD19+ cells (p = 0.041), CD3+CD4+/CD3+CD8+ ratio (p = 0.036, IFNy concentration (p = 0.010) was noted in the study group. In addition, there was a statistically significant decrease In the concentration and proportion of CD3-CD06+CD40+ (p = 0.018 and p = 0.006, respectively) compared with the control group. The Galavit® had good tolerability. There were no adverse events during the administration of Galavit® for 10 days and 30 days of follow-up.
Conclusions. Data of clinical practice have confirmed the effectiveness of Galavit® rectal suppositories for the treatment ARVI as part of complex therapy in comparison with the standard therapy in children 6-12 years old.
Keywords: ARVI, children, Galavit® suppositories, antibiotic resistance, immunomodulator
Для цитирования: Перспективы повышения эффективности комплексной терапии ОРВИ у детей в возрасте 16-12 лет / И.Н. Захарова [и др.]// Практика педиатра. 2024. № 4. С. 10—16.
For citation: Prospects for improving the effectiveness of complex therapy of acute respiratory viral infections in children aged 6-12 years / I.N.Zakharova [et al.] // Pediatrician's practica. 2024;(4): 1^^16. (in Russ.)
Актуальность
Острые респираторные вирусные инфекции (ОРВИ) относятся к наиболее частым инфекциям человека. Нестойкость постинфекционного иммунитета приводит к повторным случаям болезни в течение года [1, 2]. Многолетние наблюдения за уровнем заболеваемости ОРВИ демонстрируют более высокую распространенность инфекции среди детского населения по сравнению с взрослыми. Так, во время эпидсезона ОРВИ при уровне общей заболеваемости около 20 000 случаев на 100 тыс. населения заболеваемость среди детей составляя 50 000-80 000, значительно выше [3, 4].
Ежегодные эпидемические вспышки ОРВИ, сопровождающиеся высокой заболеваемостью среди детей, нередкими случаями их повторного заражения, определяют актуальность выбора терапии у детей. Основными задачами лечения ОРВИ являются предупреждение дальнейшего развития заболевания и профилактика осложнений, которые могут потребовать дополнительного назначения антибиотиков [5].
Это связано с тем, что вирусы, вызывающие ОРВИ, индуцируют иммуносупрессию как на местном, так и на системном уровне, что облегчает присоединение вторичной бактериальной инфекции [6]. По данным российских исследователей, на амбулаторном этапе 25-42% детей, заболевших ОРВИ, получали антибиотикотерапию, при этом в 5% случаев проводилась замена антибиотика [7, 8]. В условиях стационара частота назначения антибиотиков при ОРВИ у детей превышает 76% [7]. В связи с этим актуальным является поиск препаратов, способных уменьшить вероятность осложнений ОРВИ и профилактировать назначение антибиотиков.
Набор медикаментов, предлагаемый клиническими рекомендациями для детей, довольно ограничен. В них включены препараты со специфической активностью против вируса гриппа, препараты интерферона-альфа, препараты для симптоматической терапии. Однако следует помнить, что широкий эпидемиологический спектр возбудителей ОРВИ значительно ограничивает возможности применения противогриппозных препаратов. Антибактериальные препараты не показаны при неосложненном течении инфекции [9]. А в патогенетической терапии необходимо учитывать особенности препаратов.
Инфекционное заболевание любой этиологии может сопровождаться выбросом воспалительных цитокинов, гиперактивацией моноцитарно-макрофагальной системы, а также усилением окислительных процессов с последующим возникновением окислительного стресса. В связи с этим есть потребность в препаратах, сочетающих в себе многофункциональность и широкий спектр воздействия на инфекционно-воспалительный процесс.
В последние годы становится актуальным понятие «многоцелевая монотерапия», когда с помощью одного препарата добиваются нескольких фармакологических эффектов. В этом плане перспективным направлением терапии инфекционно-воспалительных заболеваний респираторного тракта является использование препаратов, стимулирующих продукцию собственного (эндогенного) интерферона, регулирующих естественный иммунитет, стабилизирующих и корригирующих адаптивный иммунитет, обладающих противовоспалительным эффектом. К таким лекарственным средствам относится препарат Галавит®.
Галавит® - единственный иммуномодулятор, обладающий комплексным действием. Уникальная биполярная молекулярная структура препарата Галавит® лежит в основе его многоцелевого механизма действия: иммуномодулирующее, противовоспалительное, антиоксидантное, регенеративное [10].
Механизм иммуномодулирующего действия Галавита® связан со способностью избирательно регулировать (повышая или понижая в зависимости от исходных значений) функционально-метаболическую активность клеток врожденного и адаптивного иммунитета (моноцитов, макрофагов, нейтрофилов, натуральных киллеров и др.). Такое двойное действие препарата определяет возможность его применения на разных стадиях ОРВИ различной степени тяжести.
Усиливая фагоцитарную активность моноцитов и макрофагов, бактерицидную активность нейтрофилов и цитотоксическую активность NK-клеток при ее исходном дефиците, препарат повышает неспецифическую резистентность организма к инфекционным заболеваниям бактериальной, вирусной и грибковой этиологии, способствует более быстрой элиминации возбудителя из организма, сокращает частоту, выраженность и длительность инфекций. Кроме того, Галавит® стимулирует выработку эндогенных интерферонов (IFN-a, IFN-ү) клетками-продуцентами; нормализует антителообразование, повышает функциональную активность антител [11].
Противовоспалительное действие реализуется путем обратимого (6-8 ч) ингибирования продукции провоспалительных цитокинов (IL-1, IL-6, TNF-a) гиперактивированными моноцитами/макрофагами, снижая выраженность и длительность интоксикационно-воспалительного процесса [10]. Галавит® восстанавливает угнетенную фагоцитарную функцию макрофагов и нейтрофилов, которая играет ключевую роль в патогенезе воспалительной реакции [12]. При этом в отличие от НПВП Галавит® не обладает побочными эффектами, присущими данной группе препаратов.
Антиоксидантное действие реализуется за счет прямого инактивирования ряда радикальных соединений, блокирования выработки гиперактивированными макрофагами активных форм кислорода, регуляции активности антиоксидантных ферментных систем, тем самым снижая уровень оксидантного стресса и защищая ткани и органы от разрушительного воздействия радикалов. Препарат способствует повышению выработки моноцитами/макрофагами ростовых факторов в очаге воспаления и, таким образом, ускорению процессов регенерации [13].
Практические рекомендации по иммуномодулирующим препаратам в амбулаторной практике (ПРИМА) (2021) одобряют применение иммуномодулирующих препаратов при ОРВИ для детей, в том числе посещающих детские образовательные учреждения, имеющих хронические очаги инфекции и имеющих сопутствующие соматические заболевания [14].
В настоящее время препарат Галавит® выпускается в лекарственных формах: подъязычные таблетки, порошок для приготовления раствора для внутримышечного введения, ректальные суппозитории. Введение препарата в форме ректальных суппозиториев -удобный и безболезненный способ доставки препарата, особенно у детей, которые могут отказываться от приема еды или лекарств на фоне лихорадочного периода. Время полной деформации суппозитория не превышает 15 минут после введения [15]. При ректальном введении лекарство быстро попадает в общий кровоток, что обеспечивает начало фармакологического действия в более ранние сроки.
Ранее проведенные исследования препарата Галавит® с участием детей показали благоприятный профиль безопасности в виде отсутствия проявлений побочного действия препарата при внутримышечном введении [16, 17].
Цель работы: оценить клинико-иммунологическую эффективность препарата Галавит® при ОРВИ у детей в возрасте от 6 до 12 лет по сравнению со стандартной схемой терапии.
Материалы и методы
В 2022-2023 гг. на базе Детской городской клинической больницы им. З.А. Башляевой ДЗМ проведено сравнительное наблюдательное исследование эффективности суппозиториев Галавит® при ОРВИ у детей. В исследовании приняли участие 83 ребенка от 6 до 12 лет, соответствующие критериям включения. Основными критериями включения были: нахождение на стационарном и амбулаторном лечении с диагнозом ОРВИ (острый назофарингит (насморк) код МКБ J00, острый фарингит - J02, острый ларингит и трахеит - J04, острые инфекции верхних дыхательных путей множественной и неуточненной локализации - J06), обратившиеся за медицинской помощью не позднее 72 часов с момента заболевания. Пациенты не включались в исследование, если на момент скрининга или в предшествующие три месяца принимали другие лекарственные средства с иммуномодулирующим эффектом; имели на момент скрининга осложнения ОРВИ, отличающиеся от нозологий, указанных в критериях включения.
Препарат Галавит® назначали в соответствии с инструкцией по применению и индивидуальными особенностями пациента. В случае отказа родителей / законных представителей пациента от назначения препарата Галавит® им предлагалось участие в исследовании в контрольной группе. Родители / законные представители всех пациентов подписали информированное согласие на участие в исследовании.
Первичной конечной точкой выбрано количество пациентов, у которых развились осложнения ОРВИ (острый отит, острый синусит, пневмония, сепсис и иные, по мнению исследователя) с момента начала приема Галавит® в основной группе и с момента включения в исследование в контрольной группе. Вторичные конечные точки включали сроки клинического купирования ОРВИ, измеряемые в сутках с момента начала лечения; количество пациентов с нежелательными явлениями и серьезными нежелательными явлениями в группах исследования; иммунологические показатели пациентов основной и контрольной групп до начала лечения и на 15 сутки терапии.
Сформировано две группы: основная (51 ребенок) и контрольная (32 ребенка). Все пациенты получали терапию ОРВИ, назначенную лечащим врачом в соответствии с Клиническими рекомендациями и Стандартами. Пациентам основной группы дополнительно назначался Галавит® по одному суппозиторию 50 мг ежедневно в течение 5 дней, затем по 1 суппозиторию 50 мг через день в течение 10 дней.
При включении в исследование и на 15 день наблюдения у всех участников основной и контрольной групп проводилось лабораторное обследование, включавшее общий (клинический) анализ крови (ОАК) с оценкой лейкоцитарной формулы, иммунологический анализ крови, исследование уровня витамина D.
В рамках протокола данного исследования планировалось изучение популяции FAS (Full Analysis Set, популяция полного анализа), популяции PPAS (Per Protocol Analysis Set, популяция анализа по протоколу) и популяции SAS (Safety Analysis Set, популяция безопасности). При проведении анализа все три популяции оказались идентичными.
Для проведения статистического анализа был использован язык программирования статистических расчетов IBM SPSS Statistics 26. За уровень статистической значимости было принято значение p < 0,05. Описание количественных показателей представлено с использованием 95% доверительного интервала (ДИ) для среднего, медианы с межквартильным диапазоном, минимальным и максимальным значением. Оценка распределения по критерию Шапиро -Уилка подтвердила отсутствие нормального распределения данных. Поэтому статистический анализ количественных переменных производился с использованием критерия Манна - Уитни.
Специальных методов замещения пропущенных данных в процессе анализа не применялось.
Результаты исследования
Основная (n = 51) и контрольная (n = 32) группы были сопоставимы по возрасту. Медиана возраста в обеих группах составила 8 лет (95% ДИ 7,61-8,98 и 95% ДИ 6,52-8,59 для основной и контрольной групп соответственно: p = 0,465). Доля мальчиков в основной и контрольной группах составила 49% и 40,6% соответственно.
Первичная конечная точка исследования не была рассчитана, т. к. осложнения ОРВИ не были зарегистрированы ни у одного из участников обеих групп.
Анализ сроков купирования клинических проявлений ОРВИ выявил статистически значимое сокращение длительности инфекции в основной группе (5,88 дней против 6,56 в контрольной) (табл. 1).
Таблица 1.
Сроки купирования клинических проявлений ОРВИ в основной (n = 51) и контрольной группах (n = 32), дни
| Показатель | Основная группа | Контрольная группа | р |
| Среднее значение (М ± m) | 5,88 ± 0,93 | 6,56 ± 1,35 | 0,033 |
Показатели ОАК обеих групп не имели статистически значимых различий как на исходном уровне, так и через 15 дней наблюдения.
Клиническая эффективность по основным симптомам
На исходном уровне у пациентов основной группы концентрация иммуноглобулинов (Ig) M была статистически значимо выше (р = 0,04), на 15 день наблюдения статистически значимое различие сохранилось (р = 0,05), что, вероятно, связано с иммуномодулирующим действием Галавита®. Концентрация IgA, IgG, IgE была сопоставимой между группами до и после лечения (табл. 2).
Таблица 2.
Концентрация иммуноглобулинов на исходном уровне и на 15 день наблюдения у пациентов основной (n = 51) и контрольной групп (n = 32)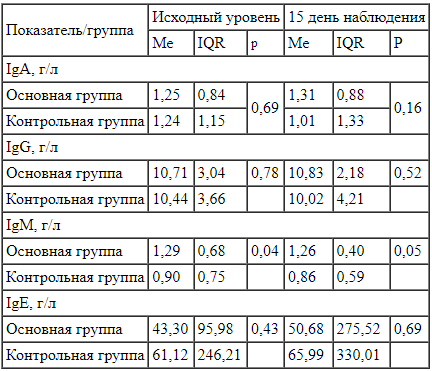 Сравнение показателей иммунограммы выявило, что на исходном уровне у пациентов основной группы была статистически значимо выше концентрация интерферона-гамма (IFNy) (р = 0,014). На 15 день наблюдения в основной группе отмечено статистически значимое повышение доли клеток Т-лимфоцитов (CD3+CD19+) (р = 0,041), соотношения Т-хелперы / Т-цитотоксические клетки (CD3+CD4+/CD3+CD8+) (p = 0,036), концентрации IFNy (р = 0,015). Кроме того, произошло статистически значимое снижение концентрации и доли клеток натуральных киллеров (NK-киллеров) (CD3-CD56+CD45+) (р = 0,018 и р = 0,006 соответственно) по сравнению с контрольной группой (табл. 3).
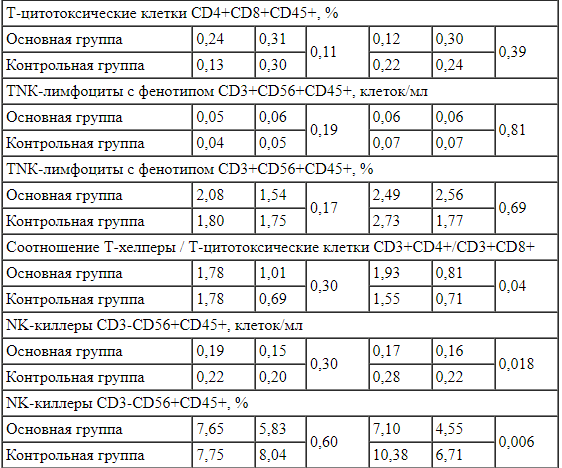
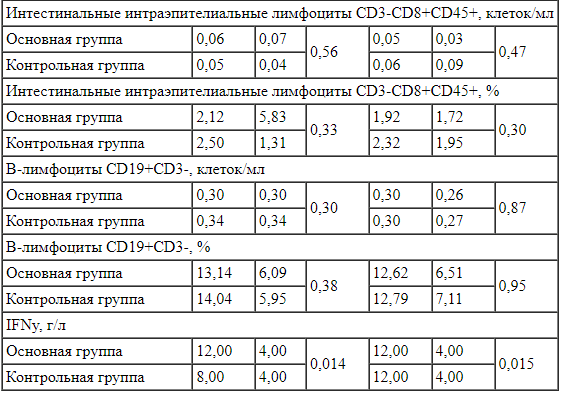
Сравнение показателей иммунограммы выявило, что на исходном уровне у пациентов основной группы была статистически значимо выше концентрация интерферона-гамма (IFNy) (р = 0,014). На 15 день наблюдения в основной группе отмечено статистически значимое повышение доли клеток Т-лимфоцитов (CD3+CD19+) (р = 0,041), соотношения Т-хелперы / Т-цитотоксические клетки (CD3+CD4+/CD3+CD8+) (p = 0,036), концентрации IFNy (р = 0,015). Кроме того, произошло статистически значимое снижение концентрации и доли клеток натуральных киллеров (NK-киллеров) (CD3-CD56+CD45+) (р = 0,018 и р = 0,006 соответственно) по сравнению с контрольной группой (табл. 3).
Таблица 3.
Показатели иммунограммы на исходном уровне и на 15 день наблюдения у пациентов основной (n = 51) и контрольной групп (n = 32)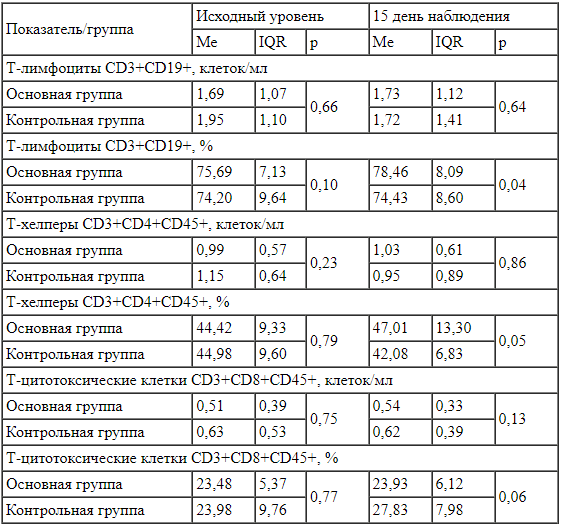
 В течение 15 дней приема Галавит® и последующего наблюдения не было зарегистрировано ни одного случая нежелательных явлений.
В течение 15 дней приема Галавит® и последующего наблюдения не было зарегистрировано ни одного случая нежелательных явлений.
Заключение
В рамках данного наблюдательного исследования возможности применения ректальных суппозиториев Галавит® у детей показано, что препарат позволяет добиться благоприятных изменений в состоянии пациентов.
У детей, получавших Галавит®, показано статистически значимое сокращение сроков купирования клинических проявлений ОРВИ практически на сутки (р = 0,033).
Анализ показателей иммунограммы до и после лечения подтвердил иммуномодулирующее действие препарата Галавит®. Отмечена статистически значимо большая концентрация IgM, интерферона-гамма, доля Т-лимфоцитов, концентрация и доля клеток NK-киллеров, повышение иммуно-регуляторного индекса. А также снижение концентрации нейтрофилов как показателя выраженности воспаления.
Изменения клеточного состава свидетельствуют о сохранении гиперактивации клеток натуральных киллеров после реконвалесценции ОРВИ у пациентов, не получавших Галавит®, и нормализации иммунного ответа при терапии препаратом.
Результаты исследования подтвердили благоприятный профиль безопасности препарата Галавит®. Не отмечено ни одного случая развития нежелательных явлений как в процессе приема препарата, так и в последующие 15 дней и 30 дней наблюдения.
Выводы
Полученные данные подтвердили эффективность ректальных суппозиториев Галавит® для лечения ОРВИ при применении в составе комплексной терапии в сравнении со стандартной схемой терапии у детей 6-12 лет. Механизм действия препарата, позволяющий добиваться нескольких фармакологических эффектов (иммуномодулирующего, противовоспалительного, антиоксидантного, регенеративного), и данные клинических исследований позволяют считать препарат Галавит® важным компонентом патогенетической терапии воспалительных заболеваний любой этиологии, в том числе у детей.
Применение препарата Галавит® в комплексной терапии и в реабилитации больных с инфекционной патологией респираторного тракта способствует повышению неспецифической резистентности, снижению частоты возникновения и тяжести инфекционных осложнений в остром периоде и в периоде реконвалесценции, сокращению длительности реабилитационного периода, приводя к выздоровлению и улучшению качества жизни пациентов, перенесших инфекционное заболевание.
Литература
1. Пожарская В.В. Некоторые факторы, оказывающие влияние на заболеваемость ОРВИ детей (10-18 лет), проживающих на территории Мурманской области // Труды Кольского научного центра РАН. Серия: Естественные и гуманитарные науки. 2024. Т. 4, № 1. С. 170-178.
2. Профилактика гриппа и острой вирусной инфекции у детей с рекуррентной респираторной патологией / А.М. Закирова [и др.] // Медицинский совет. 2024. № 18 (1). С. 41-48.
3. Особенности циркуляции возбудителей ОРВИ на фоне появления и широкого распространения SARS-CoV-2 в 2018-2021 годы / Е.И. Бурцева [и др.] // Эпидемиология и вакцинопрофилактика. 2022. Т. 21, № 4. С. 16-25.
4. Особенности эпидемической ситуации по острым респираторным вирусным инфекциям с учетом пандемического распространения COVID-19 / Т.А. Семененко [и др.] // Эпидемиология и вакцинопрофилактика. 2022. Т. 21, № 4. С. 4-15.
5. Клинические рекомендации. Острые респираторные вирусные инфекции (ОРВИ) у детей. 2023 [Electronic resource].
6. Мизерницкий Ю.Л., Мельникова И.М. Дифференцированная иммунокоррекция у детей с частыми респираторными инфекциями. М. : Оверлей, 2009. 144 с.
7. Николаева С.В., Хлыповка Ю.Н., Горелов А.В. Анализ влияния различных схем терапии на течение вирусных инфекций респираторного тракта у детей // Русский медицинский журнал. Медицинское обозрение. 2023. Т. 7, № 11. С. 713-717.
8. Алимова Х.П., Алибекова М.Б., Рахимова С.Р. Применение антибиотиков у детей // Вестник экстренной медицины. 2020. Т. 13, № 4. С. 100-107.
9. Современные подходы к ведению детей с острой респираторной вирусной инфекцией / А.А. Баранов [и др.] // Педиатрическая фармакология. 2023. Т. 20, № 2. С. 162174.
10. Влияние иммуномодулятора Галавит® на течение хронического рецидивирующего тонзиллита / В. Свистушкин, Г. Никифорова, М. Леонова, И. Покозий // Врач. 2016. № 8. С. 20-25.
11. Immune-Modulating Drug MP1032 with SARS-CoV-2 Antiviral Activity In Vitro: A potential Multi-Target Approach for Prevention and Early Intervention Treatment of COVID-19 / S. Schumann [et al.] // International Journal of Molecular Sciences. 2020. Vol. 21. Р 8803.
12. Черноусов Ф.А., Винницкий Л.И. Профилактика послеоперационных осложнений с применением иммуномодулятора Галавита: метаанализ исследований // Хирургия. Consilium Medicum. 2012. № 2. P. 25-31.
13. Сологуб Т.В., Осиновец О.Ю. Иммуномодуляторы в комплексной терапии ОРВИ: возможности применения препарата Галавит // Русский медицинский журнал. 2013. № 3. С. 144-146.
14. Обновленный согласительный документ ПРИМА в помощь практическому врачу / В.А. Ревякина [и др.] // Педиатрия. Consilium Medicum. 2021. № 2. С. 109-112.
15. Государственная фармакопея Российской Федерации XV издания [Electronic resource]. 2023.
16. Бурков И.В., Царегородцев А.Д., Коренькова С.И. Эффективность препарата Галавит при внутримышечном введении у детей старше 6 лет с гнойными хирургическими заболеваниями // Российский вестник перинатологии и педиатрии. 2008. Т. 53, № 4. С. 78-83.
17. Румянцев А.Г., Щербина А.Ю. Эффективность препарата Галавит у часто и длительно болеющих детей старше 6 лет // Российский вестник перинатологии и педиатрии. 2008. T. 53, № 6. С. 100-101.



