Субклиническое повреждение миокарда и нарушения гемодинамики у детей с идиопатической желудочковой экстрасистолией
СтатьиА.С. Шарыкин1, 2, д-р мед. наук, профессор, Д.В., Замараева1, канд. мед. наук, А.Н. Гришкин2, Н.Д., Тележникова2, Е.В. Карелина2, И.И. Трунина1, 2, д-р мед. наук, профессор
Ключевые слова: желудочковая экстрасистолия, дети, тропонин I, фракция выброса левого желудочка, ударный индекс, двойное произведение
Keywords: premature ventricular contractions, children, troponin I, left ventricular ejection fraction, stroke index, double product
Резюме. Желудочковая экстрасистолия (ЖЭ) у детей в большинстве наблюдений протекает доброкачественно, однако в ряде случаев может приводить к нарушению функции сердца. Свидетельством этого могут быть изменения лабораторных (тропонин I) и инструментальных показателей, которые предшествуют клиническим изменениям, – фракции выброса левого желудочка и ударного индекса (мл/м2) на синусовом ритме, а также двойного произведения. Цель исследования – выявить субклиническое повреждение миокарда и его причины у детей с частой идиопатической ЖЭ, сопровождающейся снижением сердечного выброса и сократимости миокарда. Материал и методы. В иследование были включены 44 ребенка с установленным диагнозом «желудочковая экстрасистолия» (медиана (Ме) количества эктопических комплексов 20 478; интерквартильный размах (Q1–Q3) 13 190–34 517, Ме частоты экстрасистолии за сутки 13,0%, Q1–Q3 8,0–22,4%). Проводилось сопоставление клинических и лабораторно-инструментальных данных и поиск наиболее значимых факторов, влияющих на состояние миокарда у детей при ЖЭ. Эхокардиографические показатели измерялись на синусовом ритме. Результаты. Удовлетворительное состояние сердца сохранялось только у 15 (34%) человек. У 21 (47,7%) был повышен уровень тропонина I, у 13 (29,5%) снижена фракция выброса левого желудочка, у 18 (40,9%) – снижен ударный индекс, а у 39 (88,6%) детей фактическое двойное произведение (Ме 111,6, Q1–Q3 96,9–128,3) было статистически значимо выше, чем должное для данного возраста и пола (Ме 88,9, Q1–Q3 85,2–109,0), p = 0,0001). Всего у 29 (66%) детей имелось субклиническое повреждение или дисфункция миокарда, которые могут быть субстратом для формирования сердечной недостаточности. Шансы развития дисфункции миокарда возрастали при частоте ЖЭ более 10% (отношение шансов 1,63, доверительный интервал 1,23–2,16, p = 0,009). Заключение. У детей с частотой ЖЭ более 10% резко возрастает риск развития дисфункции миокарда, который проявляется снижением фракции выброса и ударного индекса левого желудочка. Наиболее вероятная причина этого – относительная ишемия миокарда, возникающая в связи с более высокими энергетическими потребностями миокарда при ЖЭ. Лабораторные маркеры повреждения миокарда повышаются почти у половины детей с частой ЖЭ.
Summary. Premature ventricular contractions (PVCs) are often benign in children, but in some cases, they can lead to cardiac dysfunction. Variation in laboratory tests (troponin I) and instrumental parameters (left ventricular ejection fraction, stroke index in sinus rhythm, rate pressure product (RPP)) evidences such abnormalities and precedes clinical changes. Objective – to identify subclinical myocardial damage and its causes in children with frequent idiopathic PVCs, accompanied by a decrease in stroke index and myocardial contractility. Materials and methods. The study included 44 children diagnosed with premature ventricular contractions (Me of PVCs frequency 20 478; Q1–Q3: 13 190–34 517, Me of PVCs density in a 24-hour period 13.0%; Q1–Q3: 8.0–22.4%). We compare clinical and laboratory-instrumental data due to reveal most significant factors influencing on myocardial function in children with PVCs. Echocardiographic parameters were measured in sinus rhythm. Results. Normal cardiac function was observed only in 15 (34%) patients. 21 (47.7%) patients had a high level of troponin I, 13 (29.5%) patients had systolic dysfunction of the left ventricle, 18 (40.9%) patients had low stroke index, and in 39 (88.6%) patients the actual RPP (Me 111.6, Q1–Q3: 96,9–128,3) was significantly higher than the expected RPP for such age and gender (Me 88.9, Q1–Q3: 85.2–109.0), p = 0.0001). Thus, 29 (66%) children had subclinical myocardial damage or dysfunction, which can be a cause of heart failure in the future. The chances of developing myocardial dysfunction increased with a PVCs density of more than 10% (OR = 1.63, CI: 1.23–2.16, p = 0.009). Conclusion. The risk of developing myocardial dysfunction is significantly increased in children with a PVCs density more than 10% in a 24-hour period. It leads to systolic dysfunction of the left ventricle and a decrease in cardiac index. The most likely reason for this is the relative myocardial ischemia that occurs due to higher myocardial energy requirements in patients with PVCs. Laboratory markers of myocardial injury are elevated in almost half of children with frequent PVCs.
Для цитирования: Субклиническое повреждение миокарда и нарушения гемодинамики у детей с идиопатической субклинической желудочковой экстрасистолией / А.С. Шарыкин [и др.] // Практика педиатра. 2023. № 4. С. 43–50.
For citation: Sharykin A.S. et al. Subclinical myocardial injury and hemodynamic disorders in children with idiopathic subclinical ventricular extrasystole. Pediatrician's Practice. 2023;(4):43–50. (In Russ.)
1 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
2 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
Введение
Частота желудочковой экстрасистолии (ЖЭ) у детей без органических заболеваний сердца (идиопатической ЖЭ) варьирует, по разным данным, от 27 до 41% [1, 2]. Обычно такой ЖЭ в детском возрасте не придают большого значения в связи с бессимптомным течением в большинстве случаев и уменьшением аритмии со временем [3–5]. Вместе с тем сообщается, что возникновение более 15 000 желудочковых экстрасистол за сутки (>10% от общего количества кардиоциклов за сутки) может быть ассоциировано с риском вторичных изменений миокарда [4, 6], снижением систолической функции левого желудочка и его дилатацией [7–9]. У взрослых подобные нарушения расценивают как аритмогенно-индуцированную кардиомиопатию [10]. Точных данных о частоте и механизмах развития у детей дисфункции сердца при тахикардиях или идиопатической ЖЭ нет, что связано с отсутствием клинической симптоматики и редкостью научных исследований на эту тему [11–13]. Однако с развитием эндоваскулярных методов лечения ЖЭ и увеличением частоты плановых эхокардиографических исследований [14, 15] появилась возможность более подробно описать то, какие механизмы лежат в основе дисфункции сердца, какова степень повреждения миокарда при ЖЭ и при какой частоте ЖЭ оно начинает появляться.
Цель исследования – выявить субклиническое повреждение миокарда и его причины у детей с частой идиопатической ЖЭ, сопровождающейся снижением сердечного выброса и сократимости миокарда.
Материал и методы
Из пациентов, госпитализированных в кардиологическое отделение Детской городской клинической больницы им. З.А. Башляевой (г. Москва) в период с января 2018 г. по декабрь 2021 г. с диагнозом «желудочковая экстрасистолия», были отобраны 44 ребенка в возрасте от 1 до 17 лет включительно с документированной идиопатической ЖЭ (более 5000 экстрасистол за 24 ч), не получающих антиаритмическую терапию и не имеющих симптомов сердечной недостаточности (основная группа). Мальчиков было 23 (52,3%), девочек – 21 (47,7%).
В контрольную группу вошли 44 ребенка без нарушений ритма сердца и патологий других органов и систем, которые проходили обследование в кардиологическом отделении в указанный период; по возрасту и полу детей (22 мальчика, 22 девочки) контрольная группа соответствовала основной.
В исследование не включались дети с любыми заболеваниями сердечно-сосудистой системы, приводящими к изменению нормальной структуры сердца, – кардиомиопатиями, миокардитами, врожденными пороками сердца (кроме открытого овального окна диаметром до 3 мм) или генетически обусловленными каналопатиями, а также пациенты, имевшие в пределах 3 предшествующих месяцев клинические проявления респираторных или других инфекционных заболеваний.
Согласно общепринятым рекомендациям по диагностике ЖЭ [4, 16] анализировали данные электрокардиограммы (ЭКГ) в 12 отведениях и результаты суточного мониторирования ЭКГ (холтеровского мониторирования). Оценивали частоту экстрасистол за сутки и их плотность – долю эктопических комплексов от общего количества кардиоциклов.
В ходе эхокардиографии (эхоКГ) применяли рекомендуемые способы оценки размеров, объемов полостей сердца и толщины миокарда ЛЖ [17]. При этом изображения сердца были синхронизированы с ЭКГ, и его основные показатели измеряли на синусовом ритме. Степень отклонения структур сердца от популяционных норм оценивали по z-фактору, рассчитанному в соответствии с рекомендациями, описанными в научной литературе [18]. Полученные данные обрабатывали в полуавтоматическом режиме с помощью собственной компьютерной программы ZscoreCalculator [19]. Учитывая большой разброс абсолютных величин ударного объема (УО) в зависимости от возраста и антропометрических показателей пациентов, его представляли индексированным по площади поверхности тела – как ударный индекс (УИ, мл/м2). Фракцию выброса левого желудочка (ФВ ЛЖ) измеряли по методу Teichholz.
Дополнительно в качестве показателя величины коронарного кровотока/потребления кислорода миокардом оценивали двойное произведение (ДП), равное произведению значения систолического артериального давления на среднюю частоту сердечных сокращений, разделенную на 100 [20, 21]. Полученную величину сопоставляли с должной частотой сердечных сокращений [22], артериальным давлением [23] и ДП для данного возраста и пола.
Для выявления латентно текущего воспалительного процесса анализировали формулу крови, скорость оседания эритроцитов, уровень С-реактивного белка, результаты исследований методом полимеразной цепной реакции на наличие основных вирусных агентов (вируса простого герпеса 1-го и 2-го типов, вируса Эпштейна – Барр, цито- мегаловируса, вируса герпеса человека 6-го типа), IgM, IgА и IgG к Chlamydia pneumoniae,Mycoplasma pneumoniae, антител к герпесвирусным инфекциям. Критериями текущего воспалительного процесса считали наличие повышенного уровня С-реактивного белка, и/или результат полимеразной цепной реакции, и/или выявление IgM, IgА.
У всех пациентов основной группы был определен уровень кардиального тропонина I в венозной крови (TnI). Для оценки уровня TnI использовался приборный количественный экспресс-тест RAMP (Response Biomedical, Канада) с диапазоном измеряемых значений 0,03–32,00 нг/мл. Согласно данным производителя, 99-й перцентиль верхней границы нормы для взрослой популяции – 0,1 нг/мл. Учитывая отсутствие референсных значений данного теста для детей, мы опирались на собственные данные, полученные в предыдущих исследованиях. При повышении уровня TnI более 0,07 нг/мл результат интерпретировался как «повышенный/положительный» [24].
Статистический анализ данных выполнен с помощью пакета программ SPSS, версия 26.0 (IBM SPSS Statistics, США). Количественные показатели описывали с указанием медианы (Ме) и интерквартильного размаха (Q1–Q3). Для оценки различий между двумя независимыми выборками использовали U-критерий Манна – Уитни. Для оценки степени связи признаков рассчитывали коэффициент корреляции по Спирмену ( r). Результаты считались статистически значимыми при p < 0,05. Для количественного определения силы ассоциации между двумя событиями рассчитывали отношение шансов (ОШ) c 95%-ным доверительным интервалом (ДИ).
Результаты
Медиана возраста детей в основной группе составила 7,9 года (Q1–Q3 1,6–14,7 года). Медиана площади поверхности тела 0,98 м 2 (Q1–Q3 0,49–1,65 м 2). Ни у одного ребенка не было клинических симптомов сердечной недостаточности. Медиана возраста детей в контрольной группе составила 7,1 года (Q1–Q3 2,0–12,0 года), площадь поверхности тела 0,93 м 2 (Q1–Q3 0,53–1,33 м2). При сравнении основной и контрольной групп статистически значимых возрастных и антропометрических различий не выявлено (p = 0,7).
Только 15 (34,1%) из 44 детей с ЖЭ предъявляли жалобы при поступлении в стационар. У 6 (13,6%) из них клиническая картина была неспецифична и заключалась в повышенной утомляемости, плохой переносимости физических нагрузок, жалобах на головокружение. Из 44 детей 9 (20,5%) ощущали колющую боль в области сердца, сердцебиения, «перебои» в работе сердца.
При анализе анамнестических данных обращало на себя внимание, что у 33 (75%) из 44 пациентов диагноз «желудочковая экстрасистолия» был установлен случайно во время диспансеризации или при рутинном проведении ЭКГ перед поступлением в школу/спортивную секцию. У 7 (15,9%) человек обнаружены лабораторные признаки текущего воспалительного процесса, однако без клинической симптоматики.
Медиана частоты эктопических комплексов за 24 ч составляла 20 478 (Q1–Q3 13 190–34 517), что соответствовало 13,0% (Q1–Q3 8,0–22,4%) за сутки. У пациентов с клиническими симптомами плотность экстрасистол (Ме 18,4%, Q1–Q3 13,0–22,4%) была больше, чем у асимптомных детей (Ме 10,6%, Q1–Q3 7,3–12%, p = 0,043). Однако статистически значимой взаимосвязи между наличием жалоб и уровнем TnI или изменениями ФВ/УИ у них установлено не было (p > 0,05).
Так как референсные значения УИ у детей редко являются предметом научного исследования и, как правило, их можно получить лишь дополнительным расчетным способом из опубликованных данных об УО [25, 26], в качестве пороговых величин нами использованы нижние квартили (Q1) УИ и ФВ, полученные в контрольной группе (табл. 1).
Таблица 1. Основные показатели эхокардиограммы у пациентов контрольной группы (n = 44)
| Показатель | Ме | Q1 | Q3 |
| Возраст, годы | 7,1 | 2,0 | 12,0 |
| Площадь поверхности тела, м2 | 0,93 | 0,53 | 1,33 |
| Ударный индекс, мл/м2 | 42,0 | 39,0 | 48,1 |
| Фракция выброса левого желудочка, % | 67,0 | 63,9 | 71,1 |
Таким образом, при статистической обработке данных сниженными считали УИ <39 мл/м 2 и ФВ ЛЖ <63%.
В основной группе лишь в 15 (34%) случаях не было выявлено нарушений функции сердца или повышения уровня TnI. У 21 (47,7%) ребенка с ЖЭ был повышен уровень TnI (Ме 0,21 нг/мл, Q1–Q3 0,13–0,25 нг/мл), у 13 (29,5%) снижена ФВ ЛЖ (Ме 60,6%, Q1–Q3 58–61,8%), а у 18 (40,9%) – снижен УИ (Ме 36,3 мл/м 2, Q1–Q3 33,8–37,4 мл/м2). У 39 (88,6%) детей фактическое ДП было статистически значимо выше, чем ожидаемое ДП: Ме 111,6, (Q1–Q3 96,9–128,3), против Ме 88,9 (Q1–Q3 85,2–109, p = 0,0001), и лишь в 5 (11,4%) случаях были незначительно ниже последнего.
Ни у одного пациента не было дилатации ЛЖ (конечный диастолический размер ЛЖ: Ме –0,18, Q1–Q3 –0,78…0,44).
Подробно соотношения между анализируемыми показателями приведены в табл. 2.
Таблица 2. Парные сопоставления основных показателей пациентов при желудочковой экстрасистолии (Ме; Q1–Q3)
| Показатель | n (%) | Величина показателя | p | Уровень тропонина I, нг/мл | p | Фракция выброса, % | p | Частота экстрасистол, % | p | Двойное произведение | p |
| Фракция выброса <63% | 13 (29,5) | 60,6; 58–61,8 | p = 0,0001 | 0,14; 0,03–0,22 | p = 0,047 | – | – | 17,0; 13,3–29,7 | p = 0,028 | 113,6; 97,5–131,5 | p = 0,600 |
| Фракция выброса ≥63% | 31 (70,4) | 69,6; 65,7–73,9 | 0,03; 0,03–0,12 | – | 11,7; 6,8–21,3 | 110; 96,9–127,0 | |||||
| Ударный индекс <39 мл/м2 | 18 (40,9) | 36,3; 33,8–37,4 | p = 0,0001 | 0,12; 0,03–0,25 | p = 0,036 | 63,4; 60,4–66,7% | p = 0,012 | 13,9; 10,2–19 | p = 0,600 | 115,6; 106,9–134,9 | p = 0,033 |
| Ударный индекс ≥39 мл/м2 | 26 (59,1) | 45,3; 41,4–48,4 | 0,03; 0,03–0,14 | 69,5%; 63,6–73,9% | 11,7; 6,8–23 | 107; 91,9–124,1 | |||||
| Частота экстрасистол ≥10% | 32 (72,7) | 18,4; 12,9–24,5 | p = 0,0001 | 0,10; 0,03–0,22 | p = 0,070 | 64,4; 61,4–70,1 | p = 0,037 | – | – | 111,6; 94,6–126,3 | p = 0,700 |
| Частота экстрасистол <10% | 12 (27,3) | 6,0; 3,6–7,8 | 0,03; 0,03–0,08 | 71,5; 65,1–73,9 | – | 112,1; 99,3–134,4 | |||||
| Уровень тропонина I повышен | 21 (47,7) | 0,21; 0,13–0,25 | p = 0,0001 | – | – | 63,7; 61,2–70,2 | p = 0,100 | 15,7; 12–24,5 | p = 0,041 | 121,5; 106,8–134,0 | p = 0,030 |
| Уровень тропонина I не повышен | 23 (52,3) | 0,03; 0,03–0,03 | – | 68,5; 64,1–72,8 | 10,8; 6,0–20,6 | 106,2; 94,5–119,9 | |||||
| Воспалительный процесс есть | 7 (15,9) | – | – | 0,13; 0,03–0,29 | p = 0,300 | 63,1; 60,5–64,8 | p = 0,052 | 14,35; 10,6–18,4 | p = 0,900 | 94,5; 91,3–100,1 | p = 0,017 |
| Воспалительного процесса нет | 37 (84,1) | – | 0,03; 0,03–0,17 | 68,2; 62,6–73,5 | 12,9; 8,0–22,4 | 114,5; 99,6–132,0 |
Примечание: полужирным шрифтом отмечены статистически значимые различия.
Связь уровня TnI с частотой экстрасистол. По результатам корреляционного анализа нами была установлена прямая статистически значимая связь между уровнем TnI и следующими двумя показателями: частотой аритмии за сутки (r = 0,366; p = 0,022) и количеством парных экстрасистол (r = 0,354; p = 0,034). Была статистически значимая разница между частотой аритмии в подгруппе детей с повышенным уровнем TnI и частотой в подгруппе с его нормальным уровнем (Ме 15,7%, Q1–Q3 12–24,5%, против Ме 10,8%, Q1–Q3 6,0–20,6%, p = 0,041).
Связь сократительной и насосной функции ЛЖ с частотой ЖЭ. Так как ФВ ЛЖ и УИ ЛЖ не являются тождественными характеристиками работы ЛЖ и их изменения не всегда протекают синхронно (рис. 1), они оценивались нами по отдельности.
Рис. 1. Изменения ударного индекса (УИ) и фракции выброса (ФВ) у детей с желудочковой экстрасистолией. Двусторонняя стрелка указывает на несинхронные изменения показателей
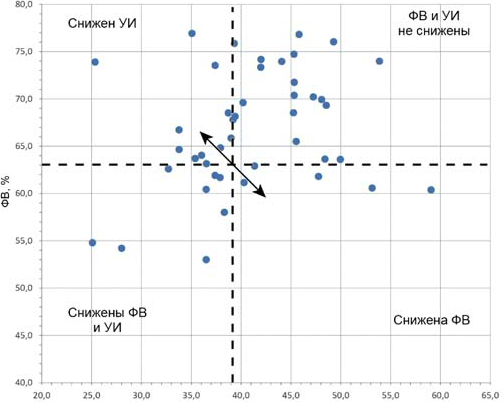
В нашем исследовании было установлено, что дети со сниженной ФВ ЛЖ имели статистически значимо более высокую частоту аритмии за сутки по сравнению с пациентами без нарушения сократимости миокарда (Ме 17,0%, Q1–Q3 13,3–29,7% против Ме 11,7%, Q1–Q3 6,8–21,3%, p = 0,028).
Так как в научной литературе при частоте экстрасистолии более 10% за сутки она обозначается как «частая» [3], мы провели сравнительный анализ изменений сократимости ЛЖ, основываясь на данном пороге. У детей с «частой» ЖЭ (≥10%) ФВ ЛЖ была статистически значимо меньше, чем у детей с редкой ЖЭ (Ме 64,4%, Q1–Q3 61,4–70,1% против Ме 71,5%, Q1–Q3 65,1–73,9%, p = 0,037). Таким образом, шансы на снижение ФВ ЛЖ в первой подгруппе были выше в 1,63 раза (ДИ 1,23–2,16, p = 0,009).
Что касается УИ, его снижение также сочеталось с более высокой частотой ЖЭ (Ме 13,9%, Q1–Q3 10,2–19,0% против Ме 11,7%, Q1–Q3 6,8–23,0% в группе с нормальным УИ), однако не достигало порога статистической значимости (p = 0,600).
Связь сократительной и насосной функции ЛЖ с уровнем TnI. В ходе корреляционного анализа нами была установлена статистически значимая обратная связь между ФВ ЛЖ и уровнем TnI (r = −0,298; p = 0,049). Уровень TnI у детей со сниженной ФВ ЛЖ достоверно превышал его величину у пациентов с нормальной ФВ ЛЖ (Ме 0,14 нг/мл, Q1–Q3 0,03–0,22 нг/мл против Ме 0,03 нг/мл, Q1–Q3 0,03–0,12 нг/мл, p = 0,047).
В настоящем исследовании также впервые была установлена у детей с ЖЭ статистически значимая обратная связь между УИ и уровнем TnI; его значения при сниженном УИ были выше, чем при неизмененном УИ (Ме 0,12 нг/мл, Q1–Q3 0,03–0,25 нг/мл, против Ме 0,03 нг/мл, Q1–Q3 0,03–0,14 нг/мл, p = 0,036), а шансы на снижение УИ при повышенном уровне TnI были значимо больше: ОШ 3,78, ДИ 1,06–13,45 (p = 0,037).
Оценка уровня коронарного кровотока. Величина ДП, отражающего потребление кислорода миокардом, колебалась в широких пределах. При этом у 39 (88,6%) детей фактическое ДП было значительно выше должного ДП (Ме 111,6, Q1–Q3 96,9–128,3 против Ме 88,9, Q1–Q3 85,2–109, p = 0,0001) и лишь в 5 (11,4%) случаях было или равно, или незначительно ниже последнего. Также нами установлено, что у детей с высоким TnI фактическое ДП было статистически значимо больше, чем у детей с нормальными значениями TnI (Ме 121,5 Q1–Q3 106,8–134 против Ме 106,2, Q1–Q3 94,5–119,9, p = 0,03). В результате была установлена статистически значимая прямая корреляционная связь между уровнем TnI и величиной фактического ДП (r = 0,3797, p = 0,0187, рис. 2).
Рис. 2. Корреляции между фактическим двойным произведением (ДП) и уровнем тропонина I (TnI), а также ожидаемым ДП и TnI. Достоверная корреляция регистрируется только в первом случае (r = 0,3797, p = 0,0187)
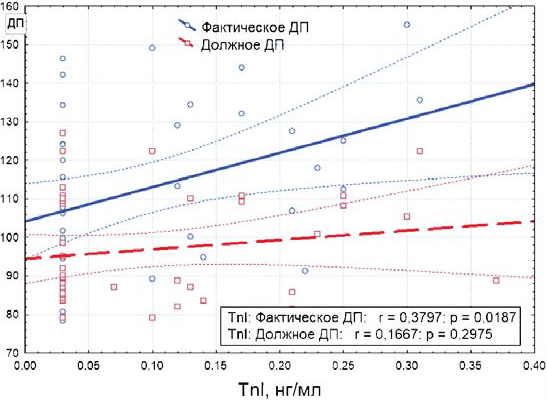
Кроме того, пациенты со сниженным УИ имели статистически значимо более высокие значения фактического ДП, чем пациенты с неизмененным УИ (Ме 115,6, Q1–Q3 106,9–134,9 против Ме 107,0, Q1–Q3 91,9–124,1, p = 0,033).
Обсуждение
Мономорфные ЖЭ у детей со структурно нормальным сердцем обычно считаются доброкачественными. Однако в последнее десятилетие это общее мнение стало оспариваться исходя из опыта лечения ЖЭ у взрослых. Во многих сообщениях начиная с 1998 г. [27] у пациентов с частыми преждевременными желудочковыми сокращениями стали описывать дисфункцию ЛЖ и увеличение его диастолического размера. Так как улучшение и даже нормализация функции сердца наступали после медикаментозного лечения или радиочастотной абляции эктопического очага, патологию стали обозначать как аритмогенно-индуцированную кардиомиопатию [10].
У детей дисфункция ЛЖ, развившаяся при ЖЭ, была впервые описана B. Kakavand и соавт. в 2010 г. [7] (4 пациента в возрасте от периода новорожденности до 17 лет). У 2 из них улучшение наступило спонтанно, у других – после применения антиаритмических средств. Во всех случаях снижение количества экстрасистол предшествовало на 2–4 мес улучшению функции сердца. Это в значительной мере поддерживало предположение о том, что и у детей ЖЭ может вызывать обратимую кардиомиопатию. В последующем аналогичные наблюдения детей в нарастающем количестве представляли специалисты из США, Канады, Китая: у 20–47% детей частые экстрасистолы вызывали заметную дилатацию и/или дисфункцию ЛЖ, которые были обратимы после катетерной абляции или медикаментозного лечения [9–12, 28].
Причины формирования аритмогенно-индуцированной кардиомиопатии точно не установлены. Большое количество выдвигаемых версий свидетельствует о многофакторности процесса. Среди обсуждаемых – диссинхронный паттерн сокращения желудочков, транзиторные изменения уровня внутриклеточного кальция, а также мембранного ионного потока, ишемия несоответствия между возросшей потребностью миокарда в кислороде и его доставкой из-за потери эффективного сердечного выброса (при отсутствии ограничивающего кровоток стеноза коронарных артерий) [14, 29–34]. К этому можно добавить гипотетическое снижение насосной функции желудочка в некоторых случаях вследствие изменения концентрации TnI, который способен снижать чувствительность миофиламентов к Ca 2+ [35]. Перечисленные процессы повреждения миокарда при отсутствии лечения ЖЭ могут приводить к самоподдерживающемуся патологическому статусу.
Нами у детей с ЖЭ впервые выявлено субклиническое повреждение миокарда, характеризующееся повышением уровня TnI. Традиционно одной из причин повреждения миокарда считается инфекционно-воспалительный процесс [36]. Однако в нашемисследовании его удалось выявить лишь у 7 (15,9%) пациентов, причем повышение уровня TnI установлено только у 4 (57,1%) из них. Таким образом, на 1-е место выдвигаются другие факторы, связанные с нарушением кровоснабжения миокарда. К ним можно отнести дефект диастолы (уменьшение времени коронарного кровотока), особенно в условиях хронической диссинхронии, перемежающееся уменьшение-увеличение потребления миокардом кислорода из-за меняющейся нагрузки на желудочки, увеличение базального потребления кислорода миокардом из-за увеличенной частоты сердечных сокращений.
При снижении ударного выброса ЛЖ ведущим клиническим симптомом становится тахикардия, призванная компенсировать дефицит минутного объема. При прогрессировании дисфункции сердца могут появиться и другие признаки сердечной недостаточности. Однако у наблюдаемых нами детей имелись в основном редкие и неспецифические симптомы (головокружения, плохая переносимость физических нагрузок). Ощущения сердцебиений, «перебоев» и болей в сердце можно считать более характерными для ЖЭ, однако они отмечались только в 9 (20,5%) случаях. В то же время повышенная нагрузка на сердце выявлялась достаточно часто, характеризуясь изменениями ДП, которое давно используется для оценки коронарного резерва и сосудистого русла у взрослых больных. Низкое ДП при максимальной физической нагрузке (например, при сердечной недостаточности) либо повышенное ДП в состоянии покоя, наблюдаемое при микрососудистых заболеваниях (например, при метаболическом синдроме), считаются признаками нарушения кровоснабжения миокарда [20, 21]. Нами данный показатель впервые использован для оценки степени изменения коронарного кровотока у детей с ЖЭ. Выявлено, что фактическое ДП (Ме 111,6, Q1–Q3 96,9–128,3) достоверно превышало должное ДП (Ме 88,9, Q1–Q3 85,2–109, p = 0,0001) уже в покое, что может свидетельствовать об избыточной работе сердечной мышцы вследствие частых сокращений. Это, в свою очередь, способно приводить к субклиническому повреждению миокарда и потенциальному развитию его аритмогенной дисфункции. Данный факт подтвержден статистически значимой корреляционной связью между величиной ДП и уровнем TnI (r = 0,3797, p = 0,0187).
Следует отметить, что в публикациях об аритмогенно-индуцированной кардиомиопатии у взрослых практически не анализируется время возникновения ЖЭ и сроки развития кардиомиопатии. Y. Sun и соавт. [13] в своей работе показали, что у бессимптомных детей ФВ и сердечный выброс на синусовом ритме остаются в пределах нормы. Однако при каждой экстрасистоле они снижаются, и усредненная ФВ и выброс (на синусовом ритме + во время экстрасистол) также убывают, особенно заметно при частоте ЖЭ >10%. В нашем исследовании выявлено снижение механической и сократительной функции ЛЖ в виде УИ и ФВ ЛЖ, не достигающих ожидаемого уровня уже на синусовом ритме. Причины доминирования того или иного нарушения могут крыться в том, что преобладает у данного пациента – значительная диссинхрония, нарушающая механику выброса в относительно сохранном миокарде, или степень повреждения миокарда.
Полученные данные свидетельствуют о формировании субстрата возможной сердечной недостаточности у детей с «частой» ЖЭ. На наш взгляд, более редкое возникновение аритмогенно-индуцированной кардиомиопатии в детском возрасте может быть объяснено большей устойчивостью «молодого» миокарда к стрессам, сохранением способности кардиомиоцитов к репликации и росту, а также отсутствием фиброзных очагов. Однако база для аритмогенно-индуцированной кардиомиопатии закладывается, и при сохранении высокой экстрасистолической нагрузки она может реализоваться во взрослом возрасте.
Важным является установление порога «безопасности» для ЖЭ. Ориентация на клиническую симптоматику является недостаточной – у многих детей жалобы отсутствовали полностью, а при их наличии не было корреляций со степенью тяжести дисфункции сердца. Латентное формирование аритмогенно-индуцированной кардиомиопатии отмечают и другие исследователи [8, 37]. Наиболее значимым показателем можно считать частоту аритмии. По литературным данным, «частой» считается ЖЭ при количестве экстрасистол >15 000 за сутки или более 10% от общего количества кардиоциклов [3, 6]. Наши наблюдения указывают на последнюю величину как порог, после которого резко возрастают шансы развития дис- функции миокарда (ОШ 1,63, ДИ 1,23–2,16, p = 0,009). Медианы суточной частоты ЖЭ для сниженной ФВ и/или УИ равнялись 17,0 и 13,9% соответственно. При таком уровне аритмии и наличии дисфункции сердца уже требуется терапия ЖЭ в соответствии с рекомендациями отечественных кардиологических ассоциаций [38]. Полученные данные позволяют формировать более дифференцированный диагностический и лечебный подход при частой желудочковой эктопии.
Заключение
В ходе обследования детей с частой идиопатической ЖЭ на доклинической стадии заболевания было установлено, что 66% из них имели нарушения в работе сердца различной степени выраженности, проявляющиеся в повышении уровня маркера повреждения миокарда TnI и/или в снижении УИ/ФВ ЛЖ.
Исследование уровня TnI у детей с ЖЭ не считается обязательным и рутинным. Однако полученные результаты свидетельствуют о возникновении субклинических повреждений миокарда почти у половины обследованных детей. Наиболее вероятной причиной этого является относительная ишемия миокарда, возникающая в связи с более высокими энергетическими потребностями миокарда при ЖЭ, о чем свидетельствует повышенное ДП. Изменения ДП прямо коррелируют с уровнем TnI.
Шансы на развитие дисфункции миокарда существенно возрастают при частоте ЖЭ более 10% и реализуются в виде снижения ФВ и УИ ЛЖ. Данные процессы могут составлять базу для будущего формирования аритмогенно-индуцированной кардиомиопатии, для подтверждения чего необходимы длительные наблюдения за пациентами, имеющими повышенный уровень TnI в детском возрасте.
Выражение признательности
Авторы исследования выражают признательность главному врачу Детской городской клинической больницы им. З.А. Башляевой д-ру мед. наук, проф. Исмаилу Магомедовичу Османову за содействие в проведении исследования.
- Cardiac arrhythmias in healthy children revealed by 24-hour ambulatory ECG monitoring / M. Nagashima [et al.] // Pediatric Cardiology. 1987. Vol. 8, No. 2. P. 103–108. DOI: 10.1007/BF02079464.
- Dickinson D.F., Scott O. Ambulatory electrocardiographic monitoring in 100 healthy teenage boys // British Heart Journal. 1984. Vol. 51, No. 2. P. 179–183. DOI: 10.1136/hrt.51.2.179.
- PACES/HRS Expert Consensus Statement on the Evaluation and Management of Ventricular Arrhythmias in the Child with a Structurally Normal Heart / J.E. Crosson [et al.] // Heart Rhythm. 2014. Vol. 11, No. 9. P. 55–78. DOI: 10.1016/j.hrthm.2014.05.010.
- Желудочковая экстрасистолия у детей / А.А. Баранов [и др.] // Педиатрическая фармакология. 2018. Т. 15, № 6. С. 435–446. DOI: 10.15690/pf.v15i6.1981.
- Cağdaş D, Celiker A, Ozer S. Premature ventricular contractions in normal children // Turkish Journal of Pediatrics. 2008. Vol. 50, No. 3. P. 260–264.
- Школьникова М.А., Березницкая В.В. Диагностика и медикаментозное лечение желудочковых экстрасистолий у детей // Российский вестник перинатологии и педиатрии. 2008. Т. 53, № 2. С. 60–67.
- Kakavand B., Ballard H.O., Disessa T.G. Frequent ventricular premature beats in children with a structurally normal heart: a cause for reversible left ventricular dysfunction? // Pediatric Cardiology. 2010. Vol. 31, No. 7. P. 986–990. DOI: 10.1007/s00246-010-9740-7./li>
- Spector Z.Z., Seslar S.P. Premature ventricular contraction-induced cardiomyopathy in children // Cardiology in the Young. 2016. Vol. 26, No. 4. P. 711–717. DOI: 10.1017/S1047951115001110.
- Characteristics of premature ventricular contractions in healthy children and their impact on left ventricular function / S. Abadir [et al.] // Heart Rhythm. 2016. Vol. 13, No. 11. P. 2144–2148. DOI: 10.1016/j.hrthm.2016.07.002.
- Prabhu S., Kistler P.M. Can the Past Re-Shape the Future? New Insights Into PVC-Mediated Cardiomyopathy From the CHFSTAT Trial and the Retelling of a Familiar Story // JACC: Clinical Electrophysiology. 2021. Vol. 7, No. 3. P. 391–394. DOI: 10.1016/j.jacep.2020.11.020.
- Left ventricular dysfunction is associated with frequent premature ventricular complexes and asymptomatic ventricular tachycardia in children / R.A. Bertels [et al.] // Europace. 2017. Vol. 19, No. 4. P. 617–621. DOI: 10.1093/europace/euw075.
- Risk factors for left ventricle enlargement in children with frequent ventricular premature complexes / B. Chen [et al.] // American Journal of Cardiology. 2020. Vol. 131. P. 49–53. DOI: 10.1016/j.amjcard.2020.06.042.
- Th e infl uence of premature ventricular contractions on left ventricular function in asymptomatic children without structural heart disease: an echocardiographic evaluation / Y. Sun [et al.] // International Journal of Cardiovascular Imaging. 2003. Vol. 19, No. 4. P. 295–299. DOI: 10.1023/a:1025418531853.
- Чернышев А.А., Ковалев И.А., Татарский Р.Б. Радиочастотная аблация идиопатической желудочковой экстрасистолии у детей: эффективность и влияние на внутрисердечную гемодинамику // Вестник аритмологии. 2012. № 70. С. 50–55.
- Первый опыт оценки влияния желудочковых экстрасистол на суточный выброс левого желудочка у детей / Е.П. Осипова [и др.] // Российский кардиологический журнал. 2021. Т. 26, № S6. С. 22.
- Макаров Л.М. Холтеровское мониторирование. 4-е изд. М. : Медпрактика-М, 2017.
- Lang RM, Bierig M, Devereux RB et al. Recommendations for Chamber Quantifi cation: A Report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantifi cation Writing Group, Developed in Conjunction with the European Association of Echocardiography, a Branch of the European Society of Cardiology // Journal of the American Society of Echocardiography. 2005. Vol. 18. P. 1440–1463.
- Regression equations for calculation of z scores of cardiac structures in a large cohort of healthy infants, children, and adolescents: an echocardiographic study / M.D. Pettersen [et al.] // Journal of the American Society of Echocardiography. 2008. Vol. 2. P. 922–934.
- Шарыкин А.С., Рушайло-Арно А.А., Субботин П.А. Свидетельство о государственной регистрации программы для ЭВМ № 2016610878 ZscoreCalculator V.12. Дата регистрации в Реестре программ для ЭВМ 21.01.2016.
- Hemodynamic predictors of myocardial oxygen consumption during static and dynamic exercise / R.R. Nelson [et al.] // Circulation. 1974. Vol. 50, No. 6. P. 1179–1189. DOI: 10.1161/01.cir.50.6.1179.
- Kalff V., Duff y S.J., Kaufmann P.A. Rate-pressure product-derived global coronary fl ow reserve (CFR): an unrecognized parameter available during all standard exercise ECG stress tests and conventional exercise SPECT myocardial perfusion studies (exMPS) // Journal of Nuclear Cardiology. 2014. Vol. 21, No. 2. P. 400–401. DOI: 10.1007/s12350-013-9850-8.
- Нормативные параметры ЭКГ у детей и подростков / под ред. М.А. Школьниковой, И.М. Миклашевич, Л.А. Калинина. М. : Ассоциация детских кардиологов России, 2010.
- Александров А.А., Кисляк О.А., Леонтьева И.В. Клинические рекомендации. Диагностика, лечение и профилактика артериальной гипертензии у детей и подростков // Системные гипертензии. 2020. Т. 17, № 2. С. 7–35.
- Замараева Д.В. Клиническая значимость тропонина I у детей с сердечно-сосудистой патологией : автореф. дис. ... канд. мед. наук. М., 2022. 23 с.
- Echocardiographic Reference Ranges of Non-invasive Myocardial Work Indices in Children / T.T.M. Pham [et al.] // Pediatric Cardiology. 2022. Vol. 43, No. 1. P. 82–91. DOI: 10.1007/s00246-021-02695-x.
- Normal ranges of non-invasive left ventricular myocardial work indices in healthy young people / X. Luo [et al.] // Frontiers in Pediatrics. 2022. Vol. 10. 1000556. DOI: 10.3389/fped.2022.1000556.
- Duff ee D.F., Shen W.K., Smith H.C. Suppression of frequent premature ventricular contractions and improvement of left ventricular function in patients with presumed idiopathic dilated cardiomyopathy // Mayo Clinic Proceedings. 1998. Vol. 73, No. 5. P. 430–433. DOI: 10.1016/S0025-6196(11)63724-5.
- Spector Z.Z., Seslar S.P. Premature ventricular contraction- induced cardiomyopathy in children // Cardiology in the Young. 2016. Vol. 26, No. 4. P. 711–717. DOI: 10.1017/S1047951115001110.
- Сцинтиграфическая семиотика аритмогенной дисфункции сердца при наличии желудочковых экстрасистол у детей и подростков / Ю.Б. Лишманов [и др.] // Медицинская радиология и радиационная безопасность. 2013. Т. 58, № 3. С. 39–44.
- Cellular mechanism of premature ventricular contraction-induced cardiomyopathy / Y. Wang [et al.] // Heart Rhythm. 2014. Vol. 11, No. 11. P. 2064–2072. DOI: 10.1016/j.hrthm.2014.07.022.
- Left Ventricular Dyssynchrony Predicts the Cardiomyopathy Associated With Premature Ventricular Contractions / T.E. Walters [et al.] // Journal of the American College of Cardiology. 2018. Vol. 72, No. 23, Pt A. P. 2870–2882. DOI: 10.1016/j.jacc.2018.09.059.
- Left ventricular myocardial dysfunction in arrhythmogenic cardiomyopathy with left ventricular involvement: A door to improving diagnosis / Y. Vives-Gilabert [et al.] // International Journal of Cardiology. 2019. Vol. 274. P. 237–244. DOI: 10.1016/j.ijcard.2018.09.024.
- Yoldaş T., Örün U.A. What is the Signifi cance of Elevated Troponin I in Children and Adolescents? A Diagnostic Approach // Pediatric Cardiology. 2019. Vol. 40, No. 8. P. 1638–1644. DOI: 10.1007/s00246-019-02198-w.
- Гемодинамические эффекты желудочковой экстрасистолии у детей по данным эхокардиографии / К.Б. Алексеева [и др.] // Российский электронный журнал лучевой диагностики. 2021. Т. 11, № 2. С. 143–152. DOI: 10.21569/2222-7415-2021- 11-2-143-152.
- Bers D.M. Cardiac excitation-contraction coupling // Nature. 2002. Vol. 415, No. 6868. P. 198–205. DOI: 10.1038/415198a.
- What Raises Troponins in the Paediatric Population? / D. Chong [et al.] // Pediatric Cardiology. 2018. Vol. 39, No. 8. P. 1530–1534. DOI: 10.1007/s00246-018-1925-5.
- Left Ventricular Dysfunction in Outpatients with Frequent Ventricular Premature Complexes / K.M. Park [et al.] // Texas Heart Institute Journal. 2022. Vol. 49, No. 1. e207265. DOI: 10.14503/THIJ-20-7265.
- Желудочковые нарушения ритма. Желудочковые тахикардии и внезапная сердечная смерть. Клинические рекомендации 2020 / Д.С. Лебедев [и др.] // Российский кардиологический журнал. 2021. Т. 26, № 7. С. 4600. DOI: 10.15829/1560-4071-2021-4600.

