Тактика повышения охвата вакцинацией детей, родившихся с очень низкой и экстремально низкой массой тела, с использованием персонализированного подхода
СтатьиА.К. Миронова1,2, канд. мед. наук, И.М. Османов1,3, д-р мед. наук, профессор, Л.Н. Мазанкова1,2, д-р мед. наук, профессор, О.И. Потянова1, Е.В. Моисеева1
1 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой департамента здравоохранения Москвы»
2 ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России
3 ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России
Резюме. В статье представлен анализ причин низкого охвата вакцинацией недоношенных детей, родившихся с очень низкой (ОНМТ) и экстремально низкой (ЭНМТ) массой тела, на основе которого разработан и внедрен в клиническую практику персонализированный подход к тактике повышения охвата вакцинацией детей.
Ключевые слова: недоношенный ребенок, вакцинация, вакцинопрофилактика
Summary. The article presents an analysis of the reasons for the low vaccination coverage of premature infants born with those born with very low and extremely low body weight, on the basis of which a personalized approach to the tactics of increasing vaccination coverage of children has been developed and implemented in clinical practice.
Keywords: premature baby, vaccination, vaccination prevention
Роль вакцинопрофилактики в детском возрасте трудно переоценить, особенно у детей, родившихся с очень низкой (ОНМТ) и экстремально низкой (ЭНМТ) массой тела, с учетом их высокой восприимчивости к различным вакциноуправляемым инфекциям. У данного контингента детей инфекционные заболевания могут иметь особенно тяжелое течение с высоким риском летального исхода [1-5]. В данном контексте совершенно очевидна высокая актуальность внедрения новых подходов и форм повышения охвата вакцинацией недоношенных детей согласно Национальному календарю профилактических прививок.
В настоящее время отечественными авторами полностью признана и поддерживается позиция Всемирной организации здравоохранения и других стран по поводу необходимости вакцинации недоношенных детей, начиная с двух месяцев (восемь недель жизни) соответственно паспортному возрасту [6-8]. В России, как и в других странах, Национальный календарь профилактических прививок утверждается на государственном уровне (приказы Минздрава России № 125н от 21 марта 2014 г. и № 1122н от 6 декабря 2021 г.).
Так, в Методических рекомендациях Союза педиатров России [9] прописано, что вакцинация указанной группы детей, как и доношенных, должна проводиться в установленном порядке в соответствии с Национальным календарем прививок (приказ Минздрава России № 1122 от 06.12.21) с учетом хронологического возраста, который считают со дня рождения ребенка.
Вместе с тем, несмотря на наличие необходимых регламентирующих документов, охват вакцинацией детей, родившихся с ОНМТ и ЭНМТ, остается крайне низким [1, 10-13].
На основании изложенного выше целью настоящего исследования явился анализ причин низкого охвата вакцинацией недоношенных детей, родившихся с ОНМТ и ЭНМТ, для разработки персонализированного подхода к тактике его повышения.
Нами был проведен анализ вакцинации недоношенных детей на базе Центра восстановительного лечения (ЦВЛ) для детей, родившихся с ОНМТ и ЭНМТ, на базе ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ».
Для достижения указанной цели дети, родившиеся с ОНМТ и ЭНМТ, были распределены на две группы.
В группу I вошли 207 детей, наблюдавшихся до внедрения вакцинации в работу ЦВЛ. Они были прикреплены к ЦВЛ в 2015 году, анализ охвата вакцинацией проводился до достижения ими 36 месяцев корригированного возраста (до 2018 г). У детей данной группы были оценены сроки начала, объем вакцинации согласно Национальному календарю профилактических прививок, а также были проанализированы медицинские отводы от вакцинации. Вакцинация у этих детей проводилась вне ЦВЛ - в амбулаторных учреждениях по месту прикрепления (либо в других медицинских учреждениях).
В группу II включены 1654 ребенка, которые состояли на учете в ЦВЛ с 2018 по 2021 гг., в период внедрения вакцинации в работу ЦВЛ. У этих детей была возможность пройти вакцинацию в соответствии с Национальным календарем прививок непосредственно на базе ЦВЛ.
В группе I 142 (68,6%) ребенка родились с ОНМТ, 65 (31,4%) - с ЭНМТ. Значимых гендерных различий в данной группе выявлено не было, но при этом преобладали мальчики: 78 (55,1%) мальчиков и 64 (44,85%) девочки с ОНМТ; 37 (56,5%) мальчиков и 28 (43,5%) девочек с ЭНМТ. У всех детей были оценены сроки начала и объем вакцинации при постановке на учет в ЦВЛ и при последующем наблюдении (табл. 1).
Таблица 1.
Сроки начала вакцинации детей группы I согласно Национальному календарю профилактических прививок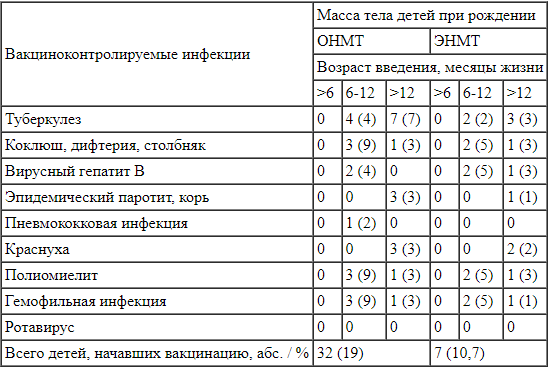 Примечание. n - число детей, начавших вакцинацию в указанном возрасте; (n) - количество полученных вакцин детьми группы I в указанном возрастном интервале.
Примечание. n - число детей, начавших вакцинацию в указанном возрасте; (n) - количество полученных вакцин детьми группы I в указанном возрастном интервале.
Проведенный анализ продемонстрировал, что ни один из 207 недоношенных детей, родившихся с ОНМТ и ЭНМТ, до шестимесячного возраста не был вакцинирован от туберкулеза, дифтерии, столбняка, коклюша, гепатита В, пневмококка, гемофильной инфекции, полиомиелита. Отмечен также низкий охват вакцинацией против перечисленных инфекций и после шести месяцев жизни. Среди детей с ОНМТ в течение первых 12 месяцев жизни вакцинация была начата лишь у 19%, с ЭНМТ - всего у 10,7%. То есть 81% детей группы I до 24 месяцев жизни не были охвачены вакцинацией. Среди них было 110 (77%) детей, родившихся с ОНМТ, и 58 (89%) - с ЭНМТ.
Анализ причин столь низкого охвата вакцинацией показал ведущую роль двух факторов: в 55% случаев - медицинские отводы, обусловленные наличием сопутствующих заболеваний; в 45% - отказ родителей от прививок.
Для оценки общего преморбидного фона и анализа обоснованности имеющихся медицинских отводов нами была проанализирована структура заболеваемости у детей группы I, родившихся с ОНМТ и ЭНМТ, при постановке на учет в ЦВЛ (рис. 1).
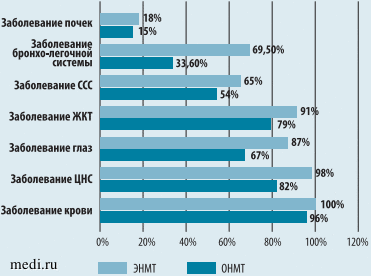 Рис. 1. Структура заболеваемости у детей группы I
Рис. 1. Структура заболеваемости у детей группы I
Как представлено на рисунке 1, частота заболеваемости у детей с ЭНМТ была выше, чем у детей с ОНМТ. При этом у большинства детей, родившихся с ОНМТ и ЭНМТ, имелись заболевания крови (у 96 и 100% соответственно), представленные преимущественно анемиями. У 82% детей с ОНМТ и практически у каждого ребенка с ЭНМТ (98%) встречались болезни нервной системы, которые сопровождались неонатальными судорогами, потребовавшими лечения на постгоспитальном этапе у 10,2% детей с ОНМТ и у 36,2% - с ЭНМТ. Вентрикулоперитонеальное шунтирование в связи с окклюзионной гидроцефалией было выполнено у 4 (6,1%) детей с ЭНМТ. Заболевания глаз диагностированы у 67% детей с ОНМТ и у 91% - с ЭНМТ, в частности у 71% детей выявлена ретинопатия недоношенных с последующим проведением лазеркоагуляций по показаниям. У 33,6% детей с ОНМТ и у 69,5% с ЭНМТ имелась бронхолегочная дисплазия (БЛД). На момент постановки на учет в ЦВЛ у 79 и 91% детей соответственно были диагностированы заболевания органов желудочно-кишечного тракта, которые чаще были представлены функциональными нарушениями. Пищевая аллергия выявлена у 36 (25,5%) детей с ОНМТ и у 25 (39,1%) - с ЭНМТ, дефицит веса - у 9 (13,0%) и 8 (5,1%) соответственно. Патология сердечно-сосудистой системы имела место у 54% детей с ОНМТ и у 65% - с ЭНМТ, у 10 (8,4%) пациентов выявлены врожденные пороки развития (ВПР) сердца с недостаточностью кровообращения.
С учетом выявленной структуры заболеваемости нами был проведен анализ непосредственных причин медицинских отводов от вакцинации, которые зафиксированы в 45% случаев (табл. 2).
Таблица 2.
Причины медицинских отводов от вакцинации у детей группы I
| Причина медицинского отвода | Масса тела при рождении | |
| ЭНМТ n (Абс./%) | ОНМТ n (Абс./%) | |
| Недоношенность | 18 (9) | 4 (2) |
| Заболевания центральной нервной системы (ЦНС), из них: | ||
| Перенесенное ВЖК I-III | 6 (3) | 11 (5,3) |
| Последствия перинатального поражения ЦНС | 3 (1,5) | 6 (3) |
| Эпилепсия в состоянии клинико-медикаментозной ремиссии | 1 (0,5) | - |
| Неонатальные судороги в анамнезе | 7 (3,4) | 13 (6) |
| Всего: | 17 (8) | 30 (15) |
| Дефицит веса | 6 (2,4) | 2 (1) |
| БЛД | 4 (2) | 2 (1) |
| ВПР | 1 (0,5) | 4 (2) |
| Пищевая аллергия | - | 3(1,5) |
| Другие заболевания | - | 2 (1) |
| Всего: | 46 (22) | 47 (23) |
В структуре медицинских отводов ведущее место занимали заболевания ЦНС (23%). Другими причинами медицинских отводов явились: глубокая недоношенность (11%), дефицит веса (3,4%), БЛД (3%), ВПР (2,5%), пищевая аллергия (1,5%), другие заболевания (1%).
Помимо этого, у детей группы I, начавших вакцинацию до 12 месяцев жизни, обращали на себя внимание длительные медицинские отводы после перенесенных острых инфекционных заболеваний, которые нерационально увеличивали интервалы между последующими введениями вакцин, тем самым нарушая график вакцинопрофилактики.
Более детальный анализ показал, что в подавляющем большинстве случаев медицинские отводы не были обоснованы, шли в разрез с существующими нормативными документами, в которых четко прописаны абсолютные противопоказания (табл. 3) [8].
Таблица 3.
Абсолютные противопоказания к проведению вакцинации согласно нормативным документам Минздрава России
| Вакцина | Противопоказания |
| Все вакцины | Сильная реакция или поствакцинальное осложнение на предыдущее введение. Непереносимость компонента вакцины, выражающаяся в тяжелых системных аллергических или анафилактических реакциях |
| Все живые вакцины, в том числе оральная полиомиелитная вакцина, ротавирусная вакцина | Иммунодефицитное состояние (первичное, подтвержденное). Иммуносупрессия, злокачественное новообразование. Инвагинация кишечника в анамнезе, пороки развития желудочно-кишечного тракта (только для ротавирусной вакцины) |
| БЦЖ | Масса тела ребенка при рождении менее 2000 г. Келоидный рубец после предыдущей вакцинации. Генерализованная БЦЖ-инфекция, выявленная у других детей в семье. ВИЧ-инфекция с обнаружением нуклеиновых кислот.\ ВИЧ-инфекция у матери, не получавшей трехэтапную химиопрофилактику |
| АКДС (цельноклеточная) | Прогрессирующее заболевание нервной системы. Афебрильные судороги в анамнезе. Возраст старше 3 лет 11 месяцев 29 дней |
| АаКДС (бесклеточная) | Энцефалопатия неясной этиологии, развившаяся в течение семи дней после предыдущего введения любой коклюшной вакцины. Прогрессирующая энцефалопатия |
| Живая коревая вакцина, живая паротитная вакцина, краснушная вакцина, а также комбинированные ди/тривакцины (корь -паротит / корь - краснуха - паротит) | Анафилактическая реакция на белок перепелиного яйца (кроме краснушной), аминогликозиды. Анафилактическая реакция на белок куриного яйца (кроме краснушной), аминогликозиды |
| Вакцина против вирусного гепатита В | Анафилактическая реакция на пекарские дрожжи |
| Вакцины АДС, АДС-м, АД-м | Постоянных противопоказаний нет |
Согласно Методическим рекомендациям Союза педиатров России (2019), начинать вакцинацию недоношенных детей можно уже на втором этапе выхаживания [9] при достижении ребенком массы тела более 1500-2000 г. и при соответствующем мониторировании жизненно важных функций.
На этом же этапе выхаживания начинается проведение и пассивной сезонной иммунизации недоношенных детей против респираторно-синцитиальной (РВС) инфекции паливизумабом. Продолжение курса паливизумаба проводится амбулаторно в специализированных центрах [15, 16]. При этом важно отметить, что пассивная иммунизация против РСВ не должна влиять на соблюдение основного графика вакцинопрофилактики и может проводиться параллельно с активной иммунизацией, предусмотренной Национальным календарем прививок. Это согласовывается с опытом вакцинации недоношенных детей, включая детей с низкой массой тела, отраженным также и в международных рекомендациях: прививать в соответствии с паспортным возрастом, по обычным схемам в стандартных дозировках [17-19].
Следует отметить, что ни один ребенок из группы I не получал вакцинацию на базе второго этапа выхаживания в стационаре.
После выписки из стационара эти дети в установленном порядке должны были получить вакцинацию в поликлинике по месту прикрепления. Однако наш анализ показал крайне низкий охват (в течение первых 12 месяцев жизни вакцинация была начата лишь у 32 (19%) детей с ОНМТ и всего у 7 (10,7%) детей с ЭНМТ (см. табл. 2).
В этой связи в качестве дополнительного и эффективного ресурса для проведения вакцинопрофилактики детей, родившихся с ОНМТ и ЭНМТ, могут быть задействованы центры восстановительного лечения и катамнестические кабинеты для недоношенных детей, родившихся с ОНМТ и ЭНМТ, созданные на базе многопрофильных стационаров (при их наличии). Это позволяет более тщательно оценить состояние здоровья ребенка с выявлением истинных причин для медицинских отводов к вакцинации с учетом потенциально отягощенного преморбидного фона.
С учетом результатов представленного анализа в нашем центре в 2018 году была впервые внедрена вакцинации недоношенных детей.
Всего за период 2018-2021 гг. вакцинацией было охвачено 1191 (72%) детей, рожденных с ОНМТ и ЭНМТ, из 1654 детей, состоящих на учете в центре. Данные пациенты составили группу II (п = 1654), среди которых 901 (54%) - с ОНМТ и 753 (46%) - с ЭНМТ при рождении. Существенных различий по гендерному признаку в группе II выявлено не было, и отмечалось недостоверное преобладание мальчиков (53%), как и в группе I.
Учитывая, что средний возраст прикрепления к ЦВЛ приходился на 3-4 месяца жизни, то вакцинация в ЦВЛ, соответственно, тоже начиналась в этот период. Следует подчеркнуть, что из указанного количества наблюдаемых только у 14 (0,8%) детей, родившихся с ОНМТ, вакцинация была начата до момента постановки на учет в ЦВЛ. Им была проведена частичная вакцинация (6 детям - от пневмококка, 5 - от ротавирусной инфекции и 3 - от столбняка, коклюша, дифтерии, полиомиелита, вирусного гепатита В и гемофильной инфекции типа b). Указанные показатели еще раз подтверждают крайне низкий охват вакцинацией недоношенных детей и тенденцию к ее отсроченному началу.
Оценка структуры заболеваемости в группе II также продемонстрировала высокую частоту поражения органов нервной, бронхолегочной, сердечно-сосудистой систем и желудочно-кишечного тракта, наиболее выраженную у детей, родившихся с ЭНМТ (рис. 2).
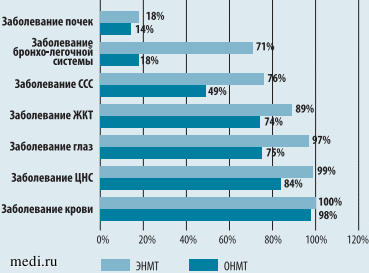 Рис. 2. Структура заболеваемости детей группы II
Рис. 2. Структура заболеваемости детей группы II
Как видно из рисунка 2, структура заболеваемости в группе II существенно не отличалась от таковой в группе I. Также превалировали заболевания крови (98 и 100% соответственно) представленные преимущественно анемиями, болезни нервной системы (84 и 99%) и органов зрения (75 и 97%). Распространенность БЛД среди детей с ОНМТ стала меньше, чем среди пациентов с ЭНМТ (18 и 33,6% соответственно), а среди детей с ЭНМТ практически не изменилась (71 и 69,5%, соответственно) (рис. 1, 3).
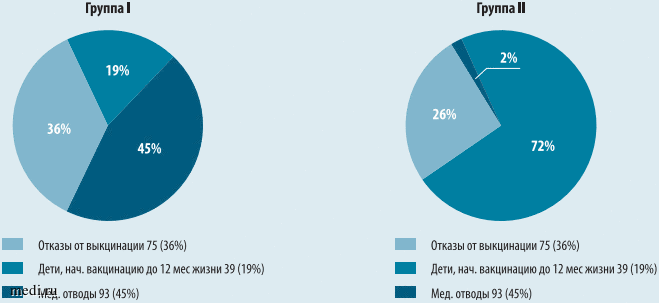 Рис. 3. Доля медицинских отводов в группах I и II
Рис. 3. Доля медицинских отводов в группах I и II
При планировании и проведении вакцинации мы руководствовались принципом максимально персонализированного подхода. Так, перед началом вакцинации обязательным являлся осмотр педиатра и выполнение клинических анализов крови и мочи. Врач-педиатр на первом приеме составлял индивидуальный график прививок, направленный на максимально быстрое восстановление сроков согласно Национальному календарю прививок. При этом им же определялись показания для консультации узких специалистов с последующим выполнением необходимых дополнительных лабораторных и инструментальных исследований с учетом отягощенности преморбидного фона.
Все индивидуальные графики составлялись на основе возможных сроков начала вакцинации (в зависимости от момента постановки на учет в ЦВЛ). При этом следует отметить, что мультидисциплинарный подход позволял минимизировать все возможные риски.
Учитывая большое число детей, перенесших врожденную пневмонию, и детей с формированием БЛД, а также достаточно высокий процент детей с ВПР сердца, вакцинация нами чаще начиналась с введения вакцин против пневмококка и гемофильной инфекции [20, 21]. Такой подход позволяет минимизировать риск развития острых заболеваний дыхательной системы, к которым дети из указанной группы особенно уязвимы.
Если состояние здоровья ребенка позволяет начинать вакцинацию до трехмесячного возраста, целесообразно сначала применять вакцину против ротавирусной инфекции для предупреждения высокого риска тяжелого течения и развития осложнений при данном заболевании [22]. В последующем проводится вакцинация против дифтерии, столбняка, коклюша, полиомиелита и гемофильной инфекции.
Следует отметить, что при ревакцинация против столбняка, коклюша, дифтерии, полиомиелита, пневмококковой, гемофильной инфекции, вакцинации против вирусного гепатита А нам удалось войти в сроки, установленные Национальным календарем прививок, у 879 (53%) детей.
Что касается сезонной вакцинации против гриппа, то она может проводиться у данной группы детей с шестимесячного возраста в установленным порядке перед эпидемическим сезоном.
Таким образом, описанная тактика повышения охвата вакцинацией детей с ОНМТ и ЭНМТ позволила войти в рамки Национального календаря прививок уже к 1,5-2-летнему возрасту детей указанных групп (табл. 4).
Таблица 4.
Сроки начала вакцинации детей группы II от вакциноуправляемых инфекций согласно Национальному календарю профилактических прививок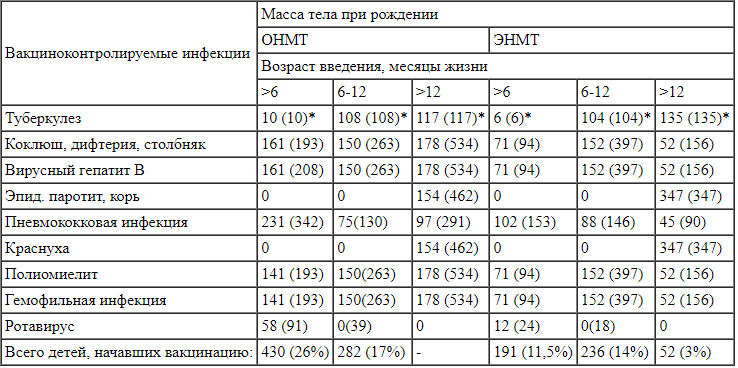 Примечание. * n - число детей, начавших вакцинацию в указанном возрасте; (n) - количество полученных вакцин среди детей подгруппы II в указанном возрастном интервале.
Примечание. * n - число детей, начавших вакцинацию в указанном возрасте; (n) - количество полученных вакцин среди детей подгруппы II в указанном возрастном интервале.
Как видно из таблицы 4, среди детей, родившихся с ОНМТ, 430 (26%) начали вакцинацию в ЦВЛ до 6, еще 282 (17%) - до 12 месяцев жизни. Среди детей, родившихся с ЭНМТ, 191 (11,5%) и 236 (14%) соответственно. Еще 52 (3%) ребенка с ЭНМТ приступили к вакцинации сразу после 12 месяцев жизни, что позволило войти в рамки Национального календаря прививок до двухлетнего возраста.
Следовательно, число детей из группы II, получавших вакцинацию в ЦВЛ, составило 72% (n = 1191), среди которых детей, родившихся с ОНМТ, было 675 (75%), с ЭНМТ - 479 (64%).
При этом медицинские отводы от вакцинации были установлены лишь у 36 (2%) детей и исключительно после заключения невролога при подозрении на эпилепсию и грубые задержки психомоторного развития. Среди этих детей преобладали пациенты, родившиеся с ЭНМТ, - 30 (4%), родившихся с ОНМТ было 6 (0,7%).
Помимо этого были определены временные медицинские отводы кардиологами, гематологами, неврологами и пульмонологами у 245 (15%) детей, которые начали вакцинацию после 6 месяцев жизни (с ЭНМТ - 167, с ОНМТ - 78 детей).
Как известно, одной из распространенных причин низкого охвата вакцинацией детей является отказ родителей. В группе II 427 (26%) родителей отказались от вакцинации детей. Результаты нашего исследования при этом демонстрируют уменьшение частоты отказов родителей от вакцинации в группах I и II практически в 1,5 раза (с 36 до 26%). Это стало возможным также благодаря дополнительному комплексу мероприятий, проводимых в ЦВЛ: индивидуальные беседы специалистов разных направлений с родителями, персонализированный подход и наблюдение за ребенком, комплексная оценка состояния здоровья и рисков, регулярное проведение школ для родителей («Мамина школа», «Недоношенный ребенок», «Инфекционные заболевания у недоношенного ребенка и их профилактика») с особым акцентом на профилактику инфекционных заболеваний.
Данная целенаправленная работа одновременно сопровождалась всесторонней информационной поддержкой. Для этого были разработаны и изданы специальные популярные буклеты и руководства для родителей, в которых были освещены все возможные риски и осложнения у невакцинированного недоношенного ребенка. Для повышения охвата вакцинацией активно использовались также ресурсы социальных сетей, в том числе с предоставлением возможности для родителей в режиме online задавать вопросы как педиатрам, так и узким специалистам. Кроме того, ежегодно, на базе ЦВЛ проводится комплекс мероприятий, приуроченных к международному Дню недоношенного ребенка, где ключевое внимание уделяется вопросам вакцинопрофилактики. Указанный комплекс мероприятий позволил существенно повысить охват вакцинацией недоношенных детей.
Так, у 147 (9%) детей причиной позднего начала вакцинации (после 6 месяцев жизни) являлись отказы родителей. Вместе с тем, в процессе активной работы с родителями стало возможным начать вакцинацию после шестимесячного возраста у всех указанных детей. В итоге в результате комплексных скоординированных действий удалось достичь охвата вакцинацией в объеме 72% (n = 1191). При этом важно отметить, что после 6 месяцев жизни медицинские отводы от вакцинации в исследуемой группе детей были зафиксированы только в 36 (2%) случаев против 45% ранее установленных медицинских отводов (в группе I).
Немаловажным является и тот факт, что ни у одного из вакцинированных детей не было зарегистрировано осложнений, а побочные реакции отмечались лишь у двоих детей после введения комплексной вакцины против дифтерии, столбняка, коклюша. Оба ребенка родились с ОНМТ, у одного из них был зафиксирован подъем температуры до фебрильных цифр (выше 38,5оС), а у другого помимо гипертермии были выявлены фебрильные судороги. Указанные обстоятельства были учтены при дальнейшей вакцинации.
Заключение
Таким образом, результаты нашего исследования доказывают необоснованно низкий охват вакцинацией недоношенных детей при отсутствии соответствующих мероприятий, направленных на ее повышение. Меры должны быть комплексными и объединять усилия врачей и родителей, представителей общественности и средств массовой информации. При этом безусловно приоритетным является персонализированный подход с оценкой массы тела, наличия истинных медицинских отводов с началом вакцинации в максимально ранние декретированные сроки при первичном обращении ребенка в медицинское учреждение.
Использование в педиатрической практике персонализированного подхода позволяет существенно повысить охват вакцинацией с составлением обоснованного индивидуального графика прививок для ребенка, родившегося недоношенным, и в максимально короткое время войти в сроки, установленные Национальным календарем прививок.
Литература
1. Флоринская Е.Б., Кешишян Е.С. Вакцинация недоношенных детей // Российский вестник перинатологии и педиатрии. 2021. Т. 66, № 6. С. 66.
2. Таточенко В.К. Вакцинация недоношенных и маловесных детей // Педиатрическая фармакология. 2013. Т. 10, № 4. С. 30-36.
3. Langkamp D.L., Davis J.P. Increased risk of reported pertussis and hospitalization associated with pertussis in low birth weight children // The Journal of Pediatrics. 1996. Vol. 128. Р. 654-659.
4. Союз педиатров России. Клинические рекомендации по вакцинопрофилактике пневмококковой инфекции у детей. М., 2018.
5. Issues of vaccination in premature infants: an overview / P. Manzoni [et al.] // Italian Journal of Pediatrics. 2015. Vol. 41. A20.
6. Cortese M.M., Parashar U.D. Centers for Disease Control and Prevention (CDC). Prevention of rotavirus gastroenteritis among infants and children: recommendations of the Advisory Committee on Immunization Practices (ACIP) // Morbidity and Mortality Weekly Report. 2009. Vol. 58(RR-2). Р 1-25.
7. О Календаре профилактических прививок. Приложение 4 «Перечень медицинских противопоказаний к проведению профилактических прививок» : приказ Минздрава России от 18 декабря 1997 г. No 375 (ред. от 30.12.1998 г.). М., 1997.
8. Вакцинопрофилактика. Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок : Методические указания МУ 3.3.1.1095-02, утвержденные Главным государственным санитарным врачом Российской Федерации 9 января 2002 г.
9. Иммунопрофилактика инфекционных болезней у недоношенных детей : Методические рекомендации / под ред. А.А. Баранова [и др.]. М. : ПедиатрЪ, 2019. 51 с.
10. Вакцинация недоношенных детей / Е.В. Анциферова [и др.] // Педиатрия. Журнал им. Г.Н. Сперанского. 2020. Т. 99, № 1. С. 111-116.
11. Sisson H. Vaccinating preterm infants: why the delay? // Infant. 2014. Vol. 10, № 3. Р 84-86.
12. Association of Routine Infant Vaccinations with Antibody Levels among Preterm Infants / E.D.M. Rouers [et al.] // Journal of the American Medical Association. 2020. Vol. 324, No. 11. Р 1068-1077.
13. Недоношенные дети: безопасность вакцинации и специфический иммунный ответ / С.М. Харит [и др.] // Эпидемиология и вакцинопрофилактика. 2015. Т. 14, № 4. С. 61-66.
14. Оценка безопасности применения пентавакцины у недоношенных детей: опыт центра семейной вакцинопрофилактики / Д.А. Новикова [и др.] // Вопросы современной педиатрии. 2015. Т 14, № 3. С. 392-395.
15. Клинические рекомендации по иммунопрофилактике респираторно-синцитиальной вирусной инфекции у детей. М. : Союз педиатров России, 2016.
16. О мероприятиях, направленных на профилактику респираторно-синцитиальной вирусной инфекции у детей в городе Москве за счет средств бюджета города Москвы : Распоряжение департамента здравоохранения г. Москвы от 26.08.2022. М., 2022.
17. Update on vaccination of preterm infants: a systematic review about safety and efficacy/effectiveness. Proposal for a position statement by Italian Society of Pediatric Allergology and Immunology jointly with the Italian Society of Neonatology / E. Chiappini [et al.] // Expert Review of Vaccines. 2019. Vol. 18, No. 5. С. 523-545.
18. D'Angio C. Active immunization of premature and low birthweight infants: A review of immunogenicity, efficacy, and tolerability // Paediatr Drugs. 2007. Vol. 9, No. 1. Р 17-32.
19. Baxter D. Vaccine responsiveness in premature infants. Human Vaccines and Immunotherapeutics. 2010. Vol. 6, No. 6. Р. 506-511.
20. PUNS Study Group. Schedules for Pneumococcal Vaccination of Preterm Infants: An RCT / A. Kent [et al.] // Pediatrics. 2016. Vol. 138, No. 3. Р e20153945.
21. 13-valent pneumococcal conjugate vaccine (PCV13) in preterm versus term infants / F Martinon-Torres [et al.] // Pediatrics. 2015. Vol. 135, No. 4. Р 876-886.
22. Клинические рекомендации по вакцинопрофилактике ротавирусной инфекции у детей. М.: Союз педиатров России, 2017.
Комментарии
ПРАКТИКА ПЕДИАТРА

