Обмен кальция и фосфатов в норме и при патологии у детей
СтатьиЭ.А. Юрьева1, д-р мед. наук, профессор, И.М. Османов2, 3, д-р мед. наук, профессор, Е.С. Воздвиженская1, канд. биол. наук, Е.И. Шабельникова1, канд. мед. наук
1 Научно-исследовательский клинический институт педиатрии им. акад. Ю.Е. Вельтищева ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России, г. Москва
2 ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
3 ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова Минздрава России», г. Москва
Опубликовано в журнале:
«Практика педиатра» № 4, 2021, стр. 24-30
Ключевые слова: кальций, фосфаты, обмен, патофизиология, диагностика
Keywords: calcium, phosphates, metabolism, pathophysiology, diagnostics
Резюме. Проанализированы современные представления о физиологии и основных показателях, отражающих наличие нарушений кальций-фосфорного обмена. Эти нарушения несут риск развития различных болезней, включая патологию почек, костей и кальцификацию мягких тканей. Описано действие кальция и фосфора в клетках и внеклеточной жидкости, рецепторный аппарат компонентов, регулирующих обмен этих электролитов, особенности гормональной регуляции, структурной и сигнальной функции кальция и фосфатов. Перечислены негормональные препараты, применяемые (наряду с гормональными) для оптимальной щадящей коррекции нарушений кальций-фосфорного обмена.
Summary. The modern concepts of physiology and the main indicators reflecting the presence of disorders of calcium-phosphorus metabolism are analyzed. These disorders carry the risk of developing various diseases, including kidney pathology, bone and soft tissue calcification. The effect of calcium and phosphorus in cells and extracellular fluid, the receptor apparatus of the components regulating the exchange of these electrolytes, the features of hormonal regulation, the structural and signaling functions of calcium and phosphates are described. The non-hormonal drugs used (along with hormonal ones) for optimal gentle correction of calcium-phosphorus metabolism disorders are listed.
Для цитирования: Обмен кальция и фосфатов в норме и при патологии у детей / Э.А. Юрьева, И.М. Османов, Е.С. Воздвиженская, Е.И. Шабельникова // Практика педиатра. 2021. № 4. С. 24-30.
For citation: Yuryeva E.A., Osmanov I.M., Vozdvizhenskaya E.S., Shabelnikova E.I. Calcium and phosphate metabolism in normal and pathological conditions in children. Pediatrician's Practice 2021(4)24-30. (In Russ.)
Наиболее интенсивно обмен кальция и фосфатов, его нарушения и способы диагностики этих нарушений изучались в конце XX и начале XXI в. Кальций в организме человека составляет примерно 1 кг, из которого 99% находится в составе скелета в виде гидроксиапатита, а 1% - во внеклеточном матриксе и в клетках мягких тканей. В клетках кальций в виде гидроксиапатитных растворимых запасов тщательно изолирован от цитозоля (митохондриальный запас кальция). Сывороточная концентрация кальция составляет 2,5 ммоль/л, а цитозольная в 1000 раз меньше, что критически важно для функций клетки. Кальций выполняет ряд важнейших функций в организме. Кальций, содержащийся в костях, обеспечивает структуру и прочность скелета, а имеющийся в экстрацеллюлярной жидкости и в цитозоле - необходим для поддержания многочисленных биохимических процессов. Концентрация кальция в обоих случаях поддерживается на строго определенном уровне [1]. Кроме того, сохранение трансмембранного соотношения Са/Mg, как и К/Nа, важно для контроля клеточной возбудимости и регуляции многих процессов внутриклеточного метаболизма. Активные ткани - нервная, печеночная, мышечная - имеют более высокое соотношение Са/Mg по сравнению с кожей и эритроцитами. В более активных тканях концентрация фосфатов выше, чем в неактивных: в активных тканях фосфор интенсивнее включается в клеточный энергетический метаболизм в виде фосфорных эфиров. Во взрослом организме содержится около 600 г фосфора, из которых 85% приходится на скелет, а примерно 15% находится в клетках (в виде фосфорных эфиров - АТФ) и составляет 104 ионов. Внеклеточное содержание в 2 раза выше и поддерживается менее строго, чем концентрация кальция и магния. Магний имеет большое значение для обмена Са/Р; в организме человека содержится 25 г магния. Две трети этого количества находятся в составе скелета и 1/3 -в мягких тканях. Магний в костях локализуется на кристаллической поверхности. В клетках мягких тканей магний играет важную роль как кофактор многих ферментативных реакций и нейромышечной возбудимости [2, 3].
Метаболизм, кишечная адсорбция и почечная экскреция кальция и фосфора определяют гомеостазис этих ионов в организме. В сыворотке кальций представлен в трех фракциях: ионизированный (около 30%), белково-связанный (около 40%) и кальций в комплексе в основном с цитратами и фосфатными ионами (около 19%). Ультрафильтруется ионизированный и комплексный кальций. Примерно 90% белково-связанного кальция - с альбумином, остальная часть - с глобулинами, поэтому изменения концентрации альбумина могут оказывать большое влияние на концентрацию кальция в сыворотке. Связывание кальция с карбоксильной группой (СООН) альбумина в высокой степени зависит от рН крови. При ацидозе эта связь ослабевает, а при алкалозе - усиливается с соответствующим снижением уровня ионизированного кальция сыворотки при сохранении количества общего кальция. Концентрация ионизированного кальция тщательно поддерживается на оптимальном уровне (50% от общего) под действием паратиреоидного гормона (ПТГ) и 1,25(ОН)D3 (гормональная форма витамина D). Физиологическая функция ионизированного кальция включает: 1) участие в качестве кофактора в процессе коагуляции (факторы VII, IX, Х и протромбин); 2) поддержание оптимального количества ионов для минерализации скелета; 3) участие в стабилизации плазматических мембран путем связывания фосфолипидов в липидном бислое и регуляции проницаемости мембран для натрия. Снижение уровня ионизированного кальция в сыворотке повышает проницаемость для натрия и ослабляет активность всех возбудимых тканей, а повышение уровня ионизированного кальция сопровождается обратным эффектом. Фосфаты в сыворотке также содержатся в белково-связанном состоянии и только 10% - в виде комплексов с Na, Ca, Mg. Фильтруется 90% комплексов фосфатов (кроме белково-связанных). Концентрация фосфатов в сыворотке довольно широко меняется в зависимости от возраста, пола, диеты, рН и различных гормонов. Адекватное содержание фосфатов в сыворотке необходимо для минерализации костной ткани [4].
Внутриклеточная жидкость содержит кальций (около 1-5%) в основном в связанном состоянии с кальмодулином (тропонином), в то время как митохондрии и микросомы содержат 90-99% внутриклеточного кальция. Выход кальция из этих органелл (кальциевый сигнал) тщательно контролируется, является энергозависимым и служит специфическим физиологическим функциям данной клетки, обеспечивая возбуждение и сокращение мышц (запасенный в саркоплазматическом ретикулуме кальций в мышечных клетках) и другие эффекты. Кальциевый сигнал в немышечных клетках обеспечивает выход секреторных продуктов - инсулина, альдостерона. Таким образом, кальций является вторичным посредником функций клеток (наряду с циклическим АМФ) [5].
Транспорт фосфатов в клетку - процесс пассивный, в основном связанный с транспортом кальция, и внутри клеток он происходит главным образом в митохондриях, а также в цитозоле в виде органических эфиров (АТФ, АДФ, АМФ).
При росте детей минеральный баланс остается положительным, однако с возрастом, иммобилизацией такой баланс становится нулевым и даже отрицательным (снижается адсорбция, повышается экскреция минералов). При этом тубулярный аппарат почек играет доминирующую роль в поддержании минерального гомеостазиса.
Концентрацию магния в сыворотке в основном обеспечивает реабсорбция в почках (96% профильтровавшегося в первичную мочу) и кишечная адсорбция (усваивается 30% пищевого магния). Ежедневная потребность в кальции составляет 300-400 мг, а в магнии - 190-700 мг. Кишечная адсорбция кальция, фосфора и магния обеспечивает потребности организма в этих минералах для увеличения массы тела, минерализации костей у детей и для обмена и ремоделирования костей у взрослых. Адсорбция кальция, фосфора и магния происходит в двенадцатиперстной и тощей кишке, зависит от их наличия в пище и от присутствия в сыворотке витамина D3 [6]. В таблице представлены факторы риска снижения или повышения кишечной адсорбции кальция.
Таблица.
Факторы риска снижения/повышения кишечной адсорбции кальция [7]
| Снижение | Повышение |
| Дефицит 1,25(ОН)D3 | Повышение уровня 1,25(ОН)D3 |
| Витамин-D-дефицитный рахит, I тип (дефицит 25-ОН-D-1-а-гидроксилазы) | Гиперпаратиреоз |
| 1,25(ОН) D3-резистентный рахит | Cаркоидоз и другие внепочечные гранулемы |
| Хроническая почечная болезнь |
Идиопатический синтез 1,25(ОН)D3, при котором может наблюдаться гиперкальциурия, повышение чувствительности к 1,25(ОН)D3 или усиление адсорбции по витамин-D-зависимому механизму |
| Гипопаратиреоз | |
| Витамин-D3-зависимый рахит, тип II | |
| Отсутствие или аномальный рецептор к 1,25(ОН)D3 или к другим гормональным рецепторам | |
| Кишечные болезни |
Снижение адсорбции магния встречается при мальабсорбции кишечника или при злоупотреблении слабительными. Адсорбция фосфатов в кишечнике зависит от их содержания в диете (60-80% адсорбируется), снижается при дефиците витамина D. Повышенная адсорбция фосфатов в кишечнике является мощным фактором развития вторичного гиперпаратиреоза (ГПТ), подобно ситуации со снижением уровня кальция в сыворотке. Агентами, снижающими адсорбцию фосфатов в кишечнике, являются алюминий и кальций, образующие с фосфором нерастворимые соли.
Изменение почечной экскреции минералов характерно для различных болезней, включая патологию костного обмена и нефролитиаз, и используется для диагностики данных заболеваний. Для исключения возможных потерь суточной мочи при ее сборе экскрецию минералов за сутки предлагается определять по соотношению количества минерала к суточной экскреции креатинина как более устойчивого показателя, независимого от количества пищи, а только от количества мышечной ткани, пола, возраста, веса пациента [5]. Мочевая экскреция кальция оценивается также в соотношении с уровнем анионов, повышение экскреции которых может быть фактором высокого риска образования мочевых конкрементов (оксалатов, фосфатов, цитратов, сульфатов). В норме из профильтровавшегося кальция (около 10 г) 98% реабсорбируется и только 2% выделяется с мочой (от 40 мг (1 ммоль) до 300 мг (7,5 ммоль) в зависимости от диеты). При заболеваниях (вторичном гиперпаратиреозе и др.) экскреция кальция может увеличиваться до 20 ммоль. Основная часть кальция реабсорбируется в проксимальных канальцах при участии Са/Mg-АТФазы, а другая часть реабсорбируется в дистальных канальцах и зависит от активности паратгормона и изменений рН мочи. При ацидозе реабсорбция кальция в дистальных канальцах значительно снижается. Повышение экскреции кальция может происходить и под действием диуретиков на толстый сегмент восходящей части петли Генле (фуросемид повышает, гипотиазид снижает). При повышении содержания натрия в пище снижается реабсорбция и увеличивается экскреция кальция из-за конкуренции за транспортные системы. Так же действует повышение потребления белков с пищей (сульфаты). Выделение больших количеств кальция с мочой является высоким риском образования кристаллов в ткани почек и в просвете канальцев (нефрокальциноз, нефролитиаз) [7, 8].
Магний в основном реабсорбируется в проксимальных канальцах и петле Генле. Суточная потребность составляет 300-400 мг, из которых 40% адсорбируется в кишечнике. Экскретируется примерно 5% из профильтровавшегося - 7-10 мг/сут [6].
Фосфаты в основном реабсорбируются в проксимальных канальцах и немного - в дистальных, экскретируется 1,8-7,8 мг в день (19-32 ммоль). Потребность в фосфатах - 1,3 г в сутки, адсорбируется 60% поступившего с пищей количества. Паратгормон всегда снижает реабсорбцию фосфатов. Увеличение содержания фосфатов в сыворотке обусловлено прямой стимуляцией обмена в кости (и резорбцией) и выхода из нее не только кальция, но и фосфатов, а также за счет стимуляции адсорбции в кишечнике (под действием ПТГ, 1,25(OH)D3). Гиперфосфатемия контролируется за счет ослабления реабсорбции в почках. Само по себе повышение уровня фосфатов в сыворотке стимулирует секрецию ПТГ независимо от кальция и 1,25(OH)D3. В настоящее время известны дополнительные регуляторы обмена фосфатов - фактор роста фибробластов 23 (FGF23) и белок Klotho (кофактор рецептора), действующие в ответ на фосфатемию и стимуляцию 1,25(ОН)Dз [9, 10].
Пептид обладает фосфатурическим действием (как ПТГ), обусловливая снижение содержания фосфатов в сыворотке. FGF23 реализует свой эффект через сложный рецептор, состоящий из собственно FGFR-рецептора и корецептора Klotho, трансмембранного белка (130 кДа) - бета-глюкозидазы. Этот белок способен объединять FGFR и С-терминал FGF23, что обеспечивает концентрацию FGFR-рецептора, делая его высокоспецифичным. При генетически обусловленном отсутствии Klotho в организме сохраняется высокое содержание в крови фосфатов и кальция, несмотря на достаточное количество 1,25(OH)D3 [11]. Рецептор и корецептор фактора роста фибробластов секретируются главным образом в почках и паращитовидной железе - двух наиболее важных органах, участвующих в регуляции реабсорбции фосфатов. Сочетанное действие рецептора и кофактора на почку заключается в регуляции реабсорбции фосфатов и в снижении содержания их в крови путем ослабления активности Na/P-котранспортера (NPT2a и NPT2c). FGF23 угнетает также активность 1-а-гидроксилазы и увеличивает активность 24-ОН-гидроксилазы, образующей негормональную форму витамина D (24,25D3). В результате снижается кишечная экспрессия NPT2. Кроме того, FGF23 снижает секрецию ПТГ посредством стимуляции рецепторов. Высокофосфатная диета и 1,25(OH)D3 стимулируют синтез FGF23, а ограничение потребления фосфатов с пищей снижает его синтез. В свою очередь, 1,25(OH)D3 стимулирует экспрессию гена Klotho. Фосфаты могут накапливаться в крови при снижении его почечной экскреции (хронической почечной недостаточности). В таких случаях хороший эффект оказывает ограничение количества фосфатов в рационе питания (задержка прогрессирования вторичного гиперпаратиреоза [12, 13].
Дефицит 1,25(OH)D3 и активация ренин-ангиотензинной системы формируют структурную перестройку паращитовидной железы и Klotho в почке, в связи с чем важно обеспечить блокаду этой системы ингибиторами АПФ и поддержание эффективного статуса 1,25(OH)D3 для профилактики и лечения нарушений кальций-фосфорного обмена [14].
Гормональная регуляция кальций-фосфорного обмена довольно хорошо изучена. Все три гормона, регулирующих этот обмен (ПТГ, 1,25(OH)D3 и кальцитонин) функционируют в тесном взаимодействии, влияют как на синтез, так и на активность друг друга в зависимости от потребностей организма.
Паратгормон в ответ на изменения концентрации сывороточного кальция обеспечивает интегральную деятельность тубулярной реабсорбции кальция, резорбцию костей и 1,25(ОН)D3-зависимую адсорбцию кальция в тонком кишечнике. Именно дистальная тубулярная реабсорбция и остеокласт-ная резорбция кости отвечают за контроль кальциевого гомеостазиса [13].
Паратгормон обеспечивает реабсорбцию кальция в дистальных канальцах почек, повышает мобилизацию кальция в костях, активирует синтез 1,25(OH)D3 в проксимальных канальцах почек и повышает адсорбцию кальция в кишечнике. Одновременно паратгормон снижает реабсорбцию фосфатов в проксимальных канальцах почек. Само по себе снижение уровня фосфатов в сыворотке крови сопровождается усилением адсорбции кальция в кишечнике. Изменение сывороточной концентрации фосфатов чаще всего взаимосвязано с сывороточным кальцием, но изменение содержания фосфатов в сыворотке может быть и независимым от кальция и паратгормона (повышение при гипопаратиреозе и снижение при гипофосфатемическом рахите). Хроническая гиперфосфатемия является либо результатом снижения почечной экскреции при хронической почечной недостаточности, либо следствием гипопаратиреоза. Хроническая гипофосфатемия ассоциируется с семейным гипофосфатемическим рахитом или с первичным ГПТ и сочетается с болезнью костей. В итоге нормализация содержания кальция в сыворотке после мобилизации его из костей и увеличения адсорбции в кишечнике приводит к снижению экскреции фосфатов (нормализации реабсорбции) и нормализации их концентрации в сыворотке без дополнительного изменения уровня сывороточного кальция [11].
Помимо кальция и фосфора в крови, секрецию ПТГ повышают магний, алюминий и ряд гормонов (глюкагон, секретин, кортизол, кальцитонин), гистамин и другие агенты. Повышение уровня ПТГ в сыворотке крови происходит при гемодиализе под влиянием препаратов алюминия, который связывает фосфаты (контроль гиперфосфатемии). Активный ПТГ (N-терминали) в норме быстро исчезает из кровотока путем его инактивации в почках, печени, макрофагах, куп-феровских клетках, а также в неактивном виде (С-тер-минали) выводится почками. Но частично он остается циркулировать. При снижении уровня кальция в сыворотке под действием ПТГ происходит модуляция активности специфических клеток в костях и почках: 1) стимуляция выхода кальция и фосфора из костей; 2) стимуляция реабсорбции кальция (на 10-70%) и подавление реабсорбции фосфатов в почечных канальцах; 3) стимуляция синтеза 1,25(OH)D3 в почках (активация 1-ОН-гидроксилазы); 4) одновременное усиление адсорбции кальция и фосфора в кишечнике. В результате усиливается синтез коллагена во внеклеточном матриксе, повышается уровень сывороточного кальция и снижается уровень фосфатов в сыворотке. Задержка ПТГ в крови обусловливает избыточный выход Са/Р с поверхности костей и резорбцию. В клетке ПТГ действует через вторичный посредник - циклический АМФ, содержание которого повышается в моче при ГПТ, а при псевдогипопаратиреозе, наоборот, пациент не отвечает повышением уровня цАМФ в моче на введение ПТГ: нет увеличения содержания кальция в сыворотке и фосфора в моче, а также прироста цАМФ в моче из-за потери рецептора к ПТГ.
Витамин D выполняет разные функции в организме человека. Основная часть 1-ги-дроксилазы, преобразующей 24(OH)D3 в гормональную форму витамина D и располагающейся в митохондриях клеток проксимальных канальцев, активируется паратгормоном. Предшествующая форма витамина D - 25(OH)D3 - поступает либо с пищей, либо из кожи, где образуется под действием УФ-лучей. Кроме гормональной формы витамина D, в митохондриях клеток эпителия проксимальных канальцев образуется собственно витамин D - 24,25(OH)D3 под действием 24-гидроксилазы в небольших количествах при активации ее повышенным количеством 1,25(OH)D3 [13].
Определено, что функцию дополнительной регуляции кальций-фосфорного обмена выполняют 1,25(ОН)D3-рецепторы (VDR), которые выявлены более чем в 25 тканях организма (в основном в почках, костях, мышцах, печени, нервной, мозговой ткани, тимусе, паращитовидной железе и др.). Напротив, 24,25(OH)D3 малоэффективен как регулятор кальций-фосфорного обмена, а действует более как эндокринный регулятор синтеза эстрогенов, гормона роста, пролактина, инсулина и имеет рецепторы в хондроцитах и паращитовидной железе, а также в небольших количествах - в костях. Синтез 24,25(OH)D3 не зависит от ПТГ. Для обеспечения биологического эффекта 1,25(OH)D3 использует путь сигнальной трансдукции - как геномный, так и негеномный: 1) ядерный, цитозольный рецепторы обеспечивают активацию генома - образование нового белка (кальбидин D, тубулин); 2) взаимодействие с мембранным рецептором, обеспечивающим активацию вольтаж-зависимых кальциевых каналов и повышение уровня внутриклеточного кальция. Oтмечается чрезвычайное разнообразие биологической активности 1,25(OH)D3. Помимо негеномного действия на кальций-фосфорный обмен в кишечнике, в костях (переход промоноцитов в моноциты, остеокласты), в почках, на рост и дифференциацию различных гематопоэтических клеток в костном мозге (в частности, иммунокомпетентных), он участвует в функционировании иммунной системы [1, 14] и эпидермиса, в частности посредством селективных генов. В разных тканях витамин D действует путем связывания с VDR, стероидом ядерного рецептора и внутриклеточным фактором транскрипции. Регуляция экспрессии VDR является одним из механизмов реакции на кальцитриол, так что полиморфизм этого рецептора влияет на эффективность кальцитриола. Oписано снижение уровня VDR при ряде болезней [15, 16].
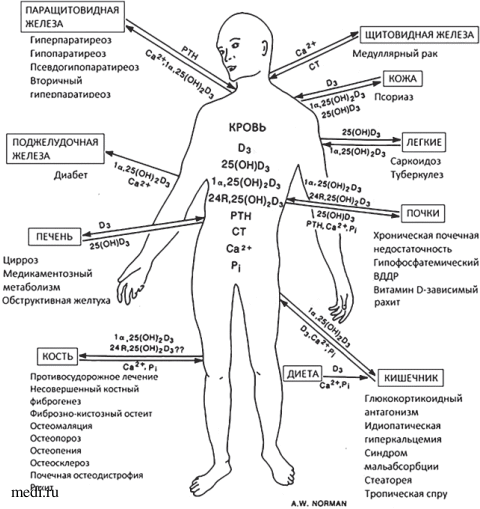 Схема болезней человека, имеющих отношение к функциям 1,25(OH)D3 и витамин-D-эндокринной системе [17]
Схема болезней человека, имеющих отношение к функциям 1,25(OH)D3 и витамин-D-эндокринной системе [17] Клинические проявления болезней могут быть обусловлены нарушением обмена витамина D у родителей, снижением образования 1,25(OH)D3 с изменением действия на органы-мишени, нарушением взаимодействия обеих форм витамина D с другими кальциемическими гормонами [17].
Кальцитонин - пептидный гормон из 32 аминокислот, который секретируется в клетках щитовидной железы, ингибирует остеокластную резорбцию кости и снижает повышенную концентрацию кальция в крови. Используется как лекарственный препарат при остеопорозе, болезни Педжета, онкогенной гиперкальциемии. Секреция кальцитонина контролируется содержанием кальция в крови, зависит от пола и возраста: у мужчин кальцитонин в крови выше, чем у женщин, а с возрастом секреция кальцитонина снижается. Содержание кальцитонина в крови может быть маркером медуллярной карциномы щитовидной железы. Метаболизм кальцитонина происходит в почках в течение нескольких минут. Наиболее активный кальцитонин содержится в организме немлекопитающих: лекарственную форму получают из лосося. Источником кальцитонина могут быть питуитарные и нейроэндокринные клетки, особенно при опухолях. Кроме того, кальцитонин подавляет активность остеоцитов и стимулирует активность остеобластов, оказывает анальгезирующее действие. Кальцитонин действует также как противовоспалительное средство, способствует ускорению срастания переломов и заживлению ран, улучшает глюкозотолерантность. Повышение уровня кальцитонина в кровотоке может быть обусловлено не только медуллярной карциномой щитовидной железы, но и болезнями почек (хронической почечной недостаточностью), остеодистрофией (снижает деградацию), гиперкальциемией в связи с повышением адсорбции кальция в кишечнике. Высокие концентрации кальцитонина в крови сочетаются с гиповолемией и гипофосфатемией. Возможно, кальцитонин действует как нейротрансмиттер, так как найдены рецепторы к кальцитонину в центральной нервной системе, оказывает урикозурическое и гипотензивное действие через цАМФ и кальциевые каналы. Клиническое использование назальной формы кальцитонина значительно расширяет возможности терапии [1].
Для коррекции нарушений кальций-фосфорного обмена предлагается ограничивать поступление фосфатов с пищей начиная с самых ранних стадий хронической болезни почек. При этом мониторинг должен включать не только исследование уровня ультрагемофильтрации, ПТГ, белка, фосфатов, кальция (как факторов, непосредственно связанных с механизмами регуляции обмена фосфатов), но и определение почечной экскреции этих анионов. Последнее в настоящее время является единственным реальным маркером, позволяющим оценивать эффективность терапии, риск прогрессирования вторичного ГПТ и функцию активации FGF23 на ранних стадиях хронической болезни почек в рутинной клинической практике [11, 12].
В связи с наличием свидетельств о роли коллагеназ, TGFa, рецепторов фактора роста эндотелия, Klotho, кальцитриола в активации ренин-ангиотензинной системы подчеркивается важность эффективной блокады ренин-ангиотензинной системы и поддержания достаточного синтеза кальцитриола в профилактике нарушений обмена Са/Р и вторичного ГПТ (необходимо назначать в комплексе лечения ингибиторы ангиотензин-превращающего фермента (энап и др.) и проводить коррекцию дефицита 1,25(ОН)D3). Комбинация ограничения потребления фосфатов, назначение агентов, снижающих адсорбцию фосфатов, блокаторов ренин-ангиотензин-ной системы и поддержание нормального статуса 1,25(ОН)D3 способствует эффекту в отношении профилактики и лечения нарушений кальций-фосфорного обмена на всех стадиях хронической болезни почек и вторичного ГПТ. Помимо этих мероприятий в большинстве случаев терапевтический эффект дополняется активаторами Са-чувствительных рецепторов (CaSR) для снижения риска кальцификации мягких тканей и резорбции кости, а также для воздействия на разные молекулярные механизмы кальций-фосфорного обмена и для предупреждения возможных неблагоприятных воздействий.
В качестве агентов, снижающих адсорбцию фосфатов, используются карбонаты, ацетаты, кетоглютараты кальция. Для повышения усвоения кальция используются кальцимиметики, повышающие активность Са-чувствительных рецепторов (СаSR) и действующие не хуже 1,25(ОН)D3, но без риска кальцификации мягких тканей (при передозировке). К кальцимиметикам относятся органические и неорганические поликатионы, стимулирующие СаSR, связывающиеся с его внешним доменом: альфа-аминокислоты и фенилалкиламины, алостерические модуляторы СаSR, повышающие чувствительность к кальцию и препятствующие избыточной секреции паратгормона в ПЩЖ, снижающие содержание Са/Р в крови. К таким препаратам относятся: сенсипар, милепар, цинакальцет гидрохлорид и др. (внутрь по 1 г в день) [18]. Имеются сведения об успешном использовании активаторов рецепторов витамина D в качестве лечебных средств при нарушении чувствительности этого рецептора, в частности перикальцитриола, доксекальцитриола и др. [15]. Хороший лечебный и профилактический эффект при нарушении кальций-фосфорного обмена в организме оказывают бисфосфонаты - синтетические аналоги естественных регуляторов обмена кальция (неорганических пирофосфатов). К этому классу препаратов относятся этидронат, фозамакс, клодронат, бонефос, памидронат, отечественный ксидифон и др. [19, 20].
Таким образом, в систему регулирования обмена кальция и фосфатов в организме включены три органа-мишени (кости, почки, кишечник), а также три эндокринные системы с взаимозависимыми функциями, тщательно регулирующие обмен и гомеостазис кальция и фосфатов в организме (паратгормон, гормональная форма витамина D - 1,25(QH)D3 и кальцитонин). Получены новые данные о патогенетической роли нарушения функции рецепторов кальция, витамина D и регуляторов обмена фосфатов (FGF23 и Klotho). Для диагностики нарушений фосфорно-кальциевого обмена у детей при патологии необходимо определять не только концентрацию в крови и экскрецию с мочой этих электролитов и регулирующих их обмен гормонов, но и уровень гломерулярной фильтрации, протеинурии, экскреции цитратов, метаболитов коллагена и др. Подчеркивается значение комплексных мер для коррекции нарушений кальций-фосфорного обмена (помимо гормональной терапии), диетических мероприятий, а также назначения негормональных препаратов, активирующих чувствительность клеточных рецепторов регуляторов кальций-фосфорного обмена и синтетических регуляторов обмена кальция - бисфосфонатов. Показано, что такие препараты эффективно предупреждают возможные неблагоприятные воздействия гормональной терапии.
Литература
1. Moe S.M. Disorders involving calcium, phosphorus and magnesium // Primary Care. 2008. Vol. 35, No. 2. P 215.
2. Fleisch H. Bisphosphonates in bone disease. London: Academic Press, 2000. P 16-26.
3. Felsenfeld A.J., Levine B.S., Rodriguez M. Pathophysiology of calcium, phosphorus, and magnesium dysregulation in chronic kidney disease // Seminars in Dialysis. 2015. Vol. 28. P 564-577.
4. Goyal R., Jialal I. Hyperphosphatemia. In: StatPearls. Treasure Island (FL): StatPearls Publishing, 2021.
5. Association of mineral metabolism biomarkers with chronic kidney disease in Chinese adults / J. Li [et al.] // Clinical and Experimental Nephrology. 2021. Mar 16.
6. The relationship between magnesium levels and mortality in the respiratory intensive care unit / M.O. Cirik [et al.] // Medicine (Baltimore). 2020. Vol. 99. e23290.
7. Lеmann J. Intestinal absorption of Ca, Mg, and P In: Primer on metabolic bone disorders and disorders of mineral metabolism. Raven Press, 1993. P. 46-50.
8. Omata M., Fukagawa M., Kakuta T. Vascular calcification -pathological mechanism and clinical application. Vascular calcification in chronic kidney disease-mineral and bone disorder (CKD-MBD) // Clinical Calcium. 2015. Vol. 25. P 645-653.
9. Reduced renal a-Klotho expression in CKD patients and its effect on renal phosphate handling and vitamin D metabolism / J.R. Stubbs [et al.] // Journal of Bone and Mineral Research. 2012. Vol. 27. P. 38-46.
10. Reduced renal a-Klotho expression in CKD patients and its effect on renal phosphate handling and vitamin D metabolism / H. Sakan [et al.] // PLoS One. 2014. Vol. 9. e86301.
11. Добронравов В.А. Современный взгляд на патофизиологию вторичного гиперпаратиреоза: роль фактора роста фибробластов 23 и Klotho // Нефрология 2011. Т. 15, № 4. С. 11-20.
12. High-phosphorus diets reduce aortic lesions and cardiomyocyte size and modify lipid metabolism in Ldl receptor knockout mice / S.M. Grundmann [et al.] // Scientific Reports. 2020. Vol. 10. P. 20748.
13. Correlation between parathyroid hormone levels with urinary magnesium excretion in patients with non-dialysis dependent chronic kidney disease / R.S. Carneiro Dias [et al.] // Journal of Nephrology and Renovascular Disease. 2020. Vol. 13. P 341-348.
14. Lorenzo Sellares V, Torregrosa V Changes in mineral metabolism in stage 3, 4, and 5 chronic kidney disease (not on dialysis) // Nefrologia. 2008. Vol. 28, Suppl 3. P 67-78.
15. Особенность содержания VDR в миометрии у пациентов с эклампсией / Э.Н. Васильева [и др.] // Современные проблемы науки и образования. 2015. № 5ю С. 10-5.
16. Земченков А.Ю., Герасимчук Р.П. Активаторы рецепторов витамина D и сосудистая кальцификация // Нефрология и диализ. 2009. Т. 11, № 4. С. 276-280.
17. Norman A.W, Roth J., Orcci L. The vitamin D endocrine system: steroid metabolism, hormone receptors, and biological response (calcium binding proteins) // Endocrine Reviews. 1982. Vol. 3. P 331-366.
18. Ростомян Л.Г., Рожинская Л.Я., Егжатян Л.М. Кальцимиметики - новый класс препаратов для лечения гиперпаратиреоза // Остеопороз и остеопатии. 2008. № 2. С. 29-37.
19. Вельтищев Ю.Е., Юрьева Э.А. Регуляция фосфорно-кальциевого обмена в норме и при патологии. Рига: РМИ, 1987. С. 67-62.
20. Матковская Т.А., Попов К.И., Юрьева Э.А. Бисфосфонаты. Свойство, строение, применение в медицине. М.: Химия, 2001. 224 c.
Комментарии
ПРАКТИКА ПЕДИАТРА

