Опыт проведения пассивной иммунизации против РСВ-инфекции у глубоконедоношенных детей
СтатьиА.К. Миронова, канд. мед. наук, И.М. Османов, д-р мед. наук, профессор, ГБУЗ «Детская городская клиническая больница им. З.А. Башляевой Департамента здравоохранения г. Москвы»
Опубликовано в журнале:
«Практика педиатра» № 4, 2021, стр. 31-36
Ключевые слова: респираторно-синцитиальная вирусная инфекция, пассивная иммунизация, паливизумаб, глубоконедоношенные дети, дети с очень низкой и экстремально низкой массой тела
Keywords: respiratory syncytial viral infection, passive immunization, Palivizumab, deeply premature infants, children born extremely preterm
Резюме. В статье представлен обзор литературы и собственные данные, полученные в результате десятилетнего проведения пассивной иммунизации детей из групп риска развития тяжелых форм инфекций нижних дыхательных путей, вызванных респираторно-синцитиальным вирусом. Продемонстрирована эффективность и хорошая переносимость препарата паливизумаб. В группе глубоконедоношенных детей, прошедших полный курс пассивной иммунизации против этой инфекции препаратом паливизумаб, респираторно-синцитиальный вирус не участвует в возникновении заболеваний дыхательных путей, в отличие от детей, не получавших иммунизацию.
Summary. The article presents a review of the literature and own data obtained as a result of ten years of passive immunization of children born extremely preterm. The efficacy and good tolerability of the drug Palivizumab has been shown. It has been demonstrated that in the group of preterm infants who received a full course of passive immunization against respiratory syncytial viral infection with Palivizumab, the respiratory syncytial virus does not participate in the occurrence of respiratory tract diseases, unlike children who did not receive immunization.
Для цитирования: Миронова А.К., Османов И.М. Опыт проведения пассивной иммунизации против РСВ-инфекции у глубоконедоношенных детей // Практика педиатра. 2021. № 4. С. 31-6.
For citation: Mironova A.K., Osmanov I.M. Experience of passive immunization against RSV infection in preterm infants. Pediatrician's Practice 2021;(4):31-6. (In Russ.)
Респираторно-синцитиальный вирус (РСВ) является наиболее частой причиной развития инфекций нижних дыхательных путей среди младенцев и детей во всем мире [1-5] (рис. 1).
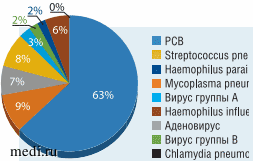 Рис. 1. Частота инфекций нижний дыхательных путей, вызванных различными возбудителями
Рис. 1. Частота инфекций нижний дыхательных путей, вызванных различными возбудителями
На долю РСВ приходится более 38% в структуре острых респираторных вирусных инфекций у детей раннего возраста [6] (рис. 2).
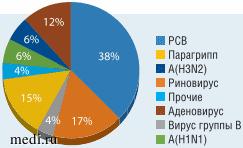 Рис. 2. Частота острых респираторных инфекций, вызванных различными вирусами
Рис. 2. Частота острых респираторных инфекций, вызванных различными вирусами
По оценкам Всемирной организации здравоохранения РСВ является причиной развития острых респираторных инфекций более чем у 80% детей в возрасте до 1 года и самой частой причиной развития бронхиолитов и пневмоний у детей в возрасте до 2 лет жизни [7]. Более 95% детей до 24 мес жизни хотя бы единожды перенесли инфекцию, вызванную РСВ, и более 60% детей к 2 годам переносят ее повторно [8-9].
При этом важно отметить, что инфекции нижних дыхательных путей, вызванные РСВ, считаются основной причиной госпитализации в течение 1-го года жизни [10]. Во многом это связано с особенностями самого вируса, который характеризуется тропностью к клеткам респираторного тракта и способен при репликации образовывать синцитий - скопление псевдогигантских клеток, связанных между собой цитоплазматическими отростками [8-10]. Помимо этого, РСВ нарушает выработку цитокинов. Активация Th2-зависимых процессов обусловливает бронхиальную гиперреактивность и обструкцию дыхательных путей, что ведет к тяжелому течению инфекции и ее отдаленным последствиям [9]. Это в том числе объясняет и формирование слабого и нестойкого иммунитета после перенесенной болезни, что делает возможным повторные заражения. При этом если у условно здоровых новорожденных и детей раннего возраста РСВ-инфекция, как правило, протекает в легкой и среднетяжелой форме и характеризуется чаще поражением верхних дыхательных путей, сопровождаясь ринореей, небольшим повышением температуры тела и продуктивным кашлем [11], то у детей из группы высокого риска эта инфекция имеет крайне тяжелое течение с поражением нижних дыхательных путей, приводящим к апноэ, тахипноэ и гипоксемии, что требует длительной госпитализации, поддерживающей кислородной терапии вплоть до искусственной вентиляции легких [12]. Многочисленными исследованиями доказано, что тяжелое течение РСВ-инфекции влечет за собой отдаленные последствия - периодическую обструкцию дыхательных путей в будущем и высокий риск развития бронхиальной астмы [13-15], что обусловливает необходимость более частого обращения за медицинской помощью и общее ухудшение качества жизни данной группы детей [16].
К факторам повышенного риска тяжелого течения РСВ-инфекции относятся недоношенность, хронические заболевания легких и врожденные пороки сердца (табл. 1).
Таблица 1.
Факторы повышенного риска тяжелого течения инфекции, вызванной респираторно-синцитиальным вирусом [1-8]
| Заболевания | Патофизиология |
|
Недоношенность |
Низкий уровень материнских антител |
|
Незрелость дыхательных путей |
|
|
Бронхиальная гиперреактивность |
|
|
Бронхолегочная дисплазия |
Сниженный легочный резерв, снижение оксигенации и вентиляции |
|
Бронхиальная гиперчувствительность |
|
|
Врожденные пороки сердца |
Легочная гипертензия |
| Гиперволемия малого круга кровообращения | |
| Несоответствие между объемом вентиляции и перфузии | |
| Склеротические изменения («синий порок») |
Следует добавить, что помимо факторов, указанных в табл. 1, уменьшают защитные свойства организма и повышают риск тяжелого течения РСВ любые иммунодефицитные состояния.
Так, частота жизнеугрожающих состояний (табл. 2) [16] и смертность среди детей из групп высокого риска по развитию тяжелых форм течения РСВ-бронхиолита значительно выше, чем у исходно здоровых детей [17] (рис. 3).
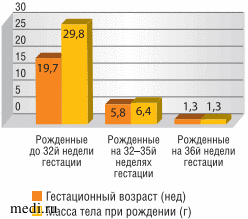 Рис. 3. Смертность (на 100 тыс.) при бронхиолите у детей раннего возраста (<1 года)
Рис. 3. Смертность (на 100 тыс.) при бронхиолите у детей раннего возраста (<1 года)
Таблица 2.
Частота жизнеугрожающих состояний у детей с тяжелым течением бронхиолита, вызванного респираторно-синцитиальным вирусом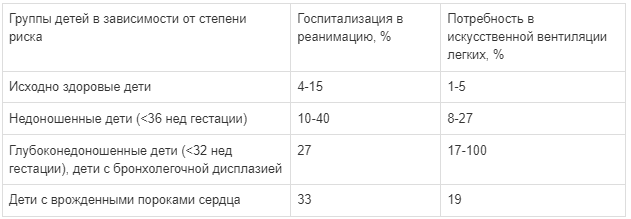 Если в группе исходно здоровых доношенных детей на 100 тыс. заболевших приходится 1,3 случая смерти по причине РСВ-ин-фекции, то у детей, родившихся до 32-й недели гестации, этот показатель выше в 15 раз, а у детей, родившихся с экстремально низкой массой тела (ЭНМТ) (≤1000 г), он увеличивается в 23 раза.
Если в группе исходно здоровых доношенных детей на 100 тыс. заболевших приходится 1,3 случая смерти по причине РСВ-ин-фекции, то у детей, родившихся до 32-й недели гестации, этот показатель выше в 15 раз, а у детей, родившихся с экстремально низкой массой тела (ЭНМТ) (≤1000 г), он увеличивается в 23 раза.
Все это создает необходимость дополнительной защиты детей групп высокого риска тяжелого течения РСВ-инфекции. Однако в связи с тем, что в настоящий момент не существует специализированного лечения РСВ, а также вакцинации против РСВ, эффективным способом борьбы с ним является профилактика, а именно пассивная иммунизация против РСВ препаратом «Паливизумаб» у детей с высоким риском тяжелого течения РСВ-инфекции.
Паливизумаб - первый в мире препарат моноклональных антител, применяемый в педиатрии [18]. Он был получен генноинженерным путем, не является препаратом крови и не несет риска заражения. Паливизумаб представляет собой гуманизированные моноклональные антитела класса IgG1, воздействующие на эпитоп А белка слияния F РСВ и обладает выраженной нейтрализующей и ингибирующей слияние клеток активностью против штаммов РСВ подтипов А и В. Молекула паливизумаба состоит из человеческих (95%) и мышиных (5%) аминокислотных последовательностей (рис. 4).
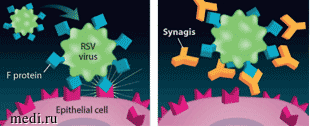 Рис. 4. Действие паливизумаба:
Рис. 4. Действие паливизумаба:
а - поверхностный белок РСВ (F-белок) опосредует взаимодействие вируса с мембраной эпителиальных клеток и способствует его проникновению в клетку;
б - паливизумаб, обладая высокой аффинностью к F-белку РСВ, связывается с ним и подавляет его активность.
Паливизумаб блокирует проникновение вируса в клетку и распространение инфекции [19]. Множественные международные и отечественные исследования доказали безопасность и хорошую переносимость паливизумаба в ходе применения в 60 странах мира на протяжении 20 лет. В России паливизумаб был одобрен в 2010 г., в то время как в США и странах Европы его начали применять с 1998 г.
В РФ профилактика тяжелой инфекции нижних дыхательных путей, вызванной РСВ, показана следующим группам детей, находящихся в зоне высокого риска развития тяжелых форм РСВ-инфекции:
- дети в возрасте до 6 мес, рожденные на 35-й неделе беременности или ранее;
- дети в возрасте до 2 лет, которым требовалось лечение по поводу бронхолегочной дисплазии в течение последних 6 мес;
- дети в возрасте до 2 лет с гемодинамически значимыми врожденными пороками сердца.
Программа проведения пассивной иммунизации против РСВ в России является территориальной и в настоящий момент уже реализована более чем в 70 субъектах. Правила ее проведения и показания к ней более подробно регламентируются внутренними нормативными документами. Так, в г. Москве ежегодно перед началом сезона иммунизации издается распоряжение Департамента здравоохранения г. Москвы с указанием срока начала иммунизации, показаний и регламента проведения пассивной иммунизации препаратом «Паливизумаб».
Иммунизация проводится в подразделениях 3-го уровня оказания медицинской помощи, которыми являются детские стационары, ЦВЛ, КДО, КДЦ. Схема применения препарата «Паливизумаб» включает 5 инъекций. Первую инъекцию выполняют в стационаре - в отделениях патологии новорожденных и недоношенных детей или других профильных отделениях перед выпиской из стационара; при вспышке РСВ выполнение 1-й инъекции детям из групп риска возможно уже в условиях отделения реанимации и интенсивной терапии новорожденных.
Так, на базе Детской городской клинической больницы им. З.А. Башляевой сформирован неонатальный комплекс, включающий 3 этапа выхаживания глубоконедоношенных детей, представленный отделением реанимации и интенсивной терапии новорожденных, отделением для недоношенных детей и центром восстановительного лечения детей, родившихся с очень низкой массой тела (ОНМТ) и ЭНМТ, где дети находятся под амбулаторным медицинским наблюдением до 3 лет жизни. Такая маршрутизация пациентов позволяет соблюдать этапность и преемственность в наблюдении и лечении глубоконедоношенных детей. Это относится и к проведению пассивной иммунизации, которая начинается еще при нахождении ребенка в стационаре, где с родителями проводят подробную разъяснительную беседу, объясняют важность проведения пассивной иммунизации и выполняют первую инъекцию. После выписки из стационара пациенты охотно продолжают проведение пассивной иммунизации на амбулаторном этапе. Интервалы между 1-м и 2-м введением препарата составляют 28-30 дней, между последующими введениями - 28 ± 4 дня. Своевременное выполнение последующих инъекций необходимо, так как действие паливизумаба начинается с момента введения и сохраняется на протяжении 4-5 нед. Соответственно, при более длительных интервалах между инъекциями существует риск заражения РСВ.
При этом важно отметить, что иммунизация считается завершенной при выполнении курса из 5 инъекций с обязательным соблюдением вышеуказанных интервалов. Такая схема иммунизации позволяет достичь следового эффекта с пролонгированной защитой ребенка на протяжении еще 2 мес после последней инъекции, что в целом составляет 7 мес и позволяет обеспечить потенцирование эффекта, которого достаточно для достижения необходимой сезонной иммуногенности от РСВ-инфекции.
Перед проведением иммунизации врач проводит физикальный осмотр ребенка, сбор анамнеза, в том числе аллергологического, термометрию и измерение массы тела, после чего выдает заключение об отсутствии противопоказаний к проведению пассивной иммунизации паливизумабом.
Ранее, при использовании сухих форм паливизумаба, требовалось около 20-30 мин для подготовки препарата к инъекции, т. е. для его разведения и растворения. С 2021 г. паливизумаб стал доступен в виде жидких форм и специальной подготовки уже не требует. Ребенку вводят препарат внутримышечно из расчета 15 мг/кг массы тела, при необходимом объеме более 1,0 мл препарат делят на 2 равные дозы, которые вводят в два бедра. Далее ребенок находится под наблюдением в течении 30 мин, после чего врач проводит повторный осмотр с термометрией и далее отпускает ребенка домой.
К противопоказаниям относится выраженная аллергическая реакция к одному из компонентов, входящих в состав паливизумаба, которая проявляется в виде выраженной местной аллергической реакции на введение препарата.
За 10 сезонов проведения пассивной иммунизации в России в Детской городской клинической больнице им. З.А. Башляевой курс пассивной иммунизации против РСВ прошли более 806 детей. Среди них преобладали глубоконедоношенные дети и дети с бронхолегочной дисплазией (рис. 5).
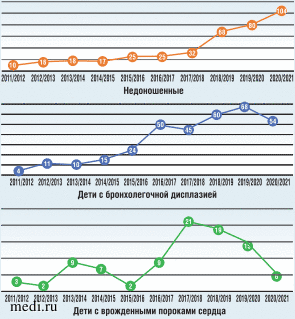 Рис. 5. Результаты пассивной иммунизации детей против респираторно-синцитиального вируса в Детской городской клинической больнице им. З.А. Башляевой
Рис. 5. Результаты пассивной иммунизации детей против респираторно-синцитиального вируса в Детской городской клинической больнице им. З.А. Башляевой
Начиная с сезона 2018/19 гг. более 75% детей прошли полный курс иммунизации - 5 инъекций, в то время как до 2015 г. средняя кратность введения составляла 2,3 дозы (табл. 3).
Таблица 3.
Средняя кратность введения препарата «Паливизумаб» в Детской городской клинической больнице им. З.А. Башляевой
| Сезон | Среднее количество полученных доз |
| 2014/15 | 2,3 |
| 2015/16 | 3,2 |
| 2016/17 | 3,6 |
| 2017/18 | 3,5 |
| 2018/19 | 3,7 |
| 2019/20 | 3,9 |
| 2020/21 | 4,2 |
Часть детей получила 1-ю инъекцию в условиях стационара, а последующие продолжили получать в других медицинских учреждениях, что не позволило достоверно оценить полноту курса препарата. В другом случае дети, рожденные уже в течение сезона проведения пассивной иммунизации, получали 1-ю инъекцию позже, в связи с этим у них меньше количество введенных доз.
Большое число детей, прошедших полный курс пассивной иммунизации против РСВ, безусловно, связано с налаженной маршрутизацией пациентов, нуждающихся в проведении пассивной иммунизации против РСВ, достаточной обеспеченностью медицинского учреждения препаратом, достаточно хорошей осведомленностью медицинских работников г. Москвы. Однако число детей с гемодинамически значимыми врожденными пороками сердца, получающих паливизумаб, нестабильно и имеет тенденцию к снижению, что может свидетельствовать о недостаточном охвате данной группы пациентов и требует дальнейшей проработки.
Эффективность пассивной иммунизации препаратом «Паливизумаб» детей, наблюдающихся в ЦВЛ, определялась по отсутствию госпитализаций по поводу тяжелых форм бронхиолитов и пневмоний, вызванных РСВ, в отделения реанимации и интенсивной терапии. Было отмечено значительное снижение частоты обострений бронхолегочной дисплазии и отсутствие побочных реакций при введении препарата. За 10 сезонов проведения иммунизации отсутствовали летальные исходы, связанных с РСВ-инфекцией или другой инфекцией нижних дыхательных путей.
Считаем целесообразным привести результаты анализа заболеваемости небольшой группы глубоконедоношенных детей (n = 65), родившихся с ОНМТ и ЭНМТ, которые находились под наблюдением в нашем центре в 2018-2021 гг., но, по ряду причин, не прошли пассивную иммунизацию паливизумабом. Заболевания органов дыхания с гипертермией были зафиксированы в 30 (46%) случаях, в том числе с необходимостью проведения антибактериальной терапии у 11 детей. В связи с тяжестью заболевания 7 (10,8%) пациентов были госпитализированы, из них состояние 3 (4,6%) пациентов потребовало нахождения в отделении реанимации и интенсивной терапии. Тест на РСВ, выполненный 7 детям с тяжелым течением заболевания, дал положительный результат в 3 случаях.
Таким образом, хочется еще раз отметить важность проведения пассивной иммунизации против РСВ у детей из групп высокого риска развития тяжелого течения РСВ-инфекции. Дети, рожденные с ОНМТ и ЭНМТ, благоприятно переносят иммунизацию паливизумабом без каких-либо нежелательных реакций.
В иммунизированной группе детей РСВ не участвует в возникновении заболеваний дыхательных путей, в отличие от неиммунизированных глубоконедоношенных детей.
Детям с ЭНМТ и ОНМТ необходимо и возможно проводить пассивную иммунопрофилактику РСВ-ин-фекции начиная со 2-го этапа выхаживания.
Литература
1. Emergence of new antigenic epitopes in the glycoproteins of human respiratory syncytial virus collected from a US surveillance study, 2015-17 / B. Lu [et al.] // Scientific Reports. 2019. Vol. 9, No. 1. P. 9898.
2. Piedimonte G., Perez M.K. Respiratory syncytial virus infection and bronchiolitis // Pediatrics in Review. 2014. Vol. 35, No. 12.
3. Respiratory syncytial virus vaccines / Ed. by S.A. Plotkin [et al.]. Plotkin’s Vaccines. 7th edn. Philadelphia, 2018. P. 943-939.
4. Rossi G.A., Colin A.A. Infantile respiratory syncytial virus and human rhinovirus infections: respective role in inception and persistence of wheezing // European Respiratory Journal. 2015. Vol. 45, No. 3. P. 774-789.
5. Respiratory syncytial virus (RSV). Vaccine Knowledge Project. November 22, 2019.
6. Острые инфекции нижних дыхательных путей у детей до 2 лет вызванные РСВ в 2-12 раз повышают риск бронхиальной астмы.
7. Respiratory syncytial virus-associated hospitalizations among young children / B. Rha [et al.] // Pediatrics. 2020. Vol. 146, No. 1.
8. Hacking D., Hull J. Respiratory syncytial virus - viral biology and the host response // Journal of Infection. 2002. Vol. 45, No. 1. P. 18-24.
9. RSV Global Epidemiology Network. Global, regional, and national disease burden estimates of acute lower respiratory infections due to respiratory syncytial virus in young children in 2015: a systematic review and modelling study / T. Shi [et al.] // Lancet. 2017. Vol. 390(10098). P. 946-958.
10. Black C.P. Systematic review of the biology and medical management of respiratory syncytial virus infection // Respiratory Care. 2003. Vol. 48. P. 209-231.
11. Olszewska W., Zambon M., Openshaw PJ.M. Development of vaccines against common colds // British Medical Bulletin. 2002. Vol. 62. P. 99-111.
12. Respiratory syncytial virus bronchiolitis in infancy is an important risk factor for asthma and allergy at age 7 / N. Sigurs [et al.] // American Journal of Respiratory and Critical Care Medicine. 2000. Vol. 161. P. 1501-1507.
13. Hospitalization for RSV bronchiolitis before 12 months of age and subsequent asthma, atopy and wheeze: a longitudinal birth cohort study / J. Henderson [et al.] // Pediatric Allergy and Immunology. 2005. Vol. 16. P. 386-392.
14. Stein R.T., Sherrill D., Morgan W.J. Respiratory syncytial virus in early life and risk of wheeze and allergy by age 13 years // Lancet. 1999. Vol. 354. P 541-545.
15. Sigurs N. A cohort of children hospitalised with acute RSV bronchiolitis: impact on later respiratory disease // Paediatric Respiratory Reviews. 2002. Vol. 3. P. 177-183.
16. Greenough A. Role of ventilation in RSV disease: CPAP, ventilation, HFO, ECMO // Respiratory Reviews. 2009. Vol. 1, Suppl 10. P. 26-28.
17. Respiratory syncytial virus hospitalizations among American Indian and Alaska native infants and the General United States infant population / Holman R.C. [et al.] // Pediatrics. 2004. Vol. 114. P 437-444.
18. Expert consensus on palivizumab use for respiratory syncytial virus in developed countries / Sanchez Luna M. [et al.] // Paediatric Respiratory Reviews. 2020. Vol. 33. P 35-44.
19. Young J. Development of a potent respiratory syncytial virus-specific monoclonal antibody for the prevention of serious lower respiratory tract disease in infants // Respiratory Medicine. 2002. Vol. 96, Suppl. B. P S31-S35.

