Острые миелоидные лейкозы у взрослых. Клинические рекомендации.
Статьи
Острые миелоидные лейкозы у взрослых
- Национальное гематологическое общество
Оглавление
- Ключевые слова
- Список сокращений
- Термины и определения
- 1. Краткая информация
- 2. Диагностика
- 3. Лечение
- 4. Реабилитация
- 6. Дополнительная информация, влияющая на течение и исход заболевания
- Критерии оценки качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение Б. Алгоритмы ведения пациента
- Приложение В. Информация для пациентов
- Приложение Г.
Ключевые слова
острый миелоидный лейкоз,
острый лейкоз,
костный мозг,
бластные клетки
химиотерапия,
трансплантация костного мозга,
минимальная резидуальная болезнь,
цитогенетическое исследование,
полная ремиссия,
рецидив,
факторы риска
классификация ВОЗ
Список сокращений
алло-ТГСК - трансплантация аллогенных гемопоэтических стволовых клеток
алло-ТКМ - трансплантация аллогенного костного мозга
ауто-ТГСК – трансплантация аутологичных стволовых гемопоэтических клеток
ауто-ТКМ - трансплантация аутологичного костного мозга
БЛРС – бетта-лактамазы расширенного спектра
ВДЦ – высокие дозы цитарабина
ВИЧ – вирус иммунодефицита человека
ВОЗ – Всемирная организация здравоохранения
ДНК – дезоксирибонуклеиновая кислота
ЖКТ – желудочно-кишечный тракт
ИА - инвазивный аспергиллез
КМ – костный мозг
КТ - компьютерной томографии
ЛДГ - лактатдегидрогеназа
МДС - миелодиспластический синдром
МДЦ - малые дозы цитарабина
МОБ - минимальная остаточная болезнь
МП - меркаптопурин
МПЗ – миелопролиферативное заболевание
МРБ - минимальная резидуальная болезнь
МС - миелоидная саркома
ОЛ - острый лейкоз
ОЛЛ - острый лимфобластный лейкоз
ОМЛ – острый миелоидный лейкоз
ПР - полная ремиссия
ПЦР – полимеразная цепная реакция
РКИ – рандомизированное клиническое исследование
РНК – рибонуклеиновая кислота
РТПХ – реакция «трансплантат против хозяина»
ТКМ - трансплантация костного мозга
УЗИ - ультразвукового исследование
ХТ - химиотерапии
ЦМВ - цитомегаловирус
ЭКГ - электрокардиографии
Эхо-КГ - эхо-электрокардиографии
FAB классификация – французско-американско-британская классификация
FISH - флюоресцентная in situ гибридизация
NCCN - Национальная общественная противораковая сеть
Термины и определения
Полной ремиссией (ПР) острого миелоидного лейкоза (ОМЛ) принято называть то состояние кроветворной ткани, при котором в пунктате костного мозга обнаруживается 5% и менее бластных клеток при нормальном соотношении всех ростков кроветворения, при количестве нейтрофилов в периферической крови более 1,0 х 109/л, при количестве тромбоцитов более или равном 100 х 109/л, при отсутствии экстрамедуллярных очагов лейкемического роста. Указанные показатели должны сохраняться в стабильном состоянии в течение 1 месяца и более.
Резистентная форма ОМЛ по мнению большинства российских экспертов констатируется при отсутствии полной ремиссии после завершения двух курсов индукционной терапии.
Ранняя смерть – смерть больного в период индукционной терапии (1--2 курса).
Рецидив ОМЛ констатируется при обнаружении в пунктате костного мозга более 5% бластных клеток.
Минимальной резидуальной болезнью (МРБ), или минимальной остаточной болезнью (МОБ) называют небольшую популяцию опухолевых клеток, которая не может быть зафиксирована с помощью светового микроскопа, но обнаруживается более тонкими методами исследования, выявляющими 1 лейкемическую клетку на 104-6 исследуемых.
Цитогенетическая ремиссия – это полная клинико-гематологическая ремиссия, при этом цитогенетическими методами не выявляются исходные аномалии кариотипа; кариотип должен быть нормальным.
Цитогенетический рецидив острого лейкоза (ОЛ) констатируется при наличии в пунктате костного мозга митозов с хромосомными аберрациями, обнаруживается в дебюте заболевания на фоне сохраняющейся клинико-гематологической ремиссии.
Молекулярная ремиссия – это полная клинико-гематологическая ремиссия при отсутствии исходно определявшихся методом ПЦР молекулярных маркеров ОЛ (дважды проведенный анализ).
Молекулярный рецидив – появление исходно определявшихся молекулярных маркеров ОЛ в двух повторных анализах (проведенных с коротким интервалом времени) на фоне сохраняющейся клинико-гематологической ремиссии.
Трансплантация костного мозга (ТКМ) - под этим термином объединены трансплантация гемопоэтических стволовых клеток костного мозга периферической крови, пуповинной (плацентарной) крови.
Общая выживаемость. Для построения кривой общей выживаемости анализируют временные параметры всех больных, включенных в исследование. Точкой отсчета является день начала терапии. Событием считается только смерть больного от любой причины (ранняя летальность, смерть в период ремиссии от любой причины, смерть в период рецидива).
Безрецидивная выживаемость. При построении кривой безрецидивной выживаемости учитывают данные только тех больных, у которых была достигнута полная ремиссия. Точкой отсчета считается дата достижения полной ремиссии. Событиями считаются рецидив и смерть от любой причины (в период консолидации или поддерживающего лечения, от рецидива, в период ремиссии от другой причины, например, суицида).
Вероятность сохранения полной ремиссии (обратное от вероятности развития рецидива). При построении кривой вероятности сохранения полной ремиссии учитываются данные только о тех больных, у которых достигнута полная ремиссия. При этом точкой отсчета служит дата достижения полной ремиссии. Событием считается только рецидив заболевания. Цензурируют всех больных, кто жив в полной ремиссии в момент проведения анализа.
Бессобытийная выживаемость. Этот показатель оценивает выживаемость всех больных, включенных в анализ, с момента начала терапии.
Индукция ремиссии. Период начального лечения, целью которого является максимально быстрое и существенное сокращение опухолевой массы и достижение полной ремиссии, называется периодом (обычно 1-2 курса). Именно в этот период на фоне применения цитостатических средств количество лейкемических клеток в костном мозге уменьшается примерно в 100 раз, т.е. в момент констатации полной ремиссии в костном мозге морфологически определяется менее 5% опухолевых клеток.
Консолидация ремиссии. Вторым этапом терапии ОЛ - закрепление достигнутого противоопухолевого эффекта (обычно 1--2 курса). В настоящее время в большинстве случаев консолидация является наиболее агрессивным и высокодозным этапом при лечении ОЛ. Задачей этого периода является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток.
Противорецидивное или поддерживающее лечение. Продолжение цитостатического воздействия в меньших дозах, чем в период индукции ремиссии, на возможно остающийся опухолевый клон.
Профилактика или, при необходимости, лечение нейролейкемии. Принципиальным этапом при лечении некоторых вариантов ОЛ (лимфобластных, промиелоцитарных, миеломоно- и монобластных) являются. Этот этап распределяется на все периоды программного лечения - индукцию ремиссии, консолидацию и поддерживающее лечение.
Резистентная форма ОЛ по мнению большинства российских экспертов констатируется при отсутствии полной ремиссии после завершения двух курсов индукционной терапии.
Важно отметить, что по международным критериям резистентность при ОМЛ можно оценивать лишь через 7 дней после завершения курса полихимиотерапии. Если больной умирает в течение курса химиотерапии (ХТ) и в течение 7 дней после него, определить, резистентная у него форма лейкоза или нет, нельзя, и больных относят к категории неудач в лечении как неопределенный исход.
Ранняя смерть – смерть больного в период индукционной терапии (1-2 курса). Следует подчеркнуть, что этот критерий является обобщающим для понятия гибели больного в процессе индукционной терапии. Этот критерий как таковой, отсутствует в международных рекомендациях. Он рассматривается, наряду с резистентностью, в категории неудач в лечении и объединяет два понятия: 1) аплазия -- смерть больного, пережившего после окончания курса ХТ 7 дней, в период миелотоксического агранулоцитоза и аплазии кроветворной ткани, доказанной пункцией костного мозга; 2) неопределенность эффекта – а) смерть больного в течение 7 дней после завершения ХТ; б) смерть больного в период проведения курса ХТ; в) смерть больного, пережившего после окончания курса ХТ 7 дней и более, у которого в периферической крови не выявляются бластные клетки, но пункция костного мозга не выполнена.
1. Краткая информация
1.1 Определение
Острый миелоидный лейкоз – это клональное опухолевое заболевание кроветворной ткани, связанное с мутацией в клетке-предшественнице гемопоэза, следствием которой становится блок дифференцировки и бесконтрольная пролиферация незрелых миелоидных клеток [1, 2].
1.2 Этиология и патогенез
ОМЛ является следствием повреждения - мутации - в генетическом материале клоногенной кроветворной клетки. В результате этого происходит нарушение контроля за клеточным циклом, изменение процесса транскрипции и продукции ряда ключевых белков. Вследствие бесконтрольной пролиферации в отсутствие дифференцировки происходит накопление патологических клеток. Тот факт, что патогенез острых лейкозов связан с генетическими поломками, довольно часто подтверждается обнаружением различных хромосомных аберраций (транслокаций, делеций, инверсий и т.д.). В большинстве случаев конкретная причина возникновения ОМЛ остается неизвестной. Однако существует несколько предрасполагающих факторов, которые значительно увеличивают риск развития этого заболевания. Четко доказанная взаимосвязь между ионизирующей радиацией при взрыве атомной бомбы, а также химио- и радиотерапией по поводу других опухолей с повышенным риском возникновения острых лейкозов заставила изучить другие возможные лейкемогенные факторы (низкие дозы радиации, химические вещества, курение, электромагнитные волны). Доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет. Ряд исследователей предполагает, что около 20% ОМЛ являются следствием курения. Бензол при длительном воздействие на организм человека дает лейкемогенный эффект, но при небольших концентрациях этого вещества, с которыми чаще всего сталкиваются люди на производстве, не доказана взаимосвязь с повышенным риском возникновения ОМЛ. При изучении постоянного воздействия малых доз радиации пока не получено доказательств в пользу увеличения частоты заболеваемости острыми лейкозами. Впервые взаимосвязь между предшествующей химиотерапией, лучевым лечением каких-либо других опухолевых заболеваний и увеличенным риском развития ОМЛ была отмечена у пациентов, излеченных от лимфогранулематоза. Доказано, что не столько кумулятивная доза, сколько интенсивность дозового воздействия обусловливает повышение частоты заболеваемости ОМЛ. Риск развития вторичного ОМЛ наиболее высок в период от 2 до 9 лет после завершения предшествующей химиотерапии. В 85% случаев вторичные лейкозы возникают в сроки до 10 лет от окончания лечения [1, 2].
1.3 Эпидемиология
Считается, что ОМЛ заболевает в среднем 3--5 человек на 100 тыс. населения в год. При этом заболеваемость резко возрастает в возрасте старше 60 лет, и составляет 12--13 человек на 100 тыс. у людей в возрасте старше 80 лет. Медиана возраста этого заболевания составляет 65 лет. При численности населения 140 млн жителей РФ расчетный показатель заболеваемости (исходя из Европейский и Американских данных) должен составлять около 5 тыс. заболевших.
По результатам регистрационного исследования, выполненного Российской исследовательской группой по изучению ОЛ в ряде регионов РФ, медиана возраста диагностики ОМЛ составляет 53 года, что более чем на 10 лет меньше, чем в западных странах. Эти показатели свидетельствуют как о не достаточной диагностике ОМЛ у больных старшей возрастной группы, так и меньшей продолжительности жизни населения в нашей стране. И хотя ОМЛ относят к орфанным заболеваниям, социальная значимость лечения этого самого грозного заболевания системы крови определяет необходимость организации адекватной специализированной помощи, предусматривающей взаимодействие многих медицинских дисциплин, совокупность клинических, лабораторных, инструментальных и научных исследований, преемственность стационарной и амбулаторной помощи [1, 2].
1.4 Кодирование по МКБ 10
C92.0 Острый миелоидный лейкоз
Исключение: обострение хронического миелоидного лейкоза (C92.1)
C92.1 Хронический миелоидный лейкоз
C92.2 Подострый миелоидный лейкоз
C92.3 Миелоидная саркома (хлорома, гранулоцитарная саркома)
C92.4 Острый промиелоцитарный лейкоз
C92.5 Острый миеломоноцитарный лейкоз
C92.7 Другой миелоидный лейкоз
C92.9 Миелоидный лейкоз неуточненный
1.5 Классификация
Диагноз острого миелоидного лейкоза устанавливают при обнаружении в костном мозге 20% бластных клеток и более (детальнее – см. далее).
Перечень вариантов ОМЛ и других опухолей с миелоидной дифференцировкой (ВОЗ, 2008) [1, 3, 4]:
Классификация ВОЗ (2008) подразделяет все ОМЛ, основываясь на их цитогенетических и молекулярно-генетических особенностях, и именно эти особенности формируют клинико-патологические группы:
ОМЛ с устойчиво выявляемыми генетическими аномалиями
ОМЛ с t(8;21)(q22;q22); RUNX1-RUNX1T1
ОМЛ с inv(16)(p13.1q22) or t(16;16)(p13.1;q22); CBFB-MYH11
ОПЛ с t(15;17)(q22;q12); PML-RARA
ОМЛ с t(9;11)(p22;q23); MLLT3-MLL
ОМЛ с t(6;9)(p23;q34); DEK-NUP214
ОМЛ с inv(3)(q21q26.2) or t(3;3)(q21;q26.2); RPN1-EVI1
ОМЛ (мегакариобластный) с t(1;22)(p13;q13); RBM15-MKL1
Предварительная подкатегория: ОМЛ с нормальным кариотипом и мутированным геном NPM1
Предварительная подкатегория: ОМЛ с нормальным кариотипом и мутированным геном CEBPA
ОМЛ с изменениями, связанными с миелодисплазией
Миелоидные неоплазии, связанные с предшествующей ХТ (исключенная категория)
ОМЛ, по-другому не специфицированные (NOS)
Острый миелобластный лейкоз с минимальной дифференцировкой
Острый миелобластный лейкоз без созревания
Острый миелобластный лейкоз с созреванием
Острый миеломонобластный лейкоз
Острый монобластный/моноцитарный лейкоз
Острый эритромиелоз
Острый мегакариобластный лейкоз
Острый лейкоз из базофилов
Острый панмиелоз с миелофиброзом (син.: острый миелофиброз; острый миелосклероз)
Миелоидная саркома (син.: экстрамедуллярная миелоидная опухоль; гранулоцитарная саркома; хлорома)
Миелоидные опухоли, связанные с синдромом Дауна
Транзиторный аномальный миелопоэз (син.: транзиторное МПЗ)
Миелоидный лейкоз, связанный с синдромом Дауна
Опухоль из плазмацитоидных дендритных клеток
Острые лейкозы неясной линии дифференцировки
Острый недифференцированный лейкоз
Острый лейкоз смешанного фенотипа с t(9;22)(q34;q11.2); BCR-ABL1
Острый лейкоз смешанного фенотипа с t(v;11q23); реарранжировка гена MLL
Острый лейкоз смешанного фенотипа, B/миелоидный, NOS
Острый лейкоз смешанного фенотипа, T/миелоидный, NOS
Предварительная подкатегория: лимфобластный лейкоз/лимфома из клеток натуральных киллеров?
Следует отметить, что BCR-ABL1-позитивный ОЛ может быть диагностирован как ОЛ смешанного фенотипа, но терапия больным с этим вариантом проводится по программам лечения BCR-ABL1-позитивного острого лимфобластного лейкоза (ОЛЛ).
Подгруппа «ОМЛ с устойчиво выявляемыми хромосомными аномалиями» объединяет несколько вариантов ОМЛ:
«ОМЛ с t(8;21)(q22;q22); RUNX1-RUNX1T1»
«ОМЛ с inv(16)(p13.1q22) или t(16;16)(p13.1;q22); CBFB-MYH11» (при выявлении указанных хромосомных перестроек, несмотря на число бластных клеток в пунктате костного мозга, всегда устанавливают диагноз острого миелоидного лейкоза).
«ОПЛ с t(15;17)(q22;q12); PML-RARA»; транслокации RARA с другими партнерами выделяются в отдельные формы ОМЛ, например, ОМЛ с t(11;17)(q23;q12); ZBTB16-RARA; ОМЛ с t(11;17)(q13; q12); NUMA1-RARA; ОМЛ с t(5;17)(q35;q12); NPM1-RARA; ОМЛ с STAT5BRARA.
Ранее выделяемая категория «ОМЛ с аномалиями 11q23 (MLL)» была пересмотрена в категорию «ОМЛ с t(9;11)(p22;q23); MLLT3-MLL»; другие транслокации, отличающиеся от тех, что включают MLLT3, должны быть отдельно указаны в диагнозе, например ОМЛ с t(6;11)(q27;q23); MLLT4-MLL; ОМЛ с t(11;19)(q23;p13.3); MLLMLLT1; ОМЛ с t(11;19)(q23;p13.1); MLL-ELL; ОМЛ с t(10;11)(p12;q23); MLLT10- MLL
Были выделены три новых подгруппы: «ОМЛ с t(6;9)(p23;q34); DEK-NUP214», «ОМЛ с inv(3)(q21q26.2) or t(3;3)(q21; q26.2); RPN1-EVI1» и «ОМЛ (мегакариобластный) с t(1; 22)(p13;q13); RBM15-MKL1», редкий вариант ОЛ, наиболее часто диагностируемый у детей.
У больных ОМЛ с нормальным кариотипом были выделены две новые категории: «ОМЛ с мутированным геном NPM1 (нуклеофозмин (ядерный фосфопротеин B23, нуматрин))» и «ОМЛ с мутированным геном CEBPA (белок, связывающий энхансер CCAAT альфа (CCAAT/enhancer binding protein (C/EBP) alpha))». Накапливается все больше доказательств в пользу того, что эти мутации определяют нарушения дифференцировки гемопоэтических клеток, и относятся к так называемым мутациям 2-го класса.
Мутации в гене fms-связанной тирозинкиназы 3 (fms-related tyrosine kinase, FLT3) обнаруживаются при многих вариантах ОМЛ, и их относят к мутациями 1-го класса, т.е. к тем, которые определяют преимущество опухолевых клеток в пролиферации и/или выживании. ОМЛ с мутациями FLT3 не выделяется в отдельную категорию, однако, необходимо определять эти мутации, так как они имеют прогностическую значимость.
Ранее выделяемая подгруппа «ОМЛ с мультилинейной дисплазией» в классификации ВОЗ (2008) определяется как «ОМЛ с изменениями, связанными с миелодисплазией». ОМЛ могут относиться к категории «ОМЛ с изменениями, связанными с миелодисплазией», если:
1) существует предшествующая история миелодиспластического синдрома (МДС) или иного миелопролиферативного заболевания (МПЗ);
2) существуют цитогенетические аномалии, ассоциированные с миелодисплазией:
а - комплексный кариотип (3 хромосомных аномалии и более);
б - несбалансрованные перестройки: -7 or del(7q); -5 or del(5q); i(17q) or t(17p); -13 or del(13q); del(11q); del(12p) or t(12p); del(9q); idic(X)(q13);
в - сбалансированные перестройки (транслокации):
t(11;16)(q23;p13.3); t(3;21)(q26.2;q22.1); t(1;3)(p36.3; q21.1); t(2;11)(p21;q23); t(5;12)(q33;p12); t(5;7)(q33;q11.2); t(5;17)(q33;p13); t(5; 10)(q33;q21); t(3;5)(q25;q34).
3) мультилинейная дисплазия или, если 50% и более клеток в двух и более линиях клеточной дифференцировки имеют черты дисплазии;
4) отсутствуют «устойчиво выявляемые хромосомные аномалии»;
5) не проводилась ХТ по поводу другого заболевания.
ОМЛ, как другие миелоидные опухоли, возникшие вследствие ранее проводимой ХТ по поводу других заболеваний, в отдельную форму ОМЛ не выделяются.
Прогностические факторы
Прогностические факторы могут быть подразделены на 2 основные группы:
1-я группа – факторы, основанные на характеристиках пациента и состоянии его общего здоровья;
2-я группа – факторы, обусловленные биологическими характеристиками лейкемического клона;
3-я группа, отмеченная в этой главе, является не объективным критерием, а субъективным, но исключительно принципиальным, фактором, особенно в условиях Российской Федерации.
Факторы прогноза, связанные с пациентом
Возраст является одним из универсальных, независимых и устойчивых факторов прогноза. Долгосрочные результаты лечения больных ОМЛ в возрасте старше 60 лет значительно хуже в сравнении с таковыми у больных моложе 60 лет.
Это обусловлено, как минимум, двумя причинами. Во-первых, увеличением с возрастом частоты неблагоприятных цитогенетических поломок: отмечается постепенное нарастание случаев с несбалансированными хромосомными аберрациями, с комплексным и моносомнным кариотипом. Одновременно с этим снижается частота обнаружения сбалансированных аберраций, включая такие благоприятные варианты как транслокации t(8;21), t(15;17) и инверсия 16-й хромосомы inv(16). Не исключено, что данный феномен может быть обусловлен тем, что с возрастом увеличивается частота возникновения ОМЛ из предшествующего МДС. Другой признак, который определяет негативное влияние возраста на прогноз ОМЛ – присоединение сопутствующих заболеваний, наличие которых определяет значительное ухудшение общесоматического статуса по сравнению с молодыми больными при прочих равных условиях.
Факторы прогноза, связанные с заболеванием (ОМЛ)
Факторы, связанные с заболеванием и влияющие на результаты терапии, следует анализировать на всех этапах лечения. Это обусловлено тем, что лейкоз-ассоциированные факторы прогноза позволяют оценить объем опухолевой массы, чувствительность бластных клеток к цитостатическим препаратам, скорость элиминации лейкемических клеток и объем минимальной остаточной (резидуальной) болезни (МРБ).
Прежде всего, необходимо учитывать такие вполне доступные клинико-гематологические параметры, ассоциированные с неблагоприятным течением ОМЛ как лейкоцитоз выше 100 х 10^9/л, удлинение сроков от момента диагностики заболевания до начала терапии, персистировании бластных клеток в периферической крови ко времени завершения индукционного курса, недостижение полной ремиссии после первого индукционного курса.
Одним из важнейших факторов прогноза, сопряженных с ОМЛ, является кариотип лейкемических клеток. Исследование кариотипа необходимо проводить в обязательном порядке всем больным с подозрением на ОМЛ. Данные цитогенетического исследования позволяют верифицировать ОМЛ в случаях, когда принципиальным является не количество бластных клеток (меньше или больше 20%), а обнаружение характерных хромосомных аберраций. Речь идет, в частности, о так называемом CBF (Сore Binding Factor) ОМЛ, который объединяет случаи с транслокацией t(8;21) и инверсией inv(16) независимо от отсутствия или наличия дополнительных хромосомных аберраций.
Помимо этого на основании изучения кариотипа представляется возможным стратифицировать больных ОМЛ на 3 основные группы: благоприятного, промежуточного и неблагоприятного прогноза (табл.1). Подразделение больных ОМЛ на эти группы целесообразно с точки зрения выбора тактики постремиссионной терапии: применение цитарабина в высоких дозах, использование трансплантации аллогенных стволовых гемопоэтических клеток. Следует отметить, что у половины больных ОМЛ определяется нормальный кариотип лейкемических клеток. Это может служить основанием в ряде случаев для проведения FISH-исследования или молекулярно-генетических исследований с целью поиска отдельных химерных генов, ассоциированных с определенным клинико-гематологическим фенотипом ОМЛ и прогнозом: RUNX1-RUNX1T1 (t(8;21)), CBFB-MYH11 (inv16), PML-RARa (t(15;17)), MLLT3-MLL (t(9;11)), DEK-NUP214 и ряда других.
Вместе с тем, необходимым является и поиск у больных ОМЛ с нормальным кариотипом мутаций отдельных генов с установленным прогностическим потенциалом. Молекулярно-генетическая стратификация больных ОМЛ на группы риска представлена в табл. 1.
Факторы прогноза, связанные с неадекватной ХТ
В Российской Федерации, к сожалению, существует такой фактор неблагоприятного прогноза как неадекватное цитостатическое воздействие в период индукции/консолидации (уменьшение расчетных доз цитостатических препаратов и значительное удлинение интервалов между курсами), или неадекватная предлеченность. Еще в начале 1970-х годов, на первых этапах становления ХТ ОМЛ американскими исследователями было доказано, что эффективность программы “5+2” статистически значимо хуже, чем программы “7+3”. Более 20 лет назад в Российских исследованиях было продемонстрировано, что уменьшение доз антрациклиновых антибиотиков и цитарабина в классической программе “7+3” приводит к существенному ухудшению показателей общей и безрецидивной выживаемости.
В тех ситуациях, когда цитогенетическое и/или молекулярное исследование не выполнено, определить группу риска у больного не представляется возможным. Однако можно ориентироваться на «синтетические» - объединяющие молекулярно-генетические и клинические признаки ОМЛ - рекомендации европейских экспертов, которые подразделяют больных на две основные группы: благоприятного и неблагоприятного прогноза. Эти рекомендации с добавлениями от российских экспертов представлены в табл. 2. [1, 3-5].
1.6 Клиническая картина
В основном они связаны с замещением нормальной гемопоэтической ткани опухолевыми клетками (анемия, тромбоцитопения, гранулоцитопения), инфильтрацией ими различных органов и продукцией различных цитокинов. Дебют ОМЛ может быть острым cо значительным повышением температуры тела, резкой слабостью, интоксикацией, кровоточивостью, тяжелыми инфекциями. Однако нередко диагноз устанавливают случайно при профилактическом осмотре или в случае госпитализации по другой причине. У пожилых больных нередко на фоне анемизации появляется или усугубляется стенокардия, возникают нарушения ритма, в связи с чем их госпитализируют в кардиологическое отделение.
При объективном обследовании может не наблюдаться никаких симптомов. Но довольно часто выявляется увеличение периферических лимфатических узлов, печени, селезенки (что наиболее характерно для моно- и миеломонобластном лейкозе), гиперплазия десен (при миеломоно- и монобластных вариантах), инфильтрация кожи (миеломоно- и монобластных вариантах), геморрагический синдром различной степени тяжести - от петехиальных высыпаний до тяжелых кровотечений, боли в костях, артралгии, неврологическая симптоматика (менингеальные знаки - головная боль, ригидность затылочных мышц, симптом Кернига, парез лицевого, глазодвигательного и других нервов, парезы нижних конечностей и т.д.). В анализах крови могут быть неспецифические изменения: трехростковая цитопения, или анемия, или только лейкопения или лейкоцитоз, или тромбоцитопения. Бластные клетки могут не определяться в анализе периферической крови и, наоборот, составлять 90-95% всех лейкоцитов. Количество лейкоцитов также варьирует от менее 1,0 до 200-300х109/л. Примерно в 15% случаев в дебюте заболевания определяется более 100х109/л.
Дифференциальная диагностика ОМЛ проста, поскольку, если есть его морфологическое подтверждение (бластные клетки в пунктате или в периферической крови), диагноз очевиден. Трудности возникают на первых этапах - при анализе мазков периферической крови, когда бластных клеток нет. Увеличение числа лейкоцитов со сдвигом формулы влево при различных инфекционных процессах может вызывать сомнения в диагнозе ОЛ, но в таких случаях никогда не обнаруживаются типичные бластные клетки. Увеличение числа лейкоцитов при тяжелых инфекциях, сепсисе (например, менингококковом) может сопровождаться снижением числа тромбоцитов, анемией, геморрагическим синдромом, тем не менее, никогда не выявляются характерные бластные клетки. Нередко требуется дифференциальная диагностика с инфекционным мононуклеозом и некоторыми другими вирусными инфекциями, тем более, что клиническая симптоматика (повышение температуры тела, боли в горле, увеличение лимфатических узлов, печени, селезенки) может напоминать таковую при ОЛ. Следует также дифференцировать ОМЛ с бластным кризом хронического миелолейкоза (присутствие филадельфийской хромосомы не всегда помогает, так как этот маркер может обнаруживаться и при острых лейкозах, возникших de novo). Но это не принципиально, так как и в том и другом случае показана агрессивная химиотерапия.
Особого внимания заслуживают внекостномозговые проявления ОЛ, особенно нейролейкемия, которая может определяться и в момент диагностики ОЛ. Возникновение нейролейкемии обусловлено метастазированием лейкозных клеток в паутинную и мягкую мозговые оболочки головного и спинного мозга. В ряде случаев наблюдается лейкозная инфильтрация периферических нервов с разнообразными двигательными и чувствительными нарушениями, или обнаруживается очаговое поражение вещества головного мозга. Нейролейкемия характеризуется менингеальным и гипертензивным синдромом: отмечается постоянная головная боль, возможна рвота, вялость, выявляется отек дисков зрительных нервов, может быть нистагм, косоглазие, другие признаки поражения черепно-мозговых нервов, выявляется ригидность затылочных мышц, симптом Кернига. При ОМЛ нейролейкемия довольно редка в дебюте болезни, тем не менее встречается при миеломоно- и монобластных вариантах, особенно при тех формах лейкозов, когда обнаруживают поломку 16 хромосомы – inv(16) (у 30% таких больных при отсутствии профилактики возникает нейролейкемия). При ОМЛ к экстрамедуллярным относят поражения кожи (лейкемиды - чаще всего это багрово-синюшные уплотнения, узелки в коже), сетчатки, десен, яичек, яичников. Описаны поражения лимфатических узлов, легких, кишечника, сердечной мышцы, мочеточников. При ОМЛ экстрамедуллярные поражения мягких тканей ранее называли “хлоромой”. В настоящее время для обозначения поражения мягких тканей и органов используют термин миелоидная или гранулоцитарная саркома [2].
2. Диагностика
2.1 Жалобы и анамнез
Клинические проявления при ОМЛ обычно связаны с изменениями в гемограмме – цитопенией:
Нейтропения – бактериальные инфекции, проявляющиеся как правило лихорадкой;
Анемия – слабость, утомляемость. Общая слабость присутствует у большинства пациентов и может наблюдаться за несколько месяцев до установления диагноза;
Тромбоцитопения – геморрагический синдром в виде петехий, кровоточивости десен, рецидивирующих носовых кровотечений, гиперполименорреи.
В некоторых случаях могут наблюдаться оссалгии, В-симптомы (лихорадка, снижение массы тела, выраженная потливость).
В ряде случаев у пациентов в течение нескольких месяцев до обращения может наблюдаться немотивированная слабость.
При остром миеломонобластном лейкозе и остром монобластном лейкозе характерна гиперплазия десен и пациенты могут первоначально обращаться к стоматологу.
-
Рекомендовано при ОМЛ тщательный сбор анамнеза заболевания с уточнением терапии, которая проводилась в связи с данным заболеванием и ранее по поводу других заболеваний, а также подробное описание жалоб больного.
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а) [2].
2.2 Физикальное обследование
-
Рекомендуется при осмотре больного ОМЛ включает измерение роста и массы тела, температуры тела; оценку состояния кожных покровов, костно-суставной системы; выявление признаков геморрагического синдрома; наличие гепатоспленомегалии, лимфоаденопатии; наличие признаков дисфункции сердца, легких, печени, органов эндокринной системы [2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а)
Комментарии: При физическом обследовании у части пациентов (в основном с острым миеломонобластным лейкозом, острым монобластным лейкозом, бластным кризом хронического миелолейкоза) выявляются признаки пролиферативного синдрома – спленомегалия, увеличение лимфатических узлов, кожные лейкемиды. Лейкемиды выявляются в 13% случаев и имеют вид узлов c измененным цветом кожи над ними. В остальном проявления малоспецифичны и включают симптомы, связанные с анемией и тромбоцитопенией.
2.3 Лабораторная диагностика
-
Рекомендуется выполнение общего анализа периферической крови с подсчетом лейкоцитарной формулы и определением числа тромбоцитов [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
Комментарии:Как правило, выявляется нормохромная, нормоцитарная анемия различной степени тяжести. Количество ретикулоцитов в пределах нормы или снижено. Примерно у 75% пациентов имеется тромбоцитопения. Средний уровень лейкоцитов на этапе установления диагноза около 15х10^9/л. 20% пациентов имеют лейкоцитоз более 100х10/л
-
Рекомендуется выполнить биохимическое исследование крови (общий белок, белковые фракции, мочевина, креатинин, билирубин, аминотрансферазы, ЛДГ, магний, натрий, калий, кальций, глюкоза) [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
-
Рекомендуется выполнить исследование свертывающей системы крови (АЧТВ, протромбиновый индекс по Квику, тромбиновое время, фибриноген) [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
-
Рекомендуется выполнить исследование общего анализа мочи [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
-
Рекомендуется определение маркеров ВИЧ, сифилис и гепатитов В и С (иммуноферментный метод и ПЦР) [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
-
Рекомендуется определение маркеров герпесвирусной инфекции (иммуноферментный метод и ПЦР) [1, 7-9].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2b).
-
Рекомендуются микробиологические исследования (посев со слизистой оболочки рта и кишечника, посев крови; посев мочи) [1, 7-9].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а).
-
Рекомендуется определение группы крови с фенотипом по системе резус [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
-
Рекомендуется выполнить морфологическое и цитохимическое исследование аспирата костного мозга [1, 2, 4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
Комментарии: Для установления диагноза ОМЛ в мазке периферической крови или костного мозга необходимо наличие 20% или более бластных клеток. Следует подчеркнуть, что пункцию костного мозга необходимо выполнять во всех случаях, независимо от процентного содержания бластных клеток в периферической крови. При ОМЛ с t(15;17), t(8;21), inv(16) or t(16;16) и при некоторых случаях острого эритромиелоза доля бластных клеток может быть менее 20%. Для идентификации линии клеточной дифференцировки выполняется цитохимическое исследование бластных клеток.
-
Рекомендуется выполнить иммунофенотипическое исследование аспирата костного мозга [1-4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
Комментарии: Иммунофенотипирование выполняют с помощью мультипараметрической проточной цитофлюориметрии (обычно как минимум 3- или 4-цветной). Особенно это исследование необходимо для установления диагноза ОМЛ с минимальной дифференцировкой, острого мегакариоцитарного лейкоза и ОЛ с неопределенной дифференцировкой. Также его используют для более четкого определения принадлежности бластных клеток к той или иной линии клеточной дифференцировки после установления морфологического диагноза ОМЛ. Далее для достоверной диагностики билинейного или бифенотипического ОЛ необходимо выполнить расчеты в соответствии со шкалой EGIL и ВОЗ (табл.3) : если сумма баллов для каждой линии кроветворения составляет более 2, то указанный диагноз может быть установлен Объединенная цитохимическая и иммунофенотипическая характеристика бластных клеток при острых миелоидных лейкозах представлена в табл. 4.
-
Рекомендуется выполнить цитогенетическое исследование аспирата костного мозга [1-4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
Комментарии: Стандартное цитогенетическое исследование является необходимым компонентом диагностических процедур у пациента с подозрением на ОЛ. Хромосомные аномалии детектируются в примерно у половины больных ОМЛ. Для определения кариотипа достоверным считается только исследование как минимум 20 метафаз. Аномалии в кариотипе могут устанавливаться и на основании исследования клеток периферической крови.
-
Рекомендуется выполнить детекцию реарранжировок генов методом флюоресцентная in situ гибридизация (FISH) из аспирата костного мозга [1-4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2a).
- Комментарии: Исследование выполняется при отсутствии результата стандартного цитогенетического исследования (мало материала, не было получено митозов) или получен нормальном кариотипе, но при этом имеются яркие клинико-лабораторные симптомы. При ОМЛ исследуются RUNX1-RUNX1T1, CBFB-MYH11, MLL и EVI1 или потеря хромосомы 5q и 7 FISH зачастую необходим для идентификации слияний MLL при транслокациях региона 11q23.
-
Рекомендуется выполнить молекулярное исследование аспирата костного мозга на химерные гены RUNX1-RUNX1T1, CBFB-MYH1, PML/RARA [1-4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а).
Комментарии: ОМЛ с мутациями в генах NPM1 или CEBPA определены ВОЗ как условные категории. Скрининг этих двух маркеров, так же как и FLT3, должен выполняться при проведении клинических испытаний. Экспрессия генов ERG, MN1, EVI1, BAALC, мутации генов WT1, RUNX1, MLL, KITRAS, TP53, TET2, IDH1и определение МРБ исследуются в рамках Клинических исследований. Молекулярный скрининг на указанные маркеры самостоятельного значения не имеет, но как вспомогательный метод может быть использован при отсутствии результатов стандартного цитогенетического исследования.
-
Рекомендуется выполнить люмбальную пункцию с исследованием ликвора [1, 2, 4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2а).
Комментарии: При ряде вариантов ОМЛ высока вероятность вовлечения оболочек головного мозга. Поэтому всем больным показано выполнение диагностической люмбальной пункции с морфологическим исследованием ликвора.
Если уровень тромбоцитов не удается повысить до 30х10^9/л и выше, от пункции можно воздержаться до восстановления показателей после курса. Если у больного определяется лейкоцитоз выше 100х10^9/л, то первую люмбальную пункцию следует отложить до редукции числа лейкоцитов менее 10х10^9/л.
-
Рекомендуется выделять и сохранять первичную ДНК или РНК из клеток костного мозга больных в биобанке, или направлять материал на хранение в лаборатории Федеральных Центров [1, 2, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2в).
Комментарии: Сохранение первичного биологического материала (ДНК, выделенная из костно-мозговых клеток, или замороженные клетки) для выполнения в будущем молекулярных исследований, позволяющих четко определить группы риска.
2.4 Инструментальная диагностика
-
Рекомендуется выполнение электрокардиографии (ЭКГ) [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2a).
Комментарии: выявление нарушения проводимости импульсов в сердечной мышце;
-
Рекомендуется выполнение компьютерной томографии (КТ) головного мозга [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: выявление изменений головного мозга;
-
Рекомендуется выполнение рентгенографии и/или КТ органов грудной клетки [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: выявление изменений легочной ткани и органов средостения;
-
Рекомендуется выполнение ультразвукового исследование (УЗИ) органов брюшной полости [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: определение размеров печени, селезенки и внутрибрюшных лимфатических узлов, а также оценка состояния органов брюшной полости;
-
Рекомендуется выполнение Эхо-электрокардиографии (Эхо-КГ) исследование [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
Комментарии: оценка функционального состояния сердечной мыщцы;
-
Рекомендуется выполнение УЗИ органов малого таза у женщин и предстательной железы у мужчин [1, 2].
Уровень убедительности рекомендаций D (уровень достоверности доказательств – 2).
-
Рекомендуется выполнение УЗИ периферических и внутрибрюшных лимфоузлов[1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2).
2.5 Иная диагностика
-
Рекомендуется выполнение определение статуса больного (по шкалам ECOG/WHO), оценка коморбидности [1, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2a).
-
Рекомендуется выполнение женщинам репродуктивного возраста теста на беременность [1, 4].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2b).
-
Рекомендуется выполнение HLA-типирование больного и сиблингов с целью поиска потенциального донора костного мозга [1, 4, 6].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2a).
-
Рекомендуется консультация невропатолога [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендуется консультация окулиста [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендуется консультация отоларинголога [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
-
Рекомендуется консультация гинеколога [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
В дальнейшем контрольные обследования больного (общий анализ периферической крови, биохимическое исследование крови, общий анализ мочи) проводится 1 раз в неделю или по необходимости.
На фоне постремиссионной терапии рекомендовано повторять пункции костного мозга перед каждым курсов ХТ предусмотренным протоколом. После окончания терапии желательно выполнять пункции костного мозга 1 раз в 3 месяца в течение первого года. Большинство рецидивов происходят в течение 1--3 лет после окончания терапии. Стандартизованные временные точки взятия костного мозга необходимы при мониторинге МРБ. Исследование общего анализа крови выполняется каждый месяц в течение первых 2 лет и затем 1 раз в 2--3 месяца до 5 лет от начала лечения [1, 2].
3. Лечение
Эффективность ХТ острых лейкозов зависит от двух ключевых факторов – специфичности цитостатического воздействия и адекватности сопроводительного лечения. Конечно, биологические особенности лейкемического клона – цитогенетические аномалии, молекулярные маркеры, кинетические свойства опухолевых клеток, их химиочувствительность – определяют в рамках современной ХТ прогноз заболевания, но только при условии соблюдения основного принципа лечения ОЛ – максимум эффективности (за счет специфичности и адекватности воздействия) при минимуме токсичности (за счет грамотной сопроводительной терапии). Долгосрочные результаты лечения ОМЛ взрослых в течение последних 20 лет, несмотря на совершенствование терапии выхаживания и использования ряда новых препаратов, принципиально не изменились. В среднем 5-летняя общая выживаемость больных в возрасте до 60 лет по данным больших кооперативных исследовательских групп составляет 35-50%, варьируя от 10 до 90% в зависимости от молекулярно-генетических особенностей лейкемии. Доля летальных исходов, связанных с лечением, у этих больных составляет 7-18%. В лечении пожилых больных долгосрочные результаты не претерпели практически никаких изменений в течение 3 последних десятилетий, и 5-летняя выживаемость не превышает 10-12%. Именно ОМЛ является той областью клинической гематологии, в которой продолжаются интенсивные как клинические, так и лабораторные исследования, направленные на хоть какой-то положительный сдвиг в устоявшихся долгосрочных результатах [1-5].
Международные эксперты настоятельно советуют включать больных в клинические исследования и сохранять биологические образцы для возможности их сопоставления в дальнейшем с полученными результатами терапии и установления корреляции между лабораторными данными и исходом заболевания. Использование принципов «доказательной» медицины в такой области как гематология является необходимым, поскольку, пожалуй, ни в какой другой области медицинских знаний не приходится постоянно сталкиваться с критическими ситуациями и принятием критических решений [1-5].
В 2010 г. были опубликованы Рекомендации европейских экспертов по диагностике и лечению ОМЛ [4]. В течение десятка лет в США разрабатываются и постоянно обновляются рекомендации, так называемой Национальной общественной противораковой сети (NCCN) [5]. В последние годы был достигнут значительный прогресс в понимании молекулярно-генетической и эпигенетической основы развития ОМЛ, что позволило определить новые диагностические и прогностические маркеры заболевания. В классификации ВОЗ (2008) учтены и генетические и молекулярные варианты ОМЛ [3]. Изданы Европейские рекомендации по оптимальной интеграции трансплантации аллогенного костного мозга в программную терапию ОМЛ [6].
При всех ОЛ существует несколько основных этапов терапии - индукция ремиссии (табл. 5), консолидация (табл. 6), поддерживающая терапия (табл. 7) и профилактика нейролейкемии для некоторых вариантов ОЛ [1, 2]. После стандартной индукционной терапии (7+3) или терапии аналогичной интенсивности, оценка ответа обычно осуществляется на 21—28-й день после начала терапии либо на момент восстановления показателей периферической крови. Время может варьировать в зависимости от протоколов. Если полная ремиссия после двух курсов индукции не достигнута, то констатируется первичная резистентность, и больным проводят терапию по программам лечения рефрактерных форм лейкемии. Сразу же необходимо подчеркнуть, что недостижение полной ремиссии после первого индукционного курса является достоверным фактором плохого долгосрочного прогноза ОМЛ, поэтому уже сразу после первого курса (при условии адекватности доз и длительности цитостатического воздействия) больные должны рассматриваться в качестве потенциальных кандидатов для выполнения трансплантации аллогенного костного мозга [1, 4].
Группа Российских экспертов полагает, алло-ТКМ показана всем больных ОМЛ в первой полной ремиссии в возрасте моложе 60 лет, кому не выполнены молекулярно-генетические исследования, естественно, с учетом трансплантационных рисков и коморбидностей. Если цитогенетические и молекулярные исследования были выполнены, то показания к выполнению алло-ТКМ в первой полной ремиссии ОМЛ рассматриваются в рамках международных критериев (табл. 8). Представленная в табл. 9 информация, может служить подсказкой в принятии решения о выполнении ТКМ у больного ОМЛ в первой полной ремиссии. Если риск развития рецидива превышает на ХТ интегрированные риски после алло-ТКМ, то решение принимается в пользу ТКМ [1, 4, 6].
Принципы лечения ОМЛ и протоколы определяются возрастом больного.
3.1 Лечение больных ОМЛ в возрасте от 18-60 лет
-
Рекомендуется начинать индукционная терапия сразу после того, как все диагностические мероприятия будут завершены [1-4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
-
Не рекомендуется начинать немедленно проведение адекватной цитостатической терапии при:
1) тяжелая застойная сердечная недостаточность (фракция выброса менее 50%), нестабильная стенокардия, грубые нарушения ритма и проводимости с нестабильностью гемодинамики, острый инфаркт миокарда (анамнез менее 1 месяца);
2) почечная недостаточность (показатель сывороточного креатинина более 0,2 ммоль/л (или более 200 мг/мкл); за исключением случаев, обусловленных лейкемической инфильтрацией почек);
3) печеночная недостаточность (за исключением случаев, обусловленных лейкемической инфильтрацией органа), острый вирусный гепатит В или С;
4) тяжелая пневмония (дыхательная недостаточность -- одышка более 30 дыхательных движений в мин, артериальная гипоксемия менее 80 mm Hg, при этом, следует иметь в виду, что если в течение 2-3 дней не удается стабилизировать состояние больного, курс ХТ должен быть начат, поскольку нередко диагностируется исходное поражение легочной ткани лейкемическими клетками, и без специфической терапии шансы на излечение пневмонии чрезвычайно малы);
5) сепсис (при нестабильности гемодинамики); только высокая лихорадка без характерных признаков сепсиса не может служить поводом к отсрочке ХТ);
6) угрожающие жизни кровотечения (желудочно-кишечный тракт, профузное маточное, кровоизлияние в головной мозг);
7) тяжелые психические нарушения (бред, тяжелый депрессивный синдром и другие проявления продуктивной симптоматики);
8) физическая несостоятельность, требующая постоянного ухода, кахексия (показатель общего белка ниже 35 г/л);
9) декомпенсированный сахарный диабет (сахар крови выше 15 ммоль/л);
10) неконтролируемое течение сопутствующего онкологического заболевания [1].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
Комментарии: В том случае, если на момент поступления у больного было одно из вышеуказанных состояний, но его в результате интенсивного симптоматического лечения удалось купировать или взять под контроль (сепсис, пневмония, кровотечение, диабет и т.д.), то больному по истечении 3--7 дней может быть начата цитостатическая ХТ. Если в ходе симптоматического лечения сопутствующей патологии отмечается увеличение числа лейкоцитов, процентного содержания бластных клеток в периферической крови, или исходно уровень лейкоцитов составляет 100 х 10^9/л и более, целесообразно к терапии осложнений добавить гидроксимочевину в дозе 100 мг/кг в день, и в случае необходимости для профилактики тумор-лизис синдрома выполнить плазмаферез. Если состояние больного вследствие крайне тяжелых осложнений, связанных с заболеванием, или вследствие тяжелой сопутствующей патологии, не удается стабилизировать в течение максимум 7 дней, допускается рассмотреть вопрос о паллиативном цитостатическом воздействии (например, цитарабин в малых дозах).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
Комментарии: 7-дневное введение цитарабина может быть выполнено в дозе 100--200 мг/м2 либо 2 раза в сутки как короткая инфузия либо в виде непрерывной в/в инфузии в сочетании с 3-дневным введением антрациклинов (даунорубицина в дозе как минимум 60 мг/м2 или идарубицина в дозе 12 мг/м2 или митоксантрона 10 мг/м2).
-
Не рекомендуется использование доксорубицина при проведении курса “7 + 3 в индукции ремиссии ОМЛ [1-5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
-
Не рекомендуется использовать цитарабин в высоких дозах в индукционных курсах при ОМЛ [1, 4, 5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарии: это возможно только в рамках клинических исследований.
-
Рекомендуется проведение 1 или 2 курсов ХТ (в зависимости от того, после какого курса - 1-го или 2-го - достигается полная ремиссия) индукции ремиссии и 3 курса консолидации ВДЦ [1, 4, 5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
Комментарии: Возможные варианты дозировок цитарабина - 3 г/м2, 1,5 г/м2 и 1 г/м2 2 раза в день 1, 3, 5 дни с одинаковой эффективностью.
-
Рекомендуется при недостижении полной ремиссии после первого индукционного курса “7+3”, руководствоваться в выборе второго индукционного курса клинической ситуацией [1].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b).
Комментарии: Возможны 3 варианта: 1) повторение курса, аналогичного первому; 2) изменение интенсивности химиотерапевтического воздействия - выполнение высокодозного курса; 3) проведение курса цитарабином в малых дозах.
Исключением из этой рекомендации может быть ОМЛ, при котором после первого курса индукции либо не произошло уменьшения процента бластных клеток в костном мозге более чем на 50%, либо отмечена прогрессия заболевания (увеличился процент бластных клеток, появились отсутствующие ранее экстрамедуллярные очаги). В этой ситуации вторым индукционным курсом целесообразно признать курс с цитарабином в высоких дозах в сочетании с новыми антрациклиновыми антибиотиками.
-
Рекомендуется при развитии у больного после первого индукционного курса жизнеугрожающих осложнений, потребовавших реанимационных мероприятий (септический шок, инфаркт миокарда, миокардит и др), или активного аспергиллеза, интенсивная индукционная/консолидирующая может быть временно заменена курсами цитарабином в малых дозах [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: Также целесообразно иметь в виду, что, особенно у больных, которым в дебюте заболевания была определена благоприятная цитогенетическая группа. Могут быть выполнены 1-2 курса МДЦ, и после купирования всех осложнений целесообразно вернуться к высокодозной консолидации и выполнить минимум 2 курса высокодозной консолидации (ВДЦ). МДЦ могут остаться основной терапией в течение 3 лет только у больных острым эритромиелозом (М6-вариант) и мегакариобластным (М7-вариант).
-
Рекомендуется проводить профилактику нейролейкемии с помощью интратекальных введений при миеломонобластном (М4) и монобластном (М5) варианте ОМЛ, при лейкоцитозе свыше 30 х 10^9/л, при всех формах ОМЛ, при которых диагностируют экстрамедуллярные образования, а также миелоидной саркоме [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b).
-
Рекомендуется проведение поддерживающая терапия при ОМЛ [1].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2b).
Комментарии: Поддерживающая терапия должна выполняться в течение, как минимум, одного года от начала лечения (4 курса индукции/консолидации и 6 курсов поддерживающей терапии) или в течение 2 лет от начала терапии (4 курса индукции/консолидации и 9-12 курсов поддерживающей терапии). Большинство зарубежных исследовательских групп по лечению ОМЛ не рекомендуют проведение поддерживающий терапии.
-
Не рекомендуется выполнение трансплантация аутологичных стволовых гемопоэтических клеток/костного мозга (ауто-ТСГК/ауто-ТКМ) у больных ОМЛ [5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2a).
-
Рекомендуется выполнение трансплантация аллогенного костного мозга или аллогенных гемопоэтических стволовых клеток (алло-ТКМ/алло-ТГСК), как этапа постремиссионной терапии, у больных из группы высокого риска и больных из группы промежуточного риска, с нормальным кариотипом и неблагоприятными молекулярными маркерами в первой полной ремиссии [1-6].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Все больные, которым не выполнены цитогенетические и молекулярно-генетические исследования на момент установления диагноза, рекомендовано выполнение алло-ТКМ в период первой полной ремиссии [1]. Для больных из группы высокого риска, в том числе с FLT3-ITD алло-ТКМ следует рассматривать как обязательный этап лечения. Именно для этой группы больных крайне важно выполнение HLA-типированию пациента до начала первого индукционного курса, а после достижения первой полной ремиссии - начало поиска потенциальных доноров.
-
Не рекомендуется выполнение трансплантация алло-ТКМ/алло-ТГСК в период первой полной ремиссии ОМЛ больным из группы благоприятного риска [1, 4-6].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: За исключением случаев - ОМЛ с t(8;21) и лейкоцитозом выше 20х10^9/л, больные старше 35 лет, ОМЛ с t(8;21) и с inv16 и мутациями KIT или персистенцией высокого уровня МРБ, для которых алло-ТКМ является оптимальным вариантом, ОМЛ с нормальным кариотипом и благоприятным молекулярным профилем, но с гиперлейкоцитозом ?100 х 10/л
-
Рекомендуется при констатации первичной резистентности ОМЛ, проведение терапии по программам лечения рефрактерных форм ОМЛ [1-5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1а).
Комментарии: Терапия цитарабином в высоких дозах (если его не применяли в первой линии индукции) в сочетании с антрациклинами может рассматриваться в качестве индукции ремиссии перед алло-ТКМ. Для улучшения результатов ТКМ у больных с рефрактерными ОМЛ, используют режимы кондиционирования. – последовательное применение интенсивной ХТ и через 3 дня режима кондиционирования пониженной интенсивности с последующей алло-ТКМ (так называемый, протокол FLAMSA-RIC) и в дальнейшем - профилактическое использование трансфузий донорских лимфоцитов и/или терапия гипометилирующими препаратами (азацитидином, децитабином).
-
Не рекомендуется выполнение ТКМ пациентам, у которых не достигнута ремиссия после нескольких линий индукционной терапии [1-6].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2b).
Комментарии: Эти больные должны включаться в клинические исследования по изучению новых лекарственных препаратов.
-
Рекомендуется у больных вторичным ОМЛ придерживаться алгоритма выбора терапевтической тактики таковому как при «de novo» ОМЛ [1, 2].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2b).
Комментарии: Выбор тактики лечения вторичного ОМЛ должен проводиться с учетом цитогенетического варианта лейкоза, типа предшествующей терапии, возраста и соматического статуса больного и наличия отдельных осложнений. В случае доступности HLA-совместимого донора больной должен быть ориентирован на проведение алло-ТКМ.
3.2 Лечение пациента с ОМЛ старшей возрастной группы
Выделяют три основных «технологии» лечения ОМЛ у пожилых больных. Первый подход – это интенсивная ХТ, подобная таковой у молодых, представляющая собой в большинстве случаев сочетание цитарабина с антрациклинами и направленную на достижение ПР. Алло-ТГСК является оптимальной постремиссионной опцией в рамках этой концепции. Второй подход – это низкоинтенсивная терапия, в частности применение низкодозного цитарабина, эффективность которого, по крайней мере, у больных в возрасте 70 лет и старше, можно повысить с помощью пролонгированного использования в течение 28 дней, и гипометилирующих агентов (азацитидин, децитабин). Достижение ПР в этой модели не является обязательным. Третий выбор – симптоматическая (сопроводительная) терапия, направленная на уменьшение клинической симптоматики и улучшение качества жизни [1, 2, 4-6].
-
Рекомендуется больных ОМЛ в возрасте 60-75 лет рассматривать в качестве кандидатов на выполнение стандартных программ интенсивного лечения («7+3») [1, 2, 4, 5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2b).
Комментарии: Оценка «пригодности» вида терапии для пациента старше 60 лет должна строиться на основании учета возраста пациента, объективного определения тяжести состояния, цитогенетического и молекулярно-генетического вариантов заболевания и анализа сопутствующей патологии. Выбор конкретного антрациклина (даунорубицин, идарубицин или митоксантрон) существенно не влияет на конечные результаты. Стандартной считается доза даунорубицина 45 мг/м2.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Вариантами низкоинтенсивной химиотерапии могут быть: курсы терапии малыми дозами 10 мг/м2/сут х 28 дней с интервалом 28-30 дней, либо комбинированная терапия малых доз цитарабина с децитабином и идарубицином (табл.5). Кандидатами для низкоинтенсивной терапии также являются больные в возрасте от 60 до 75 лет с плохим соматическим статусом, наличием коморбидностей или дисфункцией органов
-
Рекомендуется для пожилых пациентов ОМЛ можно рассматривать в качестве терапии выбора проведение терапии азацитидином [1, 4, 5].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Терапия азацитидином 75 мг/м2 х 7 дней с интервалом 21 день (табл.5).
3.3 Терапия рецидивов ОМЛ
К сожалению, у большинства больных (60-70%), у кого достигнута полная ремиссия ОМЛ, в течение 3 лет развивается рецидив заболевания. В целом, прогноз пациентов после рецидива неблагоприятен и терапевтических подходов крайне мало. Долгосрочная выживаемость зависит от способности успешно индуцировать повторную ремиссию и возможности проведения ТКМ в качестве консолидации. Больные с очень ранним рецидивом (длительностью ремиссии менее полугода), неблагоприятными цитогенетическими аномалиями и старшего возраста имеют плохой прогноз [1, 4-5].
-
Рекомендуется при развитии рецидива ОМЛ, в качестве 2 линии терапии, использовать цитарабин в средней (1 г/м2) или высокой дозе (2-3 г/м2), либо сочетание цитарабина с антрациклинами.
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: Для пациентов с ожидаемой избыточной токсичностью ХТ возможной опцией является использование цитарабина в дозе 10 мг/м2 2 раза в день подкожно в течение 28 дней. У больных с продолжительностью ремиссии более 12 мес может быть использовано сочетание цитарабина в стандартных дозах (100 мг/м2 2 раза в день или 200 мг/м2 в день непрерывно в 1—7-й дни) и идарубицина (12 мг/м2 1 раз в день в 1—3-й дни).
-
Рекомендуется при достижении очередной ремиссии ОМЛ, в качестве консолидирующей терапии, выполнение алло-ТКМ [1, 4-6].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарии: Если выполнение алло-ТКМ невозможно (например, из-за отсутствия подходящего донора), ауто-ТКМ может рассматриваться в качестве второй линии терапии, но ее эффективность четко не определена
-
Рекомендуется при развитии рецидива ОМЛ после алло-ТКМ прекращение иммуносупрессивной терапии и выполнение трансфузии лимфоцитов донора (ТЛД) [6].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарии: Больным с поздним рецидивом (более 1 года после алло-ТКМ) может быть выполнена вторая алло-ТКМ, после достижения повторной ремиссии.
3.4 «Молекулярная» терапия
Прогресс в изучении молекулярного патогенеза ОМЛ привел к разработке новых «молекулярных» препаратов, т.е. молекул, механизм действия которых связан с влиянием на белки, функция которых изменяется в результате мутации или транслокации. Например, генетические изменения приводят к мутациям в генах, активирующих каскады трансдукции сигнала (например, FLT3, KIT, RAS), к слиянию генов или мутациям, приводящим к повышению или угнетению транскрипционной активности (например, PML-RARA, RUNX1-RUNX1T1, CBFB-MYH11, CEBPA) или к нарушению функции генов, вовлеченных в передачу сигнала (например, NPM1, NUP98, NUP)Хотя для некоторых препаратов, действующих на молекулярном уровне, и была продемонстрирована эффективность при ОМЛ, уже на стадии клинических испытаний было понятно, что большинство из них необходимо использовать в сочетании со стандартными цитостатическими препаратами [1, 4-6].
3.5 Ведение больных с особыми ситуациями
Гиперлейкоцитоз
Гиперлейкоцитозом обычно считается число лейкоцитов более 100 х 10^9/л, и это состояние закономерно связано с увеличением показателя смертности в индукции из-за геморрагических осложнений, синдрома лизиса опухоли и инфекционных осложнений [1, 2].
-
Рекомендуется при диагностике ОМЛ с гиперлейкоцитозом назначение гидроксимочевины в дозе от 50 до 100 мг/кг в день(не более 3-х дней) и, при снижении лейкоцитов до 50 х 10^9/л, начинать курса ХТ. Если число лейкоцитов в крови не уменьшается в течение 2 дней, то рекомендуется начать ХТ без дальнейшего приема гидроксимочевины [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Если на фоне гиперлейкоцитоза (более 100 х 10^9/л) имеются очевидные признаки “лейкоцитарных стазов”, наряду с назначением гидроксимочевины целесообразно проведение 2-3 сеансов лейкафереза. До снижения лейкоцитов не рекомендуются переливания эритроцитной массы вследствие вероятного увеличения вязкости крови.
При появлении признаков тумор-лизис синдрома на фоне цитолитического синдрома рекомендуется выполнение плазмафереза в небольшом объеме (1-1,2 л) с замещением альбумином и плазмой, с целью профилактики легочного дистресс-синдрома и острой почечной недостаточности. Чтобы избежать «обвального» цитолиза, в указанной ситуации, можно сначала ввести только цитарабин и затем выполнить плазмаферез, а введение даунорубицина приурочить ко второму введению цитарабина или даже отложить на 3-5 дни курса, а первые 3 дня выполнять плазмаферезы через 2-3 часа после введения цитарабина.
Вовлечение ЦНС
Изначальное вовлечение ЦНС при ОМЛ встречается менее чем у 5% больных. Как ранее отмечалось, зарубежные исследователи не рекомендуют выполнять профилактику нейролейкемии у больных без неврологической симптоматики, однако российские исследователи считают профилактику нейролейкемии обязательным этапом лечения при миеломонобластном (М4) и монобластном (М5) варианте ОМЛ, при лейкоцитозе свыше 30х10^9/л, при всех формах ОМЛ, при которых диагностируют экстрамедуллярные образования [1, 2].
-
Рекомендуется выполнение всем больным ОМЛ диагностической люмбальной пункции [1, 2].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b).
Комментарии: Нейролейкемия диагностируется при обнаружении в спинномозговой жидкости при первой диагностической люмбальной пункции бластных клеток при любом цитозе или цитоза 15/3 и более (т.е. более 5 клеток в 1 мкл).
-
Рекомендуется при диагностике нейролейкемии, проведение терапии нейролейкемии - выполнение люмбальных пункций с интратекальными введением стандартного набора препаратов (метотрексат 15 мг, цитарабин 30 мг, дексаметазон 4 мг) интервалом в 3 дня. После нормализации показателей ликвора должно быть сделано минимум три пункции с таким же интервалом между введениями и в дальнейшем пункции выполняют перед каждым курсом запланированного протокола [1, 2].
-
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2b).
Миелоидная саркома
Миелоидная саркома (МС) (син: экстрамедуллярная миелоидная опухоль, гранулоцитарная саркома, хлорома) – это опухоль, состоящая из миелоидных клеток-предшественниц, возникающая в любом месте, отличном от костного мозга (наиболее часто, в коже, лимфатических узлах, ЖКТ, костях, мягких тканях и яичках). МС может развиваться de novo, предшествуя ОМЛ, возникать параллельно развитию ОМЛ или презентировать в качестве бластной трансформации МДС, МПЗ или МДС/МПЗ. Диагноз устанавливается на основании биопсии опухолевого образования и использовании в дальнейшем цитохимических (отпечатки) и иммуногистохимических (биоптат) методов [1, 2].
-
Рекомендуется при диагностике миелоидной саркомы использовать в качестве первого индукционного курса программу 7+3 с даунорубицином или идарубицином (цитарабин в/в 100 мг/м2 2 раза в день в 1—7-й дни, даунорубицином 60 мг/м2 или идарубицин 12 мг/м2 в 1—3-й дни). В качестве второго курса (независимо от того получена была полная ремиссия/регрессия или нет) целесообразно применять программу НАМ (цитарабин 3 г/м2 2 раза в день в 1—3-й дни, митоксантрон 10 мг/м2 в 3--5-й дни), в дальнейшем – два курса консолидации цитарабином в высоких дозах (3 г/м2 2 раза в день в 1, 3, 5-й дни) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: При миелоидной саркоме показано проведение программы нейропрофилактики.
3.6 Сопроводительная терапия
-
Рекомендуется при проведении химиотерапии, с целью профилактики тошноты и рвоты, использовать антиэметики [1].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
-
Не рекомендуется использование при ОМЛ ростовых факторов [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Их применение может быть рассмотрено в исключительных случаях.
-
Не рекомендуется проведение первичной профилактики бактериальных инфекций при ОМЛ антибиотическими препаратами [7-9].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2).
Комментарии: Профилактика бактериальных инфекций (селективная деконтаминация кишечника) не проводится по причине высокой частоты инфекций, вызванных энтеробактериями с продукцией бета-лактамаз расширенного спектра. Их применение может быть рассмотрено в исключительных случаях.
-
Рекомендуется проведение в ходе индукции ОМЛ профилактики инвазивных микозов позаконазолом в клиниках, где частота возникновения инвазивный аспергиллез (ИА) превышает 10% [7-9].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Больным, имевшим на курсах ХТ инвазивный аспергиллез, проводится вторичная противогрибковая профилактика, и используют тот препарат, при назначении которого было достигнуто излечение от ИА. В большинстве случаев с этой целью применяют вориконазол.
-
Рекомендуется в качестве антибиотиков первого этапа при фебрильной нейтропении использовать цефоперазон/сульбактам, пиперациллин/тазобактам, цефепим, цефтазидим [7-9].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Модификация антимикробной терапии проводят в соответствии с данными проведенного обследования (КТ, микробиологические исследования и т.д.). Назначение карбапенемов в качестве антибиотиков первого этапа при фебрильной нейтропении обосновано у больных с септическим шоком, а также в клиниках, где в этиологии инфекций, преобладают энтеробактерии с продукцией БЛРС.
-
Рекомендуется в качестве порогового уровня необходимости трансфузий тромбоконцентратов, число тромбоцитов в периферической крови - 10х10^9/л, при условии отсутствия геморрагий и/или инфекционных эпизодов [1, 4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Любое проявление геморрагического синдрома (петехиальные высыпания, особенно на слизистой полости рта, на лице и передней поверхности грудной клетки, любые кровотечения), повышение температуры тела выше 37,5оС даже в отсутствии явного очага инфекции, диагностика любого инфекционного процесса, - требует немедленного увеличения объема трансфузий тромбоцитов и поддержание их на уровне не менее 20 х 10^9/л.
-
Рекомендуется при выявлении признаков аллосенсибилизации, переливать концентраты тромбоцитов по подбору. С целью преодоления аллосенсибилизации можно рекомендовать и выполнение серии (не менее 4--5) плазмаферезов (0,5 объема циркулирующей плазмы за сеанс с замещением альбумином) и выполнение трансфузий б-льших (12-16), чем средние (6-8) дозы тромбоконцентратов [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется поддерживать целевые показатели гемоглобина при ОМЛ на уровне не ниже 80 г/л (гематокрит не менее 20%) [1,4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
-
Не рекомендуется больным ОМЛ выполнение трансфузий гранулоцитов [1,4].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
4. Реабилитация
Специальных методов реабилитации при ОМЛ не существует. Реабилитация при возникновении осложнений в течение заболевания и лечения проводится в рамках соответствующих нозологий. После окончания лечения рекомендуется вести здоровый образ жизни, исключить инсоляцию и физиопроцедуры.
6. Дополнительная информация, влияющая на течение и исход заболевания
Молекулярно-генетические и клинические признаки ОМЛ, разделяющие больных на благоприятную и неблагоприятную прогностические группы
|
Цитогенетические маркеры |
Молекулярные маркеры |
Клинические факторы |
|
Благоприятные прогностические факторы: |
||
|
t(15;17), (t(8;21)(q22;q22); inv(16)(p13.1q22) или t(16;16)(p13.1;q22) |
Мутированный CEBPA (биаллельная мутация), мутированный NPM1 без FLT3-ITD при нормальном кариотипе |
Негативные маркеры МРБ |
|
Неблагоприятные прогностические факторы: |
||
|
inv(3)(q21q26.2) или t(3;3)(q21;q26.2); t(9;22), t(6;9)(p23;q34); t(v;11)(v;q23); -5 или del(5q); -7; аберрации (17р); комплексный кариотип, моносомный кариотип |
Увеличена экспрессия Evi1; MLL-реаранжировки; FLT3-ITD-мутация; DNMT3A-мутация; С-KIT-мутация (для t(8;21); inv(16)) BAALC-экспрессия ERG-экспрессия MN1-экспрессия WT1-полиморфизм BCR-ABL-позитивность |
Вторичный ОМЛ Старший возраст (40—60 лет), для inv(16) старше 35 лет Гиперлейкоцитоз (>100х10^9/л для любого варианта, для t(8;21) - >20х10^9/л) М0-вариант по FAB Экспрессия CD34 на бластных клетках Экстрамедуллярные поражения (особенно, кожа) Отсутствие ремиссии после первого курса Перситенция маркеров МРБ |
6.1 Беременность
-
Рекомендуется проведение лечения ОМЛ на фоне беременности мульдисциплинарной командой врачей, включающей гематолога, акушера-гинеколога, анестезиолога-реаниматолога, в стационаре, имеющей возможности оказания акушерской помощи родоразрешения в экстренных ситуациях [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется беременным женщинам выполнять полный объем диагностических исследований при ОМЛ, как и у не беременных больных, в соответствии с классификацией ВОЗ [1, 3, 4].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3).
-
Не рекомендуется выполнение стандартных рентгенологических метод обследований при беременности [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 2).
Комментарии: С диагностической целью при беременности целесообразно применение магниторезонансных методов исследование, а также ультразвуковые исследования, в том числе легочной ткани.
-
Не рекомендуется отсрочка начала лечение ОМЛ при установлении диагноза во время беременности [1].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 3).
-
Рекомендуется при диагностике ОМЛ в течение первого триместра беременности, выполнить искусственное прерывание беременности по медицинским показаниям [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Однако, если женщина и ее семья настаивают на пролонгировании
беременности, лечение может быть начато и в первом триметре беременности.
-
Рекомендуется при диагностике ОМЛ на сроке беременности 13-34 недели (после завершения первого триместра беременности), рекомендуется проведения ПХТ по программе «7+3» на фоне беременности при условии адекватного мониторинга плода и акушерской помощи [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется при диагностике ОМЛ после 36 недели выполнить родоразрешение до начала химиотерапии [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: При гиперлейкоцитозе родоразрешение выполняется в ходе циторедуктивной терапии.
-
Рекомендуется в выборе лекарственных веществ во время беременности, в том числе цитостатических и антибиотических препаратов, руководствоваться соотношением риска-пользы для матери и плода [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Цитостатические препараты рассчитываются в соответствии с выбранной программой лечения (без редукции доз) на поверхность тела больной с корректировкой по весу во время лечения. При жизнеугрожающих осложнениях у матери возможно назначение антибиотических препаратов без учета их возможного тератогенного воздействия на плод (сульфаметоксазол/триметаприм при пневмоцистной пневмонии, ганцикловир при цитомегаловирусной инфекции и т.д.)
-
Рекомендуется на фоне беременности, с учетом возможного тератогенного воздействия метотрексата, выполнение интратекальных введений цитостатических препаратов без использования метотрексата [1].
-
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется в ходе химиотерапии на фоне беременности регулярно выполнять УЗИ матки и плода и фетальное доплерографическое мониторирование плода [1].
-
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется планировать срок родоразрешения с учетом дней введения цитостатических препаратов - не ранее чем через 2-3 недели после введения цитостатических препаратов, с целью уменьшение вероятности миелосупрессии у плода [1, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
-
Рекомендуется выполнять родоразрешение методом кесарева сечения [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: Выбор способа родоразрешение определяется состоянием плода, соматическим статусом пациентки, гематологическими показателями и строго в соответствии с акушерскими показаниями. Самопроизвольные роды могут быть выбраны как способ родоразрешения только при наличии у больной ремиссии ОМЛ, удовлетворительных показателей гемограммы и хорошем соматическом статусе пациентки и состоянии плода.
-
Не рекомендуется выполнять при родоразрешении эпидуральную анестезию при тромбоцитопении <80х10^9/л и/или нейтропения (<1х10^9/л) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 1).
-
Рекомендуется при плановом преждевременном родоразрешении на сроке 24-35 недель проводить профилактику ОРДС плода – в/в введение дексаметазона 8-12 мг/сут. 2 дня в течение недели до родов [1].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Критерии оценки качества медицинской помощи
Список литературы
-
Программное лечение заболеваний системы крови, под ред. Савченко В.Г. М.: Практика; 2012: 155—245.
-
Савченко В.Г., Паровичникова Е.Н. Глава «Острые лейкозы» в книге «Клиническая онкогематология», под ред. Волковой М.А., М.: Медицина; 2001: 156-207.
-
Swerdlow S., Campo E., Yarris N.L. et al., eds. WHO classification of tumors of hematopoietic and lymphoid tissues. Geneva: WHO PRESS; 2008: 110—55.
-
D?hner H., Estey E.H., Amadori S., Appelbaum F.R., B?chner T., Burnett A.K., et al.; European LeukemiaNet. Diagnosis and management of acute myeloid leukemia in adults: recommendations from an international expert panel, on behalf of the European LeukemiaNet. Blood. 2010; 115(3): 453--74. doi: 10.1182/blood-2009-07-235358.
-
National Comprehensive Cancer Network (NCCN) GUIDELINES FOR AML TREATMENT Version 2.2013. httр://www.nccn.org/professionals/physician_gls/pdf/aml.pdf
-
Cornelissen J.J., Gratwohl A., Schlenk R.F., Sierra J., Bornh?user M., Juliusson G., et al. The European LeukemiaNet AML Working Party consensus statement on allogeneic HSCT for patients with AML in remission: an integrated-risk adapted approach. Nat. Rev. Clin. Oncol. 2012; 9(10): 579—90. doi: 10.1038/nrclinonc.2012.150.
-
Averbuch D., Orasch C., Cordonnier C., Livermore D.M., Mikulska M., Viscoli C., et al.; ECIL4, a joint venture of EBMT, EORTC, ICHS, ESGICH/ESCMID and ELN. European guidelines for empirical antibacterial therapy for febrile neutropenic patients in the era of growing resistance: summary of the 2011 4th European Conference on Infections in Leukemia. Haematologica. 2013; 98(12): 1826—35. doi: 10.3324/haematol.2013.091025
-
ECIL-4, 2011; Targeted therapy against multi-resistant bacteria in leukemic and hematopoietic stem cell transplant recipients: Guidelines of the 4th European conference on Infections in Leukemia (ECIL-4, 2011. D. Averbuch et al. Haematologica 2013.
-
ECIL-5, 2013; https://www.ebmt.org/Contents/Resources/Library/ECIL/ Documents/2014%20ECIL5/ECIL5antifungalprophylaxis%20%2020062014%20Final.pdf
Приложение А1. Состав рабочей группы
Афанасьев Б.В. д.м.н., профессор, директор НИИ детской гематологии и трансплантологии им. Р.М.Горбачевой, Санкт-Петербургский государственный медицинский университет, Санкт-Петербург
Баранова О.Ю. к.м.н., старший научный сотрудник отделения гематологии ФГБУ Российский онкологический научный центр им. Н. Н. Блохина, Москва;
Бондаренко С.Н. к.м.н., НИИ детской гематологии и трансплантологии им. Р.М.Горбачевой, Санкт-Петербургский государственный медицинский университет, Санкт-Петербург,
Гапонова Т.В. к.м.н., заместитель генерального директора ФГБУ Гематологический Научный центр Минздрава России, Москва
Грицаев С.В. д.м.н., главный научный сотрудник отделения химиотерапии гемобластозов, депрессий кроветворения и трансплантации костного мозга ФГБУ Российский НИИ гематологии и трансфузиологии ФМБА России, Санкт-Петербург
Капорская Т.С. к.м.н., заведующая отделением гематологии ГБУЗ Иркутская ордена "Знак Почета" областная клиническая больница, Иркутск,
Клясова Г.А. д.м.н., профессор, заведующая научно-клинической лабораторией микробиологии ФГБУ Гематологический Научный центр Минздрава России, Москва,
Константинова Т.С. ГБУЗ СО Областной гематологический центр Свердловской областной клинической больницы №1, Екатеринбург,
Кузьмина Л.А. к.м.н., заведующая научно-клиническим отделение трансплантации костного мозга ФГБУ Гематологический Научный центр Минздрава России, Москва,
Лапин В.А. к.м.н., заведующий отделением гематологии ГБУЗ ЯО Областная клиническая больница, Ярославль
Паровичникова Е.Н. д.м.н., заведующая научно-клиническим отделом химиотерапии гемобластозов, депрессий кроветворения и трансплантации костного мозга ФГБУ Гематологический Научный центр Минздрава России, Москва,
Савченко В.Г. академик, д.м.н., профессор, Генеральный директор ФГБУ Гематологический Научный центр Минздрава России, Москва,
Самойлова О.С. к.м.н., заведующая отделение гематологии ГБУЗ Нижегородской области Нижегородская областная клиническая больница им. Н.А.Семашко, Нижний Новгород,
Семочкин С.В. д.м.н., профессор, ФГБУ ФНКЦ детской гематологии, онкологии и иммунологии им.Д.Рогачева Минздрава России, Москва
Соколов А.Н. к.м.н., старший научный сотрудник научно-клинического отделения химиотерапии гемобластозов и депрессий кроветворения ФГБУ Гематологический Научный центр Минздрава России, Москва,
Троицкая В.В. к.м.н., заведующая научно-клиническим отделением химиотерапии гемобластозов и депрессий кроветворения ФГБУ Гематологический Научный центр Минздрава России, Москва,
Шатохин С.В. д.м.н., профессор, ГБОУ ВПО Ростовский государственный медицинский университет Минздрава России, Ростов-на-Дону
Конфликт интересов: авторы не имеют конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
-
Специалисты гематологи;
-
Специалисты онкологи;
-
Специалисты терапевты;
-
Специалисты акушеры-гинекологи;
-
Специалисты анестезиологи-реаниматологи;
-
Клинические фармакологи;
-
Студенты медицинских ВУЗов.
Методология сбора доказательств
Российская исследовательская группа по изучению ОЛ с 1992 г. провела 4 рандомизированных клинических исследования у больных ОМЛ в возрасте от 16 до 60 лет, и одно пилотное исследование по лечению ОМЛ у больных старше 60 лет, в которых принимали участие гематологические центры из более, чем 30 городов России. Результаты этих исследований неоднократно опубликованы и обсуждены на ежегодных рабочих совещаниях исследовательской группы. Кроме того, при создании национальных рекомендаций использован опыт и ряда федеральных гематологических центров.
Таким образом, итоги этих исследований и опыт по внедрению программной терапии ОМЛ в регионах РФ, а также заключения Европейских и Американских экспертных групп, были положены в основу настоящих рекомендаций.
Методы, использованные для сбора/селекции доказательств:
-
поиск публикаций в специализированных периодических печатных изданиях с импакт-фактором более 0,3;
-
поиск в электронных базах данных.
Методы, использованные для анализа доказательств:
-
обзоры опубликованных мета-анализов;
-
систематические обзоры с таблицами доказательств.
Методы, использованные для определения качества и силы доказательств:
-
консенсус экспертов;
-
оценка уровня доказательности (табл.14).
Методология разработки рекомендаций
При отборе публикаций, как источников доказательств, использованная в каждом исследовании методология изучалась для того, чтобы убедиться в соответствии ее принципам доказательной медицины. Результат изучения влиял на уровень доказательности, присваиваемый публикации, что в свою очередь влияет на силу, вытекающих из нее рекомендаций.
Методологическое изучение фокусировалось на особенностях дизайна исследования, которые оказывали существенное влияние на качество результатов и выводов.
С целью исключения влияния субъективных факторов каждое исследование оценивалось независимо, как минимум двумя независимыми членами авторского коллектива. Различия в оценке обсуждались на совещаниях рабочей группы авторского коллектива данных рекомендаций.
На основании анализа доказательств последовательно были разработаны разделы клинических рекомендаций с оценкой силы в соответствии с рейтинговой схемой рекомендаций.
Методы, использованные для формулирования рекомендаций:
-
консенсус экспертов;
-
оценка значимости рекомендаций в соответствии с уровнем доказательности (см. табл. 1).
Индикаторы доброкачественной клинической практики (Good Practice Points – GPPs):
Доброкачественная практика рекомендаций основывается на квалификации и клиническом опыте авторского коллектива.
Методология валидизации рекомендаций
Методы валидизации рекомендаций:
внутренняя экспертная оценка;
внешняя экспертная оценка.
Уровни доказательств.
Уровень А. Доказательства основаны на данных многих рандомизированных клинических исследований или мета-анализов, систематических обзорах.
Уровень В. Доказательства основаны на данных одного рандомизированного клинического исследования или многих нерандомизированных исследований.
Уровень С. Согласованные мнения экспертов и (или) немногочисленные исследования, ретроспективные исследования, регистры.
Уровень D. Мнение экспертов.
Самый высокий уровень рекомендаций – А.
Таблица П1 Достоверность доказательств
|
Достоверность рекомендаций |
Уровень достоверности |
Мероприятие |
|
A |
1а |
Систематический обзор РКИ |
|
1b |
РКИ |
|
|
B |
2а |
Систематический обзор когортных исследований |
|
2b |
Когортное исследование |
|
|
За |
Систематический обзор "случай-контроль" исследований |
|
|
3b |
Исследование "случай-контроль" |
|
|
C |
4 |
Серия случаев |
|
D |
5 |
Мнение экспертов |
Приложение Б. Алгоритмы ведения пациента
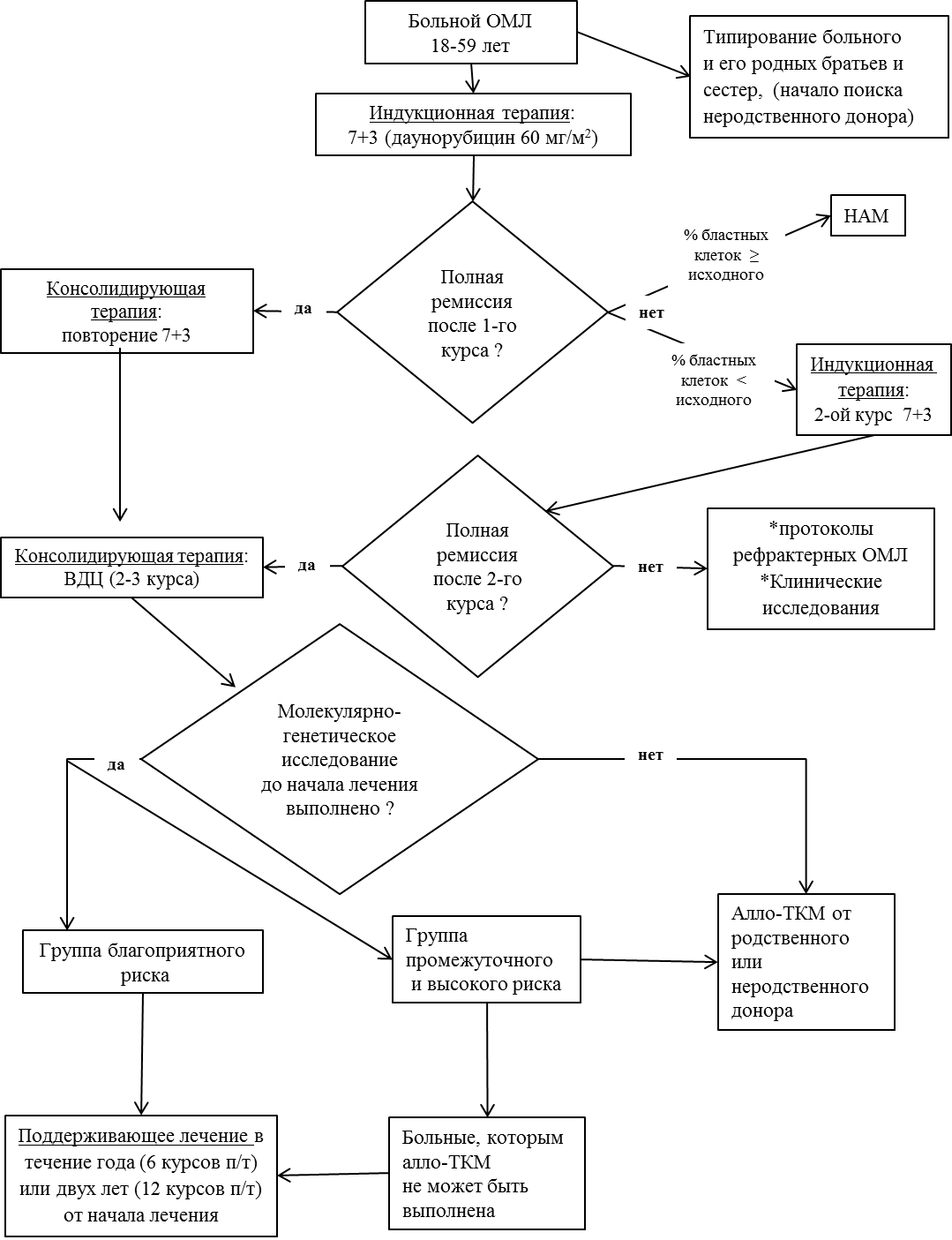
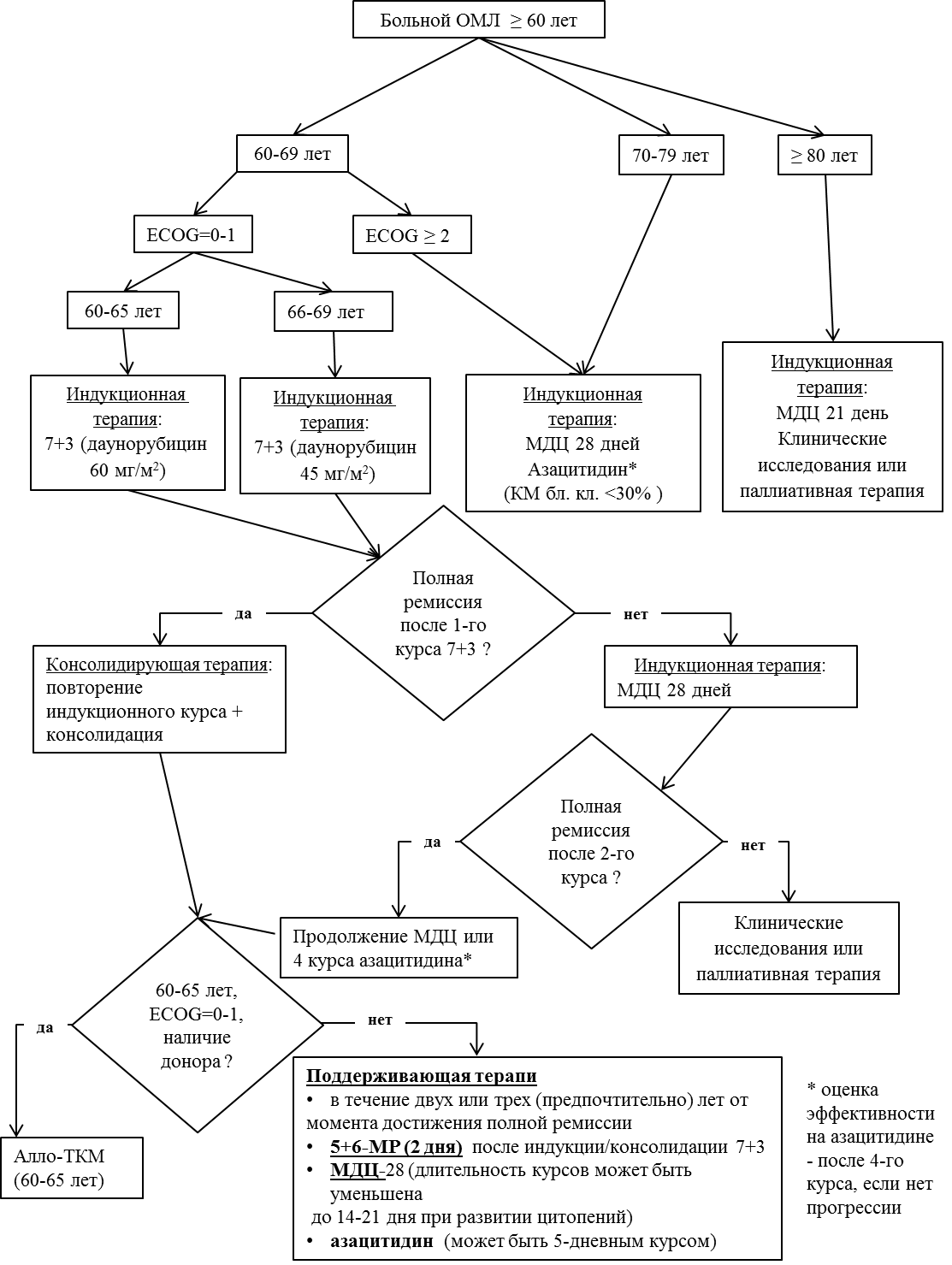
Приложение В. Информация для пациентов
Острый миелоидный лейкоз называется также, острым миелобластным лейкозом и острым нелимфобластным лейкозом. ОМЛ развивается тогда, когда возникает дефект ДНК в незрелых клетках костного мозга. Точная причина ОМЛ неизвестна. ОМЛ проявляется в любом возрасте и является наиболее частой формой острого лейкоза у взрослых. ОМЛ вызывает неконтролируемый рост «бластных», то есть незрелых, клеток крови и костного мозга, которые не могут нормально функционировать. Пациенты с ОМЛ имеют пониженное количество зрелых клеток крови всех типов: эритроцитов, тромбоцитов и лейкоцитов. В зависимости от типа клеток, на которые болезнь главным образом воздействует, ОМЛ делится на несколько видов. Точный диагноз ставится после исследования образцов крови и костного мозга. Выбор лечения при ОМЛ зависит от разновидности болезни и других факторов, таких как наличие и тип хромосомных нарушений. Симптомы ОМЛ также зависят от разновидности болезни. У пациентов с пониженным содержание эритроцитов проявляются классические симптомы анемии: быстрая утомляемость, одышка, бледный цвет лица. У пациентов с низким содержанием тромбоцитов могут возникать длительные кровотечения и образовываться синяки. Признаком изменения содержания лейкоцитов являются частые инфекции и боли в костях и суставах.
Лечение
Лекарственная терапия (химиотерапия)
Пациенты с ОМЛ почти всегда получают химиотерапию, которая начинается сразу после установления диагноза. Цель такого лечения, называемого индукционной терапией, добиться ремиссии и восстановить нормальное кроветворение. Ремиссия острого лейкоза – это нивелирование патологических проявлений процесса под воздействием противолейкозной терапии. На стадии терапии индукции обычно используются следующие препараты: даунорубицин и цитарабин. Такая химиотерапия очень интенсивна и влияет не только на злокачественные, но и на здоровые клетки крови, в результате чего пациенты, получающие индукционную терапию, могут страдать от различных побочных эффектов, таких как тошнота, слабость, повышенная чувствительность инфекциям. У большинства пациентов в течение нескольких недель после индукционной терапии восстанавливается нормальное кроветворение, и констатируется ремиссия ОМЛ. В этот момент принимается решение о применении того или иного метода дальнейшего лечения. Это может быть продолжение химиотерапии с целью консолидации (закрепления) ремиссии, направленное на более полное уничтожению лейкозных клеток и поддерживающая терапия. Другой метод лечения – проведение аллогенной трансплантации костного мозга.
Трансплантация гемопоэтических стволовых клеток
В качестве источника гемопоэтических стволовых клеток (незрелые клетки - предшественницы кроветворения, из которых в впоследствии развиваются три типа клеток крови: лейкоциты, эритроциты и тромбоциты), в настоящее время, используют костный мозг, пуповинную кровь или периферическую кровь донора. Какой бы источник не использовался, стволовые клетки вводятся в организм пациента после проведения высокодозной химиотерапии или лучевой терапии, призванной полностью уничтожить лейкозные клетки больного. Предтрансплантационная химиотерапия уничтожает также иммунную систему пациента, которую вводимые клетки донора должны восстановить.
Аллогенная трансплантация требует наличия родственного или неродственного донора, гистосовместимого с пациентом по системе HLA. В качестве родственного донора обычно выступает родной брат или сестра. Если родственного донора не найдено, врач проводит поиск в базах данных Российских и/или Зарубежных Регистров доноров. Независимо от того, родственный или неродственный донор найден, процедура трансплантации одна и та же: производится забор гемопоэтических стволовых клеток донора, которые затем внутривенно вводятся пациенту.
Приложение Г.
Таблица 1 Молекулярно-генетическая классификация ОМЛ
|
Цитогенетическая группа риска |
Мутации |
Итоговая группа риска |
|
|
Благоприятная t(15;17), (t(8;21)(q22;q22); inv(16)(p13.1q22) или t(16;16)(p13.1;q22) |
Любые |
|
Благоприятная |
|
Промежуточная |
FLT3-ITD-негативность |
Есть мутации генов NPM1 и IDH1 или IDH2 |
|
|
Нормальный кариотип |
FLT3-ITD-негативность |
Нет мутаций: ASXL1, MLL-ITD, PHF6, ТЕТ2 |
Промежу-точная |
|
t(9;11)(p22;q23); Цитогенетические повреждения, не классифицируемые |
FLT3-ITD-негативность или позитивность |
Есть мутации CEBPA |
|
|
как благоприятные или неблагоприятные |
FLT3-ITD-позитивность |
Нет мутаций: MLL-ITD, ТЕТ2 и DNMT3A и отсутствие трисомии 8 |
|
|
|
FLT3-ITD-негативность |
Есть мутации: ASXL1, MLL-ITD, PHF6, ТЕТ2 |
Неблаго-приятная |
|
|
FLT3-ITD-позитивность |
Есть мутации: MLL-ITD, ТЕТ2 и DNMT3A или есть трисомия 8, без мутаций в гене CEBPA |
|
|
Неблагоприятная
inv(3)(q21q26.2) или t(3;3)(q21;q26.2); t(6;9)(p23;q34); t(v;11)(v;q23); -5 или del(5q); -7; аберрации (17р); комплексный кариотип, моносомный кариотип |
Любые |
|
|
Примечание. Серым цветом выделена итоговая благоприятная группа риска;
белым – итоговая промежуточная группа риска; желтым – итоговая неблагоприятная группа риска.
Таблица 2. Бальная оценка по шкале при оценке клеточной линии по данным иммунофенотипирования
|
Баллы |
Антигены |
||
|
В-клеточной линии |
Т-клеточной линии |
миелоидной линии |
|
|
2 |
CD79 |
CD3цит/мем |
Анти –МРО |
|
цит IgM |
Анти TCR ?/? |
(антилизоцим) |
|
|
Цит CD22 |
Анти TCR ?/? |
|
|
|
1 |
CD19 |
CD2 |
CD13 |
|
CD10 |
CD5 |
CD33 |
|
|
CD20 |
CD8 |
CDw65 |
|
|
|
CD10 |
CD117 |
|
|
0,5 |
TdT |
TdT |
CD14 |
|
CD24 |
CD7 |
CD15 |
|
|
|
CD1a |
CD64 |
Таблица 3. Экспрессия поверхностно-клеточных и цитоплазматических маркеров для диагностики ОМЛ и ОЛ смешанного фенотипа
|
Диагноз |
Маркеры |
Антигены кластеров дифференцировки |
|
ОМЛ |
Предшественников |
CD34, CD38, CD117, CD133, HLA-DR |
|
гранулоцитов |
СD13, CD15, CD16, CD3, сМРО |
|
|
Моноцитов |
Неспецифическая эстераза (NSE), CD11c, CD14, CD64, лизоцим, CD4, CD11b, CD36, NG2 гомолог* (не используется в РФ) |
|
|
Мегакариоцитов |
CD41 (гликопротеин IIb/IIIa), CD61, (гликопротеин IIIa), CD42, (гликопротеин 1b) |
|
|
Эритроидные |
CD235a (гликофорин A) |
|
|
Диагноз ОЛ смешанного фенотипа |
Миелоидная линия |
MPO или подтверждение моноцитарной дифференцировки (как минимум два из следующих: NSE, CD11c, CD14, CD64, лизоцим) |
|
B-линия |
CD19 (сильная) + как минимум 1 из следующих: CD79a, cCD22, CD10, или CD19 (слабая) + как минимум 2 из следующих: CD79a, cCD22, CD10 |
|
|
T-линия |
cCD3, или поверхностный CD3 |
Примечание * -- в большинстве случаев ОМЛ с аномалией 11q23 обнаруживают экспрессию NG2-гомолога (кодируемого геном CSPG4), детектируемую с помощью моноклонального антитела 7.1.
Таблица 4. Варианты курсов химиотерапии (индукция и консолидация ремиссии).
|
Программа индукции/ консолидации |
Препараты |
|
7+3(1) |
Цитарабин 100 мг/м2 в/в 2 раза в сутки в 1--7-й дни
|
|
7+3 (2) |
Цитарабин 200 мг/м2 в/в круглосуточно, в 1--7-й дни
|
|
7+3 + VP-16 |
Цитарабин 100 мг/м2 в/в 2 раза в сутки в 1--7-й дни Даунорубицин 45 мг/м2 в/в 1 раз в день в 1--3-й дни Этопозид 120 мг/м2 в/в 1 раз в день в 17--21-й дни |
|
ADE |
Цитарабин 100 мг/м2 в/в 2 раза в сутки 1-10 дни Даунорубицин 50 мг/м2 в/в 1 раз в день 1-3 дни Этопозид 100 мг/м2 в/в 1 раз в день 1- 5 дни |
|
7 + 3 + 7 |
Цитарабин 100 мг/м2 в/в 2 раза в день в 1--7-й дни Даунорубицин 45 мг/м2 в/в 1 раз в день в 1--3-й дни Этопозид 75 мг/м2 в/в 1 раз в день в 1--7-й дни |
|
ICE |
Идарубицин 12 мг/м2 в/в 1 раз в день в 1, 3, 5-й дни Цитарабин 100 мг/м2 в/в 24-часовая инфузия в 1--7-й дни Этопозид 100 мг/м2 в/в 1 раз в день в 1--3-й дни |
|
IVA (1) |
Идарубицин 12 мг/м2 в/в 1 раз в день во 2, 4, 6-й дни Этопозид 100 мг/м2 в/в раз в день в 3--7-й дни Цитарабин 100 мг/м2 в/в 24-часовая инфузия в 1--7-й дни |
|
IVA (2) |
Идарубицин 12 мг/м2 в/в 1 раз в день во 2, 4-й дни Этопозид 100 мг/м2 в/в 1 раз в день во 2--6-й дни Цитарабин 100 мг/м2 в/в 24-часовая инфузия в 1--6-й дни |
|
MAV |
Митоксантрон 10 мг/м2 в/в 1 раз в день в 4--8-й дни Цитарабин 100 мг/м2 в/в 24-часовая инфузия в 1--8-й дни Этопозид 100 мг/м2 в/в 1 раз в день в 4--8-й дни |
|
FLAG-IDA |
Г-КСФ 5 мкг/кг со дня 0 – до выхода из цитопении Флударабин 30 мг/м2 30-минутная инфузия в 1--4-й дни Цитарабин 1000 мг/м2 в/в 4-часовая инфузия после флударабина в 1--4-й дни Идарубицин 8 мг/м2 в/в 1 раз в день в 1, 3-й дни |
|
HidAC-3-7 |
Цитарабин 3 г/м2 в/в 2 раза в сутки в 1, 3, 5, 7-й дни Даунорубицин 45 мг/м2 в/в 1 раз в день в 1-3-й дни Этопозид 75 мг/м2 в/в 1 раз в день в 1-7-й дни |
|
Азацитидин |
Азацитидин 75 мг/м2 7 дней, интервал 21 день |
|
Dac-Ida-Ara-C |
Децитабин 20 мг/м2 в/в 1 раз в день, 1-3 дни Идарубицин 3 мг/м2 в/в струйно, 1 раз в день, 4-8 дни (гипоплазия/бластные клетки в КМ на 5-ый день <5%) 4-10 дни (бластные клетки в КМ на 5-ый день >5%) Цитарабин 15 мг/м2 п/к 2 раза в сутки 4-10 дни (гипоплазия/ бластные клетки в КМ на 5-ый день <5%) 4-17 дни (бластные клетки в КМ на 5-ый день >5%) |
|
Aza-Ida-Ara-C |
Азацитидин 75 мг/м2 п/к 1 раз в день, 1-3 дни Идарубицин 3 мг/м2 в/в струйно, 1 раз в день, 4-8 дни (гипоплазия/бластные клетки в КМ на 5-ый день <5%) 4-10 дни (бластные клетки в КМ на 5-ый день >5%) Цитарабин 15 мг/м2 п/к 2 раза в сутки 4-10 дни (гипоплазия/ бластные клетки в КМ на 5-ый день <5%) 4-17 дни (бластные клетки в КМ на 5-ый день >5%) |
|
МДЦ |
Цитарабин 10 мг/м2 п/к 2 раза в сутки 28 дней |
Таблица 5. Курсы консолидации, используемые разными исследовательскими группами
|
Программа консолидации |
Препарат |
|
НD-ARA-С |
Цитарабин 3 г/м2 2 раза в день в 1, 3, 5-й дни |
|
MidAC |
Цитарабин 1 г/м2 в/в 2 раза в день в 1--3-й дни Митоксантрон 10 мг/м2 в/в 1 раз в день в 1--5-й дни |
|
НАМ (1) |
Цитарабин 3 г/м2 в/в 2 раза в день в 1--3-й дни Митоксантрон 10 мг/м2 в/в 1 раз в день в 3--5-й дни |
|
НАМ (2) |
Цитарабин 3 г/м2 в/в 3-часовая инфузия 1 раз в день в 1--3-й дни Митоксантрон 12 мг/м2 в/в 1 раз в день во 2 и 3-й дни |
|
A-НАМ |
Цитарабин 1 г/м2 в/в 1 раз в день 12-часовая инфузия в 1--3-й дни Митоксантрон 12 мг/м2 в/в 1 раз в день в 2--3-й дни ATRA 45 мг/м2 3-5 дни, затем 15 мг/м2 в 6--28-й дни |
|
ID-Ara-C/DNR |
Цитарабин 3 г/м2 в/в 2 раза в день 2-часовая инфузия 1-4 дни Даунорубицин 45 мг/м2 в/в 1 раз в день в 3-5-й дни |
|
НАD |
Цитарабин 3 г/м2 в/в 2 раза в день 2-часовая инфузия в 1--5-й дни Даунорубицин 45 мг/м2 в/в 1 раз в день в 3-5-й дни |
|
H-MAC |
Цитарабин 3 г/м2 в/в 2-часовая инфузия 2 раза в сутки в 1--6-й дни Митоксантрон 10 мг/м2 в/в 1 раз в день в 4-6-й дни |
|
I-MAC |
Цитарабин 1 г/м2 в/ в 2-часовая инфузия 2 раза в сутки в 1--6-й дни Митоксантрон 10 мг/м2 в/в 1 раз в день в 4-6-й дни |
|
FA |
Флударабин 30 мг/м2 30-минутная инфузия в 1-5-й дни Цитарабин 1,4 г/м2 в/ в 4-часовая инфузия через 3,5 часа после флударабина в 1-5-й дни |
|
FLARIDA |
Флударабин 30 мг/м2 30-минутная инфузия в 1--4-й дни Цитарабин 500-1000 мг/м2 в/в 4-часовая инфузия после флударабина в 1--4-й дни Идарубицин 6-8 мг/м2 в/в 1 раз в день в 1, 3-й дни |
Таблица 6. Курсы поддерживающего лечения
|
Программа |
Препарат |
|
5 + 6-МП (2) |
Цитарабин 100 мг/м2 в/в 2 раза в день в 1--5-й дни, или 50 мг/м2 подкожно 2 раза в день в 1--5-й дни 6-Меркаптопурин 60 мг/м2 в сутки в 2 приема внутрь в 1--5-й дни |
|
5 + ЦФ (1) |
Цитарабин 100 мг/м2 в/в 2 раза в день в 1--5-й дни, или 100 мг/м2 подкожно 2 раза в день в 1--5-й дни Циклофосфан 1000 мг/м2 в 3-й день |
|
5 + ЦФ (2) |
Цитарабин 100 мг/м2 в/в 2 раза в день в 1--5-й дни, или 50 мг/м2 подкожно 2 раза в день в 1--5-й дни Циклофосфан 650 мг/м2 в 1-й день |
|
5 + 6-МП (1) |
Цитарабин 100 мг/м2 в/в 2 раза в день в 1--5-й дни, или 100 мг/м2 подкожно 2 раза в день в 1--5-й дни 6-Меркаптопурин 60 мг/м2 в сутки в 2 приема внутрь в 1--5-й дни |
|
Азацитидин |
Азацитидин 75 мг/м2 7 дней, интервал 21 день |
|
Dac -Ara-C |
Децитабин 20 мг/м2 в/в 1 раз в день, 1-3 дни Цитарабин 15 мг/м2 п/к 2 раза в сутки 4-17 дни |
|
Aza -Ara-C |
Азацитидин 75 мг/м2 п/к 1 раз в день, 1-3 дни Цитарабин 15 мг/м2 п/к 2 раза в сутки 4-17 дни |
|
МДЦ |
Цитарабин 10 мг/м2 п/к 2 раза в сутки 21-28 дней |
Таблица 7. Синтетические показания к алло-ТКМ в первой полной ремиссии ОМЛ в зависимости от молекулярно-генетических, клинических характеристик ОМЛ и риска трансплантационной летальности
|
Группа интегрированного риска |
Определение группы риска |
Риск развития рецидива в зависимости от выполнения |
Бальная оценка прогноза летальности, не связанной с рецидивом, которая позволяет считать алло-ТКМ предпочтительным вариантом консолидации |
|||
|
ХТ или ауто-ТКМ, % |
алло-ТКМ, % |
шкала ЕВМТ |
шкала HCT-CI |
риск смерти, не связанный с рецидивом, % |
||
|
Благоприятный |
|
35--40 |
15--20 |
<1 |
<1 |
10--15 |
|
Промежуточный |
>20х109/л
|
50--55 |
20--25 |
<2 |
< 2 |
< 20--25 |
|
Плохой |
|
70--80 |
30--40 |
< 3--4 |
< 3--4 |
< 30 |
|
Очень плохой |
Моносомный кариотип Аномалии 3q26 Гиперэкспрессия Evi-1 |
>90 |
40--50 |
< 5 |
< 5 |
< 40 |
Таблица 8. Факторы риска, ассоциированные с трансплантационной летальностью
|
Предтрансплантационный показатель |
Перитрансплантационный показатель |
Посттрансплантационный показатель |
|
Благоприятный фактор: родственный HLA-совместимый донор более короткий срок между диагностикой ОЛ и ТКМ принадлежность к белой расе |
Немиелоаблативное кондиционирование Источник стволовых клеток (костный мозг или периферическая кровь) Т-деплеция трансплантата |
Ранняя иммунная реконституция |
|
Неблагоприятный фактор: старший возраст реципиента пол донора и реципиента коморбидность ЦМВ-серостатус полиморфизм генов цитокинов неродственный донор HLA-несовместимость физикальный статус рефрактерная лейкемия ОМЛ, ассоциированный с предшествующей ХТ |
Миелоаблативный режим кондиционирования Альтернативный источник трансплантата (пуповинная кровь) |
Тяжелая острая РТПХ (III--IV) Персистирующая хроническая РТПХ, экстенсивной формы |
Таблица 9.Основные лекарственные препараты, используемые в лечении ОМЛ
- азацитидин**, 100 мг, флакон;
- даунорубицин**, порошок лиофилизированный для приготовления раствора для инъекций или раствор для внутривенного введения 20мг;
- децитабин, 50 мг, флакон;
- идарубцин**, 5 мг, флакон;
- меркаптопурин**, таблетка 50 мг;
- митоксантрон**, 10 мг, флакон;
- цитарабин**, порошок лиофилизированный для приготовления раствора для инъекций 100 мг, 1000 мг.
- филграстим**, раствор для инъекций 0,3мг/мл, 1 мл;
- ондансетрон**, раствор для инъекций 8 мг/4мл.
- гидроксимочевина**, таблетка 500 мг.
- аллопуринол **, таблетка 100 мг
- флударабин**, концентрат для приготовления раствора для внутривенного введения 50 мг;
- этопозид** концентрат для приготовления раствора для инфузий 100 мг;
- третиноин** капсулы 10 мг;
- циклофосфамид** порошок для приготовления раствора для внутривенного введения 200 мг.

