Ликсумия - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер:
ЛП 002737
Торговое наименование препарата:
Ликсумия®
Международное непатентованное наименование:
ликсисенатид.
Лекарственная форма:
раствор для подкожного введения.
Состав:
| Компоненты | Раствор 0,05 мг/мл (10 мкг/доза) |
Раствор 0,1 мг/мл (20 мкг/доза) |
||
| Содержание в 1 мл |
Содержание в 1 дозе |
Содержание в 1 мл |
Содержание в 1 дозе |
|
| Активное вещество: | ||||
| Ликсисенатид | 0,05 мг | 0,01 мг | 0,1 мг | 0,02 мг |
| Вспомогательные вещества: | ||||
| Глицерол 85 % | 18,0 мг | 3,6 мг | 18,0 мг | 3,6 мг |
| Натрия ацетата тригидрат | 3,5 мг | 0,70 мг | 3,5 мг | 0,70 мг |
| Метионин | 3,0 мг | 0,60 мг | 3,0 мг | 0,60 мг |
| Метакрезол | 2,7 мг | 0,54 мг | 2,7 мг | 0,54 мг |
| 1 М раствор хлористоводородной кислоты или 1 М раствор натрия гидроксида |
до рН 4,5 | до рН 4,5 | до рН 4,5 | до рН 4,5 |
| Вода для инъекций | до 1 мл | до 0,2 мл | до 1,0 мл | до 0,2 мл |
Описание:
Прозрачная бесцветная жидкость.
Фармакотерапевтическая группа:
гипогликемическое средство - глюкагоноподобного полипептида рецепторов агонист.
Код АТХ:
А10ВХ10.
Фармакологические свойства
Фармакодинамика
Механизм действия
Ликсисенатид является сильным и селективным агонистом рецепторов глюкагоноподобного пептида-1 (ГПП-1). Рецептор ГПП-1 является мишенью для нативного ГПП-1, эндогенного гормона внутренней секреции, который потенцирует глюкозозависимую секрецию инсулина бета-клетками панкреатических островков. Действие ликсисенатида связано с его специфическим взаимодействием с рецепторами ГПП-1, приводящим к увеличению внутриклеточного содержания циклического аденозинмонофосфата (цАМФ). Ликсисенатид стимулирует секрецию инсулина бета-клетками панкреатических островков в ответ на гипергликемию. При снижении концентрации глюкозы в крови до нормальных значений стимуляция секреции инсулина прекращается, что уменьшает риск развития гипогликемии. При гипергликемии ликсисенатид одновременно подавляет секрецию глюкагона, однако при этом сохраняется защитная реакция секреции глюкагона в ответ на гипогликемию.
Показана тенденция к инсулинотропной активности ликсисенатида, включая увеличение биосинтеза инсулина и стимуляцию бета-клеток панкреатических островков у животных. Ликсисенатид замедляет опорожнение желудка, уменьшая за счет этого скорость повышения концентрации глюкозы в крови после приема пищи. Влияние на опорожнение желудка может также способствовать снижению массы тела.
Фармакодинамические эффекты
При введении 1 раз в сутки пациентам с сахарным диабетом 2 типа ликсисенатид улучшает гликемический контроль за счет быстро развивающегося после его введения и продолжительного снижения концентрации глюкозы в крови после еды и натощак.
Этот эффект ликсисенатида на концентрацию глюкозы в крови после еды был подтвержден в 4-недельном исследовании, в котором проводилось сравнение применения ликсисенатида с применением лираглутида 1,8 мг 1 раз в сутки. Ликсисенатид в дозе 20 мкг 1 раз в сутки продемонстрировал большее снижение площади под кривой концентрации глюкозы в крови после стандартного приема пищи, по сравнению с применением лираглутида 1,8 мг один раз в сутки: уменьшение, по сравнению с исходным значением AUC0:30-4:30 ч (площади под кривой «концентрация-время») для концентрации глюкозы в крови после стандартного приема пищи составляло: -227,25 ч*мг/дл (-12,61 ч*ммоль/л) в группе ликсисенатида и -72,83 ч*мг/дл (-4,04 ч*ммоль/л) в группе лираглутида.
Клиническая эффективность и безопасность
Влияние препарата Ликсумия® на гликемический контроль было изучено в 6-ти рандомизированных двойных слепых, плацебо-контролируемых клинических исследованиях и одном рандомизированном, открытом, контролируемом активным препаратом (эксенатидом) исследовании, в которые, в общей сложности, вошло 3825 пациентов с сахарным диабетом 2 типа (ликсисенатид применялся у 2445 пациентов (48,2 % мужчин и 51,8 % женщин). 768 пациентов (447 пациентов были рандомизированы для приема ликсисенатида) были в возрасте >65 лет и 103 пациента (57 пациентов были рандомизированы для приема ликсисенатида) были в возрасте >75 лет.
Завершенные клинические исследования фазы III показали, что 90 % пациентов к концу 24-недельного периода лечения продолжали лечение препаратом Ликсумия® в поддерживающей дозе 20 мкг один раз в сутки.
Влияние на гликемический контроль
При применении препарата Ликсумия® отмечено большее, по сравнению с плацебо, снижение показателя гликозилированного гемоглобина (HbA1C) в крови (независимо от сопутствующего лечения). Кроме этого, препарат Ликсумия® при однократном введении в течение суток показал не меньшее снижение показателя HbAic, чем эксенатид при двукратном введении в течение суток. Это влияние на снижение показателя HbA1C сохранялось в долгосрочных исследованиях до 2-х лет.
Снижение показателя НЬА1C было достоверным при ежедневном однократном введении препарата Ликсумия®, как утром, так и вечером.
Добавление ликсисенатида к лечению пероральными гипогликемическими препаратами
Препарат Ликсумия® в сочетании с метформином, пероральным гипогликемическим препаратом группы сульфонилмочевины, или с комбинациями этих препаратов в конце 24-недельного периода лечения, по сравнению с плацебо, показал клинически и статистически значимое снижение показателя HbA1C, концентрации глюкозы в крови натощак и через 2 ч после еды (проба со стандартной пищевой нагрузкой).
Добавление ликсисенатида к монотерапии метформином
В плацебо-контролируемых исследованиях добавление ликсисенатида к метформину приводило к снижению показателя HbA1C на 0,83 % и снижению такового на 0,42 % при добавлении плацебо. Процент пациентов, достигших снижения показателя НЬА1C до <7 %, составлял 43 % в группе ликсисенатида и 24 % в группе плацебо.
В контролируемом активным препаратом (эксенатид) исследовании в конце основного 24-недельного периода лечения однократное в течение суток введение препарата Ликсумия® показало не меньшее снижение показателя HbA1C, по сравнению с двукратным в течение суток введением эксенатида (соответственно, на 0,79 % и 0,96 %,); при этом наблюдался практически одинаковый процент пациентов, достигших снижения показателя HbA1C до <7 %: 48,5 % в группе ликсисенатида и 49,8 % в группе эксенатида.
Добавление ликсисенатида к лечению одним из пероралъных гипогликемических препаратов группы сульфонилмочевины в монотерапии и в сочетании с метформином
Добавление ликсисенатида к лечению одним из пероральных гипогликемических препаратов группы сульфонилмочевины в монотерапии и в сочетании с метформином приводило к снижению показателя НЬА1C на 0,85 % по сравнению с таковым при добавлении плацебо, составляющим -0,10%. Процент пациентов, достигших снижения показателя HbAic до <7 %, составлял 36,4 % при добавлении ликсисенатида и 13,5 % при добавлении плацебо.
Добавление ликсисенатида к комбинированной терапии, включающей базальный инсулин
Препарат Ликсумия® при его совместном применении с базальным инсулином в монотерапии, или с комбинацией базального инсулина с метформином, или с комбинацией базального инсулина с пероральным гипогликемическим препаратом группы сульфонилмочевины вызывал статистически значимое снижение показателя HbA1C и концентрации глюкозы через 2 ч после стандартного приема пищи по сравнению с плацебо. К концу основного 24-недельного периода лечения в группе препарата Ликсумия®, по сравнению с группой плацебо, наблюдалось большее снижение суточной дозы инсулина, по сравнению с его дозами до добавления к лечению препарата Ликсумия®.
При добавлении ликсисенатида к лечению базальным инсулином в монотерапии или в комбинации с метформином наблюдалось снижение показателя НbА1C на 0,74 % против -0,38 % при добавлении плацебо, а при добавлении ликсисенатида к лечению базальным инсулином в монотерапии или в комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины наблюдалось снижение показателя HbA1C на 0,77 % против -0,11 % при добавлении плацебо.
Влияние на концентрацию глюкозы в плазме крови натощак
В плацебо-контролируемых исследованиях средние значения снижения концентрации глюкозы в плазме крови натощак, достигаемого при лечении препаратом Ликсумия® к концу 24-недельного периода лечения, находились в диапазоне от -0,42 ммоль/л до -1,19 ммоль/л.
Влияние на постпрандиальную (после приема пищи) концентрацию глюкозы в крови
Лечение препаратом Ликсумия®, независимо от сопутствующей терапии, приводило к статистически превосходящему эффект плацебо снижению 2-часовой постпрандиальной (определяемой через 2 ч после стандартного приема пищи) концентрации глюкозы в крови. К концу 24-недельного периода лечения во всех исследованиях, в которых проводилось определение постпрандиальной концентрации глюкозы в крови, это снижение 2-часовой постпрандиальной концентрации глюкозы в крови находилось в диапазоне от -4,51 ммоль/л до -7,96 ммоль/л (по сравнению значениями 2-часовой постпрандиальной концентрации глюкозы в крови до применения препарата Ликсумия®); у 26,2 % - 46,8 % пациентов наблюдались 2-часовые постпрандиальные концентрации глюкозы в крови ниже 7,8 ммоль/л.
Влияние на массу тела
Во всех контролируемых исследованиях лечение препаратом Ликсумия® в комбинации с метформином, базальным инсулином и/или пероральным гипогликемическим препаратом группы сульфонилмочевины к концу основного 24-недельного периода лечения приводило к среднему снижению массы тела до -2,96 кг, которое сохранялось в долгосрочных исследованиях до 2-х лет.
Снижение массы тела не зависело от возникновения тошноты и рвоты.
Влияние на функцию бета-клеток панкреатических островков
Препарат Ликсумия® улучшает функцию бета-клеток панкреатических островков, определяемую с помощью гомеостатической модели для оценки функции бета-клеток (НОМА-ß).
У пациентов с сахарным диабетом 2 типа (n=20) после однократного введения препарата Ликсумия® было продемонстрировано восстановление первой фазы секреции инсулина и улучшение второй фазы секреции инсулина в ответ на внутривенное болюсное введение глюкозы.
Влияние на частоту сердечных сокращений (ЧСС)
В плацебо контролируемых клинических исследованиях III фазы не наблюдалось увеличения средних значений ЧСС.
В 4-недельном клиническом исследовании, по сравнению с лираглутидом в группе ликсисенатида (20 мкг 1 раз в сутки), ЧСС уменьшалось в среднем на 3,6 удара в минуту, а в группе лираглутида (1,8 мг 1 раз в сутки) ЧСС уменьшалось на 5,3 удара в минуту.
Влияние на артериальное давление (АД)
В плацебо-контролируемых исследованиях III фазы наблюдалось снижение средних значений систолического и диастолического АД на 2,1 мм рт. ст. и на 1,5 мм рт. ст., соответственно.
Фармакокинетика
Абсорбция После подкожного введения ликсисенатида пациентам с сахарным диабетом 2 типа скорость его абсорбции является высокой и не зависит от введенной дозы. Независимо от дозы и того, вводился ли ликсисенатид однократно или ежедневно многократно, у пациентов с сахарным диабетом 2 типа медиана времени достижения максимальной концентрации ликсисенатида в крови (tmax) составляет 1-3,5 ч. Отсутствуют клинически значимые различия в скорости абсорбции ликсисенатида, когда он вводится подкожно в область живота, область бедра или область плеча.
Распределение
Ликсисенатид имеет умеренную степень связи с белками крови у человека (55 %). Независимо от вводимой дозы, объем распределения после подкожного введения ликсисенатида у пациентов с сахарным диабетом 2 типа составляет 90-140 л после однократного введения и 90-120 л при повторном введении (в состоянии достижения равновесной концентрации ликсисенатида в крови).
Метаболизм
Как пептид, ликсисенатид выводится с помощью гломерулярной фильтрации с последующей канальцевой реабсорбцией и метаболической деградацией, приводящей к образованию более мелких пептидов и аминокислот, которые повторно вовлекаются в белковый обмен.
Выведение
После повторного введения пациентам с сахарным диабетом 2 типа среднее значение периода полувыведения (t½) обычно находилось в диапазоне 1,5-4,5 ч, и среднее значение клиренса находилось в диапазоне 20-67 л/ч (в состоянии достижения равновесной концентрации ликсисенатида в крови).
Особые группы пациентов
Половая принадлежность
По данным анализа популяционных фармакокинетических данных половая принадлежность не влияет на фармакокинетику ликсисенатида.
Пациенты пожилого возраста
По данным анализа популяционных фармакокинетических показателей у пациентов с сахарным диабетом 2 типа и анализа фармакокинетических исследований, проведенных у лиц пожилого возраста без сахарного диабета, возраст не оказывает клинически значимого воздействия на фармакокинетику ликсисенатида.
Этническая принадлежность
По данным фармакокинетических исследований, проведенных у лиц европеоидной расы, японцев и китайцев, этническая принадлежность не оказывает клинически значимого эффекта на фармакокинетику ликсисенатида.
Пациенты с печеночной недостаточностью
Так как ликсисенатид выводится, главным образом, почками, не проводилось никаких фармакокинетических исследований у пациентов с острым или хроническим нарушением функции печени. Не ожидается, что нарушение функции печени способно повлиять на фармакокинетику ликсисенатида.
Пациенты с почечной недостаточностью
Не наблюдалось значимых различий в средних значениях клиренса, максимальной концентрации в крови (Сmах) и площади под фармакокинетической кривой «концентрация-время» (AUC) ликсисенатида при нормальной функции почек и при почечной недостаточности легкой степени. При увеличении степени тяжести недостаточности средние значения Сmах и AUC увеличивались.
Показания к применению
Сахарный диабет 2 типа у взрослых для достижения гликемического контроля у пациентов, сахарный диабет которых не контролируется проводимой гипогликемической терапией.
Препарат Ликсумия® показан в комбинации со следующими пероральными гипогликемическими лекарственными средствами:
- метформином,
- пероральным гипогликемическим препаратом группы сульфонилмочевины,
- комбинацией этих лекарственных средств.
Препарат Ликсумия® показан в комбинации с базальным инсулином:
- в монотерапии,
- в комбинации с метформином,
- в комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины.
Противопоказания
- Гиперчувствительность к активному веществу или любому из вспомогательных веществ препарата.
- Беременность.
- Период грудного вскармливания.
- Сахарный диабет 1 типа.
- Диабетический кетоацидоз.
- Тяжелые заболевания желудочно-кишечного тракта, включая гастропарез.
- Тяжелая почечная недостаточность (клиренс креатинина менее 30 мл/мин).
- Дети и подростки до 18 лет.
С осторожностью
При панкреатите в анамнезе.
Применение при беременности и в период грудного вскармливания
Беременность
Отсутствует достаточное количество данных по применению препарата Ликсумия® у беременных женщин. Исследования, проведенные у животных, продемонстрировали эмбрио- и фетотоксическое действие. Потенциальный риск применения препарата Ликсумия® во время беременности у человека неизвестен. Применение препарата Ликсумия® во время беременности противопоказано. Во время беременности рекомендуется применение инсулина. Если пациентка планирует беременность, или у нее диагностирована беременность, лечение препаратом Ликсумия® следует прекратить.
Период грудного вскармливания
Неизвестно, проникает ли ликсисенатид в грудное молоко. Применение препарата Ликсумия® противопоказано во время периода грудного вскармливания (в связи с отсутствием опыта применения).
Способ применения и дозы
Дозы
Начальная доза составляет 10 мкг препарата Ликсумия® один раз в сутки в течение 14 дней.
Затем доза препарата Ликсумия® должна быть увеличена до 20 мкг один раз в сутки. Эта доза является поддерживающей.
Когда препарат Ликсумия® добавляется к уже проводимой терапии метформином, прием метформина может быть продолжен без изменения его дозы.
Когда препарат Ликсумия® добавляется к уже проводимой терапии пероральным гипогликемическим препаратом группы сульфонилмочевины или к терапии комбинацией перорального гипогликемического препарата группы сульфонилмочевины и базального инсулина, для уменьшения риска развития гипогликемии можно рассмотреть вопрос о снижении дозы перорального гипогликемического препарата группы сульфонилмочевины или базального инсулина (см. раздел «Особые указания»).
Применение препарата Ликсумия® не требует специального мониторинга концентрации глюкозы в крови. Однако при применении его в комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины или базальным инсулином может потребоваться мониторинг концентрации глюкозы в крови или самоконтроль (контроль самим пациентом) концентрации глюкозы в крови для коррекции дозы перорального гипогликемического препарата группы сульфонилмочевины или базального инсулина.
Особые группы пациентов
Дети и подростки моложе 18 лет
В настоящее время безопасность и эффективность применения препарата Ликсумия® у пациентов моложе 18 лет не изучена.
Лица пожилого возраста
Не требуется коррекции дозы в зависимости от возраста пациента.
Пациенты с печеночной недостаточностью
Не требуется коррекции дозы у пациентов с печеночной недостаточностью.
Пациенты с почечной недостаточностью
Не требуется коррекции дозы у пациентов с легкой почечной недостаточностью (клиренс креатинина 50-80 мл/мин) и умеренной почечной недостаточностью (клиренс креатинина 30-50 мл/мин).
Отсутствует терапевтический опыт применения препарата Ликсумия® у пациентов с тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл/мин) или с терминальной стадией почечной недостаточности, в связи с чем применение препарата Ликсумия® у этой группы пациентов противопоказано.
Способ применения
Препарат Ликсумия® вводится 1 раз в сутки в пределах 1 ч до первого в течение дня приема пищи или в пределах 1 ч до вечернего приема пищи. В случае пропуска введения очередной дозы, ее следует ввести в пределах 1 ч до следующего приема пищи.
Препарат Ликсумия® вводится подкожно в область бедра, брюшной стенки или плеча.
Препарат Ликсумия® нельзя вводить внутривенно и внутримышечно.
До использования шприц-ручка Ликсумия® должна храниться в холодильнике при температуре 2-8°С в своей упаковке для того, чтобы защитить ее от воздействия света. После первого использования шприц-ручка Ликсумия® должна храниться при температуре не выше 30°С.
После каждого использования шприц-ручку Ликсумия® следует закрывать колпачком для того, чтобы защитить ее от воздействия света. Шприц-ручку Ликсумия® не следует хранить с присоединенной иглой. Не использовать шприц-ручку Ликсумия®, если она была заморожена.
Шприц-ручка Ликсумия® подлежит утилизации через 14 дней.
Более подробную информацию по проведению инъекций с помощью шприц-ручки Ликсумия® см. ниже в разделе «Описание шприц-ручек Ликсумия® и инструкция по их использованию».
Побочное действие
Частота возникновения нежелательных реакций (HP) определялась следующим образом: очень часто: >10%; часто: >1% - <10%; нечасто: >0,1% - <1%; редко: >0,01% - <0,1%; очень редко: <0,01%.
В 8-ми крупных плацебо-контролируемых и контролируемых активным препаратом клинических исследованиях III фазы более 2600 пациентов получали препарат Ликсумия® в монотерапии или в комбинации с метформином, пероральным гипогликемическим препаратом группы сульфонилмочевины (в сочетании с метформином или без сочетания с метформином) или базальным инсулином (в сочетании с метформином, или без сочетания с метформином, или в сочетании с пероральным гипогликемическим препаратом группы сульфонилмочевины, или без сочетания с пероральным гипогликемическим препаратом группы сульфонилмочевины).
Наиболее частыми HP, о которых сообщалось в клинических исследованиях, были тошнота и рвота. Эти реакции были, главным образом, слабовыраженными и преходящими.
Ниже представлены HP, сообщения о которых поступали из плацебо-контролируемых и контролируемых активным препаратом клинических исследований III фазы, которые за весь период лечения (включая период, превышающий основной 24-недельный период лечения в исследованиях, в которых лечение проводилось в общей сложности >76 недель) возникали с частотой >5% (если их частота была выше у пациентов, принимавших препарат Ликсумия®, по сравнению с пациентами, принимавшими все другие препараты сравнения, включая плацебо); а также с частотой >1% у пациентов в группе препарата Ликсумия®, если их частота более чем в 2 раза превышала частоту возникновения этой HP у пациентов, получавших любой из препаратов сравнения (включая плацебо).
Инфекционные и паразитарные заболевания
Часто
Грипп, инфекции верхних отделов дыхательных путей.
Нарушения обмена веществ и питания
Очень часто
Гипогликемия, протекающая с клинической симптоматикой (когда препарат Ликсумия® применяется в комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины и/или базальным инсулином).
Нарушения со стороны нервной системы
Очень часто
Головная боль.
Часто
Головокружение.
Нарушения со стороны желудочно-кишечного тракта
Очень часто
Тошнота, рвота, диарея.
Часто
Диспепсия.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто
Боли в спине.
Гипогликемия
У пациентов, получающих препарат Ликсумия® в монотерапии или в комбинации с метформином, гипогликемия с клиническими проявлениями развивалась часто, а ее частота у пациентов, которым вводился препарат Ликсумия®, была подобной таковой при введении плацебо во время всего периода лечения.
У пациентов, которым вводился препарат Ликсумия® в сочетании с пероральным гипогликемическим препаратом группы сульфонилмочевины или базальным инсулином, частота развития гипогликемии, протекающей с клинической симптоматикой, была очень частой.
Во время всего периода лечения препаратом Ликсумия® частота возникновения протекающей с клинической симптоматикой гипогликемии была незначительно выше, чем при применении плацебо, когда препарат Ликсумия® применялся в комбинации:
- с пероральным гипогликемическим препаратом группы сульфонилмочевины и метформином,
- с монотерапией базальным инсулином,
- с комбинацией базального инсулина и метформина.
За время всего периода лечения, когда препарат Ликсумия® применялся в сочетании с монотерапией пероральным гипогликемическим препаратом группы сульфонилмочевины, гипогликемия с клиническими проявлениями возникала у 22,7 % пациентов, получавших лечение препаратом Ликсумия®, и у 15,2% у пациентов, получавших плацебо. Когда препарат Ликсумия® применялся в тройной комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины и базальным инсулином, гипогликемия с клиническими проявлениями возникала у 47,2 % пациентов, получавших лечение ликсисенатидом, и у 21,6 % пациентов, получавших плацебо. В целом за весь период приема препарата в контролируемых клинических исследованиях III фазы частота возникновения тяжелой гипогликемии с клиническими проявлениями соответствововала градации «нечасто» (у 0,4 % у пациентов, получавших препарат Ликсумия®, и у 0,2 % у пациентов, получавших плацебо).
Нарушения со стороны желудочно-кишечного тракта
Тошнота и рвота были наиболее часто встречающимися HP, о которых сообщалось в течение основного 24-недельного периода лечения. Частота возникновения тошноты была выше у пациентов, получавших лечение препаратом Ликсумия® (26,1 %), чем у пациентов, получавших плацебо (6,2 %). Частота возникновения рвоты также была выше у пациентов, получавших лечение препаратом Ликсумия® (10,5 %), чем у пациентов, получавших плацебо (1,8 %). Эти HP были, главным образом, слабовыраженными и преходящими и возникали в течение первых 3-х недель после начала лечения. В течение последующих недель они постепенно уменьшались.
У пациентов, получавших лечение препаратом Ликсумия®, частота возникновения тошноты была ниже (24,5%), чем у пациентов, получавших лечение эксенатидом 2 раза в сутки (35,1%), а частота других HP со стороны желудочно-кишечного тракта в обеих группах лечения была одинаковой.
Реакции в месте введения
Реакции в месте введения в течение 24-недельного периода лечения наблюдались у 3,9 % пациентов, получавших препарат Ликсумия®, в то время как у пациентов, получавших плацебо, они наблюдались с частотой 1,4%. Большинство реакций были слабовыраженными по интенсивности и обычно не приводили к прекращению лечения.
Иммуногенность
В связи с потенциально иммуногенными свойствами лекарственных препаратов, содержащих белки или пептиды, после лечения препаратом Ликсумия® у пациентов возможно образование антител к ликсисенатиду. В конце 24-недельного периода лечения в плацебо-контролируемых исследованиях у 69,4 % пациентов, получавших лечение ликсисенатидом, имелись положительные результаты исследования на наличие антител к ликсисенатиду. Однако изменение показателя HbA1C, по сравнению с таковым до применения ликсисенатида, было одинаковым, вне зависимости от положительного или отрицательного результата анализа на наличие антител к ликсисенатиду. Из получавших лечение ликсисенатидом пациентов, у которых определялся показатель HbA1C, у 79,3 % имелся отрицательный результат анализа на наличие антител к ликсисенатиду или титр антител к ликсисенатиду был ниже нижней границы возможности его количественного определения, а у остальных 20,7 % пациентов имелись количественно определяемые титры антител к ликсисенатиду.
Не наблюдалось каких-либо различий в общем профиле безопасности у пациентов в зависимости от статуса антител к ликсисенатиду, за исключением увеличения частоты реакций в месте введения у антитело-позитивных пациентов. Большинство реакций в месте введения были слабовыраженными, независимо от наличия или отсутствия антител к ликсисенатиду.
Отсутствовала перекрестная иммунологическая реактивность с нативным глюкагоном или эндогенным ГПП-1.
Аллергические реакции
Аллергические реакции, возможно связанные с применением ликсисенатида (такие как анафилактические реакции, ангионевротический отек и крапивница) в течение основного 24-недельного периода лечения, наблюдались у 0,4 % пациентов, получавших препарат Ликсумия®, по сравнению с менее чем 0,1 % пациентов в группе плацебо.
Преждевременное прекращение применения препарата
Частота прекращения лечения препаратом из-за возникновения нежелательных реакций составляла 7,4 % в группе препарата Ликсумия® и 3,2 % в группе плацебо. Наиболее частыми HP, приводящими к отмене лечения в группе препарата Ликсумия®, были тошнота (3,1 %) и рвота (1,2 %).
Передозировка
Симптомы передозировки
Во время 13-недельного клинического исследования пациентам с сахарным диабетом 2 типа вводились дозы ликсисенатида до 30 мкг 2 раза в сутки. Эти дозы хорошо переносились, наблюдалось только увеличение частоты возникновения нарушений со стороны желудочно-кишечного тракта.
Лечение
В случае передозировки, в зависимости от клинических проявлений и симптомов у пациента, следует проводить соответствующее поддерживающее лечение, а доза препарата Ликсумия® должна быть снижена до предписанной дозы.
Взаимодействие с другими лекарственными средствами
Ликсисенатид является пептидом и не метаболизируется с помощью изоферментов цитохрома Р450. В in vitro исследованиях, проведенных у человека, ликсисенатид не нарушал активности протестированных изоферментов цитохрома Р450 или транспортеров.
Задержка опорожнения желудка при применении ликсисенатида может повлиять на скорость абсорбции лекарственных препаратов, принимаемых внутрь. Для принимаемых внутрь лекарственных препаратов, эффективность которых особенно зависит от пороговых концентраций, пациентам следует рекомендовать принимать эти лекарственные препараты, как минимум, за 1 ч до или спустя 11 ч после инъекции ликсисенатида.
Парацетамол
После однократного приема парацетамола в дозе 1000 мг, AUC и t½ парацетамола не изменялись, независимо от времени его приема (до или после инъекции ликсисенатида). При приеме через 1 ч или 4 ч после инъекции 10 мкг ликсисенатида Сmах парацетамола снижалась на 29 % и 31 %, соответственно, а медиана tmax увеличивалось на 4,5 ч и 2 ч, соответственно. Исходя из этих данных, не требуется коррекции дозы парацетамола при его применении совместно с ликсисенатидом.
Пероральные контрацептивные лекарственные средства
После однократного приема внутрь перорального контрацептивного лекарственного препарата (этинилэстрадиол 0,03 мг/левоноргестрел 0,15 мг) за 1 ч до или спустя 11 ч после подкожной инъекции ликсисенатида Cmax, AUC, t½ и tmax этинилэстрадиола и левоноргестрела не изменялись. Прием внутрь этинилэстрадиола и левоноргестрела через 1 ч или 4 ч после подкожной инъекции ликсисенатида не оказывал влияния на их AUC и t½, в то время как Сmах этинилэстрадиола снижалась на 52 % (при приеме через 1 ч) и 39 % (при приеме через 4 ч), а Сmах левоногестрела снижалась на 46 % (при приеме через 1 ч) и 20 % (при приеме через 4 ч), а также медиана tmax увеличивалась на 2-4 ч. Снижение Сmах имеет ограниченное клиническое значение, и не требуется коррекции дозы пероральных контрацептивных препаратов.
Аторвастатин
При одновременном применении утром ликсисенатида и аторвастатина в дозе 40 мг системная экспозиция аторвастатина не изменялась, его Cmax незначительно снижалась, а tmax увеличивалось на 1,5-4 ч.
Если аторвастатин принимался вечером, а ликсисенатад утром, то не наблюдалось увеличения tmax, но AUC и Сщзх увеличивались на 27 % и 66 %, соответственно.
Эти изменения не были клинически значимыми, и поэтому не требуется коррекции дозы аторвастатина при его совместном применении с ликсисенатидом.
Варфарин
После одновременного применения варфарина 25 мг и ликсисенатида не наблюдалось влияния на AUC или MHO (международное нормализованное отношение), в то время как tmax увеличивалось до 7 ч.
Исходя из этих данных, не требуется коррекции дозы варфарина при его совместном применении с ликсисенатидом.
Дигоксин
После одновременного применения ликсисенатида и дигоксина в дозе 0,25 мг AUC дигоксина не изменялась, tmax увеличивалось на 1,5 ч и Cmax уменьшалось на 26 %. Исходя из этих данных, не требуется коррекции дозы дигоксина при его совместном применении с ликсисенатидом.
Рамиприл
После одновременного применения ликсисенатида и рамиприла в дозе 5 мг в течение 7 дней AUC рамиприла увеличивалась на 21 %, в то время как Сmах снижалась на 63 %. AUC и Сmах активного метаболита (рамиприлата) не изменялись. tmax рамиприла и рамиприлата увеличивалось приблизительно на 2,5 ч.
Исходя из этих данных, не требуется коррекции дозы рамиприла при его совместном применении с ликсисенатидом.
Особые указания
Применение при сахарном диабете 1 типа
Отсутствует терапевтический опыт применения препарата Ликсумия® у пациентов с сахарным диабетом 1 типа, и его применение у таких пациентов противопоказано. Применение препарата Ликсумия® при диабетическом кетоацидозе противопоказано.
Риск панкреатита
Применение агонистов рецепторов ГПП-1 ассоциировалось с риском развития острого панкреатита. Характерным симптомом острого панкреатита являются длительно сохраняющиеся сильные боли в животе. При подозрении на развитие панкреатита следует прекратить лечение препаратом Ликсумия®; при подтверждении диагноза острого панкреатита возобновлять лечение препаратом Ликсумия® нельзя. Следует с осторожностью применять препарат у пациентов с панкреатитом в анамнезе.
Применение при тяжелом гастропарезе
Применение агонистов рецепторов ГПП-1 может ассоциироваться с нежелательными реакциями со стороны желудочно-кишечного тракта. Применение препарата Ликсумия® у пациентов с тяжелыми заболеваниями желудочно-кишечного тракта, включая гастропарез, до настоящего времени не изучалось, и поэтому у таких пациентов применение препарата Ликсумия® противопоказано.
Риск развития гипогликемии Пациенты, получающие лечение препаратом Ликсумия® в сочетании с пероральным гипогликемическим препаратом группы сульфонилмочевины или с комбинацией базального инсулина и перорального гипогликемического препарата группы сульфонилмочевины, могут иметь повышенный риск развития гипогликемии. Для уменьшения риска развития гипогликемии может быть рассмотрен вопрос о снижении дозы перорального гипогликемического препарата группы сульфонилмочевины или базального инсулина.
Влияние на способность управлять транспортными средствами или заниматься другими потенциально опасными видами деятельности
Не проводилось исследований по влиянию препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности.
При применении препарата в комбинации с пероральным гипогликемическим препаратом группы сульфонилмочевины или базальным инсулином пациенты должны быть информированы о необходимости соблюдения мер предосторожности для предупреждения возникновения гипогликемии во время управления транспортными средствами или при занятии другими потенциально опасными видами деятельности.
Форма выпуска
Раствор для подкожного введения 0,05 мг/мл (10 мкг/доза) и 0,1 мг/мл (20 мкг/доза).
По 3 мл препарата в картридж из бесцветного стекла (тип I). Картридж укупорен с одной стороны пробкой (ламинат из синтетической изопреновой резины и бромбутиловой резины), обжатой алюминиевым колпачком, с другой стороны закрыт притертым поршнем из бромбутиловой резины. Картридж вмонтирован в одноразовую шприц-ручку.
Для раствора 0,05 мг/мл (10 мкг/доза): по 1 шприц-ручке вместе с инструкцией по применению в картонную пачку, снабженную фиксатором.
Для раствора 0,1 мг/мл (20 мкг/доза): по 1, 2 или 6 шприц-ручек вместе с инструкцией по применению в картонную пачку, снабженную фиксатором.
Комплект: по 1 шприц-ручке с раствором 0,05 мг/мл (10 мкг/доза) и 1 шприц-ручке с раствором 0,1 мг/мл (20 мкг/доза) вместе с инструкцией по применению в картонную пачку, снабженную фиксатором.
Условия хранения
Хранить в защищенном от света месте при температуре от 2°С до 8°С.
Не замораживать.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускается по рецепту.
Производитель
Санофи-Авентис Дойчланд ГмбХ, Германия.
Industriepark Hoechst, Brueningstrasse 50, D-65926 Frankfurt (Main), Germany.
Юридическое лицо, на имя которого выдано регистрационное удостоверение
Санофи, Франция.
Претензии потребителей направлять по адресу в России:
125009, г. Москва, ул. Тверская, 22.
Описание шприц-ручек Ликсумия® и инструкция по их использованию
Перед использованием шприц-ручки Ликсумия® внимательно прочитайте инструкцию и получите у лечащего врача информацию по правильной технике проведения инъекции. Если Вы не способны сами полностью следовать инструкции (например, если Вы слепы или у Вас есть серьезные проблемы со зрением), используйте шприц-ручку только в том случае, если у Вас есть возможность воспользоваться помощью человека, который способен следовать инструкциям.
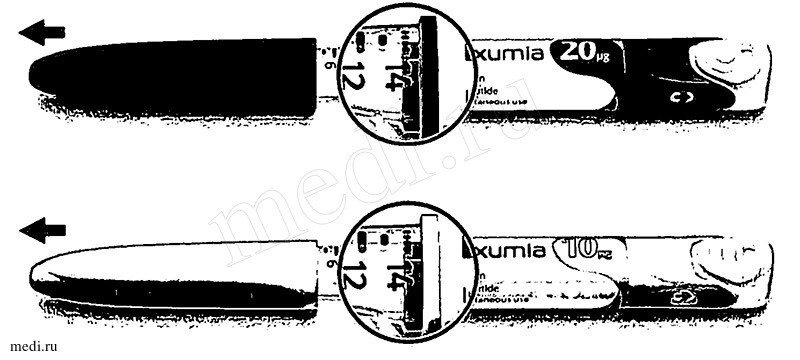
Препарат Ликсумия® выпускается в виде предварительно заполненных шприц-ручек для инъекций, в каждой из которых содержится 14 доз. Выпускается 2 вида шприц-ручек Ликсумия®, которые окрашены в разные цвета и имеют разный тактильный элемент на кнопке введения дозы и колпачке шприц-ручки: шприц-ручка с разовой дозой 20 мкг ликсисенатида в 0,2 мл имеет бордовый цвет и тактильный элемент в виде кругов, а шприц-ручка с разовой дозой 10 мкг ликсисенатида в 0,2 мл имеет зеленый цвет и тактильный элемент в виде линий.
Внешний вид шприц-ручки Ликсумия® 20 мкг
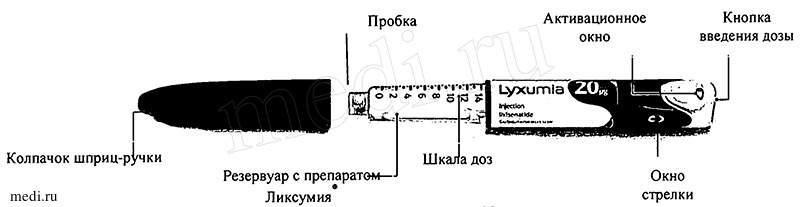
Внешний вид шприц-ручки Ликсумия® 10 мкг
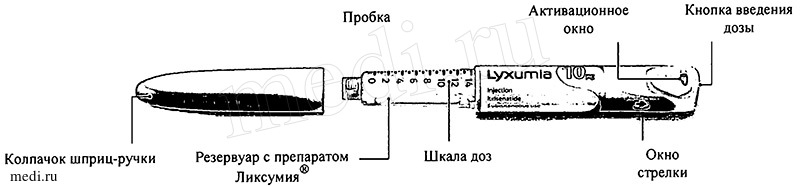
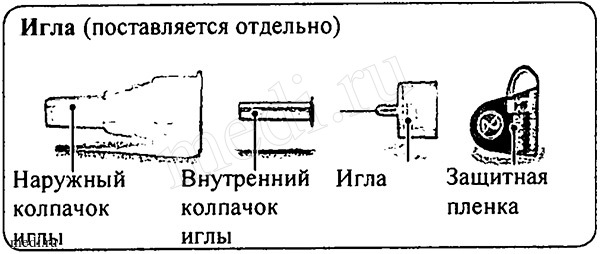
Используйте с Вашей шприц-ручкой Ликсумия® одноразовые иглы для шприц-ручек с просветом 29-32 G.
Черный поршень будет продвигаться по дозировочной шкале после каждой инъекции.
Важные рекомендации
- Вводите только по одной дозе в сутки.
- Эта шприц-ручка предназначена для использования только одним человеком. Не пользуйтесь ей вместе с кем-либо.
- Если Вы делаете инъекцию другому человеку или если Ваша инъекция проводится другим человеком, следует соблюдать особую осторожность для того, чтобы избежать случайного повреждения иглой, что может привести к передаче инфекций, передающихся через кровь.
- Всегда проверяйте маркировку на шприц-ручке, ее цвет и тактильный элемент на колпачке и кнопке введения дозы, чтобы удостовериться, что у Вас имеется шприц-ручка с нужной Вам дозой, и у нее не истек срок годности.
- Каждая шприц-ручка Ликсумия® содержит 14 соответствующих доз. Нет необходимости набора требуемой дозы.
- Проверьте внешний вид резервуара с препаратом Ликсумия®. Жидкость должна быть прозрачной, бесцветной и не содержать механических включений. В противном случае не используйте эту шприц-ручку.
- Всегда используйте новую стерильную иглу для каждой инъекции. Это поможет избежать контаминации и закупорки иглы.
- Всегда имейте запасную шприц-ручку Ликсумия® на случай, если Ваш экземпляр шприц-ручки потеряется или повредится.
- Не пытайтесь извлечь жидкость из резервуара шприц-ручки Ликсумия® с помощью шприца.
- После первой активации Вашей шприц-ручки Ликсумия® она может использоваться в течение 14 дней.
- Вы должны активировать Вашу шприц-ручку Ликсумия® перед использованием ее в первый раз, чтобы удостовериться в том, что она работает правильно и что доза для Вашей первой инъекции является правильной.
- Когда Вы активируете Вашу шприц-ручку Ликсумия® первый раз, не вводите себе раствор. Вместо этого для того, чтобы собрать выделяющийся при активации шприц-ручки Ликсумия® избыток раствора используйте подходящий контейнер (бумажный стаканчик или ткань).
- Перед первым использованием каждой новой шприц-ручки Ликсумия® процесс активации должен проводиться только однократно.
- Не повторяйте процесс активации перед каждой инъекцией, в противном случае Вы не получите все 14 доз из шприц-ручки Ликсумия®.
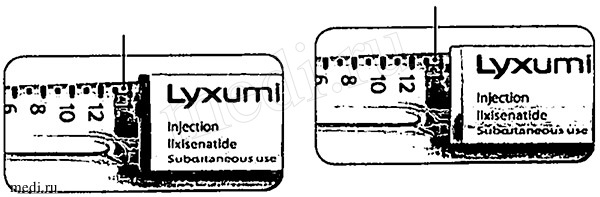
На рисунке ниже показано, как выглядит шприц-ручка перед активацией и после активации.
Не активированная
(Оранжевое окно)

Активированная ручка - готова для проведения инъекций
(Белое окно)
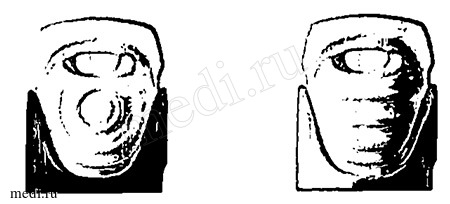
Активация шприц-ручки Ликсумия®.
Этап 1. Снятие колпачка и проверка шприц-ручки
Проверьте, является ли активационное окно оранжевым.
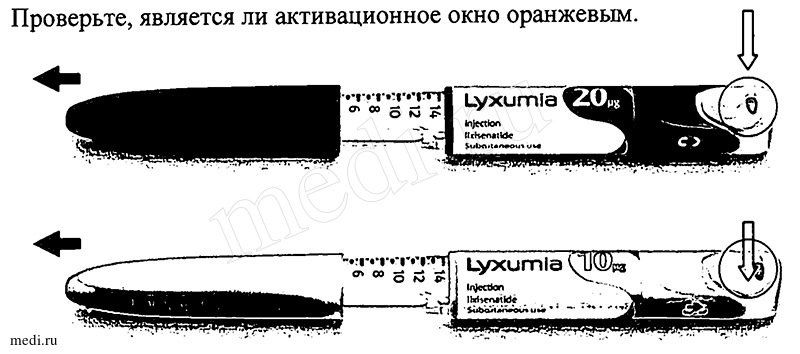
Проверьте раствор. Он должен быть прозрачным, бесцветным и не содержать механических включений. В противном случае не используйте эту шприц-ручку.
В новой шприц-ручке черный поршень не должен быть виден на дозировочной шкале.
Этап 2. Присоединение иглы и удаление колпачков иглы
Протрите пробку (на конце картриджа) ватным тампоном, смоченным спиртом.
Удалите защитную пленку с наружного колпачка иглы.
Расположите на одной линии иглу и шприц-ручку и держите их прямо, когда Вы плотно закрепляете иглу на шприц-ручке.
Соблюдайте осторожность, чтобы не уколоться открытой иглой.
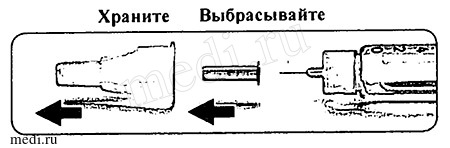
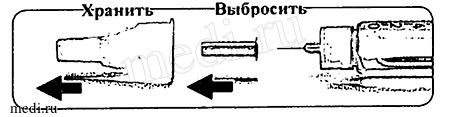
Снимите наружный колпачок иглы и храните его для того, чтобы позднее удалить иглу. Снимите внутренний колпачок и выбросите его.
Храните Выбрасывайте
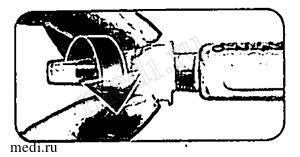
Этап 3. Оттягивание кнопки введения дозы и проверка стрелки
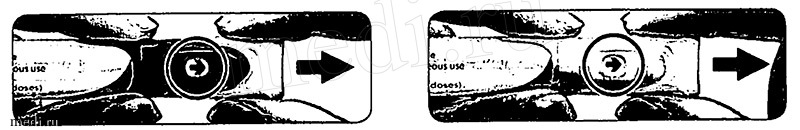
Проверьте, чтобы стрелка указывала на кнопку введения дозы.
Полностью оттяните кнопку введения дозы.
Стрелка должна поменять свое направление и стать направленной на иглу.
Проверьте, чтобы стрелка указывала на иглу.

Этап 4. Нажатие и удерживание кнопки введения дозы для активации шприц-ручки
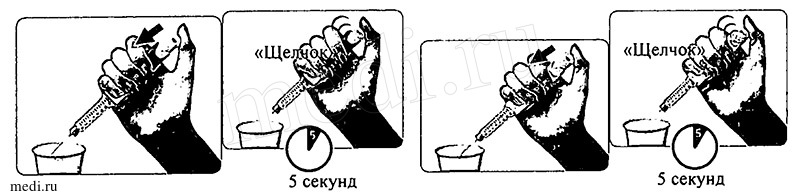
Направьте иглу в подходящий контейнер (например, бумажный стаканчик или ткань), в который будет выпущен избыточный раствор для дальнейшего уничтожения.
Нажмите на кнопку введения дозы до упора.
Вы можете почувствовать и услышать «щелчок».
Удерживайте кнопку введения дозы в нажатом состоянии и медленно сосчитайте до пяти для того, чтобы вытекли последние капли.
Этап 5. Проверка активирована ли шприц-ручка
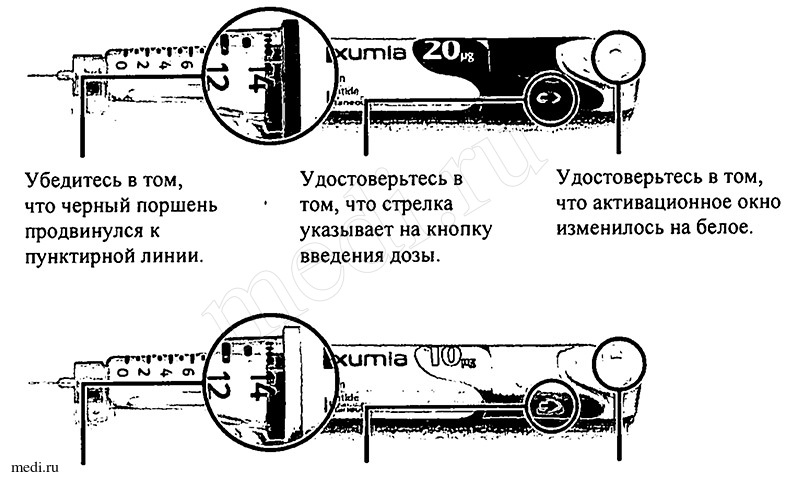
Если этого не происходит, не используйте данную шприц-ручку.
Теперь эта шприц-ручка активирована. Не повторяйте активацию для этой шприц-ручки.
Переходите непосредственно к этапу С для введения Вашей первой дозы.
Вам не нужно заменять иглу между активацией и первой инъекцией.
Если Вы случайно ввели себе препарат до активации Вашей шприц-ручки, не исправляйте эту ошибку путем введения себе второй инъекции. Свяжитесь с Вашим лечащим врачом для получения рекомендаций по контролю за концентрацией глюкозы в крови.
Ежедневное использование шприц-ручки
Переходите к этому разделу только тогда, когда активационное окно является белым.
Каждый день вводите только ОДНУ дозу.
Этап А. Снимите колпачок и проверьте шприц-ручку
Проверьте внешний вид раствора в резервуаре шприц-ручки. Она должна быть прозрачной, бесцветной и не содержать механических включений. В противном случае не используйте эту шприц-ручку.
Проверьте количество доз в шприц-ручке по указанию черного поршня.
Проверьте маркировку, цвет и тактильные элементы Вашей шприц-ручки, чтобы удостовериться в том, что Вы используете правильный препарат.
Удостоверьтесь в том, что активационное окно является белым. Если оно оранжевое, то перейдите в раздел «Активация шприц-ручки»
Этап В. Присоединение новой иглы и удаление колпачков иглы
Протрите резиновую герметизирующую пробочку (на конце картриджа) ватным тампоном, смоченным спиртом.
Удалите защитную пленку с наружного колпачка иглы.
Расположите на одной линии иглу и шприц-ручку и держите их прямо, когда Вы плотно закрепляете иглу на шприц-ручке.
Соблюдайте осторожность, чтобы не уколоться открытой иглой.
Снимите наружный колпачок иглы и храните его для того, чтобы позднее удалить иглу.
Снимите внутренний колпачок и выбросите его.
Всегда используйте новую стерильную иглу для каждой инъекции.
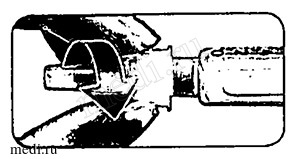
Этап С. Оттягивание кнопки введения дозы и проверка направления стрелки

Удостоверьтесь в том, что стрелка направлена в сторону кнопки введения дозы.
До упора оттяните кнопку введения дозы.
Удостоверьтесь в том, что стрелка изменила свое направления и направлена в сторону иглы.
Теперь шприц-ручка готова для проведения инъекции.

Этап D. Нажатие на кнопку введения дозы и удерживание ее в этом положении для того, чтобы ввести дозу
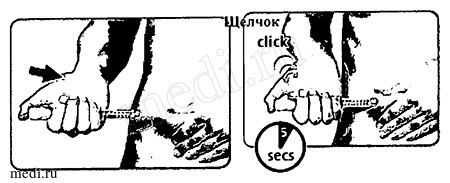
Соберите кожу в складку и введите иглу.
Места инъекций
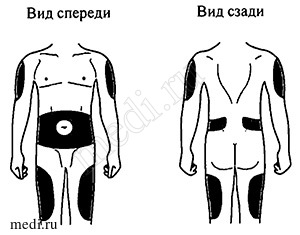
Препарат Ликсумия® может вводиться подкожно в любую из указанных синим цветом на рисунках областей, которые находятся на бедре, животе и плече.
Нажмите на кнопку введения дозы до упора. Вы можете почувствовать или услышать «щелчок».
Удерживайте кнопку введения дозы в нажатом состоянии и медленно сосчитайте до пяти (5), чтобы получить полную дозу.
Теперь Вам введена Ваша доза.
Каждый день вводите только ОДНУ дозу.
Примечание
- Маленькие воздушные пузырьки в резервуаре являются нормальным явлением. Они не повлияют на величину введенной дозы и не причинят Вам вреда.
- Возникновение ощущения препятствия во время всего процесса надавливания на кнопку введения дозы, может быть связано с закупоркой иглы или ее ненадлежащим подсоединением. Следует извлечь иглу из кожи и удалить иглу из шприц-ручки, подсоединить новую иглу и попробовать ввести препарат снова. Если и после этого жидкость не вытекает наружу, то это говорит о том, что шприц-ручка Ликсумия® испорчена, и ее использовать нельзя.
Этап Е. Проверка продвижения поршня

Черный поршень должен продвинуться по шкале доз.
(На примере выше шкала доз показывает, что осталось 13 инъекций)
Этап F. Удаление и выбрасывание иглы после каждой инъекции
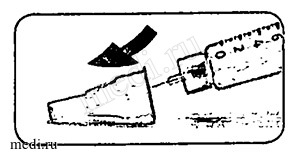
Положите наружный колпачок иглы на плоскую поверхность. Введите иглу в наружный колпачок иглы.
Установите наружный колпачок иглы на прежнее место.

Надавите на наружный колпачок, чтобы прижать его к игле используйте его для того, чтобы выкрутить иглу из шприц-ручки.
Поместите иглу в резистентный к проколам контейнер или уничтожьте ее в соответствии с указаниями Вашего врача.

Закройте шприц-ручку колпачком.
Повторяйте все этапы в разделе «Ежедневное использование шприц-ручки» для проведения Ваших следующих ежедневных инъекций.
Через 14 дней после активации выбросите шприц-ручку, даже если в ней осталось некоторое количество препарата.
Хранение
Общая информация
- Храните шприц-ручку Ликсумия® в безопасном месте, недоступном для детей.
- Защищайте шприц-ручку от пыли и загрязнений.
- Надевайте колпачок шприц-ручки после каждого использования с целью защиты содержимого картриджа от воздействия света.
- Активируйте новую шприц-ручку непосредственно перед ее использованием в первый раз.
До активации
- Храните неиспользованные шприц-ручки в холодильнике (при температуре 2-8 °С; 36-46 °F). Не замораживайте шприц-ручки Ликсумия® и не используйте шприц-ручки Ликсумия®, если они были заморожены.
После активации
- Храните шприц-ручку Ликсумия® при температуре не выше 30°С.
- Не храните шприц-ручку с присоединенной иглой.
- После активации шприц-ручка Ликсумия® может использоваться в течение 14 дней.
Следует выбросить использованную шприц-ручку Ликсумия® через 14 дней, даже если в ней остается некоторое количество препарата. - Закрывайте шприц-ручку колпачком шприц-ручки после каждого использования с целью защиты содержимого картриджа от воздействия света.
Таблица активации и утилизации
| Шприц-ручка | Дата активации | Дата утилизации |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 | ||
| 6 |
Уход за шприц-ручкои
- Следует осторожно обращаться со шприц-ручкой Ликсумия®.
- Вы может очищать наружную поверхность Вашей шприц-ручки Ликсумия®, протирая ее влажной тряпочкой.
- Не замачивайте, не мойте или не смазывайте шприц-ручку Ликсумия®, так как это может повредить ее.
- Если Вы подозреваете, что шприц-ручка может быть повреждена, не используйте ее. Получите новую шприц-ручку. Не пытайтесь самостоятельно чинить шприц-ручку.
Утилизация
После введения 14 доз шприц-ручка Ликсумия® является пустой и не будет больше работать. Вы должны безопасно уничтожить шприц-ручку после того, как из нее будет введено 14 доз.
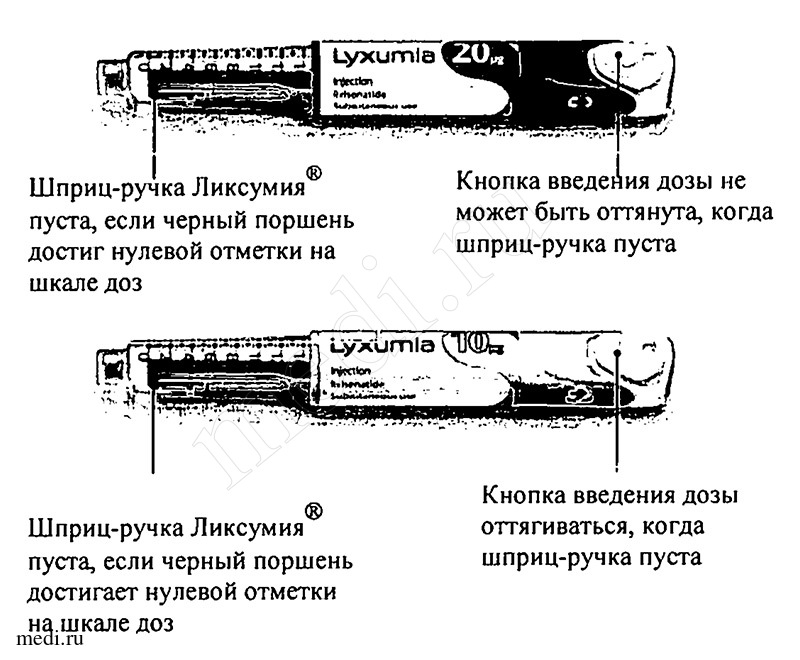
Наденьте колпачок на Вашу шприц-ручку Ликсумия® перед тем, как выбросить ее в отходы.
Комментарии
ПРАКТИКА ПЕДИАТРА
