Лемтрада - инструкция по применению
Синонимы, аналоги Статьи
Регистрационный номер: ЛП-003714.
Торговое название препарата: Лемтрада®.
Международное непатентованное название: алемтузумаб.
Лекарственная форма: концентрат для приготовления раствора для инфузий.
Состав
1 мл препарата содержит:
действующее вещество: алемтузумаб - 10 мг;
вспомогательные вещества: динатрия эдетата дигидрат - 0,0187 мг, фосфатный забуференный солевой раствор pH 7,2 (калия хлорид - 0,2 мг, калия дигидрофосфат - 0,2 мг, натрия хлорид - 8 мг, динатрия гидрофосфат безводный1 - 1,15 мг, полисорбат-80 - 0,1 мг, вода для инъекций - до 1 мл).
Описание
Прозрачная или опалесцирующая бесцветная или светло-желтая жидкость.
Фармакотерапевтическая группа: селективный иммунодепрессант.
Код ATX: L04AA34.
Фармакологические свойства
Механизм действия
Алемтузумаб - это гуманизированное IgGl каппа моноклональное антитело к гликопротеинам CD52 с молекулярной массой 21-28 кДа. Производится по технологии рекомбинантной ДНК с использованием суспензионной культуры клеток яичника китайского хомячка. Алемтузумаб представляет собой человеческий IgGl (вариабельные и константные участки каппа цепи) с участками, определяющими комплементарность, полученными от моноклональных антител мыши (крысы). Молекулярная масса антитела составляет примерно 150 кДа.
Алемтузумаб связывается с гликопротеинами СD52, которые присутствует в больших количествах на поверхности В- и Т-лимфоцитов, и в более низких количествах - на поверхности естественных клеток-киллеров, моноцитов и макрофагов. На поверхности нейтрофилов, плазматических клеток и стволовых клеток костного мозга гликопротеины СD52 не определяются или определяются в небольших количествах. Действие алемтузумаба реализуется путем антитело-зависимого цитолиза и комплемент-опосредованного лизиса, которые развиваются после связывания алемтузумаба с В- и Т-лимфоцитами.
Точный механизм действия алемтузумаба при рассеянном склерозе до конца не изучен, но, предположительно, может быть связан с иммуномодулирующим эффектом после истощения популяции лимфоцитов и их последующей репопуляции, включая:
- изменение количества, процентного соотношения и свойств некоторых подтипов лимфоцитов,
- увеличение уровня регуляторных Т-лимфоцитов,
- увеличение уровня В- и Т-лимфоцитов памяти,
- транзиторное влияние на врожденную иммунную систему (например, на нейтрофилы, макрофаги и естественные клетки-киллеры).
Снижение количества циркулирующих В- и Т-лимфоцитов и их последующая репопуляция уменьшает вероятность рецидива, что, в конечном счете, замедляет прогрессирование заболевания.
Фармакодинамика
Препарат Лемтрада® снижает количество циркулирующих В- и Т-лимфоцитов после каждого курса лечения, при этом наименьшее количество клеток отмечается через месяц после курса лечения. Со временем популяция лимфоцитов восстанавливается, при этом восстановление популяции В-клеток обычно завершается в течение 6 месяцев. Количество лимфоцитов с экспрессией СDЗ+ и СD4+ увеличивается до нормы гораздо медленнее и обычно не восстанавливается до исходных значений к 12 месяцу после лечения. Приблизительно у 40 % пациентов общее количество лимфоцитов достигало нижней границы нормы через 6 месяцев после каждого курса лечения, а приблизительно у 80 % пациентов общее количество лимфоцитов достигало нижней границы нормы через 12 месяцев после каждого курса лечения.
Лемтрада® оказывает транзиторное действие на нейтрофилы, моноциты, эозинофилы, базофилы и естественные клетки-киллеры.
Клиническая эффективность и безопасность
Безопасность и эффективность препарата Лемтрада® оценивались в ходе 3 рандомизированных клинических исследований с участием пациентов с рецидивирующе-ремиттирующим рассеянным склерозом (РРРС), с активным препаратом сравнения, и со скрытием выбора метода лечения от оценивающего результат специалиста.
В Таблице 1 представлена информация по дизайну/демографическим показателям пациентов Исследований 1 и 2, а в Таблице 2 - информация по результатам этих исследований.
Таблица 1:
дизайн и демографические показатели пациентов исследований 1 и 2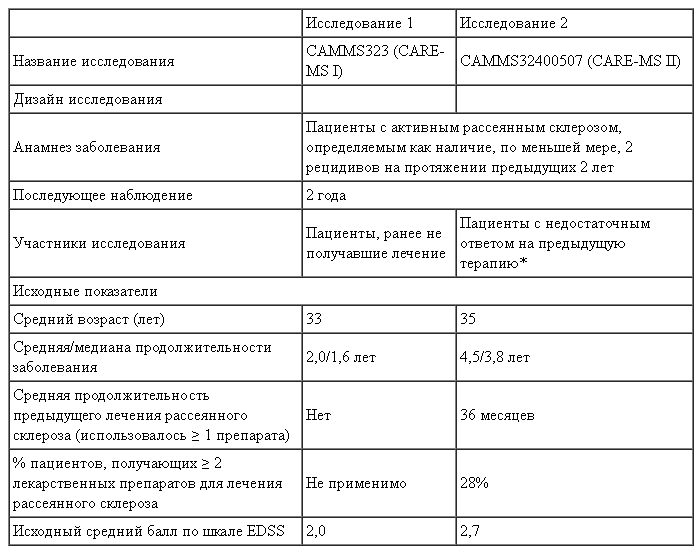
Таблица 2:
Основные клинические и МРТ конечные точки Исследований 1 и 2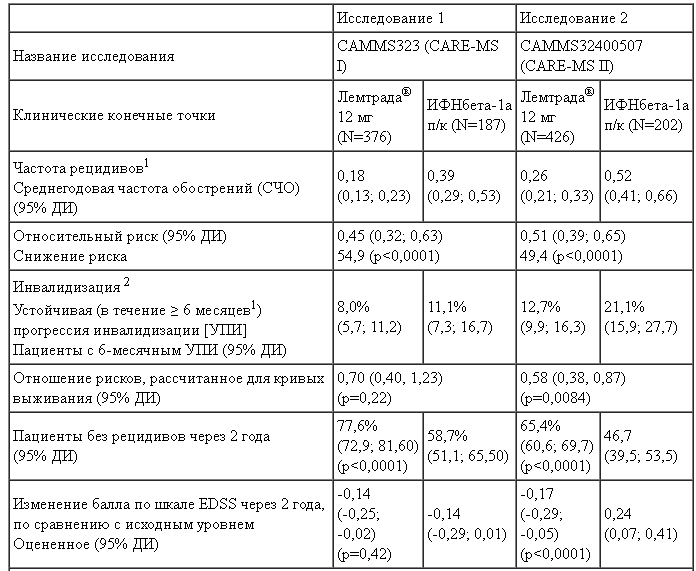
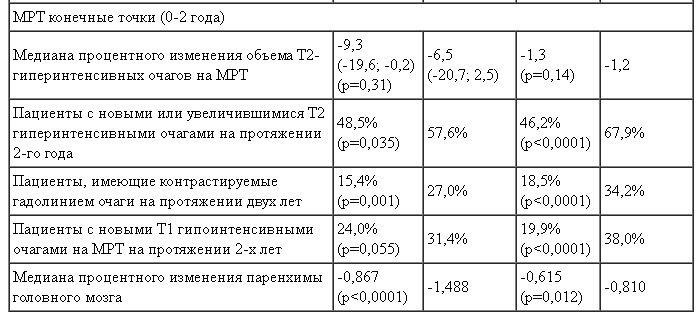
1 Комбинированные первичные конечные точки: СЧО и УПИ. Исследование признавалось успешным, если была достигнута, по меньшей мере, одна из двух комбинированных конечных точек.
2 Наступление события УПИ определялось как сохраняющиеся на протяжении 6 месяцев увеличение баллов по Расширенной шкале оценки состояния инвалидизации (ЕDSS), по меньшей мере, на 1 балл при исходном балле ≥ 1,0 и на 1,5 балла при исходном уровне ЕDSS 0 баллов.
Рисунок 1: Время до устойчивой (в течение ≥ 6 месяцев) прогрессии инвалидизации [УПИ] в Исследовании 2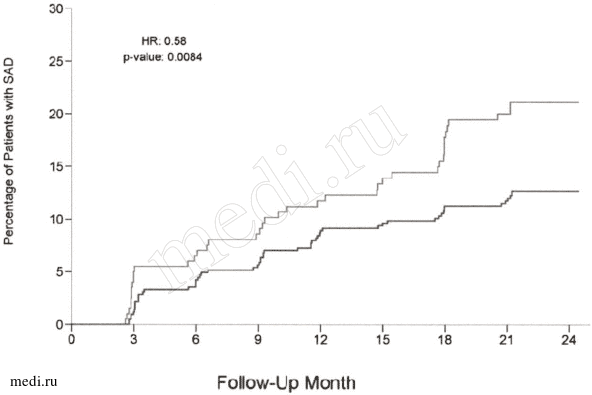
Верхний график - алемтузумаб.
Нижний график - ИФНбета-1а (подкожно).
Percentage of Patients with SAD - процент пациентов с УПИ.
Follow-Up Month - месяцы наблюдения.
HR (hazard ratio) - отношение рисков, рассчитанное для кривых выживания,
p-value - р-значение
Тяжесть рецидива
Кроме влияния на частоту рецидивов, дополнительный анализ, проведенный в рамках Исследования 1 (CAMMS323), показал, что, по сравнению с использованием ИФНбета-1а, применение препарата Лемтрада® в дозе 12 мг в сутки приводило к значимому снижению числа пациентов с тяжелыми рецидивами (снижение на 61%, р=0,0056), а также к значимому снижению числа рецидивов, требующих назначения стероидов (снижение на 58%, р<0,0001). Дополнительный анализ, проведенный в рамках Исследования 2 (САММS32400507), показал, что, по сравнению с использованием ИФНбета-1а, применение препарата Лемтрада® в дозе 12 мг в сутки приводило к значимому снижению числа пациентов с тяжелыми рецидивами (снижение на 48%, р=0,0121), а также к значимому снижению числа рецидивов, требующих назначения стероидов (снижение на 56%, р<0,0001) или госпитализации (снижение на 55%, р=0,0045).
Устойчивое снижение инвалидизации (УСИ)
Время до начала УСИ определялось в случае сохранения на протяжении 6 месяцев уменьшения баллов по ЕDSS, по меньшей мере, на 1 балл при исходном балле ≥ 2. УСИ является мерой устойчивого улучшения с точки зрения инвалидизации. В рамках Исследования 2 УСИ достигли 29% пациентов, получавших препарат Лемтрада®, и лишь 13% пациентов, получавших ИФНбета-1а подкожно. Различие было статистически значимым (р=0,0002).
В рамках Исследования 3 (фаза 2 исследования САММS223) оценивались безопасность и эффективность препарата Лемтрада® при применении его пациентами с РРРС на протяжении 5 лет. Критериями включения в исследование были: 0-3 балла по шкале ЕDSS, по меньшей мере, 2 клинических эпизода рассеянного склероза в течение предыдущих 2 лет и ≥ 1 очага, контрастируемого гадолинием. Ранее участники не должны были получать лечение по поводу рассеянного склероза. В рамках исследования пациенты получали либо препарат Лемтрада® в дозе 12 мг в сутки (N=108) или 24 мг в сутки (N=108), который вначале (0 месяц) вводили 1 раз в сутки на протяжении 5 дней, а затем (12 месяц) - 1 раз в сутки на протяжении 3 дней, либо ИФНбета-1а в дозе 44 мкг (N=107) 3 раза в неделю на протяжении 3 лет. 46 пациентов получили третий курс препарата Лемтрада® (24 месяц) по 12 мг в сутки или 24 мг в сутки на протяжении 3 дней.
Через 3 года у пациентов, получавших препарат Лемтрада® по сравнению с пациентами, получавшими ИФНбета-1а подкожно, риск 6-месячного УПИ снизился на 76% (отношение рисков, рассчитанное для кривых выживания 0,24 [95% ДИ: 0,110; 0,545]. р<0.0006), а среднегодовая частота обострений снизилась на 67% (отношение рисков 0.33 [95% ДИ: 0,196; 0,552], р<0,0001). На протяжении 2 лет последующего наблюдения применение алемтузумаба в дозе 12 мг в сутки привело к значимому (р<0,0001) снижению баллов по шкале ЕDSS, по сравнению с применением ИФНбета-1а (сравнение выполнялось с исходным уровнем).
Через 5 лет препарат Лемтрада® снизил риск УПИ на 69 % (отношение рисков, рассчитанное для кривых выживания 031 [95% ДИ: 0,161; 0,598], р=0.0005), а среднегодовую частоту обострений - на 66% (отношение рисков 0,34 [95% ДИ: 0,202; 0.569], р<0,0001) (по сравнению с подкожным введением ИФНбета-1а).
В открытом продолжении клинических исследований препарата Лемтрада® некоторые пациенты «в случае необходимости» (при документальном подтверждении возобновления активности рассеянного склероза) получали дополнительные дозы препарата. В рамках дополнительных курсов препарат Лемтрада® в дозе 12 мг в сутки вводили на протяжении 3 дней подряд (суммарная доза 36 мг), по меньшей мере, через 12 месяцев после предыдущего курса лечения. Польза и риски > 2 курсов лечения до конца не установлены, однако полученные результаты позволяют предположить, что дополнительные курсы терапии не привели к изменению профиля безопасности. Дополнительные курсы терапии должны проводиться не ранее, чем через 12 месяцев после предыдущего курса.
Иммуногенность
Как и любые другие лекарственные препараты белкового происхождения, алемтузумаб обладает потенциальной иммуногенностью. Полученные данные отражали процент пациентов с положительными результатами на наличие антител к алемтузумабу (по данным фермент-связанного иммуносорбентного исследования (ELISA), подтвержденного анализом конкурентного связывания). Затем положительные образцы изучались на наличие признаков ингибирования in vitro методом проточной цитометрии. В рамках контролируемых клинических исследований с участием пациентов с рассеянным склерозом для выявления антител к алемтузумабу образцы сыворотки собирали через 1, 3 и 12 месяцев после каждого курса терапии. Во время исследований антитела к алемтузумабу обнаруживались приблизительно у 85 % пациентов, получавших препарат Лемтрада®, при этом у 92 % из этих пациентов были положительными результаты тестирования также и на наличие антител, ингибирующих связывание препарата Лемтрада® in vitro. Те пациенты, у которых выработались антитела к алемтузумабу, продолжали демонстрировать их наличие на протяжении 15 месяцев с момента первого введения препарата. Взаимосвязи между наличием антител к алемтузумабу или ингибирующих антител к алемтузумабу и снижением эффективности, изменением фармакодинамики или развитием нежелательных реакций, включая реакции, связанные с инфузиями. не выявлено.
Частота выявления антител в значительной степени зависит от чувствительности и специфичности используемого метода анализа. Кроме того, частота выявления антител (включая ингибирующие антитела) может зависеть от целого ряда факторов, таких как методика анализа, обработка образцов, время забора образцов, одновременный прием других препаратов и сопутствующие заболевания. По этим причинам сравнение частоты выявления антител к препарату Лемтрада® с частотой выявления антител к другим препаратам может быть ошибочным.
Фармакокинетика
Фармакокинетику алемтузумаба оценивали в исследовании с участием 216 пациентов с рецидивирующе-ремиттирующим рассеянным склерозом, получавших внутривенные инфузии препарата в дозах 12 мг или 24 мг в сутки в течение 5 дней подряд, а затем - в течение 3 дней подряд через 12 месяцев после начального курса терапии. Концентрация препарата в сыворотке крови в пределах одного курса лечения возрастала после введения каждой последующей дозы, а максимальная концентрация (Сmах) достигалась после последней инфузии курса. Введение препарата в дозе 12 мг в сутки позволяло достичь значение Сmax, равное 3014 нг/мл, на 5 сутки начального курса лечения и 2276 нг/мл - на 3 сутки второго курса лечения. Период полувыведения составлял приблизительно 4-5 дней и его значения существенно не различались в ходе начального и последующего курсов терапии; концентрации в сыворотке крови в течение приблизительно 30 дней после каждого курса лечения были низкими или неопределяемыми.
Алемтузумаб - белок, предполагаемым путем метаболизма которого является распад на небольшие пептиды и отдельные аминокислоты под действием широко распространенных протеолитических ферментов. Классические исследования биотрансформации не проводились.
Имеющиеся данные не позволяют сделать выводы о влиянии расы и пола на фармакокинетику препарата Лемтрада®. Фармакокинетика препарата не изучалась у пациентов в возрасте 55 лет и старше.
Показания к применению
Препарат Лемтрада® показан для лечения взрослых пациентов с активным рецидивирующе-ремиттирующим рассеянным склерозом (РРРС), т.е. перенесших два или более обострения в течение последних двух лет.
Противопоказания
- Повышенная чувствительность к алемтузумабу или к какому-либо из вспомогательных веществ препарата.
- ВИЧ-инфекция.
- Возраст до 18 лет (безопасность и эффективность препарата не установлены) (см. в разделе «Особые указания» подраздел «Педиатрическая популяция»).
Ограничения по применению препарата во время беременности приведены в разделе «Применение при беременности и в период грудного вскармливания».
Применение при беременности и в период грудного вскармливания
Беременность
Данные о применении препарата Лемтрада® для лечения беременных женщин с рассеянным склерозом ограничены. Препарат Лемтрада® можно применять во время беременности, только если предполагаемая польза превышает потенциальный риск для плода.
Известно, что человеческий иммуноглобулин проходит через плацентарный барьер; алемтузумаб также может проходить через плацентарный барьер, и, следовательно, потенциально представляет риск для плода. В исследованиях на животных было выявлено токсическое действие на репродуктивную функцию. Неизвестно, способен ли алемтузумаб оказывать вредное воздействие на плод при его введении беременной женщине или негативно влиять на репродуктивную функцию.
Заболевания щитовидной железы представляют особый риск для беременных женщин. При отсутствии лечения гипотиреоза во время беременности имеется повышенный риск невынашивания беременности и воздействия на плод, результатами которого могут быть задержка умственного развития и карликовость. У беременных женщин с диффузным токсическим зобом (болезнь Грейвса, Базедова болезнь) антитела к рецепторам тиреотропного гормона могут передаваться развивающемуся плоду и вызвать развитие транзиторного диффузного токсического зоба у новорожденного.
Период грудного вскармливания
Алемтузумаб был обнаружен в молоке лактирующих мышей и у их детёнышей.
Неизвестно, проникает ли алемтузумаб в грудное молоко у людей. Однако нельзя исключить наличие риска для ребенка, получающего грудное молоко. Таким образом, грудное вскармливание должно быть прекращено на протяжении всего курса лечения препаратом Лемтрада®, а также в течение 4 месяцев после выполнения последней инфузии в рамках любого курса лечения. При этом польза от передачи иммунитета через грудное молоко может превосходить риски от возможного попадания алемтузумаба в организм ребенка.
Женщины детородного возраста
После окончания каждого из курсов терапии препаратом Лемтрада® концентрация алемтузумаба в сыворотке крови была низкой или находилась на неопределяемом уровне приблизительно в течение 30 дней. Женщины детородного возраста должны использовать надёжные методы контрацепции во время лечения препаратом Лемтрада® и в течение 4 месяцев после последней инфузии препарата Лемтрада®.
Влияние на фертильность
Достоверные данные по клинической безопасности, касающиеся влияния препарата Лемтрада® на репродуктивную функцию, отсутствуют. В рамках дополнительного исследования с участием 13 мужчин, получавших алемтузумаб (в дозах 12 мг или 24 мг), не было получено никаких подтверждений развития аспермии, азооспермии, устойчивого снижения количества сперматозоидов, нарушений подвижности или увеличения числа морфологических изменений сперматозоидов.
Известно, что рецепторы СD52 присутствует в тканях репродуктивных органов человека и грызунов. Данные, полученные в исследованиях на животных, выявили наличие влияния на репродуктивную функцию у гуманизированных мышей, однако имеющиеся данные не позволяют судить о том, влияет ли применение препарата Лемтрада® на репродуктивную функцию человека.
Способ применения и дозы
Терапия алемтузумабом должна назначаться и проводиться под контролем невролога, имеющего опыт лечения пациентов с рассеянным склерозом, при доступности специалистов и оборудования для своевременной диагностики и лечения наиболее часто возникающих нежелательных реакций, особенно аутоиммунных заболеваний и инфекций. Терапия должна проводиться в условиях доступа к средствам для купирования реакций гиперчувствительности и/или анафилактических реакций.
Пациенты должны быть проинформированы о рисках, связанных с терапией алемтузумабом, а также о необходимости находиться под наблюдением в период лечения и в течение 48 месяцев после последней инфузии.
Премедикация
Пациентам необходимо проводить премедикацию кортикостероидами непосредственно перед введением препарата Лемтрада® в каждые первые 3 дня каждого курса лечения. В ходе клинических исследований премедикацию пациентам проводили с помощью 1000 мг метилпреднизолона, который вводили в каждый из первых 3 дней каждого курса лечения препаратом Лемтрада®.
Кроме того, дополнительно, можно рассмотреть вопрос о проведении перед введением препарата Лемтрада® премедикации антигистаминными средствами и/или антипиретиками (жаропонижающими средствами).
У всех пациентов необходимо применять пероральные средства для профилактики герпеса, начиная их применение в первый день каждого курса лечения и продолжая в течение как минимум 1 месяца после лечения препаратом Лемтрада®. При проведении клинических исследований пациентам вводили ацикловир в дозе 200 мг 2 в сутки или эквивалент.
Дозировка
Рекомендованная дозировка препарата Лемтрада® - 12 мг в сутки в виде внутривенной инфузии.
Проводят 2 курса терапии.
Первый курс терапии: 12 мг в сутки в течение 5 последовательных дней (общая доза - 60 мг).
Второй курс терапии: 12 мг в сутки в течение 3-х последовательных дней (общая доза - 36 мг). Проводится через 12 месяцев после первого курса терапии. Более длительный перерыв между курсами инфузий не изучался.
Пропущенные дозы не следует вводить в один и тот же день с введением запланированных
Способ применения
Содержимое флакона перед введением следует визуально проверить на наличие твердых частиц и изменение цвета. Не используйте препарат в случае наличия в растворе видимых частиц или изменения цвета.
Не встряхивайте флакон перед использованием.
Для внутривенного введения наберите 1,2 мл концентрата из флакона в стерильный шприц, соблюдая правила асептики. Введите набранный концентрат в 100 мл раствора натрия хлорида 9 мг/мл (0.9%) для инфузий или раствора глюкозы (5%) для инфузий. Нельзя разводить данный лекарственный препарат другими растворами. Осторожно переверните емкость для перемешивания раствора.
Препарат Лемтрада® не содержит антимикробных консервантов и, следовательно, необходимо соблюдать меры предосторожности, чтобы сохранить приготовленный раствор в стерильном состоянии. Рекомендуется вводить разведенный препарат немедленно. Каждый флакон предназначен только для однократного использования.
Любое количество неиспользованного лекарственного средства или отходы после его использования должны быть утилизированы в соответствии с местными нормативными требованиями.
Длительность внутривенной инфузии составляет приблизительно 4 часа. Если инфузия плохо переносится пациентом, можно уменьшить скорость введения препарата.
В случае крайней необходимости допускается хранение готового для применения раствора в защищенном от света месте при температуре 2 °- 8 °С не более 8 часов.
Побочное действие
При проведении совокупного анализа безопасности препарата Лемтрада® в выборку были включены 1188 пациентов с РРРС, получавших препарат Лемтрада® (в дозах 12 мг или 24 мг) в рамках контролируемых клинических исследований. При этом длительность последующего наблюдения в целях оценки безопасности составила 2363 пациенто-лет, а медиана последующего наблюдения - 24 месяца.
Наиболее важными нежелательными реакциями были: аутоиммунные заболевания (нарушения функции щитовидной железы, иммунная тромбоцитопеническая пурпура (ИТП), нефропатии, цитопении), инфузионные реакции и инфекционные заболевания.
Наиболее частыми нежелательными реакциями (≥20% пациентов) были сыпь, головная боль, лихорадка и инфекции дыхательных путей.
Приведенная ниже таблица основана на совокупных данных по безопасности за период 24 месяца, полученных в рамках исследований с участием пациентов с РРРС, получавших препарат Лемтрада® в дозе 12 мг в сутки в течение 5 последовательных дней в начале исследования и в течение 3 последовательных дней через 12 месяцев исследования. Нежелательные реакции, которые возникали у ≥0,5 % пациентов, указаны по системноорганным классам (СОК) согласно Медицинскому словарю регуляторной деятельности (MedDRA) и по терминам предпочтительного употребления (ТПУ). Частота оценивалась согласно следующим условным обозначениям: очень часто (≥ 1/10); часто (≥ 1/100 - < 1/10); нечасто (≥ 1/1000 - < 1/100). Внутри каждой группы частоты встречаемости нежелательные реакции представлены в порядке уменьшения их серьезности.
Нежелательные реакции, наблюдавшиеся у ≥ 0,5 % пациентов, получавших препарат Лемтрада® в дозе 12 мг в клинических исследованиях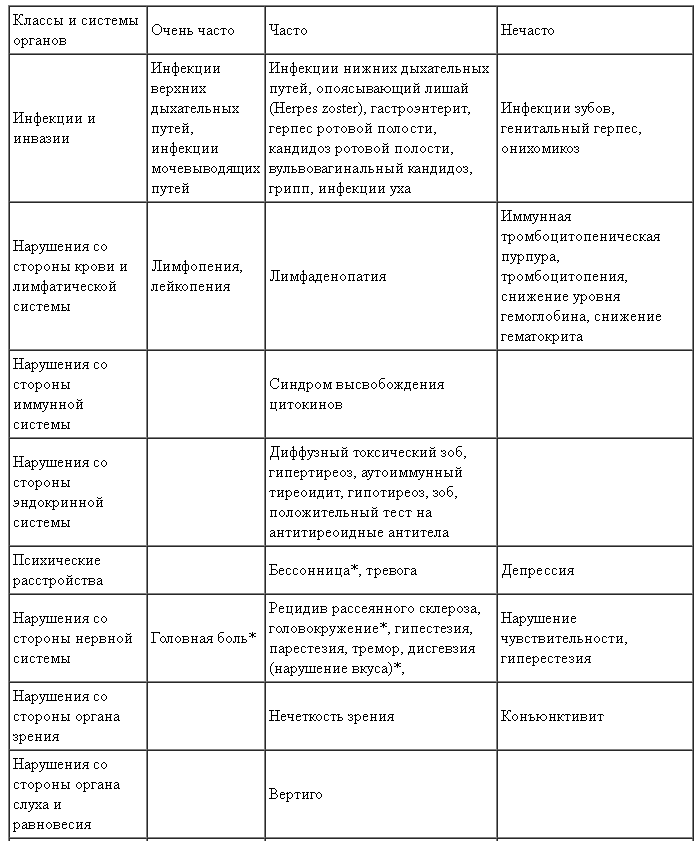
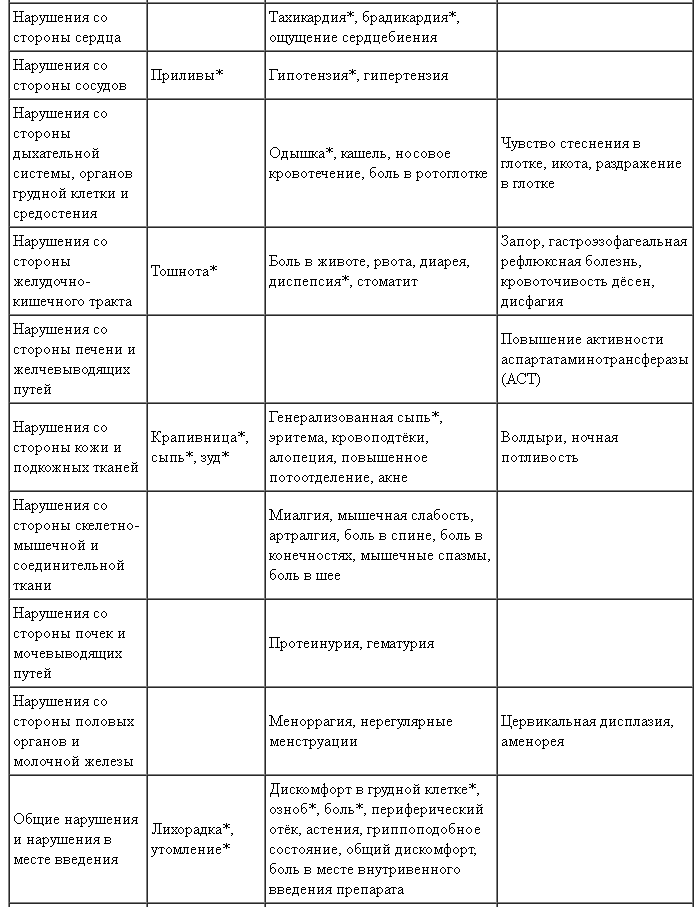

Описание отдельных нежелательных реакций
Термины, обозначенные звёздочкой (*) в таблице, включают нежелательные реакции, которые упоминаются при описании инфузионных реакций. Инфузионные реакции могут также включать фибрилляцию предсердий и анафилаксию, которые встречаются реже чем в 0,5 % случаях.
Передозировка
В ходе контролируемых клинических исследований два пациента с рассеянным склерозом по ошибке получили почти по 60 мг препарата Лемтрада® (т.е. полную дозу начального курса лечения) в одной инфузии, что привело к развитию тяжёлых нежелательных реакций (головная боль, сыпь, гипотензия или синусовая тахикардия). Применение препарата Лемтрада® в дозах, превышающих изученные в клинических исследованиях, может увеличить интенсивность и/или продолжительность инфузионных реакций или усилить воздействие препарата на иммунную систему.
Антидот при передозировке препарата Лемтрада® неизвестен. Лечение заключается в прекращении применения препарата и проведении поддерживающей терапии.
Взаимодействие с другими лекарственными средствами
Исследования с участием пациентов с рассеянным склерозом, направленные на изучение взаимодействия препарата Лемтрада®, применяемого в рекомендованных дозах, с другими лекарственными средствами, не проводились. В контролируемом клиническом исследовании у пациентов с рассеянным склерозом, которые незадолго до этого получали лечение бета-интерфероном и глатирамера ацетатом, возникла необходимость прекращения лечения за 28 дней до начала терапии препаратом Лемтрада®.
При лечении пациентов с рассеянным склерозом препарат Лемтрада® не назначали совместно с другими антинеопластическими или иммуносупрессивными препаратами или вслед за ними. Также, как в случае с другими иммуномодуляторами, принимая решение о назначении препарата Лемтрада®, следует учитывать потенциальные сочетанные воздействия данных лекарственных средств на иммунную систему пациента. Применение препарата Лемтрада® совместно с любым из препаратов данных групп может увеличить риск иммуносупрессии. Ввиду отсутствия исследований по изучению совместимости, не следует смешивать алемтузумаб с другими лекарственными препаратами. Не следует добавлять другие лекарственные средства или одновременно вводить их по одной и той же линии для внутривенных инфузий.
Для разведения данного лекарственного препарата не следует использовать иные растворители, кроме указанных в разделе «Способ применения и дозы».
Известные случаи несовместимости алемтузумаба и поливинилхлоридных (ПВХ) инфузионных пакетов, ПВХ инфузионных систем с выстилкой из ПВХ или полиэтилена, а также фильтров с низким уровнем связывания белков отсутствуют.
Особые указания
Необходимо прекратить прием интерферонов бета и глатирамера ацетат за 28 дней до начала лечения препаратом Лемтрада®.
Применение препарата Лемтрада® не рекомендуется пациентам, у которых наблюдается неактивное или стабильное течение заболевания.
Наблюдение за пациентами
Лечение рекомендуется проводить в виде двух курсов инфузий (см. раздел «Способ применения и дозы»). При этом пациенты должны находиться под наблюдением в период лечения и в течение 48 месяцев после последней инфузии.
Премедикация
Пациентам необходимо проводить премедикацию кортикостероидами непосредственно перед введением препарата Лемтрада® в каждые первые 3 дня каждого курса лечения. В ходе клинических исследований премедикацию пациентам проводили с помощью 1000 мг метилпреднизолона, который вводили в каждый из первых 3 дней каждого курса лечения препаратом Лемтрада®.
Кроме того, дополнительно, можно рассмотреть вопрос о проведении перед введением препарата Лемтрада® премедикации антигистаминными средствами и/или антипиретиками (жаропонижающими средствами).
У всех пациентов необходимо применять пероральные средства для профилактики герпеса, начиная их применение в первый день каждого курса лечения и продолжая в течение, как минимум, 1 месяца после лечения препаратом Лемтрада®. При проведении клинических исследований пациентам вводили ацикловир в дозе 200 мг 2 в сутки или эквивалент.
Почечная или печёночная недостаточность
В клинических исследованиях препарата Лемтрада® не участвовали пациенты с почечной или печёночной недостаточностью.
Педиатрическая популяция
Безопасность и эффективность препарата Лемтрада® у детей с рассеянным склерозом в возрасте от рождения до 18 лет не установлена. Нет опыта применения алемтузумаба у детей в возрасте от рождения до 10 лет для лечения рассеянного склероза.
Пожилые пациенты
В клинических исследованиях не принимали участия пациенты старше 55 лет. Нет данных о том, отличается ли ответ на лечение данной возрастной группы от такового у более молодых пациентов.
Инфузионные реакции
В контролируемых клинических исследованиях инфузионными реакциями считались любые нежелательные реакции, отмечавшиеся во время инфузии препарата Лемтрада® или в течение 24 часов после окончания инфузии. Большая часть из них может быть вызвана высвобождением цитокинов во время инфузии. В контролируемых клинических исследованиях у большинства пациентов с рассеянным склерозом, которые получали препарат Лемтрада®, развивались инфузионные реакции легкой или умеренной степени тяжести во время и/или в течение 24 часов после введения препарата Лемтрада® в дозе 12 мг. Наиболее частыми реакциями были головная боль, сыпь, лихорадка, тошнота, крапивница, кожный зуд, бессонница, озноб, «приливы», повышенная утомляемость, одышка, дисгевзия. дискомфорт в грудной клетке, генерализованная сыпь, тахикардия, брадикардия. диспепсия, головокружение и боль. Серьёзные реакции возникали у 3 % пациентов и включали лихорадку, крапивницу, фибрилляцию предсердий, тошноту, дискомфорт в грудной клетке и гипотонию. Клинические проявления анафилаксии могут быть сходными с клиническими проявлениями инфузионных реакций, но они, как правило, являются более тяжёлыми и жизнеугрожающими. В отличие от инфузионных реакций, анафилактические реакции встречаются редко.
Для уменьшения тяжести инфузионных реакций рекомендуется проведение премедикации. В контролируемых клинических исследованиях большая часть пациентов получала антигистаминные препараты и/или антипиретики (жаропонижающие средства), по меньшей мере, перед одной инфузией препарата Лемтрада®. Проведение премедикации не исключает развитие инфузионных реакций. Рекомендуется тщательно наблюдать за состоянием пациента во время инфузии препарата Лемтрада® и в течение 2 часов после её окончания. В случае развития инфузионных реакций, при необходимости следует провести соответствующее симптоматическое лечение. Как правило, длительность инфузии составляет 4 часа. Если инфузия плохо переносится пациентом, можно снизить скорость введения препарата. При возникновении тяжёлых инфузионных реакций нужно немедленно прекратить инфузию препарата. Во время проведения клинических исследований анафилактические или иные тяжёлые реакции, требующие прерывания лечения, отмечались очень редко.
Врач должен быть информирован о сердечно-сосудистых заболеваниях пациента, так как инфузионные реакции могут вызывать осложнения со стороны сердца, например, тахикардию.
Во время проведения инфузии должны быть доступны средства для лечения анафилактических или иных тяжёлых реакций.
Аутоимунные заболевания
На фоне лечения препаратом Лемтрада® могут образовываться аутоантитела, что может привести к развитию аутоиммунных заболеваний, включая заболевания щитовидной железы, иммунную тромбоцитопеническую пурпуру (ИТП) или, редко, нефропатию (например, анти-ГМБ болезнь [гломерулонефрит, обусловленный антителами к гломерулярной базальной мембране]). Следует соблюдать осторожность при лечении пациентов, имеющих в анамнезе иные (не рассеянный склероз) аутоиммунные заболевания. В то же время имеющиеся данные позволяют предположить, что лечение алемтузумабом не утяжеляет течение уже имеющихся аутоиммунных заболеваний.
Заболевания щитовидной железы
Аутоиммунные заболевания щитовидной железы были выявлены в течение 48 месяцев после первой инфузии приблизительно у 36% пациентов с рассеянным склерозом, которые получали препарат Лемтрада® в дозе 12 мг в рамках клинических исследований. Как в группе пациентов, получавших препарат Лемтрада®, так и в группе пациентов, получавших интерферон бета-1а (ИНФбета-1а), частота выявления заболеваний щитовидной железы была выше у пациентов с такой патологией в анамнезе. Пациенты, имеющие заболевания щитовидной железы, должны получать препарат Лемтрада® только в тех случаях, когда предполагаемая польза терапии превышает предполагаемый риск. У участников исследований отмечались как гипертиреоз, так и гипотиреоз. В большинстве случаев эти нарушения были легкой или умеренной степени тяжести. Тяжёлые заболевания наблюдались менее чем у 1 % пациентов и более чем у одного пациента, и включали тяжелые случаи диффузного токсического зоба, гипертиреоза и гипотиреоза. Для лечения заболеваний щитовидной железы применялась стандартная медикаментозная терапия, однако некоторым пациентам потребовалось хирургическое вмешательство. В клинических исследованиях пациентам, у которых развивались заболевания щитовидной железы, допускалось проведение повторного курса лечения препаратом Лемтрада®. Имеются ограниченные данные о том, что у пациентов, получавших повторный курс, обычно не наблюдалось ухудшения течения заболевания щитовидной железы. Вопрос о продолжении лечения препаратом Лемтрада® следует рассматривать индивидуально, учитывая при этом клиническое состояние пациента. Исследования функции щитовидной железы, такие как контроль уровня тиреотропного гормона, следует проводить до начала лечения и затем каждые 3 месяца в течение 48 месяцев после последней инфузии. По окончании этого периода анализы выполняются на основании клинических данных, позволяющих предположить нарушение функций щитовидной железы.
В клинических исследованиях не было выявлено связи между уровнем антител к тиреоидной пероксидазе (АТ-ТПО) и развитием нежелательных явлений со стороны щитовидной железы. У половины пациентов с исходными положительными титрами АТ-ТПО и у четверти пациентов с исходными отрицательными титрами АТ-ТПО в дальнейшем отмечались заболевания щитовидной железы. Подавляющее большинство (приблизительно 80 %) пациентов, у которых после лечения развились нежелательные явления со стороны щитовидной железы, имели исходный отрицательный титр АТ-ТПО. Следовательно, нежелательные явления со стороны щитовидной железы может развиться у пациента вне зависимости от исходного результата АТ-ТПО, и пациент периодически должен проходить все обследования, как описано выше.
Иммунная тромбоцитопеническая пурпура (ИТП)
Тяжелые случаи ИТП наблюдались примерно у 1 % пациентов с рассеянным склерозом, принимавших участие в контролируемых клинических исследованиях. Один случай ИТП не был вовремя диагностирован, так как он произошел до введения требований обязательного ежемесячного контроля клинического анализа крови. Пациент скончался от геморрагического инсульта. ИТП обычно развивается в период от 14 до 36 месяцев после первой инфузии препарата. Симптомы ИТП могут включать (но не ограничиваться ими) легко возникающие кожные кровоизлияния, точечные кровоизлияния (петехии), спонтанные кожно-слизистые кровотечения (например, носовое кровотечение, кровохарканье), более обильные, чем обычно, либо нерегулярные менструальные кровотечения. Кровохарканье может также быть проявлением анти-ГМБ болезни (см. ниже), поэтому следует проводить соответствующую дифференциальную диагностику. Пациент должен быть информирован о возможности возникновения этих симптомов, и в случае любых сомнений немедленно обращаться к врачу.
Полный клинический анализ крови с подсчетом форменных элементов следует выполнить до начала лечения, и затем ежемесячно в течение 48 месяцев после последней инфузии. После окончания данного периода анализы выполняются на основании клинических данных, позволяющих предположить ИТП. При подозрении на ИТП следует немедленно выполнить полный клинический анализ крови.
При подтверждении диагноза ИТП долны быть немедленно предприняты соответствующие меры, включая срочное направление к специалисту. Данные клинических исследований по изучению рассеянного склероза показали, что соблюдение требований режима мониторинга крови, а также обучение распознаванию признаков и симптомов ИТП, привело к ранней диагностике и лечению ИТП в большинстве случаев, развившихся при применении первого курса терапии.
Потенциальный риск развития ИТП, связанный с повторным лечением препаратом Лемтрада®, неизвестен.
Нефропатии
Нефропатии, включая анти-ГМБ болезнь, наблюдались у 0,3 % пациентов с рассеянным склерозом, принимавших участие в контролируемых клинических исследованиях. Как правило, они отмечались в течение 39 месяцев после последней инфузии препарата Лемтрада®. В клинических исследованиях отмечено два случая анти-ГМБ болезни. Оба случая были тяжёлыми, однако благодаря клиническому и лабораторному мониторингу были своевременно выявлены, и их лечение было успешным.
Клинические проявления нефропатии могут включать повышение уровня креатинина в сыворотке крови, гематурию и/или протеинурию. Несмотря на отсутствие случаев альвеолярного кровотечения в ходе клинических исследований, этот вид кровотечения, проявляющийся кровохарканьем, может развиваться при анти-ГМБ болезни. Кровохарканье также может быть признаком ИТП (см. выше), поэтому следует провести надлежащую дифференциальную диагностику. Пациент должен быть информирован о необходимости внимательно относиться к возможности появления этих симптомов, а в случае их развития немедленно обратиться за медицинской помощью.
Анти-ГМБ болезнь может привести к развитию почечной недостаточности, требующей проведения диализа и/или трансплантации при несвоевременно начатой терапии. При отсутствии лечения может возникнуть угроза для жизни.
Необходимо определить уровень креатинина и провести клинический анализ мочи с микроскопией осадка до начала терапии препаратом Лемтрада®. Данные обследования необходимо проводить ежемесячно в течение курса лечения, а также в дальнейшем в течение 48 месяцев после последней инфузии препарата Лемтрада®. Выявление клинически значимых отклонений от исходного значения креатинина сыворотки крови, необъяснимой гематурии и/или протеинурии может свидетельствовать о развитии нефропатии. Пациент должен быть немедленно направлен к соответствующему специалисту. Ранняя диагностика и лечение нефропатии могут снизить риск неблагоприятного исхода. После окончания периода 48 месяцев после последней инфузии анализы выполняются на основании клинических данных, позволяющих предположить нарушение функции почек.
Потенциальный риск развития нефропатии, связанный с повторным лечением препаратом Лемтрада®, неизвестен.
Цитопении
В клинических исследованиях аутоиммунные цитопении, такие как нейтропения. гемолитическая анемия и панцитопения, отмечались нечасто. Для своевременного выявления цитопений следует ежемесячно выполнять полный клинический анализ крови (см. подраздел «Иммунная тромбоцитопеническая пурпура»). Если цитопения подтверждается, следует немедленно предпринять соответствующие меры, включая направление пациента к специалисту.
Инфекционные заболевания
В контролируемых клинических исследованиях продолжительностью до двух лет с участием пациентов с рассеянным склерозом инфекционные заболевания возникали у 71 % пациентов, получавших препарат Лемтрада® в дозе 12 мг, тогда как в группе пациентов, получавших интерферон бета-1а (ИФНбета-1а) (44 мкг 3 раза в неделю), они возникали у 53 % пациентов; большинство этих инфекционных заболеваний были легкой или умеренной степени тяжести. Инфекционные заболевания, возникавшие более часто у пациентов, получавших препарат Лемтрада®, по сравнению с группой ИФНбета-1а, включали назофарингит, инфекции мочевыводящих путей, инфекции верхних дыхательных путей, синусит, герпес ротовой полости, грипп и бронхит. В контролируемых клинических исследованиях с участием пациентов с рассеянным склерозом тяжёлые инфекционные заболевания развивались у 2,7 % пациентов, получавших препарат Лемтрада®, и у 1 % пациентов, получавших ИФНбета-1а. Тяжёлые инфекционные заболевания в группе пациентов, получавших препарат Лемтрада®, включали аппендицит, гастроэнтерит, пневмонию, опоясывающий лишай и инфекции зубов. Как правило, продолжительность заболеваний была обычной, и они разрешались после применения стандартного медикаментозного лечения.
В клинических исследованиях тяжёлые инфекции, вызванные вирусом ветряной оспы (Varicella zoster), включая первичное и повторное инфицирование, чаще отмечались у пациентов, получавших препарат Лемтрада® в дозе 12 мг (0,3%), чем у пациентов, получавших ИФНбета-1а (0 %). В группе пациентов, получавших препарат Лемтрада® в дозе 12 мг, отмечались также случаи инфицирования вирусом папилломы человека (ВПЧ) (2 %), в том числе цервикальная дисплазия. Рекомендуется проводить ежегодный осмотр пациенток на предмет выявления ВПЧ.
В контролируемых клинических исследованиях также были выявлены случаи туберкулёза, как в группе пациентов, получавших препарат Лемтрада®, так и в группе пациентов, получавших ИФНбета-1а. Активный и латентный туберкулёз был отмечен у 0.3 % пациентов, получавших препарат Лемтрада®. Чаще всего эти случаи регистрировались в эндемичных зонах. До начала лечения в соответствии с локальными требованиями необходимо провести скрининг на наличие активного или латентного туберкулёза.
У пациентов, получавших лечение препаратом Лемтрада®, отмечались случаи развития листериоза/листериозного менингита. Эти инфекции развивались, обычно, в течение одного месяца после инфузии препарата Лемтрада®. Для снижения данного риска, пациенты, получающие препарат Лемтрада®", должны избегать употребления в пищу сырого и недостаточно термически обработанного мяса, сыров мягких сортов и непастеризованной молочной продукции в течение, как минимум, одного месяца после лечения препаратом Лемтрада®.
В контролируемых клинических исследованиях с участием пациентов с рассеянным склерозом поверхностные грибковые инфекции, особенно кандидоз полости рта и вагинальный кандидоз, чаще возникали у пациентов, получавших препарат Лемтрада®" (12 %), чем у пациентов, получавших ИФНбета-1а (3 %).
Если у пациента наблюдается активное инфекционное заболевание, врач должен отложить начало лечения препаратом Лемтрада®" до достижения полного контроля над течением заболевания.
Нет данных о влиянии препарата Лемтрада® на реактивацию вирусов гепатита В (ВГ-В) или гепатита С (ВГ-С), поскольку пациентов с признаками активных или хронических инфекционных заболеваний исключали из участия в клинических исследованиях. До начала лечения препаратом Лемтрада®" следует проводить скрининг на носительство вирусов ВГ-В и/или ВГ-С. Следует проявлять осторожность при назначении препарата Лемтрада® носителям вирусов ВГ-В и/или ВГ-С, поскольку есть риск реактивации вируса и развития необратимой печёночной недостаточности у пациентов этой группы.
Злокачественные новообразования
Так же, как и в случае с другими иммуномодуляторами, следует с осторожностью назначать препарат Лемтрада® пациентам с предшествовавшими и/или имеющимися злокачественными новообразованиями. В настоящий момент неизвестно, повышает ли алемтузумаб риск развития злокачественной опухоли щитовидной железы, поскольку аутоиммунное заболевание щитовидной железы может само по себе быть фактором риска малигнизации.
Контрацепция
Женщины детородного возраста должны использовать надёжные методы контрацепции во время лечения препаратом Лемтрада® и в течение 4 месяцев после последней инфузии препарата Лемтрада®.
Вакцинация
Пациентам рекомендуется соблюдать локальные требования к иммунизации не позднее чем за 6 недель до начала лечения препаратом Лемтрада®. Способность организма формировать иммунный ответ на какую-либо вакцину после лечения препаратом Лемтрада® не изучена.
В контролируемых клинических исследованиях с участием пациентов с рассеянным склерозом безопасность иммунизации живыми вирусными вакцинами после курса лечения препаратом Лемтрада® не изучалась. Пациентам, недавно прошедшим курс лечения препаратом Лемтрада®, не рекомендуется проводить иммунизацию живыми вирусными вакцинами.
Тестирование на антитела к вирусу ветряной оспы/вакцинация против инфекции, вызванной вирусом Varicella zoster
Как и в случае с любым другим иммуномодулирующим препаратом, до начала курса лечения препаратом Лемтрада® пациентам сотсутствием в анамнезе ветряной оспы и вакцинации против инфекции, вызванной вирусом Varicella zoster, следует пройти тестирование на антитела к вирусу Varicella zoster. Вакцинацию пациентов с отрицательным тестом антител к вирусу Varicella zoster следует проводить до начала лечения препаратом Лемтрада®. Для того, чтобы эффект вакцинации проявился полностью, лечение препаратом Лемтрада® нужно назначать не ранее, чем через 6 недель после вакцинации.
Рекомендуемые лабораторные исследования для наблюдения за пациентами
Лабораторные тесты следует выполнять с определенной периодичностью во время всего курса лечения, а также в течение 48 месяцев после последней инфузии препарата Лемтрада®, что позволит своевременно диагностировать аутоиммунные заболевания:
- Полный клинический анализ крови с подсчётом форменных элементов (до начала лечения и затем ежемесячно);
- Определение концентрации креатинина в сыворотке крови (до начала лечения и затем ежемесячно);
- Общий анализ мочи и микроскопия осадка (до начала лечения и затем ежемесячно);
- Исследование функции щитовидной железы, например, определение уровня тиреотропного гормона (ТТГ) (до начала лечения и затем каждые 3 месяца).
По окончании периода длительностью 48 месяцев после последней инфузии дополнительные обследования проводятся при появлении любых клинических признаков нефропатии или нарушения функции щитовидной железы.
Информация об использовании алемтузумаба вне рамок спонсируемых компанией исследовании до регистрации препарата Лемтрада®
Следующие нежелательные реакции были выявлены при использовании алемтузумаба для лечения В-клеточного хронического лимфоцитарного лейкоза (В-ХЛЛ), а также для лечения других заболеваний, как правило, в более высоких дозах (например. 30 мг) и с большей частотой, чем рекомендовано для лечения рассеянного склероза. Поскольку информация об этих реакциях поступала спонтанно и размер популяции, получавшей лечение, не определен, не всегда есть возможность достоверно оценить их частоту или выявить связь с приёмом алемтузумаба.
Аутоиммунные заболевания
Аутоиммунные заболевания, о развитии которых сообщалось на фоне терапии алемтузумабом, включают нейтропению, гемолитическую анемию (включая один летальный случай), приобретённую гемофилию, анти-ГМБ болезнь и заболевания щитовидной железы. Тяжёлые и иногда аутоиммунные заболевания с летальным исходом, включая аутоиммунную гемолитическую анемию, аутоиммунную тромбоцитопению, апластическую анемию, синдром Гийена-Барре и хроническую воспалительную демиелинизирующую полирадикулонейропатию, описаны у пациентов без рассеянного склероза и получавших алемтузумаб. У одного пациента со злокачественным новообразованием, получавшего алемтузумаб, была отмечена положительная реакция Кумбса. У другого пациента с онкологическим заболеванием инфузия привела к летальному исходу в связи с развитием реакции «трансплантат против хозяина».
Инфузионные реакции
Тяжёлые и иногда инфузионные реакции с летальным исходом, включая бронхоспазм, гипоксию, обморок, лёгочные инфильтраты, острый респираторный дистресс-синдром, остановку дыхания, инфаркт миокарда, аритмии, острую сердечную недостаточность и остановку сердца, наблюдались у пациентов без рассеянного склероза и получавших алемтузумаб в более высоких дозах и с большей частотой, чем рекомендовано для лечения рассеянного склероза. Как правило, эти реакции протекали тяжелее, чем у пациентов с рассеянным склерозом. Также сообщалось о тяжёлых анафилактических реакциях и других реакциях гиперчувствительности, включая анафилактический шок и отёк Квинке.
Инфекции и инвазии
Сообщалось о тяжёлых и иногда с летальным исходом вирусных, бактериальных, протозойных и грибковых инфекционных заболеваниях, включая случаи, вызванные реактивацией латентных инфекций, у пациентов без рассеянного склероза и получавших алемтузумаб в более высоких дозах и с большей частотой, чем рекомендовано для лечения РС. Как правило, эти инфекции протекали тяжелее, чем у пациентов с рассеянным склерозом. Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) наблюдалась с одинаковой частотой у пациентов с В-ХЛЛ, как получавших, так и не получавших терпию алемтузумабом.
Заболевания крови и лимфатической систем
Тяжёлые кровотечения на фоне терапии алемтузумабом наблюдались у пациентов без рассеянного склероза.
Нарушения со стороны сердца
У пациентов без рассеянного склероза и получавших потенциально кардиотоксичные препараты до начала терапии алемтузумабом, отмечались застойная сердечная недостаточность, кардиомиопатия и снижение фракции выброса.
Лимфопролиферативные заболевания, вызванные вирусом Эпштейна-Барр
В не спонсируемых компанией исследованиях наблюдались лимфопролиферативные заболевания, вызванные вирусом Эпштейна-Барр.
Влияние на способность управлять транспортными средствами и работать с механизмами
Исследований по оценке влияния препарата Лемтрада® на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности не проводилось.
У многих пациентов во время лечения препаратом Лемтрада® или в течение 24 часов после проведения инфузии развивались инфузионные реакции. Некоторые из этих реакций (например, головокружение) могут оказать временное влияние на способность пациента управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности. С учетом возможных побочных эффектов, необходимо соблюдать осторожность при управлении транспортом и работе с механизмами.
Форма выпуска
По 1,2 мл концентрата для приготовления раствора для инфузий, 10 мг/мл во флаконы из прозрачного бесцветного стекла гидролитического типа I номинальной вместимостью 2 мл, которые укупоривают серыми бутилкаучуковыми пробками и закатывают алюминиевыми колпачками, снабженными отрывными пластиковыми дисками.
По 1 флакону вместе с инструкцией по применению помещают в картонную пачку.
Условия хранения
Хранить в защищенном от света месте при температуре 2 °- 8 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не использовать по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
Джензайм Европа БВ, Нидерланды.
Фирма-производитель (выпускающий контроль качества)
1)Джензайм Лтд., Великобритания.
Genzyme Ltd., United Kingdom.
37 Hollands Road, Haverhill, Suffolk, CB9 8PU, United Kingdom.
2)Джензайм Ирландия Лимитед, Ирландия.
Genzyme Ireland Limited, Ireland.
IDA Industrial Park, Old Kilmeaden Road, Waterford, Ireland.
Производитель готовой лекарственной формы
Берингер Ингельхайм Фарма ГмбХ и Ко. КГ. Германия.
Boehringer Ingelheim Pharma GmbH & Co. KG, Germany.
Birkendorfer Str. 65, 88397 Biberach an der Riss, Germany.
Претензии потребителей направлять по адресу в России:
АО «Санофи Россия».
125009, г. Москва, ул. Тверская, д. 22.
Комментарии
ПРАКТИКА ПЕДИАТРА
