Иннонафактор - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер
ЛП 002662 - 260417
Торговое наименование препарата:
Иннонафактор
МНН:
нонаког альфа.
Лекарственная форма:
лиофилизат для приготовления раствора для внутривенного введения.
Состав
1 флакон с препаратом содержит:
|
активное вещество: нонаког альфа (rFIX) |
250 ME |
500 ME |
1000 ME; |
|
вспомогательные вещества: |
|||
|
гистидин |
3,88 мг, |
7,76 мг, |
15,52 мг; |
|
сахароза |
25,0 мг, |
50,0 мг, |
100,0 мг; |
|
глицин |
48,8 мг, |
97,6 мг, |
195,2 мг; |
|
натрия хлорид |
5,85 мг, |
11,7 мг, |
23,4 мг; |
|
полисорбат 80 |
0,14 мг, |
0,28 мг, |
0,56 мг. |
1 флакон с растворителем содержит: воду для инъекций
Описание:
аморфная масса белого цвета.
5 мл или 10 мл.
Характеристика препарата
Активным веществом препарата Иннонафактор является рекомбинантный фактор свертывания крови IX (нонаког альфа), представляющий собой одноцепочечный гликопротеин с молекулярной массой около 55 кДа, состоящий из 415 аминокислотных остатков. Нонаког альфа принадлежит к семейству сериновых протеаз и является витамин К-зависимым фактором свертывания крови.
Рекомбинантный фактор свертывания крови IX продуцируется модифицированной перевиваемой линией клеток яичников китайского хомячка СНО 1Е6 с использованием технологий рекомбинантной ДНК.
Фармакотерапевтическая группа:
гемостатическое средство.
Код ATX: B02BD09
Фармакологические свойства
Фармакодинамические свойства
Структурные и функциональные свойства рекомбинантного фактора свертывания крови IX сходны с эндогенным фактором свертывания крови IX. В процессе свертывания крови фактор IX активируется фактором свертывания крови Vila в комплексе с тканевым фактором по внешнему механизму свертывания крови, а также фактором свертывания крови Х1а по внутреннему механизму свертывания крови. Активированный фактор свертывания крови IX в комбинации с активированным фактором свертывания крови VIII приводят к активации фактора свертывания крови X, который обеспечивает превращение протромбина в тромбин. Тромбин активизирует процесс преобразования фибриногена в фибрин с образованием кровяного сгустка.
У пациентов, страдающих гемофилией В, активность фактора свертывания крови IX значительно снижена, что требует проведения заместительной терапии, которая обеспечивает временную нормализацию содержания фактора IX и устранение геморрагических проявлений заболевания.
Фармакокинетические свойства
Значение степени восстановления активности Иннонафактора находится в диапазоне от 32,2 до 55,9 % и в среднем составляет 42±8,4 %. Показатель повышения активности Иннонафактора (К-value) составляет от 0,77 до 1,41 МЕ/дл на МЕ/кг и в среднем равен 1,05±0,21 МЕ/дл на МЕ/кг. Максимальная концентрация (Cmax) Иннонафактора составляет 53,18 МЕ/дл (от 41,6 до 70,3 МЕ/дл). AUCo-964 составляет 1069,9 МЕ*ч/дл. Период полувыведения Иннонафактора варьирует от 16,5 до 33 часов (в среднем - 24 ±7,7 часов). Среднее значение клиренса составляет 3,62 дл/ч.
Показания к применению
Лечение и профилактика кровотечений у пациентов с гемофилией В (врожденной недостаточностью фактора свертывания крови IX) в возрасте 18 лет и старше.
Противопоказания к применению
Повышенная чувствительность к белкам хомячков или непереносимость любого из компонентов, входящих в состав препарата. Возраст моложе 18 лет (опыт применения отсутствует).
Способ применения и дозы
Иннонафактор вводится внутривенно струйно медленно в течение 2-5 минут, после восстановления лиофилизата прилагаемым растворителем. Скорость введения определяется врачом и может зависеть от переносимости препарата пациентом.
Препарат не следует вводить капельно или смешивать с инфузионными растворами, ввиду отсутствия информации о длительном инфузионном введении фактора свертывания крови IX.
Доза фактора свертывания крови IX выражается в международных единицах (ME). 1 ME фактора свертывания крови IX эквивалентна количеству фактора IX в 1 мл плазмы крови здорового человека.
Активность фактора свертывания IX в плазме крови выражается либо в процентах (соответствует нормальным значениям плазмы крови человека), либо в международных единицах на единицу объема (МЕ/дл).
Расчет требуемой дозы фактора свертывания крови IX основан на эмпирических исследованиях, согласно которым введение 1 ME нонакога альфа на кг массы тела повышает активность фактора свертывания FIX в плазме крови в среднем на 0,8 - 1,0 МЕ/дл (диапазон вариации - от 0,7 до 1,4 МЕ/дл) у взрослых пациентов.
Необходимая доза введения Иннонафактора рассчитывается по следующей формуле:
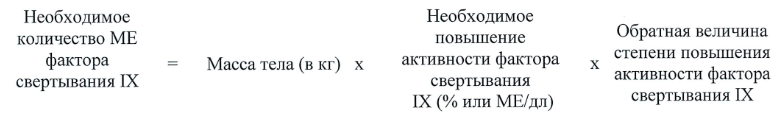
Таким образом, при среднем повышении активности фактора свертывания IX, соответствующем 0,8 МЕ/дл:

При развитии приведенных ниже в таблице геморрагических состояний, активность фактора IX в плазме крови не должна опускаться ниже указанных уровней (в % от нормальной или в МЕ/дл) в течение соответствующего периода времени.
При обширных оперативных вмешательствах заместительную терапию нонакогом альфа необходимо контролировать при помощи коагуляционного анализа (определения активности фактора свертывания крови IX в плазме крови). Возможны индивидуальные особенности реакции пациентов на лечение фактором свертывания крови IX, вследствие разных показателей восстановления активности in vivo и периода полувыведения препарата. Применение рекомбинантного фактора свертывания крови IX более 1 раза в сутки, как правило, не требуется.
Иннонафактор может применяться в качестве долгосрочной профилактики кровотечений у пациентов, страдающих тяжелой формой гемофилии В. Средняя доза препарата при применении в качестве вторичной профилактики у пациентов, ранее получавших терапию факторами свертывания, составляет в среднем 40 - 50 МЕ/кг с интервалом введения от 3 до 4 дней. У пациентов молодого возраста может потребоваться сокращение интервалов между введениями или повышение дозы препарата.
Таблица расчета доз препарата при различных кровотечениях и в хирургической практике
|
Тяжесть кровотечения или вид оперативного вмешательства |
Необходимая активность фактора IX (% или МЕ/дл) |
Периодичность введения (часы)/ продолжительность терапии (дни) |
|
Кровотечение: |
||
|
Ранний гемартроз, кровоизлияние в мышцу или кровотечение в полости рта |
20-40 |
Повторные инъекции препарата каждые 24 часа, как минимум 1 день до остановки кровотечения, что определяется по разрешению болевого синдрома или заживлению раны. |
|
Более выраженные гемартроз, кровоизлияние в мышцу или гематома |
30-60 |
Повторные инъекции каждые 24 часа в течение 3-4 дней или более, до разрешения болевого синдрома и острого нарушения функции. |
|
Жизнеугрожающее кровотечение |
60-100 |
Повторные инъекции каждые 8-24 часа до устранения угрозы жизни. |
|
Оперативное вмешательство: |
||
|
Малое, включая удаление зуба |
30-60 |
Повторные инъекции каждые 24 часа, в течение минимум 1 дня, до заживления раны. |
|
Обширное |
80-100 (до и после операции) |
Повторные инъекции каждые 8-24 часа, до адекватного заживления раны, затем терапия на протяжении не менее 7 дней для поддержания активности фактора IX на уровне 30-60 % или МЕ/дл. |
Применение у пациентов с заболеваниями печени и почек
Необходимость изменения дозы препарата Иннонафактор у пациентов с заболеваниями печени и почек в клинических исследованиях не изучалась.
Применение в педиатрии
Опыт применения препарата Иннонафактор у пациентов моложе 18 лет отсутствует.
Применение при беременности и в период лактации
Влияние препарата Иннонафактор на репродуктивную систему в ходе доклинических исследований на животных не оценивалось. Учитывая редкость возникновения гемофилии В у женщин, данные о применении препаратов фактора свертывания крови IX при беременности и в период лактации отсутствуют. В связи с чем, применять препарат Иннонафактор у беременных женщин следует только при наличии жизненных показаний.
Правила приготовления раствора для инъекции
Правила приготовления раствора для внутривенного введения
Общие положения
1. Тщательно вымойте руки перед проведением нижеописанных процедур и выполняйте правила асептики в процессе приготовления и введения раствора препарата.
2. Открытые медицинские материалы используйте, по возможности, быстро, чтобы сократить до минимума время их контакта с атмосферным воздухом.
3. Возьмите флакон с препаратом и растворителем, вынутые из холодильника, и слегка нагрейте, например, подержав их в руках. Не допускается нагревание препарата выше 37 °С.
4. Поставьте оба флакона на чистую ровную поверхность.
5. Снимите защитную пластиковую накладку с каждого флакона.
6. Обработайте резиновые пробки флаконов салфеткой спиртовой. Дайте им высохнуть перед использованием. Не прикасайтесь руками или другими предметами к обработанным поверхностям.
Использование канюль
7. Откройте блистерную упаковку канюли. Снимите защитный колпачок с иглы канюли
(рис. 1).
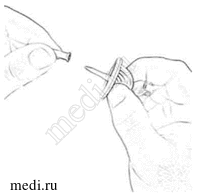
Рисунок 1
8. Введите пластиковую иглу канюли вертикально в центр резиновой пробки флакона с растворителем до упора (рис. 2).
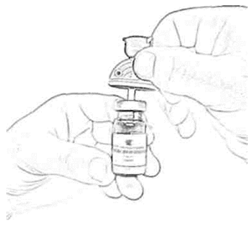
Рисунок 2
9. Откройте блистерную упаковку шприца, отогнув до середины бумажное покрытие, откройте синюю защитную крышечку канюли и вставьте шприц в отверстие канюли (рис. 3). Убедитесь в плотности соединения.

Рисунок 3
10. Переверните флакон вверх дном и отберите в шприц, указанное ниже количество растворителя, плавно оттягивая поршень,
- для дозировки 250 ME - 2,5 мл;
- для дозировки 500 ME - 5 мл;
- для дозировки 1000 ME - 10 мл.
11. Откройте блистерную упаковку второй канюли, снимите защитный колпачок с иглы и введите пластиковую иглу в центр резиновой пробки флакона с препаратом, до упора (рис. 4).
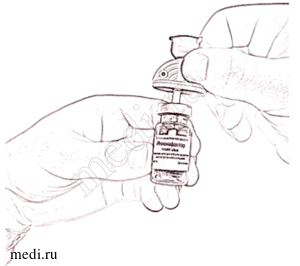
Рисунок 4
12. Удалите наполненный шприц из первой канюли (см. поз. 10), оставив переходник в пробке флакона с остатком растворителя. Следите за тем, чтобы кончик шприца не соприкасался с рукой или другими посторонними предметами.
13. Вставьте наполненный шприц с растворителем во вторую канюлю, помещенную на флаконе с лиофилизатом, открыв синюю защитную крышечку (рис. 5). Убедитесь в плотности соединения.
14. Осторожно нажимая на стержень поршня и слегка наклоняя флакон, медленно введите соответствующий объем растворителя (см. п. 10) по стенке флакона через канюлю (рис. 5), избегая пенообразования и соприкосновения иглы с раствором препарата. Эффект «вспенивания» появляется, если растворитель попадает непосредственно на лиофилизат.
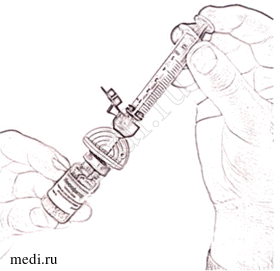
Рисунок 5
15. Осторожно покачивайте флакон круговыми движениями, пока лиофилизат не растворится полностью (рис. 6). Не встряхивайте флакон. При наличии любых включений или мутности не используйте приготовленный раствор.

Рисунок 6
16. Держа флакон в слегка наклоненном положении, медленно и плавно оттягивая поршень, отберите из него весь приготовленный раствор в шприц через канюлю. Перевернув флакон вверх дном, удалите пузырьки воздуха из шприца (рис. 7). Отложите флакон со шприцем и канюлей до следующей манипуляции.

Рисунок 7
17. Откройте блистерную упаковку катетера для периферических вен.
18. Не меняя положения поршня (см. п. 16), удалите наполненный шприц из канюли, оставив переходник в пробке пустого флакона.
Дальнейшие манипуляции описаны в конце раздела «Использование адаптера для флаконов», подраздел «Общие положения», начиная с пункта 17.
Использование адаптера для флаконов.
7. Откройте блистерную упаковку адаптера для флаконов.
8. Наденьте адаптер на флакон с растворителем до слабого щелчка - прокола пробки (рис. 8).
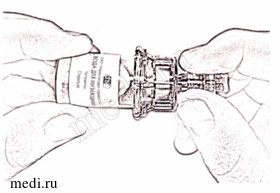
Рисунок 8
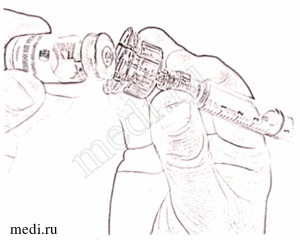
9. Откройте блистерную упаковку шприца с резьбовым соединением, отогнув до середины бумажное покрытие, и вверните резьбовой разъем шприца в резьбовой разъем адаптера (рис. 9). Убедитесь в плотности соединения.

Рисунок 9
10. Переверните флакон вверх дном и отберите в шприц, указанное ниже количество растворителя, плавно оттягивая поршень,
- для дозировки 250 ME - 2,5 мл;
- для дозировки 500 ME - 5 мл;
- для дозировки 1000 ME - 10 мл.
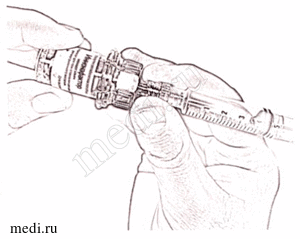
12. Осторожно нажимая на стержень поршня и слегка наклоняя флакон, медленно введите соответствующий объем растворителя (см. п. 10) по стенке флакона через адаптер (рис. 12), избегая пенообразования и соприкосновения иглы с раствором препарата. Эффект «вспенивания» появляется, если растворитель попадает непосредственно на лиофилизат.
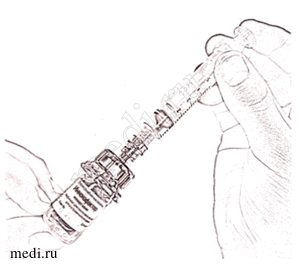
Рисунок 12
13. Осторожно покачивайте флакон круговыми движениями, пока лиофилизат не растворится полностью (рис. 13). Не встряхивайте флакон. При наличии любых включений или мутности не используйте приготовленный раствор.

Рисунок 13
14. Держа флакон в слегка наклоненном положении, медленно и плавно оттягивая поршень, отберите из него весь приготовленный раствор в шприц через адаптер. Перевернув флакон вверх дном, удалите пузырьки воздуха из шприца (рис. 14). Отложите флакон со шприцем и адаптером до следующей манипуляции.

Рисунок 14
15. Откройте блистерную упаковку катетера для периферических вен.
16. Не меняя положения поршня (см. п. 14), удалите наполненный шприц из адаптера, оставив переходник в пробке пустого флакона.
Общие положения
17.Снимите защитную заглушку с трубки катетера. Присоедините шприц к катетеру, (шприц с резьбовым соединением провер ните по часовой стрелке до упора) (рис. 15). Убедитесь в плотности соединения.
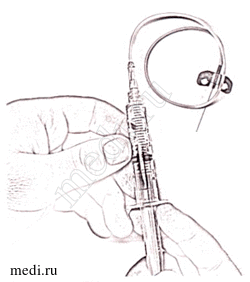
Рисунок 15
18. Обработайте место инъекции прилагаемой салфеткой спиртовой.
19. Снимите защитный колпачок с иглы катетера. Удалите воздух из присоединенной системы для внутривенного введения и введите раствор внутривенно струйно медленно (в течение 2-5 минут), закрепив иглу пластырем фиксирующим.
20. Обеспечьте безопасную утилизацию всех использованных материалов.
Компоненты комплекта для приготовления раствора для внутривенного введения изображены на рисунке 16.
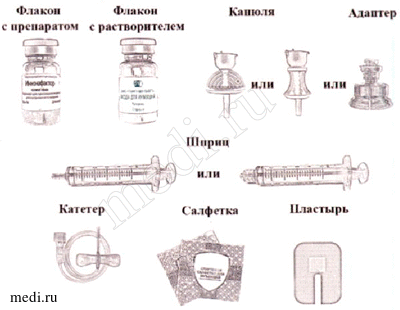
Рисунок 16
Если необходимо ввести более одной дозы препарата, аналогичным образом приготовьте раствор во флаконе из другой упаковки, используя прилагаемый растворитель, а затем соедините растворы в шприце большего объема (не прилагается) и введите приготовленный раствор в обычном порядке.
Приготовленный раствор должен использоваться сразу после разведения.
Если инъекция по какой-либо причине откладывается, флакон с раствором препарата следует хранить при температуре от 2 до 8 °С не более 3 часов без замораживания. Неиспользованный за это время раствор не должен применяться, он подлежит утилизации.
Побочное действие
Применение нонакога альфа в некоторых случаях может сопровождаться развитием ряда побочных эффектов со следующей частотой: нечастые (с частотой от > 1/1000 до < 1/100) и редкие (с частотой от >1/10000 до <1/1000). Наиболее значимыми побочными эффектами являются: анафилаксия, флегмона, флебит и образование нейтрализующих антител.
Внутри каждой категории частоты побочные эффекты приведены в порядке снижения степени их серьезности.
Нарушения со стороны нервной системы
Нечастые: головокружение, головная боль, предобморочное состояние, изменение вкусового восприятия.
Редкие: тремор, сонливость, нарушение вкусовых ощущений.
Нарушения со стороны пищеварительной системы
Нечастые: тошнота. Редкие: рвота, диарея.
Системные нарушения и осложнения в месте введения
Нечастые: флегмона в области введения, флебит в области введения, кожные и другие реакции в месте введения (в том числе жжение и ощущение стягивания), дискомфорт в месте введения, боль в месте введения.
Редкие: лихорадка.
Нарушения со стороны иммунной системы
Нечастые: образование нейтрализующих антител (ингибиторов фактора свертывания крови IX) кратковременно в низком титре (см. раздел «Особые указания»).
Редкие: гиперчувствительность, аллергические реакции, в том числе анафилаксия (см. раздел «Особые указания»), ларингоспазм, бронхоспазм или респираторный дистресс-синдром (диспноэ), свистящий кашель, снижение артериального давления, ангионевротический отек, отек гортани, тахикардия, чувство стеснения в грудной клетке, крапивница, кожные высыпания, ощущение жжения в области нижней челюсти и черепа, озноб (дрожь), ощущение покалывания, «приливы» крови к лицу, заторможенность, беспокойство, сухой кашель или чихание, снижение четкости зрения (см. раздел «Особые указания»), аллергический ринит, слабость, анафилаксия.
Респираторные, торакальные и медиастинальные нарушения
Нечастые: кашель, приводящий к гипоксии.
Прочие
Редкие: дрожь, реакции фоточувствительности.
Изменения лабораторных показателей
Нечастые: повышение активности аспартатаминотрансферазы, повышение активности аланинаминотрансферазы, повышение концентрации билирубина, повышение активности креатинфосфокиназы, повышение активности щелочной фосфатазы.
Имеются данные о возможности развития цианоза и снижении артериального давления.
Нарушения со стороны мочевыделительной системы
Имеются данные о развитии инфаркта почки через 12 дней после введения нонакога альфа по поводу геморрагического состояния у 1 пациента с антителами к вирусу гепатита С.
Тромботические осложнения
На фоне лечения нонакогом альфа сообщалось о случаях развития тромбозов, в том числе, угрожающего жизни синдрома верхней полой вены у новорожденных, находившихся в тяжелом состоянии и получавших нонаког альфа в виде длительной инфузии через центральный венозный катетер. Также зарегистрированы случаи тромбофлебита периферических вен и тромбоза глубоких вен преимущественно после длительных внутривенных инфузий, не зарегистрированных в качестве метода введения данного препарата.
Неадекватный ответ и неадекватная степень восстановления активности фактора свертывания крови IX
Имеется информация о случаях неадекватного ответа и неадекватной степени восстановления активности фактора свертывания крови IX при применении нонакога альфа.
При развитии любых побочных эффектов, которые, предположительно, могут быть связаны с введением препарата, необходимо снизить скорость введения или приостановить его.
Передозировка
Случаев передозировки Иннонафактора не описано.
Взаимодействие с другими препаратами
Лекарственного взаимодействия не описано.
Особые указания
У пациентов, ранее получавших терапию препаратами фактора свертывания крови IX, иногда отмечается образование активных нейтрализующих антител (ингибиторов). Анализ на наличие ингибиторов к фактору свертывания крови IX, титр которых измеряется в единицах Бетезда (БЕ), проводится при невозможности достичь ожидаемого уровня активности фактора свертывания крови IX или остановить кровотечение при введении рассчитанной дозы, с помощью адекватных тестов. При наличии высоких концентраций ингибиторов к фактору свертывания крови IX терапия нонакогом альфа может оказаться неэффективной. В данном случае может потребоваться использование альтернативных методов лечения. Ведение таких пациентов должно осуществляться врачами, имеющими опыт лечения пациентов с гемофилией В.
В клинических исследованиях препарата Иннонафактор не было включено достаточного количества пациентов в возрасте 65 лет и старше, что не позволяет оценить различие ответа на лечение по сравнению с более молодым возрастом. При назначении Иннонафактора пациентам различного возраста может потребоваться индивидуальная коррекция дозы препарата.
Внутривенное введение любых белковых препаратов, в том числе рекомбинантного фактора свертывания крови IX, может сопровождаться развитием реакции гиперчувствительности, связанной с наличием следовых остаточных количеств белков штамма-продуцента, переносимых в ходе технологического процесса производства. При использовании рекомбинантного фактора свертывания крови IX возможно также развитие анафилактических и анафилактоидных реакций.
Кроме этого, аллергические реакции могут быть связаны с появлением ингибиторов к фактору свертывания крови IX, в связи с чем пациенты с аллергическими реакциями в анамнезе должны быть обследованы на наличие ингибиторов. Необходимо учитывать, что у пациентов, имеющих ингибиторы к фактору свертывания крови IX, может отмечаться повышение риска анафилактических реакций и при последующих введениях фактора свертывания крови IX. Имеются данные о более высоком риске образования ингибиторных антител, а также развития острых реакций гиперчувствительности у пациентов с делецией гена фактора свертывания крови IX. В случае выявления у пациентов делеции гена, кодирующего синтез фактора свертывания крови IX, необходимо тщательное наблюдение за возможным развитием клинических проявлений острых реакций гиперчувствительности, особенно в течение начальной фазы терапии.
Пациентов необходимо информировать о ранних клинических признаках реакций гиперчувствительности, в том числе появлении затруднения дыхания, крапивницы, кожного зуда, развитии отека, ощущения сдавления грудной клетки, бронхоспазма, ларингоспазма, свистящего дыхания, артериальной гипотензии, снижения четкости зрения и анафилаксии. При развитии аллергической реакции или анафилактического шока необходимо немедленно прекратить введение препарата Иннонафактор и начать соответствующую стандартную терапию. При развитии тяжелых аллергических реакций следует рассмотреть вопрос о назначении альтернативной гемостатической терапии. Принципы лечения зависят от вида и тяжести побочных эффектов.
Ввиду наличия риска развития аллергических реакций, первые введения препарата Иннонафактор целесообразно выполнять под медицинским наблюдением в учреждениях, где имеются условия для оказания соответствующей экстренной помощи.
Дозы и длительность заместительной терапии зависят от степени дефицита фактора свертывания крови IX, локализации и выраженности кровотечения, общего состояния пациента, клинического эффекта проводимой терапии и индивидуальных параметров фармакокинетики пациента. Доза препарата Иннонафактор может отличаться от доз плазменных препаратов фактора свертывания крови IX. Для обеспечения необходимой активности фактора IX в крови при заместительной терапии рекомендуется контролировать уровень фактора свертывания крови IX в плазме посредством коагуляционного анализа.
Несмотря на то, что препарат Иннонафактор не содержит других активных веществ, необходимо иметь в виду риск развития тромбозов и синдрома диссеминированного внутрисосудистого свертывания (ДВС). Поскольку назначение ранее применявшихся факторов свертывания крови II, IX, X в комбинации и протромбинового комплекса ассоциировалось с развитием тромбоэмболических осложнений, риск их развития будет возрастать при лечении препаратами фактора свертывания крови IX пациентов, страдающих ДВС синдромом и пациентов с признаками фибринолиза.
Учитывая потенциальный риск тромбоэмболии при введении рекомбинантного фактора свертывания крови IX пациентам, страдающим заболеваниями печени, в послеоперационном периоде, имеющим риск развития тромбозов или ДВС-синдрома, необходимо осуществление наблюдения для выявления ранних проявлений тромботических осложнений с использованием соответствующих тестов, а при их развитии - проведение соответствующего лечения. В каждой из этих ситуаций следует оценивать соотношение потенциальной пользы терапии рекомбинантным фактором свертывания крови IX и риска развития этих осложнений.
С целью снижения вероятности развития агглютинации в шприце или системе для внутривенного введения целесообразно ограничить попадание в них крови при введении препарата. В случае развития агглютинации эритроцитов в системе или шприце необходимо утилизировать использовавшиеся расходные материалы (систему для внутривенных инфузий, шприц и раствор препарата Иннонафактор) и повторить введение с использованием новой упаковки препарата.
При попытках индукции иммунной толерантности у больных гемофилией В, вырабатывающих ингибиторы фактора свертывания крови IX и имевших аллергические реакции в анамнезе, отмечались случаи развития нефротического синдрома. Безопасность и эффективность применения препарата Иннонафактор с целью индукции иммунной толерантности не определены.
Влияние на способность управлять транспортными средствами
Исследования влияния препарата на способность к управлению автомобилем и работе с механизмами, требующими повышенной концентрации внимания, не проводились.
Форма выпуска
Лиофилизат для приготовления раствора для внутривенного введения по 250 ME, 500 ME или 1000 ME в стеклянных флаконах, укупоренных пробками резиновыми с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 5 или 10 мл растворителя (воды для инъекций) в стеклянных флаконах, укупоренных колпачками комбинированными с элементами эластомерными.
1 флакон с препаратом и 1 флакон с растворителем - в контурной ячейковой упаковке из пленки поливинилхлоридной или полиэтилентерефталатной.
1 контурная ячейковая упаковка в комплекте с расходными медицинскими материалами: шприцем без иглы вместимостью 5 или 10 мл, 2 иглами для разведения, фильтром инъекционным, катетером для периферических вен, пластырем фиксирующим, 2 салфетками спиртовыми и инструкцией по применению помещены в пачку из картона.
Каждый компонент расходных медицинских материалов помещен в стерильную одноразовую упаковку из пленки поливинилхлоридной и бумаги ламинированной. Салфетка спиртовая упакована в многослойный материал, состоящий из фольги алюминиевой и пленки полиэтиленовой.
На стыки крышки и дна с передней и задней гранями пачки наклеены самоклеящиеся немаркированные этикетки для контроля первого вскрытия.
Срок годности
Препарата - 2 года, растворителя - 2 года 6 мес.
Не использовать позже срока, указанного на упаковке.
Условия хранения
В защищенном от света месте, при температуре от 2 до 8 С. Не замораживать. Хранить в местах, недоступных для детей.
Условия отпуска из аптек
Юридическое лицо, на имя которого выдано регистрационное удостоверение
АО «ГЕНЕРИУМ»,
Российская Федерация, 601125, Владимирская обл., Петушинский район, пос. Бельгийский, корпус 17,
Производитель
АО «ГЕНЕРИУМ»,
Российская Федерация, 601125, Владимирская обл., Петушинский район, пос. Бельгийский, корпус 17.
АО «Эс Джи Биотех» (упаковка и выпускающий контроль качества),
Российская Федерация, 601125, Владимирская обл., Петушинский район,
пос. Вольгинский, ул. Владимирская, дом 18.
Претензии потребителей направлять в адрес
АО «ГЕНЕРИУМ», Российская Федерация,
601125, Владимирская обл., Петушинский район,
пос. Вольгинский, корпус 17.
Комментарии
ПРАКТИКА ПЕДИАТРА
