Эраксис - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер:
ЛП-001066
Торговое название препарата:
Эраксис®Международное непатентованное название:
анидулафунгинЛекарственная форма:
лиофилизат для приготовления концентрата для приготовления раствора для инфузийСостав
1 флакон содержит:активное вещество: Анидулафунгин, стабилизированный фруктозой 122 мг в пересчете на анидулафунгин 100 мг
вспомогательные вещества: фруктоза 102,5 мг, маннитол 512,5 мг, полисорбат- 80 256,3 мг, винная кислота 11,5 мг.
Описание
Белая или почти белая лиофилизированная массаФармакотерапевтическая группа:
противогрибковый препарат системного примененияКодАТХ:
J02AX06Фармакологические свойства
ФармакодинамикаАнидулафунгин является полусинтетическим эхинокандином, липопептидом, синтезированным из продукта ферментации Aspergillus nidulans.
Анидулафунгин селективно ингибирует 1,3-ß-D гликан синтетазу, важный компонент клеточной стенки грибов. В клетках млекопитающих 1,3-ß-D гликан синтетаза отсутствует. Установлено, что анидулафунгин обладает фунгицидной активностью в отношении Candidaspp., а также подавляет клеточный рост Aspergillus fumigatus.
Активность in vitro
К анидулафунгину чувствительны Candida spp., включая C. albicans, С. glabrata, C. krusei, C. parapsilosis, С. tropicalis, С. dubliniensis, С. lusitaniae и С. guilliermondii, а также Aspergillus spp., включая A. fumigatus, A. flavus, A. niger и A. terreus. Анидулафунгин активен в отношении возбудителей микозов, резистентных к противогрибковым препаратам других классов.
МПК определяли по стандартному методу CLSI М27 и М38 для дрожжей. Связь между активностью анидулафунгина in vitro и клиническим результатом не установлена.
Активность in vivo
В эксперименте анидулафунгин, введенный парентерально был эффективен в отношении Candida spp. как при нормальном, так и при нарушенном иммунитете. Лечение анидулафунгином увеличивало выживаемость, а также уменьшало вызванное Candida spp. поражение органов. В эксперименте моделировали развившиеся на фоне нейтропении диссеминированную инфекцию, вызванную С. albicans, резистентный к флуконазолу кандидоз пищевода/полости рта, вызванный С. albicans, а также резистентную к флуконазолу диссеминированную инфекцию, вызванную C. glabrata. Анидулафунгин также был эффективен при экспериментальном аспергиллезе, вызванном Aspergillus fumigatus.
Комбинация с другими противогрибковыми препаратами
Исследования in vitro показали, что анидулафунгин в комбинации с флуконазолом, итраконазолом и амфотерицином В не является антагонистом указанных препаратов в отношении штаммов Candida spp. Клиническое значение этих результатов неизвестно.
В исследованиях in vitro оценивали чувствительность Aspergillus spp. к анидулафунгину в комбинации с итраконазолом, вориконазолом и амфотерицином В. При комбинации анидулафунгина и амфотерицина В было показано отсутствие взаимодействия между препаратами у 16 из 26 изолятов, в то время как у 18 из 26 изолятов наблюдали синергизм при комбинации анидулафунгина с итраконазолом или вориконазолом. Клиническое значение этих результатов неизвестно.
Фармакокинетка
Общие фармакокинетические характеристики
Анидулафунгин при однократном введении имеет линейную фармакокинетику в широком диапазоне суточных доз (от 15 мг до 130 мг).
Коэффициент вариабельности показателя площади под фармакокинетической кривой «концентрация-время» (AUC) для здоровых добровольцев, больных и в особых группах пациентов исследования составил около 25 %. Равновесное состояние достигалось в первые сутки после приема насыщающей дозы (удвоенной поддерживающей дозы).
Распределение
Анидулафунгин быстро распределяется в тканях организма (время полуабсорбции составляет около 0,5-1 час). Объем распределения составляет около 30-50 л, что примерно равно общему объему жидкости в организме. Анидулафунгин в значительной степени связывается с белками плазмы крови (степень связывания > 99 %).
Метаболизм
Метаболизм анидулафунгина в печени не установлен. Поскольку анидулафунгин не является клинически значимым субстратом, индуктором или ингибитором изоферментов цитохрома Р450, маловероятно, что анидулафунгин оказывает клинически значимое влияние на метаболизм препаратов, который происходит с участием системы цитохрома Р450.
При физиологических значениях температуры и рН анидулафунгин претерпевает медленную химическую деградацию, превращаясь в пептид с открытым кольцом, лишенный противогрибковой активности. Время полураспада анидулафунгина при физиологических условиях составляет приблизительно 24 часа. In vivo пептид с открытым кольцом последовательно расщепляется на другие пептиды и элиминируется, в основном, путем экскреции с желчью.
Выведение
Клиренс анидулафунгина составляет около 1 л/час. Период полувыведения (Т1/2) составляет около 24 часов, а терминальное время полувыведения составляет 40-50 часов.
В клиническом исследовании на здоровых добровольцах с использованием единой дозы (около 88 мг) меченого радиоактивным изотопом углерода (14C) анидулафунгина, установлено, что около 30 % введенной дозы элиминировалось кишечником в течение 9 дней, причем доля неизмененного продукта составляла менее 10 %. Менее 1 % введенного меченого препарата выводилось почками. Через 6 дней после приема препарата концентрации анидулафунгина снижались ниже предела определения. Через 8 недель после приема препарата его концентрации в крови, моче и кале были пренебрежимо малы.
Особые группы пациентов
Пациенты с грибковыми инфекциями
По данным популяционного фармакокинетического анализа фармакокинетика анидулафунгина у пациентов с грибковыми инфекциями аналогична таковой у здоровых лиц. В диапазоне суточных доз от 100 мг до 200 мг и при скорости инфузии 1 мг/мин максимальная равновесная концентрация (Cmax) и минимальная концентрация (Cmin) составляют около 7 мг/л и 3 мг/л, соответственно, а средняя равновесная AUC - около 110 мг·час/л.
Вес
Вес пациента практически не влияет на фармакокинетику анидулафунгина.
Пол
Концентрации анидулафунгина в плазме крови здоровых мужчин и женщин были сходными. В исследованиях с использованием нескольких доз анидулафунгина было показано, что у мужчин клиренс анидулафунгина несколько ускорен (приблизительно на 22 %).
Пожилые пациенты
У пожилых людей (пациенты в возрасте ≥ 65 лет, средний клиренс 1,07 л/час) по данным популяционного фармакокинетического анализа средний клиренс анидулафунгина несколько отличается от такового в других возрастных группах (пациенты в возрасте < 65 лет, средний клиренс 1,22 л/час), при этом колебания значений клиренса анидулафунгина были сходными.
ВИЧ инфицированные пациенты
Коррекция дозы у ВИЧ-инфицированных пациентов с различными типами антиретровирусной терапии не требуется.
Недостаточность функции печени
Анидулафунгин не метаболизируется в печени. Концентрация анидулафунгина в плазме крови у пациентов с печеночной недостаточностью любой степени (классы А, B и С по классификации Чайлд-Пью) не увеличивалась. Хотя у пациентов с тяжелой степенью печеночной недостаточности (класс С по классификации Чайлд-Пью) наблюдалось небольшое уменьшение AUC, оно не выходило за рамки величин у здоровых добровольцев.
Недостаточность функции почек
Анидулафунгин практически не выводится почками (клиренс < 1 %). В клинических исследованиях у пациентов с легкой, средней, тяжелой или терминальной стадией почечной недостаточности фармакокинетика анидулафунгина была сходной с таковой у пациентов с нормальной функцией почек. Анидулафунгин не выводится при гемодиализе и его можно применять независимо от времени проведения гемодиализа.
Дети
Фармакокинетика анидулафунгина изучалась у 24 иммуноскомпрометированных детей (от 2 до 11 лет) и подростков (от 12 до 17 лет) с симптомами нейтропении. Равновесное состояние достигалось в первые сутки после приема насыщающей дозы (или удвоенной поддерживающей дозы), а равновесные Cmax и AUCSS возрастали в дозозависимом порядке. После введения препарата в суточных поддерживающих дозах 0,75 мг/кг/сут и 1,5 мг/кг/сут детям в возрасте от 2 до 17 лет системные показатели были сопоставимы с таковыми у взрослых при введении препарата в дозах 50 мг/сут и 100 мг/сут, соответственно.
Показания к применению
Инвазивный кандидоз, включая кандидемию.Кандидоз пищевода
Противопоказания
Повышенная чувствительность к анидулафунгину или другим компонентам препаратаПовышенная чувствительность к другим препаратам класса эхинокандинов (например, каспофунгину)
С осторожностью
Действие на печеньЛабораторные признаки нарушения функции печени наблюдали у здоровых лиц и пациентов, принимавших анидулафунгин. Значительные нарушения функции печени наблюдали у пациентов с серьезными заболеваниями, получавшими наряду с анидулафунгином сопутствующую терапию другими препаратами. Были описаны отдельные случаи тяжелой печеночной недостаточности, гепатит или обострение течения печеночной недостаточности, однако связь этих нарушений с приемом анидулафунгина не установлена. Пациенты, у которых развилась печеночная недостаточность в период терапии анидулафунгином, должны находиться под тщательным контролем, и решение о продолжении терапии анидулафунгином должно приниматься после оценки соотношения риск-польза.
Применение при беременности и в период лактации
В экспериментальных исследованиях репродуктивная токсичность анидулафунгина не выявлена. Возможный риск для человека неизвестен. Данных контролируемых исследований о применении анидулафунгина у беременных женщин нет.Поэтому при беременности анидулафунгин следует применять, только если ожидаемая польза для матери явно превосходит потенциальный риск для плода.
На экспериментальных моделях показано, что анидулафунгин выделяется с молоком. Неизвестно, выделяется ли анидулафунгин с грудным молоком у женщин. Решение о продолжении/прекращении терапии анидулафунгином следует принимать с учетом пользы грудного вскармливания для ребенка и пользы терапии анидулафунгином для матери.
Способ применения и дозы
До начала терапии следует получить материал для посева и других лабораторных исследований (включая гистологическое исследование) для выделения и идентификации возбудителя заболевания. Лечение можно начать до получения результатов лабораторных исследований. Однако после получения этих результатов необходимо скорректировать противогрибковую терапию.Препарат Эраксис® вводят внутривенно. Скорость инфузии не должна превышать 1,1 мг/мин, что эквивалентно 1,4 мл/мин для дозировки 100 мг.
Минимальная продолжительность инфузии – 90 мин.
Инвазивный кандидоз, включая кандидемию
В первые сутки препарат Эраксис ® вводят однократно в дозе 200 мг, далее в дозе 100 мг/сут. Продолжительность лечения зависит от клинического ответа пациента. Противогрибковую терапию следует продолжать не менее 14 дней после исчезновения симптомов инфекции и эрадикации возбудителя.
Кандидоз пищевода
В первые сутки препарат Эраксис ® вводят однократно в дозе 100 мг, далее в дозе 50 мг/сут. Продолжительность лечения зависит от клинического ответа пациента и составляет не менее 14 дней, и не менее 7 дней после исчезновения симптомов инфекции. При риске рецидива кандидоза пищевода у пациентов с ВИЧ-инфекцией следует определить необходимость противорецидивной противогрибковой терапии после курса лечения анидулафунгином.
Инструкция по приготовлению раствора для инфузий
Препарат Эраксис ® выпускается во флаконах для однократного применения.
Препарат Эраксис ® следует восстанавливать водой для инъекций и затем развести только 0,9 % раствором натрия хлорида для инфузий или 5 % раствором декстрозы для инфузий.
ВНИМАНИЕ: совместимость восстановленного анидулафунгин а с другими препаратами для внутривенного введения, а также растворами, неизвестна.
Восстановление
В асептических условиях во флакон добавляют 30 мл воды для инъекций и получают раствор, содержащий анидулафунгин в концентрации около 3,33 мг/мл. Восстановление может занять около 5 минут.
Восстановленный раствор можно хранить при температуре 25 °С в течение 24 часов. При обнаружении видимых частиц и/или видимого окрашивания раствор следует уничтожить.
Разведение и инфузия
В асептических условиях восстановленный раствор переносят из флакона в инфузионный пакет (или флакон), содержащий 0,9 % раствор натрия хлорида для инфузий или 5 % раствор декстрозы для инфузий для достижения необходимой концентрации анидулафунгина. В таблице ниже приведены необходимые объемы раствора и растворителя, а также скорость инфузии и минимальная продолжительность инфузии.
Готовый раствор для инфузии следует хранить при температуре 25 °С и использовать в течение 48 часов.
Приготовление раствора для инфузий
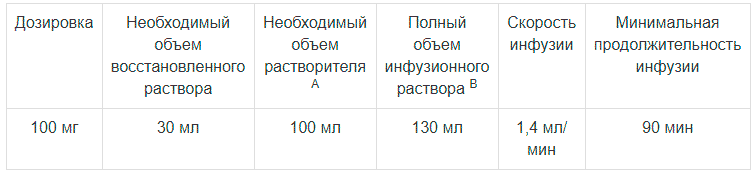
A 0,9 % раствор натрия хлорида для инфузий или 5 % раствор декстрозы для инфузий
В Концентрация раствора для инфузий составляет около 0,77 мг/мл.
Недостаточность функции печени
У пациентов с легкой, средней и тяжелой степенью печеночной недостаточности (классы А, В и С по классификации Чайлд-Пью) коррекция дозы препарата Эраксис® не требуется.
Недостаточность функции почек
У пациентов с любой степенью почечной недостаточности, включая пациентов, получающих гемодиализ, коррекция дозы препарата Эраксис® не требуется. Препарат может применяться независимо от времени проведения гемодиализа.
Особые группы пациентов
У взрослых пациентов в зависимости от их возраста, пола, веса, расовой принадлежности и наличия ВИЧ-инфекции коррекция дозы препарата Эраксис® не требуется.
Применение у детей и подростков
Опыт применения препарата Эраксис® у детей ограничен. Применение у детей до 18 лет не рекомендуется за исключением случаев, когда потенциальная польза от применения превышает возможный риск.
Побочное действие
По данным клинических исследований нежелательные явления, наблюдавшиеся на фоне приема препарата Эраксис®, были слабыми или умеренными и редко приводили к отмене препарата.Связанные с инфузией препарата нежелательные явления включали сыпь, крапивницу, «приливы», зуд, одышку, бронхоспазм и артериальную гипотензию.
Перечисленные ниже нежелательные явления, связанные с применением препарата были классифицированы в соответствии с частотой: частые (≥ 1/100, ≤ 1/10); нечастые (≥ 1/1000, < l/100), частота неизвестна (данные постмаркетинговых исследований).
Инфекции
Нечастые: фунгемия, колит, ассоциированный с Clostridium difficile, кандидоз, кандидоз ротовой полости.
Нарушения метаболизма
Частые: гиперкалиемия, гипокалиемия, гипомагниемия.
Нечасто: гипергликемия, гиперкальциемия, гипернатриемия.
Со стороны сердечно-сосудистой системы
Частые: «приливы» крови к коже лица
Нечастые: фибрилляция предсердий, синусовая аритмия, желудочковая экстрасистолия, блокада правой ножки пучка Гиса; тромбоз, артериальная гипертензия, ощущение жара.
Со стороны желудочно-кишечного тракта
Частые: диарея, повышение концентрации биллирубина, повышение активности гамма-глутамилтрансферазы, щелочной фосфатазы, аспартатаминотрансферазы, аланинаминотрансферазы.
Нечастые: боль в верхней части живота, рвота, непроизвольная дефекация, тошнота, запор, холестаз.
Со стороны системы кроветворения и лимфатической системы
Частые: тромбоцитопения, коагулопатия.
Нечасто: тромбоцитоз.
Со стороны нервной системы
Частые: судороги, головная боль.
Со стороны опорно-двигательного аппарата и соединительной ткани:
Нечастые: боль в спине.
Со стороны кожи и подкожных тканей
Частые: сыпь, зуд.
Нечастые: крапивница, генерализованный зуд.
Со стороны органа зрения
Нечастые: боль в глазах, нарушения зрения, нечеткое зрение.
Со стороны дыхательной системы
Частота неизвестна: бронхоспазм.
Со стороны иммунной системы
Частота неизвестна: анафилактический шок, анафилактические реакции.
Общие и местные реакции
Нечастые: боль в месте инфузии.
Лабораторные показатели
Частые: снижение числа тромбоцитов, повышение концентрации креатинина в сыворотке крови, удлинение интервала QT на ЭКГ.
Нечастые: снижение концентрации магния и калия в сыворотке крови, повышение количества тромбоцитов, повышение концентрации мочевины в сыворотке крови, повышение активности амилазы, липазы в сыворотке крови, изменения на ЭКГ.
В отчете по безопасности на основе полного клинического исследования (II и III фаза, 669 пациентов) описаны следующие нежелательные явления (все из них нечастые, ≥ 1/1000, < l/100): нейтропения, лейкопения, анемия, гиперурикемия, гипокальциемия, гипонатриемия, гипоальбуминемия, гипофосфатемия, возбуждение, делирий, спутанность сознания, слуховые галлюцинации, головокружение, парестезия, демиелинизация центральных отделов варолиева моста, изменение вкуса, синдром Гийена-Барре, тремор, расстройство зрительного восприятия, глухота на одно ухо, флебит, поверхностный тромбофлебит, артериальная гипотензия, лимфангит, диспепсия, сухость во рту, язва пищевода, некроз печени, ангионевротический отек, гипергидроз, миалгия, моноартрит, почечная недостаточность, гематурия, гипертермия, озноб, периферические отеки, реакция в месте введения, повышение активности креатинфосфокиназы в сыворотке крови, повышение активности лактатдегидрогеназы в сыворотке крови, снижение количества лимфоцитов.
Передозировка
При передозировке анидулафунгина необходимо применять симптоматическую терапию.При случайном однократном введении анидулафунгина в дозе 400 мг в качестве насыщающей дозы клинически значимых нежелательных явлений не наблюдалось.
При введении анидулафунгина 10 здоровым добровольцам в насыщающей дозе 260 мг с последующим дозированием по 130 мг в сутки препарат переносился хорошо. Дозозависимой токсичности не выявлено. У 3 из 10 испытуемых наблюдали преходящее бессимптомное повышение уровня трансаминаз (менее 3-кратного превышения нормы).
Анидулафунгин не выводится при гемодиализе.
Взаимодействие с другими лекарственными средствами
Доклинические испытания in vitro и in vivo, а также клинические исследования показали, что анидулафунгин не является клинически важным субстратом, индуктором или ингибитором изоферментов цитохрома Р450. Исследование лекарственных взаимодействий проводили только у взрослых пациентов. Анидулафунгин демонстрировал незначительную величину почечного клиренса (< 1 %). При комбинированной терапии вероятность взаимодействия с другими лекарственными средствами минимальна.Исследования in vitro показали, что анидулафунгин не метаболизируется цитохромом Р450 человека или изолированными гепатоцитами человека, и что в клинически значимых концентрациях анидулафунгин только незначительно ингибирует активность изоферментов цитохромом Р450 человека (CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYPЗА).
При совместном применении с анидулафунгином не наблюдалось никаких клинически значимых лекарственных взаимодействий со следующими лекарственными средствами.
Циклоспорин (субстрат изофермента цитохрома CYP3A4)
При введении анидулафунгина здоровым добровольцам в дозе 100 мг/сут после насыщающей дозы 200 мг/сут или в комбинации с циклоспорином в дозе 1,25 мг/кг перорально 2 раза в сутки, циклоспорин лишь незначительно влиял на равновесные Cmaxанидулафунгина, однако AUC при этом возрастала на 22 %. Исследование in vitro показало, что анидулафунгин не влияет на метаболизм циклоспорина. Наблюдавшиеся нежелательные явления совпадали с описанными в других исследованиях, где изучался только анидулафунгин. При совместном применении ни для одного из препаратов коррекции дозы не требуется.
Вориконазол (ингибитор и субстрат изоферментов цитохрома CYP2C19, CYP2C9, CYP3A4)
В исследовании 17 здоровых добровольцев получали анидулафунгин в дозе 100 мг/сут после насыщающей дозы 200 мг; только вориконазол 200 мг 2 раза в сутки перорально после насыщающей дозы 400 мг 2 раза в первые сутки; затем оба препарата. При этом равновесные Cmax и AUC при совместном применении препаратов изменялись незначительно. При совместном применении не требуется коррекция дозы ни для одного из препаратов.
Такролимус (субстрат изофермента цитохрома CYP3A4)
В исследовании 35 здоровых добровольцев принимали такролимус однократно перорально в дозе 5 мг, затем получали анидулафунгин в дозе 100 мг/сут после ударной дозы 200 мг; затем - оба препарата. Равновесные Cmax и AUC анидулафунгина и такролимуса при совместном применении препаратов изменялись незначительно. При совместном применении не требуется коррекция дозы ни для одного из препаратов.
Липосомальный амфотерицин B
Фармакокинетику анидулафунгина изучали у 27 пациентов, получавших анидулафунгин в дозе 100 мг/сут, которым также вводили липосомальный амфотерицин В в дозе до 5 мг/кг/сут. Популяционный фармакокинетический анализ показал, что комбинированный прием липосомального амфотерицина В незначительно влиял на фармакокинетику анидулафунгина. Коррекция дозы анидулафунгина не требуется.
Рифампицин (мощный индуктор цитохрома Р450)
Фармакокинетику анидулафунгина изучали у 27 пациентов, получавших анидулафунгин в дозе 50 мг/сут или 75 мг/сут, которым также вводили рифампицин в дозе до 600 мг/сут. Комбинированный прием рифампицина незначительно влиял на фармакокинетику анидулафунгина. Коррекция дозы анидулафунгина не требуется.
Особые указания
Данные о применении анидулафунгина у пациентов с нейтропенией ограничены.Связанные с инфузией препарата Эраксис® нежелательные явления возникают реже, если скорость инфузии не превышает 1,1 мг/мин.
При развитии любых анафилактических реакций, следует прекратить терапию анидулафунгином и назначить соответствующее лечение.
Лиофилизат
Лиофилизат можно хранить в течение 96 часов при температуре 25 °С, затем его можно снова поместить в холодильник.
Восстановленный раствор
Восстановленный раствор можно хранить при температуре 25 ºС в течение 24 часов. Химическая и физическая стабильность восстановленного раствора составляет 24 часа при температуре 25 °C.
С микробиологической точки зрения при приготовлении и хранении в асептических условиях восстановленный раствор можно применять в течение 24 часов при температуре 25 °C.
Раствор для инфузий
Раствор для инфузий можно хранить в течение 48 часов при температуре 25 °С или хранить замороженным в течение 72 часов. Химическая и физическая стабильность инфузионного раствора составляет 48 часов при температуре 25 °C.
С микробиологической точки зрения при приготовлении и хранении в асептических условиях раствор для инфузий можно применять в течение 48 часов после приготовления при температуре 25 °C.
Фармацевтическая несовместимость
Раствор препарата Эраксис® не следует смешивать или вводить совместно с другими препаратами или электролитами за исключением 0,9 % раствора натрия хлорида для инфузий (9 мг/мл) или 5 % раствора декстрозы для инфузий (50 мг/мл).
Влияние на способность управлять транспортными средствами, механизмами
Данных о влиянии анидулафунгина на способность к вождению автотранспорта и управление механизмами нет. В связи с опасностью развития неврологических нарушения (головокружение, судороги, нарушение зрительного восприятия), Эраксис® следует с осторожностью назначать лицам, управляющим транспортом и занимающимся видами деятельности, требующими повышенной концентрации внимания и быстрой двигательной реакции.
Форма выпуска
Лиофилизат для приготовления концентрата для приготовления раствора для инфузий 100 мг.100 мг лиофилизата во флакон прозрачного бесцветного стекла (тип I), укупоренный резиновой пробкой и герметичным алюминиевым колпачком с пластиковой крышкой типа «флип-офф».
1 флакон вместе с инструкцией по применению помещают в картонную пачку.
Срок годности
Лиофилизат - 3 года.Восстановленный раствор - не более 24 часов.
Раствор для инфузий - не более 48 часов.
Не применять по истечении срока годности, указанного на упаковке.
Условия хранения
Лиофилизат - при температуре от 2 до 8 °С.Восстановленный раствор - при температуре 25 °С.
Раствор для инфузий - при температуре 25 °С.
Хранить в недоступном для детей месте.
Условия отпуска
По рецептуПроизводитель
Фармация и Апджон Кампани, СШААдрес: 7000 Портейдж Роуд, Каламазу, МИ 49001, США
Претензии потребителей направлять по адресу ООО «Пфайзер»:
123317 Москва, Пресненская наб., д. 10, БЦ «Башня на Набережной» (Блок С)
Комментарии
ПРАКТИКА ПЕДИАТРА
