Элонва - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер:
Торговое название:
Элонва®Международное непатентованное название:
корифоллитропин альфаЛекарственная форма:
раствор для подкожного введенияСостав препарата:
Активное вещество: корифоллитропин альфа 100 мкг или 150 мкгВспомогательные вещества: натрия цитрата дигидрат 3,68 мг, сахароза 35,0 мг, L-метионин 0,25 мг, полисорбат 20 0,10 мг, хлористоводородная кислота 0,1 М или натрия гидроксид 0,1 М до pH 7,0, вода для инъекций (извлекаемый объем) до 0,50 мл.
Описание:
Прозрачный раствор от бесцветного до светло-желтого цветаФармакотерапевтическая группа:
фолликулостимулирующее средствоКод ATX:
G03GA09Фармакологические свойства
ФармакодинамикаКорифоллитропин альфа - это гликопротеин, который продуцируется клетками яичников китайских хомячков с помощью рекомбинантной ДНК технологии.
Корифоллитропин альфа — это стимулятор роста фолликулов пролонгированного действия, который по фармакодинамическим свойствам сопоставим с рекомбинантным фолликулостимулирующим гормоном (рФСГ), но обладает значительно более длительным действием. Препарат вызывает и поддерживает рост фолликулов в течение недели, поэтому одна подкожная инъекция рекомендуемой дозы препарата Элонва® может заменить первые 7 ежедневных инъекций любых препаратов рФСГ при проведении контролируемой стимуляции яичников. Увеличение длительности фолликулостимулирующей активности было достигнуто за счет присоединения карбокситерминального пептида бета-субъединицы хорионического гонадотропина человека (ХГЧ) к бета-цепи человеческого ФСГ. Корифоллитропин альфа не обладает активностью ХГЧ и лютеинизирующего гормона (ЛГ).
Фармакокинетика
Показатели фармакокинетики корифоллитропина альфа не зависели от дозы в широком диапазоне доз (7,5-240 мкг). Распределение, метаболизм и выведение корифоллитропина альфа сходны с таковыми других гонадотропинов, таких как ФСГ, ХГЧ и ЛГ.
Всасывание
После однократного подкожного введения корифоллитропина альфа максимальная концентрация в плазме достигалась через 44 ч (34-57 ч1). Абсолютная биодоступность составила 58% (48-70%1).
Экспозиция корифоллитропина альфа зависит от массы тела. В клинических исследованиях концентрации корифоллитропина альфа в плазме были сходными после введения корифоллитропина альфа в дозах 100 мкг и 150 мкг женщинам с массой тела ?60 кг и >60 кг соответственно.
Распределение
После всасывания в кровь корифоллитропин альфа распределяется в основном в яичники и почки.
В равновесном состоянии объем распределения и клиренс составляют 9,2 л (6,5-13,1 л1) и 0,13 л/ч (0,10-0,18 л/ч1) соответственно.
Метаболизм
В метаболизме корифоллитропина альфа, преимущественно, участвуют почки. В результате метаболизма образуются фармакологически неактивные альфа и бета i субъединицы (включая карбокси-терминальный пептид), которые, преимущественно, выводятся почками.
Выведение
Период полувыведения корифоллитропина альфа составляет 69 ч (59-79 ч1).
Корифоллитропин альфа выводится, преимущественно, почками. Выведение может быть снижено у пациентов с почечной недостаточностью. Микросомальные ферменты печени незначительно участвуют в метаболизме и выведении корифоллитропина альфа. Хотя данные о применении корифоллитропина альфа пациентами с печеночной недостаточностью отсутствуют, влияние печеночной недостаточности на фармакокинетический профиль корифоллитропина альфа маловероятно.
Показания к применению
Контролируемая стимуляция яичников в комбинации с антагонистами гонадотропин рилизинг-гормона (ГнРГ) с целью образования множественных фолликулов у женщин, участвующих в программе вспомогательной репродукции.Противопоказания
Применение при беременности и в период грудного вскармливания
БеременностьПрименение препарата Элонва® во время беременности противопоказано.
После контролируемой стимуляции яичников гонадотропинами в клинической практике, тератогенного эффекта не выявлено. Клинические данные не позволяют исключить тератогенный эффект корифоллитропина альфа, в случае его непреднамеренного введения во время беременности. В доклинических исследованиях тератогенного эффекта, связанного с использованием лекарственного препарата не наблюдали.
Период грудного вскармливания
Применение препарата Элонва® в период грудного вскармливания противопоказано.
Способ применения и дозы
Применение препарата Элонва® должно проводиться под контролем врача, имеющего опыт лечения бесплодия.Препарат можно применять, только если раствор в шприце прозрачный.
Дозы:
Женщинам с массой тела ?60 кг однократно вводят 100 мкг.
Женщинам с массой тела >60 кг однократно вводят 150 мкг.
Рекомендуемые дозы были установлены только при комбинированном использовании с антагонистом ГнРГ.
В 1-й день стимуляции препарат Элонва® вводят однократно подкожно (предпочтительно под кожу живота) в раннюю фолликулярную фазу менструального цикла.
На 5-й или 6-й день стимуляции, в зависимости от количества и размера растущих фолликулов и/или концентрации эстрадиола в крови, должно быть начато использование антагониста ГнРГ для предотвращения преждевременного повышения концентрации ЛГ.
На 8-й день стимуляции (через 7 дней после инъекции препарата Элонва®) лечение может быть продолжено ежедневным введением рФСГ до тех пор, пока размеры фолликулов не будут соответствовать критериям для введения триггерной дозы ХГЧ (3 фолликула ?17 мм). Суточная доза рФСГ зависит от ответа яичников, который регулярно мониторируется при ультразвуковом исследовании, начиная с 5-го или 6-го дня стимуляции. Если ответ нормальный, то рекомендуемая суточная доза составляет 150 ME рФСГ.
Прием рФСГ в день использования ХГЧ может быть пропущен в зависимости от ответа яичников. Обычно достаточное созревание фолликулов достигается на 9 день лечения (диапазон длительности лечения составляет от 6 до 18 дней).
При созревании 3-х фолликулов до размера ? 17 мм, производится однократное введение от 5000 ME до 10000 ME ХГЧ в этот же или следующий день для индукции финального созревания ооцитов. В случае чрезмерного ответа яичников необходимо использовать рекомендации по минимизации риска развития СГЯ.
Применение у особых групп пациентов
Почечная недостаточность.
Клинических исследований препарата у пациентов с почечной недостаточностью не проводилось. Так как выведение корифоллитропина альфа у таких пациентов может быть снижено, применение препарата Элонва® у женщин с почечной недостаточностью не рекомендовано.
Печеночная недостаточность.
Хотя данные по применению препарата у пациентов с печеночной недостаточностью отсутствуют, влияние печеночной недостаточности на выведение корифоллитропина альфа маловероятно.
Дети
Применение препарата Элонва® у детей не соотносится с показанием.
Способ введения
Подкожная инъекция препарата может быть произведена самой женщиной или другим лицом, если врач предоставил соответствующие рекомендации.
Рекомендации для пациентов но подготовке и выполнению подкожной инъекции
Компоненты шприца с иглой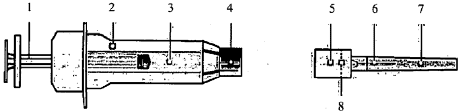
1. Поршень
2. Шприц
3. Раствор
4. Колпачок шприца
5. Колпачок иглы
6. Игла
7. Футляр иглы
8. Перфорация
Подготовка к инъекции
|
|
1. - Обработайте кожу в месте предполагаемой инъекции дезинфицирующим средством. | |
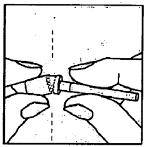 | 2. - Сломайте колпачок иглы по линии перфорации, извлеките футляр, содержащий иглу. - НЕ снимайте футляр с иглы. - Положите футляр, содержащий иглу, на сухую чистую поверхность. | |
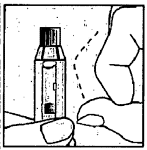 | 3. - Держите шприц колпачком вверх (вертикально). - Осторожно постучите пальцем по шприцу, чтобы пузырьки воздуха поднялись вверх. | |
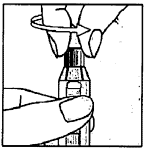 | 4. - Держите шприц вертикально. - Открутите колпачок шприца против часовой стрелки. | |
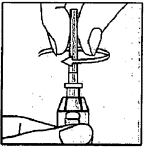 | 5. - Держите шприц вертикально - Прикрутите к нему футляр иглы, содержащий иглу, по часовой стрелке. | |
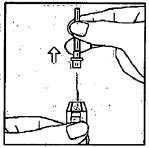 | 6. - Держите шприц вертикально. - Снимите футляр с иглы и выбросьте его. - БУДЬТЕ ОСТОРОЖНЫ с иглой! | |
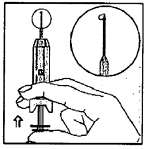 | 7. - Зажмите шприц между указательным и средним пальцами и держите его вертикально. - Поместите большой палец на поршень. - ОСТОРОЖНО нажмите на поршень, чтобы на кончике иглы появилась капелька раствора. | |
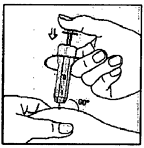 | 8. - Большим и указательным пальцами сделайте кожную складку - Введите иглу под углом 90° в складку кожи. - ОСТОРОЖНО надавливайте на поршень до упора. - ДОСЧИТАЙТЕ ДО ПЯТИ, чтобы ввести весь раствор. | |
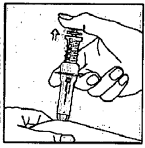 |
9. - Уберите большой палец с поршня. - Игла автоматически уберется в шприц и будет заблокирована. | |
Побочное действие
Основными нежелательными реакциями в клинических исследованиях при лечении препаратом Элонва® были СГЯ (5,2 %), боль и дискомфорт внизу живота (4,1% и 5,5 % соответственно), головная боль (3,2 %), тошнота (1,7 %), утомляемость (1,4 %) и жалобы со стороны молочных желез (болезненные ощущения, боль, дискомфорт, нагрубание молочных желез, увеличение груди) (1,2 %).В таблице приведены основные нежелательные реакции (по системам органов и частоте), которые наблюдались при применении препарата в клинических исследованиях.
(часто (? 1%, < 10%), нечасто (? 0,1%, < 1%)).
| Класс система/орган | Частота | Нежелательные эффекты |
| Нарушения со стороны нервной системы | Часто Нечасто | Головная боль Головокружение |
| Нарушения со стороны желудочно-кишечного тракта | Часто Нечасто | Тошнота Боль в животе, рвота, диарея, запор, вздутие живота |
| Нарушения со стороны мочеполовой системы и молочных желез | Часто Нечасто |
СГЯ, боль и дискомфорт в области малого таза, жалобы со стороны молочных желез Перекрут яичника |
| Общие и местные реакции | Часто | Утомляемость |
Кроме того, описаны эктопическая беременность, невынашивание беременности и многоплодная беременность, которые рассматриваются как осложнения методов вспомогательной репродукции.
Передозировка
Введение более одной рекомендованной дозы препарата Элонва® во время одного цикла контролируемой стимуляции яичников и/или применение рФСГ в слишком высоких дозах может привести к увеличению риска развития СГЯ (см. Особые указания).Взаимодействие с другими лекарственными препаратами
Взаимодействие с другими препаратами не изучалось. Корифоллитропин альфа не является субстратом для изоферментов цитохрома Р450, поэтому не ожидается взаимодействия с другими препаратами.Особые указания
Признаки СГЯ возникают под влиянием приема ХГЧ или беременности (эндогенный ХГЧ). Ранний СГЯ обычно развивается в течение 10 дней после введения ХГЧ и может сопровождаться избыточным ответом яичников на стимуляцию гонадотропинами. Обычно ранний СГЯ проходит самостоятельно после начала менструации. Поздний СГЯ развивается более чем через 10 дней после введения ХГЧ в результате беременности. Учитывая риск развития СГЯ, пациенток следует наблюдать в течение, по крайней мере, 2 недель после введения ХГЧ.
Чтобы уменьшить риск развития СГЯ, до лечения и регулярно во время лечения необходимо проводить ультразвуковой мониторинг растущих фолликулов и/или определять концентрацию эстрадиола в плазме. В программах вспомогательной репродукции риск развития СГЯ повышен при наличии 18 и более фолликулов диаметром ? 11 мм. Если общее число фолликулов составляет ?30, вводить ХГЧ не следует.
В зависимости от ответа яичников можно принять следующие меры для профилактики СГЯ:
Для поддержки лютеиновой фазы следует избегать введения ХГЧ.
Чтобы минимизировать риск развития СГЯ, необходимо использовать рекомендуемые дозы и схемы применения препарата Элонва® и тщательно контролировать ответ яичников.
Влияние на способность управлять транспортными средствами и работать с механизмами
Реакции на управление транспортными средствами и использование сложной техники не изучались.Элонва® может вызвать головокружение. Пациенток следует предупредить, что при головокружении не следует садиться за руль или пользоваться сложной техникой.
Форма выпуска
По 100 или 150 мкг активного вещества в растворе для подкожного введения по 0,5 мл, в одноразовом шприце объемом 1 мл из бесцветного стекла типа I (Евр. Фарм.) с автоматической системой блокировки иглы.Одноразовый шприц с одной стороны закупорен навинчивающимся пластиковым колпачком с резиновой прокладкой (Евр. Фарм.), а с другой стороны пластиковым поршнем с накрученной на нем резиновой поршневой пробкой (Евр. Фарм.).
1 одноразовый стерильный предварительно заполненный шприц с автоматической системой блокировки иглы в комплекте с 1 стерильной иглой в индивидуальной упаковке помещают в прозрачный запаянный пластиковый контейнер.
1 прозрачный пластиковый контейнер и инструкцию по применению помещают в картонную пачку.
Условия хранения
При температуре от 2 до 8 °С, в защищенном от света месте. Не замораживать.Хранить в недоступном для детей месте.
Срок годности
3 года. Не использовать по истечении срока годности.Условия отпуска
По рецептуЮридическое лицо, на имя которого выдано регистрационное удостоверение
Н.В. Органон, НидерландыПроизводитель
Произведено:Веттер Фарма-Фертигунг ГмбХ и Ко. КГ, Германия
Vetter Pharma-Fertigung GmbH & Co. KG, Schutzenstrasse 87, 88212 Ravensburg, Germany
Выпускающий контроль качества:
Органон (Ирландия) Лтд., Ирландия
Organon (Ireland) Ltd., Drynam Road, Swords, Co. Dublin, Ireland
Претензии потребителей направлять по адресу
ООО «МСД Фармасьютикалс»ул. Павловская, д. 7, стр. 1 г. Москва, Россия, 115093
Комментарии
ПРАКТИКА ПЕДИАТРА