Блинцито - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер
ЛП-004035
Торговое наименование
Блинцито
Международное непатентованное или группировочное наименование
Блинатумомаб
Лекарственная форма
Порошок для приготовления концентрата для приготовления раствора для инфузий
Состав
Каждый флакон с препаратом содержит:
Действующее вещество: блинатумомаб - 35 мкг*;
Вспомогательные вещества: лимонной кислоты моногидрат - 3,68 мг, трегалозы дигидрат -105,0 мг, лизина гидрохлорид - 25,55 мг, полисорбат 80 - 0,70 мг, натрия гидроксид - до рН 7,0. Каждый флакон с раствором стабилизатора для приготовления раствора для инфузий содержит: лимонной кислоты моногидрат - 52,5 мг, лизина гидрохлорид - 2283,8 мг, полисорбат 80 - 10 мг, натрия гидроксид - до рН 7,0, вода для инъекций - до 10 мл.
* номинальный объем блинатумомаба; для извлечения 35 мкг блинатумомаба берется избыток в количестве 38,5 мкг.
Описание
Белого или светло-желтого цвета порошок или аморфная масса.
Восстановленный лекарственный препарат: жидкость от бесцветного до светло-желтого цвета, прозрачная или слегка опалесцирующая, свободная от механических включений.
Раствор стабилизатора для приготовления раствора для инфузий: жидкость от бесцветного до светло-желтого цвета, прозрачная или слегка опалесцирующая, свободная от механических включений.
Фармакотерапевтическая группа
Противоопухолевые препараты, моноклональные антитела
Код АТХ
L01FX07
Фармакологические свойства
Фармакодинамика
Механизм действия
Блинатумомаб является биспецифическим активатором T-клеток и представляет собой молекулу, селективно связывающуюся с антигеном CD19, экспрессируемым на поверхности В-клеток, и антигеном CD3, экспрессируемым на поверхности Т-клеток. Блинатумомаб активирует эндогенные Т-клетки, соединяя CD3-комплекс Т-клеточного рецептора (ТКР) с CD19 на доброкачественных и злокачественных B-клетках. Противоопухолевая активность блинатумомаба не зависит от наличия Т-лимфоцитов, имеющих специфичные ТКР, и пептидных антигенов на поверхности опухолевых клеток, а является поликлональной по природе и независимой от вида молекул человеческого лейкоцитарного антигена (ЧЛА) на клетках-мишенях. Опосредованное блинатумомабом образование цитолитического синапса между Т-клеткой и опухолевой клеткой приводит к высвобождению протеолитических ферментов, разрушающих клетки-мишени, как в стадии пролиферации, так и в стадии покоя. Блинатумомаб транзиторно активирует экспрессию молекул клеточной адгезии, выработку цитолитических белков, высвобождение воспалительных цитокинов и пролиферацию Т-клеток и приводит к ликвидации клеток CD19+.
Фармакодинамические эффекты
У пациентов в исследованиях наблюдались стабильные иммунные фармакодинамические ответы. Во время непрерывной внутривенной инфузии в течение 4 недель, фармакодинамический ответ характеризовался активацией и начальным перераспределением Т-клеток, быстрой элиминацией периферических В-клеток и транзиторным повышением цитокинов.
После начала инфузии блинатумомаба или увеличения дозы наблюдалось перераспределение периферических Т-клеток (т.е. адгезия Т-клеток к эндотелию и/или трансмиграция в ткани кровеносных сосудов). У большинства пациентов количество Т-клеток первоначально снижалось в течение 1-2 дней, а затем возвращалось к исходным уровням в течение 7-14 дней. У некоторых пациентов наблюдалось увеличение количества Т-клеток выше исходного уровня (экспансия Т-клеток).
У большинства пациентов уровни периферических В-клеток быстро снижались до неопределяемого уровня в ходе лечения при дозах ≥ 5 мкг/м2 в сутки или ≥ 9 мкг/сутки. Восстановления количества периферических В-клеток в течение 2 недель перерыва между циклами лечения не наблюдалось. Неполное снижение количества В-клеток происходило при использовании препарата в дозах 0,5 мкг/м2 в сутки и 1,5 мкг/м2 сутки, а у нескольких не ответивших на терапию пациентов - при применении препарата в более высоких дозах. Количество лимфоцитов в периферической крови у детей не оценивалось.
Было отмечено повышение концентраций IL-6, IL-10, и IFN-ү при определении уровней цитокинов IL-2, IL-4, IL-6, IL-8, IL-10, IL-12, TNF-a и IFN-ү. Транзиторное повышение уровня цитокинов наблюдалось в первые 2 дня после начала инфузии препаратом Блинцито. Повышенные уровни цитокинов возвращались к исходным в течение 24-48 часов во время инфузии. В последующих циклах лечения повышение цитокинов наблюдалось у меньшего количества пациентов с меньшей интенсивностью по сравнению с первоначальными 48 часами первого цикла лечения. Фармакокинетика
Фармакокинетика
блинатумомаба у взрослых пациентов носит линейный характер в диапазоне доз от 5 до 90 мкг/м2/день (приблизительно эквивалентных от 9 до 162 мкг/день). После непрерывной внутривенной инфузии равновесная концентрация в сыворотке (Css) была достигнута в течение суток и оставалась стабильной со временем. Увеличение средних значений Css было приблизительно пропорционально дозе в исследованном диапазоне доз. При клинических дозах 9 мкг/день и 28 мкг/день для лечения рецидивирующего или рефрактерного острого лимфобластного лейкоза (ОЛЛ) средняя (SD) Css составляла 228 (356) пг/мл и 616 (537) пг/мл соответственно. Параметры фармакокинетики блинатумомаба у пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов были аналогичны таковым у пациентов с рецидивирующим или рефрактерным ОЛЛ.
Распределение
Расчетный средний (SD) объем распределения в терминальной фазе (Vz) при непрерывной внутривенной инфузии блинатумомаба составил 4,35 (2,45) л.
Метаболизм
Метаболический путь блинатумомаба не изучался. Ожидается, что, как и другие терапевтические белки, препарат Блинцито будет деградировать на малые пептиды и аминокислоты посредством катаболических путей.
Выведение
Расчетный средний (SD) системный клиренс при непрерывной внутривенной инфузии у пациентов, получавших блинатумомаб в клинических исследованиях, составлял 3,11 (2,98) л/час. Среднее (SD) время полувыведения составляло 2,10 (1,41) часа. При тестируемых клинических дозах незначительные количества блинатумомаба выводились из организма в моче.
Площадь поверхности тела, пол и возраст
Чтобы оценить влияние демографических признаков на фармакокинетику блинатумомаба, был проведен фармакокинетический анализ в популяциях. Результаты показывают, что возраст (от 7 месяцев до 80 лет) и пол не влияют на фармакокинетику блинатумомаба. Площадь поверхности тела (от 0,37 до 2,70 м2) влияет на фармакокинетику препарата. Несмотря на то что данное влияние у взрослых было незначительным, у детей рекомендуется расчет дозы в зависимости от площади поверхности тела.
Фармакокинетика у отдельных групп пациентов
Пациенты с почечной недостаточностью
Формальные исследования фармакокинетики блинатумомаба у пациентов с почечной недостаточностью не проводились.
Анализ фармакокинетики показал приблизительно 2-кратное различие в средних значениях клиренса блинатумомаба у пациентов с умеренной почечной дисфункцией и нормальной функцией почек. Поскольку была выявлена высокая вариабельность между пациентами (CV % до 96,8 %), а значения клиренса у пациентов с почечной недостаточностью были в основном в пределах, наблюдаемых у пациентов с нормальной функцией почек, клинически значимого влияния функции почек на клинические исходы не ожидается.
Пациенты с печеночной недостаточностью
Формальные фармакокинетические исследования блинатумомаба у пациентов с печеночной недостаточностью не проводились. Для оценки влияния печеночной недостаточности на клиренс блинатумомаба использованы исходные уровни аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT). В рамках популяционного анализа фармакокинетики было высказано предположение об отсутствии связи между активностью АЛТ и АСТ, с одной стороны, и клиренсом блинатумомаба, с другой стороны.
Дети
При применении у детей с рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов фармакокинетика блинатумомаба в диапазоне доз от 5 до 30 мкг/м2/сутки носит линейный характер. При применении в рекомендованных дозах 5 и 15 мкг/м2/сутки средние значения (SD) равновесных концентраций (Css) составили 162 (179) и 533 (392) пг/мл соответственно. Рассчитанные значения среднего (SD) объема распределения (Vz), клиренса (CL) и терминального периода полувыведения (t1/2,z) составили 3,91 (3,36) л/м2, 1,88 (1,90) л/ч/м2 и 2,19 (1,53) ч соответственно.
При оценке фармакокинетики блинатумомаба у пациентов с впервые рецидивирующим ОЛЛ из предшественников B-лимфоцитов высокого риска средние значения Css с расчетным стандартным отклонением (SD) при применении дозы 15 мкг/м2/сутки и клиренса составили 921 (1010) пг/мл и 0,988 (0,450) л/ч/м2 соответственно. Между наблюдавшимися значениями и значениями у пациентов с рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов нет клинически значимых различий. Объем распределения и время полувыведения оценить невозможно.
Показания к применению
Блинцито показан в качестве монотерапии для лечения CD19-положительного рецидивирующего или рефрактерного острого лимфобластного лейкоза (ОЛЛ) из предшественников B-лимфоцитов у взрослых. Пациенты с положительным по филадельфийской хромосоме ОЛЛ из предшественников B-лимфоцитов должны быть резистентны к терапии как минимум двумя ингибиторами тирозинкиназы (ИТК) и не иметь альтернативных вариантов лечения.
Блинцито показан в качестве монотерапии для лечения CD19-положительного, отрицательного по филадельфийской хромосоме ОЛЛ из предшественников B-лимфоцитов у взрослых в фазе первой или второй полной ремиссии с наличием минимальной остаточной болезни (МОБ) ≥ 0,1 %.
Блинцито показан в качестве монотерапии для лечения CD19-положительного, отрицательного по филадельфийской хромосоме рецидивирующего или рефрактерного ОЛЛ из предшественников B-лимфоцитов (после по крайней мере двух линий предшествующей терапии или после перенесенной аллогенной трансплантации гемопоэтических стволовых клеток) у детей в возрасте 1 года или старше.
Блинцито показан в качестве монотерапии для лечения детей в возрасте 1 года и старше с первым рецидивом CD19-положительного, отрицательного по филадельфийской хромосоме ОЛЛ из предшественников B-лимфоцитов высокого риска в составе консолидирующей терапии (см. раздел «Способ применения и дозы»).
Противопоказания
Гиперчувствительность к блинатумомабу или к любому из компонентов препарата, перечисленных в разделе «Состав».
Тяжелая степень почечной недостаточности.
Тяжелая степень печеночной недостаточности.
Период грудного вскармливания (см. раздел «Применение при беременности и в период грудного вскармливания»).
Применение при беременности и в период грудного вскармливания
Беременность
Исследования репродуктивной токсичности блинатумомаба не проводились. В исследовании эмбриофетальной токсичности, проведенном на мышах с использованием мышиной суррогатной молекулы, никакие признаки эмбриотоксичности или тератогенности не обнаружены. У беременных мышей наблюдалось ожидаемое истощение В- и Т-клеток, но гематологические эффекты на плод не оценивались.
Данные о применении блинатумомаба беременными женщинами отсутствуют.
Блинатумомаб не следует применять во время беременности, если потенциальная польза для матери не превышает возможный риск для плода.
Женщины с детородным потенциалом должны использовать эффективные методы контрацепции в течение курса терапии блинатумомабом, а также в течение минимум 48 часов после этого (см. раздел «Особые указания»).
При применении препарата во время беременности у новорожденных может наблюдаться истощение B-клеток, обусловленное его фармакологическими свойствами. Следовательно, необходим контроль состояния новорожденных на предмет истощения B-клеток, а вакцинацию живыми вирусными вакцинами следует отложить до восстановления количества B-клеток у ребенка (см. раздел «Особые указания»).
Период грудного вскармливания
Не установлено, проникает ли блинатумомаб в грудное молоко, но, с учетом потенциальной возможности развития нежелательных эффектов у детей грудного возраста, грудное вскармливание противопоказано во время и по крайней мере в течение 48 часов после введения препарата Блинцито.
Фертильность
Исследования для оценки воздействия препарата Блинцито на фертильность не проводились. Никакого воздействия на репродуктивные органы самцов или самок мыши в 13-недельном исследовании токсичности с мышиной суррогатной молекулой не обнаружено.
Способ применения и дозы
Лечение необходимо начинать по назначению и под контролем врача, имеющего опыт лечения гематологических злокачественных новообразований.
Для инициации терапии рецидивирующего или рефрактерного ОЛЛ рекомендована госпитализация пациента в течение минимум первых 9 дней первого цикла и первых 2 дней второго цикла.
При лечении отрицательного по филадельфийской хромосоме ОЛЛ из предшественников В-лимфоцитов с МОБ рекомендована госпитализация пациента в течение минимум первых 3 дней первого цикла терапии и первых 2 дней последующих циклов.
Детям с первым рецидивом ОЛЛ из предшественников В-лимфоцитов высокого риска рекомендована госпитализация минимум на первые 3 дня цикла терапии.
Для пациентов, имеющих в анамнезе или в настоящее время клинически значимую патологию центральной нервной системы (ЦНС) (см. раздел «Особые указания»), рекомендована госпитализация в течение минимум первых 14 дней первого цикла и минимум 2 дней второго цикла терапии (длительность необходимой госпитализации клинически оценивается в зависимости от переносимости препарата Блинцито во время первого цикла терапии). Следует соблюдать осторожность, так как наблюдались отсроченные впервые проявившиеся неврологические нарушения.
Во всех случаях инициации и возобновления (после перерыва на 4 или более часа) цикла терапии рекомендуются наблюдение медицинского работника или госпитализация пациента.
Инфузионные пакеты с препаратом Блинцито должны быть подготовлены для выполнения инфузии в течение 24 часов, 48 часов, 72 часов или 96 часов. См. раздел «Способ введения».
Режим дозирования
Рецидивирующий или рефрактерный ОЛЛ из предшественников B-лимфоцитов
Пациент с рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов может получить 2 цикла терапии. Продолжительность цикла терапии - 28 дней (4 недели); введение препарата осуществляется путем длительной внутривенной инфузии. После каждого цикла терапии следует перерыв длительностью 14 дней (2 недели).
Пациенты, достигшие полной ремиссии (ПР/ПРг*) после двух циклов терапии, могут получить до 3 дополнительных консолидирующих циклов препарата Блинцито по результатам индивидуальной оценки соотношения пользы и рисков.
Рекомендуемая суточная доза препарата определяется массой тела пациента (см. таблицу 1). Пациенты с массой тела ≥ 45 кг должны получать препарат в фиксированной дозе, у пациентов с массой тела менее 45 кг доза рассчитывается в соответствии с площадью поверхности тела (ППТ).
Таблица 1.
Рекомендуемые дозы препарата Блинцито для пациентов с рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов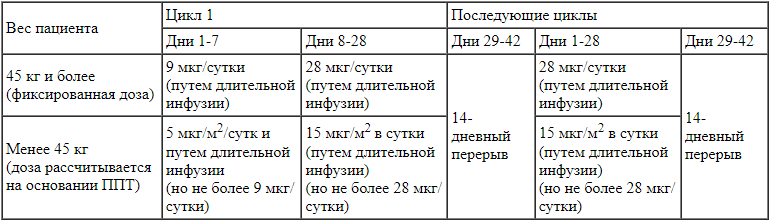 Первый рецидив ОЛЛ из предшественников B-лимфоцитов высокого риска
Первый рецидив ОЛЛ из предшественников B-лимфоцитов высокого риска
Дети с первым рецидивом ОЛЛ из предшественников B-лимфоцитов высокого риска могут получить 1 цикл терапии препаратом Блинцито после индукционной терапии и 2 блоков консолидирующей химиотерапии. Продолжительность одного цикла терапии составляет 28 дней (4 недели); введение препарата осуществляется путем длительной инфузии. Рекомендуемые суточные дозы, зависящие от массы тела ребенка, представлены в таблице 2.
Таблица 2.
Рекомендуемые дозы препарата Блинцито для постиндукционной химиотерапии у детей с первым рецидивом ОЛЛ из предшественников B-лимфоцитов высокого риска Рекомендации по премедикации и дополнительной лекарственной терапии
Рекомендации по премедикации и дополнительной лекарственной терапии
У взрослых пациентов за 1 ч до начала каждого цикла терапии Блинцито необходимо внутривенное введение дексаметазона в дозе 20 мг.
Детям дексаметазон в дозе 10 мг/м2 (но не более 20 мг) должен быть назначен перорально или внутривенно за 6-12 ч до начала инфузии Блинцито (в 1 день первого цикла терапии). Затем дексаметазон в дозе 5 мг/м2 назначается перорально или внутривенно за 30 минут до начала инфузии препарата Блинцито (в 1-й день 1-го цикла).
Для снижения температуры тела в течение первых 48 часов каждого цикла терапии рекомендуется применение антипиретиков (например, парацетамола).
До и в течение курса терапии препаратом Блинцито с целью профилактики рецидива ОЛЛ в центральной нервной системе рекомендовано интратекальное профилактическое введение химиотерапевтических препаратов.
Пре-фаза терапии пациентов с большой опухолевой массой
Пациенты, имеющие ≥ 50 % лейкемических бластов в костном мозге или ≥ 15 000 лейкемических бластов в 1 мкл периферической крови, должны получать дексаметазон (в дозе не выше 24 мг/сутки).
ОЛЛ из предшественников В-лимфоцитов с наличием МОБ
При рассмотрении вопроса о применении препарата Блинцито с целью терапии МОБ-положительного ОЛЛ из предшественников В-лимфоцитов без филадельфийской хромосомы, результаты количественного определения МОБ должны быть подтверждены результатами валидированного метода анализа с минимальной чувствительностью 10-4 Клинический анализ МОБ, вне зависимости от выбора методики, необходимо проводить в квалифицированной лаборатории, использующей методику, соответствующую общепринятым техническим требованиям.
Пациенты могут получить 1 цикл индукционной терапии с последующим проведением до 3 дополнительных консолидирующих циклов терапии препаратом Блинцито. Длительность одного индукционного или консолидирующего цикла терапии препаратом Блинцито составляет 28 дней (4 недели), в течение которых проводится непрерывная внутривенная инфузия препарата, с последующим перерывом длительностью 14 дней (2 недели) (общая длительность - 42 дня). У большинства пациентов, у которых отмечался ответ на блинатумомаб, данный ответ был достигнут после 1 цикла. Поэтому потенциальную пользу и риски, связанные с продолжением терапии у пациентов, не демонстрирующих гематологического и/или клинического улучшения после 1 цикла терапии, должен оценивать лечащий врач.
Рекомендованные дозы для пациентов с массой тела не менее 45 кг:
| Циклы терапии | |
| Индукционный цикл 1 | |
| 1-28 дни | 29-42 дни |
| 28 мкг/сутки | Перерыв 14 дней |
| Консолидирующие циклы 2-4 | |
| 1-28 дни | 29-42 дни |
| 28 мкг/сутки | Перерыв 14 дней |
Премедикация и рекомендации по дополнительной лекарственной терапии
Необходимо внутривенное введение преднизона (100 мг) или эквивалентных препаратов (например, дексаметазона в дозе 16 мг) за 1 час до начала каждого цикла терапии препаратом Блинцито.
Рекомендовано применение антипиретика (например, парацетамола) с целью снижения пирексии в течение первых 48 ч каждого цикла терапии.
Рекомендовано проведение интратекальной профилактической химиотерапии до и во время терапии препаратом Блинцито с целью профилактики рецидива ОЛЛ в центральной нервной системе.
Коррекция дозы
У пациентов с рецидивирующим или рефрактерным ОЛЛ из предшественников В-лимфоцитов и пациентов с отрицательным по филадельфийской хромосоме МОБ-положительным ОЛЛ из предшественников В-лимфоцитов, получающих препарат Блинцито, следует рассмотреть вопрос о временной или полной отмене препарата Блинцито при развитии следующих тяжелых (3 степени) или угрожающих жизни (4 степени) проявлений токсичности (см. раздел «Особые указания»): синдрома выброса цитокинов, синдрома лизиса опухоли, нейротоксичности, повышения активности печеночных ферментов и других клинически значимых нежелательных явлений.
Если перерыв в терапии после развития нежелательного явления не превышает 7 дней, следует продолжить тот же цикл терапии до суммарной продолжительности 28 дней инфузии, считая дни как до, так и после временного прекращения данного цикла. Если период временного прекращения терапии после развития нежелательного явления превышал 7 дней, начинают новый цикл терапии. Если период разрешения проявлений токсичности составляет более 14 дней, необходимо полностью отменить препарат Блинцито, за исключением наличия других рекомендаций в таблице ниже.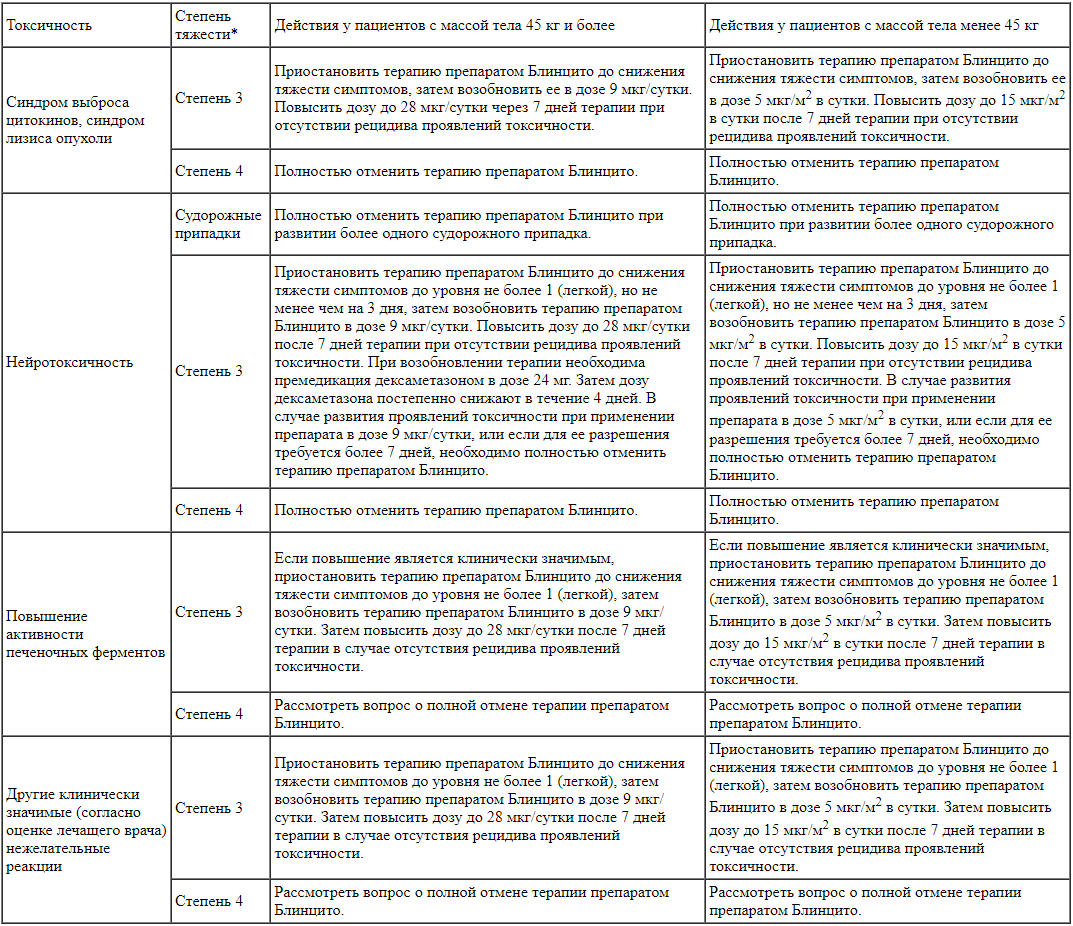 * Согласно Общим терминологическим критериям для оценки нежелательных явлений (CTCAE) NCI версии 4.0 степень 3 - тяжелые, степень 4 - жизнеугрожающие.
* Согласно Общим терминологическим критериям для оценки нежелательных явлений (CTCAE) NCI версии 4.0 степень 3 - тяжелые, степень 4 - жизнеугрожающие.
Дозирование в особых случаях
Пожилой возраст
Коррекция дозы препарата у пациентов пожилого возраста (≥ 65 лет) не требуется. Опыт применения препарата Блинцито у пациентов в возрасте ≥ 75 лет ограничен.
Нарушение функции почек
Согласно результатам анализа фармакокинетики не требуется коррекция дозы у пациентов с нарушением функции почек легкой или средней степени тяжести (см. раздел «Фармакокинетика»). Безопасность и эффективность применения препарата Блинцито у пациентов с тяжелым нарушением функции почек не исследовались.
Нарушение функции печени
Согласно результатам анализа фармакокинетики исходная функция печени не оказывала влияние на значение экспозиции блинатумомаба, и поэтому коррекция начальной дозы препарата в данной ситуации не требуется (см. раздел «Фармакокинетика»). Безопасность и эффективность препарата Блинцито у пациентов с тяжелой печеночной недостаточностью не исследовались.
Детский возраст
Безопасность и эффективность препарата Блинцито у детей < 1 года не установлены. Данные о применении препарата у детей в возрасте < 7 месяцев отсутствуют. Доступные в настоящее время данные о применении препарата у детей приведены в разделе «Побочное действие».
Особые инструкции по применению и обращению
Приготовление в асептических условиях
При приготовлении раствора для инфузий необходимо соблюдение правил асептики.
Приготовление раствора препарата Блинцито должно:
- осуществляться в асептических условиях обученным персоналом в соответствии со стандартами надлежащей практики, что особенно касается приготовления растворов лекарственных препаратов для парентерального применения в асептических условиях;
- осуществляться в условиях ламинарного потока воздуха или в вытяжном шкафу для работы с биологическими средствами, используя стандартные меры защиты для безопасного обращения со средствами, предназначенными для внутривенного введения.
С целью минимизации ошибок, в том числе применения препарата в недостаточной дозе и передозировки, представляется весьма важным, чтобы инструкции по приготовлению и введению, представленные в настоящем разделе, строго соблюдались.
Прочие инструкции
- Препарат Блинцито совместим с инфузионными пакетами и кассетами для помп, изготовленными из полиолефина, поливинилхлорида, не содержащего диэтилгексилфталата (ДЭГФ), или этиленвинилацетата (ЭВА).
- После окончания инфузии весь неиспользованный остаток лекарственного средства и сопутствующие отходы следует утилизировать в соответствии с требованиями, изложенными в действующих документах.
Приготовление раствора для инфузий
Необходимы следующие расходные материалы, не включенные в упаковку:
- стерильные одноразовые шприцы;
- иглы размером 21-23 G (рекомендуется);
- вода для инъекций;
- инфузионный пакет с 250 мл раствора натрия хлорида 9 мг/мл (0,9 %) для инъекций;
- С целью минимизации количества асептических переносов используйте предварительно заполненный инфузионный пакет объемом 250 мл. В расчете дозы препарата Блинцито учитывается фактический объем раствора натрия хлорида 9 мг/мл (0,9 %) для инъекций, который обычно составляет 265-275 мл.
- Необходимо использовать только инфузионные пакеты / кассеты для помп, изготовленные из полиолефина, ПВХ, не содержащего диэтилгексилфталат (ДЭГФ), или этиленвинилацетата (ЭВА). - система для внутривенных инфузий, изготовленная из полиолефина, ПВХ без ДЭГФ, или ЭВА, с установленным стерильным апирогенным фильтром с диаметром пор 0,2 мкм и низким связыванием белков.
Необходимо убедиться в том, что система совместима с инфузионной помпой.
Восстанавливайте препарат Блинцито водой для инъекций. Не восстанавливайте содержимое флаконов препарата Блинцито раствором (стабилизатором).
Заполняйте систему для внутривенных инфузий, используя только тот пакет, в котором содержится ПРИГОТОВЛЕННЫЙ раствор препарата Блинцито для инфузий. Не заполняйте систему раствором натрия хлорида 9 мг/мл (0,9 %) для инъекций.
Восстановление препарата Блинцито
1. Определите необходимое количество флаконов препарата Блинцито согласно назначенной дозе и длительности инфузии.
2. Восстановите порошок для приготовления концентрата Блинцито в каждом флаконе с помощью шприца и 3 мл воды для инъекций. Вливая воду во флакон с лиофилизированным порошком Блинцито, направляйте ее по стенке флакона, а не на сам порошок.
- Не восстанавливайте порошок для приготовления концентрата Блинцито раствором (стабилизатором).
- При добавлении воды для инъекций к порошку для приготовления концентрата получается раствор объемом 3,08 мл с конечной концентрацией препарата Блинцито 12,5 мкг/мл.
3. Аккуратно перемешайте содержимое вращательными движениями, избегая чрезмерного вспенивания.
- Не встряхивайте.
4. При восстановлении и перед инфузией осмотрите раствор на наличие механических включений и на предмет изменения цвета. Полученный раствор должен быть прозрачным или слегка опалесцирующим, бесцветным или слегка желтым.
- Не используйте раствор, содержащий хлопья или осадок.
Подготовка инфузионного пакета с препаратом Блинцито
При подготовке каждого инфузионного пакета с препаратом Блинцито проверяйте назначенную дозу и длительность инфузии. Во избежание ошибок при подготовке инфузионных пакетов с препаратом Блинцито руководствуйтесь объемами, указанными в таблицах 3 и 4.
- В случае пациентов с массой тела 45 кг и более см. таблицу 3.
- В случае пациентов с массой тела менее 45 кг см. таблицу 4.
1. Необходимо использовать предварительно заполненный инфузионный пакет с раствором натрия хлорида 9 мг/мл (0,9 %) для инъекций номинальным объемом 250 мл, фактический объем которого обычно составляет 265-275 мл.
2. Для создания внутреннего покрытия инфузионного пакета с помощью шприца, соблюдая правила асептики, перенесите 5,5 мл раствора (стабилизатора) в инфузионный пакет. Аккуратно перемешайте содержимое пакета, избегая вспенивания. Утилизируйте оставшийся раствор (стабилизатор).
3. С помощью шприца, соблюдая правила асептики, перенесите необходимый объем восстановленного раствора препарата Блинцито в инфузионный пакет с раствором натрия хлорида 9 мг/мл (0,9 %) для инъекций и раствором (стабилизатором). Аккуратно перемешайте содержимое пакета, избегая вспенивания.
- Объемы восстановленного раствора препарата Блинцито для пациентов с массой тела 45 кг и более представлены в таблице 3.
- Объемы восстановленного раствора препарата Блинцито для пациентов с массой тела менее 45 кг (доза рассчитывается на основании ПИТ) представлены в таблице 4.
- Утилизируйте флакон со всем неиспользованным восстановленным раствором препарата Блинцито.
4. В асептических условиях присоедините к инфузионному пакету систему для внутривенных инфузий, установив стерильный фильтр с диаметром пор 0,2 мкм. Необходимо убедиться в том, что система для внутривенных инфузий совместима с инфузионной помпой.
5. Удалите воздух из инфузионного пакета. Это особенно важно при использовании амбулаторной инфузионной помпы.
6. Заполните систему для внутривенных инфузий, используя только тот пакет, в котором содержится ПРИГОТОВЛЕННЫЙ раствор препарата Блинцито для инфузий.
7. Если немедленного использования не последовало, храните препарат при температуре 28 °C.
Таблица 3.
Для пациентов с массой тела 45 кг и более: объем раствора натрия хлорида 9 мг/мл (0,9 %) для инъекций, раствора (стабилизатора) и восстановленного раствора препарата Блинцито для добавления в инфузионный пакет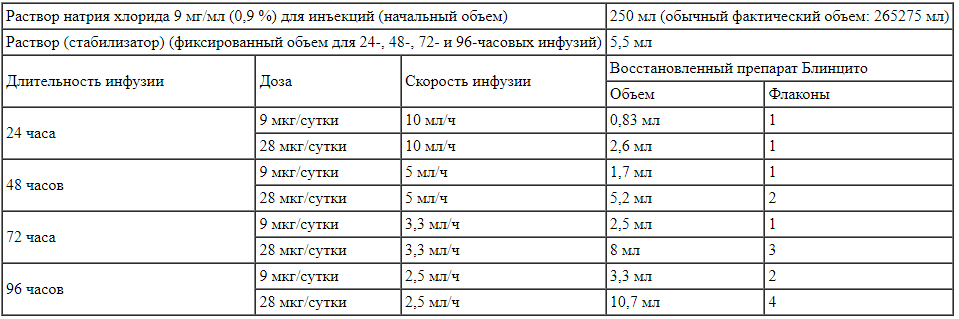 Таблица 4.
Таблица 4.
Для пациентов с массой тела менее 45 кг: объем раствора натрия хлорида 9 мг/мл (0,9 %) для инъекций, раствора (стабилизатора) и восстановленного раствора препарата Блинцито для добавления в инфузионный пакет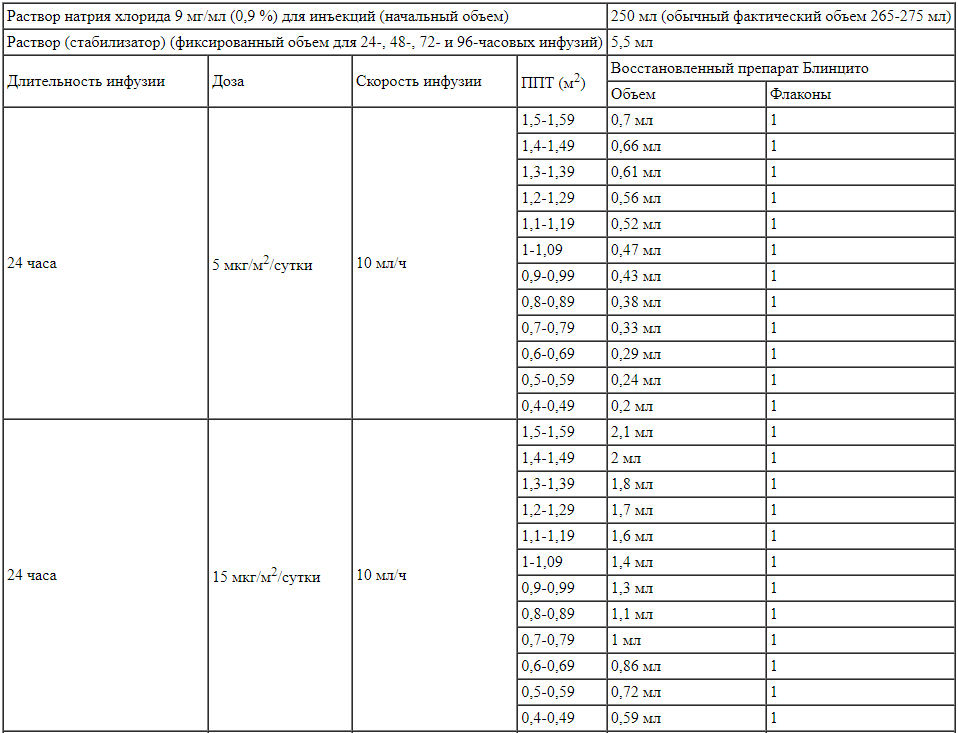

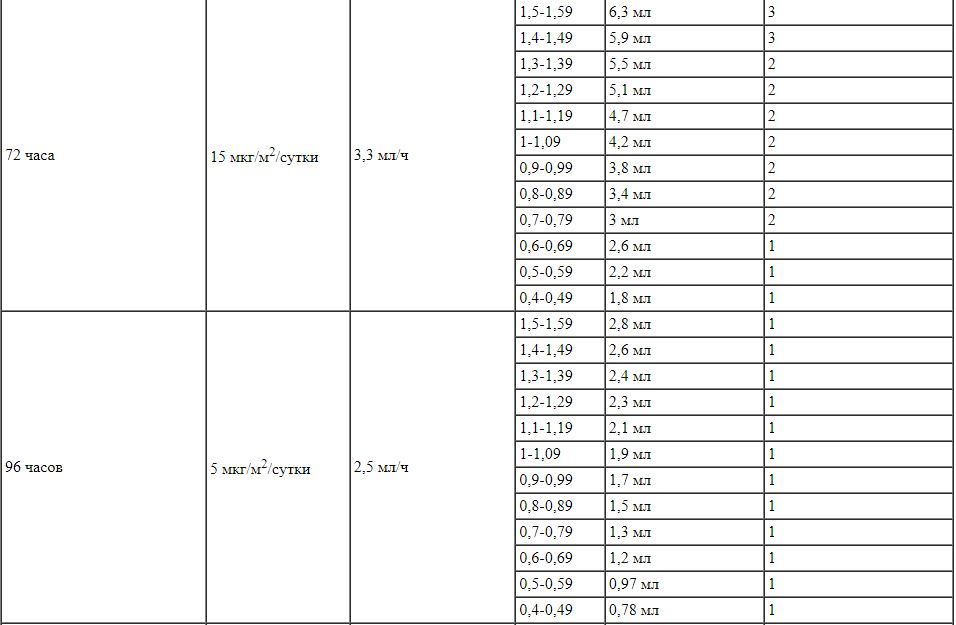
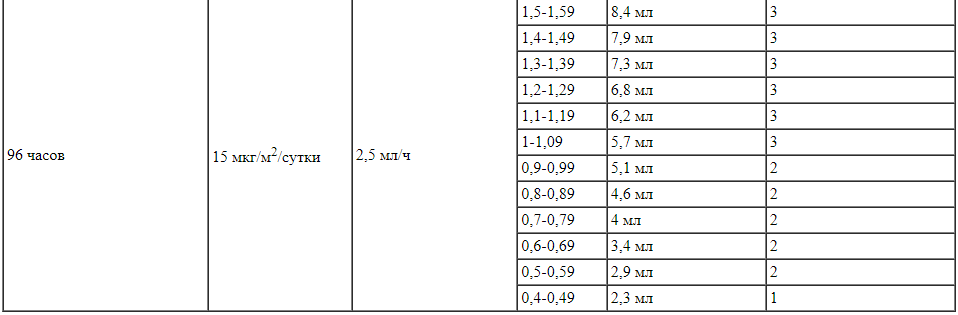 Способ введения
Способ введения
См. инструкции по приготовлению лекарственного препарата в разделе «Особые инструкции по применению и обращению».
Препарат Блинцито вводится с использованием инфузионной помпы путем длительной внутривенной инфузии с постоянной скоростью введения в течение до 96 часов. Помпа должна быть программируемой и неэластомерной, а также иметь режим блокировки и систему сигнализации.
Начальный объем препарата (270 мл) превышает объем препарата, который необходимо ввести пациенту (240 мл), и обеспечивает заполнение системы для внутривенных инфузий и получение пациентом полной дозы препарата Блинцито.
Инфузия приготовленного раствора препарата Блинцито для инфузий, согласно инструкциям по использованию приготовленных инфузионных пакетов с препаратом, осуществляется с постоянной скоростью из перечисленных ниже:
- скорость инфузии - 10 мл/ч (длительность инфузии - 24 часа);
- скорость инфузии - 5 мл/ч (длительность инфузии - 48 часов);
- скорость инфузии - 3,3 мл/ч (длительность инфузии - 72 часа);
- скорость инфузии - 2,5 мл/ч (длительность инфузии - 96 часов).
Приготовленный раствор препарата Блинцито для инфузий вводится с помощью системы для внутривенных инфузий с установленным стерильным апирогенным фильтром с диаметром пор 0,2 мкм и низким связыванием белков.
Важное примечание: не промывайте инфузионную систему или внутривенный катетер, через которые вводится препарат Блинцито, особенно при замене инфузионного пакета. Промывка при замене инфузионного пакета или завершении инфузии может привести к передозировке и развитию осложнений. При использовании многопросветного венозного катетера препарат Блинцито должен вводиться через определенный просвет.
Выбор длительности инфузии должен осуществляться лечащим врачом с учетом частоты замены инфузионных пакетов и массы тела пациента. Целевая доставляемая терапевтическая доза препарата Блинцито при этом не изменяется.
Замена инфузионного пакета
Необходима замена инфузионного пакета с периодичностью не реже 1 раза в 96 часов; данная процедура осуществляется медицинским работником ввиду необходимости соблюдения стерильности.
Побочное действие
Обзор профиля безопасности
Описанные в данном разделе нежелательные явления были выявлены в клинических исследованиях у пациентов с ОЛЛ из предшественников B-лимфоцитов (N = 1045).
Наиболее серьезными нежелательными реакциями, которые могут развиваться в процессе терапии блинатумомабом, являются: инфекции (22,6 %), неврологические нарушения (12,2 %), нейтропения/фебрильная нейтропения (9,1 %), синдром выброса цитокинов (2,7 %) и синдром лизиса опухоли (0,8 %).
Наиболее частыми нежелательными реакциями являлись: пирексия (70,8 %), инфекции, обусловленные неуточненным патогеном (41,4 %), инфузионные реакции (33,4 %), головная боль (32,7 %), тошнота (23,9 %), анемия (23,3 %), тромбоцитопения (21,6 %), отеки (21,4 %), нейтропения (20,8 %), фебрильная нейтропения (20,4 %), диарея (19,7 %), рвота (19,0 %), кожные высыпания (18,0 %), повышение активности печеночных ферментов (17,2 %), кашель (15,0 %), бактериальные инфекции (14,1 %), тремор (14,1 %), синдром высвобождения цитокинов (13,8 %), лейкопения (13,8 %), запор (13,5 %), снижение концентрации иммуноглобулинов (13,4 %), вирусные инфекции (13,3 %), гипотензия (13,0 %), боль в спине (12,5 %), озноб (11,7 %), боль в животе (10,6 %), тахикардия (10,6 %), бессонница (10,4 %), боль в конечности (10,1 %) и грибковые инфекции (9,6 %).
Табличный перечень нежелательных реакций
Перечисленные ниже нежелательные реакции сгруппированы по классам систем органов и категориям частоты встречаемости. При этом категории частоты встречаемости определяли на основе исходных значений частоты каждой нежелательной реакции в клинических исследованиях у пациентов с ОЛЛ из предшественников B-лимфоцитов (N = 1045). В рамках каждого класса систем органов нежелательные реакции представлены в порядке убывания степени серьезности.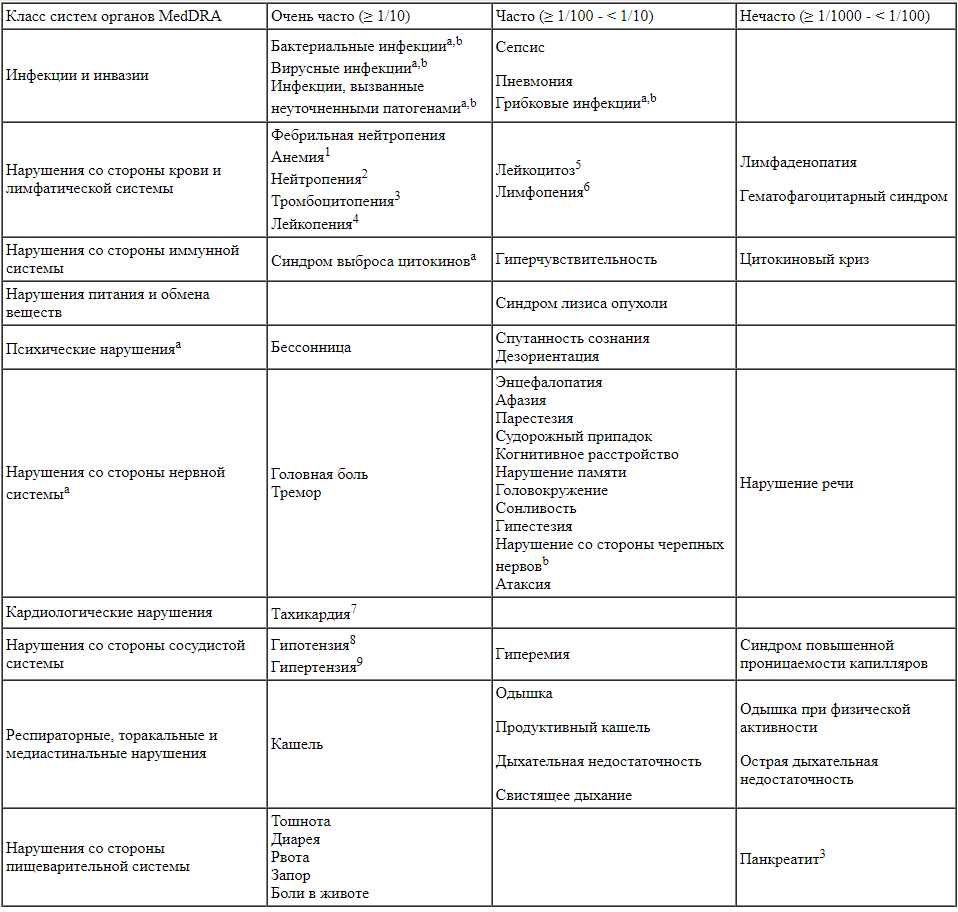
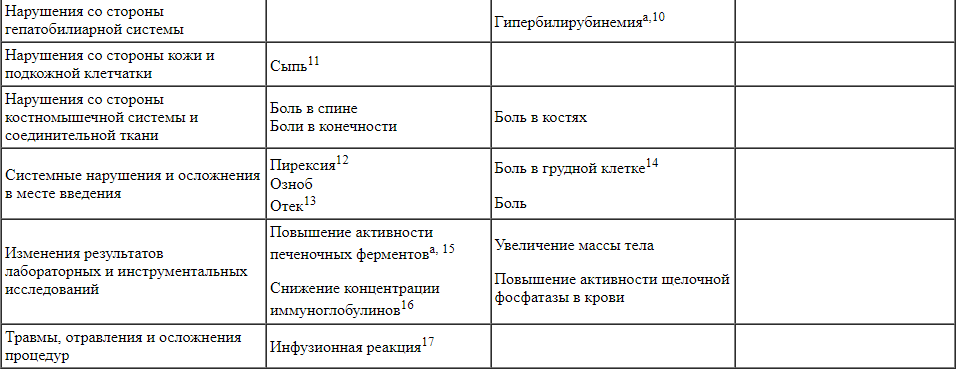 a Дополнительная информация представлена в разделе «Описание отдельных нежелательных реакций».
a Дополнительная информация представлена в разделе «Описание отдельных нежелательных реакций».
b Групповые термины MedDRA высокого уровня (MedDRA версии 23.0).
Термины нежелательных явлений, соответствующие идентичным патологическим состояниям, группировались в виде одной нежелательной реакции в приведенной выше таблице. При этом термины группировались следующим образом.
1 Анемия включала анемию и снижение концентрации гемоглобина.
2 Нейтропения включала нейтропению и снижение количества нейтрофилов.
3 Тромбоцитопения включала снижение количества тромбоцитов и тромбоцитопению.
4 Лейкопения включала лейкопению и снижение количества лейкоцитов.
5 Лейкоцитоз включал лейкоцитоз и повышение количества лейкоцитов.
6 Лимфопения включала снижение количества лимфоцитов и лимфопению.
7 Тахикардия включала синусовую тахикардию, суправентрикулярную тахикардию, тахикардию, предсердную тахикардию и желудочковую тахикардию.
8 Гипотензия включала снижение артериального давления и гипотензию.
9 Гипертензия включала повышение артериального давления и гипертензию.
10 Гипербилирубинемия включала повышение концентрации билирубина в крови и гипербилирубинемию.
11 Кожные высыпания включали эритему, кожные высыпания, кожные высыпания эритематозные, кожные высыпания генерализованные, кожные высыпания макулезные, кожные высыпания макулопапулезные, кожные высыпания зудящие, кожные высыпания в месте установки катетера, кожные высыпания пустулезные, кожные высыпания генитальные, кожные высыпания папулезные и кожные высыпания везикулезные.
12 Пирексия включала повышение температуры тела и пирексию.
13 Отек включал отек костного мозга, периорбитальный отек, отек век, отек глаз, отек губ, отек лица, локальный отек, генерализованный отек, отек, периферический отек, отек в месте инфузии, отек почек, отек мошонки, отек половых органов, отек легких, отек гортани, ангиоотек, отек околоротовой полости и лимфатический отек.
14 Боль в груди включала дискомфорт в груди, боль в грудной клетке, скелетно-мышечную боль в грудной клетке и некардиогенную боль в грудной клетке.
15 Повышение активности печеночных ферментов включало повышение активности аланинаминотрансферазы, повышение активности аспартатаминотрансферазы, повышение активности гамма-глутамилтранспептидазы, повышение активности печеночных ферментов, повышение показателя функциональной пробы печени и повышение активности трансаминаз.
16 Снижение концентрации иммуноглобулинов включало снижение концентрации иммуноглобулина G в крови, снижение концентрации иммуноглобулина A в крови, снижение концентрации иммуноглобулина M в крови, снижение концентрации глобулинов, гипогаммаглобулинемию, гипоглобулинемию и снижение концентрации иммуноглобулинов.
17 Инфузионные реакции - составной термин, включавший инфузионную реакцию и следующие нежелательные явления, отмечавшиеся в течение первых 48 часов инфузии и длившиеся в течение ≤ 2 дней: пирексию, синдром выброса цитокинов, гипотензию, миалгию, острое повреждение почек, гипертензию, кожные высыпания, тахипноэ, отек лица, отечность лица и эритематозные кожные высыпания.
Описание отдельных нежелательных реакций
Неврологические нарушения
В рамках рандомизированного клинического исследования III фазы (N = 267) и несравнительного клинического исследования II фазы (N = 189) с участием пациентов с отрицательным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов, получавших препарат Блинцито, у 66,0 % пациентов отмечалась одна или несколько неврологических нежелательных реакций (в том числе психические нарушения), главным образом со стороны ЦНС. Серьезные и ≥ 3 степени тяжести неврологические нежелательные реакции отмечались у 11,6 % и 12,1 % пациентов, соответственно; из них наиболее часто встречавшимися серьезными нежелательными явлениями являлись энцефалопатия, тремор, афазия и спутанность сознания. Большинство неврологических нарушений (80,5 %) являлись клинически обратимыми и разрешились после приостановления терапии препаратом Блинцито. Медиана времени до развития первого нежелательного явления находилась в рамках первых двух недель терапии. Был зарегистрирован один случай энцефалопатии с летальным исходом в несравнительном исследовании II фазы, проводившемся на ранних сроках программы клинических исследований.
Неврологические нежелательные явления отмечались у 62,2 % взрослых пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов (N = 45). Серьезные неврологические нежелательные явления и неврологические нежелательные явления степени 3 или выше отмечались в случае каждой из этих категорий у 13,3 % взрослых пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников В-лимфоцитов.
Неврологические нежелательные явления отмечались у 71,5 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников В-лимфоцитов (N = 137); у 22,6 % пациентов отмечались серьезные нежелательные явления. Нежелательные явления ≥ 3 и ≥ 4 степени отмечались у 16,1 % и 2,2 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников В-лимфоцитов, соответственно.
Принципы клинического ведения неврологических нарушений описаны в разделе «Особые указания».
Инфекции
У пациентов, получавших препарат Блинцито, регистрировались угрожающие жизни или летальные (≥ 4 степени) вирусные, бактериальные и грибковые инфекции. Дополнительно к этому, в клиническом исследовании II фазы у взрослых пациентов с рецидивирующим или рефрактерным отрицательным по филадельфийской хромосоме ОЛЛ из предшественников В-лимфоцитов отмечались случаи реактивации вирусных инфекций (например, полиомы (BK)). У пациентов с рецидивирующим или рефрактерным отрицательным по филадельфийской хромосоме ОЛЛ из предшественников В-лимфоцитов, имевших индекс общего состояния ECOG = 2 на момент исходной оценки отмечалось повышение частоты серьезных инфекций по сравнению с пациентами, у которых индекс общего состояния ECOG составлял < 2. Принципы клинического ведения инфекции приведены в разделе «Особые указания».
Синдром выброса цитокинов (СВЦ)
В рамках рандомизированного клинического исследования III фазы (N = 267), а также несравнительного клинического исследования II фазы (N = 189) с участием пациентов с отрицательным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников В-лимфоцитов, получавших препарат Блинцито, у 14,7 % пациентов отмечался СВЦ. Случаи серьезного СВЦ отмечались у 2,4 % пациентов; медиана времени до их развития составляла 2 дня.
Синдром выброса цитокинов отмечался у 8,9 % взрослых пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов (N = 45); у 2,2 % пациентов отмечались серьезные нежелательные явления. О нежелательных явлениях степени ≥ 3 или ≥ 4 не сообщалось.
Синдром выброса цитокинов отмечался у 2,9 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов (N = 137). Нежелательные явления 3 степени и серьезные нежелательные явления отмечались соответственно у 1,5 % и 1,5 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов; нежелательных явлений ≥ 4 степени не отмечалось.
Синдром повышенной проницаемости капилляров отмечался у одного пациента в клиническом исследовании II фазы с участием взрослых пациентов с отрицательным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов и у одного пациента в клиническом исследовании II фазы с участием взрослых пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов. Синдром повышенной проницаемости капилляров не отмечался у взрослых пациентов в клиническом исследовании II фазы с участием пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов.
Принципы клинического ведения СВЦ приведены в разделе «Особые указания».
Повышение активности печеночных ферментов
В рамках рандомизированного клинического исследования III фазы (N = 267) и несравнительного клинического исследования II фазы (N = 189) с участием пациентов с отрицательным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов, получавших Блинцито, у 22,4 % пациентов отмечалось повышение активности печеночных ферментов и возникновение соответствующих признаков или симптомов. Серьезные нежелательные реакции и нежелательные реакции ≥ 3 степени (в частности, повышение активности АЛТ, повышение активности АСТ и повышение концентрации билирубина в крови) отмечались у 1,5 % и 13,6 % пациентов, соответственно. Медиана времени до развития первого эпизода данных нежелательных реакций составляла 4 дня с момента начала терапии препаратом Блинцито.
Повышенная активность печеночных ферментов отмечалась у 17,8 % взрослых пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов (N = 45); у 2,2 % пациентов отмечались серьезные нежелательные явления. Нежелательные явления степени ≥ 3 и ≥ 4 отмечались соответственно у 13,3 % и 6,7 % взрослых пациентов с положительным по филадельфийской хромосоме рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов.
Повышение активности печеночных ферментов отмечалось у 12,4 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов (N = 137). Нежелательные явления ≥ 3 и ≥ 4 степени, соответственно, отмечались у 8,0 % и 4,4 % взрослых пациентов с МОБ-положительным ОЛЛ из предшественников B-лимфоцитов.
Длительность нежелательных реакций со стороны печени обычно была короткой, и они быстро разрешались, часто - без прекращения терапии препаратом Блинцито.
Принципы клинического ведения случаев повышения активности печеночных ферментов описаны в разделе «Особые указания».
Панкреатит
Случаи панкреатита (угрожавшего жизни или летального) отмечались у пациентов, получавших препарат Блинцито в клинических исследованиях и в пострегистрационном применении. Медиана времени до развития данных нежелательных реакций составляла 7,5 дней. Принципы клинического ведения панкреатита описаны в разделе «Особые указания».
Лейкоэнцефалопатия, в том числе прогрессирующая мультифокальная лейкоэнцефалопатия
Наблюдались случаи лейкоэнцефалопатии. У пациентов, у которых на МРТ/КТ головного мозга выявлялись изменения, соответствующие лейкоэнцефалопатии, были отмечены серьезные нежелательные явления, в том числе спутанность сознания, тремор, когнитивное расстройство, энцефалопатия и судороги. Хотя существует вероятность развития прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ), до настоящего времени в клинических исследованиях подтвержденные случаи ПМЛ не зарегистрированы.
Дети
Препарат Блинцито исследовался у детей с рецидивирующим или рефрактерным ОЛЛ из предшественников B-лимфоцитов в рамках несравнительного исследования I/II фазы применения препарата с эскалацией и последующей оценкой подбора доз (MT103-205), в которое было включено 70 детей в возрасте от 7 месяцев до 17 лет, получавших препарат в рекомендуемом режиме дозирования.
Наиболее часто регистрировавшимися серьезными нежелательными явлениями являлись: пирексия (11,4 %), фебрильная нейтропения (11,4 %), синдром выброса цитокинов (5,7 %), сепсис (4,3 %), инфекция, связанная с использованием устройства (4,3 %), передозировка (4,3 %), судорожные припадки (2,9 %), дыхательная недостаточность (2,9 %), гипоксия (2,9 %), пневмония (2,9 %) и полиорганная недостаточность (2,9 %).
Нежелательные реакции, отмечавшиеся у детей, получавших препарат Блинцито, были аналогичны по типу регистрировавшимся у взрослых пациентов. Нежелательными реакциями, отмечавшимися более часто (различие составляло ≥ 10 %) у детей по сравнению со взрослыми, являлись: анемия, тромбоцитопения, лейкопения, пирексия, инфузионные реакции, увеличение массы тела и артериальная гипертензия.
Виды и частота нежелательных явлений были аналогичны у детей различных подгрупп (выделенных в зависимости от пола, возраста и географического региона).
При применении препарата в дозе, превышавшей рекомендуемую, в рамках исследования MT103-205 был зарегистрирован случай летальной сердечной недостаточности на фоне угрожающего жизни синдрома выброса цитокинов (СВЦ) и синдрома лизиса опухоли (СЛО); см. раздел «Особые указания».
Применение препарата Блинцито также оценивалось у детей с первым рецидивом ОЛЛ из предшественников В-лимфоцитов высокого риска в рандомизированном контролируемом открытом исследовании фазы III (20120215), в рамках которого 54 пациента в возрасте от 1 года до 18 лет получали препарат в рекомендуемой дозе для лечения впервые рецидивирующего ОЛЛ из предшественников В-лимфоцитов высокого риска. Профиль безопасности препарата Блинцито в исследовании 20120215 соответствует профилю безопасности у исследованной популяции детей с рецидивирующим или рефрактерным ОЛЛ из предшественников В-лимфоцитов.
Другие особые популяции
Опыт применения препарата Блинцито у пациентов пожилого возраста (≥ 75 лет) ограничен. В целом, профиль безопасности у пациентов пожилого возраста (≥ 65 лет) и пациентов младше 65 лет, получавших препарат Блинцито, были сопоставимыми. Однако пожилые пациенты могут быть более подвержены серьезным неврологическим явлениям, таким как когнитивное расстройство, энцефалопатия и спутанность сознания.
Пациенты пожилого возраста с МОБ-положительным ОЛЛ, получающие препарат Блинцито, могут иметь повышенный риск развития гипогаммаглобулинемии по сравнению с более молодыми пациентами. Во время проведения терапии препаратом Блинцито пациентам пожилого возраста рекомендовано контролировать концентрацию иммуноглобулинов.
Безопасность применения препарата Блинцито у пациентов с тяжелым нарушением функции почек не оценивалась.
Иммуногенность
В клинических исследованиях при ОЛЛ у взрослых пациентов, получавших препарат Блинцито, лишь у < 3 % обследованных пациентов регистрировались антитела к блинатумомабу. У шести из этих пациентов были обнаружены антитела к блинатумомабу с нейтрализующей активностью in vitro. Не обнаружены антитела к блинатумомабу в клинических исследованиях с участием детей, получавших блинатумомаб, при рецидивирующем или рефрактерном ОЛЛ.
При подозрении на продукцию антител к блинатумомабу с клинически значимым эффектом необходимо связаться с организацией, принимающей претензии от потребителя в Российской Федерации с целью обсуждения проведения анализа на наличие антител.
Передозировка
Зарегистрированы случаи передозировки препарата Блинцито, в том числе один пациент получил данный препарат в дозе, в 133 раза превышавшей рекомендуемую терапевтическую, в течение одной инфузии. Передозировка приводила к развитию нежелательных реакций, соответствовавшим реакциям, наблюдавшимся при применении препарата в рекомендуемой терапевтической дозе (повышение температуры тела, тремор и головная боль). В случае передозировки необходимо временно прекратить инфузию и обеспечить контроль состояния пациента. Вопрос о возобновлении терапии препаратом Блинцито в правильной терапевтической дозе должен рассматриваться после разрешения всех симптомов и не ранее чем через 12 ч после прекращения инфузии (см. раздел «Способ применения и дозы»).
Взаимодействие с другими лекарственными средствами
Формальные исследования по оценке лекарственных взаимодействий не проводились. Результаты исследования in vitro с использованием гепатоцитов человека свидетельствуют о том, что блинатумомаб не оказывает влияния на активность изоферментов CYP450.
В начальном периоде терапии препаратом Блинцито отмечается транзиторный выброс цитокинов в течение первых дней терапии, что может подавлять активность изоферментов CYP450. Пациенты, получающие лекарственные средства, воздействующие на активность CYP450 и транспортеров субстратов с узким терапевтическим индексом, должны наблюдаться на предмет нежелательных эффектов (например, варфарин) или концентрации данных препаратов в крови (например, циклоспорин) в течение этого периода времени. Доза одновременно используемого лекарственного средства должна корректироваться при необходимости.
Особые указания
Прослеживаемость
Для улучшения прослеживаемости биологических лекарственных препаратов необходимо точно документировать наименование и номер серии применяемого препарата.
Неврологические нарушения
В процессе применения препарата отмечались случаи неврологических нарушений, в том числе с летальным исходом. Неврологическими нарушениями 3 или более высокой степени (согласно Общим терминологическим критериям для оценки нежелательных явлений версии 4.0) (т.е. тяжелыми или угрожающими жизни), отмечавшимися после начала терапии блинатумомабом, являлись энцефалопатия, судорожные припадки, нарушения речи, нарушения сознания, спутанность сознания, дезориентация и нарушения координации движений и равновесия. У пациентов, у которых отмечались неврологические нарушения, медиана времени до их первого эпизода находилась в диапазоне первых 2 недель терапии; большинство из них разрешились после временного прекращения терапии, и они нечасто приводили к досрочной отмене препарата Блинцито.
Пожилые пациенты могут быть более склонны к развитию серьезных неврологических нарушений, в частности, когнитивных расстройств, энцефалопатии и спутанности сознания. Пациенты, имеющие в анамнезе неврологические нарушения (в частности головокружение, гипестезию, гипорефлексию, тремор, дизестезию, парестезию и нарушение памяти), характеризовались более высокой частотой неврологических нарушений (в частности тремора, головокружения, спутанности сознания, энцефалопатии и атаксии) на фоне терапии. У данных пациентов медиана времени до развития первого неврологического нарушения соответствовала первому циклу терапии.
Опыт применения препарата у пациентов с наличием в анамнезе или в настоящее время клинически значимой патологии ЦНС (в частности эпилепсии, судорожных припадков, пареза, афазии, инсульта, тяжелых повреждений головного мозга, деменции, болезни Паркинсона, патологии мозжечка, синдрома органического поражения головного мозга и психозов) ограничен, поскольку они исключались из клинических исследований. Существует вероятность повышенного риска неврологических нарушений в этой популяции пациентов. Необходимо тщательно соотносить потенциальную пользу терапии с риском неврологических нарушений и с особой осторожностью использовать препарат Блинцито у этих пациентов.
Опыт применения блинатумомаба у пациентов с документированным поражением ЦНС или спинномозговой жидкости (СМЖ) при ОЛЛ ограничен. Однако в клинических исследованиях пациенты получали блинатумомаб после элиминации бластов из СМЖ в результате применения терапии, направленной на ЦНС (например, интратекальной химиотерапии). Поэтому после элиминации бластов из СМЖ возможно начало терапии препаратом Блинцито.
Рекомендуется проведение неврологического обследования до начала терапии препаратом Блинцито и клинический мониторинг пациентов на предмет признаков и симптомов неврологических нарушений (например, путем теста почерка). Для коррекции этих признаков и симптомов до разрешения может потребоваться временная или полная отмена терапии препаратом Блинцито (см. раздел «Способ применения и дозы»). При развитии судорожных припадков рекомендуется вторичная профилактика соответствующим антиконвульсантом (например, леветирацетамом).
Инфекции
У пациентов, получавших блинатумомаб, отмечались серьезные инфекции, в том числе сепсис, пневмония, бактериемия, оппортунистические инфекции и инфекции в месте установки катетера, некоторые из которых угрожали жизни или привели к летальному исходу. У взрослых пациентов, имевших индекс общего состояния Восточной объединенной онкологической группы США (ECOG) на момент исходной оценки 2, отмечалось повышение частоты серьезных инфекций по сравнению с пациентами, у которых индекс общего состояния ECOG составлял < 2. Опыт применения препарата Блинцито у пациентов с активными неконтролируемыми инфекциями ограничен.
Пациенты, получающие препарат Блинцито, должны клинически наблюдаться на предмет признаков и симптомов инфекций и получать соответствующее лечение. Коррекция инфекций может требовать временного или полного прекращения терапии препаратом Блинцито (см. «Способ применения и дозы»).
Синдром выброса цитокинов и инфузионные реакции
У пациентов, получавших препарат Блинцито, отмечались случаи синдрома выброса цитокинов (СВЦ), которые угрожали жизни или привели к летальному исходу (≥ 4 степени) (см. раздел «Побочное действие»).
Серьезные нежелательные явления, которые могли являться признаками или симптомами СВЦ, являются пирексия, астения, головная боль, гипотензия, повышение концентрации общего билирубина и тошнота; нечасто эти нежелательные явления приводили к досрочной отмене терапии препаратом Блинцито. Медиана времени до развития СВЦ составляла 2 дня. Пациенты должны тщательно наблюдаться на предмет признаков и симптомов этих нежелательных явлений. Синдром диссеминированного внутрисосудистого свертывания (ДВС) и синдром повышенной проницаемости капилляров (СППК) (например, гипотензия, гипоальбуминемия, отеки и гемоконцентрация) часто отмечаются при СВЦ (см. раздел «Побочное действие»). Пациенты, у которых отмечается развитие СППК, должны получать соответствующее лечение.
Случаи гемофагоцитарного синдрома/синдрома активации макрофагов нечасто отмечались при СВЦ.
Инфузионные реакции могут быть клинически неотличимы от проявлений СВЦ (см. раздел «Побочное действие»). Инфузионные реакции обычно развиваются быстро (в течение 48 часов после начала инфузии). Однако у ряда пациентов отмечались отсроченные инфузионные реакции или таковые развивались во время последующих циклов терапии. Пациенты должны тщательно наблюдаться на предмет инфузионных реакций, особенно в начале первого и второго циклов терапии, и получать соответствующее лечение. С целью уменьшения выраженности пирексии в течение первых 48 часов каждого цикла терапии рекомендуется использование антипиретиков (например, парацетамола). С целью снижения риска СВЦ важно начинать терапию препаратом Блинцито (в 1-7 дни 1 цикла терапии) в рекомендуемой начальной дозе (см. раздел «Способ применения и дозы»).
Коррекция этих реакций может требовать временного или полного прекращения терапии препаратом Блинцито (см. раздел «Способ применения и дозы»).
Синдром лизиса опухоли (СЛО)
У пациентов, получавших препарат Блинцито, отмечались случаи СЛО, в том числе жизнеугрожающие или летальные (≥ 4 степени).
В процессе терапии препаратом Блинцито необходимы соответствующие профилактические меры, в том числе агрессивная гидратация и антигиперурикемическая терапия (например, аллопуринолом или расбуриказой) с целью профилактики и коррекции СЛО, особенно у пациентов с выраженным лейкоцитозом или значительной опухолевой массой. Пациенты должны тщательно наблюдаться на предмет признаков и симптомов СЛО, в том числе с контролем функции почек и водного баланса в течение первых 48 часов после первой инфузии препарата. В клинических исследованиях у пациентов с нарушением функции почек средней тяжести отмечалось повышение частоты СЛО по сравнению с пациентами с нормальной функцией почек или ее нарушением легкой степени тяжести. Коррекция этих реакций может требовать временного или полного прекращения терапии препаратом Блинцито (см. раздел «Способ применения и дозы»).
Нейтропения и фебрильная нейтропения
У пациентов, получавших препарат Блинцито, отмечались случаи нейтропении и фебрильной нейтропении, в том числе жизнеугрожающие. Необходим мониторинг лабораторных показателей (в том числе, но не только: количества лейкоцитов и абсолютного количества нейтрофилов) в течение инфузии препарата Блинцито, особенно в течение первых 9 дней первого цикла терапии, а также адекватная коррекция данных реакций.
Повышение активности печеночных ферментов
Терапия препаратом Блинцито ассоциировалась с транзиторным повышением активности печеночных ферментов. Большинство данных случаев наблюдались в течение первой недели терапии и не требовали временного прекращения или полной отмены препарата Блинцито (см. раздел «Побочное действие»).
Необходим мониторинг активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), гамма-глутамилтранспептидазы (ГГТП) и концентрации общего билирубина в крови до начала и в процессе терапии препаратом Блинцито, особенно в течение первых 48 ч первых двух циклов терапии. Коррекция этих реакций может требовать временного или полного прекращения терапии препаратом Блинцито (см. раздел «Способ применения и дозы»).
Панкреатит
Случаи панкреатита, в том числе жизнеугрожающие или летальные, отмечались у пациентов, получавших препарат Блинцито в клинических исследованиях и в процессе его применения в период после регистрации препарата. Высокодозная терапия стероидами может, в некоторых случаях, способствовать развитию панкреатита.
Пациенты должны тщательно наблюдаться на предмет симптомов и признаков панкреатита путем объективного обследования, лабораторных анализов сыворотки крови (амилазы и липазы) и исследований брюшной полости (например, ультразвукового исследования) и других адекватных диагностических исследований. Коррекция панкреатита может требовать временного или полного прекращения терапии препаратом Блинцито (см. раздел «Способ применения и дозы»).
Лейкоэнцефалопатия, в том числе прогрессирующая мультифокальная лейкоэнцефалопатия Случаи лейкоэнцефалопатии по данным магнитно-резонансной томографии (МРТ) головного мозга отмечались у пациентов, получавших препарат Блинцито, особенно получавших ранее лучевую терапию на область черепа и антилейкемическую химиотерапию (в том числе системную терапию высокими дозами метотрексата или интратекальную терапию цитарабином). Клиническое значение этих изменений, регистрируемое при лучевых исследованиях, неизвестно. Вследствие потенциального риска развития прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ) пациенты должны наблюдаться на предмет соответствующих признаков и симптомов. При подозрении на ее развитие следует рассмотреть вопрос о проведении консультации невролога, проведении МРТ головного мозга и исследовании спинномозговой жидкости (СМЖ) - см. раздел «Побочное действие».
Рецидив CD 19-отрицательного ОЛЛ
У пациентов с рецидивом, получавших препарат Блинцито, наблюдались случаи СD19-отрицательного ОЛЛ из предшественников B-лимфоцитов. При проведении исследования костного мозга необходимо уделять особое внимание оценке экспрессии CD19.
Трансформация ОЛЛ в острую миелоидную лейкемию (ОМЛ)
Трансформация ОЛЛ в ОМЛ редко отмечалась у пациентов с рецидивом, получавших препарат Блинцито, в том числе у пациентов без иммунофенотипических и (или) цитогенетических аномалий в первичном диагнозе. Необходим контроль всех пациентов с рецидивом на наличие ОМЛ.
Иммунизация
Безопасность иммунизации живыми вирусными вакцинами в процессе или после завершения терапии препаратом Блинцито не исследовалась. Поэтому не рекомендуется вакцинация живыми вирусными вакцинами в течение минимум 2 недель до начала терапии препаратом Блинцито, в течение курса терапии им и до восстановления количества B-лимфоцитов до нормального уровня после последнего цикла терапии.
Вследствие потенциального истощения B-лимфоцитов у новорожденных после введения блинатумомаба в период беременности, необходим контроль состояния новорожденных на предмет истощения количества B-лимфоцитов, а также необходимо отложить иммунизацию живыми вирусными вакцинами до восстановления количества B-лимфоцитов у ребенка (см. раздел «Применение при беременности и в период грудного вскармливания»).
Контрацепция
Женщины с детородным потенциалом должны использовать эффективные методы контрацепции в течение курса терапии препаратом Блинцито, а также в течение минимум 48 часов после этого (см. раздел «Применение при беременности и в период грудного вскармливания»).
Ошибки применения препарата
Отмечались случаи ошибок применения препарата Блинцито. Исключительную важность имеет соблюдение инструкции по приготовлению (в том числе восстановлению и разведению) и введению препарата с целью минимизации данных ошибок (в том числе применения препарата в недостаточной дозе и передозировки) (см. раздел «Способ применения и дозы»).
Вспомогательные вещества с известным действием
Препарат Блинцито содержит менее 1 ммоль (23 мг) натрия в объеме, вводимом в течение 24 часов, т.е. может рассматриваться как практически не содержащий натрия.
Влияние лекарственного препарата для медицинского применения на способность управлять транспортными средствами, механизмами
Препарат Блинцито оказывал значительное влияние на способность управлять транспортными средствами и механизмами. Возможно развитие спутанности сознания и дезориентации, нарушение координации движений и равновесия, а также повышение риска судорожных припадков и нарушений сознания (см. раздел «Особые указания»). Вследствие потенциального риска неврологических нарушений пациенты, получающие блинатумомаб, должны воздерживаться от управления автомобилем, участия в опасной трудовой или иной деятельности, в частности, управлении транспортными средствами или работе с тяжелыми или потенциально опасными механизмами, в процессе терапии данным препаратом. Пациенты должны быть проинструктированы о возможности развития у них неврологических нарушений.
Форма выпуска
Порошок для приготовления концентрата для приготовления раствора для инфузий, 35 мкг: по 35 мкг активного вещества во флаконе объемом 4 мл из стекла I гидролитического класса с эластомерной пробкой, алюминиевым колпачком и отламывающимся полипропиленовым колпачком.
Раствор стабилизатора для приготовления раствора для инфузий: по 10 мл во флаконе из стекла I гидролитического класса с эластомерной пробкой, алюминиевым колпачком и отламывающимся полипропиленовым колпачком. 1 маркированный флакон с лекарственным препаратом и 1 маркированный флакон с раствором стабилизатора помещают в контурную ячейковую упаковку из пластика. Одну контурную ячейковую упаковку вместе с инструкцией по применению помещают в картонную пачку.
На каждую пачку наклеивают прозрачные защитные этикетки для контроля первого вскрытия, имеющие продольную цветную полосу.
Условия хранения
Хранить при температуре от 2 до 8 °C в оригинальной упаковке для защиты от света. Не замораживать. Хранить в недоступном для детей месте!
После вскрытия упаковки
Максимальное время хранения флакона с порошком препарата Блинцито и раствором стабилизатора для приготовления раствора для инфузий* при температуре от 23 до 27 °С составляет 8 часов.
Максимальное время хранения флакона восстановленного раствора препарата Блинцито* при температуре от 23 до 27 °С составляет 4 часа; при температуре от 2 до 8 °C - 24 часа.
Максимальное время хранения приготовленного инфузионного пакета, содержащего раствор препарата Блинцито для инфузий**, при температуре от 23 до 27 °C составляет 96 часов*; при температуре от 2 до 8 °C - 10 суток.
*Хранить флаконы с порошком препарата Блинцито и раствором стабилизатора для приготовления раствора для инфузий в защищенном от света месте.
**Время хранения включает в себя время инфузии. Если инфузионный пакет, содержащий раствор препарата Блинцито для инфузий, не использован в указанные сроки и при указанных температурах, он должен быть утилизирован; повторное охлаждение в холодильнике не допускается.
Срок годности
5 лет.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
Амджен Европа Б.В.
Минервум 7061
4817 ZK Бреда
Нидерланды
Производитель
Производитель готовой лекарственной формы / фасовщик (первичная упаковка)
Берингер Ингельхайм Фарма ГмбХ и Ко. КГ, Биркендорфер Штрассе 65, 88397 Биберах-на-Риссе, Германия или
Амджен Технолоджи (Айрлэнд) Анлимитед Компани, Поттери Роуд, Дан Лэйри, Графство Дублин, Ирландия.
Упаковщик (вторичная (потребительская) упаковка)
Амджен Европа Б.В., Минервум 7061, 4817 ZK Бреда, Нидерланды или
Открытое акционерное общество «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), 450077, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28, Россия.
Выпускающий контроль качества
Амджен Европа Б.В., Минервум 7061, 4817 ZK Бреда, Нидерланды или Открытое акционерное общество «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), 450077, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28, Россия.
Организация, принимающая претензии от потребителей
ООО «Амджен»
123112, Москва; Пресненская набережная, д. 8, строение 1; 7 этаж
Комментарии
ПРАКТИКА ПЕДИАТРА
