Абаджио - инструкция по применению
Синонимы, аналоги СтатьиРегистрационный номер:
ЛП-002520Торговое название препарата:
Абаджио®.Международное непатентованное название:
терифлуномид.Лекарственная форма:
таблетки, покрытые пленочной оболочкой.Состав
В 1 таблетке, покрытой пленочной оболочкой*, содержится:
активное вещество: терифлуномид - 14,0 мг;
вспомогательные вещества:
ядро таблетки: лактозы моногидрат - 76,0 мг; кукурузный крахмал - 38,0 мг; гидроксипропилцеллюлоза - 3,5 мг; целлюлоза микрокристаллическая - 10,5 мг; карбоксиметилкрахмал натрия - 7,5 мг; магния стеарат - 0,5 мг;
оболочка таблетки (Opadray® система покрытия пленкой 03F20651 голубой): гипромеллоза - 3,607 мг; титана диоксид E 171 - 0,902 мг; тальк - 0,271 мг; макрогол - 0,158 мг; алюминиевый лак индигокармина Е 132 - 0,062 мг.
* В процессе приготовления таблеток, покрытых оболочкой, для связывания и пленочного покрытия используется вода очищенная (ЕФ, Ф.США/НФ), которая удаляется в процессе обработки.
Описание:
пятиугольные таблетки, покрытые пленочной оболочкой бледноголубого цвета; на одной стороне таблетки отпечатано «14», на другой выгравирован логотип фирмы.
На поперечном разрезе ядро белого или почти белого цвета.
Фармакотерапевтическая группа:
селективный иммунодепрессант.
Код АТХ:
L04AA.Фармакологические свойства
Фармакодинамика
Механизм действия
Терифлуномид - иммуномодулирующий лекарственный препарат с противовоспалительными свойствами, селективно и обратимо ингибирующий митохондриальный фермент дигидрооротатдегидрогеназу (ДГО-ДГ), который необходим для синтеза пиримидина de novo. Таким образом, терифлуномид блокирует пролиферацию стимулированных лимфоцитов, для которых необходим синтез пиримидина de novo. Точный механизм, с помощью которого терифлуномид оказывает свое терапевтическое действие при рассеянном склерозе, изучен неполностью, но он может включать уменьшение числа активированных лимфоцитов в центральной нервной системе (ЦНС). Возможно, что терифлуномид уменьшает число периферических активированных лимфоцитов, которые могут мигрировать в ЦНС.
Фармакодинамические эффекты
Иммунная система (влияние на количество иммунных клеток в крови)
Влияние на количество иммунных клеток в крови: в ходе плацебо-контролируемых исследований прием терифлуномида в дозе 14 мг один раз в день приводил к незначительному снижению среднего количества лимфоцитов в периферической крови (менее чем на 0,3 x 109/л), которое наблюдалось в течение первых 3-х месяцев лечения, после чего количество лимфоцитов в периферической крови стабилизировалось на достигнутом уровне и сохранялось на этом уровне до окончания лечения.
В клиническом исследовании, у пациентов, получавших лечение терифлуномидом, сохранялись адекватные иммунные реакции на сезонную противогриппозную вакцинацию, что соответствовало поддержанию реакции активной иммунизации. Пациенты в обеих группах приема терифлуномида (7 мг и 14 мг в сутки) после вакцинации достигали серопротективных титров антител: после вакцинации более 90 % пациентов достигли титра антител ≥ 40 к штаммам H1N1 и В. Для штамма H3N2, титры антител ≥ 40 были достигнуты у > 90 % пациентов в группе прима терифлуномида в дозе 7 мг в сутки, и у 77 % пациентов в группе приема терифлуномида в дозе 14 мг в сутки.
В другом рандомизированном, двойном слепом, плацебо-контролируемом фармакодинамическом исследовании, проведенном у здоровых добровольцев, был изучен иммунный ответ на введение инактивированной вакцины против бешенства (неоантигена). По окончании схемы вакцинации геометрические средние титров антител к антирабической вакцине (вакцине против бешенства) в группе терифлуномида были ниже, чем в группе плацебо, достигая поствакцинального лечебного соотношения значений титров антител в группе терифлуномида против группы плацебо [90% ДИ], составляющего 0,53 [0,35, 0,81]. Однако у всех добровольцев титры антирабитических антител после вакцинации были выше 0,5 МЕ/мл (титра, являющегося пороговым для серопротекции). В том же исследовании, у добровольцев, получавших терифлуномид, способность к проявлению кожных реакции гиперчувствительности замедленного типа на повторное введение таких антигенов, как антигены Candida Albicans, Trichophyton или очищенный дериват (производное) белка туберкулина, не отличалась от таковой у добровольцев группы плацебо.
Влияние на интервал QT
В ходе плацебо-контролируемого исследования, проведенного с участием здоровых добровольцев, терифлуномид при средних концентрациях в равновесном состоянии не показал какого-либо потенциала для удлинения интервала QTcF по сравнению с плацебо: самое большое среднее различие между терифлуномидом и плацебо составило 3,45 мс с верхней границей 90%-го доверительного интервала, равной 6,45 мс. При этом ни одно значение QTcF не было ≥ 480 мс, и ни одно изменение длительности этого интервала не было > 60 мс по сравнению с исходным значением.
Влияние на функцию почечных канальцев
В ходе плацебо-контролируемых исследований наблюдалось 20-30 % снижение концентрации мочевой кислоты в сыворотке крови у пациентов, принимавших терифлуномид, по сравнению с группой плацебо. Среднее снижение содержания фосфора в сыворотке составило около 10-15 % в группе терифлуномида по сравнению с группой плацебо. Такие эффекты считаются связанными с увеличением почечной канальцевой экскреции и не связаны с изменениями в функции почечных клубочков.
Клиническая эффективность и безопасность
Эффективность Абаджио была продемонстрирована в ходе исследований EFC6049/TEMSO и TOWER, которые были посвящены оценке ежедневного приема терифлуномида в дозе 7 мг и 14 мг у пациентов с рецидивирующим рассеянным склерозом (РРС).
В целом 1088 пациентов с РРС были рандомизированы в исследование TEMSO для приема в течение 108 недель терифлуномида в дозе 7 мг (n=366) или 14 мг (n=359), или приема плацебо (n= 363). Все пациенты имели установленный диагноз рассеянного склероза (РС) (на основании критериев МакДональда (2001)), рецидивирующее течение с или без прогрессирования; пациенты перенесли, как минимум, 1 рецидив в течение года, предшествующего исследованию или, как минимум, 2 рецидива за 2 года, предшествующих исследованию. При включении в исследование пациенты имели средний балл по Расширенной шкале оценки инвалидизации (EDSS - Expanded Disability Status Scale) составлял ≤ 5,5. Средний возраст изучаемой группы пациентов составлял 37,9 лет. Большинство пациентов имели ремиттирующую форму рассеянного склероза (91,5 %), также были представлены подгруппы пациентов с вторичным прогрессирующим (4,7 %) или прогрессирующе-рецидивирующим рассеянным склерозом (3,9 %). Среднее количество обострений в течение года перед включением в исследование составляло 1,4, при этом исходно у 36,2 % пациентов были очаги, накапливающие контрастное вещество гадолиний. Медиана баллов EDSS у пациентов на момент включения в исследование составляла 2,50: у 249 пациентов (22,9 %) исходный балл EDSS составлял более 3,5. Средняя продолжительность заболевания с момента появления первых симптомов была 8,7 лет. Большинство пациентов (73 %) не принимало препаратов, изменяющих течение рассеянного склероза (ПИТРС) в течение 2-х лет перед включением в исследование. Результаты исследования представлены в таблице 1.
В целом 1169 пациентов с РРС были включены в исследование TOWER для приёма терифлуномида в дозе 7 мг (n=408) или 14 мг (n=372), или приема плацебо (n=389). Длительность лечения составила 48 недель после включения последнего пациента. Все пациенты имели установленный диагноз рассеянного склероза (на основании критериев МакДональда (2001)), рецидивирующее течение с или без прогрессии, и перенесли, как минимум, один рецидив в течение года, предшествующего исследованию, или, как минимум, 2 рецидива за два года перед исследованием. При включении в исследование пациенты имели балл по Расширенной EDSS, составляющий ≤ 5,5.
Средний возраст исследуемой группы пациентов составлял 37,9 лет. Большинство пациентов имели рецидивирующе-ремиттирующий рассеянный склероз (97,5%), но были подгруппы пациентов с вторично-прогрессирующим (0,8 %) или прогрессирующе-рецидивирующим рассеянным склерозом (1,7%). Среднее количество рецидивов в течение года перед включением в исследование составляло 1,4. Медиана баллов EDSS у пациентов на момент включения в исследование составляла 2,50. Средняя продолжительность заболевания с момента появления первых симптомов составляла 8 лет. Большинство пациентов (67,2 %) не принимало препаратов, изменяющих течение заболевания, в течение 2-х лет перед включением в исследование. Результаты исследования представлены в таблице 1.
Таблица 1 -
Главные результаты (для утвержденной дозы, популяция ITT-пациенты, начавшие лечение)
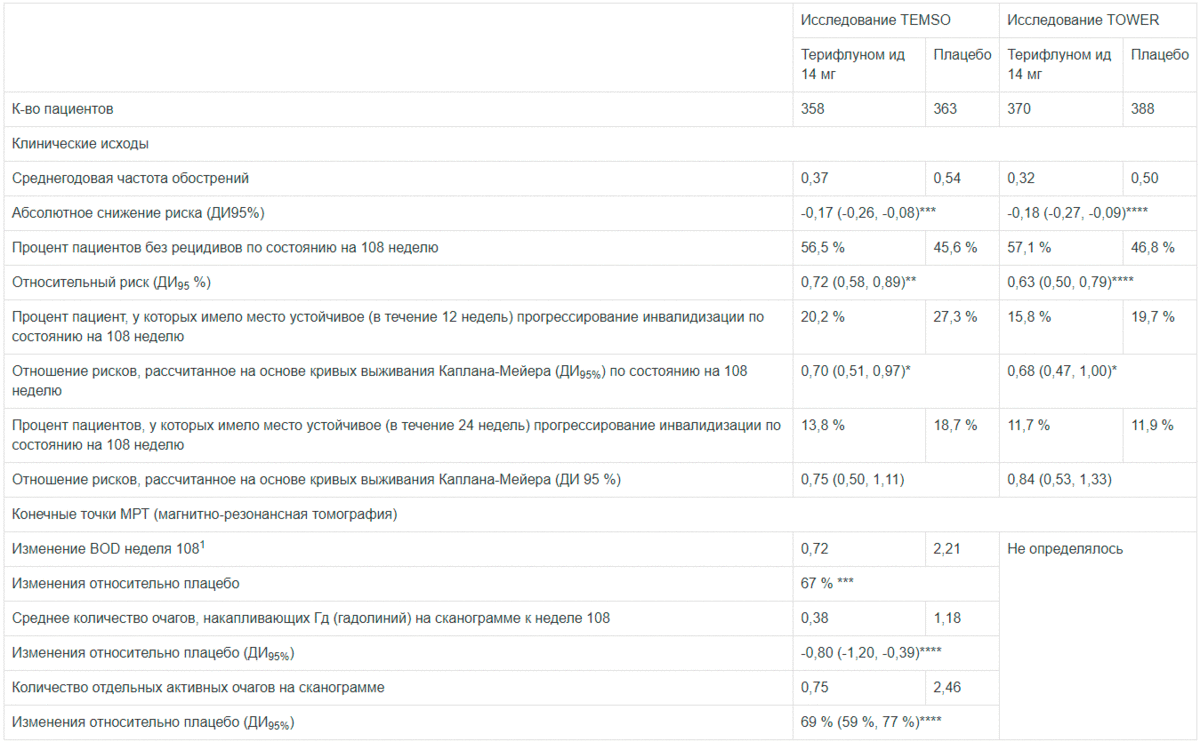
****р<0,0001 ***p<0,001 **p<0,01 *p<0,05 в сравнении с Плацебо . BOD: общий объём очагов в мл (Т2 и гипоинтенсивных Т1)
Эффективность у пациентов с высокой активностью заболевания.
В исследовании TEMSO в подгруппе пациентов с высокой активностью заболевания (n=127) наблюдался устойчивый эффект терапии терифлуномидом в отношении обострений РС и устойчивого (в течение 12 недель) прогрессирования инвалидизации. В соответствии с дизайном исследования высокая активность заболевания определялась при наличии 2 или более рецидивов в течение года c визуализацией одного или более накапливающих гадолиний очагов на МРТ головного мозга. Подобный анализ подгрупп в исследовании TOWER не проводился, так как не было получено данных МРТ.
Отсутствуют данные о пациентах, не отвечающих на полный и адекватный курс лечения (в среднем 1 год терапии) бета-интерфероном, и имеющих как минимум 1 рецидив в течение предыдущего года на фоне терапии, и как минимум 9 Т2-гиперинтенсивных очагов на МРТ головного мозга или, как минимум, 1 очаг, накапливающий гадолиний, или о пациентах, у которых частота возникновения обострений не изменилась или уменьшилась в течение предыдущего года при сравнении с предыдущими 2 годами.
Клиническое исследование TOPIC было двойным слепым, плацебо контролируемым, исследованием, в ходе которого оценивали принимаемые один раз в сутки дозы терифлуномида 7 мг и 14 мг в течение 108 недель пациентам с первым клиническим демиелинизирующим эпизодом (средний возраст 32,1 лет). Основным критерием оценки было время до второго клинического эпизода (рецидива). В общей сложности 618 пациентов были рандомизированы в группы, получающие 7 мг (n=205) или 14 мг (n=216) терифлуномида, или плацебо (n=197). Риск второго клинического обострения на протяжении 2 лет составил 35,9 % в группе плацебо и 24,0 % в группе лечения терифлуномидом в дозе 14 мг (отношение рисков: 0,57, 95% доверительный интервал: 0,38 - 0,87, p=0,0087). Результаты, полученные в ходе клинического исследования TOPIC, подтвердили эффективность терифлуномида при рецидивирующе-ремиттирующем рассеянном склерозе (РРРС) (в том числе при раннем РРРС с первым клиническим демиелинизирующим эпизодом и МРТ-очагами различной давности и локализации).
Эффективность терифлуномида сравнивали с эффективностью подкожного введения интерферона бета-1а (в рекомендованной дозе, составляющей 44 мкг, три раза в неделю) в рамках исследования с участием 324 пациентов (TENERE). Минимальная продолжительность лечения составила 48 недель; максимальная -114 недель. Время до терапевтической неудачи (подтвержденный рецидив или полное прекращение лечения, независимо от того, что произошло в первую очередь) был первичной конечной точкой. Количество пациентов, окончательно прекративших лечение, в группе терифлуномида 14 мг составило 22 из 111 (19,8 %). Причинами были нежелательные явления (10,8 %), недостаточная эффективность (3,6 %), другие причины (4,5 %) и потеря для дальнейшего наблюдения (0,9 %). Количество пациентов, окончательно прекративших лечение, в группе интерферона бета-1а составило 30 из 104 (28,8 %). Причинами были нежелательные явления (21,2 %), недостаточная эффективность (1,9 %), другие причины (4,8 %) и невыполнение условий протокола (1 %). Статистически достоверных отличий по влиянию на первичную конечную точку между терифлуномидом 14 мг/день и п/к интерфером бета-1а 44 мг не было выявлено. Процент пациентов с подтвержденной терапевтической неудачей к 96-ой неделе по методу Каплана-Мейера составил 41,1 % на фоне терифлуномида 14 мг по сравнению с 44,4 % на фоне интерферона бета-1а (p=0,5953).
Клинические данные об эффективности и безопасности применения терифлуномида у детей и подростков в возрасте до 18 лет отсутствуют.
Фармакокинетика
Всасывание
Биодоступность препарата приблизительно 100 %. На фоне курсового перорального приема терифлуномида среднее значение времени достижения максимальных концентраций в плазме крови (Tmax) составляет от 1 до 4 часов.
Пища не оказывает клинически значимого влияния на фармакокинетику терифлуномида.
После приема внутрь 7 мг и 14 мг терифлуномида его системная экспозиция увеличивается пропорционально дозе.
На основании средних прогнозированных фармакокинетических параметров, рассчитанных на основании анализа популяционной фармакокинетики (PopPK) с использованием данных о здоровых добровольцах и пациентах с рассеянным склерозом, при приеме терифлуномида наблюдалось медленное достижение равновесной концентрации (приблизительно 95 % равновесной концентрации достигается через 100 дней (3,5 месяца)), а предполагаемый коэффициент накопления терифлуномида при достижении равновесной концентрации составляет 34 (при оценке по площади под кривой «концентрация-время» (AUC)).
Распределение
Терифлуномид в высокой степени (> 99%) связывается с белками плазмы крови, вероятно, с альбуминами, и, преимущественно распределяется в плазме. Объем распределения после однократного внутривенного введения препарата составляет 11 л.
Биотрансформация
Терифлуномид умеренно метаболизируется и является единственным веществом, которое определяется в плазме крови. Главным путем биотрансформации для незначительного количества метаболитов терифлуномида является гидролиз с окислением в качестве второстепенного пути метаболизма. Второстепенные пути метаболизма включают окисление, N-ацетилирование и конъюгацию с сульфатом.
Выведение
Терифлуномид выделяется через желудочно-кишечный тракт, в основном, с желчью в неизмененном виде и, возможно, путем прямой секреции. В течение 21 дня выводится 60,1 % от принятой дозы препарата, причем через желудочнокишечный тракт (с калом) 37,5 % и через почки (с мочой) 22,6 %. При применении ускоренной процедуры выведения терифлуномида с применением колестирамина, дополнительно выделяется 23,1 % (в основном с калом). После однократного внутривенного введения общий клиренс терифлуномида из организма составляет 30,5 мл/ч.
Терифлуномид медленно выводится из плазмы крови. Без ускоренной процедуры выведения терифлуномида достижение концентрации терифлуномида в плазме крови менее 0,25 мг/л занимает в среднем 6 месяцев, а из-за индивидуальных различий в клиренсе терифлуномида оно может занять до 2-х лет. Ускоренная процедура выведения терифлуномида может быть применена в любое время после прекращения приема препарата Абаджио®.
Выведение может быть ускорено с помощью одной из следующих процедур:
- прием внутрь колестирамина по 8 г каждые 8 часов в течение 11 дней. Если прием колестирамина по 8 г три раза в день плохо переносится, может быть использована схема приема колестирамина по 4 г каждые 8 часов.
- прием внутрь 50 г порошка активированного угля каждые 12 часов в течение 11 дней.
Если какая-либо ускоренная процедура выведения терифлуномида плохо переносится, и если нет необходимости быстрого снижения концентрации терифлуномида в плазме крови, то колестирамин и активированный уголь не обязательно принимать ежедневно.
К концу 11 дней обе схемы лечения успешно ускоряли выведение терифлуномида, приводя к снижению концентрации терифлуномида в плазме крови более чем на 98 %.
Если пациент отвечал на лечение препаратом Абаджио®, применение ускоренной процедуры выведения терифлуномида может привести к возвращению активности заболевания.
Фармакокинетика у особых групп пациентов
Половая принадлежность, пациенты пожилого возраста
На основании результатов популяционного анализа фармакокинетики у здоровых добровольцев и у пациентов с рассеянным склерозом было выявлено, несколько причин внутренней вариабельности фармакокинетических показателей: возраст, масса тела, пол, раса и концентрации альбумина и билирубина в крови. Тем не менее, их влияние остается ограниченным (изменение фармакокинетических показателей ≤ 31 %).
Печеночная недостаточность
Печеночная недостаточность легкой и средней степени не оказывает влияния на фармакокинетику терифлуномида. Поэтому коррекции дозы у пациентов с печеночной недостаточностью легкой и средней степени не предполагается. Фармакокинетика терифлуномида у пациентов с тяжелой печеночной недостаточностью не изучалась (см. раздел «Противопоказания»).
Почечная недостаточность
Тяжелая почечная недостаточность не оказывает влияния на фармакокинетику терифлуномида. Поэтому коррекции дозы у пациентов с тяжелой почечной недостаточностью не требуется.
Показания к применению
Лечение взрослых пациентов с рецидивирующе-ремиттирующим рассеянным склерозом (РРРС).Противопоказания
Гиперчувствительность к действующему веществу или какому-либо из вспомогательных веществ препарата.Тяжелая печеночная недостаточность (класс С по шкале Чайлд-Пью).
Беременность. Перед началом терапии терифлуномидом необходимо исключить беременность.
Женщины с детородным потенциалом, не использующие надежные способы контрацепции во время лечения терифлуномидом; после завершения лечения терифлуномидом женщинам нельзя беременеть до тех пор, пока плазменная концентрация терифлуномида остается выше 0,02 мкг/мл (см. раздел «Применение при беременности и в период грудного вскармливания»).
Период грудного вскармливания.
Тяжелый иммунодефицит, например СПИД.
Тяжелое нарушение костномозгового кроветворения или клинически значимую анемию, лейкопению, нейтропению или тромбоцитопению.
Тяжелая почечная недостаточность, требующая проведения гемодиализа (недостаточность клинического опыта применения).
Тяжелые активные инфекции до момента выздоровления от них.
Тяжелая гипопротеинемия (например, при нефротическом синдроме).
Дефицит лактазы, непереносимость галактозы, глюкозо-галактозная мальабсорбция.
Возраст до 18 лет.
Беременность и период грудного вскармливания
БеременностьАдекватных и строго контролируемых исследований по применению препарата Абаджио® у беременных женщин не проводилось. Однако по данным исследований, проведенных на животных, препарат Абаджио® при его применении у беременных женщин может повышать риск гибели плода и оказывать тератогенное действие. Поэтому применение терифлуномида при беременности противопоказано (см. раздел «Противопоказания»).
На основании данных, полученных на животных, минимальный риск ожидается при концентрации терифлуномида в плазме крови человека менее 0,02 мкг/мл. Если применение препарата Абаджио® должно быть прекращено, рекомендуется проведение ускоренной процедуры выведения терифлуномида (см. раздел «Фармакокинетика», подраздел «Выведение» и раздел «Особые указания»).
Женщинам детородного возраста до начала лечения необходимо оценить возможный серьезный потенциальный риск для плода и использовать эффективные способы контрацепции в период лечения препаратом Абаджио®, а также после прекращения терапии до достижения концентрации препарата в плазме не более 0,02 мкг/мл (обычно этот период составляет 8 месяцев). В случае задержки менструации на фоне приема препарата Абаджио® необходимо срочно информировать об этом врача и выполнить тест на беременность. В случае положительного результата врач должен обсудить с пациенткой все риски, связанные с применением препарата во время беременности, проверить остаточную концентрацию терифлуномида. В случае если концентрация превышает 0,02 мг/л, рекомендуется провести процедуру ускоренного выведения терифлуномида.
Женщинам, принимающим препарат Абаджио® и планирующим беременность, следует рекомендовать проведение процедуры ускоренного выведения терифлуномида для быстрого снижения концентрации терифлуномида в плазме крови. В связи с индивидуальными отклонениями в процессе выведения терифлуномида может потребоваться контроль концентраций терифлуномида в плазме в течение 2-х лет после прекращения терапии. Процедуру ускоренного выведения терифлуномида можно также использовать в любое время после прекращения терапии препаратом Абаджио®.
Применение у мужчин
Риск эмбриофетальной токсичности, связанной с лечением терифлуномидом мужчины, считается низким.
Фертильность
Результаты исследований на животных не продемонстрировали какого-либо влияния терифлуномида на фертильность. Хотя отсутствуют соответствующие данные для человека, воздействие на мужскую и женскую фертильность считается маловероятным.
Период грудного вскармливания
Исследования на животных продемонстрировали, что терифлуномид попадает в грудное молоко. Неизвестно, попадает ли терифлуномид в грудное молоко у женщин.
В связи с тем, что многие лекарственные препараты попадают в грудное молоко, а также в связи с вероятностью развития у грудных детей серьезных нежелательных реакций, связанных с действием препарата Абаджио®, следует принять решение или о прекращении грудного вскармливания, или о прекращении приема препарата, учитывая необходимость его приема для матери.
Способ применения и дозы
Режим дозированияРекомендованная доза препарата Абаджио® составляет 14 мг в день.
Таблетки следует принимать целиком, запивая водой, независимо от приема пищи.
Побочное действие
Краткое описание профиля безопасности (по данным клинических исследований)В общей сложности в клинических исследованиях терифлуномида принимали участие 2267 пациентов (1155 пациентов принимали ежедневную дозу 7 мг, а 1112 пациентов - дозу 14 мг). В четырех плацебо-контролируемых исследованиях (1045 и 1002 пациента в группах 7 мг и 14 мг терифлуномида, соответственно) и одном исследовании с активным препаратом сравнения (по 110 пациентов в каждой группе лечения терифлуномидом) средняя продолжительность применения препарата у пациентов с рецидивирующим рассеянным склерозом (РРС) составила около 672 дней.
Терифлуномид является основным метаболитом лефлуномида. Информация о профиле безопасности лефлуномида у пациентов с ревматоидным или псориатическим артритом может быть применима к терифлуномиду, принимаемому пациентами с рассеянным склерозом.
Анализ объединённых данных плацебо-контролируемых исследований основывался на опыте применения терифлуномида один раз в день 2047 пациентами с рецидивирующими формами рассеянного склероза. У пациентов, получающих терапию терифлуномидом, наиболее часто сообщалось следующих о нежелательных реакциях: головная боль, диарея, повышение активности аланинаминотрансферазы (АЛТ), тошнота и алопеция. Обычно головная боль, диарея, тошнота и алопеция были легкой или умеренной степени тяжести, преходящими и редко приводящими к прекращению лечения.
Ниже приведены нежелательные реакции, развивающиеся при применении препарата Абаджио® в дозе 7 мг и 14 мг и возникавшие с частотой ≥ 1 % и на ≥ 1 % чаще, чем при приеме плацебо, в ходе плацебо-контролируемых исследований. Частоту определяли следующим образом: очень часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); редко (≥ 1/10000, < 1/1000); очень редко (< 1/10000); частота неизвестна (установить частоту по имеющимся данным не представляется возможным).
Инфекции и паразитарные заболевания
Часто: грипп, инфекции верхних дыхательных путей, инфекции мочевыводящих путей, бронхит, синусит, фарингит, цистит, вирусные гастроэнтериты, оральный герпес, инфекции зубов, ларингит, микоз стоп.
Частота неизвестна: Тяжелые инфекции, включая сепсис (постмаркетинговый опыт применения).
Нарушения со стороны крови и лимфатической системы
Часто: нейтропения, анемия.
Нечасто: тромбоцитопения легкой степени тяжести (тромбоциты < 100х109/л).
Нарушения со стороны иммунной системы
Часто: аллергические реакции легкой степени тяжести.
Частота неизвестна: реакции гиперчувствительности (немедленного типа и замедленного типа), включая анафилаксию и ангионевротический отек (отек Квинке) (постмаркетинговый опыт применения).
Нарушения психики
Часто: чувство тревоги.
Нарушения со стороны нервной системы
Очень часто: головная боль.
Часто: парестезия, пояснично-крестцовый радикулит, запястный туннельный синдром.
Нечасто: гиперестезия, невралгия, периферическая нейропатия.
Нарушения со стороны сердца
Часто: ощущение сердцебиения.
Нарушения со стороны сосудов
Часто: артериальная гипертензия (см. раздел «Особые указания»).
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Частота неизвестна: интерстициальные заболевания лёгких (постмаркетинговый опыт применения).
Нарушения со стороны пищеварительной системы
Очень часто: диарея, тошнота.
Часто: боли в эпигастральной области, рвота, зубная боль.
Частота неизвестна: панкреатит, стоматит (афтозный или язвенный) (постмаркетинговый опыт применения).
Нарушения со стороны кожи и подкожных тканей
Очень часто: алопеция.
Часто: сыпь, акне (угревые высыпания).
Частота неизвестна: тяжелые кожные реакции, включая эпидермальный некролиз или синдром Стивенса-Джонсона (постмаркетинговый опыт применения).
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: мышечно-скелетные боли, миалгия, артралгия.
Нарушения со стороны почек и мочевыводящих путей
Часто: поллакиурия (учащенное мочеиспускание).
Нарушения со стороны половых органов и молочной железы
Часто: меноррагия (обильные менструации).
Общие расстройства
Часто: боль.
Лабораторные и инструментальные данные
Очень часто: повышение активности АЛТ (см. раздел «Особые указания»). Часто: повышение активности гамма-глютамилтрансферазы (ГТТ), аспартатаминотрансферазы (АСТ), (см. раздел «Особые указания»), уменьшение массы тела, уменьшение количества нейтрофилов в периферической крови, уменьшение количества лейкоцитов в периферической крови, повышение активности креатининфосфокиназы в крови.
Травмы, интоксикации, осложнения манипуляций
Нечасто: посттравматическая боль.
Описание отдельных нежелательных реакций
Алопеция
Алопеция была описана, как истончение волос, снижение плотности волосяного покрова, потеря волос, связанная или не связанная с изменениями в текстуре волос у 13,9 % пациентов, принимавших терифлуномид в дозе 14 мг по сравнению с 5,1 % пациентов, принимавших плацебо. Большая часть случаев была описана как диффузное или генерализованное поражение всего скальпа (без полной потери волос). В большинстве случаев данная нежелательная реакция отмечалась в течение первых 6 месяцев, с ее спонтанным разрешением у 121 из 139 (87,1 %) пациентов. В группе терифлуномида 1,3 % пациентов прекратили лечение в связи с развитием алопеции по сравнению с 0,1 % в группе плацебо.
Нежелательные реакции со стороны печени (данные из плацебо-контролируемых исследований)
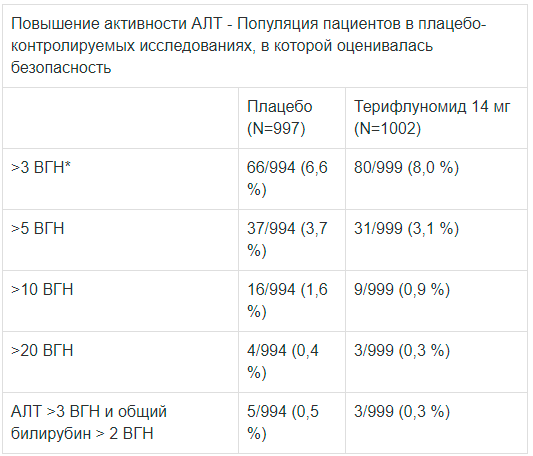
*ВГН - верхняя граница нормы
В группах пациентов, получавших терифлуномид, по сравнению с плацебо чаще наблюдалось увеличение активности АЛТ менее или равное 3 ВГН. Процент пациентов, у которых отмечалось повышение АЛТ выше 3-х ВГН, был сопоставим в обеих группах. Такое повышение активности АЛТ отмечалось в основном в первые шесть месяцев лечения. После прекращения лечения активность фермента АЛТ возвращалась к норме. Время до нормализации активности фермента АЛТ варьировало от нескольких месяцев до нескольких лет.
Влияние на артериальное давление (данные из плацебо-контролируемых исследований)
- Повышение систолического артериального давления выше 140 мм рт. ст. у 19,9 % пациентов, принимавших ежедневно терифлуномид в дозе 14 мг, в сравнении с 15,5 % при приеме плацебо.
- Повышение систолического артериального давления выше 160 мм рт. ст. у 3,8 % пациентов, принимавших ежедневно терифлуномид в дозе 14 мг в сравнении с 2,0 % при приеме плацебо.
- Повышение диастолического артериального давления выше 90 мм рт. ст. у 21,4 % пациентов, принимавших ежедневно терифлуномид в дозе 14 мг, в сравнении с 13,6 % при приеме плацебо.
Инфекции
В плацебо-контролируемых исследованиях в группе терифлуномида 14 мг не наблюдалось увеличения количества случаев тяжелых инфекций (2,7 % против 2 % в группе плацебо). Тяжелые оппортунистические инфекции (инфекции, вызываемые условно-патогенными микроорганизмами) развивались в 0,2 % случаев в каждой из групп.
При постмаркетинговом применении наблюдались тяжелые инфекции, включая сепсис, иногда с летальным исходом.
Гематологические эффекты
В плацебо-контролируемых исследованиях на фоне применения препарата Абаджио® наблюдалось умеренное уменьшение количества лейкоцитов в периферической крови (< 15 % от исходного уровня, в основном уменьшение количества нейтрофилов и лимфоцитов). В то же время у некоторых пациентов отмечалось более выраженное уменьшение количества лейкоцитов. Данная нежелательная реакция возникала в течение первых 6 недель. Затем на фоне продолжающегося лечения количество лейкоцитов в периферической крови стабилизировалось на сниженном уровне (< 15 % уменьшение от исходного уровня). Влияние на снижение количества эритроцитов в периферической крови (< 2 %) и количества тромбоцитов в периферической крови (< 10%) было менее выраженным.
Периферическая нейропатия
Периферическая нейропатия (полинейропатии и мононейропатии (туннельный запястный синдром) развивались чаще в группе пациентов, принимавших терифлюномид 14 мг по сравнению с группой пациентов, принимавших плацебо в плацебо-контролируемых исследованиях. В основных плацебо-контролируемых исследованиях периферическая полинейропатия, подтверждённая исследованиями нервной проводимости, была отмечена у 1,9 % пациентов (17 из 898 пациентов) в группе терифлуномида 14 мг в сравнении с 0,4 % пациентов (4 из 898 пациентов) в группе плацебо. У 5 пациентов с периферической нейропатией, принимавших терифлуномид в дозе 14 мг, было прекращено лечение; у 4 из них сообщалось выздоровлении после прекращения лечения.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы)
В клинических исследованиях на фоне приёма терифлуномида не зафиксировано повышения риска возникновения злокачественных опухолей. Риск возникновения злокачественных опухолей, а именно лимфопролиферативных заболеваний, увеличивается при применении некоторых других лекарственных препаратов, влияющих на иммунную систему (класс-эффект).
Передозировка
СимптомыИнформации по передозировке или отравлении терифлуномидом у человека нет. Здоровые добровольцы принимали терифлуномид в дозе 70 мг ежедневно в течение 14 дней. Наблюдаемые нежелательные реакции соответствовали профилю безопасности терифлуномида при приёме пациентами с рассеянным склерозом.
Лечение
В случае значимой передозировки или отравления для ускоренного выведения терифлуномида рекомендуется прием колестирамина или активированного угля. Рекомендованной процедурой является прием колестирамина в дозе 8 г 3 раза в сутки в течение 11 дней, в случае плохой переносимости этой дозы, можно снизить дозу колестирамина до 4 г 3 раза в сутки. В качестве альтернативного варианта можно принимать по 50 г активированного угля каждые 12 ч на протяжении 11 дней.
Взаимодействие с другими лекарственными средствами и другие формы взаимодействий
Взаимодействия, связанные с воздействием других лекарственных средств на фармакокинетику терифлуномидаГлавный путь биотрансформации терифлуномида - гидролиз; второстепенный путь - окисление, с минимальным участием в нем изоферментов цитохрома системы P450 (CYP) и изоферментов моноаминоксидазы, содержащих флавин. Мощные индукторы изоферментов цитохрома Р450 (CYP): одновременное ежедневное применение рифампицина (индуктора изоферментов CYP2B6, 2C8, 2C9, 2C19, 3A) в дозе 600 мг один раз в сутки в течение 22 дней, а так же прием индуктора эффлюксных переносчиков P-гликопротеина [P-gp] и белка резистентсности к раку молочной железы [BCRP] и терифлуномида (разовая доза, составляющая 70 мг) приводили к снижению системной экспозиции терифлуномида приблизительно на 40 %. Во время лечения терифлуномидом рифампицин и другие известные индукторы CYP и переносчиков белков, такие как карбамазепин, фенобарбитал, фенитоин и Зверобой продырявленный следует назначать с осторожностью.
Колестирамин или активированный уголь
Не рекомендован одновременный прием терифлуномида и колестирамина или активированного угля, поскольку это ведёт к быстрому и существенному уменьшению концентрации терифлуномида в плазме крови, за исключением случаев, когда необходимо ускоренное выведение терифлуномида. Считается, что механизм ускоренного выведения обусловлен прерыванием печеночнокишечной рециркуляции терифлуномида и/или желудочно-кишечным диализом терифлуномида.
Взаимодействия, связанные с влиянием терифлуномида на фармакокинетику других лекарственных средств
Воздействие терифлуномида на субстрат CYP2C8: репаглинид
Было отмечено увеличение среднего значения Cmax и AUC для репаглинида (1,7-и 2,4-кратное, соответственно) после приема повторных доз терифлуномида, что позволяет предположить, что терифлуномид является ингибитором изофермента CYP2C8 in vivo. Поэтому на фоне приема терифлуномида лекарственные средства, метаболизирующиеся с помощью изофермента CYP2C8, такие как репаглинид, паклитаксел, пиоглитазон или розиглитазон, следует применять с осторожностью.
Воздействие терифлуномида на пероральные контрацептивы: 0,03 мг этинилестрадиола и 0,15 мг левоноргестрела
На фоне приема повторных доз терифлуномида было отмечено увеличение средних значений Cmax и AUC0-24 для этинилестрадиола (1,58- и 1,54-кратное, соответственно) и Cmax и AUC0-24 левоногрестрела (1,33- и 1,41-кратное, соответственно). Хотя не ожидается, что взаимодействие с терифлуномидом окажет неблагоприятное воздействие на эффективность пероральных контрацептивов, следует его учитывать при выборе и коррекции доз пероральных контрацептивов при их комбинации с терифлуномидом.
Воздействие терифлуномида на субстрат изофермента CYP1A2 (кофеин)
Прием повторных доз терифлуномида снижал средние значения Cmax и AUC кофеина (субстрата изофермента CYP1A2) на 18 % и 55 %, соответственно, что позволяет предположить, что терифлуномид in vivo является слабым индуктором изофермента CYP1A2. В связи с этим лекарственные препараты, метаболизирующиеся с помощью изофермента CYP1A2 (такие, как дулоксетин, алосетрон, теофиллин и тизанидин), следует применять с осторожностью во время лечения терифлуномидом, поскольку это может привести к снижению эффективности этих препаратов.
Воздействие терифлуномида на варфарин
Прием повторных доз терифлуномида не оказывал влияния на фармакокинетику S-варфарина, что свидетельствует о том, что терифлуномид не является ингибитором или индуктором изофермента CYP2C9. Тем не менее, было отмечено уменьшение на 25 % пикового Международного Нормализованного Отношения (МНО) при одновременном применении терифлуномида и варфарина, по сравнению с монотерапией варфарином. Поэтому при одновременном применении варфарина и терифлуномида рекомендуется тщательное наблюдение за пациентом и мониторинг МНО.
Влияние терифлуномида на субстраты переносчиков органических анионов 3 (ПОА3)
На фоне курсового приема терифлуномида наблюдается увеличение С max и AUC (1,43 и 1,54-кратное, соответственно) цефаклора, что свидетельствует в пользу того, что in vivo терифлуномид является ингибитором ПОА3. Поэтому следует соблюдать осторожность при одновременном применении терифлуномида и субстратов ПОА3, таких как цефаклор, бензилпеницилин, ципрофлоксацин, индометацин, кетопрофен, фуросемид, циметидин, метотрексат и зидовудин.
Влияние терифлуномида на субстраты BCRP и/или транспортирующие органические анионы полипептиды В1 и В3 (ОАТР1В1/В3)
На фоне приема повторных доз терифлуномида наблюдалось увеличение средних значений Cmax и AUC (2,64 и 2,51-кратное, соответственно) розувастатина. Однако не наблюдалось заметного влияния данного увеличения системной экспозиции розувастатина в плазме крови на активность HMG-СоА редуктазы. Рекомендуется 50 % снижение дозы розувастатина при его одновременном приеме с терифлуномидом. Другие субстраты BCRP (такие как метотрексат, топотекан, сульфасалазин, даунорубицин, доксорубицин) и субстраты семейства ОАТР, особенно ингибиторы HMG-CoA редуктазы (такие как симвастатин, аторвастатин, правастатин, метотрексат, натеглинид, репаглинид, рифампицин) одновременно с терифлуномидом следует применять с осторожностью. Пациенты должны находиться под тщательном наблюдением на предмет появления признаков и симптомов повышения системной экспозиции этих лекарственных средств, и, при необходимости, следует рассмотреть вопрос о снижении их доз.
Особые указания
Лечение должно проводиться под наблюдением врача, имеющего опыт лечения пациентов с рассеянным склерозом.Мониторинг
До начала лечения следует провести следующие исследования:
- измерение артериального давления;
- определение активности AЛT;
- общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов в периферической крови.
Во время лечения терифлуномидом следует регулярно контролировать следующие параметры:
- артериальное давление;
- активность АЛТ;
- в случае появления новых симптомов и признаков (например, инфекции) во время лечения необходимо выполнить общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов в периферической крови.
Процедура ускоренного выведения терифлуномида из организма
Терифлуномид медленно выводится из плазмы: концентрации в плазме достигают значений ниже 0,02 мг/л в среднем за 8 месяцев, хотя из-за индивидуальных отклонений в процессе выведения лекарственных веществ выведение может длиться до 2-х лет.
Выведение препарата можно ускорить с помощью ускоренной процедуры выведения терифлуномида, описанной в разделе «Фармакокинетика», подраздел «Выведение», приводящей к снижению более чем на 98 % концентрации терифлуномида в плазме крови.
Пациенты старшей возрастной группы
Препарат Абаджио® необходимо назначать с осторожностью пациентам в возрасте 65 лет и старше в связи с недостаточным количеством данных об эффективности и безопасности терифлуномида в данной возрастной группе.
Почечная недостаточность
У пациентов с почечной недостаточностью легкой, средней или тяжелой степени, не находящихся на гемодиализе, коррекции дозы не требуется.
Пациенты с почечной недостаточностью тяжелой степени, находящиеся на гемодиализе, не принимали участия в клинических исследованиях. Этой группе пациентов противопоказан прием терифлуномида.
Пациенты детского возраста
Безопасность и эффективность Абаджио® у детей и подростков в возрасте до 18 лет не установлена
Печеночная недостаточность
У пациентов с печёночной недостаточностью легкой или средней степени коррекция дозы не требуется.
Терифлуномид противопоказан пациентам с тяжелой печёночной недостаточностью.
У пациентов, принимавших препарат Абаджио®, наблюдалось повышение активности ферментов печени. Повышения активности АЛТ в основном отмечались в течение первых 6 месяцев лечения. В половине случаев показатели вернулись к норме без отмены препарата. В клинических исследованиях применение терифлуномида прекращалось, если повышение активности АЛТ дважды превышало ВГН в 3 раза. Активность трансаминаз в сыворотке крови возвращалась к норме в течение, приблизительно, 2 месяцев после отмены препарата Абаджио®.
Следует контролировать показатели активности трансаминаз и концентрации билирубина в сыворотке крови в течение 6 месяцев до начала лечения препаратом Абаджио®. Активность АЛТ следует определять каждые 2 недели в течение шести месяцев после начала применения препарата Абаджио®. Вопрос о мониторинге показателей функции печени также следует рассматривать, когда препарат Абаджио® применяется одновременно с другими потенциально гепатотоксичными препаратами. Вопрос об отмене препарата Абаджио® следует рассматривать при подтверждении повышения активности трансаминаз в сыворотке крови, более чем в три раза превышающем ВГН. Следует мониторировать активность трансаминаз и концентрацию билирубина в сыворотке крови на фоне терапии препаратом Абаджио®, особенно у пациентов, у которых развиваются такие симптомы, указывающие на нарушение функции печени, как необъяснимая тошнота, рвота, боли в животе, повышенная утомляемость, анорексия, желтуха и/или потемнение мочи. Если подозревается, что повреждение печени вызвано применением препарата Абаджио®, его прием следует прекратить и начать процедуру ускоренного выведения терифлуномида (см. раздел «Фармакокинетика», подраздел «Выведение») с еженедельным контролем показателей функции печени до их нормализации. Если вызванное применением терифлуномида повреждение печени маловероятно, по причине выявления какой-либо другой вероятной причины, может быть рассмотрен вопрос о возобновлении лечения терифлуномидом.
Абаджио® необходимо назначать с осторожностью пациентам, злоупотребляющим алкоголем.
Поскольку терифлуномид в высокой степени связывается с белками крови, в основном с альбуминами, концентрация несвязанного терифлуномида в плазме может повышаться у пациентов с гипопротеинемией, например, при нефротическом синдроме. Терифлуномид не следует назначать пациентам с выраженной гипопротеинемией.
Артериальное давление
На фоне применения терифлуномида может отмечаться повышение артериального давления. Необходимо проконтролировать артериальное давление перед началом лечения терифлуномидом, и периодически впоследствии. В случае повышения артериального давления необходимо проводить соответствующую антигипертензивную терапию до и на фоне лечения терифлуномидом.
Инфекции
У пациентов с тяжелыми активными инфекции начало лечения терифлуномидом необходимо откладывать до полного выздоровления.
В плацебо-контролируемых исследованиях при приёме терифлуномида повышения частоты тяжелых инфекций не наблюдалось. Однако, с учетом иммуномодулирующего эффекта препарата Абаджио®, в случае развития у пациента тяжелой инфекции необходимо рассмотреть необходимость прекращения лечения препаратом, и перед возобновлением терапии необходимо оценить возможные преимущества и риски. В связи с длительным периодом полувыведения препарата необходимо рассмотреть необходимость проведения процедуры ускоренного выведения терифлуномида с помощью колестирамина или активированного угля.
Пациенты, принимающие препарат Абаджио®, должны немедленно сообщать о симптомах инфекций врачу. Пациенты с активными острыми и хроническими инфекциями не должны начинать лечение препаратом Абаджио® до полного излечения. Примем препарата Абаджио® не рекомендуется при тяжелом иммунодефиците, нарушениях со стороны костного мозга или при тяжелых неконтролируемых инфекциях.
Безопасность препарата Абаджио® у пациентов с латентной формой туберкулеза неизвестна. Скрининг на туберкулёз в клинических исследованиях систематически не проводился. Пациентам, имеющим положительный тест на туберкулёз при скрининге, перед началом приёма препарата Абаджио® необходимо пройти соответствующее лечение.
Влияние на органы дыхания
В клинических исследованиях терифлуномида не наблюдалось случаев интерстициальных легочных нарушений. При постмаркетинговом применении препарата Абаджио® наблюдались интерстициальные болезни легких, включая острый интерстициальный пневмонит.
Во время лечения лефлуномидом, активным метаболитом которого является терифлуномид, сообщалось о развитии интерстициальных болезней легких, обострении ранее существовавших интерстициальных болезней легких. Интерстициальные болезни легких могут развиваться остро в любое время в течение лечения и иметь различные клинические проявления.
Интерстициальные болезни легких могут приводить к летальному исходу. Развитие новых или ухудшение существующих легочных симптомов, таких как кашель и одышка, сочетающихся с лихорадкой или без лихорадки, может быть причиной для прекращения терапии и для дальнейшего соответствующего обследования пациента. В случае необходимости отмены препарата следует рассмотреть вопрос о начале процедуры ускоренного выведения терифлуномида (см. раздел «Фармакокинетика», подраздел «Выведение»).
Гематологические эффекты
В плацебо-контролируемых исследованиях наблюдалось уменьшение среднего количества лейкоцитов в крови приблизительно на 15 % от исходного уровня (главным образом, нейтрофильных лейкоцитов и лимфоцитов) и количества тромбоцитов приблизительно на 10 %. Перед началом терапии препаратом Абаджио® и во время лечения необходимо проводить клинический анализ крови с определением лейкоцитарной формулы и количества тромбоцитов в периферической крови. На фоне терапии Абаджио необходимо проводить дополнительный мониторинг при появлении клинических симптомов и признаков, указывающих на наличие инфекции.
У пациентов с существующей анемией, лейкопенией и/или тромбоцитопенией, а также у пациентов с нарушениями костномозгового кроветворения или имеющих высокий риск подавления костномозгового кроветворения, имеется повышенный риск развития гематологических нарушений при применении препарата Абаджио®. В случае развития указанных нежелательных реакций для уменьшения концентрации терифлуномида в плазме крови необходимо рассмотреть вопрос о применении процедуры ускоренного выведения терифлуномида.
В случаях выраженных гематологических реакций, включая панцитопению, применение препарата Абаджио® и любого другого подавляющего костномозговое кроветворение препарата должен быть прекращён, и следует рассмотреть вопрос о проведении процедуры ускоренного выведения терифлуномида.
Кожные реакции
В ходе клинических исследований терифлуномида не было выявлено ни одного случая развития тяжелых кожных реакций. Такие случаи, включая развитие синдрома Стивенса-Джонсона и токсического эпидермального некролиза, редко наблюдались при постмаркетинговом применении препарата.
У пациентов, получавших лефлуномид, исходное соединение, главным метаболитом которого является терифлуномид, также сообщалось об очень редких случаях развития лекарственной реакции с эозинофилией и системными симптомами (DRESS).
В случае появления язвенного стоматита приём терифлуномида следует прекратить. Если возникает подозрение, что наблюдаемые со стороны кожи и/или слизистых оболочек реакции принимают характер тяжелых генерализованных кожных реакций (синдрома Стивенса-Джонсона или токсического эпидермального некролиза - синдрома Лайелла), приём терифлуномида и любых других препаратов, потенциально вызывающих подобные реакции, необходимо прекратить и следует немедленно начать процедуру ускоренного выведения терифлуномида. В таких случаях пациенты не должны возобновлять лечение терифлуномидом (см раздел «Противопоказания»).
Периферическая нейропатия
У пациентов, принимавших препарат Абаджио®, наблюдались случаи периферической нейропатии. После прекращения приёма препарата состояние большинства пациентов улучшалось. Тем не менее, отмечалась значительная вариабельность исхода периферической нейропатии, т.е. у некоторых пациентов нейропатия разрешилась, а у части пациентов интенсивность симптомов не менялась. Если у пациента, принимавшего препарат Абаджио®, диагностирована периферическая нейропатия, следует рассмотреть вопрос о прекращении приёма препарата Абаджио® и проведение процедуры ускоренного выведения терифлуномида.
Вакцинация
Два клинических исследования показали, что вакцинации инактивированным неоантигеном (первая вакцинация) или повторным антигеном (ревакцинация) или сенсибилизирующим антигеном (стимуляция) были безопасными и эффективными во время лечения препаратом Абаджио®. Применение живых ослабленных вакцин может быть связано с риском инфицирования и поэтому его следует избегать.
Иммуносупрессивная и иммуномодулирующая терапия
Поскольку лефлуномид является исходным соединением для терифлуномида, одновременный приём терифлуномида с лефлуномидом не рекомендован.
Одновременное применение терифлуномида с антинеопластическими или иммуносупрессивными препаратами, используемыми для лечения рассеянного склероза, не изучался. Исследования по безопасности, в которых терифлуномид принимался одновременно с интерфероном бета или с глатирамера ацетатом на протяжении до одного года, не выявили проблем с безопасностью. Безопасность этой комбинации при длительном приёме для лечения рассеянного склероза не изучалась.
Применение у женщин детородного возраста/беременных женщин
Данные, полученные в ходе исследований, проведенных у животных, свидетельствую об имеющемся риске для плода. Женщины детородного возраста должны использовать эффективные способы контрацепции для предотвращения наступления беременности во время приема препарата Абаджио®. Если терапия препаратом Абаджио® прекращается, женщины должны продолжать контрацепцию до подтвержденного снижения концентрации терифлуномида в плазме крови до 0,02 мкг/мл или ниже. Женщинам, которые планируют беременность или беременны, следует рекомендовать провести процедуру ускоренного выведения терифлуномида для быстрого уменьшения концентрации терифлуномида в плазме крови. Без процедуры ускоренного выведения терифлуномида, время достижения концентрации препарата в плазме крови меньшей или равной 0,02 мкг/мл в среднем составляет 8 месяцев; однако из-за индивидуальных различий в процессе выведения терифлуномида, этот период может длиться до 2-х лет. Процедура ускоренного выведения терифлуномида может применяться в любое время после прекращения терапии препаратом Абаджио® (см. раздел «Фармакокинетика», подраздел «Выведение»).
Переход на или с препарата Абаджио®
На основании клинических данных, относящихся к одновременному применению терифлуномида с интерфероном бета или с глатирамера ацетатом, можно сказать, что нет никакой необходимости в периоде ожидания при начале терапии терифлуномидом после интерферона бета или глатирамера ацетата, или при начале терапии интерфероном бета или глатирамера ацетатом после терапии терифлуномидом.
В связи с длительным периодом полувыведения натализумаба одновременная системная экспозиция, и, следовательно, одновременное воздействие на иммунную систему может произойти в случае начала терапии препаратом Абаджио® в течение 2-3-х месяцев после прекращения приёма натализумаба. Поэтому следует соблюдать меры предосторожности при переходе с терапии натализумабом на Абаджио®.
С учетом периода полувыведения финголимода необходим 6-недельный интервал без терапии для элиминации из организма циркулирующих веществ. От 1 до 2-х месяцев необходимо для возвращения количества лимфоцитов к норме после прекращения применения финголимода. Начало лечения препаратом Абаджио® в течение этого временного интервала может привести к одновременной системной экспозиции финголимода и терифлуномида. Это может иметь следствием аддитивное воздействие на иммунную систему. Поэтому следует соблюдать меры предосторожности при переходе с терапии финголимодом на терапию препаратом Абаджио®.
У пациентов с рассеянным склерозом медиана периода полувыведения из организма (t1/2z ) была приблизительно 19 дней на фоне приема повторных доз препарата в дозе 14 мг. Если принято решение о прекращении лечения препаратом Абаджио® в течение в 5 периодов полувыведения (приблизительно 3,5 месяца, хотя у некоторых пациентов может быть и дольше) начало другой терапии приведёт к одновременной системной экспозиции с препаратом Абаджио®. Это может привести к аддитивному воздействию на иммунную систему, что требует обязательного соблюдения мер предосторожности.
Лактоза
Поскольку таблетки препарата Абаджио® содержат лактозу, пациентам с непереносимостью галактозы, дефицитом лактазы или глюкозо-галактозной мальабсорбцией не следует принимать этот лекарственный препарат.
Влияние на способность управлять транспортными средствами и пользоваться механизмами
Препарат Абаджио® не оказывает или оказывает незначительное влияние на способность управлять автомобилем или пользоваться механизмами. Однако при возникновении нежелательных явлений со стороны нервной системы, например головокружения, следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности.Форма выпуска
Таблетки, покрытые пленочной оболочкой, 14 мг.При упаковке «Санофи Винтроп Индустрия», Франция
По 14 таблеток в блистер из фольги алюминиевой. По 2 блистера, запечатанных в картонный «карман», помещают в упаковку типа «рукав». По 1 или 3 упаковки типа «рукав» вместе с инструкцией по применению помещают в пачку картонную. На каждую открывающуюся сторону пачки картонной наклеивают антиконтрафактный стикер (контроль вскрытия).
При упаковке АО «ОРТАТ», Россия или АО «Р-Фарм», Россия По 2 блистера из фольги алюминиевой с инструкцией по применению помещают в пачку картонную. На каждую открывающуюся сторону пачки картонной наклеивают стикер контроля вскрытия.
Условия хранения
Хранить при температуре от 2до 30°С.Хранить в недоступном для детей месте.
Срок годности
3 года.Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту.Юридическое лицо, на имя которого выдано регистрационное удостоверение:
Джензайм Европа Б.В., Нидерланды
(Указывается только при упаковке Санофи Винтроп Индустрия, Франция):
Производитель
Санофи Винтроп Индустрия, Франция56 route de Choisy au Bac, 60205 Compiegne, France.
Претензии потребителей направлять по адресу в России:
АО «Санофи Россия», Россия
125009, г. Москва, ул. Тверская, д. 22.
Или (указывается только при упаковке АО «ОРТАТ», Россия):
Производитель/фасовщик (первичная упаковка):
Санофи Винтроп Индустрия, Франция.
56 route de Choisy au Bac, 60205 Compiegne, France.
Упаковщик (вторичная/потребительская упаковка/Выпускающий контроль качества)
АО «ОРТАТ», Россия.
157092, Костромская обл., Сусаниниский р-н, с. Северное, мкр-н Харитоново.
Претензии потребителей направлять по адресу в России:
АО «ОРТАТ», Россия.
157092, Костромская обл., Сусаниниский р-н, с. Северное, мкр-н Харитоново.
Производитель/фасовщик (первичная упаковка):
Санофи Винтроп Индустрия, Франция56 route de Choisy au Bac, 60205 Compiegne, France.
Упаковщик (вторичная/потребительская упаковка/Выпускающий контроль качества)
АО «Р-Фарм», Россия.150061, г. Ярославль, ул. Громова, д.15.
Претензии потребителей направлять по адресу в России:
АО «Р-Фарм», Россия
150061, г. Ярославль, ул. Громова, д.15.
Комментарии
ПРАКТИКА ПЕДИАТРА
