Исследование раздельных и сочетанных эффектов Aктовегина, Инфезола и Мексидола при моделировании нарушений углеводного и липидного обмена в эксперименте
СтатьиНа правах рукописи
Артюкова Марина Михайловна
14.00.25 - фармакология, клиническая фармакология
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
Старая Купавна - 2007
Работа выполнена на кафедре поликлинической терапии и функциональной диагностики с курсом эндокринологии ГОУВПО "Мордовский государственный университет имени Н.П. Огарева"
Научный руководитель:
доктор медицинских наук, профессор А.В. Зорькина
Официальные оппоненты:
доктор медицинских наук, профессор В.Л.Ковалева
доктор биологических наук профессор В.П.Балашов
Ведущая организация: Федеральное государственное образовательное учреждение высшего профессионального образования "Российский государственный медицинский университет"
Ученый секретарь диссертационного совета, доктор биологических наук, профессор Л.В.Корольченко
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы.
Несмотря на достигнутые успехи клинической медицины, метаболический синдром, включающий дислипидемию, сахарный диабет, ожирение и артериальную гипертонию, представляет собой одну из актуальнейших проблем общественного здравоохранения (Чазова И.Е., Мычка В.Б., 2004; Кобалова Ж.Д., Толкачева В.В., 2005; Клебанова Е.М., Балаболкин М.И., 2006; Haffher S.M., 2000) и значительно повышает риск развития фатальных сердечнососудистых осложнений (Смирнова Е.Н, 2000; Титов В.Н., 2001; Палферова Е.А., 2005; Laasko M., Lehto S., 1997).
Большой интерес клиницистов в последнее время привлекает проблема патогенеза и лечения неалкогольного стеатогепатоза печени (Мансуров Х.Х. с соавт., 2005, Подымова С.Д., 2006; Буеверов А., 2006; Crespo J. et al., 2001; Angulo P., 2002), который диагностируется при метаболическом синдроме (Корнеева О.Н с соавт., 2005; Кобалова Ж.Д, Толкачева В.В., 2005; Буеверов А., 2006). При этом поражение печени является и следствием и одной из существенных причин дальнейшего усугубления нарушения обмена веществ (Подымова С.Д., 1993; Артюнов А.Г. с соавт., 2005; Ройтберг Г.Е. с соавт., 2005).
Учитывая существенный вклад в патогенез метаболического синдрома оксидативного стресса (Балаболкин М.И. с соавт., 2004; Аметов А.С. с соавт., 2005; Суслова Т.Е. с соавт., 2005; Руяткина Л.А. с соавт., 2005; Memisogullari R. et al., 2003; Schrauwen P. et al., 2006), выступающего одним из наиболее значимых факторов поражения печени (Ройтберг Г.Е. с соавт., 2005; Poli G. 2000; G. Robertson et al., 2001), представляется целесообразным применение лекарственных препаратов антиоксидантного действия уже на ранних этапах формирования метаболического синдрома.
Одним из перспективных лекарственных средств является триоксипиридина сукцинат, проявляющий липидснижающее и антиоксидантное действие при сахарным диабете (Клебанова Е.М. с соавт., 2006). В то же время недостаточно изученным остается влияние на метаболические процессы в условиях их нарушения препаратов, действующих преимущественно на белковый обмен.
Работа является разделом комплексной программы исследований Мордовского государственного университета им. Н.П. Огарёва "Фармакологическая коррекция повреждений, возникающих при гипоксических, токсических и радиационных воздействиях". Номер государственной регистрации темы 01200004103.
Целью работы явилось исследование влияния мексидола, актовегина, инфезола и их комбинированного применения на некоторые биохимические показатели и структуру печени при моделировании нарушений липидного и углеводного обмена в эксперименте.
В ходе исследования решались следующие задачи:
1. Изучить влияние актовегина, инфезола и мексидола на некоторые показатели обмена веществ и структуру печени при моделировании дислипидемии и гипергликемии в эксперименте.
2. Исследовать гепатопротекторное действие комбинированного применения мексидола и актовегина в условиях моделирования дислипидемии и гипергликемии.
2. Изучить влияние комбинированного применения мексидола и инфезола на некоторые биохимические показатели и структуру печени в условиях моделирования сочетанных метаболических нарушений.
Научная новизна:
Впервые показано, что в условиях моделирования нарушений углеводного и липидного обмена актовегин оказывает гиполипидемическое, дезинтоксикационное, антиоксидантное и гепатопротекторное действие.
Отмечено, что комбинированное применение актовегина и мексидола повышает гепатопротекторный эффект мексидола, потенцирует его липидкорригирующее и дезинтоксикационное действие в условиях моделирования нарушений липидного и углеводного обмена, а также потенцирует гипогликемический эффект мексидола при аллоксановом диабете.
Показано, что инфезол в условиях аллоксанового диабета и аллоксан-холестериновой дислипидемии оказывает гипогликемический, гиполипидемический, дезинтоксикационный эффект, ограничивает показатели цитолитического синдрома.
Впервые продемонстрировано, что комбинация инфезола и мексидола при аллоксановой гипергликемии уменьшает гепатопротекторное действие мексидола и в большей степени, чем монотерапия оксипиридина сукцинатом, угнетает холестеринсинтетическую функцию печени, снижает содержание триглицеридов и β-липопротеидов, ограничивает цитолитический синдром, но снижает антиоксидантный и дезинтоксикационный эффект мексидола.
Отмечено, что комбинированное применение мексидола и инфезола в условиях аллоксан-холестериновой дислипидемии снижает гепатопротекторный и антиоксидантный эффект мексидола, моделирует его липидрегулирующее и повышает дезинтоксикационное действие, в отличие от монотерапии мексидолом стимулирует альбуминсинтетическую функцию печени и предупреждает развитие гиперкалиемии.
Практическая ценность:
Полученные результаты открывают перспективу использования актовегина и инфезола в комплексной коррекции метаболического синдрома, обосновывают целесообразность комбинированного использования актовегина и мексидола при нарушениях липидного и углеводного обмена в клинике и являются экспериментальным обоснованием целесообразности дальнейшего изучения эффектов инфезола при метаболических нарушениях в эксперименте.
Основные положения, выносимые на защиту:
1. Актовегин оказывает гиполипидемическое, цитопротекторное, дезинтоксикационное, антиоксидантное и гепатопротекторное действие при моделировании нарушений липидного и углеводного обмена в эксперименте.
2. Инфезол оказывает гипогликемическое, гиполипидемическое, цитопротекторное, дезинтоксикационное действие при моделировании метаболических нарушений в эксперименте.
3. Комбинированное применение актовегина и мексидола повышает гепатопротекторный и липидкорригирующий эффект мексидола при моделировании нарушений липидного и углеводного обмена в эксперименте, а также потенцирует гипогликемический эффект мексидола при аллоксановом диабете и дезинтоксикационный при аллоксановой гипергилкемии и аллоксан-холестериновой гипергликемии.
4. Комбинированное применение инфезола и мексидола при моделировании нарушений углеводного обмена и сочетанных метаболических нарушений уменьшает гепатопротекторный эффект мексидола, угнетает холестерин-синтетическую функцию печени при аллоксановом диабете и повышает содержание холестерина липопротеидов высокой плотности при сочетанных метаболических нарушениях.
Апробация работы. Материалы работы были представлены на XII межрегиональной научно-практической конференции ГОУДПО "Пензенский институт усовершенствования врачей" - "Актуальные вопросы диагностики, лечения и реабилитации больных" (Пенза, 2006); XIV Российском национальном конгрессе "Человек и лекарство" (Москва, 2007); XII научной конференции молодых ученых аспирантов и студентов медицинского факультета ГОУВПО "Мордовский государственный университет имени Н.П.Огарева" - "Медицинские проблемы жизнедеятельности организма в норме, патологии и эксперименте" (Саранск, 2007); научно-практической конференции Санкт-Петербургской государственной медицинской академии им.И.И.Мечникова "Современная кардиология: наука и практика" (Санкт-Петербург, 2007).
Публикации. Основные положения диссертационного исследования представлены в 7 печатных работах, в том числе 1 в журнале, рекомендуемом ВАК.
Структура и объём диссертации. Диссертация изложена на 144 страницах компьютерного набора, состоит из введения, главы материалы и методы, четырех глав результатов собственных исследований, заключения, выводов, практических рекомендаций, списка использованной литературы, включающего 146 отечественных и 32 иностранных источника, иллюстрирована 24 таблицами, 28 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Актовегин - высокоочищенный гемодиализат из крови телят, состоит из аминокислот, олигопептидов, нуклеозидов, промежуточных продуктов углеводного и жирового обмена, микроэлементов (натрия, кальция, фосфора, цинка, магния) (Сыч Ю., Зилов А., 2005). Препарат улучшает утилизацию глюкозы и кислорода, активирует процессы аэробного окисления, повышает энергетический потенциал клетки (Румянцева С.А. с соавт., 2004). Показана эффективность актовегина в комплексном лечении инфаркта миокарда (Креминская В.,М., Гурьева И.В., 2004; Бояринова Г.А. с соавт., 2005), в лечении и профилактике диабетической энцефалопатии и полинейропатии (Аметов А.С. с соавт., 2004; Моргоева Ф.Э. с соавт., 2005; Сыч Ю., Зилов А., 2005). В работе использовался в виде раствора для инъекций 10%-2мл производства Hafslund Nycomed Pharma.
Инфезол-40 - препарат для парентерального питания. В состав входит на 1 л раствора для инфузий L-валин 2,25 г, L-изолейцин 2,1г, L-лейцин -2,74 г, L-лизин - 2г, L-метионин 1,75 г, L-треонин - 1,6 г, L-триптофан - 500мг, L-аланин- 4г, L-аргинин-4,55г, L-аспарагиновая кислота - 2г, глицин - 7г, L-гисти-дин-1,35г, L-глутаминовая кислота-5г, сорбит- 50г. А также натрий, калий, магний. Препарат способствует превращению аммиака в мочевину, связывает токсичные ионы аммония, которые образуются при катаболизме белков в печени. Производство Берлин-Хеми /Менарини Фарма Гмбх, выпуск флаконы по 100мл
Мексидол - (2-этил-6-метил-3-гидроксипиридина сукцинат) - синтетический водорастворимый антиоксидант из группы 3-оксипиридинов (Смирнов Л.Д. с соавт., 1992), оказывает ингибирующее влияние на ферментативное и неферментативное перекисное окисление липидов (Базанов Т.А., 1995), проявляет мембранопротекторное, антиангинальное, кардиопротекторное, дезагрегантное (Воронина Т.А. с соавт., 1992, 1993; Зорькина А.В., 1997; Галенко-Ярошевский, В.П. с соавт., 2005), антиаритмическое (Галенко-Ярошевский, П.А. с соавт., 1998), нейротропное (Воронина Т.А. с соавт., 1997; 2006), противоишемическое и липидрегулирующее свойство, а также способность оказывать нормализующее действие на углеводный и энергетический обмен (Смирнов Л.Д. с соавт., 2001), поддерживает активность аэробного гликолиза при гипоксии (Лукьянова Л.Д., 1990). В работе использовался мексидол 5% раствор в ампулах (100мг) производства ООО МЦ "Эллара".
Экспериментальные исследования проводились на 176 нелинейных белых крысах обоего пола массой 200-300 гр. Крыс выращивали в стандартных условиях вивария. В ходе эксперимента метаболические нарушения воспроизводились с использованием трех экспериментальных моделей.
Модель 1. Аллоксановая гипергликемия: подопытным животным после 24 часового лишения пищи (при сохраненном доступе к воде) внутрибрюшинно однократно вводили раствор аллоксана в дозе 135 мг/кг (И.В. Мадянов, 1997; И.А. Волчегорский, 1997). Гипергликемия развивалась к 10 суткам.
Модель 2. Холестериновая дислипидемия: ежедневно в течение 20 суток, экспериментальным животным вводили масляный раствор холестерина в дозе 40 мг/кг/сут per os (Jowsufzai S.Y.K. et al., 1976). Дислипидемия развивалась к 10 суткам. Модель 3. Аллоксан-холестериновая дислипидемия: после 24-часового лишения пищи (при сохраненном доступе к воде) внутрибрюшинно однократно вводили раствор аллоксана в дозе 135 мг/кг, затем ежедневно в течение 20 сут, вводили масляный раствор холестерина в дозе 40 мг/кг/сут per os (Артемьева О.В., 2002).
Поставлено 17 экспериментальных серий (табл.1). Исследуемые препараты вводили с 11 по 20 сутки эксперимента: мексидол и актовегин внутримышечно, инфезол внутрибрюшинно. Дозы преператов рассчитывались, исходя из средне-терапевтических с учетом межвидового переноса доз (Freireich E.J., Lehan E., Rail D. Et al, 1966).
Забой животных осуществляли на 21 сутки путем декапитации после введения тиопентала натрия в дозе 40 мг/кг внутрибрюшинно.
По окончании эксперимента оценивали в плазме крови содержание глюкозы - глюкозооксидазным методом; уровень общего холестерина (ОХ) и триглицеридов (ТГ) - энзиматическим колориметрическим методом, холестерин липопротеидов высокой плотности (ХсЛПВП) - с использованием набора реагентов "HDL-CHOLESTEROL "FL-E"; концентрацию мочевины - уреазным/фенол-гипохлоритным методом; концентрацию креатинина - по реакции Яффе с депротеинизацией; активность аспарагиновой (АСТ) и аланиновой (АЛТ) аминотрансфераз - методом Райтмана-Френкеля; содержание электролитов в сыворотке крови - калия(К) и натрия (№) по стандартной методике, прилагаемой к наборам на автоматическом анализаторе К/N "Ионометр ЭЦ-59". Индекс атерогенности [ИА=(ОХ - ХсЛПВП)/ХсЛПВП (усл. ед.)] рассчитывали по формуле А.Н. Климова (1977). Рассчитывали содержание холестерина липопротеидов очень низкой плотности (ХсЛПОНП=ТГ/2,2), холестерина липопротеидов низкой плотности (ХсЛПНП=ОХ-ХсЛПВП-ХсЛПОНП).
Таблица 1. Структура экспериментального исследования.
| N серии | Исследуемые препараты | n | |
| 1. Интактные | - | 7 | |
| Модель 1 | 2. Контроль | - | 12 |
| 3. | Мексидол 25 мг/кг в/м | 13 | |
| 4. | Актовегин 40 мг/кг в/м | 10 | |
| 5. | Мексидол 25 мг/кг в/м + Актовегин 40 мг/кг в/м | 12 | |
| 6. | Инфезол-40 2 мл в/б | 12 | |
| 7. | Инфезол-40 2 мл в/б+ Мексидол 25 мг/кг в/м | 12 | |
| Модель 2 | 8.Контроль | - | 12 |
| 9. | Мексидол 25 мг/кг в/м | 12 | |
| 10. | Актовегин 40 мг/кг в/м | 10 | |
| 11. | Мексидол 25 мг/кг в/м + Актовегин 40 мг/кг в/м | 10 | |
| Модель 3 | 12.Контроль | - | 10 |
| 13. | Мексидол 25 мг/кг в/м | 10 | |
| 14. | Актовегин 40 мг/кг в/м | 8 | |
| 15. | Мексидол 25 мг/кг в/м + Актовегин 40 мг/кг в/м | 8 | |
| 16. | Инфезол-40 в/б 2мл | 8 | |
| 17. | Инфезол-40 в/б 2 мл + Мексидол 25 мг/кг в/м | 10 |
Для оценки альбуминсинтетической функции печени и степени эндотоксикоза определяли общую концентрацию альбуминов (ОКА), эффективную концентрацию альбуминов (ЭКА) с использованием набора реактивов "ЗОНД-Альбумин" на анализаторе АКЛ-01 "Зонд". Рассчитывали резерв связывания альбумина [РСА=ЭКА/ОКА)] и индекс токсичности плазмы [ИТ=ОКА/ЭКА-1] (Грызунов Ю.А., Добрецов Г.Е., 1994).
В гомогенатах печени определяли активность каталазы (Королюк М.А., 1988), уровень малонового диальдегида при спонтанном (МДА) и железоиндуцированном окислении (FеМДА) (Конюхова С.Г., 1989). Резерв липидов для перекисного окисления липидов рассчитывали по формуле [РЛПО=(FеМДА-МДА)/МДА] (Кузьменко Д.И., Лаптев Б.И., 1999).
Гистологические изменения оценивали методом световой микроскопии. Материал фиксировали в 10% растворе нейтрального формалина и заключали в парафин. Срезы окрашивали гематоксилином и эозином.
Результаты экспериментов обрабатывали методами вариационной статистики на персональном компьютере с использованием программы Exel путем расчёта средних арифметических (М) и ошибок средних (±m). Достоверность различий (р) между сравниваемыми вариационными рядами оценивали с помощью t-критерия Стьюдента.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Моделирование аллоксановой гипергликемии приводило к росту содержания глюкозы в два раза, ОХ - на 76%, ТГ - на 141%, β-ЛП - на 65% и ХсЛПНП на 73%, росту ИА и ХсЛПОНП в 2 раза относительно данных интактной группы. О развитии цитолитического синдрома свидетельствовал рост активности АЛТ на 75%, АСТ - на 62%. Наблюдалось нарушение альбуминсинтетической функции печени. Снижение дезинтоксикационной функции печени проявилось в росте индекса токсичности плазмы крови в 12 раз, уровня креатинина - на 30%, мочевины - на 39% и развитии гиперкалиемии. Моделирование окислительного стресса подтверждалось увеличением в гомогенатах печени содержания МДА на 267% и FеМДА - на 61%. АОА и РЛПО снижались на 26% и 80%, компенсаторно возрастала активности каталазы на 59%.
При моделировании холестериновой дислипидемии у подопытных животных также увеличивалось содержание ОХ на 79%, ТГ - на 39%, ХсЛПОНП -на 41%. В 2 раза повышалось количество β-ЛП, в 2,5 раза - уровень ХсЛПНП, при этом ИА возрос на 114%. Повышалась активность маркеров цитолитического синдрома: АЛТ - на 63%, АСТ - на 32%. Индекс токсичности увеличился в 2 раза. Отмечалось повышение уровня креатинина на 39%. При этом в печени содержание МДА увеличилась на 261%, FеМДА - на 48%. АОА снижалась на 41%, РПОЛ - на 81%, активности каталазы возрастала на 114%.
На фоне аллоксан-холестериновой дислипидемии наблюдался рост ТГ на 135%, ХсЛПОНП, ОХС- на 51%, β-ЛП - на 82% и ХсЛПНП -на 57%. При сравнении с предыдущими моделями регистрировалась более выраженная гипергликемия, более низкое содержание Хс ЛПВП (на 26%) и повышение индекса атерогенности на 151%. Активность АЛТ возросла на 55%, АСТ - на 37%. Содержание общей и эффективной концентрации альбуминов снижалось на 40% и 13% соответственно. Резерв связывания альбуминов уменьшался на 32%, а индекс токсичности вырос почти в 6 раз. Отмечалось повышение уровня мочевины на 28%. В печени наблюдалось нарастание МДА более чем в 2 раза, активация каталазы на 50%, снижение: АОА на 26%, РЛПО - на 67% (р<0,001).
По сравнению с интактными животными при моделировании метаболических нарушений наблюдалось повреждение дольковой и балочной структуры печени за счет очагов некроза гепатоцитов.
Производное 3-оксипиридина мексидол проявил гепатопротекторное действие в условиях всех трех использованных в данном исследовании моделей метаболических нарушений, ограничивая грубые изменения гепатоцитов: предотвращалось нарушение балочной структуры печени (особенно на модели №1), не наблюдалось кариопикноза, снижался ядерный полиморфизм, уменьшалось количество некротизированных гепатоцитов.
Одним из механизмов реализации гепатопротекторного эффекта мексидола явилось антиоксидантное действие препарата: в условиях аллоксановой гипергликемии в ткани печени содержание МДА снижалось на 70% (р<0,001), FеМДА - на 36% (р<0,001) по сравнению с контрольной группой. В условиях холестериновой дислипидемии уровень МДА в ткани печени снижался на 61% (р<0,005), Fe-МДА - на 41% (р<0,001). На модели сочетанных метаболических нарушений (№3) МДА снижался на 36% (р<0,005). Кроме того, на фоне введения мексидола при моделировании аллоксановой гипергликемии улучшалась альбуминсинтетическая функция печени: рост общей концентрации альбуминов составил 62% (р<0,05). Уменьшение выраженности эндотоксикоза при введении мексидола проявилось на фоне аллоксановой гипергликемии в росте эффективной концентрации альбуминов на 218% (р<0,005), резерва связанного альбумина - на 99% (р<0,05), снижении индекса токсичности на 91% (р<0,001) и уровня креатинина - на 17% (р<0,05). На фоне моделирования аллоксан-холестериновой дислипидемии отмечалось снижение индекса токсичности на 48% (р<0,05). При этом, отмечалось увеличение калия в плазме крови в условиях моделирования холестериновой дислипидемии и аллоксан-холестериновой дислипидемии на 26% и 23% (р<0,05).
Нарушение липидного обмена играют значимую роль в патогенезе сахарного диабета (Козлов С.Г., Лякишев А.А., 2002; Соколик В.В. с соавт., 2005; Steiner G., 1999; MrEneny J. et al. 2000; Memisogullari R. et al., 2003). Гиполипидемическое действие мексидола проявилось в условиях всех трех использованных моделей метаболических нарушений: при аллоксановой гипергликемии в снижении ОХ на 20% (р<0,05), β-ЛП - на 35% (р<0,005), ХсЛПНП -на 61% (р<0,005), ИА на 78% (р<0,005) и росте ХсЛПВП на 58% (р<0,01) (рис.8). При моделировании холестериновой дислипидемии (рис.4) применение мексидола позволило снизить содержание ОХ на 18% (р<0,01), β-ЛП - на 52% (р<0,001), уровень ИА - на 63% (р<0,005) и повысить ХсЛПВП на 87% (р<0,01). При введении мексидола на фоне аллоксан - холестериновой дислипидемии (модель №3) отмечалось снижение ОХ и β-ЛП на 33% (р<0,05), ХсЛПНП - на 43% (р<0,05). Индекс атерогенности снизился на 49% (р<0,001).
При этом, введение мексидола в условиях модели №1 и №3 снижало уровень гипергликемии на 48% (р<0,05), хотя на фоне холестериновой дислипидемии, напротив, наблюдался рост содержания сахара в сыворотке крови на 35% (р<0,005).
Актовегин в изученной дозе также оказал гепатопротекторное действие, более значимое в условиях моделирования холестериновой дислипидемии, где сохранялось балочное строение долек, ограничивались дистрофические изменения гепатоцитов и ядерный полиморфизм (но явления кариолизиса не предотвращались). В условиях аллоксановой гипергликемии и аллоксан-холестериновой дислипидемии нарушение балочной структуры печени было менее выраженным, чем в контроле, уменьшалось количество некротизированных гепатоцитов и выраженность лимфогистиоцитарной инфильтрации портальных трактов.
Оксидативному стрессу придается большое значение в патогенезе неалкогольного стеатогепатоза при метаболических нарушениях (Pera N. et al., 1999; G. Robertson et al., 2001). При введении актовегина на фоне аллоксановой гипергликемии снижалось накопление вторичных продуктов ПОЛ в ткани печени: МДА - с 13,91±0,88 до 4,66±0,34 ммоль/л (p<0,001) и FеМДА - с 20,78±1,36 ммоль/л до 15,64±0,93ммоль/л (p<0,01). РЛПО и АОА повышались, активность каталазы снижалась (рис.1). На фоне холестериновой дислипидемии содержание МДА в ткани печени при введении актовегина также уменьшалось (рис.1). Наблюдался рост РЛПО и снижение активности каталазы. При аллоксан-холестериновой дислипидемии отмечалось снижение содержания МДА (с 8,36±0,57 до 3,81±0,26ммоль/л, р<0,001) и FeМДА (с 15,30±1,11 до 6,20±0,81 ммоль/л, р<0,001), снижалась активности каталазы и АОА (рис.1).
Рис.1. Влияние актовегина на некоторые показатели ПОЛ и антиоксидантной защиты ткани печени при моделировании нарушений углеводного и липидного обмена (в % к данным соответствующей контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля.
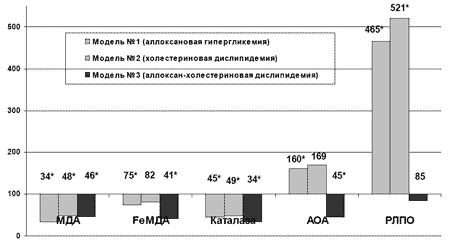
Актовегин проявил мембранопротекторный эффект на модели аллоксан-холестериновой дислипидемии, снижая активность АЛТ - на 58% (р<0,001), АСТ - на 41% (р<0,001).
Кроме того, введение актовегина улучшало альбуминсинтетическую функцию печени при аллоксановой гипергликемии: общая концентрация альбуминов повысилась на 62% (р<0,005). А снижение эндотоксикоза проявилось в увеличении эффективной концентрации альбуминов на 302% (р<0,001), резерва связывания альбуминов - на 88% (р<0,001) и снижении индекса токсичности на 87% (р<0,001), а также в уменьшении концентрации мочевины на 35% (р<0,05). Следует также отметить, что на фоне введения актовегина в условиях аллоксановой гипергликемии предотвращалось развитие гиперкалиемии (с 5,31±0,28 ммоль/л в соответствующей контрольной группе до 4,0±0,15 ммоль/л, р<0,05),
При аллоксан-холестериновой дислипидемии актовегин привел к росту эффективной концентрации альбуминов на 57% (р<0,001), резерва связывания альбуминов - на 34% (р<0,01), снижению индекса токсичности в три раза (р<0,001), а концентрации мочевины - на 35% (р<0,05). Однако при этом наблюдался рост креатинина на 50% (р<0,01). При моделировании холестериновой дислипидемии актовегин в изученной дозе не влиял на показатели эндотоксикоза, но при этом наблюдался рост содержания калия на 11% (р<0,05).
Липидрегулирующее действие актовегина проявилось в условиях всех трех моделей метаболических нарушений: на фоне аллоксановой гипергликемии снижались уровни ТГ и ХсЛПОНП на 59% (р<0,01), β-ЛП - на 35% (р<0,005), ХсЛПНП - на 52%, индекса атерогенности - на 77% (р<0,005) (рис.2). Фракция ХсЛПВП увеличилась на 78% (p<0,001). При моделировании холестериновой дислипидемии ОХ снижался на 11% (р<0,05), ТГ - на 34% (р<0,05), β-ЛП - на 50% (р<0,001), ХсЛПОНП - на 32% (р<0,05) и ХсЛПНП - на 69% (р<0,05). При этом наблюдался рост величины антиатерогенной фракции холестерина - ХсЛ-ПВП на 171% (р<0,001) и снижение индекса атерогенности на 87% (р<0,001) (рис.2). По сравнению с мексидолом в изученных дозах на фоне введения актовегина в условиях данной модели дислипидемии был отмечен более выраженный рост ХсЛПВП (р<0,05) и снижение ИА (р<0,05). Коррекция актовегином при аллоксан-холестериновой дислипидемии привела к увеличению ХсЛПВП и снижению ТГ в 2 раза (р<0,001), уменьшению ХсЛПОНП на 48% (р<0,005), β-ЛП - на 33% (р<0,05), ИА -на 72% (р<0,001) (рис.2).
Актовегин в условиях моделирования аллоксановой гипергликемии и аллоксан-холестериновой дислипидемии не предотвращал роста содержания глюкозы в плазме крови, а в условиях холестериновой дислипидемии приводил к повышению ее уровня на 56% (р<0,05).
Рис.2. Влияние актовегина на некоторые показатели липидного обмена в плазме крови при моделировании нарушений углеводного и липидного обмена (в % к данным соответствующей контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля.
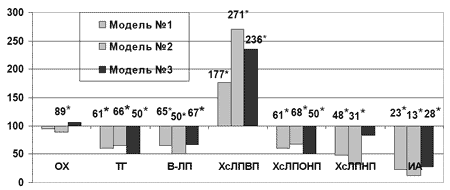
Введение инфезола в изученной дозе не оказало существенного влияния на структуру печени в условиях аллоксановой гипергликемии и аллоксан-холестериновой дислипидемии: уменьшалось только плазматическое пропитывание стенок сосудов и выраженность лимфогистиоцитарной инфильтрации, но повреждение балочной структуры печени и самих гепатоцитов не предотвращалось, прослеживались очаговые центролобулярные и парциальные некрозы, не снижалась полиморфность ядер.
Следует отметить, что позитивным эффектом при курсовом введении инфезола явилось значительное снижение уровня гликемии в условиях аллоксанового диабета - на 40% (р<0,01), в условиях аллоксан-холестериновой дислипидемии - на 62% (р<0,001). Кроме того, введение инфезола привело к снижению активности АЛТ и АСТ на 41% и 32% (р<0,05) при аллоксановой гипергликемии и АЛТ на 47% (р<0,001) при аллоксан-холестериновой дислипидемии. Уменьшалась и выраженность эндогенной интоксикации. Так, на фоне аллоксановой гипергликемии повышался уровень резерва связывания альбуминов на 88% (р<0,001), снижался индекс токсичности на 87%(р<0,001) и уровень мочевины в плазме крови - на 42% (р<0,005). При моделировании сочетанных метаболических нарушений увеличился резерв связывания альбуминов на 25% (р<0,05), снижалась концентрация мочевины на 11% (p<0,01).
Введение инфезола оказало значительное влияние на показатели липидного обмена: на фоне аллоксановой гипергликемии снижались не только ОХ, ТГ, β-ЛП, ХсЛПОНП (р<0,001) и ХсЛПНП (р<0,05)), но и антиатерогенная фракция - ХсЛПВП - на 43% (р<0,05). Рост индекса атерогенности при этом не предотвращался (рис. 3). Более благоприятным оказалось влияние препарата на показатели липидного обмена плазмы крови при моделировании аллоксан-холестериновой дислипидемии, где на фоне снижения ТГ (р<0,001), β-ЛП (р<0,001), ХсЛПНП (р<0,05), ХсЛПОНП (р<0,001) наблюдался рост ХсЛПВП в 2,8 раза (р<0,001), что привело к достоверному снижению индекса атерогенности на 84% (р<0,001) (рис.3).
Рис.3. Влияние инфезола на некоторые показатели липидного обмена в плазме крови при моделировании нарушений углеводного и липидного обмена (в % к данным соответствующей контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля.
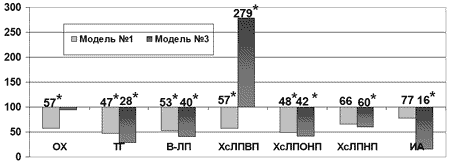
Однако, при этом на фоне введения инфезола не снижалось накопление вторичных продуктов ПОЛ в ткани печени, а при моделировании сочетанных метаболических нарушений, напротив, отмечался рост уровня ТБК-реагирующих продуктов (р<0,05). Активность каталазы в ткани печени на фоне аллоксановой гипергликемии при этом снижалась на 54% (р<0,001), АОА увеличилась в 2,8 (р<0,001), а РЛПО - в 5,5 (р<0,05).
На следующем этапе исследования мы оценили эффекты сочетанного применения препаратов на фоне моделирования метаболических нарушений. Комбинированное введение актовегина и мексидола в значительной степени предотвращало повреждение структуры печени, что проявилось в сохранности дольковой и балочной структуры печени и уменьшении дистрофических изменений гепатоцитов в условиях всех трех моделей. При этом развитие некрозов гепатоцитов на фоне аллоксановой гипергликемии предотвращалось, а в условиях холестериновой дислипидемии и аллоксан-холестериновой дислипидемии количество некротизированных гепатоцитов значительно уменьшалось, ограничивался полиморфизм их ядер и выраженность лимфогистиоцитарной инфильтрации портальных трактов.
При комбинации актовегина и мексидола на фоне аллоксановой гипергликемии несомненно позитивным моментом явилось усиление гипогликемического эффекта мексидола на 23% (с 8,06±0,42 до 6,22±0,40 ммоль/л, р<0,05) (рис.4). Кроме того, в отличие от монотерапии мексидолом, в большей степени снижалась активность АЛТ, АСТ и содержание креатинина (р<0,05) (рис. 4).
Рис.4. Влияние комбинированного применения мексидола с актовегином и инфезолом на содержание глюкозы и некоторые показатели эндотоксикоза в плазме крови белых крыс при аллоксановой гипергликемии (в % к данным соответствующей контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля, #- по сравнению с показателями монотерапии мексидолом.

Антиоксидантное действие мексидолом в печени при комбинации с актовегином не повышалось: изученные в данной работе показатели ПОЛ и антиоксидантной защиты печени не отличались от результатов с монотерапией мексидолом. Не было достоверных отличий и в показателях липидного обмена (рис.7), а также в величине индекса токсичности (рис.4) и резерва связывания альбумина, хотя общая и эффективная концентрация альбумина были ниже на 48% (р<0,05) и 47% (р<0,05) соответственно.
В условиях моделирования холестериновой дислипидемии при комбинированном введении актовегина и мексидола активность трансаминаз, а также показатели свойств альбумина не отличались от данных монотерапии мексидолом, но наблюдалось более высокое (на 30%, p<0,005) содержание глюкозы в плазме крови подопытных животных по сравнению с введением только мексидола. Но при этом, в отличие от монотерапии, предотвращалось развитие гиперкалиемии (4,28±0,19 ммоль/л по сравнению с 5,35±0,32 ммоль/л при введении мексидола, р<0,05). В условиях этой модели использование комбинации препаратов повышало эффективность липидкорригирующего действия мексидола по сравнению с монотерапией: еще больше увеличивалось содержание ХсЛПВП (на 56%, р<0,05), снижалось содержание ХсЛПНП (в 5 раз, р<0,001) и ИА (в 5 раз, р<0,001) (рис. 5). Следует особо подчеркнуть, что при этом содержание ХсЛПНП и величина ИА была достоверно ниже и показателей при монотерапии актовегином на 71% и 49% соответственно (р<0,05).
Рис.5. Влияние комбинированного применения мексидола с актовегином на некоторые показатели липидного обмена плазмы крови при холестериновой дислипидемии (в % к данным контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля, # - по сравнению с показателями монотерапии мексидолом

Комбинированное применение актовегина и мексидола на фоне холестериновой дислипидемии по сравнению с монотерапией производным 3-оксипиридина привело к повышению FеМДА на 69% (р<0,05), активности каталазы - на 62% (р<0,05), АОА - на 133% (р<0,001) и РЛПО - в 2,5 раза (р<0,001). Причем, активность каталазы и АОА превышали и данные с введением актовегина на 29% и 47% соответственно (р<0,05).
Наиболее интересным с точки зрения перспектив для дальнейшего клинического применения было комбинированное введение актовегина и мексидола в условиях моделирования сочетанных метаболических нарушений. В отличие от монотерапии мексидолом наблюдалось уменьшение активности АЛТ на 37% от уровня контрольной группы (р<0,05).
Кроме того, при комбинированном использовании актовегина и мексидола в большей степени, чем при монотерапии мексидолом, повышалась альбумин-синтетическая функции печени: общая концентрация альбумина возросла на 20% (р<0,05) (рис.6). А также уменьшалась степень эндогенной интоксикации: наблюдалось более выраженное снижение индекса токсичности (в 2 раза, р<0,05) и более значительный рост эффективной концентрации альбумина - на 36% (р<0,05), резерва связанного альбумина - на 12% (р<0,05) по сравнению с монотерапией производным 3-оксипиридина. В отличие от использования с целью коррекции только мексидола, комбинированное применение препаратов позволило снизить уровень креатинина (на 36%, р<0,05) и калия (на 9%, р<0,05), полностью предотвратив развитие гиперкалиемии (рис.6).
Рис. 6. Влияние комбинированного применения мексидола с актовегином и инфезолом на некоторые показатели эндотоксикоза плазмы крови при моделировании сочетанных нарушений углеводного и липидного обмена (в % к данным контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля, # - по сравнению с данными монотерапии мексидолом.
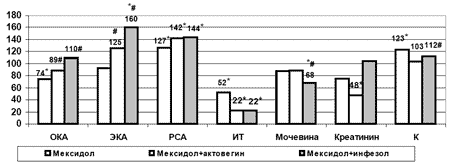
Показатели ПОЛ и антиоксидантной защиты в ткани печени при этом в основном не отличались от данных монотерапии мексидолом, ниже был только уровень FeМДА на 24% (р<0,05). Потенцирования гипогликемического эффекта также не наблюдалось: содержание глюкозы в плазме крови не отличалось от данных группы с введением только мексидола. Но при этом на фоне комбинированного использования мексидола и актовегина в условиях моделирования сочетанных нарушений липидного и углеводного обмена, по сравнению с монотерапей мексидолом, снижалось содержание ТГ на 43% (р<0,05), ХсЛПОНП на 46% (р<0,05). В большей степени (на 89%) возрастал уровень ХсЛПВП (р<0,01) и снижался индекс атерогенности (р<0,001) рис.6).
Таким образом, комбинированное применение актовегина и мексидола оказывает значительное корригирующее воздействие на ряд биохимических показателей при сочетанных метаболических нарушениях.
В отличие от комбинации с актовегином, сочетанное использование инфезола и мексидола не привело к усилению гепатопротекторного эффекта мекси дола. В условиях моделирования аллоксановой гипергликемии только несколько ограничивалось нарушение балочной структуры печени, не предотвращались дистрофические и некротические изменения гепатоцитов, не ограничивался полиморфизм их ядер и лимфогистиоцитарная пролиферация. В условиях аллоксан-холестериновой дислипидемии нарушение балочного строения печени не предотвращалось, регистрировались крупные очаги некрозов. Наблюдался выраженный полиморфизм ядер гепатоцитов, кариолизис, сохранялась лимфо-гистиоцитарная инфильтрация.
При этом в изменении лабораторных показателей наблюдались отдельные позитивные эффекты. Так, комбинация инфезола и мексидола в условиях моделирования аллоксановой гипергликемии в большей степени снижала активность АСТ, чем монотерапия мексидолом (р<0,05), и не влияла на гипогликемический эффект производного 3-оксипиридина (рис.3). Но содержание МДА в печени при этом было в 2,5 раза (р<0,001), а FeМДА - на 75% выше, чем на фоне монотерапии (р<0,05). Содержание мочевины снижалось в большей степени (р<0,05), но уровень креатинина оказался выше (р<0,05) (рис.3). Менее выраженным, чем при монотерапии мексидолом, оказалось и влияние комбинации препаратов на показатели свойств альбуминов: общая концентрация альбуминов была на 27% (р<0,05), эффективная концентрация - на 44%, резерв связанного альбумина - на 27% (р<0,05) ниже, чем при монотерапии производным 3-оксипиридина.
Следует отметить, что позитивным эффектом применения комбинации инфезола и мексидола, по сравнению с введением только мексидола, в условиях модели №1 явилось более значительное снижение содержания ОХ (на 36%, р<0,05), ТГ (на 57%, р<0,05) β-ЛП (на 57%, р<0,05). Но одновременное снижение содержания ХсЛПВП (р<0,05), свидетельствующее об угнетении холестеринсинтетической функции печени, привело к росту ИА и ХсЛПНП по сравнению с введением только производного 3-оксипиридина (рис.7).
Рис.7. Влияние комбинированного применения мексидола с актовегином и инфезолом на показатели липидного обмена плазмы крови при аллоксановой гипергликемии (в % к данным контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля, #- по сравнению с показателями монотерапии мексидолом

В условиях аллоксан-холестериновой дислипидемии на фоне введения комбинации инфезола и мексидола по сравнению с монотерапией мексидолом, несмотря на рост ОХ (на 89%, р<0,001) и β-ЛП (на 23%, р<0,05), содержание ТГ и ХсЛПОНП снижалось на 23% (р<0,05), индекс атерогенности - на 69% (р<0,001) за счет роста ХсЛПВП на 150% (р<0,001) (рис.8). Положительным моментом по сравнению с монотерапией мексидолом был рост общей концентрации альбуминов на 48%, а также дальнейшее снижение выраженности эндогенной интоксикации (рис.6) за счет повышения ЭКА на 74% (р<0,01), РСА -на 13% (р<0,001) и снижения содержание мочевины на 22% (р<0,05). В отличие от введения мексидола (р<0,05) не наблюдалось и роста содержания калия в плазме крови (рис.6).
Рис. 8. Влияние комбинированного применения мексидола с актовегином и инфезолом на некоторые показатели липидного обмена плазмы крови при моделировании сочетанных нарушений углеводного и липидного обмена (в % к данным контрольной группы); * - достоверность различия р<0,05 по сравнению с данными контроля, #- по сравнению с показателями монотерапии мексидолом

Однако, негативным эффектом при использовании комбинации инфезола и мексидола на фоне аллоксан-холестериновой дислипидемии явился рост активности цитолитических ферментов не только по сравнению с монотерапией мек-сидолом, но даже с данными контроля: АЛТ более, чем в 2 раза (р<0,001) и АСТ на 14%. В гомогенатах печени при этом отмечался рост МДА и FеМДА также не только по сравнению с монотерапией (р<0,001), но и по сравнению с контролем (на 41% и 62% соответственно, р<0,005). Активность каталазы и АОА не отличались, а РЛПО был ниже серии с применением производного 3-оксипиридина на 65% (р<0,005).
Таким образом, наибольшую эффективность на фоне моделирования сочетанных метаболических нарушений показала комбинация актовегина и мексидола.
ВЫВОДЫ
1. При моделировании нарушений липидного обмена актовегин (40 мг/кг) оказывает гиполипидемическое действие, ограничивает структурные повреждения печени и уменьшает выраженность эндогенной интоксикации.
2. В условиях моделирования сочетанных нарушений липидного и углеводного обмена актовегин в изученной дозе проявляет гиполипидемическое, гипогликемическое, цитопротекторное, дезинтоксикационное и антиоксидантное действие и уменьшает структурные повреждения печени.
3. Комбинированное применение актовегина и мексидола повышает гепатопротекторный, гиполипидемический и дезинтоксикационный эффект мексидола при моделировании нарушений липидного, углеводного обмена и сочетанных метаболических нарушений. В условиях моделирования аллоксановой гипергликемии потенцирует гипогликемическое, антиоксидантное действие мексидола и предупреждает гиперкалиемию.
4. Инфезол в изученной дозе в условиях аллоксановой гипергликемии и аллоксан-холестериновой дислипидемии не ограничивает структурные повреждения печени, но снижает холестеринсинтетическую функцию печени, оказывает гипогликемическое, дезинтоксикационное действие и снижает активность цитолитического синдрома.
5. Комбинированное применение инфезола и мексидола снижает антиоксидантный эффект мексидола в ткани печени и его гепатопротекторное действие, уменьшает холестеринсинтетическую функцию печени при аллоксановом диабете и повышает содержание холестерина липопротеидов высокой плотности и общего холестерина при сочетанных нарушениях липидного и углеводного обмена.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Целесообразно дальнейшее клиническое исследование комбинированного применения мексидола и актовегина для коррекции сочетанных метаболических нарушений липидного и углеводного обмена и повышения гиполипидемического и гепатопротекторного эффекта мексидола. Целесообразно дальнейшее экспериментальное исследование гепатопротекторного, гиполипидемического и гипогликемического действия инфезола, а также липидрегулирующего эффекта комбинированного применения инфезола и мексидола при сочетанных нарушениях липидного и углеводного обмена.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1 Хоронеко С.Е., Артюкова М.М. Морфологические аспекты адаптации организма в условиях гиперхолестеринении.// Материалы XII межрегиональной научно-практической конференции ГОУ ДПО "Пензенский институт усовершенствования врачей Федерального агентства по здравоохранению и социальному развитию" - "Актуальные вопросы диагностики, лечения и реабилитации больных" -- Пенза - 20 октября 2006 г. - С.305-307.
2. Артюкова М.М., Ершкова Н.Г., Горожанин С.В., Киселева О.М., Зорькина А.В. Влияние мексидола и актовегина на некоторые метаболические показатели при нарушении углеводного обмена в эксперименте. //XIV Российский национальный конгресс "Человек и лекарство" Сборник материалов конгресса (тезисы докладов) - Москва 2007. - С.794.
3. Зорькина А.В., Хоронеко С.Е., Артюкова М.М. Влияние мексидола и актовегина на структуру печени белых крыс при моделировании аллоксан -холестериновой дислипидемии. // Медицинские науки- №4 (16) - 2006 .- С. 30-31.
4. Ивлиева Е.Н., Бин Хатабин Х.А.А., Артюкова М.М. Коррекция метаболических нарушений лекарственными препаратами и соединениями с антиоксидантным типом действия при экспериментальных дислипидемиях. // Медицинские проблемы жизнедеятельностим организма в норме, патологии и эксперименте: материалы XII научной конференции молодых ученых аспирантов и студентов медицинского факультета Мордов. гос. ун-та. Выпуск 7.- Саранск Изд-во Мордов. Ун-та, 2007.- С.40-42.
5. Зорькина А.В., Ямашкина Е.И.. Артюкова М.М., Столярова В.В.Влияние мексидола и актовегина на некоторые биохимические показатели при индуцированном метаболическом синдроме //Материалы научно-практической конференции, "Современная кардиология: наука и практика"-Вестник Санкт-Петербургской государственной медицинской академии им. И.И.Мечникова. -2007, №2 (2), Приложение. - С. 66-67.
6. Зорькина А.В., Артюкова М.М., Бин Хатабин Х.А., Юдина Н.Д. Новые возможности в регуляции метаболического синдрома // Вестник восстановительной медицины. -2007, №4. - С.41-45.
7.Исследование влияния мексидола и актовегина на некоторые биохимические показатели при комбинированном нарушении углеводного и липидного обмена в эксперименте //Медицинские науки. - 2007, №4.-С.14-16.
Комментарии
ПРАКТИКА ПЕДИАТРА
