Раннее применение дазатиниба после развития цитогенетической или гематологической резистентности к иматинибу у пациентов с хроническим миелолейкозом
СтатьиAlfonso Quintas-Cardama, MD1; Jorge E. Cortes, MD1; Susan O’Brien, MD1; Farhad Ravandi, MD1; Gautam Borthakur, MD1; David Liu, MD, PhD2; Eric Bleickardt, MD3; Tai-Tsang Chen, PhD3; Hagop M. Kantarjian, MD1Введение. Несмотря на то что многие больные хроническим миелоидным лейкозом (ХМЛ) хорошо отвечают на терапию иматинибом, в последующем значительная часть пациентов теряет первоначальный ответ на лечение. Утрата чувствительности к иматинибу часто связана с мутациями BCR-ABL. Дазатиниб ингибирует Bcr-Abl в 325 раз сильнее иматиниба и дает высокую частоту стойких ответов в хронической фазе ХМЛ после неудачи лечения иматинибом. МЕТОДЫ. Для определения оптимального времени для назначения дазатиниба после утраты чувствительности к иматинибу были проанализированы данные исследований дазатиниба у пациентов с хронической фазой ХМЛ. Распределение больных по группам проводилось в зависимости от того, насколько рано они начинали получать дазатиниб (т. е. либо сразу после цитогенетического рецидива во время лечения иматинибом, либо после цитогенетического и гематологического рецидивов). РЕЗУЛЬТАТЫ. Среди пациентов, которые получали дазатиниб после утраты большого цитогенетического ответа (БЦО) на иматиниб, удалось достичь полного цитогенетического ответа (ПЦО) в 72 % случаев, по сравнению с 42 % случаев у пациентов, начавших лечение дазатинибом после утраты как большого цитогенетического, так и полного гематологического ответов (ПГО). Бессобытийная выживаемость (БСВ) при раннем назначении дазатиниба тоже была выше (24-месячная БСВ: 89 % после утраты БЦО на иматиниб и 29 % после утраты как БЦО, так и ПГО). Среди пациентов, которые не имели БЦО на иматиниб и получали лечение после утраты ПГО, ПЦО на дазатиниб удалось получить у 26 %, а 24-месячная БСВ составила 64 %. Во всех трех группах частота ПЦО была одинаковой у больных с наличием или отсутствием предсуществовавших мутаций BCR-ABL. ВЫВОДЫ. Результаты данного исследования свидетельствуют, что оптимальный результат достигается, если дазатиниб назначается рано после развития резистентности к иматинибу.
Cancer 2009;115:2912–21. © 2009 American Cancer Society.
КЛЮЧЕВЫЕ СЛОВА: дазатиниб, хронический миелоидный лейкоз, иматиниб, резистентность к противоопухолевому препарату.
Хронический миелоидный лейкоз (ХМЛ) — клональное миелопролиферативное заболевание, характеризующееся реципрокной хромосомной транслокацией t(9;22)(q34;q11.2), которая приводит к образованию Филадельфийской хромосомы (Ph) и химерного гена BCR-ABL. Образующийся онкобелок Bcr-Abl является конститутивно активной тирозинкиназой, придающей лейкозным клеткам преимущество в выживании за счет усиленной пролиферации и сниженного апоптоза и увеличивающей геномную нестабильность посредством подавления репарации ДНК.1 Более чем в 80 % случаев ХМЛ диагностируется во время начальной, хронической фазы заболевания.2 Без эффективного лечения пациенты с хронической стадией ХМЛ неизбежно переходят в продвинутые стадии и имеют короткую продолжительность жизни.
В настоящее время лечение ХМЛ основано на эффективной блокаде активности Bcr-Abl. Первым таргетным препаратом против BcrAbl, одобренным для лечения ХМЛ, был иматиниба мезилат (Гливек; Novartis Pharmaceuticals, Базель, Швейцария).3,4 Несмотря на то что большинство пациентов хорошо отвечают на лечение иматинибом, в международном рандомизированном исследовании III фазы интерферона и STI571 (IRIS) у 31 % участников не удалось получить полный цитогенетический ответ (ПЦО) в течение 12 мес. и ежегодно от 0,4 до 5,5 % пациентов, достигших ПЦО, теряли его3. Резистентность к иматинибу чаще всего возникает в результате мутаций, вызывающих конформационные изменения или меняющих критически важные тирозиновые остатки в иматиниб-связывающей области онкобелка Bcr-Abl.5
Дазатиниб (Спрайсел; Bristol-Myers Squibb, США) — это ингибитор Bcr-Abl II поколения, применяющийся для лечения взрослых, страдающих любой фазой ХМЛ, у которых отмечена резистентность или непереносимость иматиниба. В условиях in vitro дазатиниб в 325 раз активнее иматиниба.6
Лечение дазатинибом индуцирует высокую частоту стойкого ответа на терапию у пациентов с резистентностью или непереносимостью иматиниба, в том числе при всех изученных мутациях BCR-ABL, за исключением замены треонина на изолейцин в кодоне 315 (T315I).7–9
Время начала второй линии терапии после неудачи первоначального лечения может оказывать значительное влияние на результаты лечения в долгосрочной перспективе. Среди получавших иматиниб после неудачи лечения интерфероном-альфа (ИФН-α) более высокая чувствительность и выживаемость отмечены у тех пациентов, которым иматиниб начали вводить во время цитогенетического, а не гематологического рецидива.10,11 Также в недавнем исследовании больных с неудачей лечения иматинибом установлено, что применение терапии второй линии после гематологической резистентности или рецидива по сравнению с началом лечения после цитогенетической резистентности/рецидива является независимым прогностическим фактором низкой выживаемости (p = 0,01; трехлетняя общая выживаемость [ОВ] 57 vs 92 % соответственно).12 Анализ, представленный в настоящей статье, был проведен с целью изучить влияние раннего применения дазатиниба (т. е. после цитогенетического, а не гематологического рецидива при терапии иматинибом) на последующую частоту ответа и результаты лечения в долгосрочной перспективе.
Материалы и методы
Исследованная группа пациентов
Проведен анализ данных, полученных в 3 клинических исследованиях, посвященных терапии хронической фазы ХМЛ дазатинибом: CA180-013, CA180-017 и CA180-034 (табл. 1). CA180-013 (START-C) — это исследование II фазы, в котором пациентам с резистентностью или непереносимостью иматиниба (387 больных) назначали дазатиниб в дозе 70 мг 2 раза в сутки.7 CA180-017 (START-R) представляет собой рандомизированное исследование II фазы, в котором терапию дазатинибом сравнивали с увеличением дозы иматиниба у пациентов, которые были резистентны к иматинибу в дозах 400–600 мг/сут, в исследование включен 101 больной, получавший дазатиниб по 70 мг 2 раза в сутки13. В обоих исследованиях — CA180-013 и CA180-017 — при отсутствии ответа или прогрессировании заболевания разрешалось увеличивать дозу дазатиниба до 90 мг 2 раза в сутки; при развитии нежелательных явлений допускалось временно отменять препарат или уменьшать его дозу до 40 мг 2 раза в сутки. Исследование CA180-034 — это рандомизированное исследование III фазы по подбору оптимальной дозы у пациентов с резистентностью к иматинибу (включая как субоптимальный ответ, так и неудачу лечения) или его непереносимостью (670 больных).14 Дазатиниб назначался в одном из 4 дозовых режимов: 100 мг 1 раз в сутки (n = 167), 50 мг 2 раза в сутки (n = 168), 140 мг 1 раз в сутки (n = 167) и 70 мг 2 раза в сутки (n = 168). В случае отсутствия ответа разрешалось увеличивать дозу дазатиниба до 180 мг 1 раз в сутки или 90 мг 2 раза в сутки, а при развитии нежелательных явлений допускался перерыв в терапии или снижение дозы до 80 мг 1 раз в сутки или 40 мг 2 раза в сутки. Каждое исследование проводилось в соответствии с Хельсинкской декларацией и утверждалось экспертным советом организации или этическим комитетом каждого участвующего центра. От всех пациентов получено письменное информированное согласие. Таблица 1. Характеристика групп больных, включенных в данное исследование
| Показатель | CA180-013: START-C, n = 114a | CA180-017: START-R, n = 41b | CA180-034, n = 138c |
|---|---|---|---|
| Медиана длительности лечения, мес. | 22,7 | 24,9 | 11,9 |
| Группа больных | ХМЛ-ХС | ХМЛ-ХС | ХМЛ-ХС |
| Критерии включения при резистентности к иматинибу | Первичная или приобретенная резистентность к > 600 мг/сут иматиниба или приобретенная резистентность к ≤ 600 мг/сут иматиниба с мутацией BCR-ABL (резистентность к иматинибу высокого уровня)d | Первичная или приобретенная резистентность к 400–600 мг/сут иматиниба; исключены больные с известными мутациями BCR-ABL с резистентностью к иматинибу до включения в исследованиеd | Первичная или приобретенная резистентность или субоптимальный ответ на ≥ 400 мг/сут иматиниба Число больных, утративших ответ на иматиниб, % |
| Общее число больных, утративших ответ на лечение | 114 | 41 | 138 |
| Утрата БЦО | 47 (41) | 19 (46) | 85 (62) |
| Утрата ПГО | 50 (44) | 20 (49) | 39 (28) |
| Утрата БЦО и ПГО | 17 (15) | 2 (5) | 14 (10) |
| Медиана средней суточной дозы дазатиниба, мг | 112 | 128 | 100 |
a См. Hochhaus 2008.7
b См. Kantarjian 2007.13
c См. Shah 2007.14
d Замена лейцина на валин в кодоне 248, замена глицина на глутаминовую кислоту в кодоне 250, замена глутамина на гистидин в кодоне 252, замена тирозина на гистидин или фенилаланин в кодоне 253, замена глутаминовой кислоты на лизин или валин в кодоне 255, замена треонина на изолейцин или аланиновую кислоту в кодоне 315, замена фенилаланина на лейцин в кодоне 317 и замена гистидина на пролин или аргинин в кодоне 396.
Определение ответа и анализ данных
Полным гематологическим ответом (ПГО) считали число лейкоцитов в крови не выше верхней границы нормы (ВГН) для данной лаборатории, абсолютное число нейтрофилов 1 × 109/л и более, число тромбоцитов менее 450 × 109/л и не выше ВГН для данной лаборатории, менее 5 % миелоцитов и метамиелоцитов в крови, менее 20 % базофилов в крови, а также отсутствие экстрамедуллярных очагов кроветворения; все перечисленные критерии должны сохраняться не менее 4 нед. Цитогенетические ответы (ЦО) подразделяли по количеству Ph-позитивных метафаз в костном мозге, используя стандартные критерии: 0 % Ph-позитивных метафаз — полный ЦО (ПЦО); от 1 до 35 % — частичный ЦО (ЧЦО). Большой ЦО (БЦО) определялся как сумма ПЦО и ЧЦО (т. е. до 35 % Ph-позитивных метафаз). Большим молекулярным ответом (БМО) считали снижение числа транскриптов BCR-ABL до 0,1 и менее от международного стандартизованного соотношения BCR-ABL:ABL.
В данном анализе проводилась оценка частоты ПГО, БЦО, ПЦО, бессобытийной выживаемости (БСВ), выживаемости без трансформации (ВБТ) и общей выживаемости (ОВ). Для определения всех цитогенетических ответов во время лечения дазатинибом использовались общепринятые цитогенетические методики подсчета Ph-позитивных метафаз в костном мозге. Частота БМО анализировалась только в исследовании CA180-013; при расчете этого показателя знаменателем было число всех оцененных участников.
При анализе БСВ учитывались следующие события: трансформация в фазу акселерации или бластного криза, утрата ПГО или БЦО, увеличение числа лейкоцитов (в два раза от наименьшего уровня до более чем 20 000/ мкл или более чем на 50 000/ мкл при двух измерениях с промежутком не менее 2 нед.) для пациентов, которые не достигли полной гематологической ремиссии, а также летальный исход. В анализ ВБТ были включены следующие события: трансформация в фазу акселерации или бластного криза, летальный исход. При анализе ОВ участников исследования CA180-017, которые впоследствии стали получать иматиниб (n = 10), цензурировали на момент перехода на этот препарат.
Анализ пациентов проводился в зависимости от наличия мутаций в киназном домене Bcr-Abl до лечения дазатинибом, определявшихся методом прямого секвенирования. Регион Bcr-Abl, где располагалась связывающая фосфат АТР петля (Р-петля), был определен как расположение аминокислотных остатков от 248 до 256.
Группы больных
Целью настоящего анализа было выяснить, улучшаются ли результаты лечения больных с хронической фазой ХМЛ и неудачей лечения иматинибом, если дазатиниб назначается после утраты БЦО (раннее применение), а не после утраты как БЦО, так и ПГО (позднее применение). В данный анализ включались пациенты с хронической стадией ХМЛ и приобретенной резистентностью к иматинибу, определявшейся как утрата ПГО или БЦО. В него не были включены пациенты с непереносимостью иматиниба. Больные, отвечающие критериям включения, были разделены на 3 группы в зависимости от информации, предоставленной врачом-исследователем, о лучшем ответе на иматиниб и утрате ответа (цитогенетического и/ или гематологического) во время предыдущего лечения иматинибом до начала терапии дазатинибом. В группу 1 (утрата БЦО) вошли больные, достигшие БЦО на иматиниб и в последующем утратившие его. Утрата БЦО определялась как дальнейшее несоответствие критериям БЦО и увеличение процента Ph-позитивных метафаз до 30 и более. Ни у одного из этих больных исследователи не отметили утраты ПГО. Группа 2 (утрата БЦО и ПГО) включала пациентов, достигших как БЦО, так и ПГО и утративших в последующем оба ответа. В группу 3 (утрата ПГО) входили больные, достигшие ПГО и утратившие его впоследствии, при этом они никогда не достигали БЦО. Больные, утратившие ПГО, но достигшие БЦО, у которых исследователь не подтвердил документально утрату БЦО (n = 37), были исключены из анализа.
Результаты
Характеристики больных
Всего в данный анализ было включено 293 пациента, утративших БЦО или ПГО. В группу 1 (утрата БЦО) вошел 151 больной, в группу 2 (утрата БЦО и ПГО) — 33, в группу 3 (утрата ПГО без предшествующего БЦО) — 109 (табл. 2). Из 33 больных, утративших БЦО и ПГО во время лечения иматинибом (группа 2), одновременная утрата двух ответов отмечена у 4 пациентов. Все остальные больные также утратили БЦО, а в последующем — и ПГО.
Во всех 3 группах более 50 % больных получали более 600 мг/сут иматиниба и 60 % или большее число принимали иматиниб более 3 лет (табл. 2). Медиана длительности ХМЛ была меньше в группах с утратой БЦО (группа 1, 64 мес.) и БЦО/ПГО (группа 2, 67 мес.) по сравнению с группой больных, которые утратили ПГО и ранее не достигли БЦО (группа 3, 79 мес.).
В группе пациентов, утративших БЦО (группа 1), было меньше больных (44 %), у которых во время лечения иматинибом возникли мутации BCR-ABL, по сравнению с группами, в которых отмечалась потеря БЦО и ПГО (67 %) и ПГО (75 %). В 3 группах не отмечено больших различий по частоте отдельных мутаций BCR-ABL. Таблица 2. Исходные характеристики больныхa
| Показатель | Группа 1: утрата БЦО, раннее начало лечения (n = 151) | Группа 2: утрата ПГО и БЦО, позднее начало лечения (n = 33) | Группа 3: утрата ПГО (n = 109) |
|---|---|---|---|
| Пол, мужской/женский, % | 55/45 | 52/48 | 54/46 |
| Медиана возраста (диапазон), годы | 55 (18–81) | 60 (28–85) | 59 (21–81) |
| Медиана длительности ХМЛ (диапазон), месяцы | 64 (9–211) | 67 (13–150) | 79 (4–251) |
| Наибольшая доза иматиниба, мг/сут (%) | |||
| 400–600 | 48 | 49 | 37 |
| > 600 | 52 | 51 | 63 |
| Лечение ИФН-α в анамнезе, % | 71 | 64 | 63 |
| Трансплантация стволовых клеток в анамнезе, % | 8 | 6 | 10 |
| Лечение иматинибом в анамнезе, % | |||
| 1 | 3 | 5 | |
| 1–3 года | 33 | 27 | 35 |
| > 3 лет | 66 | 70 | 60 |
| Ответ до начала лечения дазатинибом, %b | |||
| ПГО | 49 | 6 | 12 |
| БЦО | 20 | 0 | 5 |
| Мутации BCR-ABL, число (%)c | 60 (44) | 20 (67) | 77 (75) |
| T315I | 2 (1) | 1 (3) | 1 (1) |
| F317L | 1 (1) | — | 4 (4) |
| F359C/I/V | 8 (6) | — | 6 (6) |
| Район P-петлиd | 19 (14) | 7 (23) | 30 (29) |
| L248V | 2 (1) | — | 6 (6) |
| G250E | 6 (4) | 4 (13) | 12 (12) |
| Q252H | 1 (1) | — | 2 (2) |
| Y253F/H | 8 (6) | 1 (3) | 8 (8) |
| E255K/V | 2 (1) | 2 (7) | 4 (4) |
a Больные, отвечающие критериям включения, были разбиты на группы в зависимости от информации об утрате ответа на иматиниб, предоставленной врачомисследователем.
b Определялся во время исследований дазатиниба.
c Число больных, у которых имелись образцы для исследования мутаций до начала исследования: группа 1, n = 135; группа 2, n = 30; группа 3, n = 103.
d Аминокислотные остатки 248–256.
Эффективность
После лечения дазатинибом (медиана длительности 13,8 мес., диапазон 0,2–30,6 мес.) 90 % всех анализируемых пациентов достигли ПГО, 62 % — БЦО и 51 % — ПЦО. Общая частота БМО составила 40 % среди больных, принимавших участие в исследовании CA180-013, которые были включены в данный анализ. В каждой группе у участников каждого из 3 исследований наблюдалась почти одинаковая частота ответа на лечение (табл. 3). У больных, получавших альтернативные режимы дозирования дазатиниба, не отмечено явных отличий в частоте ответа, но в некоторых случаях таких пациентов было немного. Доля пациентов, достигших ПЦО при лечении дазатинибом после утраты БЦО на иматиниб (группа 1), была близкой в случаях назначения дазатиниба в дозе 70 мг 2 раза в сутки или 100 мг 1 раз в сутки. В группах 2 и 3 только несколько пациентов получали 100 мг дазатиниба 1 раз в сутки, что не позволяет провести сравнение.
У пациентов, утративших БЦО на иматиниб (группа 1; раннее начало лечения), 72 % достигли ПЦО при лечении дазатинибом по сравнению с 42 % больных, которые начали получать препарат после утраты как БЦО, так и ПГО (группа 2; позднее начало лечения) (табл. 3). Частота БМО (данные только из исследования CA180-013) составила 60 % в группе 1 (47 оцененных пациентов) и 29 % в группе 2 (17 оцененных больных). У пациентов, получавших лечение дазатинибом после утраты ПГО, но не имевших ранее БЦО при терапии иматинибом (группа 3), 26 % достигли ПЦО и 26 % — БМО (50 оцененных больных) (табл. 3). Время до достижения ПЦО у ответивших пациентов было одинаковым в 3 группах (рис. 1). Так, у больных, ответивших на лечение, медиана времени до достижения ПЦО (95% доверительный интервал [95% ДИ]) составила 2,9 мес. (95% ДИ 2,8–3,1 мес.) в группе 1, 4,2 мес. (95% ДИ 2,8–5,8 мес.) — в группе 2 и 3,2 мес. (95% ДИ 2,8–5,5 мес.) — в группе 3. У пациентов с ПЦО большинство (80–85 %) достигли его в течение первых 6 мес. лечения. Таблица 3. Частота полного гематологического ответа, большого цитогенетического ответа (все исследования) и большого молекулярного ответа (только исследование CA180-013) у больных, получавших дазатиниб после утраты ответа на иматиниб
| Больные, n/N, % | |||
|---|---|---|---|
| Показатель | Группа 1: утрата БЦО на иматиниб | Группа 2: утрата БЦО и ПГО на иматиниб | Группа 3: утрата ПГО на иматиниб без предшествующего БЦО |
| ПГО: все больные | 139/151 (92) | 28/33 (85) | 98/109 (90) |
| БЦО: все больные | 123/151 (81) | 21/33 (64) | 38/109 (35) |
| ПЦО | |||
| Все больные | 108/151 (72) | 14/33 (42) | 28/109 (26) |
| Данные о ПЦО в зависимости от режима/дозирования | |||
| Больные, получавшие 70 мг 2 раза в сутки | 67/89 (75) | 10/25 (40) | 20/78 (26) |
| Больные, получавшие 100 мг 1 раз в сутки | 21/28 (75) | 1/1 (100) | 1/9 (11) |
| Другие режимы, 50 мг 2 раза в сутки или 140 мг 1 раз в сутки | 20/34 (59) | 3/7 (43) | 7/22 (32) |
| ПЦО в зависимости от исследования | |||
| Исследование CA180-013, 70 мг 2 раза в сутки | 36/47 (77) | 6/17 (35) | 13/50 (26) |
| Исследование CA180-017, 70 мг 2 раза в сутки | 12/19 (63) | 1/2 (50) | 5/20 (25) |
| Исследование CA180-034 | |||
| 100 мг 1 раз в сутки | 21/28 (75) | 1/1 (100) | 1/9 (11) |
| 50 мг 2 раза в сутки | 11/17 (65) | 1/2 (50) | 2/10 (20) |
| 140 мг 2 раза в сутки | 9/17 (53) | 2/5 (40) | 5/12 (42) |
| 70 мг 2 раза в сутки | 19/23 (83) | 3/6 (50) | 2/8 (25) |
| БМО: исследование CA180-013,70 мг 2 раза в суткиa | 28/47 (60) | 5/17 (29) | 13/50 (26) |
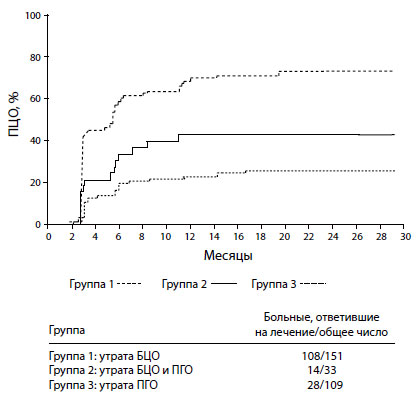
Рис. 1. Время до полного цитогенетического ответа у больных, получавших дазатиниб после утраты ответа на иматиниб.
Частота ответа у больных с мутациями BCR-ABL
В 3 исследуемых группах возникшие ранее мутации BCR-ABL, по-видимому, не влияли на частоту ПЦО, однако число больных в некоторых случаях было небольшим (табл. 4). У пациентов с мутациями BCR-ABL и больных без каких-либо мутаций BCR-ABL частота ПЦО составила соответственно 77 vs 68 % в группе 1 (утрата БЦО), 45 vs 50 % — в группе 2 (утрата БЦО и ПГО) и 25 vs 31 % — в группе 3 (утрата ПГО без предшествующего БЦО). В группах 1 и 3 частота ПЦО у пациентов с мутациями в области P-петли была близкой к этому показателю у всех остальных больных. В группе 2 частота ПЦО была ниже у пациентов с мутациями в районе P-петли, однако число больных было небольшим (n = 7).
В группе утраты БЦО (группа 1) и утраты БЦО/ ПГО (группа 2) среди оцененных пациентов с мутациями BCR-ABL и без таких мутаций частота БМО была близкой (группа 1: 62 vs 54 % соответственно; группа 2: 31 vs 33 % соответственно). В группе пациентов, утративших ПГО и никогда не имевших ранее БЦО (группа 3), частота БМО была ниже у больных с мутациями BCR-ABL по сравнению с больными без этих мутаций (24 vs 42 % соответственно). Как и в предыдущих исследованиях, у пациентов с мутацией T315I ответа на лечение не наблюдалось. Таблица 4. Частота полного цитогенетического ответа (все исследования) и большого молекулярного ответа (только в исследовании CA180-013) у больных с имеющимися мутациями BCR-ABL, получавших дазатиниб после утраты ответа на иматиниб
| Больные, n/N, % | |||
|---|---|---|---|
| Показатель | Группа 1: утрата БЦО | Группа 2: утрата БЦО и ПГО | Группа 3: утрата ПГО |
| ПЦО Отсутствие мутаций BCR-ABL | 51/75 (68) | 5/10 (50) | 8/26 (31) |
| Любая мутация BCR-ABL | 46/60 (77) | 9/20 (45) | 19/77 (25) |
| T315I | 0/2 (0) | 0/1 (0) | 0/1 (0) |
| F317L | 1/1 (100) | — | 0/4 (0) |
| F359C/I/V | 8/8 (100) | — | 1/6 (17) |
| Область P-петлиa | 13/19 (68) | 2/7 (29) | 7/30 (23) |
| L248V | 1/2 (50) | — | 2/6 (33) |
| G250E | 5/6 (83) | 1/4 (25) | 1/12 (8) |
| Q252H | 0/1 (0) | — | 1/2 (50) |
| Y253F/H | 6/8 (75) | 1/1 (100) | 2/8 (25) |
| E255K/V | 1/2 (50) | 0/2 (0) | 1/4 (25) |
| Образцы недоступны | 11/16 (69) | 0/3 (0) | 1/6 (17) |
| БМО | |||
| Отсутствие мутаций BCR-ABL | 13/24 (54) | 1/3 (33) | 5/12 (42) |
| Любая мутация BCR-ABL | 13/21 (62) | 4/13 (31) | 8/35 (23) |
| Образцы недоступны | 2/2 (100) | 0/1 (0) | 0/3 (0) |
a Остатки 248–256.
Бессобытийная выживаемость, выживаемость без трансформации и общая выживаемость
У больных, получавших дазатиниб после утраты БЦО (группа 1), по сравнению с пациентами, получавшими этот препарат после утраты БЦО и ПГО (группа 2), частота событий (определения даны выше) была ниже (рис. 2А). 24-месячная БСВ в группе 1 составила 89 %, а в группе 2 — 29 %. В группе 2 медиана БСВ равнялась 18,5 мес.; в группе 1 медиана не была достигнута. Частота ВБТ и ОВ в течение 24 мес. составила по 98 % для обоих показателей в группе 1 и по 93 % — в группе 2.
24-месячная БСВ у пациентов, получавших дазатиниб после утраты ПГО и не имевших предшествующего БЦО на иматиниб (группа 3), была ниже (64 %), чем у больных, получавших лечение после утраты БЦО (группа 1), но выше, чем у пациентов, которые получали препарат после утраты БЦО и ПГО (группа 2). Однако больные в группе 3 имели более низкие 24-месячные показатели ВБТ (79 %) и ОВ (86 %), чем пациенты в группах 1 и 2. 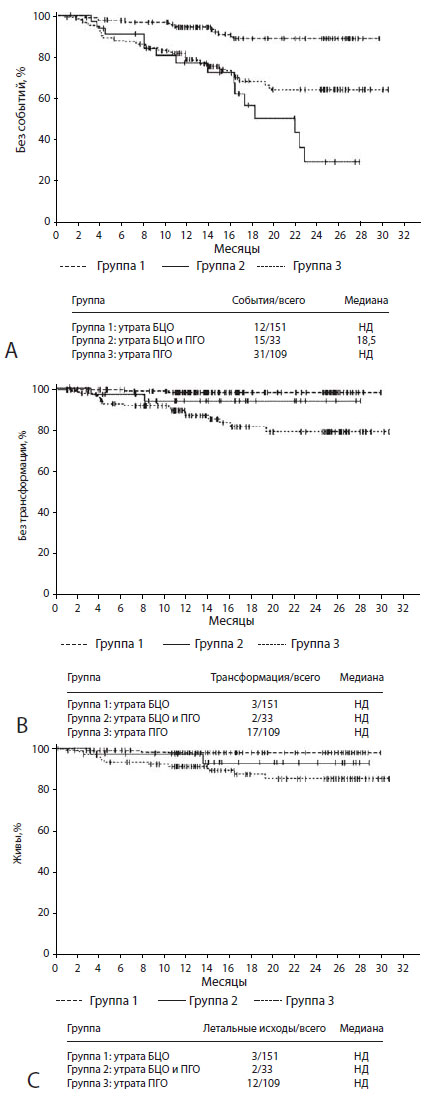
Рис. 2. Анализ выживаемости по Каплану—Мейеру больных, получавших дазатиниб после утраты ответа на лечение иматинибом. (A)
Бессобытийная выживаемость. (B) Выживаемость без трансформации. (C) Общая выживаемость. НД — не достигнута
Обсуждение
Дазатиниб — эффективное лечение для пациентов с неудачей предшествующего лечения иматинибом. Результаты настоящего анализа свидетельствуют, что наиболее высокие показатели частоты ответа на лечение, БСВ, ВБТ и ОВ могут быть достигнуты, если после неудачи лечения иматинибом лечение дазатинибом начато как можно раньше, т. е. после утраты БЦО, а не после утраты как БЦО, так и ПГО. Это согласуется с более ранними наблюдениями применения иматиниба в качестве второй линии терапии после предшествующей неудачи лечения ИФН.10,11 Следует отметить, что время достижения ответа у пациентов, ответивших на лечение, было одинаковым, о чем свидетельствуют перекрывающиеся доверительные интервалы медианы времени до наступления ПЦО, что частично может быть обусловлено небольшим размером выборки в группе 2. Вероятно, улучшение результатов при раннем начале лечения не объясняется более коротким временем достижения ответа, что может быть прогностически благоприятным при ХМЛ.15 Однако у больных, начавших лечение дазатинибом в группе 1 раньше всех, показатели ПЦО были самыми высокими. У пациентов в этой группе, получавших дазатиниб по 70 мг 2 раза в сутки или по 100 мг 1 раз в сутки, частота ПЦО была одинаковой.
В предыдущих исследованиях мутации BCR-ABL обнаружены у 50–90 % больных с приобретенной резистентностью к иматинибу.16–19 В данном анализе у пациентов, утративших как БЦО, так и ПГО на иматиниб (группа 2), а также у больных, утративших ПГО и не имевших ранее БЦО на иматиниб (группа 3), частота мутаций BCR-ABL была выше по сравнению с больными, которые утратили только БЦО (группа 1). Однако, как сообщалось ранее,7,13 частота ПЦО при лечении дазатинибом была одинаковой у больных с мутациями и без мутаций. Различия между группами также не были связаны с увеличением числа пациентов с мутацией T315I или другими мутациями, связанными с относительной нечувствительностью к дазатинибу. Однако следует с осторожностью интерпретировать данные о мутациях в настоящем анализе, принимая во внимание относительно небольшое число больных, особенно в группе 2. В отчете о пациентах с первичной цитогенетической резистентностью к иматинибу появление мутаций BCR-ABL было связано с более быстрым прогрессированием заболевания и снижением выживаемости,20 однако разница в выживаемости не отмечалась в анализе, включавшем больных с другими категориями резистентности к иматинибу, что, возможно, отражает эффективность ингибиторов Bcr-Abl второго поколения.21 Мутации могут обнаруживаться за несколько месяцев до гематологического или цитогенетического рецидива при лечении иматинибом,19 и больные, у которых развиваются мутации, имеют особенно высокий риск рецидива заболевания или прогрессирования.19–20,22,23 Однако мутации также были обнаружены у пациентов со стабильной цитогенетической ремиссией.24,25 Больные, у которых мутации BCR-ABL были выявлены во время лечения иматинибом и у которых имеются какие-либо признаки утраты ответа или прогрессирования заболевания, должны начать терапию второй линии как можно раньше.
Результаты, представленные здесь, позволяют предположить, что более высокий уровень нечувствительности к дазатинибу в группах 2 и 3 по сравнению с группой 1 обусловлен механизмами резистентности, не связанными с мутациями BCR-ABL. Описаны несколько других возможных механизмов резистентности к иматинибу: повышенная экспрессия гена BCR-ABL вследствие амплификации, снижение внутриклеточной концентрации иматиниба, обусловленное связывающими белками плазмы, снижение транспорта препарата в клетку, увеличение транспорта препарата из клетки, снижение биодоступности препарата при приеме через рот и активация киназ семейства Src, таких как Lyn.5,26,27 Однако более высокая активность дазатиниба по сравнению с иматинибом и меньшее влияние транспортных белков на поступление дазатиниба в клетку, вероятно, позволяют преодолеть эти типы резистентности к иматинибу. Более вероятным механизмом является клональная эволюция (КЭ), т. е. возникновение дополнительных хромосомных аномалий в Ph-положительных клетках, что может привести к независимости от Bcr-Abl. КЭ была обнаружена с такой же частотой, как мутации BCR-ABL, у пациентов в поздней хронической фазе ХМЛ (после лечения ИФН) и с гематологической резистентностью к иматинибу.28 В отдельном анализе больных с поздней хронической фазой ХМЛ было обнаружено, что КЭ является независимым неблагоприятным прогностическим фактором гематологического рецидива (p 29 Утрата БЦО во время лечения иматинибом свидетельствует о том, что иматиниб более не обеспечивает эффективное подавление Bcr-Abl. Продолжение лечения иматинибом до утраты ПГО создает возможность накопления в лейкозных стволовых клетках дополнительных генетических изменений, что может привести к резистентности ко всем ингибиторам Bcr-Abl. В данном анализе не было данных об относительной частоте КЭ до лечения дазатинибом и это может стать интересным объектом дальнейших исследований. Различная эффективность дазатиниба также может объясняться другими неизвестными механизмами резистентности.
Часть пациентов, которые получали дазатиниб после утраты ПГО и не имели предшествующего БЦО (группа 3), достигли ПЦО или БМО, однако частота таких ответов была ниже, чем в других группах. У больных в группе 3 также были наименьшие показатели ВБТ и ОВ. В группе 3 на показатель выживаемости без отрицательных событий (бессобытийная выживаемость — БСВ), который был выше, чем этот показатель в группе 2 (утрата и большого цитогенетического, и полного гематологического ответов), может влиять определение событий в этом анализе, особенно утрата большого цитогенетического ответа. Гораздо меньшее число пациентов в группе 3 достигли БЦО и могли в последующем иметь такое событие, как его утрата, что может частично объяснять отсутствие корреляции с БСВ у этих больных. Возможно, что пациенты этой группы, которые не достигли БЦО на иматиниб, имеют биологические особенности заболевания, отличные от таковых у пациентов, которые достигли БЦО. Требуются дальнейшие исследования характеристик больных с разными типами первичной резистентности к иматинибу.
В целом результаты данного анализа позволяют предположить, что вероятность достижения ответа на дазатиниб и улучшение выживаемости без прогрессирования заболевания у пациентов, утративших чувствительность к иматинибу, выше в том случае, если они начали получать дазатиниб как можно раньше (с момента утраты БЦО). Очень важно регулярное наблюдение во время терапии иматинибом — это позволит своевременно выявить резистентность к данному препарату и получить наибольшие преимущества от альтернативного метода лечения.
Конфликты интересов
Финансирование клинических исследований, обсуждавшихся в этом отчете, статистический анализ и помощь в написании статьи предоставлены Bristol-Myers Squibb. Литература
Д-ра Cortes, O’Brien и Kantarjian получили поддержку от Bristol-Myers Squibb и Novartis.
Д-р Ravandi получил поддержку и гонорар от BristolMyers Squibb.
Д-р Borthakur является членом Speaker’s Bureau для Bristol-Myers Squibb и Novartis.
Д-ра Liu, Bleickardt и Chen являются работниками BristolMyers Squibb.
