Влияние фузафунгина на мукоцилиарный транспорт слизистой оболочки носа здоровых людей
СтатьиМ.В.Субботина, С.В.Дудкин
ГОУ ВПО Иркутский государственный медицинский университет Минздравсоцразвития
Полость носа - уникальная единая функционирующая система, обеспечивающая адаптацию и защищающая организм от неблагоприятных факторов внешней среды. Ведущая роль в этом принадлежит клеткам мерцательного эпителия слизистой оболочки, реснички которых колеблются синхронно 6-14 раз в минуту, перемещая покрывающий их слой слизи в сторону носоглотки. Ритмичная работа ресничек регулируется гуморальными механизмами, практически не координируется нервной системой и возможна даже вне организма [10]. Предполагают, что регуляция частоты их биения связана с мембранным потенциалом клетки [15]. Одним из обязательных условий нормального функционирования носовой полости является образование назального секрета. Он сложен по составу и является суммарным продуктом секреции бокаловидных клеток и желез собственного слоя слизистой оболочки, транссудации компонентов плазмы, метаболизма клеток мерцательного эпителия и вегетирующих микроорганизмов. Основу его составляет вода (95-97%). Электролиты (натрий, калий, кальций) присутствуют в носовой слизи в количестве 1-2% [10]. Содержание белка в норме 2-3%, но при инфекционных процессах его количество резко увеличивается. Обычно в назальном секрете обнаруживаются также клеточные элементы: нейтрофилы, лимфоциты, эозинофилы. При аллергическом рините число последних резко возрастает. Выявление мицелия помогает диагностировать грибковый процесс в полости носа. Носовая слизь у здорового человека обладает бактерицидным эффектом за счет содержания иммуноглобулинов и неспецифических факторов защиты: лизоцима, трансферрина, опсонинов и др. По физико-химической структуре назальный секрет представляет собой многокомпонентный коллоидный раствор с рН 7,4±0,3 и вязкостью 1,17±0,1 сСт, состоящий из двух фаз: более жидкой (золь) и гелеобразной. В растворимой фазе содержатся электролиты, сывороточные компоненты, белки, биологически активные вещества, ферменты и их ингибиторы. Гель имеет фибриллярную структуру и образуется преимущественно за счет местно синтезированных макромолекулярных гликопротеиновых комплексов муцинов, сцепленных дисульфидными мостиками [5]. Золь покрывает апикальные поверхности клеток. Именно в этом слое реснички мерцательного эпителия (рис. 1) совершают колебательные движения и передают свою кинетическую энергию наружному слою - гелю. Передвижение носового секрета эффективно только тогда, когда окончания ресничек контактируют с его поверхностью. Мукоцилиарный транспорт (МЦТ) является сложным процессом, в котором задействованы разные механизмы: частота биения ресничек, реологические свойства слизи. Скорость его у здорового человека колеблется от 4 до 20 мм/мин, в норме за сутки транспортируется до 100 мл назального секрета, который, попадая в глотку, проглатывается. Посторонние примеси, инфекционные агенты улавливаются и оседают на слизистой оболочке носа, обезвреживаются и элиминируются за счет колебаний ресничек. Частицы из внешней среды с диаметром более 8 мк почти полностью задерживаются в носу, только очень мелкие агенты (величиной 0,5 мк) удаляются при выдохе. Около 60% жизнеспособных микроорганизмов оседает на поверхности слизистой оболочки носа, обезвреживается и транспортируется в глотку [10]. Благодаря слаженной работе секреторных клеток мерцательного эпителия, желез собственного слоя слизистой оболочки, выделяющих необходимое количество секрета определенной вязкости, и двигательной активности ресничек обеспечивается постоянное очищение полости носа от чужеродных частиц, микроорганизмов, т.е. клиренс [18]. Наиболее распространенными способами оценки МЦТ у людей являются методы, в основе которых лежит определение скорости движения слизи из передних отделов носа в носоглотку, что зависит не только от функции мерцательного эпителия, но и от реологических свойств носового секрета. О деятельности ресничек судят по скорости перемещения вдоль поверхности слизистой оболочки носа в глотку разных веществ: угольной пыли, сахарина, полимерной растворимой пленки с метиленовым синим и др. В последнее время для оценки МЦТ стали применять микроскопию выделенных из организма и нативных клеток мерцательного эпителия, измеряя частоту биения ресничек с помощью компьютерных программ.
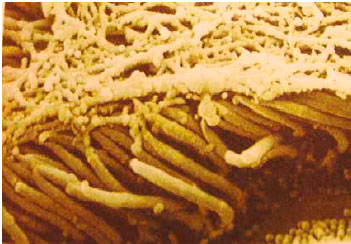
Рис. 1. Клетки мерцательного эпителия слизистой оболочки нижней носовой раковины человека с покрывающим их слоем слизи (х5700).
Причиной дисфункции слизистой оболочки носа является загрязнение воздуха пылью, газами, дымом. Кроме того, электронагреватели воздуха, батареи центрального отопления, кондиционеры способствуют распространению в окружающей человека среде мельчайших пылевых частиц, обитающих на них клещей и продуктов их жизнедеятельности. Холодный воздух зимой тоже способствует снижению местной иммунологической резистентности и очистительной способности мерцательного эпителия дыхательных путей. Избыточно сухой или влажный горячий воздух приводит к увеличению вязкости носового секрета и к блоку деятельности ресничек. При нарушении архитектоники полости носа, аномалиях бронхолегочных структур или врожденной патологии реснитчатого эпителия нормальная эвакуация слизи оказывается нарушенной изначально. Например, у больных муковисцидозом обнаружено снижение частоты биения ресничек, связанное с генетически детерминированными и фенотипически обусловленными дискриническими нарушениями и наследственным изменением функции хлорных каналов [14].
Вследствие дисфункции слизистой оболочки носа поллютанты задерживаются на ее поверхности, снижается текучесть назальной слизи. Клетки истощаются и высыхают, замедляется их регенерация. В результате этого реснички эпителия, совершая биения с прежней частотой, не могут сдвинуть с места поверхностный слой секрета. Застой его приводит к нарушению дыхательной функции носа и неизбежному инфицированию околоносовых пазух. Кроме того, у больных с сопутствующей патологией нижних дыхательных путей вязкий секрет, помимо угнетения цилиарной активности, может вызвать бронхиальную обструкцию. Таким образом, МЦТ является важнейшим механизмом самоочищения дыхательных путей, одним из основных механизмов системы местной защиты. Очищение носа от чужеродных частиц и микроорганизмов происходит благодаря движению ресничек в сторону носоглотки, последующему их проглатыванию и нейтрализации желудочным соком. Осевшие на слизистых оболочках нижних дыхательных путей микроорганизмы выводятся вместе с трахеобронхиальной слизью [20]. Если возбудителю удается преодолеть мукоцилиарный барьер, срабатывают неспецифические механизмы защиты -нейтрофилы и макрофаги, мигрирующие из кровеносного русла и способные уничтожать микроорганизмы путем фагоцитоза, за счет секреторной дегрануляции, продукции активных форм кислорода и оксида азота. В противовирусных реакциях принимают участие также естественные клетки-киллеры, располагающиеся в подслизистом слое и тесно связанные с внутриэпителиальными лимфоидными элементами. Иммунная защита слизистой оболочки обеспечивается также гуморальными факторами, среди которых наиболее важную роль играют синтезируемые в ответ на воздействие специфических антигенов секреторные иммуноглобулины [7].
Воспаление слизистых оболочек сопровождается, как правило, компенсаторным увеличением образования слизи. Изменяется состав носового секрета: уменьшается содержание воды и повышается концентрация муцинов (нейтральных и кислых гликопротеинов), что приводит к увеличению вязкости носовой слизи. Чем больше вязкость слизи, тем ниже скорость ее перемещения по дыхательным путям. Увеличение вязкости назального секрета способствует повышенной адгезии патогенных микроорганизмов на слизистых оболочках респираторного тракта, что создает благоприятные условия для их размножения. Параллельно с этим уменьшаются бактерицидные свойства носового секрета за счет снижения в нем концентрации секреторного IgA. Кроме того, инфекционные агенты, их токсины оказывают повреждающее действие на слизистые оболочки дыхательных путей. Присутствующие в дыхательных путях мукоидные штаммы микроорганизмов (синегнойной палочки и др.) повышают вязкость слизи за счет изменения соотношения кислых и нейтральных сиаломуцинов и продукции алгината [19]. Происходит не только нарушение вентиляции, но и снижение местной иммунологической защиты носовой полости с высоким риском развития затяжного или хронического воспалительного процесса [1, 3, 6]. Мерцательный эпителий, вынужденный работать длительное время в неблагоприятных условиях большого количества вязкого секрета, агрессивной микрофлоры, подвержен энергетическому истощению и функциональным нарушениям: уменьшению автоматизма, нарушению координации движений ресничек, что называют «усталостью ресничек» [15].
Острые респираторные заболевания (ОРЗ) - этиологически разнородная группа инфекционных болезней, характеризующаяся воспалением слизистых оболочек респираторного тракта. Она включает:
Заболеваемость ОРЗ составляет 18% среди взрослого населения. У детей она выше в 3,6 раза и составляет 69 000 на 100 000 детей до 14 лет [13]. ОРЗ - наиболее частая инфекционная патология детского возраста. Затраты на лечение 1 случая колеблются от 450 до 3000 и более рублей.
К числу основных факторов патогенеза воспалительных респираторных заболеваний относится нарушение механизма МЦТ. При этом перистальтические движения мелких бронхов и биение ресничек эпителия не могут обеспечить адекватный дренаж верхних и нижних дыхательных путей.
Несмотря на высокую контагиозность вирусной инфекции, некоторые люди не заболевают ею. У них, помимо МЦТ, хорошо работают другие естественные механизмы защиты, к которым относят: рефлексы кашля и чиханья, лимфоидную ткань дыхательных путей, ферменты и иммуноглобулины слизистых оболочек (рис. 2).
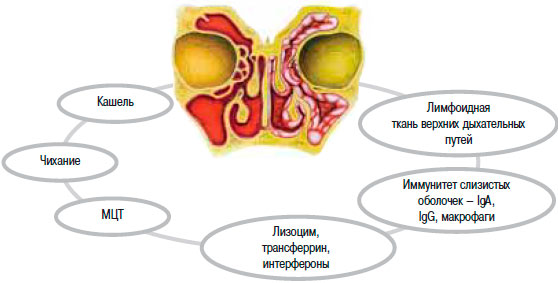
Рис. 2. Механизмы защиты дыхательных путей.
Для лечения ринитов имеется большой выбор безрецептурных эндоназальных лекарственных средств, но недостаточно изучено их влияние на состояние МЦТ. Среди лекарственных средств мало таких, которые нормализуют двигательную активность мерцательного эпителия и которые можно было бы применять профилактически при эпидемиях вирусных инфекций. Стимулируют МЦТ за счет увеличения частоты биения ресничек клеток эпителия β2-агонисты [15].
Местные эндоназальные и эндоларингеальные антимикробные препараты назначаются в виде спреев, инсуффляций, ингаляций. Главными требованиями к наносимым на слизистую оболочку лекарственным средствам являются:
Многочисленные работы, проводимые за рубежом и в нашей стране, показали, что средством, удовлетворяющим всем этим требованиям, является фузафунгин [1-3, 7, 8, 16]. Являясь ингаляционным антибиотиком, выделяемым Fusarium lateritium (штамм 437), фузафунгин (Биопарокс), выпускаемый в форме дозированного аэрозоля, используется в терапии острых ринитов, фарингитов, ларингитов и бронхитов уже около 30 лет. Благодаря малому размеру аэрозольных частиц фузафунгин способен проникать в самые дальние и труднодоступные отделы респираторного тракта - в околоносовые пазухи, мелкие бронхи. Спектр антимикробной активности фузафунгина охватывает флору, чаще всего являющуюся возбудителем инфекций верхних дыхательных путей: стрептококки, стафилококки (в том числе метициллин-устойчивые штаммы), Haemofillus influenzae, Legionella pneumoniae, а также Mycoplasma pneumoniae и Candida albicans, что позволяет снизить риск развития вторичного кандидоза. При использовании фузафунгина не наблюдается приобретенная и перекрестная устойчивость к другим препаратам. Резистентность к фузафунгину у бактерий почти не развивается [8]. Помимо антибактериальных свойств, фузафунгин обладает собственным противовоспалительным действием [7, 16], которое было продемонстрировано в эксперименте. Установлена его способность усиливать фагоцитоз, ингибировать способность бактерий к адгезии, снижать синтез провоспалительных цитокинов (интерлейкина-1, фактора некроза опухоли-α) в пораженном участке, что снимает симптомы воспаления без использования дополнительных противовоспалительных препаратов [11, 12].
Наряду с тем, что фузафунгин особенно эффективен в терапии острого ринита и фарингита, его можно применять и для лечения хронических аденоидитов у детей [2], а также в послеоперационном периоде после ринологических вмешательств [9].
На фоне применения фузафунгина происходит нормализация МЦТ слизистой оболочки ЛОР-органов, что позволяет быстро купировать жалобы больных и воспалительный процесс на ранней стадии, предупредить присоединение вторичной бактериальной инфекции и ее распространение на нижележащие отделы респираторного тракта [7, 8]. Возможно ли применение фузафунгина в качестве средства профилактики при ОРЗ? Как влияет препарат на естественные защитные механизмы носовой полости? Ответ на эти вопросы можно получить, изучив влияние фузафунгина на МЦТ слизистой оболочки носа здоровых людей как одного из важнейших критериев оценки защитной функции носа.
Целью нашего исследования явилось изучение влияния препарата Биопарокс на двигательную активность мерцательного эпителия носовой полости здоровых людей. Исследование выполнено на кафедре оториноларингологии Иркутского государственного медицинского университета.
Материалы и методы
Дизайн исследования
В данное проспективное несравнительное моноцентровое открытое исследование были включены 32 здоровых добровольца [12 (37%) мужчин и 20 (63%) женщин], средний возраст которых составил 20,5±0,5 года. Всем исследуемым был проведен предварительный оториноларингологический осмотр для выявления патологии верхних дыхательных путей. Оценку влияния фузафунгина на МЦТ слизистой оболочки носовой полости проводили с помощью сахаринового теста (СТ), используя пищевой сахарин GMBH («Hergestell», Германия) по общепринятой в международной практике методике (D.Proctor, 1983) при температуре в помещении 22-23°С. Сахарин наносили на слизистую оболочку носа в области нижней носовой раковины, отступая от ее переднего конца 1 см (рис. 3), отмечали время до появления сладкого вкуса во рту.
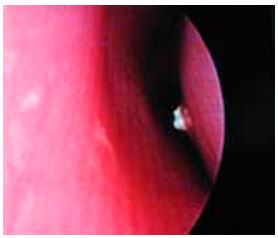
Рис. 3. Сахарин нанесен на слизистую оболочку левой нижней носовой раковины.
Таким образом, определяли изначальную транспортную функцию мерцательного эпителия носовой полости обследуемых добровольцев. После этого все они однократно получали препарат Биопарокс по 4 дозы (0,5 мг) в каждый носовой ход. СТ проводили повторно через 30 мин после использования аэрозоля.
Критерии включения добровольцев в исследование:
В исследование не включали добровольцев:
Определение влияния препарата фузафунгин на мукоцилиарный клиренс слизистой оболочки носа здоровых людей
Оценивали величину СТ до и после применения фузафунгина, эти показатели сравнивали между собой и с нормой, величину которой считали до 15-20 мин (по классификации Б.ВШеврыгина, 1985 г.).
Статистическую обработку результатов (достоверность различий) проводили с помощью t-критерия Стьюдента [4].
Результаты исследования
Все обследуемые соответствовали критериям включения. До эндоназального применения фузафунгина у всех добровольцев состояние МЦТ соответствовало норме: СТ был равен 5-17 мин (в среднем 14,43±3,3 мин). Через 30 мин после применения фузафунгина в дозе 0,5 мг в каждую половину носа он составил 14,36±4,8 мин. Выявленные различия между полученными значениями СТ у здоровых людей обоих полов до и после применения препарата фузафунгин не были достоверными (p>0,05). У 3 обследуемых зарегистрировано небольшое жжение в носу на фоне использования препарата, купировавшееся самостоятельно. Аллергических реакций не отмечалось. Результаты представлены на рис. 4.
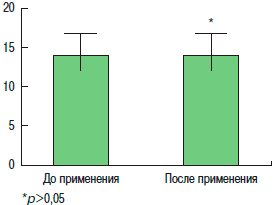
Рис. 4. Результаты СТ до и после применения препарата Биопарокс у здоровых добровольцев.
Заключение
Эндоназальное использование препарата фузафунгин не изменяет нормальную деятельность мерцательного эпителия слизистой оболочки носа здоровых людей. Таким образом, фузафунгин является безопасным препаратом в отношении основного механизма защиты верхних дыхательных путей - МЦТ, способствуя его сохранению.
ЛИТЕРАТУРА
1. Балясинская ГЛ. Биопарокс, лечение заболеваний ЛОР-органов у детей. Практические рекомендации по материалам VIII съезда педиатров России. М.: Пресса, 1998.
2. Бойко НВ. Применение Биопарокса в лечении аденоидита у детей и взрослых. Респир. забол. 2001; 1: 4-5.
3. Гаращенко ТИ., Богомильский МР. Рациональная антибиотикотерапия острых синуситов и тонзиллофарингитов у детей как профилактика осложнений. Актуальные вопросы оториноларингологии детского возраста и фармакотерапии болезней ЛОР-органов. Сб. трудов. М., 2001; с. 183-7.
4. Гублер В.В. Вычислительные методы анализа и распознавание патологических процессов. Л.: Медицина, 1978; с. 68-91.
5. Зайцева ОВ. Муколитические препараты в терапии болезней органов дыхания у детей: современный взгляд на проблему. РМЖ. 2003; 11 (1): 49-54.
6. Захарова ГП., Шабалин ВВ., Лащов А.А Современные методы оценки нарушений мукоцилиарного транспорта в диагностике хронических риносинуситов. Вестн. оториноларингол. 1998; 4:53-5.
7. Лучихин Л.А. Рациональные подходы к лечению и профилактике респираторных инфекций. Consilium Medicum. 2003; 5 (2).
8. Никифорова ГН., Свистушкин ВМ. Преимущества местной терапии при лечении инфекций верхних дыхательных путей. Консилиум провизориум. 2001; 1 (4).
9. Носуля ЕВ. и др. Клиническая эффективность применения Биопарокса после рино-хирургических вмешательств. Рос.ринол. 2001; 3: 17-21.
10. Пискунов Г.З., Прискунов СЗ. Клиническая ринология. М.: Миклош, 2002.
11. Полевщиков АВ., Рязанцев СВ. Механизмы высокой антибактериальной эффективности Биопарокса. Нов. отриноларингол. и логопатол. 2000; 1: 103-5.
12. Рязанцев В.С. Применение ингаляционного антибиотика Биопарокса в оториноларингологии. Нов. оториноларингол. и логопатол. 1997; 3:41-3.
13. Таточенко ВК. Антибактериальная терапия заболеваний дыхательных путей у детей. Консилиум. 2001; с. 3-5.
14. Черменский АГ. и др. Изучение функции реснитчатого эпителия у больных муковисцидозом и хронической обструктивной болезнью легких. Пульмонология. 2001; 3: 53-57.
15. Donovan BY, Lid В, Wong HuaMao. Mucociliary dysfunction: real and potential pathogenic mechanisms in mucus, ciliary activity and mucociliary interaction. Pediatr Pulmonol 1997; Suppl 14: 108.
16. Ghaem A, Harpey G. Assessment of fusafungine anti-inflammatory activity by rhinomanometry. Rhinology 1988; 5: 63-8.
17. Proctor DF. Nasal mucous transport and our ambient air. Laryngoscope 1983; 93 (1): 58-62.
18. Puchelle G et al Comparison of three methods for measuring nasal mucocilliary clearance in man. Acta Otolaryngol 1981; 91; 3 (4): 297-303.
19. Seybold ZV et al Impairment of airway mucocilliary transport by Pseudomonas aeruginosa products. Am Rev Respir Dis 1992; 146: 1173-6.
20. Wanner A, Salathe M, O'Riordan ТО. Mucocillyary clearance in the airways. Am J Respir Crit Care Med 1996; 154: 1868-902.
