Вторичная профилактика сердечно-сосудистых осложнений у больного гипертоническим нефритом
СтатьиОпубликовано в журнале:
Клиническая фармакология и терапия, 2006, 15 (4)
С.В.Моисеев, В.В.Фомин
Кафедра терапии и профзаболеваний ММА им. И.М.Сеченова
Больной В., 54 лет, инженер. В возрасте 45 лет после ангины появились отеки век. При амбулаторном обследовании выявлено повышение АД до 150/95 мм рт. ст., в анализе мочи белок 0,99 г/л, единичные лейкоциты в поле зрения. Диагностирован хронический пиелонефрит. В течение нескольких дней получал уросептик. В дальнейшем самочувствие оставалось удовлетворительным. Периодически беспокоили головные боли, повышение АД до 150-160/90-100 мм рт. ст., в связи с чем нерегулярно принимал клофелин. Состояние ухудшилось 2 года назад. С этого времени стойкая артериальная гипертония (АД 170-180/100-110 мм рт. ст.). Врач поликлиники диагностировал гипертоническую болезнь и назначил нифедипин по 20 мг два раза в день и атенолол 100 мг/сут. На фоне приема двух препаратов АД несколько снизилось, однако эффект был нестойким. Год назад впервые обследован в клинике.
При осмотре АД 175/110 мм рт. ст., частота сердечных сокращений 72 в минуту. В моче белок 1,9 г/сут. Уровень альбумина в сыворотке 4,5 г/сут. Обращало на себя внимание увеличение сывороточного уровня креатинина до 1,9 мг/дл и снижение скорости клубочковой фильтрации до 54 мл/мин. При ультразвуковом исследовании изменений чашечно-лоханочной системы не выявлено, почки несколько уменьшены в размерах. Диагностирован хронический гломерулонефрит с начальными проявлениями хронической почечной недостаточности. Начата терапия спираприлом (Квадроприлом) в дозе 6 мг один раз в сутки. Нифедипин короткого действия заменен на амлодипин в дозе 10 мг/сут.
Таким образом, ведущими проявлениями хронического гломерулонефрита были стойкая артериальная гипертония и небольшая протеинурия. В таких случаях дифференциальный диагноз в первую очередь проводят с гипертонической болезнью, которая сама по себе приводит к поражению почек (гипертоническому нефроангиосклерозу), сопровождающемуся нарушением их функции. Важное диагностическое значение имеет изучение анамнеза. При эссенциальной гипертонии изменения в моче обычно появляются спустя много лет после начала болезни, в то время как у нашего больного протеинурия предшествовала развитию стойкой гипертонии, поэтому диагноз хронического гломерулонефрита не вызывал сомнения. В пользу его свидетельствовала также достаточно высокая протеинурия.
Основой лечения хронического гломерулонефрита являются иммуносупрессивные средства, которые позволяют подавить активность нефропатии и предупредить необратимое ухудшение функции почек. Однако в данном случае их применение не имело смысла, так как у больного имелись признаки почечной недостаточности (повышение сывороточного уровня креатинина и снижение скорости клубочковой фильтрации), а при ультразвуковом исследовании выявлено уменьшение размеров почек. Указанные изменения свидетельствовали о наличии необратимого поражения почек, характеризующегося преобладанием фиброза почечной ткани. В этой ситуации основная цель лечения - профилактика прогрессирования почечной недостаточности путем воздействия на неиммунные механизмы развития хронического гломерулонефрита [1]:
- величина и длительность протеинурии;
- артериальная гипертония;
- гемодинамические нарушения в почках, проявляющиеся повышенной перфузией почечных клубочков с развитием гломерулярной гипертонии и гиперфильтрации;
- метаболические нарушения.
Наиболее важное значение имеет адекватный контроль АД, которое желательно снижать до нормальных значений. Следует отметить, что протеинурию сегодня рассматривают не только как симптом нефропатии, но и как фактор, способствующий ее прогрессированию. Экскретируемые с мочой белки, прежде всего альбумин, непосредственно индуцируют процессы фиброгенеза в почечной ткани, особенно в тубулоинтерстиции. Соответственно, препараты, обладающие антипротеинурическим действием, могут замедлить ухудшение функции почек.
Ведущее значение в процессе ремоделирования почек ткани придают гемодинамическим и негемодинамическим эффектам ангиотензина II, которые реализуются в основном через AT1-рецепторы (табл. 1). Внутриклубочковая гипертония и активация фиброгенных факторов вызывают нарастание фиброза и способствуют развитию и прогрессированию почечной недостаточности. Указанные эффекты ангиотензина II могут быть блокированы с помощью ингибиторов ангиотензинпревращающего фермента (АПФ), нефропротективные свойства которых подтверждены в контролируемых клинических исследованиях. В двойное слепое исследование REIN были включены 352 больных с хроническими недиабетическими заболеваниями почек, которых разделили на 2 когорты в зависимости от исходной протеинурии: 1-3 г/сут и >3 г/сут (т.е. нефротического уровня). Рандомизированным больным назначали ингибитор АПФ или плацебо. При лечении ингибитором АПФ были достоверно ниже темп снижения скорости клубочковой фильтрации (0,53 и 0,88 мл/мин/мес соответственно) и риск удвоения уровня креатинина или развития терминальной стадии почечной недостаточности (18 и 40%). Нефропротективная эффективность ингибитора АПФ оказалась более выраженной у больных с протеинурией более 3 г/сут, у которых лечение привело к уменьшению экскреции белка с мочой [2]. Таким образом, ингибиторы АПФ являются средствами выбора в лечении артериальной гипертонии у больных с нефропатией.
Таблица 1. Неблагоприятные эффекты ангиотензина II при нефропатиях
| Гемодинамические | Негемодинамические |
| Вазоконстрикция Ухудшение почечного кровотока Повышение внутриклубочкового давления | Увеличение реабсорбции натрия и воды Секреция альдостерона Активация экстрацеллюлярного матрикса Увеличение экспрессии трансформирующего фактора роста β Повышение уровня ингибитора активатора плазминогена 1-го типа |
Пациенту был назначен спираприл (Квадроприл) в дозе 6 мг один раз в сутки. Особенностью этого ингибитора АПФ является длительный период полувыведения (40 ч), который является максимальным среди современных антигипертензивных препаратов. Благодаря этому спираприл дает стойкий антигипертензивный эффект при однократном приеме. Другой особенностью препарата является двойной путь выведения (почками и печенью), что повышает его безопасность при нарушении функции почек. Эффективность и безопасность спираприла были продемонстрированы в российском исследовании КВАДРИГА, в которое были включены 235 больных артериальной гипертонией (в возрасте в среднем 51 год). Лечение продолжали в течение 12 недель. У половины пациентов к спираприлу (6 мг/сут) был добавлен гидрохлортиазид. В результате терапии АД снизилось в среднем со 160/98 до 133/83 мм рт. ст. (р<0,01) (рис. 1). При суточном мониторировании АД наблюдалось достоверное снижение суточного, дневного и ночного АД. Частота нежелательных явлений составила 8,7%, ни в одном случае отмены препарата не потребовалось. У больных почечной гипертонией монотерапия обычно недостаточно эффективна, поэтому ингибиторы АПФ часто сочетают с пролонгированными антагонистами кальция.
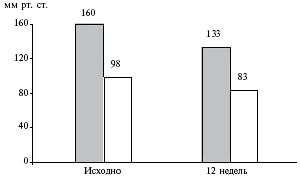
Рис. 1. Снижение систолического и диастолического АД в результате 12-недельной терапии спираприлом в дозе 6 мг/сут (±гидрохлортиазидом) в исследовании КВАДРИГА
После выписки состояние больного оставалось удовлетворительным. В результате терапии спираприлом и амлодипином АД снизилось до 130-140/90 мм рт. ст., а протеинурия - до 0,99 г/л. Сывороточный уровень креатинина оставался стабильным (1,6-1,7 мг/дл). Спустя 3 месяца после выписки начали беспокоить боли в области сердца при физической нагрузке, расцененные как стенокардия. При амбулаторном обследовании в клинике обращали на себя внимание повышение уровня общего холестерина до 280 мг/дл и холестерина липопротеидов низкой плотности до 132 мг/дл, в связи с чем к терапии добавлен симвастатин (Зорстат) в дозе 10 мг/сут.
Помимо основных факторов риска (возраст, мужской пол, артериальная гипертония) развитию коронарной болезни сердца способствовало нарушение функции почек. В когортном исследование (Rotterdam Study), начатом в 1990 году, изучались факторы риска сердечно-сосудистых болезней у 4484 пациентов, у половины из которых имелась легкая почечная недостаточность [3]. В течение 8,6 лет у 218 (4,9%) пациентов развился инфаркт миокарда. Снижение скорости клубочковой фильтрации (СКФ) на каждые 10 мл/мин/1,73 м2 ассоциировалось с увеличением риска инфаркта миокарда на 32%. Целесообразность применения статинов с целью вторичной профилактики у больных коронарной болезнью сердца была доказана еще в 1994 году в исследовании Scandinavian Simvastatin Survival Study (4S) [4]. В это исследование были включены 4444 больных стенокардией или перенесенным инфарктом миокарда и повышенным сывороточным уровнем холестерина, которые в течение 5,4 лет получали симвастатин или плацебо. В результате терапии сывороточные уровни общего холестерина и холестерина ЛНП снизились на 25 и 35% соответственно. Гиполипидемический эффект сопровождался снижением общей смертности на 30% (р=0,0003), сердечно-сосудистой смертности на 42% и риска развития основных сердечно-сосудистых исходов на 34% (р<0,00001) (рис. 2).

Рис. 2. Снижение риска (%) различных исходов при лечении симвастатином в исследовании 4S
Результаты лечения симвастатином были сопоставимыми у мужчин и женщин, а также пациентов в возрасте старше 60 лет. В последующие годы эффективность статинов во вторичной профилактике была доказана и у больных с пограничными или "нормальными" уровнями холестерина. В рекомендациях Европейского общества кардиологов по лечению стабильной стенокардии (2006 г.) их предлагается назначать всем таким пациентам. В настоящее время возможности применения статинов расширились благодаря появлению дженериков, например, Зорстата, который по эффективности и безопасности не уступает оригинальному симвастатину. Целевой уровень холестерина ЛНП у больных коронарной болезнью сердца составляет 100 мг/дл. Как указано выше, в исследовании 4S симвастатин снижал его примерно на треть. Соответственно, у нашего пациента, у которого уровень холестерина ЛНП равнялся 132 мг/дл, применение симвастатина было вполне оправданным. Лечение обычно начинают с дозы 10 мг/сут, которую при необходимости увеличивают до 20-40 мг/сут и более. Доводом в пользу назначения симвастатина обследованному пациенту являются и нефропротективные свойства статинов, обусловленные различными механизмами (прямое противовоспалительное действие, улучшение функции эндотелия, антипротеинурический эффект и т.д.).
В результате диетотерапии и терапии Зорстатом в дозе 10 мг/сут уровни общего холестерина и холестерина ЛНП нормализовались. Ухудшение состояния больного в течение последних 2 месяцев: беспокоила нарастающая одышка, появились отеки ног, сохранялись приступы стенокардии. При осмотре небольшое увеличение печени, частота сердечных сокращений 85 в минуту, АД 135/85 мм рт. ст. При рентгенографии грудной клетки определялось усиление интерстициального легочного рисунка. При эхокардиографии выявлены дилатация камер сердца (диастолический размер левого желудочка 6,2 см) и снижение фракции выброса левого желудочка (36%). К терапии были добавлены фуросемид в дозе 40 мг два раза в неделю и карведилол (Карветренд) в дозе 3,125 мг два раза в сутки, которую постепенно увеличили до 25 мг два раза в сутки.
Хроническая сердечная недостаточность является одним из основных осложнений артериальной гипертонии и коронарного атеросклероза. Ведущую роль в ее развитии играет активация нейрогуморальных систем — ренин-ангиотензиновой и симпато-адреналовой. В связи с этим основой лечения сердечной недостаточности сегодня являются ингибиторы АПФ и β-адреноблокаторы. Первые рекомендуют назначать всем больным, в том числе с бессимптомной дисфункцией левого желудочка после инфаркта миокарда (снижение фракции выброса, которое можно выявить с помощью эхокардиографии). Карведилол — это неселективный β-адреноблокатор, который одновременно блокирует α1-адренорецепторы, а также обладает антиоксидантной и антипролиферативной активностью [5]. Благоприятное влияние карведилола на выживаемость больных сердечной недостаточностью было продемонстрировано еще 10 лет назад в американской программе исследований (n=1094) [6]. Во время исследования стандартная терапия дигоксином, диуретиками и ингибиторами АПФ оставалась постоянной. Длительность наблюдения достигала 12 мес. Общая смертность в группе карведилола снизилась более чем в два раза по сравнению с плацебо (с 7,8 до 3,2%; р<0,001). Кроме того, было продемонстрировано снижение риска госпитализаций по сердечно-сосудистым причинам на 27% (р=0,036), а также суммарного риска госпитализации или смерти и прогрессирования сердечной недостаточности.
Эффективность карведилола при тяжелой сердечной недостаточности была подтверждена в исследовании COPERNICUS, в которое были включены 2289 пациентов с фракцией выброса левого желудочка менее 25% [7]. Длительность терапии карведилол ом (целевая доза 25 мг два раза в сутки) или плацебо составляла в среднем 10,4 мес. В группе карведилола риск смерти от любых причин снизился на 35% (р=0,00013) (рис. 3), а смерти или госпитализации — на 24% (р<0,001). Результаты лечения были сопоставимыми в различных подгруппах больных, в том числе с недавно развившейся декомпенсацией сердечной недостаточности. Благоприятный эффект карведилола проявлялся уже в первые несколько недель после начала лечения.
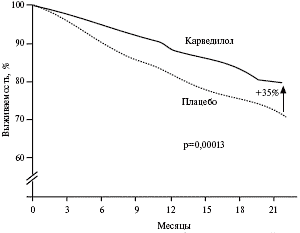
Рис. 3. Увеличение выживаемости больных тяжелой сердечной недостаточностью при лечении карведилолом в исследовании COPERNICUS
Врачи пока недостаточно широко используют β-адреноблокаторы у больных сердечной недостаточностью, особенно если они уже принимают ингибиторы АПФ. Целесообразность комбинированной терапии препаратами двух групп специально изучалась в исследовании CARMEN у 572 больных легкой сердечной недостаточностью [8]. После рандомизации больным назначали карведилол, эналаприл или их комбинацию. Первичной конечной точкой было ремоделирование левого желудочка, которое оценивали с помощью эхокардиографии через 6, 12 и 18 мес. Комбинированная терапия карведилолом и эналаприлом привела к достоверному снижению индекса конечного столического объема левого желудочка на 5,4 мл/м2 по сравнению с монотерапией эналаприлом (р=0,0015) (рис. 4). При монотерапии карведилолом этот показатель снизился на 2,8 мл/м2 (р=0,018), а при лечении одним эналаприлом не изменился. Таким образом, в этом исследовании карведилол вызывал регресс ремоделирования левого желудочка, в то время как эналаприл только задерживал прогрессирование его дисфункции. Комбинированная терапия двумя препаратами имела преимущество перед монотерапией эналаприлом.
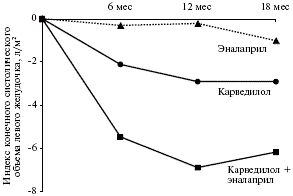
Рис. 4. Регресс ремоделирования левого желудочка при лечении карведилолом и/или эналаприлом в исследовании CARMEN
При сердечной недостаточности доказана эффективность не только карведилола, но и кардиоселективных β-адреноблокаторов - метопролола и бисопролола. Соответственно, возникает вопрос о том, какому препарату следует отдавать предпочтение. В исследовании COMET у 3029 больных сердечной недостаточностью и дисфункцией левого желудочка были сопоставлены результаты терапии карведилолом (25 мг два раза в сутки) и метопролола тартратом (50 мг два раза в сутки) [9]. При лечении карведилолом относительный риск смерти был на 17% ниже, чем в группе метопролола (р=0,0017) (рис. 5), а риск смерти от сердечно-сосудистых причин - на 20% ниже (р=0,0004). Частота госпитализаций и прогрессирования сердечной недостаточности достоверно не отличалась между двумя группами. Таким образом, карведилол по эффективности в лечении сердечной недостаточности превосходил метопролола тартрат. Лечение β-адреноблокаторами у больных сердечной недостаточностью следует начинать осторожно с минимальных доз. Например, карведилол назначают в дозе 3,125-6,25 мг два раза в сутки. Однако в последующем дозу следует постепенно увеличивать под контролем частоты сердечных сокращений. Критерием эффективности β-блокады является ее снижение по крайней мере на 25%.
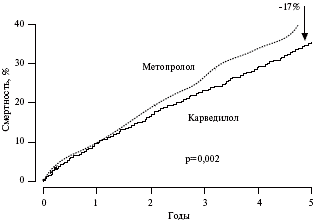
Рис. 5. Общая смертность при лечении карведилолом и метопролола тартратом в исследовании COMET
Представленное наблюдение достаточно типично. Благодаря улучшению результатов лечения нефропатий и увеличению выживаемости больных их прогноз нередко определяется сердечно-сосудистыми осложнениями, риск развития которых увеличивается при нарушении функции почек. В этих условиях возрастает роль современных стратегий профилактики сердечно-сосудистых исходов.
Литература
Квадроприл® - Досье препарата


