Роль фактора роста плаценты в прогнозе развития тяжелых
СтатьиРОССИЙСКИЙ ВЕСТНИК АКУШЕРА-ГИНЕКОЛОГА 1, 2012
К.м.н., доц. И.В. Савельева1, д.м.н., проф. С.В. Баринов2, к.м.н. Е.В. Рогова2
1Кафедра акушерства и гинекологии №1 (зав. — доц. И.В. Савельева), 2кафедра акушерства и гинекологии №2 (зав. — проф. С.В. Баринов) Омской государственной медицинской академии
С целью изучения значения показателей фактора роста плаценты (PlGF) в прогнозе развития тяжелых гестационных осложнений обследованы 89 беременных с метаболическим синдромом (МС) в I триместре беременности в сроке 8—9 нед. Контрольную группу составили 25 здоровых беременных. Установлено, что критическим значением PlGF в прогнозе развития тяжелой преэклампсии у беременных с МС является его уровень ниже 100 пг/мл. Для оценки лечебно-профилактических мероприятий была создана группа сравнения, в которую вошли 25 пациенток с МС и низким уровнем PlGF в сыворотке крови. Показано, что уровень PlGF ниже 100 пг/мл в сыворотке крови беременных с МС свидетельствует о высоком риске развития преэклампсии и отслойки плаценты. В комплекс программ профилактики развития тяжелой преэклампсии у беременных с МС должны быть включены ангиопротекторы, одним из которых является фле-бодиа 600.
Ключевые слова: беременные с метаболическим синдромом, фактор роста плаценты, прогноз и профилактика преэклампсии, флебодиа 600.
- Role of placental growth factor in the prediction of severe gestational complications in pregnant women with metabolic syndrome
I.V. Savelyeva, S.V. Barinov, E.V. Rogova - To study the values of placental growth factors (PlGF) to predict the development of severe gestational complications, 89 pregnant women with metabolic syndrome (MS) were examined in the first trimester of pregnancy at 8-9 weeks' gestation. A control group consisted of 25 healthy pregnant women. The critical value of PlGF in predicting the development of severe preeclampsia in pregnant women with MS was found to be its level below 100 pg/ml. A comparison group of 25 patients with MS and low serum PlGF levels was formed to assess therapeutic and preventive measures. Serum PlGF levels of under 100 pg/ml in pregnant women with MS suggest a high risk for preeclampsia and placental abruption. A package of severe preeclampsia prevention programs in pregnant women with MS must include angioprotectors, one of which is phlebodia 600.
- Key words: pregnant women with metabolic syndrome; placental growth factor; prognosis and prevention of preeclampsia; phlebodia 600.
Плацентарный фактор роста (PlGF) относится к семейству сосудисто-эндотелиального фактора роста (VEGF) и является одним из важнейших регуляторов формирования плаценты и васкуляризации ее ворсин [4]. В 1991 г. в Институте генетики и биофизики в Италии PlGF впервые был выделен из плаценты чистом виде [9]. Позже M. Persiko [3] установлена структура данного фактора. В целом, отсутствие PlGF не влияет на развитие взрослого организма и его способность к репродукции. Однако у мышей, в организме у которых не формируется PlGF, отмечены выраженные нарушения ангиогенеза [7]. Достаточно интересным является факт значительного снижения плотности сосудистой сети в подкожной жировой клетчатке у мышей с отсутствием гена PlGF [8].
Метаболический синдром (МС) у беременных в настоящее время является не только медицинской, но и одной из важнейших социальных проблем и определяется как комплекс метаболических, гормональных и клинических нарушений, в основе которых лежит инсулинорезистентность (ИР), компенсаторная гиперинсулинемия и абдоминальное ожирение. Результаты проведенных популяционных и эпидемиологических исследований установили выраженную связь между ожирением и другими компонентами МС. Кроме того, ожирение может выступать в роли фактора, инициирующего его проявление. Согласно отчету Американской ассоциации заболеваний сердца в 2004 г., патогенез МС в первую очередь связан с ожирением и патологическим распределением жировой ткани, а не с инсулинорезистентностью. Установлено, что чувствительность к инсулину снижается при увеличении количества жира в организме, при нормальной массе ИР не проявляется [5, 6].
Учитывая отсутствие в доступной литературе сведений об участии фактора роста плаценты в становлении ангиогенеза системы мать—плацента—плод у беременных с МС при наличии абдоминального ожирения.
Целью настоящего исследования — изучение абсолютных показателей PlGF у беременных с метаболическим синдромом, формирование групп риска возникновения тяжелых гестационных осложнений.
Материал и методы
Под наблюдением находились 89 беременных с МС (основная группа). Критерии включения беременных в исследование определялись согласно классификации ВОЗ [10]. Контрольную группу составили 25 здоровых беременных. Анализ клинико-анамнестических данных показал, что указанные группы репрезентативны. Всем пациенткам проводились общий осмотр, включая параметры роста, массы тела, вычислялся индекс массы тела (индекс Кетле), при этом прибавка массы тела за беременность не учитывалась. С целью оценки липидного спектра крови определяли содержание общего холестерина, триглицеридов, липопротеидов высокой и низкой плотности. Для вычисления индекса Caro — отношение концентрации глюкозы в крови (моль/л) к уровню инсулина (мкЕД/ мл) — и диагностики инсулинорезистентности определяли уровень глюкозы и инсулина в плазме крови. Для измерения уровня человеческого PlGF (пг/мл) в сыворотке крови беременных использовали иммунологический метод Quantikine Human PlGF, основанный на применении твердофазного иммуноферментного анализа (ИФА). Учитывая, что в настоящее время все больше исследователей [1] считают временем формирования основы тяжелых гестационных осложнений момент миграции цитотрофобласта (когда происходит торможение миграции трофобласта в спиральные артерии матки и формируется недостаточность второй волны инвазии цитотрофобласта), ИФА PlGF проводили в I триместре беременности в сроке 8—9 нед гестации.
Статистическая обработка данных проводилась с применением интегральной системы для комплексного статистического анализа и обработки данных STATISTICA 6.0 и Microsoft Excel. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05. Для расчета достоверности различий в группах применялись непараметрические критерии (Манна— Уитни, Вилкоксона, ранговый коэффициент корреляции Спирмена).
Результаты и обсуждение
За последние годы в научно-исследовательских работах появились данные о возможном прогнозировании преэклампсии в ранние сроки беременности, учитывая гипотезу эндотелиальной дисфункции, на основе изучения факторов роста. В этой связи придают большое значение эндотелиальному фактору роста (VEGF), высокое содержание которого обеспечивает расширение сосудов, низкое — сужение.
Проведенный клинический анализ течения беременности у пациенток с метаболическим синдромом свидетельствовал о развитии преэклампсии различной степени тяжести у 67 (75,3±0,43%) обследованных. Тяжелая преэклампсия (МКБ-10 014.1) имела место у 12 беременных — в 17,9±0,38% наблюдений. При этом обнаружено, что у 47 (52,8±0,50%) пациенток основной группы отмечалось раннее начало указанного осложнения гестации — в 26— 27 нед беременности, при этом регистрировались отеки голеней, а впоследствии присоединялись протеинурия и гипертензия. В контрольной группе это осложнение беременности, протекающее в легкой форме, имело место в 16,0±0,37% случаях.
Учитывая вышеизложенное, в частности, высокий процент (67,2%) раннего начала преэклампсии у беременных с МС, нам представилось возможным выявить патогенетические взаимосвязи между уровнем PlGF и развитием преэклампсии при МС у пациенток. При анализе уровней человеческого PlGF в сыворотке крови беременных основной и контрольной групп оказалось, что у беременных с МС уровень P1GF достоверно ниже (р<0,01), чем у беременных контрольной группы (соответственно 101,2±96,6 и 275,0±126,5 пг/мл) (рис. 1). Данный факт может свидетельствовать о нарушении процессов инвазии ворсин хориона и формировании недостаточности второй волны инвазии трофобласта в условиях низкого уровня PlGF в I триместре беременности.
Рис. 1. Уровень PlGF в сыворотке крови беременных обследованных групп (р<0,05).

В ходе проведенного исследования беременные основной группы были разделены на две подгруппы: с высоким уровнем PlGF (n=26; 256±130,5 пг/мл) и низким уровнем PlGF (n=63; 56,3±32,9 пг/мл). По нашим данным, критическим значением PlGF в прогнозе развития тяжелой преэклампсии у беременных с МС является его уровень ниже 100 пг/мл: при анализе корреляционной зависимости низкого уровня PlGF (ниже 100 пг/мл) и развития тяжелой преэклампсии выявлена связь средней силы (г=0,43) (рис. 2). В группе с высоким уровнем PlGF наблюдались только легкие формы преэклампсии.
Рис. 2. Корреляционная связь развития преэклампсии и низкого уровня P1GF (<100 пг/мл) у беременных с метаболическим синдромом (r =0,43).

Одним из осложнений преэклампсии является преждевременная отслойка нормально расположенной плаценты (ПОНРП). В нашем исследовании у беременных основной группы указанное осложнение встретилось в 7,9±0,27% случаев. При анализе зависимости ПОНРП от уровня PlGF в сыворотке крови беременных выявлена закономерность: чем ниже уровень PlGF, тем выше риск развития ПОНРП (р<0,05) (рис. 3).
Рис. 3. Зависимость ПОНРП от уровня PlGF в сыворотке крови (р<0,05) обследованных беременных.

Результаты проведенных исследований послужили основой совершенствования организации лечебно-профилактической помощи данному контингенту беременных и их новорожденным. Для оценки предложенных нами лечебно-профилактических мероприятий была создана группа сравнения, которую составили 25 пациенток с МС и низким уровнем PlGF (ниже 100 пг/мл) в сыворотке крови.
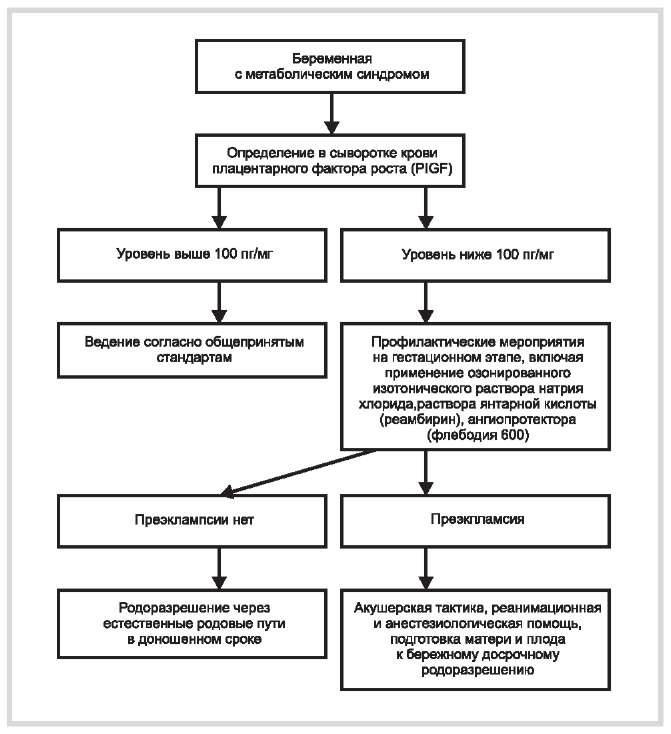
На этапе гестации в сроках 20—22 и 32—34 нед беременности пациентки группы сравнения госпитализировались в Центр экстрагенитальной патологии беременных Омска, где проводился курс профилактики преэклампсии. Для профилактики осложнений беременности нами использовались препараты магния, антиоксиданты (витамин Е, реамберин) и ангиопротекторы (флебодиа 600). Ангиопротекторы занимают особое место при проведении профилактики тяжелых осложнений беременности. В частности, флебодиа 600, препарат, обладающий венотонизирующим действием (повышает тонус вен, уменьшает венозный застой), улучшающий лимфатический дренаж (повышает тонус и частоту сокращения лимфатических капилляров, увеличивает их функциональную плотность, снижает лимфатическое давление), и, самое главное, улучшающий микроциркуляцию, повышает диффузию кислорода и перфузию его в ткани, блокирует выработку свободных радикалов, синтез тромбоксана. Изложенное позволило нам применить данный препарат с целью улучшения микроциркуляции и включить его в комплекс профилактических мероприятий тяжелой преэклампсии у беременных с метаболическим синдромом, согласно разработанному алгоритму, ведения беременных с МС и низким уровнем PlGF (рис. 4).
Рис. 4. Алгоритм ведения беременных с метаболическим синдромом и низким уровнем фактора роста плаценты в сыворотке крови.
В результате проведенных лечебно-организационных мероприятий в группе сравнения отмечено достоверное снижение частоты преэклампсии в 2 раза (с 63,3 до 32,0%) по сравнению с аналогичными показателями в основной группе (р<0,05). Преждевременной отслойки нормально расположенной плаценты в группе сравнения не было.
Таким образом, считаем целесообразным проведение определения у беременных уровня P1GF в I триместре гестации с целью прогноза развития преэклампсии и преждевременной отслойки нормально расположенной плаценты. Чем ниже уровень PlGF в I триместре беременности, тем ранее необходимо начинать комплекс мероприятий, направленных на профилактику тяжелых гестационных осложнений, подробно описанный в наших предыдущих исследованиях [2].
Выводы
1. Беременные с метаболическим синдромом относятся к группе высокого риска развития преэклампсии и преждевременной отслойки плаценты. Прогностическим тестом развития этих осложнений является определение PlGF (чувствительность 71%, специфичность 63%).
2. Низкий уровень PlGF (ниже 100 пг/мл) в сыворотке крови беременных с метаболическим синдромом свидетельствует о высоком риске развития преэклампсии и отслойки плаценты, что подтверждается корреляционнойсвязью между уровнем PlGF и тяжестью преэклампсии (r=0,43).
3. В комплекс программ профилактики развития тяжелой преэклампсии у беременных с метаболическим синдромом должны быть включены ангиопротекторы, одним из которых является флебодиа 600, назначаемые в критические сроки — 20—24 и 30—32 нед беременности.
ЛИТЕРАТУРА
1. Акушерство: Национальное руководство. Под ред. Э.К. Айламазяна, В.И. Кулакова, В.Е. Радзинского, Г.М. Савельевой. М: Гэотар-Медиа 2009; 445.
2. Варимое С.В. Экстренная медицинская помощь в акушерской практике. Омск 2009; 88.
3. Вурлее В.А., Павлович С.В. Ангиогенез и ангиогенные факторы роста в регуляции репродуктивной системы у женщин. Пробл репрод 1999; 5: 6—13.
4. Паелое К.А., Дубоеа Е.А., Щеголее А.И. Фетоплацентарный ангиогенез при нормальной беременности: роль плацентарного фактора роста и ангиопоэтинов. Акуш и гин 2010; 6:10—15.
5. Стрижоеа Н.В., Сиракамям И.К., Сарксоеа А.В. и др. Особенности течения беременности, родов, послеродового и раннего неонатального периодов при метаболическом синдроме у женщин с ожирением. Акуш и гин 2004; 6: 22—24.
6. Серое В.Н., Леуткима Ч.С, Попоеа А.Д. Клинико-метаболическая картина у беременных с ожирением и дефицитом массы тела. Вестник 2000; 4: 16—18.
7. Carmeliet P., Moons L., Luttun A. et al. Sinergism between vascular endothelial growth factor and placental growth factor contributes to angiogenesis and plasma extravasation in pathological conditions. Nat Med 2001; 7: 575—583.
8. Luttun A. Tjwa, Moons L. et al. Revascularization of ischemic tissues by P1GF treatment, and inhibition of tumor angiogenesis, arthritis and atherosclerosis by anti-Fltl. Nat Med 2002; 8: 831—840.
9. Maglione D., Guerriero V., Viglietto G. et al. Two alternative mRNAs coding for the angiogenic factor, placental growth factor (P1GF), are transcribed from a single gene of chromosome 14. Oncogene1993; 8: 925—931.
10. World Health Organization (WHO). Definition, diagnosis and classification of diabetes mellitus and its complications. Report of a WHO Consultation, part 1: diagnosis and classification of diabetes mellitus. WHO (Geneva, Switzerland) 1999.
