Арбидол: эффективность в терапии гриппа и других ОРВИ Механизм действия препарата арбидол
СтатьиИрина Анатольевна Ленева
Предыдущий раздел | Содержание | Следующий раздел
Механизм действия препарата арбидол
Многочисленные и разнонаправленные экспериментальные и клинические исследования показали, что высокая эффективность Арбидола является результатом разнообразия его биологической активности, и обусловлена не только непосредственно вирусспецифическим действием, но и опосредованно — способностью индуцировать интерферон, иммуностимулирующим эффектом, антиоксидантной активностью (13).
Вирусспецифическое действие арбидола
Вирус гриппа относится к оболочечным РНК–содержащим вирусам. Внутреннюю сторону липидной мембраны выстилает основной структурный белок М. В липидной вирусной мембране имеются ионные каналы, сформированные белком М2, в неё же снаружи погружены два поверхностных гликопротеида вируса гриппа: гемагглютинин (НА) и вирусный фермент нейраминидаза (NА), которые обуславливают исключительную изменчивость вируса гриппа. Внутри вириона находятся 8 сегментов РНК, связанных с белками полимеразного комплекса и белком нуклеокапсида (рис. 2).
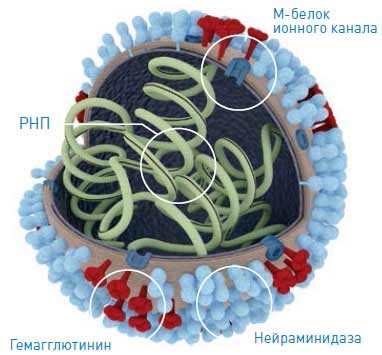
Рис. 2. Строение вируса гриппа
HA — ключевой белок, ответственный за проникновение вируса в клетку. Он взаимодействует со специфическим рецептором клетки — сиаловой кислотой, тем самым обеспечивается связывание вируса с клеткой. NA необходима для эффективного высвобождения новых синтезированных вирионов из клетки. Белок M2 формирует ионные каналы в оболочке вируса и активирует изменения вирусной структуры во время вхождения вируса в клетку.
Репродукция вируса гриппа продолжается в течение 6–8 часов в клетках верхнего и нижнего респираторного тракта и подразделяется на ранние и поздние стадии (рис. 3). К ранним стадиям относится адсорбция вируса на клеточной поверхности и проникновение вируса в клетку.
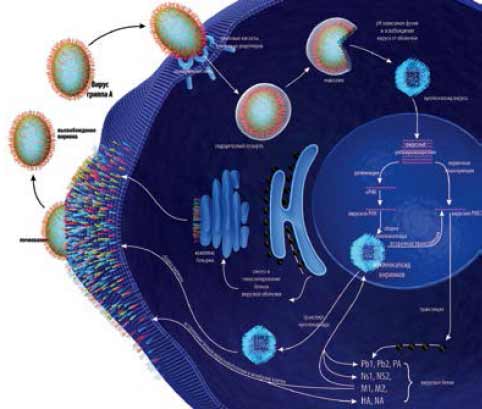
Рис. 3. Полный цикл репликации вируса гриппа
Чтобы понять, как действует препарат Арбидол, стоит более подробно остановиться на строении HA и его роли в механизме инфицирования вирусом клетки. Установлено, что HA состоит из двух субъединиц — НА1 и НА2 (рис. 4).
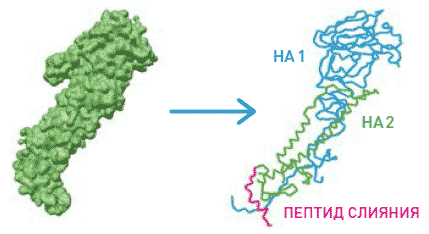
Рис. 4. Гемагглютинин и его строение: субъединицы НА1 и НА2 и пептид слияния вируса гриппа
HA1 содержит рецепторную зону, которая отвечает за связывание вируса с сиаловыми кислотами рецепторов на поверхности мембраны клетки.
После связывания НА с клеточными рецепторами вирус попадает в эндосомы, где происходит слияние липидной мембраны вируса с мембранами эндосом (рис. 5).
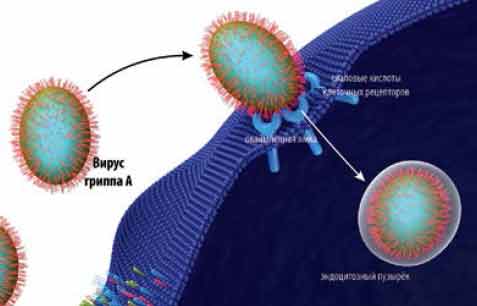
Рис. 5. Эндоцитоз вируса в клетку респираторного тракта
НА2 содержит пептид слияния — участок, индуцирующий слияние клеточной и вирусной мембран (фузию вируса). При нейтральном рН этот пептид спрятан в стволе молекулы НА, при низком рН в эндосомах молекула НА разворачивается и в ней происходят структурные изменения, пептид высвобождается, и индуцирует слияние липидной мембраны вируса с мембранами эндосом, приводящее к освобождению вирусного генома и началу транскрипции (рис. 6) (14–15).
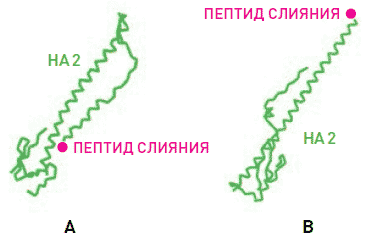
Рис. 6. Структура вируса гриппа при нейтральном рН (А) и в кислой среде (B)
Пониженное значение рН в эндосомах активирует ионные каналы, формируемые белком М2, через которые ионы Н+ проникают в вирион, понижая рН уже внутри него и приводя к освобождению рибонуклеопротеида вируса от покрывающего его белка М1 (рис. 7). Противогриппозные препараты адамантанового ряда (амантадин, ремантадин), являясь блокаторами ионных каналов, образуемых вирусным белком М2, ингибируют эту стадию вирусной репродукции.
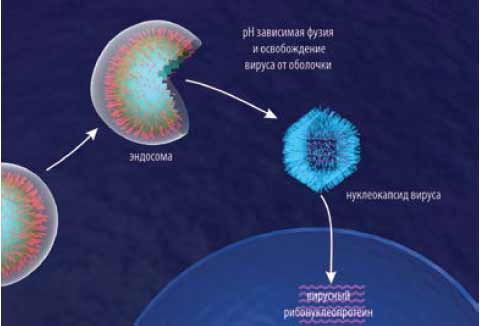
Рис. 7. Слияние мембран вируса и эндосомы (фузия) и выход рибонуклеотидов из вириона
К поздним стадиям вирусной репродукции относят первичную и вторичную транскрипцию, трансляцию и сборку вириона на клеточной поверхности, приводящую к образованию зрелых вирусных частиц и дальнейшему освобождению их из клетки (рис. 8). На этих стадиях важную роль играет фермент вируса гриппа нейраминидаза, способствуя высвобождению из клеток вновь образованных вирусных частиц и инфицированию ими новых клеток. Действие этого фермента ингибируют противогриппозные препараты второго поколения занамивир и озельтамивир.
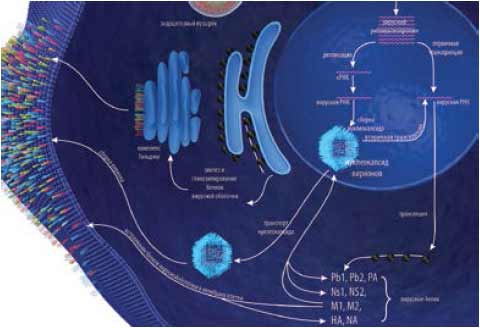
Рис. 8. Поздние стадии репликации вируса гриппа
Многочисленные исследования, проведенные как в России, так и в ряде зарубежных лабораторий показали, что Арбидол действует на ранних стадиях вирусной репродукции и ингибирует слияние вирусной липидной оболочки с внутриклеточными мембранами, предотвращая проникновение вируса внутрь клетки (рис. 8), но не влияет на вирусную транскрипцию и трансляцию, а также на активность нейраминидазы и адсорбцию вируса (16–19). Вирусспецифической мишенью действия Арбидола в цикле вирусной репродукции является НА вируса гриппа. Арбидол взаимодействует с НА вируса гриппа, увеличивая его стабильность к конформационным изменениям, индуцированным низким рН, и, как следствие, ингибирует процесс слияния липидной оболочки вируса с мембранами эндосом, приводящий к высвобождению вирусного нуклеокапсида и началу транскрипции вирусного генома (рис. 9) (17, 20–22).
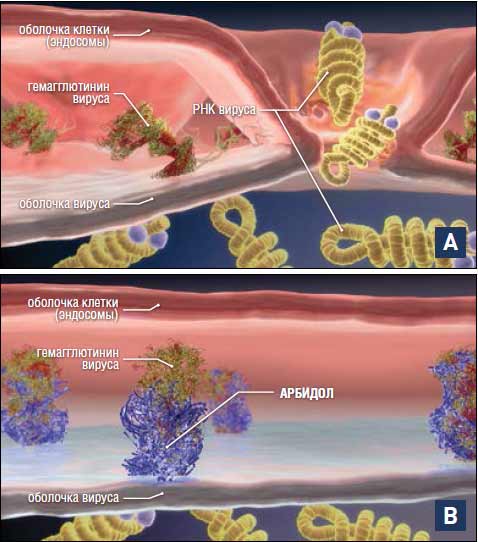
Рис. 9. Процесс фузии:
А — без Арбидола, В — в присутствии Арбидола. Арбидол ингибирует слияние мембран вируса и эндосомы
Таким образом, Арбидол по механизму вирусспецифического действия отличается от применяемых противогриппозных препаратов: блокаторов ионных каналов амантадина и ремантадина и ингибиторов нейраминидазы (NA) занамивира (Реленза) и осельтамивира (Тамифлю).
Противовирусная активность
Противовирусная активность Арбидола® подтверждена в многочисленных исследованиях in vitro и in vivo, выполненных в ведущих научных центрах России, независимых лабораториях США, Великобритании, Австралии, Франции, Китая и других стран (23–28).
Противовирусная активность арбидола в культуре клеток (in vitro) в отношении вирусов гриппа А и В человека
В многочисленных опытах in vitro и in vivo было установлено, что Арбидол обладает широким спектром противовирусной активности. С использованием иммуноферментного анализа (ИФА), модифицированного для тестирования противовирусной активности в культуре клеток, было показано, что Арбидол эффективно подавляет вирусную репродукцию эталонных штаммов всех антигенных подтипов вирусов гриппа А H1N1, H2N2, H3N2, а также вирусов гриппа В человека. Ингибирующие концентрации препарата, подавляющие вирусную репродукцию в культуре клеток на 50 % (ИК50), составляли от 1 до 12,5 мкг/мл и совпадали с ИК50, полученными для Арбидола в исследованиях других авторов (24–25).
Показана эффективность препарата в отношении не только вирусов гриппа А и В, включая сезонные и высокопатогенные подтипы A (H1N1)pdm09 и A (H5N1), но и в отношении ряда других возбудителей ОРВИ (аденовирус, РС–вирус, коронавирус и др.). Для Арбидола показана высокая активность и в отношении ремантадин– и осельтамивир–резистентных штаммов, что позволяет рассматривать его как эффективный препарат для лечения гриппа, вызванного такими штаммами.
В последние годы отмечено, что процент штаммов, резистентных к препаратам адамантанового ряда и ингибитору нейраминидазы озельтамивиру чрезвычайно возрос в мире.
Изучение действия Арбидола на репродукцию эпидемических штаммов, выделенных на территории России и резистентных к химиопрепаратам, отличным от Арбидола по механизму вирусспецифического действия, показало, что препарат ингибирует репродукцию как ремантадин–резистентных, так и озельтамивир–резистентных штаммов вирусов гриппа, причем ИК50 Арбидол в отношении этих вирусов сходны с таковыми для эталонных штаммов вирусов гриппа А и В (табл. 1)
Таблица 1. Противовирусная активность этиотропных химиопрепаратов в отношении вирусов гриппа А и В в культуре клеток MDCK
| Вирус | ИК50* (мкг/мл) | |||
| Арбидол | Рибавирин | Ремантадин | Ингавирин | |
| A /Пуэрто–Рико/8/34 (H1N1) | 6 | 2,0 | <5 | >300 |
| А/Соломоновы острова/03/06 (H1N1) | 6,0 | <5,0 | 1,5 | >200 |
| A/Aичи/2/69 (H3N2) | 7, 5 | 1,5 | 3 | >300 |
| А/Сингапур/1/57 (H2N2) | 10 | <5,0 | >20 | |
| A /Москва/1/09 (H1N1, озель-тамивир резистентный) | 5,0 | 4,0 | ||
| A/Владивосток/36/09 (H1N1, озельтамивир резистентный) | 5,0 | 3,0 | ||
| А /Москва/2/09 (H1N1, озель-тамивир резистентный) | 5,0 | <5,0 | <5 | >300 |
| А/Москва/20/09 (H3N2, ремантадин резистентный) | 7, 5 | <5,0 | >20 | >300 |
| А/Москва/30/09 (H3N2, ремантадин резистентный) | 7, 5 | <5,0 | >20 | >300 |
| В/Ли/40 | 5 | |||
| В/Москва/29/08 | 8,5 | <5,0 | >20 | >300 |
| В/Москва/79/08 | 5,5 | <5,0 | >20 | >300 |
Противовирусная активность арбидола в отношении пандемического штамма 2009 H1N1 вируса гриппа
В апреле–мае 2009 г. в США и Мексике были зафиксированы вспышки гриппа у людей, вызванные вирусом А (H1N1), получившим сначала название «свиной» или «калифорнийский» грипп. Молекулярно–генетические исследования показали, что он представляет новый вирус с уникальной комбинацией генов, происходящий от свиных, птичьих и человеческих штаммов вирусов гриппа А, и легко передается от человека к человеку. Летом 2009 года ВОЗ объявила о начале первой в этом веке пандемии гриппа. К особенностям нового пандемического варианта следует отнести, во–первых, место возникновения (Мексика, а не Китай, как это было с пандемиями XX века (30); во–вторых, — исходную резистентность к адамантановым производным, ремантадину и амантадину, связанную с мутацией S31N в каналообразующем вирусном белке М2 (12); в–третьих, высокий риск стремительного развития тяжёлых пневмоний, особенно у пациентов с отягощённым анамнезом (31). В начале пандемии до тех пор, пока новая вакцина к данному вирусу не стала доступной для широкого использования в клинической практике, этиотропные противогриппозные препараты были единственным средством для эффективной борьбы с распространением вируса. В постпандемический период наряду с вакцинацией противовирусные препараты продолжают также играть значительную роль. Они рекомендованы для лечения гриппа, протекающего в тяжелой форме и для профилактики осложненного течения болезни у пациентов, относящихся к группам риска по осложнениям при гриппе.
При этом первые рекомендации для лечения и профилактики гриппа, вызванного новым пандемическим вирусом гриппа 2009 А (H1N1) как в мире, так и в России, были даны на основе экспериментального изучения его чувствительности к химиопрепаратам.
Оказалось, что вирус гриппа типа А (H1N1) является устойчивым к действию противовирусных препаратов адамантанового ряда амантадину и ремантадину, но чувствителен к ингибиторам нейраминидазы озельтамивиру (Тамифлю) и занамивиру (Реленза) (12). Изучение чувствительности пандемического вируса к Арбидолу в культуре клеток, а также на основании молекулярно-генетического анализа, было проведено в нескольких ведущих вирусологических лабораториях России и мира.
В исследованиях были использованы вирусы гриппа А/California/04/2009, А/California/07/2009, полученные в качестве референс–штаммов из Центра по контролю заболеваемости (США, Атланта), и А/Москва/01/2009swl, выделенные от первого инфицированного новым вирусом Н1N1 пациента, прибывшего в Россию из США. Оказалось, что Арбидол эффективно подавлял размножение всех трех изученных вирусов, при этом ИК50 Арбидола для двух вирусов А/California/07/2009 и А/Moscow/01/2009swl были примерно одинаковы и составляли около 4 мкг/мл (табл. 2). ИК50 Арбидола в отношении вируса А/California/07/2009 (H1N1), определенная методом оценки цитопатической реакции с помощью МТТ, составила 5,6±1,36 мкг/мл, что близко к ИК50, полученным методом ИФА (32–33).
Таблица 2. Чувствительность различных штаммов пандемического вируса гриппа 2009 Н1N1 к противовирусным препаратам
| Вирус | Рибавирин | Ремантадин | Арбидол | ||
| ИК50* (мкг/мл) | ИК50* (мкг/мл) | Наличие мутаций в М2 белке | ИК50* (мкг/мл) | Наличие мутаций в НА | |
| А/California/07/2009 | 2,0 | >5 | Есть | 4,0 | Нет |
| А/California/04/2009 | 1,5 | >5 | Есть | 4,0 | Нет |
| А/Moscow/01/2009swl | 1,5 | >5 | Есть | 4,0 | Нет |
В конце 2009 г. в организме умерших больных стали обнаруживаться варианты вируса с мутациями в рецептор-связывающем сайте НА1 в положении 222 D на G. Полученные ранее данные свидетельствуют о приобретении вирусом в результате этой мутации специфичности к рецепторам клеток не только верхних дыхательных путей (как у сезонного вируса гриппа), но и тропности к эпителию нижних дыхательных путей, что в свою очередь приводит к развитию первичной вирусной пневмонии. Это обуславливает тяжелое течение гриппозной инфекции и нередко приводит к смертельному исходу. Оказалось, что Арбидол подавляет размножение таких вирусов, выделенных у пациентов в России, причем активность этого препарата в отношении вирусов с мутацией была одинакова с его активностью в отношении штаммов Н1N1 без данной мутации, а также других эталонных и эпидемических штаммов вирусов гриппа А и В человека (34).
Противовирусная активность арбидола в культуре клеток в отношении вирусов гриппа, имеющих птичье происхождение
В последние годы эпидемическая ситуация по гриппу осложнилась случаями инфицирования людей вирусами гриппа птиц, которые могут играть существенную роль в формировании нового пандемического штамма вируса гриппа А. С 1997 г. в странах Южной и Юго–Восточной Азии наблюдались эпизоотии среди кур, вызванные вирусами H5N1, сопровождавшиеся заболеванием людей, подчас с высокой смертностью. По данным ВОЗ, вирусом H5N1 заразились более 600 человек в 15 странах мира, при этом примерно в половине случаев с летальным исходом. Большинство случаев заражения проходило при прямом контакте с инфицированными птицами. Ущерб от эпидемии только в странах Юго-Восточной Азии превысил 10 млрд. долларов.
В конце 2005 г. — начале 2006 г. в 6 странах Евросоюза, а также в России и сопредельных с ней государствах наблюдалось распространение гриппа среди птиц, вызванного патогенным вирусом H5N1. Пока заражение людей происходит только при контакте с домашней птицей, однако опасность преодоления межвидового барьера и приобретения эпидемического потенциала отдельными вариантами высокопатогенных вирусов гриппа А H5N1 или их реассортантами остаётся достаточно высокой и требует постоянного эколого-вирусологического мониторинга. В связи с этим получение данных об активности противогриппозных препаратов в отношении этих вирусов крайне важно.
Изучение действия Арбидола на репродукцию вирусов Н5N1 показало, что в клетках MDCK препарат подавлял репродукцию двух патогенных вирусов гриппа: А/Гонконг/156/97 (Н5N1) и А/Цесарка/Гонконг/G1/97 (H9N2), вызвавших заболевания у людей в Гонконге, причем ИК50 в отношении этих вирусов составляли 30 мкг/мл и 15 мкг/мл, соответственно (табл. 3).
Таблица 3. Противовирусная активность Арбидола в отношении вирусов гриппа птиц А подтипов Н2, Н5, Н6 и Н9 в культуре клеток MDCK
| Вирус | ИК50* (мкг/мл) |
| А/Гонконг/157/97 (H5N1) | 30 ± 5 |
| А/Цесарка/Гонконг/G1/97 (H9N2) | 15 ± 3 |
| А/Утка/Гонконг/W31297 (H6N1) | 25 ± 3 |
| А/Курица/Гонконг/G9/97 (H9N2) | 15 ± 5 |
| A/Утка/Приморье/2633/01 (H5N3) | 4,5 ± 2,5 |
| A/Утка/Приморье/2621/01 (H5N2) | 4,0 ± 1 |
| A/Утка/Алтай/1285/91 (H5N3) | 7,5 ± 2,5 |
| A/Cингапур/1/57 (H2N2) | 7,5 ± 4 |
| A/Grebe/Tyva06–1/06 | 10 |
| A/Chicken/Moscow/2/07 | 11,1 |
| A/Gygnus gygnus/Krasnodar/329/07 | 9,8 |
| A/Chicken/Krasnodar/300/07 | 10,1 |
| A/Pigeon/Rostov-on-Don/6/07 | 12,5 |
| A/Chicken/Rostov-on-Don/35/07 | 12,8 |
| A/Chicken/Primorje/1/08 | 13,0 |
| A/Tyva/2/2010 | 13,9 |
Арбидол в культуре клеток MDCK также оказывал селективное ингибирующее действие на репродукцию вирусов гриппа А подтипа Н5, изолированных у диких птиц на территории России, антигенная и первичная структура НА которых была сходна с таковой у вирусов, обусловивших вспышки заболевания среди людей и кур в странах Юго–Восточной Азии. Арбидол в концентрации 10 мкг/мл подавлял инфекционный титр данных вирусов в культуре клеток в среднем на 2–3 lg и эффективно ингибировал экспрессию вирусных антигенов, выявляемую методом ИФА. Активность Арбидола в отношении этих вирусов (ИК50 от 4,5 до 7,5 мкг/мл) была сходна с активностью Арбидола в отношении антигенных серотипов вируса гриппа А человека (табл. 3). Кроме того, Арбидол подавлял репликацию высокопатогенных вирусов гриппа Н5N1, выделенных от больных птиц на территории России, при этом, как и в случае с выделенными от инфицированных людей вирусами гриппа Н5N1, ИК50 Арбидола были несколько выше, чем их ИК50, полученные для непатогенных вирусов гриппа подтипа Н5N1, выделенных от диких птиц на территории России, а также эпидемических и эталонных штаммов вируса гриппа А и В человека (34–36).
Полученные результаты показывают, что для достижения в культуре клеток ингибирующего эффекта в отношении высокопатогенных вирусов гриппа Н5N1, выделенных как от больных людей, так и больных птиц, сходного с эффектом, оказываемым Арбидолом на репродукцию вирусов гриппа А и В человека, требовались большие концентрации Арбидола, что совпадало с данными о более высоких концентрациях других противогриппозных препаратов, в частности озельтамивира, необходимых для подавления репродукции патогенных вирусов, имеющих птичье происхождение (табл. 4). Фармакокинетические исследования показали, что концентрация Арбидола зависит от дозы, при этом одноразовая терапевтическая доза составляет 200 мг, а токсикологические исследования показали безопасность и хорошую переносимость препарата при одноразовом приеме 400 мг. (94). Таким образом, возможно увеличение дозы препарата для усиления его эффекта на вирусную репродукцию.
Таблица 4. ИК50* для химиопрепаратов в отношении вирусов гриппа H1N1 sw1
| Вирус | ИК50* (мкг/мл) | |||
| Ремантадин | Арбидол | Рибавирин | Озельтамивир | |
| A/Calif/07/09 | не ингибирует | 7, 5 | 10,8 | Н. И. |
| A/IIV–Elista/ 64/2009 | не ингибирует | 6,6 | Н. И.** | 0,1 |
| A/IIV–Vladivostok/ 59/2009 | не ингибирует | 6,7 | Н. И. | 0,08 |
| A/IIV–Khabarovsk/ 149/2009 | не ингибирует | 3,2 | Н. И. | 0,2 |
| A/IIV–Anadyr/ 177/2009 | не ингибирует | 7,7 | Н. И. | 1,1 |
** — Н. И. — не изучали
Противовирусная активность арбидола в культуре клеток в отношении возбудителей ОРВИ
При оценке эффективности противовирусного препарата очень важной является широта спектра его активности. Изучение действия Арбидола в культуре клеток показало, что он подавляет размножение респираторно-синцитиального вируса, риновирусов, парагриппа, ротавирусов, коронавирусов (ТОРС) и аденовируса в культуре клеток, причем ИК50 Арбидола для этих вирусов сходны с таковыми для вируса гриппа А и В (табл. 5). Данные о противовирусной активности Арбидола в отношении возбудителей ряда ОРВИ совпадают с данными как отечественных, так и зарубежных исследователей (25, 26, 37, 38).
Таблица 5. Противовирусная активность Арбидола в отношении вирусов, вызывающих ОРВИ в культурах клеток
| Вирус | ИК50* (мкг/мл) |
| Респираторно–синцитиальный вирус | 10 |
| Аденовирус тип 5 | 20 |
| Вирус парагриппа | 5 |
| Ротавирус | 20 |
| Риновирус тип 30 | 12,5 |
| Коронавирус штамм 229 Е | 6,5 |
Отмечено, что на протяжении последних лет до 2009 г. отмечалась тенденция роста заболеваемости ОРВИ при уменьшении роста заболеваемости собственно гриппом. В настоящее время не существует эффективных вакцин для профилактики ОРВИ за исключением вакцин против гриппа А и В, поэтому применение противовирусных препаратов для лечения ОРВИ приобретает первостепенное значение. Симптомы острых респираторных вирусных заболеваний сходны, а лабораторная диагностика их на практике еще не получила широкого распространения. Однако применяемые в настоящее время для лечения этих инфекций противовирусные препараты обладают довольно узким спектром действия. Противогриппозные препараты адамантанового ряда амантадин и ремантадин эффективны только в отношении вируса гриппа А, занамивир и озельтамивир разрабатывались как ингибиторы активного сайта нейраминидазы вирусов гриппа А и В и, соответственно, являются высокоселективными ингибиторами репродукции только вирусов гриппа А и В. Таким образом, важнейшим преимуществом Арбидола перед существующими противогриппозными препаратами адамантанового ряда и ингибиторами нейраминидазы является то, что он обладает более широким спектром действия, и эффективен не только в отношении вирусов гриппа А и В, но также и в отношении целого ряда возбудителей других ОРВИ. Широкий спектр действия Арбидола в отношении возбудителей инфекций, имеющих одинаковые симптомы, позволяет рассматривать его как препарат, лечение которым можно начинать без проведения предварительной диагностики.
Противовирусная активность арбидола у животных
Данные об активности Арбидола в отношении вирусов гриппа подтипа Н5N1 в культуре клеток получили подтверждение в экспериментах на мышах. Лечение Арбидолом перорально (10 и 30 мг/кг/день) в течение 5 дней полностью защищало от гибели мышей, зараженных патогенным вирусом гриппа птиц А/Курица/Курган/2005 (H5N1), выделенным во время вспышки гриппа у кур в России (данные Центра вирусологии МО России, досье компании Фармстандарт).
Изучение эффективности Арбидола на модели гриппозной пневмонии мышей показало, что при интраназальном заражении белых мышей адаптированными к нему вирусами гриппа А/Пуэрто-Рико/8/34 (Н1N1) и А/Аичи/2/69 (H3N2) и 5-дневном лечении Арбидолом в дозах от 15 мкг/кг до 100 мг/кг у животных был отмечен терапевтический эффект, который обеспечивал снижение летальности инфицированных мышей на 40–60 %, увеличивая их продолжительность жизни в 1,7–2 раза и предотвращая потерю массы тела по сравнению с группой вирусного контроля. Эффективность Арбидола в этих опытах была сходна с эффективностью ремантадина (табл. 6).
Таблица 6. Терапевтическая эффективность химиопрепаратов на модели гриппозной инфекции у мышей
| Препарат | 10ЛД50* | ЛД80* | |||
| Показатель защиты от летального исхода (%) | Средняя продолжительность жизни (дни) | Показатель защиты от летального исхода (%) | Средняя продолжительность жизни (дни) | ||
| Арбидол | 15 мг/кг/день | 20 | 8,1 ±3,1 | 40 | 11,5±4,8 |
| 30 мг/кг/день | 10 | 7,5±2,0 | 60 | 13,7±3,1 | |
| 60 мг/кг/день | 50** | 10,6±4,5 | 50 | 13,1±2,9 | |
| 100 мг/кг/день | не изучали | не изучали | 50 | 13,1 ±2,9 | |
| Ингавирин | 5 мг/кг/день | 10 | 6,4±3,5 | 30 | 10,2±3,1 |
| 15 мг/кг/день | 0 | 7,0±2,0 | 30 | 10,5±4,5 | |
| 30 мг/кг/день | 30 | 9,3±2,0 | не изучали | не изучали | |
| 60 мг/кг/день | 30 | 8,7±4,3 | 30 | 10,4±4,8 | |
| Ремантадин | 10 мг/кг/день | 40*** | 9,5±4,6 | 60 | 13,6±4,7 |
| Вирусный контроль* | 6,1 ±1,8 | 6,9±1,3 | |||
** — р<0,01 в сравнении с контролем вируса в этом же эксперименте;
***— р<0,05 в сравнении с контролем вируса в этом же эксперименте.
Профилактическая эффективность Арбидола на этой же модели была наиболее выражена при использовании его за 96 часов до инфицирования, предотвращая смертность 40–50 % животных и потерю их веса, увеличивая продолжительность их жизни в 1,3–1,5 раза. Арбидол, также как и ремантадин, был более эффективен при лечебном и лечебнопрофилактическом использовании. В дозах 30 и 10 мг/кг/день Арбидол и ремантадин соответственно защищали от гибели 60–80 % инфицированных животных, полностью предотвращали потерю их веса и увеличивали среднюю продолжительность жизни почти в 2 раза (24).
Препарат обладает широким спектром противовирусной активности, ингибируя репродукцию трех основных антигенных подтипов H1N1, H2N2, H3N2 и ремантадин-резистентных вирусов гриппа А человека, вирусов гриппа А птиц Н5 и Н9, вызывавших заболевания людей и птиц, вирусов гриппа В и С, а также респираторно–синцитиального вируса, парагриппа, ротавирусов, коронавирусов (ТОРС) и аденовируса в культуре клеток. Данные о широком спектре действия Арбидола были подтверждены в его клинических испытаниях.
Резистентность
Обратной стороной высокой специфичности всех этиотропных химиопрепаратов является возможность формирования резистентности, то есть устойчивости к препаратам. Быстрое возникновение (через 1–2 пассажа) резистентных к амантадину и ремантадину штаммов было показано в многочисленных экспериментах на животных и в культуре клеток, а появление устойчивых штаммов в человеческой популяции может происходить уже через 2–4 дня после начала лечения этими препаратами. Последние исследования клинических изолятов показали, что процент штаммов вируса гриппа А, резистентных к препаратам адамантанового ряда, чрезвычайно возрос в мире за последние 2–3 года и достигает 90 % в некоторых странах, например в Китае и США. Высокая частота резистентности к амантадину/ремантадину стала причиной запрета их применения для лечения и профилактики гриппа А в США в эпидемическом сезоне 2005– 2007 гг. Новый пандемический вирус H1N1 (2009) также является резистентным к препаратам адамантанового ряда.
Считалось, что частота возникновения резистентных штаммов при приеме озельтамивира составляет 1,3 % у взрослых и 8,6 % у детей. Однако, с начала 2008 г. наблюдалось увеличение среди циркулирующих вирусов гриппа А подтипа Н1N1 штаммов, резистентных к озельтамивиру, достигая в некоторых странах, например, в США около 100 %. В России с февраля 2008 среди циркулирующих штаммов Н1N1 также было обнаружено 40–50 % штаммов, резистентных к озельтамивиру.
Таким образом, развитие резистентности к противовирусным препаратам — одна из важнейших проблем противовирусной химиотерапии. Факты увеличения роста резистентных к какому-либо противовирусному препарату штаммов ставит вопрос о целесообразности его применения для лечения и профилактики гриппа вообще. Это диктует необходимость постоянного мониторинга чувствительности эпидемических штаммов вирусов гриппа к химиопрепаратам и в случае необходимости своевременной замены одного препарата на другой.
Мутанты, резистентные к Арбидолу, получены пока только в опытах путем многократных (около 15) пассажей в культуре клеток в присутствии увеличивающихся концентраций Арбидола. Определение нуклеотидной последовательности Арбидол-резистентных мутантов показало, что резистентность к нему обусловлена мутациями в белке мишени в цепи НА2 в различных положениях (17) (рис. 10).
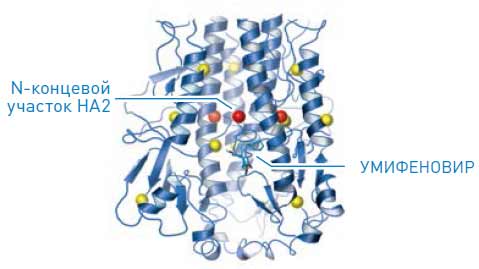
Рис. 10. Локализация в молекуле НА мутаций, ответственных за резистентность к Арбидолу (17)
Исследования свыше 500 клинических изолятов, выделенных в России в эпидемический сезон 2000–2008 гг., проведенные в ГУ НИИ вирусологии им. Ивановского РАМН, не выявили среди них ни одного резистентного к Арбидолу, в то время как 40 % из них были резистентны к ремантадину. Однако, эпидемические штаммы вирусов гриппа эталонного варианта В/Гонконг/330/1 и всех изученных вирусов гриппа А, в том числе, резистентных к ремантадину, были более чувствительны к Арбидолу, чем эпидемические штаммы вируса гриппа В эталонного варианта В/Шанхай361/02. Таким образом, несмотря на то, что Арбидол широко используется в России, до настоящего времени Арбидол– резистентные штаммы у людей не были обнаружены (29).
Кроме того, было проведено изучение возможности формирования резистентности к Арбидолу при использовании в клинической практике среди 39 пациентов с симптомами гриппа, которые принимали Арбидол в течение 5 дней. Вирусы, выделенные из носовых смывов пациентов до начала лечения и затем ежедневно в течение лечения, были изучены в отношении их чувствительности к Арбидолу в культуре клеток. Все выделенные изоляты были чувствительны к действию Арбидола, значения ингибирующих концентраций для них колебались в небольшом диапазоне от 2 мкг/мл до 15 мкг/мл и совпадали с ингибирующими концентрациями, полученными нами ранее при изучении чувствительности к Арбидолу эталонных лабораторных штаммов вирусов гриппа А и В. Изучение вирусных изолятов, выделенных от 5 пациентов, у которых нам удалось выделить вирусы в течение 4 и 5 дней приема Арбидола, не выявило снижения чувствительности к Арбидолу на фоне всего курса лечения, а определение их нуклеотидной последовательности генов показало их идентичность и отсутствие мутаций, которые определяются как ответственные за резистентность к Арбидолу в опытах in vitro (табл. 7).
Таблица 7. Чувствительность к Арбидолу изолятов вирусов гриппа, выделенных от пациентов, принимавших препарат
| Пациент | Номер изолята и день получения смыва | ИК50*(мкг/мл)Арбидола | Наличие мутаций в HA |
| мальчик, 12 лет В/Москва/ 9/05 | 51 — до приема | 6,0 | |
| 53 — 2 день | 6,5 | нет мутаций | |
| 54 — 3 день | 5,5 | нет мутаций | |
| 64 — 4 день | 7, 2 5 | нет мутаций | |
| 65 — 5 день | 7, 2 5 | нет мутаций | |
| девочка, 5 лeт В/Москва/ 71/05 | 179 — до приема | 8,0 | |
| 180 — 2 день | 6,5 | нет мутаций | |
| 181 — 3 день | 12,25 | нет мутаций | |
| 182 — 4 день | 10 | нет мутаций | |
| подросток, 14 лет А/Москва/ 8/06 (H1N1) | 253 — до приема | 5,5 | |
| 478 — 2 день | 5,0 | нет мутаций | |
| 479 — 3 день | 5,4 | нет мутаций | |
| 480 — 4 день | 6,5 | нет мутаций | |
| мальчик, 7 лет А/Москва/ 20/06 (H1N1) | 256 — до приема | 7,5 | |
| 489 — 3 день | 7,5 | нет мутаций | |
| 490 — 4 день | 9,0 | нет мутаций |
Таким образом, в настоящее время среди циркулирующих на территории России штаммов вирусов гриппа не выявлено резистентных к Арбидолу. Кроме того, в клиническом исследовании, проведенном среди 39 пациентов, инфицированных вирусами гриппа А и В, не выявлено формирования резистентности к Арбидолу на фоне 5 дневного курса лечения препаратом.
Резистентность к препарату обусловлена мутациями в том вирусном белке, который является мишенью действия препарата. Известно, что препараты адамантанового ряда являются блокаторами белка М 2, и резистентность к ним обусловлена мутациями в позициях 26, 27, 30, 31 или 34 мишени белка М2. Занамивир и озельтамивир являются ингибиторами вирусного фермента нейраминидазы, резистентность к ним обусловлена наличием мутаций в ее активном сайте. Анализ нуклеотидной последовательности штаммов А/California/07/2009, A/California/04/2009 и А/ Moscow/01/2009swl показал, что нейраминидаза этих штаммов, кодируемая сегментом NA, не содержит характерных мутаций (E–119, H–274, R–293, N–295), обуславливающих резистентность вируса к ее ингибиторам озельтамивиру и занамивиру.
Как следует из нуклеотидной последовательности изученных штаммов, в них присутствует одна определяющая мутация в положении 31 белка М2 (серин, замененный на аспаргин), что подтверждает полученные в других исследованиях, а также нами данные об устойчивости в культуре клеток этих вирусов к ремантадину. Изучение механизма действия Арбидола показало, что его мишенью является НА вируса гриппа, и резистентность к нему обусловлена мутациями в положениях K51N, Q42H, Q27N, K117R eго субъединицы HA2. Анализ генома вирусов гриппа Н1N1 показал, что в вирусах H1N1 А/California/07/2009, A/California/04/2009 и А/ Moscow/01/2009swl нет замен, ответственных за резистентность к Арбидолу, что совпадает с полученными данными об активности этого препарата в культуре клеток (32, 39).
Таким образом, результаты экспериментов показали, что Арбидол эффективен в отношении нового пандемического 2009 H1N1 вируса гриппа А. Арбидол оказывает селективное ингибирующее действие на репродукцию пандемического вируса гриппа в культуре клеток MDCK, а при анализе генома вирусов гриппа не было обнаружено замен, определяющих резистентность к Арбидолу. На основании совокупности полученных экспериментальных данных, Арбидол был рекомендован Министерством здравоохранения и социального развития Российской Федерации для профилактики и лечения гриппа, вызванного новым пандемическим 2009 вирусом гриппа А H1N1 (методические рекомендации «Схемы лечения и профилактики гриппа, вызванного вирусом типа A H1N1 для взрослых» от 17 июня 2009 года).
Предыдущий раздел | Содержание | Следующий раздел
Комментарии
ПРАКТИКА ПЕДИАТРА
