Дискогенная боль в спине: возможности патогенетической терапии
Статьи Опубликовано в журнале:«ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ»; № 12; 2015; стр. 162-168.
Г.Р. Табеева
ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М. Сеченова», Москва
Патология межпозвонковых дисков (МПД) является одной из ведущих причин боли в спине. Ввиду комплексности причин боли в спине часто бывает трудно определить степень вовлеченности патологии МПД в происхождение боли. Воспалительные реакции в ответ на повреждения МПД, как известно, участвуют в процессах дегенерации дисков и играют важную роль в происхождении собственно боли. В статье рассматриваются воспалительные механизмы болей в спине, особое внимание уделено взаимоотношениям воспалительных медиаторов и биомеханики МПД. Фактор некроза опухоли альфа (TNF-a) является ключевым медиатором воспалительных реакций в патогенезе дегенеративной болезни дисков. Рассматривается роль ингибиторов TNF-a как факторов терапевтического воздействия на процессы нейронального повреждения при болях в нижней части спины.
Ключевые слова: боль в спине, дегенеративная болезнь дисков, фактор некроза опухоли альфа (TNF-a), артрофоон.
LOW BACK PAIN: POSSIBILITIES OF PATHOGENETIC TREATMENT
G.R. Tabeeva
Sechenov First Moscow State Medical University, Moscow
Intervertebral disc (IVD) degeneration is one of the major causes of low back pain (LBP). Due to the complexity of spinal pain syndromes, it is often difficult to determine the extent of the IVD's contribution to the genesis of spinal pain. Inflammatory response to IVD' injury has been acknowledged to be important in the process of disc degeneration and may play an important role in pain generation. In this article, the inflammatory mechanisms of LBP will be discussed with special focus on interactions between inflammatory mediators and IVD biomechanics. Tumor necrosis factor-a (TNF-a) is a key mediator of inflammatory reactions in the pathogenesis of degenerative disk disease. The role of TNF-a inhibitors as a potential target of therapeutic interventions in prevention of neuronal damage and neuroprotection in LBP is discussed.
Key words: low back pain, degenerative disk disease, tumor necrosis factor-a (TNF-a).
Боль в нижней части спины (БНС) является одной из наиболее значимых с медицинской точки зрения проблем у лиц разного возраста. Ее распространенность в течение жизни достигает 70—85% в популяции [1, 2], а доля лиц, которые испытывают по этой причине хроническую дезадаптацию, составляет около 10% [1].
Одним из наиболее трудных вопросов проблемы БНС является обсуждение возможных источников болевых ощущений. Среди различных этиологических факторов патология межпозвонкового диска (МПД) рассматривается как основная причина БНС. Около 40% случаев БНС связано с дегенеративной болезнью дисков [3]. Патология МПД выявляется у 5% взрослой популяции [1]. Спинальные дегенеративные заболевания, такие как грыжи дисков, спинальный стеноз и дегенеративный спондилолистез могут приводить к БНС. Хотя большинство лиц, страдающих БНС, старше 30 лет и они имеют разной степени структурные дегенерации одного или более дисков, эти изменения далеко не всегда сопровождаются болью. Более того, эти процессы выявляются весьма часто и у лиц более молодого возраста, поэтому они не могут рассматриваться как маркеры процесса старения. В то же время в некоторых исследованиях показано, что грыжи дисков весьма часто асимптомны [4, 5]. S. Boden и соавт. [4] исследовали МРТ у лиц, не страдающих БНС, и продемонстрировали, что грыжи дисков обнаруживаются в целом в 24% случаев; у 21% лиц — в возрасте 20—39 лет, у 22% — в возрасте 40—60 лет и у 36% — в возрастной категории 60 лет и старше. Между тем, чем обусловлены различия в клинических проявлениях среди этих пациентов, не понятно.
Многочисленные терапевтические методы, применяемые в повседневной практике, могут частично облегчать боль, однако они далеко не всегда обеспечивают полное восстановление физического функционирования пациента. Проспективные наблюдения показывают, что результаты консервативного лечения, включающего медикаментозные и физические методы, в долгосрочной перспективе сопоставимы с исходами естественного течения заболевания [6], и единодушного мнения относительно эффективности используемых в настоящее время при БНС терапевтических стратегий нет. Поэтому поиск новых терапевтических мишеней для эффективного контроля над болевыми проявлениями при этой патологии остается весьма актуальной задачей.
Воспалительные механизмы дискогенной боли в спине
Процесс дегенерации МПД представляет собой каскад структурно-биохимических нарушений, начинающихся со снижения питания клеток в пределах центральных зон МПД, и следующей за ним аккумуляции продуктов клеточного метаболизма и деградации матриксных молекул. Это постепенно формирует кислую среду, которая в последующем подвергает риску выживаемость клеток. Потеря гидрофильных молекул матрикса приводит к структурным изменениям и нестабильности позвонков, что рассматривается как основная причина протрузии дисков, радикулопатии и, возможно, спинального стеноза [7, 8]. Важнейшим фактором формирования дегенеративных изменений является разрыв фиброзного кольца МПД [9, 10]. Многочисленные исследования, между тем, демонстрируют, что определяемые гистологически и на МРТ разрывы фиброзного кольца дисков у пациентов с БНС не могут рассматриваться как надежный маркер формирования болевых проявлений. Было неоднократно показано, что изолированный дефект фиброзного кольца далеко не всегда сопровождается БНС [11, 12]. Между тем этот фактор может играть важную роль в процессе формирования дегенеративного каскада.
В рамках различных процессов, ведущих к развитию дегенеративной болезни МПД, обсуждаются различные факторы, такие как кальцификация замыкательных пластинок, приводящая к нарушению физиологического транспорта питательных веществ, интенсивная механическая нагрузка, генетическая предиспозиция, факторы образа жизни, инфекции, а также процессы, связанные со старением [13]. Независимо от причины универсальным механизмом, участвующим в формировании болевых и других неврологических проявлений БНС, являются воспалительные реакции. Клинико-экспериментальные исследования убедительно показывают, что воспалительные реакции участвуют как в процессах дегенерации дисков [14], так и могут играть важную роль в генерации боли [15]. Наряду с компрессионными факторами воспалительные изменения собственно дисков могут участвовать в формировании радикулярной боли [16, 17]. Механическая компрессия периферических нервных корешков приводит к тканевому повреждению, вызывая воспалительные реакции, что в итоге также сопровождается неврологическими проявлениями радикулопатии.
Процесс дегенерации МПД характеризуется подъемом уровней воспалительных цитокинов: фактора некроза опухоли (tumor necrosis factor — TNF-a), интерлейкинов (IL-1 a/в, IL-6 и IL-17) [18]. Провоспалительные молекулы секретируются как клетками пульпозного ядра и фиброзного кольца, так и макрофагами, Т-клетками и нейтрофилами. Эти цитокины запускают каскад патофизиологических реакций со стороны клеток МПД, которые могут стимулировать аутофагию, ускоренное старение и апоптоз. В этом процессе участвуют различные секретируемые в МПД провоспалительные медиаторы: TNF-a, IL-1 a/в, IL-6, IL-17, IL-8, IL-2, IL-4, IL-10, IFN-y, хемокины, простагландины (PGE2). Среди них TNF-a и IL-1 a/в являются наиболее изученными [19]. Эти цитокины стимулируют деградацию его матрикса, продукцию хемокинов, что приводит к изменениям клеточного фенотипа. Получаемый в результате дисбаланс между катаболическими и анаболическими процессами приводит к дегенеративным изменениям, развитию протрузии и соответственно радикулярной боли. Высвобождение хемокинов из дегенерированных дисков в последующем стимулирует инфильтрацию и активацию Т- и В-клеток, макрофагов, нейтрофилов и тучных клеток, амплифицируя воспалительный каскад. Миграция иммуноцитов в структуре диска сопровождается разрастанием мелких сосудов и нервных волокон, происходящих из ганглионарных клеток задних корешков. В этой воспалительной среде выделение таких нейрогенных субстанций, как фактор роста нервов (nerve growth factor — NGF) и мозговой нейротрофический фактор (brain-derive neurotrophic factor — BDNF), генерируемых структурами МПД и иммунными клетками, вызывает активацию катионных каналов спинномозгового ганглия. Деполяризация этих каналов может инициировать дискогенную и радикулярную боль и усиливать регулируемый цитокинами дегенеративный каскад [15, 20].
Генез формирования воспалительных реакций и их значение в генерации болевых феноменов при БНС являются противоречивыми. С одной стороны, с традиционных позиций воспаление как повреждающий фактор коррелирует с прогрессированием болезни и может расцениваться и как причина, и как следствие дегенерации МПД и формирования грыжи. С другой стороны, сбалансированный воспалительный ответ может рассматриваться как естественный процесс, необходимый для восстановления функционирования МПД [21]. H. Yang и соавт. [21] провели исследование роли воспалительных медиаторов и морфологических изменений в происхождении БНС, связанной с грыжей диска. Было выявлено, что частота БНС при легких признаках дегенерации дисков была 16,7%, а при тяжелых — 28,6%. Между тем их частота у пациентов с умеренными дегенеративными изменениями была 62,5%. С помощью иммуногистохимических методов было показано, что в группе с умеренными признаками дегенерации МПД процент иммунопозитивных клеток для IL-1 в, TNF-a, iNOS и субстанции P был достоверно выше по сравнению с группами с легкими и тяжелыми признаками. На основании этих данных предполагают, что экспрессия воспалительных медиаторов зависит от тяжести дегенерации дисков, причем умеренная степень дегенеративных изменений коррелирует с наиболее высокой экспрессией воспалительных медиаторов [21]. Эти результаты полностью соответствуют клиническим наблюдениям, когда дегенерация диска часто бывает асимптомной.
Как известно, собственно активность воспалительных реакций позитивно коррелирует со степенью дегенеративных изменений МПД при БНС [15, 18]. Между тем проведенное в работе H. Yang и соавт. [21] сопоставление иммунореакивности воспалительных медиаторов в болевой и безболевой группах не выявило существенных различий. Это, с одной стороны, предполагает возможное участие в дегенеративных процессах МПД и других факторов. С другой стороны, известно, что частота БНС выше в случаях умеренных дегенеративных изменений диска с наличием гиперинтенсивности на МРТ, что сопровождается высокой экспрессией воспалительных маркеров [21]. Снижение активности воспалительных медиаторов при грубой дегенерации МПД может быть связано со снижением числа клеток МПД и их метаболической активности. Важно, что этот паттерн сочетания высокой экспрессии воспалительных медиаторов с умеренными дегенеративными изменениями МПД соотносится с наиболее высокой частотой манифестации БНС. Известно, что у пациентов с наличием вышеописанного паттерна после радиочастотой аблации симптомы БНС регрессируют при отсутствии изменений на МРТ. Основываясь на этих представлениях, облегчение боли в таких случаях можно объяснить инактиваций воспалительных медиаторов тепловым радиочастотным воздействием, которое приводит к подавлению стимуляции ноцицепторов [21].
В процессе развития дегенеративных изменений МПД повышение активности воспалительных медиаторов, действующих как алгогены, способствует их накоплению и транспортировке из пульпозного ядра к наружному фиброзному кольцу. Здесь они взаимодействуют с ноцицептивными рецепторами и способствуют прорастанию нервных волокон через разрывы внутрь фиброзного кольца вплоть до структур пульпозного ядра, что в совокупности и вызывает БНС [22, 23]. Разрывы фиброзного кольца — частый феномен в процессе дегенерации дисков [9, 10]. Нервные волокна имеют тенденцию распространяться вдоль фиброзного кольца во внутреннюю его часть, даже в ткани пульпозного ядра. В результате разрывов усиливается транспорт воспалительных цитокинов и ноцицептивных стимуляторов из пределов пульпозного ядра к ноцицептивным рецепторам фиброзного кольца [23]. Обнаруживаемая в этих случаях зона высокоинтенсивной плотности на МРТ рассматривается как феномен, отражающий локусы разрывов фиброзного кольца [24]. Избыточный транспорт макромолекул из пульпозного ядра через разрывы фиброзного кольца приводит к рекруитированию иммунных клеток в пределах пораженного диска, которое провоцирует боль. Исходя из этих представлений, обсуждаемые формы структурно-цитохимических взаимодействий при дегенеративной болезни дисков могут рассматриваться в контексте симптоматических (болевых) форм заболевания.
Основываясь на данных исследования уровня провоспалительных цитокинов при дегенеративной болезни дисков, было высказано предположение, что собственно дегенеративный процесс может инициировать нейроиммунные каскады с нарушением регуляции цитокинов в поврежденной области, что может вызывать экспрессию большого числа алгогенных медиаторов, способных продуцировать боль [23, 25]. В исследовании D. Kraychete и соавт. [26] продемонстрировано, что у лиц с грыжей МПД наблюдается повышение уровней TNF-a и IL-6 в плазме в сравнении со здоровыми. Предполагается, что повышение экспрессии цитокинов может участвовать в процессах, способных модифицировать факторы транскрипции, вовлеченные в генную экспрессию, вызывая экспансию глиальных клеток и, таким образом, приводя к повышению нейрональной гипервозбудимости. Увеличение концентрации этих субстанций в тканях области протрузии диска позволяет предполагать, что цитокины могут вызывать эндоневральный отек и демиелинизацию нервных волокон [27]. Одновременно цитокины возбуждают ноцицепторы, что предполагает их ключевую роль в периферической гипералгезии и формировании болевого ответа [27]. В различных исследованиях неоднократно показано, что клетки МПД могут продуцировать TNF-a и IL-1 в уже на начальных этапах протрузии диска [28, 29]. Кроме того, A. Koch и соавт. [30] наблюдали, что увеличение плазменных уровней провоспалительных цитокинов (IL-1 в, IL-2, IL-6, IFN-c и TNF-a) коррелирует с усилением интенсивности боли у пациентов с хронической болью. Этапы формирования асептического воспаления при поражении позвонково-двигательного сегмента дегенеративной природы представлены на рисунке.
Асептическое воспаление на уровне позвонково-двигательного сегмента и механизмы развития боли (адаптировано по D. Borenstein [31]). 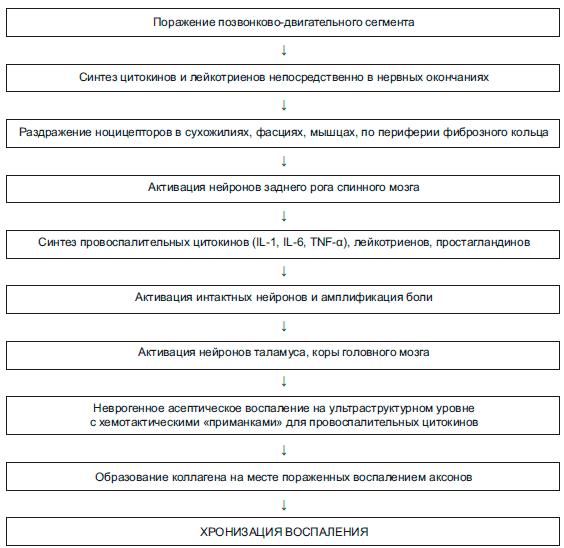
Воспалительные механизмы дискогенной БНС как возможная мишень терапевтических стратегий
Изучение воспалительных механизмов дискогенной боли является весьма перспективным направлением, прежде всего, с точки зрения развития терапевтических возможностей. Одной из возможных мишеней модуляции воспалительных механизмов выступает TNF-a, который является воспалительным маркером, вовлеченным в патофизиологические механизмы, лежащие в основе формирования вертеброгенной боли [32]. В последние 10 лет некоторые ученые предпринимают попытки использовать ингибиторы TNF-a в лечении радикулопатии. В различных исследованиях показано, что у пациентов с межпозвонковыми грыжами МПД повышен уровень TNF-a на суставной поверхности фасеточных суставов, в фиброзном кольце, пульпозном ядре и желтой связке [33]. Предполагается, что происходит утечка содержимого пульпозного ядра в эпидуральную полость, что вызывает локальное острое воспаление, отложение фиброзных элементов и адгезию [34]. Воспалительные реакции, модулируемые различными биохимическими и иммунологическими факторами, могут нарушать внутрикорешковый кровоток и целостность гематоневрального барьера, приводя, таким образом, к отеку и демиелинизации нервного корешка [35]. TNF-a — это плейотропный цитокин, действие которого может вызывать воспалительные ответы синаптических и миелиновых оболочек, стимулировать апоптоз вследствие его цитотоксических эффектов и приводить к отеку нерва и нейропатической боли [35]. В то же время эксперименты на животных и клинических моделях выявили, что ингибиторы TNF-a могут предотвращать эффекты неврального повреждения и таким образом оказывать нейропротективный эффект на нейродегенерацию [36]. Хотя уровень экспрессии TNF-a при различной интенсивности радикулярной боли носит нелинейный характер, модуляция уровня этого цитокина несомненно является важной мишенью терапевтических воздействий [37].
Одним из перспективных направлений антицитокиновой терапии является применение при дискогенной БНС релиз-активных антител (РА-АТ) к человеческому TNF-a [38]. Использование РА-АТ к TNF-a основано на представлениях о возможности модифицирующего влияния АТ на эндогенные регуляторы [39], что нашло клиническое применение в лечении некоторых воспалительных и дегенеративных заболеваний [40—44]. В частности, препарат артрофоон в качестве действующего вещества содержит РА-АТ к TNF-a. Его действие основано на модифицирующем влиянии РА-АТ на эндогенные регуляторы. Артрофоон специфически воздействует на активность TNF-a, снижает уровень АТ к этому цитокину в биологических средах организма, оказывает селективное влияние на иммунопатогенез, регулируя продукцию эндогенного TNF-a. Антивоспалительное действие аффинно очищенных АТ к этому цитокину продемонстрировано на моделях иммунного воспаления, где они тормозят экспрессию IL-1 и других провоспалительных цитокинов и увеличивают концентрацию противовоспалительных цитокинов [39]. Представленные свойства артрофоона были воспроизведены в экспериментальных исследованиях, проведенных в НИИ молекулярной биологии и биофизики Сибирского отделения РАН (Новосибирск) и НИИ фармакологии и регенеративной медицины Сибирского отделения РАН (Томск) [45, 46].
Изучение фармакологической активности артрофоона показало присутствие у него как выраженного противовоспалительного, так и анальгетического действия [7]. По данным сравнительного анализа на различных экспериментальных моделях выявлено, что эти эффекты артрофоона сопоставимы с противовоспалительным и анальгетическим действием нестероидных противовоспалительных препаратов (НПВП) [7]. Эти данные являются обоснованием клинического применения артрофоона при хронических воспалительных и дегенеративных заболеваниях суставов (ревматоидный артрит, остеоартроз, анкилозирующий спондилоартрит, подагрический артрит, псориатический артрит). Антивоспалительная активность артрофоона продемонстрирована на примере глобальных заболеваний суставов и позвоночника с выраженным воспалительным компонентом — ревматоидного артрита и анкилозирующего спондилоартрита [43, 44]. Клинические эффекты сопровождались положительной динамикой и лабораторных показателей (СОЭ, фибриноген, С-реактивный белок). Исследование уровней провоспалительных цитокинов выявило достоверное снижение через 3 мес исходно повышенного значения TNF-a, и этот эффект сохранялся к 12-му месяцу периода наблюдения. Позитивной динамикой сопровождалось применение артрофоона и в отношении других цитокинов (IL-1в, IL-6, IL-10, VEGF, EGF) [5]. Авторами отмечено, что артрофоон благоприятно влиял на местные и общие симптомы воспаления у пациентов с ревматоидным артритом. Улучшение состояния было отмечено пациентами уже к концу 1-го месяца терапии, а стойкая положительная клинико-лабораторная динамика — к 3—6-му месяцу от начала лечения. Максимальный эффект в лечении ревматоидного артрита достигается при непрерывном и длительном приеме препарата продолжительностью не менее 6 мес [44]. Артрофоон обладает хорошей переносимостью при 12-месячном курсовом применении. Он назначается совместно с другими средствами лечения ревматоидного артрита, в частности с базисными противовоспалительными препаратами, а его использование позволяет сократить потребность в применении НПВП на 50% и более. При рефрактерном к НПВП и базисным противовоспалительным препаратам ревматоидном артрите включение артрофоона в схему лечения позволяло достичь более убедительного клинического эффекта.
В нескольких открытых исследованиях [40, 41, 44] была изучена эффективность артрофоона у пациентов с остеоартритом. Авторами получены сходные результаты: к концу 3-го месяца терапии артрофооном в дозе 8 таблеток в сутки у большинства больных наблюдалось существенное снижение боли как в покое, так и при движении, отмечено уменьшение окружности коленных суставов, что свидетельствовало об уменьшении выраженности синовита и периартрикулярных воспалительных изменений и сопровождалось исчезновением или уменьшением экссудативных изменений при ультразвуковом исследовании суставов [40, 41]. При этом авторами не зарегистрировано значимых отклонений со стороны функции печени, почек и других лабораторных показателей, что позволяет использовать артрофоон в схемах лечения больных остеоартритом в течение длительного периода — более 6 мес.
Изучались эффективность и безопасность применения артрофоона у 100 пациентов с умеренной и тяжелой дискогенной БНС в сравнительном исследовании с нимесулидом [47, 48]. Оценивались параметры интенсивности болевого синдрома в спине (по визуальной аналоговой шкале), функционального состояния позвоночника (по данным тестов Шобера, Томайера), нарушения жизнедеятельности пациентов с БНС (по данным опросника Освестри), переносимости и эффективности исследуемого препарата, а также выраженности заболевания по данным отчетов врачей и самоотчетов пациентов. Проводился анализ продолжительности приема и количества дополнительных обезболивающих препаратов. Данные параметры анализировались через 14 дней, 1 и 3 мес от начала терапии. В целом динамика выраженности боли носила статистически значимый характер (р<0,001) уже через 14 дней, а динамика функционального состояния позвоночника — через 1 мес от начала терапии в обеих группах больных. Отмечено статистически значимое снижение частоты рецидивов у пациентов с хроническим интермиттирующим течением БНС на фоне приема препарата артрофоон (р<0,01) [47, 48]. В исследуемой группе терапия с использованием артрофоона, по мнению пациентов и врачей, в 76,0% случаев привела к значительному улучшению состояния (эффективность терапии — «очень хорошая» и «хорошая»). Переносимость используемого препарата оценена 32,0% больных как «очень хорошая» и 52,0% — как «хорошая». Авторы пришли к заключению, что эти данные позволяют положительно оценить применение артрофоона при БНС, особенно у пациентов с хроническим течением заболевания, требующим длительной и безопасной анальгетической и противовоспалительной терапии. Схожие результаты получены и в другом исследовании эффективности и безопасности применения артрофоона у пациентов с умеренным и выраженным болевым синдромом, ассоциированным со спондилоартрозом, с острым и хроническим вариантом течения БНС (с длительностью более 12 нед или числом эпизодов свыше 25 за 12 мес) [48].
А. П. Рачин и А. А. Логвинова [49] провели сравнительное 3-месячное клиническое исследование эффективности и безопасности препарата артрофоон (курс 3 мес) и НПВП (курс 2 нед) у пациентов с хронической, часто рецидивирующей неспецифической болью в спине. Авторами показано, что в целом НПВП характеризовались более быстрым терапевтическим эффектом. Однако прекращение приема НПВП приводило к постепенному рецидиву болевого синдрома и снижению качества жизни больного, причем 1/3 пациентов потребовалось дополнительное назначение НПВП для купирования боли. Более того, применение относительно безопасных НПВП у 10% пациентов привело к осложнениям со стороны желудочно-кишечного тракта и вызвало раннюю отмену препаратов. В то же время у пациентов, принимавших артрофоон, отмечалось стойкое, статистически достоверное улучшение состояния к концу 1-го месяца терапии, которое нарастало при дальнейшем курсовом приеме препарата. На протяжении всего периода наблюдения артрофоон демонстрировал хороший профиль безопасности — не отмечалось нежелательных лекарственных реакций. Исходя из результатов проведенного исследования, целесообразной является комбинированная схема противовоспалительного и обезболивающего лечения хронической БНС. Она включает назначение короткого курса НПВП и одновременного назначения 3-месячного курса артрофоона по 2 таблетки 2—4 раза в день в зависимости от интенсивности боли. НПВП обеспечивают быстрое снижение болевого синдрома и восстановление качества жизни пациентов. Прием НПВП коротким курсом позволяет снизить риск нежелательных явлений. Для достижения стойкого положительного результата необходим прием артрофоона, который поддерживает противовоспалительный эффект, восстанавливает качество жизни и снижает риск развития обострений заболевания. За счет уникального уровня безопасности артрофоон может применяться длительным курсом — до 2 лет, что позволяет избежать характерных для НПВП нежелательных эффектов [41, 49]. Безопасность артрофоона показана у пациентов с остеоартритом [41, 42]. Клинически ни у одного из пациентов не выявлено жалоб на боль, дискомфорт в эпигастрии, диспептические расстройства, а результаты эндоскопического исследования не показали повреждающего действия артрофоона на слизистую оболочку желудочно-кишечного тракта: случаев изъязвлений, эрозий, воспалительных процессов в желудке и двенадцатиперстной кишке не выявлено [42].
Таким образом, артрофоон представляет собой инновационный противовоспалительный препарат, отвечающий высоким требованиям эффективности и безопасности у пациентов с обострением хронической неспецифической боли в спине и боли, ассоциированной с дегенеративной болезнью дисков. Наиболее выраженный и стабильный эффект при лечении БНС наступает при длительном, 3—6-месячном курсовом приеме артрофоона. Длительное лечение артрофооном может быть рекомендовано для стабилизации патологического процесса, предупреждения рецидивирования и профилактики развития вторичного воспаления при вертеброгенной БНС. При достижении ремиссии возможен переход на поддерживающий прием препарата, доза которого подбирается индивидуально в зависимости от активности процесса и в среднем составляет 4 таблетки в сутки сублингвально вне приема пищи. Поддерживающий прием препарата позволяет избежать обострения БНС. На первых этапах терапии артрофоон следует назначать в комплексе с НПВП, так как видимый клинический эффект развивается в течение 1 мес его применения. В составе комплексной терапии артрофоон применяется с целью усиления противовоспалительной терапии и более быстрого достижения ремиссии. Назначение артрофоона целесообразно при непереносимости или наличии противопоказаний к применению НПВП. Благоприятный профиль безопасности артрофоона позволяет применять его у больных БНС независимо от возраста и сопутствующих заболеваний.
Таким образом, суммируя данные экспериментальных и клинических исследований, следует признать, что использование нового альтернативного направления терапии дегенеративных и воспалительных заболеваний опорно-двигательного аппарата, оказывающего модулирующее влияние на воспалительные механизмы болевых синдромов, является перспективным, учитывая не только его эффективность, но и хорошую переносимость. Это обосновывает оправданность более широкого использования стратегий, направленных на нейровоспалительные и нейроиммунные компоненты различных патологических состояний, в том числе в комплексных схемах их лечения.
ЛИТЕРАТУРА:
1. Andersson GB. Epidemiological features of chronic low-back pain. Lancet. 1999;354:581-585. doi: 10.1016/s0140-6736(99)01312-4 5. Van Boxem K, Cheng J, Patijn J, van Kleef M, Lataster A, Mekhail N, Van Zundert J. Lumbosacral radicular pain. Pain Pract. 2010;10:339-358.
2. Balague F, Mannion AF, Pellise F, Cedraschi C. Non-specific low back pain. Lancet. 2012;379:482-491.
3. Schroeder M, Viezens L, Schaefer C, Friedrichs B, Algenstaedt P, Ruther W, Wiesner L, Hansen-Algenstaedt N. Chemokine profile of disc degeneration with acute or chronic pain. J Neurosurg Spine. 2013;18:496-503. doi: 10.3171/2013.1.spine12483.
4. Boden SD, Davis DO, Dina TS, Patronas NJ, Wiesel SW. Abnormal magnetic-resonance scans of the lumbar spine in asymptomatic subjects. A prospective investigation. J Bone Joint Surg. 1990;72:403-408.
doi: 10.1111/j.1533-2500.2010.00370.x.
6. Luijsterburg PA, Verhagen AP, Ostelo RW, van Os TA, Peul WC, Koes BW. Effectiveness of conservative treatments for the lumbosacral radicular syndrome: a systematic review. Eur Spine J. 2007;16:881-899.
doi: 10.1007/s00586-007-0367-1.
7. Kim HJ, Suh BG, Lee DB, Lee GW, Kim DW, Kang KT, Chang BS, Lee CK, Yeom JS. The influence of pain sensitivity on the symptom severity in patients with lumbar spinal stenosis. Pain Physician. 2013;16:135-144.
8. Roberts S, Evans H, Trivedi J, Menage J. Histology and pathology of the human intervertebral disc. J Bone Joint Surg Am. 2006;88:10-14.
doi: 10.2106/jbjs.f.00019.
9. Gallucci M, Anselmi M, Di Sibio A, Gregori LM. Annular tears, fissures or HIZ? Neuroradiology. 2011;53(suppl 1):161-165.
doi: 10.1007/s00234-011-0933-4.
10. Smith LJ, Nerurkar NL, Choi KS, Harfe BD, Elliott DM. Degeneration and regeneration of the intervertebral disc: lessons from development. Dis Model Mech. 2011;4:31-41.
doi: 10.1242/dmm.006403.
11. Ricketson R, Simmons JW, Hauser BO. The prolapsed intervertebral disc. The high-intensity zone with discography correlation. Spine Phila Pa. 1976;1996;21:2758-2762.
doi: 10.1097/00007632-199612010-00010.
12. Stadnik TW, Lee RR, Coen HL, Neirynck EC, Buisseret TS, Osteaux MJ. Annular tears and disk herniation: prevalence and contrast enhancement on MR images in the absence of low back pain or sciatica. Radiology. 1998;206:49-55.
doi: 10.1148/radiology.206.1.9423651.
13. Molinos M, Almeida CR, Caldeira J, Cunha C, Goncealves RM, Barbosa MA. Inflammation in intervertebral disc degeneration and regeneration. J R Soc Interface. 2015;12:20141191.
doi: 10.10 98/rsif.2014.1191.
14. Boden SD, Davis DO, Dina TS, Patronas NJ, Wiesel SW. Abnormal magnetic-resonance scans of the lumbar spine in asymptomatic subjects. A prospective investigation. J Bone Joint Surg. 1990;72:403-408.
15. Schroeder M, Viezens L, Schaefer C, Friedrichs B, Algenstaedt P, Ruther W, Wiesner L, Hansen-Algenstaedt N. Chemokine profile of disc degeneration with acute or chronic pain. J Neurosurg Spine. 2013;18:496-503.
doi: 10.3171/2013.1.spine12483.
16. Chou R, Qaseem A, Snow V, Casey D, Cross JTJr, Shekelle P, Owens DK, Clinical Efficacy Assessment Subcommittee of the American College of Physicians; American College of Physicians; American Pain Society Low Back Pain Guidelines Panel. Diagnosis and treatment of low back pain: a joint clinical practice guideline from the American College of Physicians and the American Pain Society. Ann Intern Med. 2007;147:478-491.
17. Van Boxem K, Cheng J, Patijn J, van Kleef M, Lataster A, Mekhail N, Van Zundert J. Lumbosacral radicular pain. Pain Pract. 2010;10:339-358.
doi: 10.1111/j.1533-2500.2010.00370.x.
18. Park JY, Kuh SU, Park HS, Kim KS. Comparative expression of matrix-associated genes and inflammatory cytokines-associated genes according to disc degeneration: analysis of living human nucleus pulposus. J Spinal Disord Tech. 2011;24:352-357.
doi: 10.1097/bsd.0b013e3181fee4df.
19. Shamji MF, Setton LA, Jarvis W, So S, Chen J, Jing L, Bullock R, Isaacs RE, Brown C, Richardson WJ. Proinflammatory cytokine expression profile in degenerated and herniated human intervertebral disc tissues. Arthritis Rheum. 2010;62:1974-1982.
doi: 10.1002/art.27444.
20. Andrade P, Hoogland G, Garcia MA, Steinbusch HW, Daemen MA, Visser-Vandewalle V. El evated IL-1P and IL-6 levels in lumbar herniated discs in patients with sciatic pain. Eur Spine J. 2013;22:714-720.
doi: 10.1007/s00586-012-2502-x.
21. Yang H, Liu H, Li Z, Zhang K, Wang J, Wang H, Zheng Z. Low back pain associated with lumbar disc herniation: role of moderately degenerative disc and annulus fibrous tears. Int J Clin Exp Med. 2015;8(2):1634-1644.
22. Freemont AJ, Peacock TE, Goupille P, Hoyland JA, O'Brien J, Jayson MI. Nerve ingrowth into diseased intervertebral disc in chronic back pain. Lancet. 1997;350:178-181.
doi: 10.1016/s0140-6736(97)02135-1.
23. Ito K, Creemers L. Mechanisms of Intervertebral Disk Degeneration/Injury and Pain: A Review. Global Spine J. 2013;3:145-152.
doi: 10.1055/s-0033-1347300.
24. Aprill C, Bogduk N. High-intensity zone: a diagnostic sign of painful lumbar disc on magnetic resonance imaging. Br J Radiol. 1992;65:361-369. doi: 10.1259/0007-1285-65-773-361.
25. Schafers M, Geis C, Svensson CI, Luo ZD, Sommer C. Selective increase of tumour necrosis factor-alpha in injured and spared myelinated primary afferents after chronic constrictive injury of rat sciatic nerve. Eur J Neurosci. 2003;17(4):791-804.
doi: 10.1046/j.1460-9568.2003.02504.x.
26. Kraychete DC, Sakata RK, Issy AM, Bacellar O, Santos-Jesus R, Carvalho EM. Serum cytokine levels in patients with chronic low back pain due to herniated disc: analytical cross-sectional study. Sao Paulo Med J. 2010;128(5):259-262.
doi: 10.1590/s1516-31802010000500003.
27. Watkins LR, Maier SF, Goehler LE. Immune activation: the role of proinflammatory cytokines in inflammation, illness responses and pathological pain states. Pain. 1995;63(3):289-302.
doi: 10.1016/0304-3959(95)00186-7.
28. Nygaard OP, Mellgren SI, Osterud B. The inflammatory properties of contained and noncontained lumbar disc herniation. Spine (Phila Pa 1976). 1997;22(21):2484-2488.
doi: 10.1097/00007632-199711010-00004.
29. Yoshida M, Nakamura T, Sei A, Kikuchi T, Takagi K, Matsukawa A. Intervertebral disc cells produce tumor necrosis factor alpha, interleukin-1beta and monocyte chemoattractant protein-1 immediately after herniation: an experimental study using a new hernia model. Spine (Phila Pa 1976). 2005;30(1):55-61.
30. Koch A, Zacharowski K, Boehm O, Stevens M, Lipfert P, von Giesen HJ, Wolf A, Freynhagen R.Nitric oxide and pro-inflammatory cytokines correlate with pain intensity in chronic pain patients. Inflamm Res. 2007;56(1):32-37.
doi: 10.1007/s00011-007-6088-4.
31. Borenstein D. Эпидемиология, этиология, диагностическая оценка и лечение поясничной боли. Международный медицинский журнал. 2000;35:36-42.
32. Chia S, Qadan M, Newton R, Ludlam CA, Fox KA, Newby DE. Intra-arterial tumor necrosis factor-alpha impairs endothelium-dependent vasodilatation and stimulates local tissue plasminogen activator release in humans. Arterioscler Thromb Vasc Biol. 2003;23:695-701.
doi: 10.1161/01.atv. 00000 65195.22904.fa.
33. Andrade P, Visser-Vandewalle V, Philippens M, Daemen MA, Steinbusch HW, Buurman WA, Hoogland G. Tumor necrosis factor-alpha levels correlate with postoperative pain severity in lumbar disc hernia patients: opposite clinical effects between tumor necrosis factor receptor 1 and 2. Pain. 2011;152:2645-2652.
doi: 10.1016/j.pain.2011.08.012.
34. Lee JH, Lee SH. Clinical effectiveness of percutaneous adhesiolysis using Navicath for the management of chronic pain due to lumbosacral disc herniation. Pain Physician. 2012;15:213-221.
35. Di Martino A, Merlini L, Faldini C. Autoimmunity in intervertebral disc herniation: from bench to bedside. Expert Opin Ther Targets. 2013;17:1461-1470.
doi: 10.1517/14728222.2013.834330.
36. Zhou QH, Sumbria R, Hui EK, Lu JZ, Boado RJ, Pardridge WM. Neuroprotection with a brain-penetrating biologic tumor necrosis factor inhibitor. J Pharmacol Exp Ther. 2011;339:618-623.
doi: 10.1124/jpet.111.185876.
37. Wang YF, Chen PY, Chang W, Zhu FQ, Xu LL, Wang SL, Chang LY, Luo J, Liu GJ. Clinical Significance of Tumor Necrosis Factor-a Inhibitors in the Treatment of Sciatica: A Systematic Review and Meta-Analysis PLOS ONE. 2014;9;7:1-13.
doi: 10.1371/journal.pone.0103147.
38. Эпштейн О.И. Релиз-активность — от феномена до создания новых лекарственных средств. Бюллетень экспериментальной биологии и медицины. 2012;154:7:62-67.
39. Эпштейн О.И. Сверхмалые дозы. История одного исследования. М.: Издательство РАМН; 2008.
40. Алиханов Б.А. Артрофоон в лечении остеоартроза. Клиническая геронтология. 2004;10(12):63-66.
41. Алиханов Б.А. Опыт длительного применения сверхмалых доз антител к фактору некроза опухоли — а при остеоартрозе: эфективность и переносимость. Клиницист. 2007;4:62-67.
42. Варнакова Г.М., Кулеш Л.Д., Виноградова Т.А. Новые возможности предупреждения НПВС-гастродуоденопатий при лечении первичного остеоартрита. III Гродненские гастроэнтерологические чтения. Гродно. 2012;15-18.
43. Кудрявцева И.В., Уколова Л.А., Чижов Н.Н. Опыт применения потенцированных антител к фактору некроза опухоли — а (препарат артрофоон) в лечении анкилозирующего спондилоартрита. Поликлиника. 2005;2:20-25.
44. Мазуров В.И., Рассохин В.В. Применение артрофоона в лечении ревматоидного артрита и остеоартроза. Методические рекомендации. СПб. 2007.
45. Шерстобоев Е.Ю., Дыгай А.М., Гольдберг Е.Д., Эпштейн О.И., Сергеева С.А. Механизмы противовоспалительных свойств препарата артрофоон. XI Российский национальный конгресс «Человек и лекарство». 2004;850-851.
46. Качанова М.В., Шерстобоев Е.Ю., Бабаева А.Р., Черевкова Е.В., Дугина Ю.Л., Кислицына О.С., Эпштейн О.И., Сергеева С.А. Экспериментально-клиническое исследование влияния препарата артрофоон на продукцию провоспалительных цитокинов. Бюллетень экспериментальной биологии и медицины. 2008;145:1:64-67.
47. Шостак Н.А., Правдюк Н.Г., Корякина И.Н. Боль в нижней части спины у молодых — новый подход к терапии. Терапевтический архив. 2009;81(9):52-59.
48. Шостак Н.А., Мазуров В.И., Правдюк Н.Г., Рассохин В.В. Боль в спине, ассоциированная со спондилезом, — новый подход к лечению. Поликлиника. 2009;4:114-118.
49. Рачин А.П., Логвинова А.А., Хроническая боль в спине (подходы к диагностике и терапии. Поликлиника. 2014;5:42-45.
